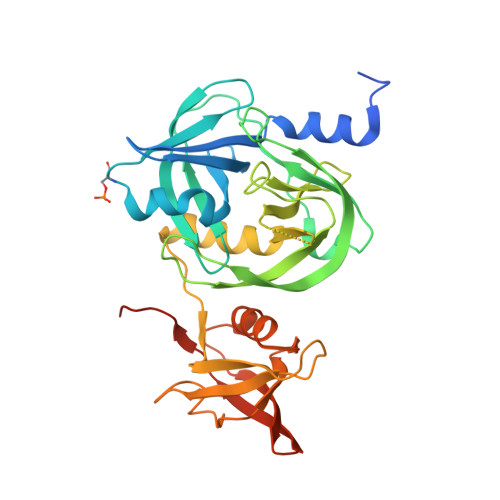
结核分枝杆菌必需的高温需求蛋白HtrA1(Rv1223)的晶体结构揭示了其独特的特征。
公共医学 : 30198900 内政部: https://doi.org/10.107/S205979831800952X 相关结构的主要引文: 5ZVJ型 PubMed摘要: 高温需要A(HtrA)蛋白是热休克诱导丝氨酸蛋白酶家族的成员,参与胞质外蛋白的质量控制和细菌在应激条件下的生存策略,并与几种病原体的毒力有关; 因此,它们是主要的药物靶点。 结核分枝杆菌具有三种假定的HtrAs:HtrA1(Rv1223)、HtrA2(Rv0983)和HtrA3(Rv0125)。 每个都有一个细胞质区、一个跨膜螺旋和一个周质区。 这里,结核分枝杆菌HtrA1突变株(mHtrA1)周质区的晶体结构由蛋白酶域(PD)和PDZ域组成 S387A型 )报告分辨率为2.7º。 尽管mHtrA1 S387A型 PD显示出与其他HtrAs相似的结构特征,其环路,尤其是L3和LA,显示出不同的构象。 环L3在三聚体的PD和PDZ结构域之间进行通信,并经历从活性构象到非活性构象的转变,如等效HtrA(DegS)的报道。 Loop LA因其在DegP中的长度(50个氨基酸)而导致低聚物的形成,其mHtrA1非常短 S387A型 (五个氨基酸),如mHtrA2(也是五个氨基酸),因此缺乏形成高级低聚物的必要相互作用。 值得注意的是,PDZ结构域中称为插入钳的有序环与相邻分子的蛋白酶结构域相互作用,这可能有助于稳定该酶的三聚体功能单元。 mHtrA1的三维结构 S387A型 本文将有助于酶特异性抗结核抑制剂的设计。