小鼠研究
发布时间: 2023年2月21日 通过 劳伦斯·塔巴克博士。
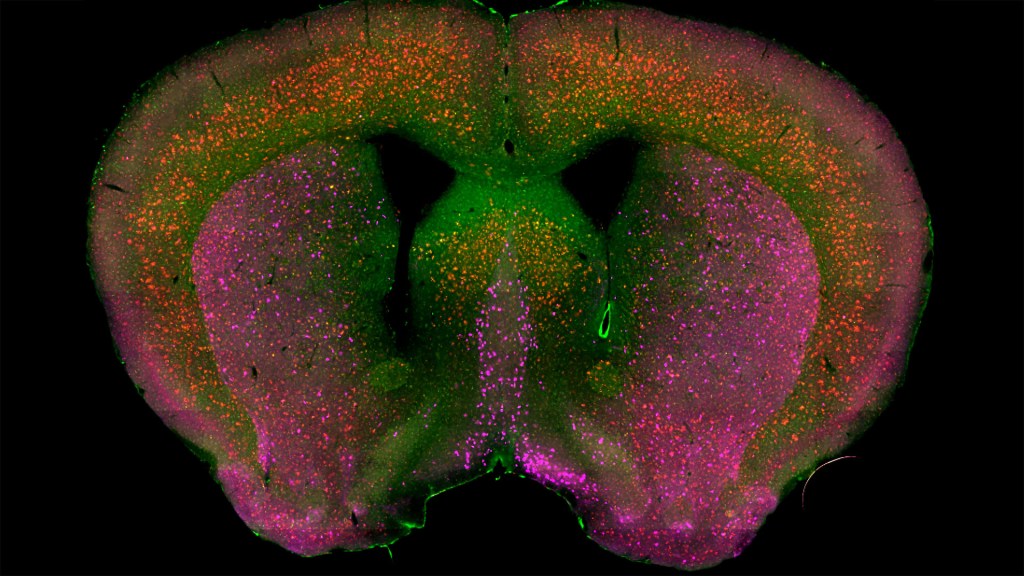
图片来源:Sakar Budhathoki、Mala Ananth、Lorna Role、David Talmage、NIH国家神经疾病和中风研究所 在中年人中检测阿尔茨海默病(AD)的早期症状并在研究中跟踪其随时间的进展仍然是一项挑战。 但在寿命较短的哺乳动物AD模型中更容易做到这一点,尤其是当与跨越大脑不同区域的尖端成像工具结合使用时。 这些工具可以帮助基础研究人员检测出早期的变化,这些变化可能会为人类提供更好的预防或治疗策略。
这张彩色快照显示了一只相对年轻的老鼠大脑中的早期炎症模式,这种老鼠的大脑发育状况与AD相似。你可以看到整个大脑前部(橙色、绿色)的炎症水平异常高 以及它的中间部分-分隔大脑两侧的隔膜。 这种程度的炎症表明大脑受到了损伤。
令人惊讶的是,在大脑中富含胆碱能神经元(粉红色)的部分没有检测到炎症,胆碱能神经元是一种独特的神经细胞,有助于控制记忆、运动和注意力。 虽然这些神经元仍然保持健康,但研究人员想知道随着AD的进展,炎症是否也会破坏它们。
这张彩色图片来自医学院学生萨卡·布达霍基,他早先曾在美国国立卫生院洛娜·罗尔实验室和国家神经疾病与中风研究所(NINDS)的大卫·塔尔马奇实验室工作。 Budhathoki与博士后科学家Mala Ananth合作,使用了一种专门设计的宽视野扫描仪,扫描大脑组织,点亮荧光标记并捕获图像。 这是Role和Talmage实验室率先采用的扫描方法之一[1,2]。
NIH的两个实验室正在探索异常炎症与大脑胆碱能信号系统损伤之间的可能联系。 事实上,针对胆碱能功能的药物仍然是AD和其他痴呆患者的一线治疗药物。 然而,研究人员仍然没有充分确定这些胆碱能神经元的丢失何时、为什么以及如何与AD相关。
这是一个丰富的基础研究领域,为未来更好地理解AD提供了希望。 这也是2022年向我们展示你的大脑! 照片和视频竞赛,由NIH的“通过推进创新神经技术®(Brain)倡议进行大脑研究”支持。
工具书类 :
[1] 神经再生:可视化神经变性的框架 Boorbor S、Mathew S、Ananth M、Talke D、Role LW、Kaufman AE。IEEE Trans-Vis计算图。 2021; 11月10日; (PP.)。
[2] NeuroConstruct:光学显微镜脑图像中神经突的三维重建和可视化 Ghahremani P、Boorbor S、Mirhosseini P、Gudisagar C、Ananth M、Talmage D、Role LW、Kaufman AE。IEEE Trans-Vis计算图。 2022年12月; 28(12):4951-4965.
链接 :
阿尔茨海默病及相关痴呆 (国家老龄化研究所/NIH)
角色实验室 (国家神经疾病和中风研究所/NIH)
Talmage实验室 (荷兰)
通过推进创新神经技术®(Brain)倡议进行的大脑研究 (国家卫生研究院)
让我们看看你的大脑! 照片和视频比赛 (大脑倡议)
NIH支持:国家神经疾病和中风研究所
发布时间: 生活快照
标签: 阿尔茨海默病 , 注意 , 脑 , BRAIN倡议 , 通过推进创新神经技术倡议进行大脑研究 , 胆碱能神经元 , 痴呆 , 成像 , 炎症 , 记忆 , 小鼠研究 , 运动 , 神经退行性病变 , 让我们看看你的大脑! , 宽场扫描仪
发布时间: 2022年11月1日 通过 Lawrence Tabak,博士。
图片来源:美国国立卫生院唐尼·布利斯; 百叶窗/Vasyl Shulga 如果你一直熬夜观看世界大赛,你可能会在这九局中期待超级巨星布莱斯·哈珀或何塞·阿尔图夫(JoséAltuve)摆正一个快速球,并将其送出球场。 像我这样的长期棒球迷可以立即分辨出主场挥杆的响声和微弱的滚地球的沉闷重击声。
我们的大脑具有如此迷人的能力,能够在瞬间分辨出“正确”和“错误”的声音。 这不仅适用于棒球,也适用于我们一天中所做的事情,无论是在乐器上弹奏出正确的音符,还是只要轻轻一按车门就可以将其关上而不会砰砰一声。
现在,美国国立卫生研究院资助的一个神经科学家团队发现,当一个人在完成一项任务后听到预期的或“正确”的声音与“错误”的声音时,大脑会发生什么。 事实证明,哺乳动物的大脑在预测声音发生的时间和理想的声音应该是什么样方面都非常擅长。 这种期望和反馈之间的任何明显不匹配,大脑的听觉中心都会做出反应。
人类和其他动物具有这种听觉能力似乎是很直观的,但研究人员不知道大脑听觉皮层中的神经元是如何做出这些快速判断来学习复杂任务的。 在期刊上发表的研究中 当代生物学 纽约大学的David Schneider开始了解这种熟悉的体验是如何真正起作用的。
为了做到这一点,施耐德和他的同事们,包括博士后尼古拉斯·奥德特(Nicholas Audette),研究了老鼠。 它们比人类更容易在实验室进行研究,虽然它们的大脑不是我们自己的微型版本,但我们的感觉系统有许多基本相似之处,因为我们都是哺乳动物。
当然,老鼠不会到处跑,也不会开关门。 因此,研究人员的第一步是训练这些动物完成一项类似于关车门的任务。 为了做到这一点,他们训练这些动物以正确的方式用爪子推动杠杆以获得奖励。 每次杠杆达到完美位置时,他们都会发出独特的音调。
在做了数千次尝试并听到了相关的声音后,这些老鼠知道该做什么,以及当它们做对了时应该发出什么样的声音。 他们的研究表明,当研究人员删除声音、播放错误的声音或在错误的时间播放正确的声音时,老鼠会注意到并调整它们的动作,就像你关上车门时发出的咔哒声不正确一样。
为了找出听觉皮层的神经元是如何反应产生观察到的行为的,Schneider的团队还记录了大脑活动。 有趣的是,他们发现,当老鼠按下杠杆并听到他们学会期待的声音时,听觉神经元几乎没有反应。 只有当声音的某些部分“关闭”时,他们的听觉神经元才会突然发出爆裂声。
正如研究人员解释的那样,从这些研究来看,哺乳动物的听觉皮层似乎对声音本身没有反应,而是对这些声音如何与预期相符或违背预期作出反应。 当研究人员完全取消声音时,如果你没有用力推车门产生熟悉的咔哒声,可能会发生这种情况,那么一组选定的听觉神经元内的活动就会像他们本应听到的那样突然激增。
施耐德的团队注意到,在日常任务中预测和处理自我生成声音的大脑区域和电路也在精神分裂症等疾病中发挥作用,在这种情况下,人们可能会听到不存在的声音或其他声音。 该团队希望他们的研究将有助于解释哪里出了问题,以及如何帮助治疗精神分裂症和其他神经疾病。 当他们期待着一扇关着的门发出令人满意的咔哒声或世界大赛本垒打的响亮爆裂声时,也许还能更多地了解到健康的大脑会经历什么。
参考 :
[1] 小鼠听觉皮层基于运动的精确预测 Audette NJ、Zhou WX、Chioma A、Schneider DM、Curr生物学。 2022年10月24日。
链接 :
我们如何倾听 ? (美国国家耳聋和其他沟通障碍研究所/NIH)
精神分裂症 (国家精神卫生研究所/NIH)
大卫·施奈德 (纽约大学,纽约)
NIH支持:国家心理健康研究所; 国家耳聋和其他沟通障碍研究所
发布时间: 新闻
标签: 听觉皮层 , 听觉神经元 , 听觉感知 , 脑 , 听力 , 听力中心 , 小鼠研究 , 神经电路 , 神经科学 , 精神分裂症 , 声音
发布时间: 2022年8月2日 通过 劳伦斯·塔巴克博士。
学分:斯蒂芬妮·格雷拉,波士顿大学,马萨诸塞州 NIH的 通过推进创新神经技术®(Brain)倡议进行大脑研究 正在彻底改变我们对人脑的理解。 正如该倡议名称所述,创新成像技术的发展将使研究人员能够以新的、越来越动态的方式观察大脑。 每年,该倡议都会在“向我们展示你的大脑!照片和视频大赛”中庆祝一些杰出的、特别有创意的进步。在8月的大部分时间里,我将在我们的博客系列《神奇的大脑》中分享一些最引人注目的发展。
在这张迷人的照片中,你看到了两个储存的记忆,科学家称之为记忆印记 海马 老鼠大脑的区域。 这些图形显示了良好记忆(绿色)和不良记忆(粉红色)的神经交叉点。 你还可以看到许多神经元的细胞核(蓝色),包括不参与记忆形成的附近神经元。
这张获奖图片由Stephanie Grella在NIH支持的实验室制作 神经学家史蒂夫·拉米雷斯 马萨诸塞州波士顿大学。这也不是第一次在博客中介绍格雷拉的技术艺术。 格雷拉不久将在芝加哥洛约拉大学建立自己的实验室,此前被捕 单个内存是什么样子的 .
为了同时捕获两个记忆,Grella使用了一种称为 光遗传学 这种强大的方法使研究人员能够对神经元进行基因工程,并使用蓝光在实验室小鼠中选择性地激活它们。 在这个案例中,格雷拉使用一种无害的病毒,用一种被称为视蛋白的光敏分子标记参与记录积极经历的神经元。 另一种分子标签被用来使这些细胞在被激活时呈现绿色。
在任何新的记忆形成后,都会有一段长达24小时的时间,在这段时间内,记忆具有可塑性。 然后,记忆趋于稳定。 但每次检索时,内存都可以在重新启动时进行修改,这一过程称为内存重新整合。
格雷拉和团队决定尝试利用记忆重组来消除现有的恐惧。 为了做到这一点,他们把老鼠放在一个以前吓到它们的环境中。 当一只老鼠恢复恐惧记忆(粉红色)时,研究人员用与积极记忆(绿色)相关的光激活,对于这些特定的老鼠来说,积极记忆包括与其他老鼠的积极互动。 目的是推翻或破坏可怕的记忆。
如图中的绿色所示,实验成功了。 虽然小鼠仍显示出一些恐惧记忆的痕迹(粉红色),但格雷拉解释说,她研究的重点是特定细胞转移到了积极记忆(绿色)。
也许更能说明问题的是,有证据表明,这些老鼠不仅仅是用一种记忆换取另一种记忆。 相反,激活积极记忆实际上抑制或抵消了动物的恐惧记忆。 希望有一天,这种方法能够启发人们克服消极和不想要的记忆,例如那些在创伤后应激障碍(PTSD)和其他心理健康问题中起作用的记忆。
链接 :
斯蒂芬妮·格雷拉 (波士顿大学,马萨诸塞州)
拉米雷斯集团 (波士顿大学)
通过推进创新神经技术®(Brain)倡议进行大脑研究 (国家卫生研究院)
向我们展示您的大脑照片和视频比赛 (脑倡议)
NIH支持:脑倡议; 普通基金
发布时间: 生活快照
标签: 脑 , 大脑成像 , BRAIN倡议 , 通过推进创新神经技术倡议进行大脑研究 , 雕刻 , 害怕 , 海马 , 回忆 , 记忆 , 心理健康 , 精神病 , 小鼠研究 , 神经元 , 神经科学 , 视蛋白 , 光遗传学 , 创伤后应激障碍 , 创伤后应激障碍 , 让我们看看你的大脑!
发布时间: 2022年2月1日 通过 Lawrence Tabak,博士。
NIH继续支持开发一些非常创新的治疗方法,以控制SARS-CoV-2,这是导致新冠肺炎的冠状病毒。 一个创新的想法涉及一种分子诱饵来阻止冠状病毒。
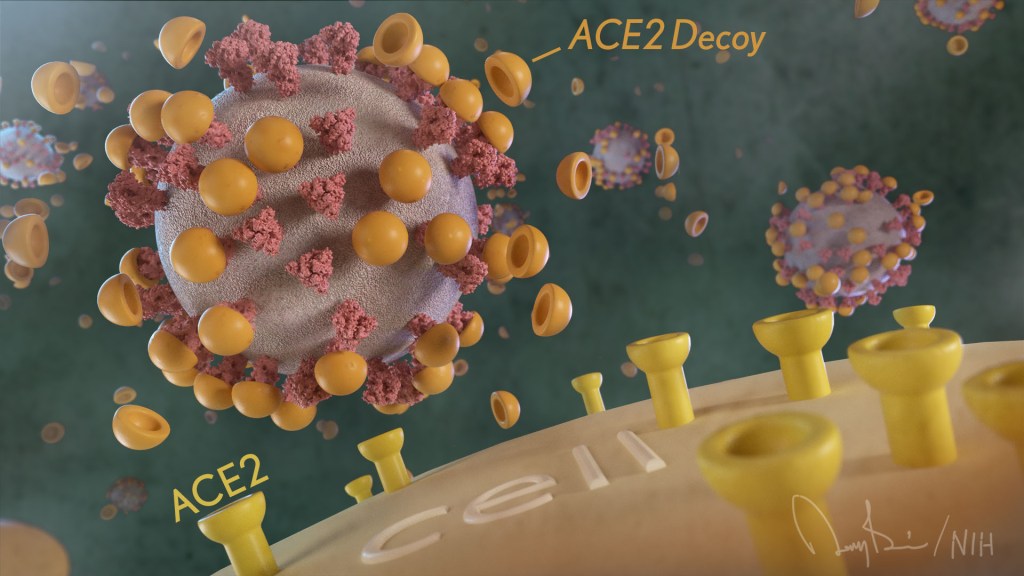
怎么样? 诱饵是一种特殊设计的蛋白质颗粒,它模拟了 ACE2受体 ,一种位于细胞表面的蛋白质,病毒的尖峰蛋白与之结合是导致感染的第一步。
其想法是,当这些ACE2诱饵被用于治疗时,它们将粘附在冠状病毒的棘突蛋白上(见上图)。 SARS-CoV-2的尖刺被诱饵紧紧包裹,因此它能够与真正的ACE2结合并感染我们的细胞。
最近,研究人员在杂志上发表了他们的初步结果 自然化学生物学 早期数据看起来很有希望[1]。 他们在严重新型冠状病毒肺炎的小鼠模型中发现,静脉输注工程化的ACE2诱饵可预防肺部损伤和死亡。 虽然还需要更多的研究,但研究人员表示,诱饵疗法可能通过吸入器直接输送到肺部,单独使用或与其他新型冠状病毒治疗联合使用。
这些发现来自伊利诺伊大学芝加哥分校团队的一个研究团队,该团队由阿斯拉·马利克(Asrar Malik)和贾利斯·雷曼(Jalees Rehman)领导,他们与伊利诺伊州大学香槟分校(University of Illinois Urbana-Champaign)的同事密切合作。 研究人员对早期测试ACE2诱饵策略的临床试验产生了兴趣[2]。 然而,在早期的试验中,临床试验发现死亡率没有降低。 ACE2候选药物可溶于体内并在体内降解,在中和病毒方面也被证明无效。
UIC团队没有放弃这个想法,而是决定尝试一下。 他们设计了一种新的可溶性ACE2,从结构上来说,它可能比原来的更好地充当诱饵。 他们的ACE2版本包含蛋白质氨基酸构建块的三个变化,与SARS-CoV-2尖峰蛋白的结合更紧密。 在实验室中,它似乎也能中和病毒以及 单克隆抗体 用于治疗新冠肺炎。
为了进行测试,他们在老鼠身上进行了研究。 正常小鼠不会因SARS-CoV-2而生病,因为病毒尖峰不能很好地与小鼠版本的ACE2受体结合。 因此,研究人员在一只携带人类ACE2并患上严重急性呼吸综合征的小鼠身上进行了研究,这种综合征与严重新冠肺炎患者的情况有些相似。
在他们的研究中,使用来自华盛顿州的原始病毒分离株和首次在巴西检测到的伽马变体(P.1),他们发现注射了治疗性ACE2蛋白的受感染小鼠死亡率要低得多,而且几乎没有严重急性呼吸综合征的迹象。 虽然该蛋白对两种病毒都有效,但感染更具攻击性的伽玛变异体需要更早的治疗。 经过治疗的老鼠也恢复了食欲和体重,表明它们正在恢复。
进一步的研究表明,诱饵结合到每一个测试变体的尖峰蛋白上,包括α、β、δ和Epsilon。 (Omicron在研究时还不可用。)事实上,与原始病毒相比,诱饵即使不能更好地结合到新的变体上,也同样有效。
研究人员将继续他们的临床前工作。如果一切顺利,他们希望将ACE2诱饵转移到临床试验中。 这种方法特别有希望的是,它可以与其他治疗方法结合使用,例如通过防止已经感染的病毒细胞生长或限制对感染的过度和破坏性免疫反应。
上周,美国17500多人因严重新型冠状病毒肺炎住院治疗。 我们必须继续尽我们所能挽救生命,这将需要许多创新的想法,如ACE2诱饵,使我们处于更好的地位,一劳永逸地战胜这种病毒。
工具书类 :
[1] 工程化ACE2诱饵减轻SARS-CoV-2变异体引起的肺损伤和死亡 . Zhang L、Dutta S、Xiong S、Chan M、Chan KK、Fan TM、Bailey KL、Lindeblad M、Cooper LM、Rong L、Gugliuzza AF、Shukla D、Procko E、Rehman J、Malik AB.Nat Chem Biol。 2022年1月19日。
[2] 重组人血管紧张素转换酶2(rhACE2)治疗新型冠状病毒肺炎(APN01-COVID-19)患者 ). ClinicalTrials.gov。
链接 :
新冠肺炎研究 (国家卫生研究院)
加速新冠肺炎治疗干预和疫苗 (国家卫生研究院)
阿斯拉·马利克 (伊利诺伊大学芝加哥分校)
贾利斯·雷曼 (伊利诺伊大学芝加哥分校)
NIH支持:国家心脏、肺和血液研究所; 国家过敏和传染病研究所
发布时间: 新闻
标签: ACE2公司 , ACE2诱饵 , 阿尔法变体 , Beta变体 , 冠状病毒 , 新冠肺炎 , 新冠肺炎治疗 , 诱饵 , Delta变量 , 药物开发 , Epsilon变体 , 伽马变量 , 肺 , 老鼠 , 小鼠研究 , 新型冠状病毒 , 大流行 , SARS-CoV-2型 , 严重急性呼吸综合征 , 穗蛋白
发布时间: 2021年9月21日 通过 弗朗西斯·柯林斯博士
在结束新冠肺炎疫情的所有进展中,值得记住的是,这里和世界各地的研究人员在解决许多其他严重健康问题方面继续取得重要进展。 作为NIH支持的一个鼓舞人心的例子,我想分享一个关于基因治疗用于治疗肌肉逐渐退化的遗传病的进展,例如Duchenne肌营养不良(DMD)。
最近发表在期刊上 单元格 研究人员开发了一种很有前途的方法,可以更有效地将治疗基因和基因编辑工具输送到肌肉中,从而需要更低的剂量[1]。 在动物研究中,新方法对肌肉的靶向性远比现有策略有效。 它提供了一种令人兴奋的方法来减少非靶向给药带来的有害副作用,这阻碍了基因治疗在许多情况下的发展。
在出生时患有DMD(这是一种X连锁疾病,因此影响男性)的男孩中,由于编码一种称为肌营养不良蛋白(dystrophin)的关键肌肉蛋白的基因突变,骨骼肌和心肌逐渐减弱。 到了10岁,大多数男孩都需要轮椅。 可悲的是,他们的预期寿命仍然不足30年。
希望有一天,基因疗法能够治疗甚至治愈杜氏肌营养不良症,并让患有该病的人活得更长、更高质量。 不幸的是,良性腺相关病毒(AAV)传统上用于将健康完整的肌营养不良蛋白基因传递到细胞中,但最终大多在肝脏而不是肌肉中。 许多其他肌肉遗传疾病的基因治疗也是如此。
病毒载体对肝脏的高剂量作用也值得关注。 最近,可悲的是,在一项高剂量AAV基因治疗试验中 X-连锁肌管性肌病(XLMTM )这是一种不同的骨骼肌疾病,可能已经存在潜在的肝脏疾病,可能会增加毒性敏感性。
为了纠正这一有关路由错误的问题,由Mohammadsharif Tabebordbar领导的研究人员在麻省理工学院博德研究所(Broad Institute of MIT)帕迪斯·萨贝蒂(Pardis Sabeti)和哈佛大学(Harvard University)以及马萨诸塞州剑桥(Cambridge,MA)哈佛大学(哈佛大学)的实验室中组装了一组优化的AAV。 与目前用于实验室研究和临床试验的肌肉纤维相比,它们已被改进为接近肌肉纤维的10倍。 事实上,研究人员称之为肌管AAV或MyoAAV。
MyoAAV可以以比传统AAV低250倍的剂量向肌肉输送治疗基因。 虽然这种方法尚未在人类身上进行试验,但动物研究表明,MyoAAV也在很大程度上避免了肝脏的损伤,这为更有效的基因治疗带来了前景,而不会有肝损伤和其他严重副作用的风险。
在 单元格 论文中,研究人员从常用的AAV9开始,展示了他们是如何产生MyoAAV的。 他们的目标是修饰蛋白质外壳,或衣壳,以创造一种AAV,这种AAV更适合专门针对肌肉。 为了做到这一点,他们求助于称为“交付”(DELIVER)的翻盖工程平台。 它是的缩写 D类 有指导的 E类 AAV衣壳的进化 L(左) 平均化 我 n个 V(V) 静脉注射 E类 转基因表达 对 不适用。
以下是DELIVER的工作原理。 研究人员通过向与细胞结合的AAV9衣壳部分添加随机氨基酸串,生成数百万种不同的AAV衣壳。 他们将这些修改过的AAV注射到小鼠体内,然后对来自全身肌肉组织细胞的RNA进行排序。 研究人员想找出不仅能进入肌肉细胞,而且能成功将治疗基因传递到细胞核以补偿基因受损版本的AAV。
这项研究不仅提供了一种AAV,还生产了几个相关的AAV,它们都具有独特的表面结构,能够专门针对肌肉细胞。 然后,该团队与马萨诸塞州剑桥哈佛大学的Amy Wagers合作,在动物研究中测试了他们的MyoAAV工具集。
然而,第一批货并不是基因。 这是基因编辑系统 CRISPR-Cas9公司 该团队发现,与传统AAV携带的CRISPR货物相比,MyoAAV正确地将基因编辑系统递送到肌肉细胞,并且还更好地修复了肌营养不良蛋白基因的功能失调拷贝。 重要的是,MyoAAV治疗动物的肌肉也表现出更大的力量和功能。
接下来,研究人员与波士顿儿童医院的Alan Beggs合作,发现MyoAAV对XLMTM小鼠模型有效。 正是在这种情况下,使用当前的AAV载体进行高剂量基因治疗导致了悲惨的结果。 XLMTM小鼠通常在10周内死亡。 但是,在接受携带矫正基因的MyoAAV后,所有六只小鼠的寿命都正常。 相比之下,以传统AAV相同方式治疗的小鼠寿命仅为21周。 此外,研究人员使用MyoAAV的剂量比目前临床试验中使用的剂量低100倍。
虽然在这种方法在人体中进行测试之前还需要进一步的研究,但MyoAAV也被用于在实验室中成功地将治疗基因导入人类细胞。这表明动物早期的成功可能在人体中持续。 该方法还有望开发具有靶向其他器官潜力的AAV,从而可能为广泛的遗传条件提供治疗。
这些新发现是该研究第一作者Tabebordbar十年工作的结果。 他孜孜不倦的工作也是个人的。 他的父亲患有一种罕见的遗传性肌肉疾病,使他不得不坐在轮椅上。 有了这一最新进展,人们希望下一代有希望的基因疗法可能很快进入临床,帮助Tabebordbar的父亲和其他许多人。
参考 :
[1] AAV衣壳变异体家族的定向进化使其能够在物种间进行有效的肌肉定向基因传递 Tabebordbar M、Lagerborg KA、Stanton A、King EM、Ye S、Tellez L、Krunnfusz A、Tavakoli S、Widrick JJ、Messemer KA,Troiano EC、Moghadaszadeh B、Peaker BL、Leacock KA、Horwitz N、Beggs AH、Wagers AJ、Sabeti PC Cell。 2021年9月4日:S0092-8674(21)01002-3。
链接 :
肌营养不良信息页面 (国家神经疾病和中风研究所/NIH)
X连锁肌管性肌病 (遗传和罕见疾病信息中心/国家转化科学促进中心/NIH)
体细胞基因组编辑 (普通基金/NIH)
穆罕默德沙里夫Tabebordbar (麻省理工大学博大学院、哈佛大学和哈佛大学,马萨诸塞州剑桥)
萨贝蒂实验室 (麻省理工大学博大学院、哈佛大学和哈佛大学)
NIH支持:Eunice Kennedy Shriver N 一 国家儿童健康与人类发展研究所; 普通基金
发布时间: 新闻
标签: AAV介导的基因传递 , AAV9型 , 腺相关病毒 , 衣壳工程 , CRISPR公司 , CRISPR/案例9 , 定向进化 , DMD公司 , 杜氏肌营养不良 , 肌营养不良蛋白 , 基因编辑 , 基因治疗 , 基因治疗载体 , 遗传病 , 基因组学 , 肝脏 , 小鼠研究 , 肌肉 , MyoAAV型 , 肌管 , 罕见病 , X连锁肌管性肌病 , XLMTM公司
发布时间: 2021年3月16日 通过 弗朗西斯·柯林斯博士
CRISPR基因编辑技术在制造非遗传性DNA改变方面具有巨大潜力,这种改变可以治疗甚至治愈广泛的毁灭性疾病,包括 艾滋病咨询门诊 到 肌营养不良 现在,一项最近的动物研究表明,另一个针对病毒RNA而非人类DNA的CRISPR系统可以作为一种吸入性抗病毒治疗,可以预先编程,以发现并消灭几乎任何流感病毒株和许多其他呼吸道病毒,包括SARS-CoV-2,导致新冠肺炎的冠状病毒。
怎么可能呢? 其他CRISPR基因编辑系统依赖于序列特异性引导RNA,将剪刀状细菌酶(Cas9)引导至基因组中的正确位置,以切断、替换或修复致病突变。 这种新的抗病毒CRISPR系统也依赖于导向RNA。但该导向将另一种称为Cas13a的细菌酶导向病毒基因组中的正确位置,以结合和切割病毒RNA,阻止病毒在肺细胞中复制。
最近发表在该杂志上的研究结果 自然生物技术 [1] 来自亚特兰大乔治亚理工学院和埃默里大学菲利普·桑坦基罗实验室。 其他小组的早期研究表明,Cas13有可能在实验室培养皿中降解流感病毒的RNA[2,3]。 在这项最新的研究中,Santangelo和他的同事们转向小鼠和仓鼠,看看这种酶是否真的能在活体动物的肺组织中起作用。
有趣的是Santangelo的团队是如何做到的。CRISPR系统不是将Cas13a蛋白本身输送到肺部,而是通过向信使RNA(mRNA)提供制造抗病毒Cas13a蛋白质的指令来工作。 这是 同样的想法 作为辉瑞和摩德纳基于mRNA的新型冠状病毒疫苗,它可以暂时引导你的肌肉细胞产生病毒尖峰蛋白,从而启动免疫反应。 在这种情况下,肺细胞翻译Cas13a mRNA以产生蛋白质。 Cas13a在导向RNA的引导下,也被输送到相同的细胞中,降解病毒RNA并阻止感染。 因为mRNA不进入细胞核,所以它不会与DNA相互作用,并引起人们对引起不必要的基因改变的潜在担忧。
研究人员设计了针对共享的、高度保守的流感病毒部分的导向RNA,这些病毒参与复制基因组和感染其他细胞。 他们还针对SARS-CoV-2的关键部分设计了另一组。
接下来,他们将Cas13a mRNA输送到动物的肺部,并使用一种适应的雾化器直接引导至动物肺部,就像那些用于将药物输送至人类肺部的雾化仪一样。 在患有流感的小鼠中,Cas13a降解了肺部的流感RNA,动物恢复正常,没有任何明显的副作用。 在SARS-CoV-2感染的仓鼠中,随着动物COVID-19样症状的改善,同样的方法限制了病毒在细胞内复制的能力。
这项发现首次表明,mRNA可用于在活体肺组织中表达Cas13a蛋白,而不仅仅是在培养皿中的细胞中。 这也是首次表明细菌Cas13a蛋白能够有效减缓或阻止SARS-CoV-2的复制。 后者带来了希望,即这种CRISPR系统可以迅速适应,以对抗任何未来发展出感染人类能力的新型冠状病毒。
研究人员报告称,这种方法有潜力对抗上个世纪在全球传播的绝大多数流感病毒株,即99%的流感病毒株。 它还应该对目前在全球传播的SARS-CoV-2的新的和更具传染性的变种同样有效。 虽然需要更多的研究来了解这种抗病毒方法的安全性,然后再将其应用于人类,但显而易见的是,像这样的基础研究进展有很大潜力帮助我们对抗过去、现在和未来威胁生命的呼吸道病毒。
工具书类 :
[1] mRNA编码的Cas13a在啮齿动物中治疗流感和SARS-CoV-2感染 Blanchard EL、Vanover D、Bawage SS、Tiwari PM、Rotolo L、Beyersdorf J、Peck HE、Bruno NC、Hincapie R、Michel F、Murray J、Sadhwani H、Vanderheyden B、Finn MG、Brinton MA、Lafontaine ER、Hogan RJ、Zurla C、Santangelo PJ。 国家生物技术。 2021年2月3日。 [在印刷前在线发布。]
[2] 利用Cas13对RNA病毒的可编程抑制和检测 Freije CA、Myhrvold C、Boehm CK、Lin AE、Welch NL、Carter A、Metsky HC、Luo CY、Abudayeh OO、Gootenberg JS、Yozwiak NL、Zhang F、Sabeti PC、Mol Cell。 2019年12月5日; 76(5):826-837.e11。
[3] 开发CRISPR作为对抗SARS-CoV-2和流感的抗病毒策略 .Abbott TR、Dhamdhere G、Liu Y、Lin X、Goudy L、Zeng L、Chemparathy A、Chmura S、Heaton NS、Debs R、Pande T、Endy D、La Russa MF、Lewis DB、Qi LS。Cell。 2020年5月14日; 181(4):865-876.e12。
链接 :
新冠肺炎研究 (国家卫生研究院)
流感 (国家过敏和传染病研究所/NIH)
Santangelo实验室 (佐治亚理工学院,亚特兰大)
发布时间: 新闻
标签: 抗病毒治疗 , 抗病毒药物 , 卡斯13a , 冠状病毒 , 新冠肺炎 , CRISPR公司 , CRISPR/病例13a , 流感 , 基因编辑 , 流感病毒 , 吸入器 , 肺 , 小鼠研究 , 信使核糖核酸 , mRNA疫苗 , 雾化器 , 非遗传基因编辑 , 新型冠状病毒 , 大流行 , 呼吸道感染 , RNA疗法 , SARS-CoV-2型 , 病毒复制
发布时间: 2021年1月7日 通过 弗朗西斯·柯林斯博士
学分:Progeria Research Foundation 我的好朋友萨姆·伯恩斯(Sam Berns)生来就患有一种罕见的遗传病,会导致快速过早衰老。 尽管Sam 去世了 在他十几岁的时候 早衰症 今天,他因真正积极的人生观而被人们铭记。 萨姆表达这一点的部分原因是,他愿意做出调整,用他的话来说,这使他能够把他一直想做的事情放在“可以做”的类别中。
本着同样的精神,代表全世界数百名患有早衰症的儿童及其家人,包括我的NIH实验室在内的一项研究合作已经取得了关键的技术进步,使非遗传基因编辑更接近治疗早衰的“可行”类别 自然 ,我们的团队利用新的基因编辑工具,首次纠正了小鼠模型中导致早衰症的单一基因拼写错误,产生了显著的有益效果[1,2]。 这项工作对纠正导致其他遗传性遗传疾病的类似单碱基错别字也有意义。
这项工作的结果对我来说令人难以置信地满意。2003年,我的NIH实验室发现了导致早衰的DNA突变。一个看似小的错误是,在一个叫做层粘连蛋白a的基因中用“T”代替了“C”( LMNA公司 )-导致产生一种有毒蛋白质,现在称为progrein。如果不进行治疗,患有progreia的儿童智力发育正常,但年龄增长速度极快,通常在青少年早期因心脏病发作或中风而过早死亡。
这一发现增加了纠正这种单字母拼写错误的可能性,可能有一天会帮助甚至治愈早衰儿童。但当时,我们缺乏安全、准确编辑DNA所需的工具。 老实说,我认为这在我有生之年是不可能的。 现在,由于基础基因组研究的进展,包括导致 2020年诺贝尔化学奖 ,这改变了。 事实上,在使用基因编辑技术方面已经取得了实质性进展,例如 CRISPR编辑系统 ,用于治疗甚至治愈广泛的破坏性遗传疾病,例如 镰状细胞病 和 肌营养不良
事实证明,最初的CRISPR系统虽然功能强大,但在剔除基因方面比纠正基因方面效果更好。 这就是为什么最近开发的一些DNA编辑代理和方法如此重要。 其中一个是由麻省理工学院布罗德学院和哈佛大学(马萨诸塞州剑桥)的David R.Liu及其实验室成员开发的,它是这些关于早衰症最新发现的关键,由一个团队报告,包括我在美国国立卫生研究院国家人类基因组研究所的实验室和田纳西州纳什维尔范德比尔特大学医学中心的Jonathan Brown。
相对较新的基因编辑系统超越了淘汰制,转而采用淘汰制[3,4]。 它的工作原理如下:与CRISPR所做的切割DNA不同,碱基编辑器通过酶促改变一个DNA碱基,将一个DNA字母直接转换为另一个。 结果很像用于修复文字处理器中的输入错误的查找和重置函数。 更重要的是,基因编辑器在不剪切DNA的情况下完成了这项工作。
我们的三个实验室(Liu、Brown和Collins)首先与马萨诸塞州皮博迪的Progeria研究基金会合作,从患有早衰症的儿童身上获取皮肤细胞。在实验室研究中,我们发现,以适当的RNA指南为目标的基础编辑可以成功纠正 LMNA公司 结缔组织细胞中的基因。 治疗使令人印象深刻的90%细胞的突变恢复到正常的基因序列。
但它对活的动物有效吗? 为了得到答案,我们在出生后3天或14天向近十几只小鼠注射了一次DNA编辑装置,大约相当于1岁或5岁的人类的成熟水平。 为了确保在小鼠身上的研究结果尽可能与未来用于人类的治疗相关,我们利用了NIH实验室开发的早衰小鼠模型,在该模型中,小鼠携带两份人类的复制品 LMNA公司 导致这种情况的基因变异。 这些小鼠几乎具备了人类疾病的所有特征
在活小鼠中,碱基编辑处理成功地编辑了许多器官中20%至60%细胞的健康基因DNA序列。 许多细胞类型将校正后的DNA序列保持了至少6个月——事实上,大动脉中最脆弱的细胞在6个月时实际上显示出几乎100%的校正,显然是因为校正后的细胞补偿了未校正的细胞。 更重要的是,经过治疗的动物的寿命从7个月增加到将近18个月。 在健康小鼠中,这大约是衰老的开始。
这是三个月来,在治疗早衰方面取得的第二个显著进展。 去年11月,根据我实验室的临床前工作和波士顿Progeria研究基金会进行的临床试验,食品和药物管理局(FDA)批准了 第一次治疗 对于条件。 它是一种叫做Zokinvy的药物,通过减少前体素的积累发挥作用[5]。 经过长期治疗,该药物能够将早衰儿童的寿命延长2.5年,有时甚至更长。 但这不是一种治疗方法。
我们希望这项基因编辑工作最终能治愈早衰症。但小鼠当然不是人类,在这种基因编辑治疗能够在人类身上安全试用之前,还有一些重要的步骤需要完成。 与此同时,基础编辑器和其他基因编辑方法不断改进,有可能应用于数千种基因疾病,在这些疾病中我们知道确切的基因拼写错误。 当我们展望2021年时,多年前设想的修复导致早衰的微小DNA错误的梦想现在已经在我们的掌握之中,并且越来越接近“可以做”的范畴。
工具书类 :
[1] 体内基底编辑拯救小鼠Hutchinson-Gilford Progeria综合征 Koblan LW等人,《自然》。 2021年1月6日。
[2] 基础编辑器修复早衰综合征中发现的突变 Vermeij WP、Hoeijmakers JHJ。 自然。 2021年1月6日。
[3] 无需双链DNA切割的基因组DNA目标碱基的可编程编辑 Komor AC、Kim YB、Packer MS、Zuris JA、Liu DR.Nature。 2016年5月19日; 533(7603):420-424.
[4] 基因组DNA中A•T到G•C的可编程碱基编辑,无需DNA切割 Gaudelli NM、Komor AC、Rees HA、Packer MS、Badran AH、Bryson DI、Liu DR、Nature。 2017年11月23日; 551(7681):464-471.
[5] FDA批准首次治疗Hutchinson-Gilford早衰综合征和一些进展性椎板病。 食品和药物管理局。 2020年11月20日。
链接 :
Progeria公司 (遗传和罕见疾病信息中心/NIH) 什么是基因组编辑和CRISPR-Cas9 ? (国家医学图书馆/NIH) 体细胞基因组编辑程序 (普通基金/NIH) 大卫·R·刘 (哈佛大学,剑桥,马萨诸塞州) 柯林斯集团 (美国国家人类基因组研究所/NIH) 乔纳森·布朗 (范德比尔特大学医学中心,田纳西州纳什维尔) NIH支持:国家人类基因组研究所 ; 国家翻译科学促进中心 ; 国家生物医学成像与生物工程研究所; 美国国家过敏症和传染病研究所; 国家普通医学科学研究所 ; 普通基金
发布时间: 新闻
标签: 老化 , 基本编辑器 , CRISPR公司 , DNA , 基因编辑 , 遗传病 , 基因组学 , 早衰症 , 遗传性疾病 , 层粘连蛋白-A , LMNA公司 , LMNA基因变异 , 小鼠模型 , 小鼠研究 , 早衰 , Progeria研究基金会 , 早老蛋白 , 罕见病 , 萨姆·伯恩斯
发布时间: 2019年7月16日 通过 弗朗西斯·柯林斯博士
今天,由于抗逆转录病毒药物的显著进步,大多数感染人类免疫缺陷病毒(HIV)的人有望过上几乎正常的寿命。 但这意味着终生服用药物。 如果这些都被阻止了,艾滋病毒在几周内就会卷土重来。 事实证明,要找到一种永久治愈艾滋病毒感染的方法要困难得多,因为艾滋病毒可以从体内彻底、永久地清除。 所以,我对最近的研究感到鼓舞,这些研究表明,在小鼠模型中消除艾滋病毒是可能的,也许随着研究的不断深入,我们将来会真正治愈人类的艾滋病毒。
这种创新的方法依赖于一个双重打击:药物和基因编辑。 首先,HIV感染小鼠接受了一种抑制病毒复制的实验性长效抗逆转录病毒治疗(ART)。 这一步骤清除了活跃的艾滋病毒感染。 但还需要更多,因为HIV可以通过将其DNA插入宿主的染色体中来“隐藏”,染色体处于休眠状态,直到病毒复制的条件合适为止。 为了找到这个传染源,研究人员给小鼠注射了一个基因编辑系统,该系统旨在剪除仍潜伏在小鼠脾脏、骨髓、淋巴结和其他细胞基因组中的艾滋病毒DNA。 结果如何? 研究人员在接受联合治疗的三分之一以上的小鼠中没有检测到艾滋病毒的迹象。
中的新研究 自然通信 是美国国家卫生研究院资助的奥马哈内布拉斯加州大学医学中心霍华德·根德尔曼实验室与费城坦普尔大学卡梅尔·哈利利实验室合作的产物[1]。 几年前,作为一名受过训练的病毒学家,Khalili意识到HIV能够整合到宿主细胞的基因组中,这意味着该病不能仅仅被认为是一种典型的病毒感染。 它也有遗传成分,这表明艾滋病毒的治愈可能需要遗传答案。
然而,当时还没有能够在不损害人类基因组的情况下从人类细胞中去除HIV DNA的工具。 近年来,随着一种称为CRISPR/Cas9的非常精确的基因编辑工具的发现和随后的开发,这种情况发生了变化。
CRISPR/Cas9编辑系统依赖于序列特异性引导RNA,将剪刀状细菌酶(Cas9)引导到基因组中的正确位置,在那里可以用来剪切、替换或修复致病突变。 目前正在努力将CRISPR/Cas9应用于治疗 镰状细胞病 , 肌肉营养不良 等等。
CRISPR/Cas9是否也能从受感染的细胞中去除HIV DNA并永远消除感染? 这种方法可能对接受抗逆转录病毒治疗的人特别有用,因为他们的脑脊液细胞中含有持续的艾滋病毒DNA。 美国国立卫生研究院最近资助的一项研究 临床研究杂志 发现HIV蓄水池与神经认知障碍之间的联系[2]
Khalili团队的早期工作表明,CRISPR确实可以从宿主细胞基因组中去除HIV DNA[3]。 问题是,当单独交付时,CRISPR无法根据需要从所有细胞中剪除病毒DNA的每一个片段,从而彻底永久地清除艾滋病毒。 将艾滋病毒基因组的负担降低到尽可能低的水平至关重要。
与此同时,Gendelman的实验室一直在致力于开发一种新的、更有效的抗逆转录病毒药物的输送方法。标准抗逆转录酶药物通常以组合方式输送,能够有效抑制HIV复制。 然而,人们需要每天服用口服药物。 此外,大多数抗逆转录病毒疗法三联疗法药物都是水溶性的,这意味着它的药物混合物会被迅速处理并由身体排出,而不会到达人体内艾滋病毒隐藏的许多地方。
为了使抗逆转录病毒药物以更少的剂量更有效地发挥作用,Gendelman的团队改变了抗逆转录酶病毒药物的化学成分,生成了脂溶性药物纳米晶。 然后将纳米晶体包装成纳米颗粒,并通过肌肉注射进行递送。 这种被称为长效缓释(LASER)ART的新药配方可以到达HIV潜伏的淋巴结、脾脏、肠道和脑组织[4]。 一旦到达那里,它就会随着时间的推移缓慢地存储和释放。 然而,像传统的ART一样,激光ART永远不能完全治愈HIV。
因此,Gendelman与Khalili合作问道:如果在激光艺术之后进行一轮CRISPR/Cas9,会发生什么? 在一系列研究中,研究人员分别测试了LASER ART和CRISPR/Cas9,包括单独测试和联合测试。 共有23只被设计成具有“人源化”免疫功能的HIV感染小鼠接受了实验性联合治疗。
正如预期的那样,无论是LASER ART还是CRISPR/Cas9本身都不足以消除小鼠体内的艾滋病毒。 然而,当LASER ART和CRISPR/Cas9按顺序递送时,结果大不相同。 研究人员在三分之一以上连续治疗的动物的脾脏或其他组织中没有发现艾滋病毒的证据。
值得注意的是,这种根除艾滋病毒的基因编辑方法正在应用于非生殖细胞(体细胞)。 NIH不支持在人类胚胎(生殖系)中使用基因编辑技术[5]。
当然,即使拥有人性化免疫系统的老鼠也不是人类。 在我们考虑进入人体临床试验之前,需要进行更多的研究来复制这些发现,并找出如何在动物模型中使这种艾滋病毒治疗方法更有效。 尽管如此,这些发现确实为人们增加了一个新的希望,即最终可能为美国和全球数以千万计的艾滋病毒感染者找到真正的治疗方法。
工具书类 :
[1] 序贯激光ART和CRISPR治疗在感染的人源化小鼠亚群中消除HIV-1 Dash PK、Kaminski R、Bella R、Su H、Mathews S、Ahooyi TM、Chen C、Mancuso P、Sariyer R、Ferrante P、Donatoni M、Robinson JA、Sillman B、Lin Z、Hilaire JR、Banoub M、Elango M、Gautam N、Mosley RL、Poluektova LY、McMillan J、Bade AN、Gorantla S、Sariyer IK、Burdo TH、Young WB、Amini S、Gordon J、Jacobon JM、Edagwa B、Khalili K、Gendelman HE。 国家公社。 2019年7月2日; 10(1):2753.
[2] Spudich S等人。脑脊液中持续感染HIV的细胞与较差的神经认知能力相关。 临床投资杂志。 2019.内政部:10.1172/JCI127413(2019)。
[3] 在动物模型中用saCas9和多重单导向RNA在体内切除HIV-1前病毒 .尹C,张T,曲X,张Y,普塔通达R,肖X,李F,肖W,赵H,戴S,秦X,莫X,Young WB,Khalili K,Hu W.Mol Ther。 2017年5月3日; 25(5):1168-1186.
[4] 创建具有改进的抗逆转录病毒谱的纳米配方卡博特孕前药 周T、苏H、达什P、林Z、迪亚瓦尔·谢蒂BL、科彻T、斯拉切特卡A、兰伯蒂B、福克斯HS、波卢埃科托娃L、戈兰特拉S、麦克米兰J、高塔姆N、莫斯利RL、阿尔努蒂Y、埃达格瓦B、根德尔曼HE。 生物材料。 2018年1月; 151:53-65.
[5] 中国研究人员关于首个基因检测婴儿的声明 NIH主任。 2018年11月28日。
链接 :
艾滋病病毒/艾滋病 (国家过敏和传染病研究所/NIH)
HIV治疗:基础 (美国卫生与公共服务部)
快速信息 (HIV.gov)
全球统计 (HIV.gov)
卡梅尔·卡利利 (宾夕法尼亚州费城坦普尔大学)
霍华德·根德尔曼 (奥马哈内布拉斯加大学医学中心)
NIH支持:国家心理健康研究所; 国家神经疾病和中风研究所; 国家过敏和传染病研究所; 国家老龄研究所; 国家药物滥用研究所; 普通基金
发布时间: 新闻
标签: 抗逆转录病毒治疗 , 艺术 , 脑脊液 , CRISPR/案例9 , 基因编辑 , 艾滋病咨询门诊 , HIV神经认知障碍 , 艾滋病病毒/艾滋病 , 人类免疫缺陷病毒 , 免疫学 , 激光艺术 , 小鼠研究 , 神经认知的 , 逆转录病毒 , 病毒学 , 病毒
发布时间: 2019年1月8日 通过 弗朗西斯·柯林斯博士
改编自Ogrodnik等人,2019年,《细胞代谢》。 肥胖影响着大约十分之四的美国成年人,增加了许多人类健康问题的风险:糖尿病、心脏病、某些癌症,甚至焦虑和抑郁[1]。 它还与衰老细胞的积累增加有关,衰老细胞是较老的细胞,即使失去生长和分裂能力,也能抵抗死亡。
现在,美国国立卫生研究院资助的研究人员发现,当瘦老鼠被喂食高脂肪食物时,它们的大脑中也有更多衰老细胞,表现出更多焦虑行为[2]。 研究人员可以使用所谓的消除衰老的药物来消除这种由肥胖引起的焦虑。 这些发现是第一批提供证据的证据,证明除许多其他慢性病外,老年药物可能为治疗一系列神经精神疾病提供新途径。
随着年龄的增长,衰老细胞在身体的许多部位积累[3]。 但细胞也可以在生命的任何时候进入衰老状态,以应对重大压力,如DNA损伤或慢性感染。 研究表明,周围有大量衰老细胞,尤其是晚年,与多种慢性疾病有关,包括骨质疏松、骨关节炎、血管疾病和全身虚弱。
衰老细胞表现出一种类似“僵尸”的行为,称为衰老相关分泌表型(SASP)。 在这种致命的、类似僵尸的状态下,细胞会加速释放蛋白质、生物活性脂质、DNA和其他因子,这些因子就像僵尸病毒一样,会诱导附近的健康细胞参与功能障碍。
事实上,这项最新研究背后的团队,由明尼苏达州罗切斯特市梅奥诊所的詹姆斯·柯克兰领导, 最近显示 将少量衰老细胞移植到幼鼠体内足以导致它们虚弱、虚弱和持续的健康问题。 这些不良反应通过一种抗衰老的鸡尾酒来缓解,包括达沙替尼(一种白血病药物)和槲皮素(一种植物化合物)。 这种药物混合物推翻了僵尸样SASP表型,迫使衰老细胞经历程序性细胞死亡,最终死亡。
先前的研究表明,衰老细胞也会在肥胖中积聚,而不仅仅是在脂肪组织中。 此外,最近的研究已将大脑中的衰老细胞与神经退行性疾病(包括阿尔茨海默病)联系起来,并在小鼠中显示达沙替尼和槲皮素有助于缓解神经退行性病[4,5]。 在杂志上发表的最新论文中 细胞代谢 Kirkland及其同事问,大脑中的衰老细胞是否也能解释肥胖患者的焦虑行为。
答案似乎是“是的”。研究人员表明,如果允许瘦老鼠吃高脂肪食物,它们会变得肥胖,并且对探索开阔空间和高架迷宫更加焦虑。
研究人员还发现,肥胖小鼠侧脑室附近白质中的衰老细胞增多,侧脑室是大脑的一部分,为脑脊液提供通道。 这些衰老的细胞也含有过多的脂肪。 解毒剂能清除这些细胞,让肥胖相关的焦虑消失吗?
为了找出答案,研究人员用一种抗衰老药物治疗了瘦鼠和肥胖鼠10周。 治疗没有导致体重的任何变化。 但是,随着大脑中衰老细胞的清除,肥胖小鼠的焦虑相关行为明显减少。 他们在没有减轻体重的情况下消除了焦虑!
需要进行更多的临床前研究,以更准确地了解该疗法的工作原理。 但是,值得注意的是,针对与衰老细胞相关的许多疾病,包括慢性肾脏病[6,7]、虚弱[8]和骨髓移植相关的早衰[9],已经在进行各种抗衰老药物的临床试验。
事实上,就在 细胞代谢 Kirkland的团队发表了一篇论文,该论文对14名与年龄相关的特发性肺纤维化患者进行了上述抗衰老药物dasatinib治疗,取得了令人鼓舞的人类首次初步结果,肺组织受损并结疤[10]。 随着我们对相关风险和益处的了解越来越多,谨慎是必要的,但可以肯定的是,在未来几年,我们将听到更多关于老年人抗衰老药的消息。
工具书类 :
[1] 成人肥胖事实 (疾病控制和预防中心)
[2] 肥胖诱导的细胞衰老引发焦虑并损害神经发生 Ogrodnik M等人,《细胞代谢》。 2019年1月3日。
[3] 衰老、细胞衰老与慢性病:新兴的治疗策略 Tchkonia T,Kirkland JL。 JAMA公司。 2018年10月2日; 320(13):1319-1320.
[4] Tau蛋白聚集与脑细胞衰老相关 Musi N、Valentine JM、Sickora KR、Baeuerle E、Thompson CS、Shen Q、Orr ME。衰老细胞。 2018年12月; 17(6):e12840。
[5] 清除衰老的胶质细胞可防止τ依赖性病理学和认知能力下降 Bussian TJ、Aziz A、Meyer CF、Swenson BL、van Deursen JM、Baker DJ。自然。 2018年10月; 562(7728):578-582.
[6] 糖尿病和慢性肾脏疾病的炎症和干细胞 临床试验.gov,2018年9月。
[7] 慢性肾脏病的衰老 。Clinicaltrials.gov,2018年9月。
[8] Fisetin对老年人虚弱、炎症的缓解及相关措施(AFFIRM-LITE) Clinicaltrials.gov,2018年12月。
[9] 造血干细胞移植幸存者研究(HTSS研究) Clinicaltrials.gov,2018年9月。
[10] 老年药物治疗特发性肺纤维化:一项首次人体开放性初步研究的结果 法官JN、Nambiar AN、Tchkonia T、LeBrasseur K、Pascual R、Hashmi SK、Prata L、Masternak MM、Kritchevsky SB、Musi N、Kirkland JL。 EBioMed公司。 2019年1月5日。 [印刷前Epub]
链接 :
健康老龄化 (国家老龄化研究所/NIH)
视频: 维尔科学峰会詹姆斯·柯克兰访谈 (Youtube)
詹姆斯·柯克兰 (明尼苏达州罗切斯特梅奥诊所)
NIH支持:国家老龄研究所; 国家神经疾病和中风研究所
发布时间: 新闻
标签: 阿尔茨海默病 , 焦虑 , 脑 , 达沙替尼 , 饮食 , 侧脑室 , 小鼠研究 , 神经精神障碍 , 肥胖 , 槲皮素 , SASP公司 , 衰老相关分泌表型 , 衰老细胞 , 抗衰老药物 , 抗衰老药 , 僵尸细胞