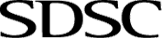胆绿素与人血红素加氧酶-1配合物的晶体结构
公共医学 : 15049686 内政部: https://doi.org/10.1021/bi035451l 相关结构的主要引文: 1S8C公司 PubMed摘要: 血红素加氧酶将血红素氧化分解为胆绿素,通过血红素作为辅因子和底物参与的过程释放铁和CO。 在这里,我们报告了产品无铁胆绿素在2.19 a时与人HO-1配合物中的晶体结构。 人胆绿素-HO-1结构与其血红素复合物的结构比较,以及最近发表的大鼠HO-1结构与胆绿素铁螯合物的复合物结构比较【Sugishima,M.,Sakamoto,H.,Higashimoto,Y.,Noguchi,M.和Fukuyama,K.(2003)《生物化学杂志》278,32352-32358】显示了两个主要差异。 首先,在活性部位缺乏Fe-His键和溶剂结构的情况下,远端和近端螺旋松弛并采用“开放”构象,这很可能会鼓励胆绿素释放。 第二,无铁胆绿素相对于血红素和胆绿素铁络合物占据不同的位置和方向。 胆绿素采用更线性的构象,从血红素部位移动到内腔。 这些结构结果提供了对HO-1催化中速率限制步骤的深入了解,即产物胆绿素释放。