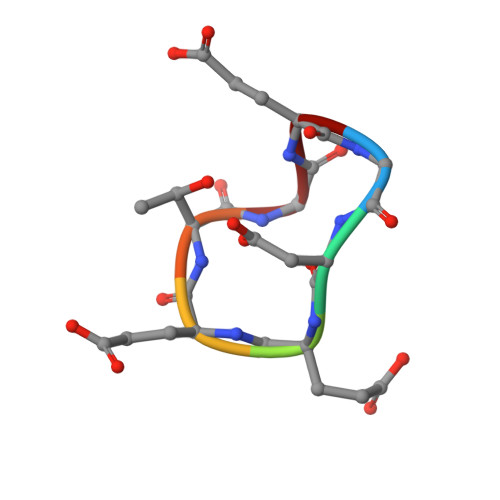
晶体接触工程,以获得适合配体浸泡实验的人类Keap1 Kelch结构域的晶体形式。
公共医学 : 23722832 内政部: https://doi.org/10.107/S174430911301124X 相关结构的主要引文: 3ZGC公司 , 3ZGD公司 PubMed摘要: Keap1是Cul3依赖的泛素连接酶复合物的底物衔接蛋白,在细胞对氧化应激的反应中起重要作用。 它将Nrf2与其Kelch结构域结合,从而触发Nrf2的泛素化和降解。 氧化应激可阻止Nrf2的降解,并导致细胞保护基因的激活。 因此,Keap1是一种很有吸引力的治疗炎症疾病的药物靶点。 通过结构研究支持药物化学研究需要一个坚固的结晶系统,其中晶体最好适合进行浸泡实验。 这有助于以常规和高通量的方式生成蛋白-甘氨酸复合物。 人类Keap1的结构已在前面描述过。 然而,在这种晶体形式中,Nrf2的结合位点被晶体接触所阻断。 分析了这种相互作用,并引入突变来破坏这种晶体接触。 一个双突变(E540A/E542A)以新的晶体形式结晶,其中Nrf2的结合位点未被阻断,可被小分子配体所利用。 报道了突变的Keap1-Kelch结构域的载脂蛋白形式(1.98μl分辨率)和通过浸泡获得的Nrf2衍生肽的配合物(2.20°分辨率)的晶体结构。