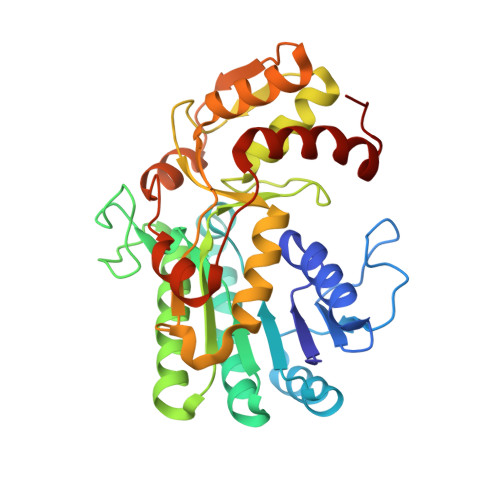
X射线结晶学和几何模拟揭示了寄生原生动物布鲁斯锥虫L-苏氨酸-3-脱氢酶的结构和功能。
公共医学 : 30198897 内政部: https://doi.org/10.107/S2059798318009208 相关结构的主要引文: 5K4季度 , 5K4T型 , 5K4单元 , 5千4伏 , 5千瓦 , 5K4年 , 5千50 , 5L9A型 , 5LC1型 PubMed摘要: 世界上最被忽视的两种热带疾病,非洲人类锥虫病(HAT)和恰加斯病,是由锥虫属原生动物寄生虫引起的。 这些生物体具有特殊的代谢途径,通常与人类不同,有可能被开发为新的药物靶点。 本研究阐明了HAT病原体布鲁斯锥虫L-苏氨酸-3-脱氢酶(TDH)的结构和功能。 TDH是L-苏氨酸代谢中的关键酶,TDH抑制剂已被证明在布氏锥虫的前环形式中具有杀锥虫活性。 TDH是人类中的一种无功能假基因,这表明可能通过靶向这种寄生虫酶来合理设计安全、特异的锥虫病治疗方法。 作为第一步,表达布鲁氏菌的TDH基因,并通过X射线晶体学求解酶的三维结构。 在多晶体结构中,布鲁斯锥虫TDH是一种二聚体短链脱氢酶,在其配体结合区域显示出相当程度的构象变化。 结构的几何模拟为了解这种酶的动态行为提供了依据。 此外,还测定了TDH与其天然底物和已知抑制剂结合的结构,从而揭示了该酶的催化机理。 总之,这些结果为未来靶向TDH或相关酶的药物设计提供了重要细节。