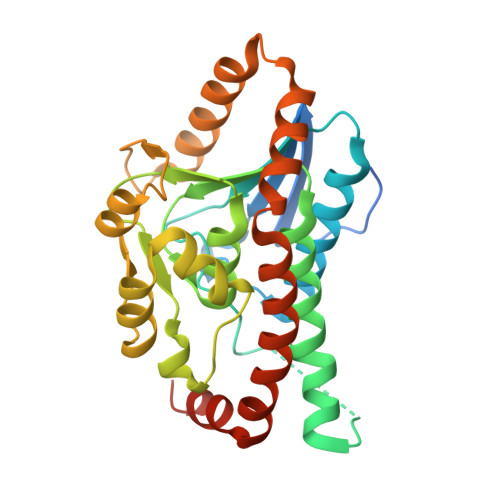
与酰基辅酶A底物类似物络合的酵母过氧化物酶体Delta(3)、Delta(2)-烯醇基辅酶A异构酶的结构:氢键网络对催化碱和氧阴离子孔反应性的重要性。
Onwukwe,G.U.公司。, 科斯基,M.K。, 皮科,P。, 施密茨(W.Schmitz)。, R.K.威伦加。(2015)Acta Crystallogr D生物晶体仪71: 2178-2191
- 公共医学: 26527136 在PubMed上搜索
- 内政部:https://doi.org/10.107/S139900471501559X
- 相关结构的主要引文:
4ZDB公司,4兹德克,4ZDD公司,4ZDE公司,4ZDF公司
- PubMed摘要:
Δ(3)、Δ(2)-烯酰基CoA异构酶(ECI)催化双键从3Z-或3E-烯酰基-CoA转移到2E-烯酰-CoA。ECI是巴豆酶超家族的成员。巴豆酶框架被许多酶用于催化酰基辅酶a硫酯的广泛反应。硫酯O原子被束缚在保守的氧阴离子空穴中。本文描述了酰基辅酶A底物类似物与过氧化物酶体酿酒酵母ECI(ScECI2)的结合模式。结合酰基辅酶A分子中定义最明确的部分是3',5'-二磷酸腺苷部分,它与环1和环2的残基相互作用,而泛烷部分定义最不明确。催化碱Glu158与Asn101侧链氢键合,并在apo结构中与Arg100侧链进一步氢键合。Arg100完全埋藏在载脂蛋白结构中,Arg100侧链的构象变化对底物结合和催化很重要。氧阴离子孔由Ala70(环2)和Leu126(螺旋3)的NH基团形成。相应肽单元Gly69 O和Gly125 O的O原子都是广泛氢键网络的一部分。这些氢键网络是巴豆酶氧阴离子空穴的一个保守特征,并讨论了它们在催化中的重要性。
组织隶属关系: 芬兰奥鲁大学生物中心和生物化学与分子医学学院。