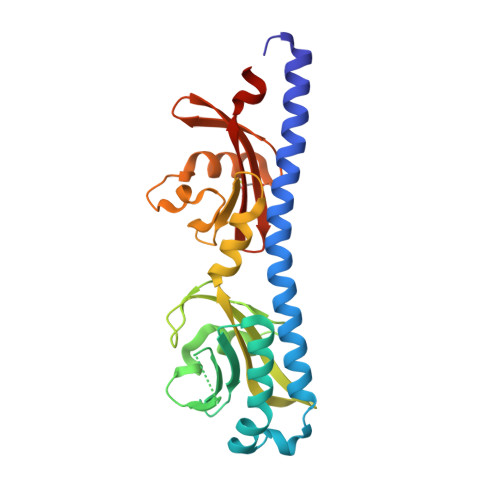
串联Per-Arnt-Sim(串联PAS)化学受体感觉域氨基酸识别和跨膜信号的结构基础。
公共医学 : 26457436 内政部: https://doi.org/10.107/S139900471501384X 相关结构的主要引文: 4个月 , 4个月 PubMed摘要: 趋化作用由甲基接受趋化蛋白(MCP)受体介导,在细菌种群生态学中起着重要作用。 本文首次对特征化MCP化学受体的周质串联Per-Arnt-Sim(PAS)传感域(PTPSD)的结构和配体诱导的构象变化进行了晶体学分析。 空肠弯曲菌Tlp3 PTPSD与异亮氨酸(化学引诱剂)的复合物分析表明,PTPSD是晶体中的二聚体。 这两个配体结合位点位于与二聚体界面相对的表面上的膜远端PAS结构域中。 突变实验表明,稳定异亮氨酸主链部分的五个高度保守的残基对结合至关重要,这表明该化学受体家族识别氨基酸的机制高度保守。 虽然PTPSD的折叠和配体结合方式不同于天冬氨酸受体Tar,但结构分析表明氨基酸化学受体的PTPSD也可能通过活塞位移机制发出信号。 PTPSD在活塞(C端螺旋线)“向上”和活塞“向下”状态之间波动。 引诱剂与远端PAS结构域的结合将其锁定在闭合形式,削弱其与近端结构域的联系,导致后者转变为开放形式,伴随着C末端螺旋向下(朝向膜)4°活塞位移。 在体内,这种运动会通过驱动跨膜螺旋2向细胞质的向下位移产生跨膜信号。