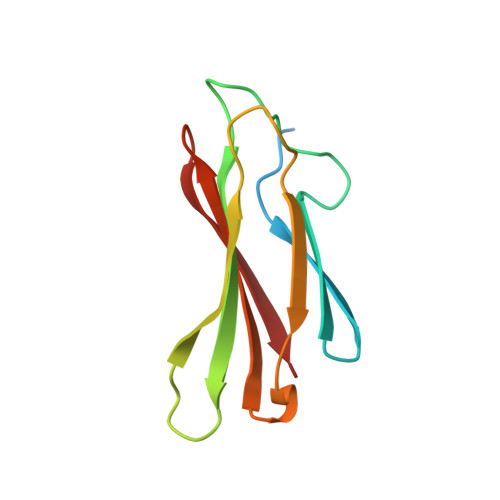肠道贾第鞭毛虫超氧化物还原酶:真核生物第一Sor的结构特征显示出对光还原高度敏感的铁中心。
公共医学 : 26527141 内政部: https://doi.org/10.107/S1399004715015825 相关结构的主要引文: 4BGL公司 , 4d7便士 PubMed摘要: 超氧化物还原酶(SOR)通常存在于原核生物中,通过将超氧化物阴离子还原为过氧化氢来保护其免受氧化应激。 该反应是在铁中心催化的,铁中心在迄今为止具有结构特征的原核SOR中高度保守。 本文报道了真核生物原生动物寄生虫肠道贾第鞭毛虫(Girdia intestualis,GiSOR)SOR的第一个结构,其分辨率为2.0º。 通过使用同步辐射X射线从同一闪速冷却蛋白质晶体中收集100K下的多组衍射数据,观察到铁中心的光还原。 在铁位在谷氨酸结合的氧化状态下的647 nm吸收带特征衰减后,使用在线紫外可见显微分光光度计监测还原。 与迄今为止在结构上表征的其他1Fe-SOR类似,该酶显示出四聚体四元结构排列。 作为一个独特的特征,蛋白质的N末端环含有特征性的EKHxP基序,无论铁氧化还原状态如何,都显示出异常高的灵活性。 与先前通过原核SORs的X射线晶体学和傅里叶变换红外光谱收集的证据不同,铁还原没有导致谷氨酸从催化金属中解离或其他结构变化; 然而,谷氨酸配体经历了X射线诱导的化学变化,揭示了GiSOR活性位点对X射线辐射损伤的高度敏感性。