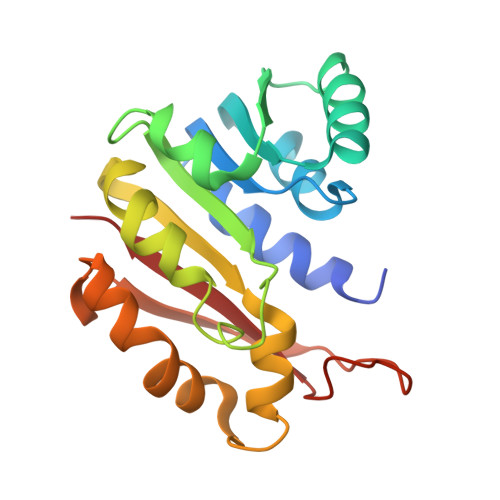
单斜胍乙酸甲基转移酶和钆离子结合特性。
公共医学 : 12925789 内政部: https://doi.org/10.107/s0907444903014719 相关结构的主要引文: 1P1B公司 , 1P1C公司 PubMed摘要: 胍基乙酸甲基转移酶(GAMT)是催化肌酸生物合成最后一步的酶。 这种酶在所有脊椎动物的肝脏中都大量存在。 用S-腺苷同型半胱氨酸(SAH)单斜修饰,将N端氨基酸37截短的重组大鼠肝脏GAMT结晶,并以2.8 a的分辨率测定晶体结构。 晶体不对称单元中有两个二聚体。 每个二聚体具有非晶体学双重对称性,并且通过沿晶体学b轴的伪-4(3)对称性与另一个二聚体相关。 单斜变质中结晶的GAMT的整体结构与四方变质中观察到的结构非常相似[Komoto et al.(2002),J.Mol.Biol.320,223-235],但含有Tyr136的环除外。 在单斜修饰中,如在四方修饰的晶体中观察到的,四个亚基中的三个亚基中的环具有催化不利的构象,而第四个亚基的环具有催化有利的构象。 从单斜和四方修饰的结构可以解释为什么Y136F突变酶保留了相当大的催化活性而Y136V突变酶失去了催化活性。 还测定了四方改性Gd衍生物的晶体结构。 通过将Gd衍生物结构与四方和单斜修饰中的天然结构进行比较,观察到Gd离子结合的有用特征,可用于蛋白质晶体学。 Gd离子可以与蛋白质结合而不改变蛋白质的天然结构,Gd原子在Cu-Kalpha辐射下产生强烈的反常色散信号; 然而,Gd-离子与蛋白质的结合需要相对特定的几何形状。