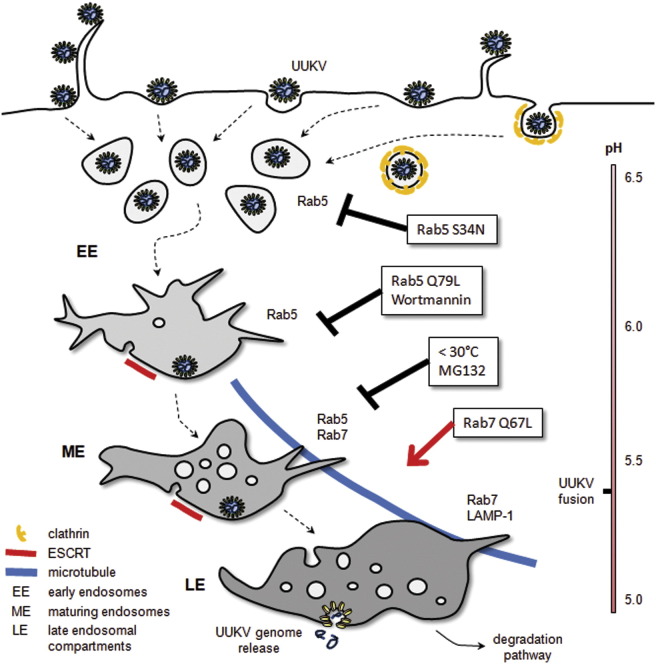
摘要 这个 布尼亚病毒科 构成了一个包膜动物病毒大家族,其中许多成员会导致严重疾病。 然而,早期的布尼亚病毒宿主细胞相互作用和进入机制基本上没有特征。 Uukuniemi病毒的研究 静脉病毒 ,我们发现病毒附着在细胞表面是特异的,但效率不高,25%的结合病毒在10分钟内被内吞,主要是通过无涂层的小泡。 病毒进入Rab5a+早期内体,随后进入Rab7a+和LAMP-1+晚期内体。 酸激活的渗透发生在内化后20-40分钟,需要早期到晚期内体的成熟。 病毒膜融合的pH阈值为5.4,进入温度对25°C以下较为敏感。 总之,我们的结果表明,Uukuniemi病毒通过酸激活的膜融合从晚期内体细胞室侵入宿主细胞。 这项研究还强调了内吞途径降解分支在促进晚穿透病毒进入中的重要性。
图形摘要
集锦 ► 布尼亚病毒Uukuniemi的胞吞作用主要是不依赖于网格蛋白的►病毒颗粒被摄取后,通过早期到晚期的内胚体►病毒通过晚期内胚体的酸活化膜融合发生渗透
结果 流式细胞术定量检测感染细胞 我们开发了一种基于荧光激活细胞分选仪(FACS)的检测方法,以量化UUKV感染,如 图S1 ,在线提供。 使用该试验,我们发现BHK-21细胞从感染到释放感染子代的完整周期持续约7小时。 在所有进一步的实验中,我们使用针对N蛋白的抗体8B11A3来监测感染,并在接触病毒7小时后采集细胞,将我们的检测限制在单个感染周期内。
据报道,只有BHK-21和胚胎鸡细胞支持生产性UUKV感染( Pettersson和Kaariainen,1973年 ). 我们评估了来自不同物种的15个细胞系,发现其中10个受到感染,4个产生病毒( 表S1 ). 在我们的研究中,我们选择了三种代表人类、啮齿动物和猴细胞的生产细胞系(分别为A549、BHK-21和BSC40)。 在A549和BSC40细胞中,一个完整的周期大约需要12小时,即比BHK-21细胞中的周期稍长(数据未显示)。 测试的两种蚊子衍生品系均未感染。
UUKV的标记 35 S-氨基酸或荧光染料 为了量化和可视化UUKV进入的早期阶段,我们使用纯化的病毒,用荧光探针进行化学标记,或用放射标记[ 35 S] 细胞培养液中的半胱氨酸和蛋氨酸。 为了使病毒荧光,我们利用了糖蛋白G中暴露的游离半胱氨酸的存在 N个 和G C类 我们将硫代硫酸盐活化荧光染料(TS-link Body-TR)(UUKV-RED)偶联到其上。 荧光和放射性标记粒子的特性如所示 图S2 标记的UUKV制剂纯度大于90%。 在放射性病毒中 35 N、G中存在S标签 N个 、和G C类 ,而G N个 和G C类 是UUKV-RED制剂中唯一荧光标记的蛋白质( 图S2 A和S2B)。 核蛋白N没有荧光,表明病毒包膜完好无损。 共聚焦荧光显微镜观察到不同标记的颗粒为单点,阴性染色后电镜观察到颗粒为132nm( 图S2 C–S2E)。 我们注意到标签对UUKV感染性没有显著影响; 滴度与未标记颗粒的滴度相似( 图S2 F) ●●●●。
UUKV细胞结合具有特异性但效率低下 要分析与单元格的绑定,请增加 35 S-标记的UUKV首先被允许在冰上与细胞结合2小时(moi为0.6-50)。 将未结合的病毒冲走,并通过闪烁计数测定剩余的细胞相关放射性。 结果表明,结合随着输入UUKV浓度的增加而增加( 图1 A) 但对于所有三种细胞系,与细胞相关的比例为7%–9%( 图1 B) ●●●●。 当结合实验的上清液添加到新细胞中时,放射性结合的比例相似,表明未结合的病毒完全能够与细胞结合( 图1 C) ●●●●。 这表明UUKV与宿主细胞的结合效率低下。
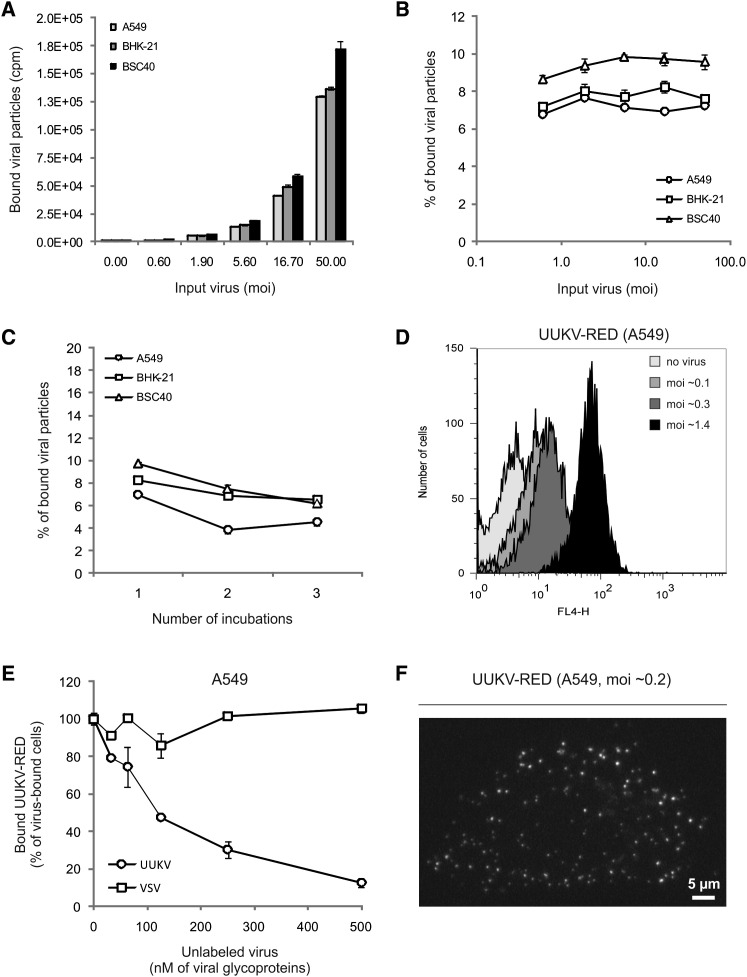
图1。
UUKV与细胞的结合效率低下
(A) 连续稀释 35 S标记的UUKV与细胞结合,并使用闪烁计数器定量样品。 误差条指示SD。
(B) 显示与(A)中相同的数据,但表示为与细胞结合的输入病毒的百分比(100×结合颗粒[cpm]/输入颗粒[cpm])。 误差条指示SD。
(C) 将之前的结合实验的上清液添加到新细胞中。 该程序重复了三次。 数据表示为(B)。 误差条指示SD。
(D) 不同数量的UUKV-RED与细胞结合,并通过流式细胞仪分析样本。
(E) 显示了未标记粒子和荧光粒子之间的结合竞争。 根据病毒糖蛋白的浓度对病毒输入进行标准化。 用不同数量的未标记颗粒(UUKV或VSV)预培养细胞,然后按(D)所述暴露于UUKV-RED(2.5 nM)。 误差条指示SD。
(F) UUKV-RED与冰上的细胞结合,并用共焦显微镜分析样品。 白点是一系列z堆叠合并成一个平面的细胞相关病毒颗粒。
FACS分析允许检测从moi 0.1以上结合的UUKV-RED( 图1 D) ●●●●。 UUKV-RED的结合被未标记UUKV的预结合以剂量依赖性的方式消除( 图1 E) 。 未标记颗粒浓度增加50倍,UUKV-RED结合减少一半,浓度增加200倍,减少10%。 水疱性口炎病毒(VSV)的预结合不影响UUKV-RED的结合( 图1 E) 。 综上所述,这些实验表明,UUKV与细胞的结合效率很低,但结合很可能涉及一个或多个特定的附着因子或受体。
UUKV-RED在4°C下与A549结合后,通过共聚焦显微镜可以在细胞表面看到单个病毒颗粒( 图1 F) ●●●●。 当感染倍数(moi)仅为0.2时,每个细胞的斑点数超过100个,这表明感染性微粒和非感染性微粒的比率很低。
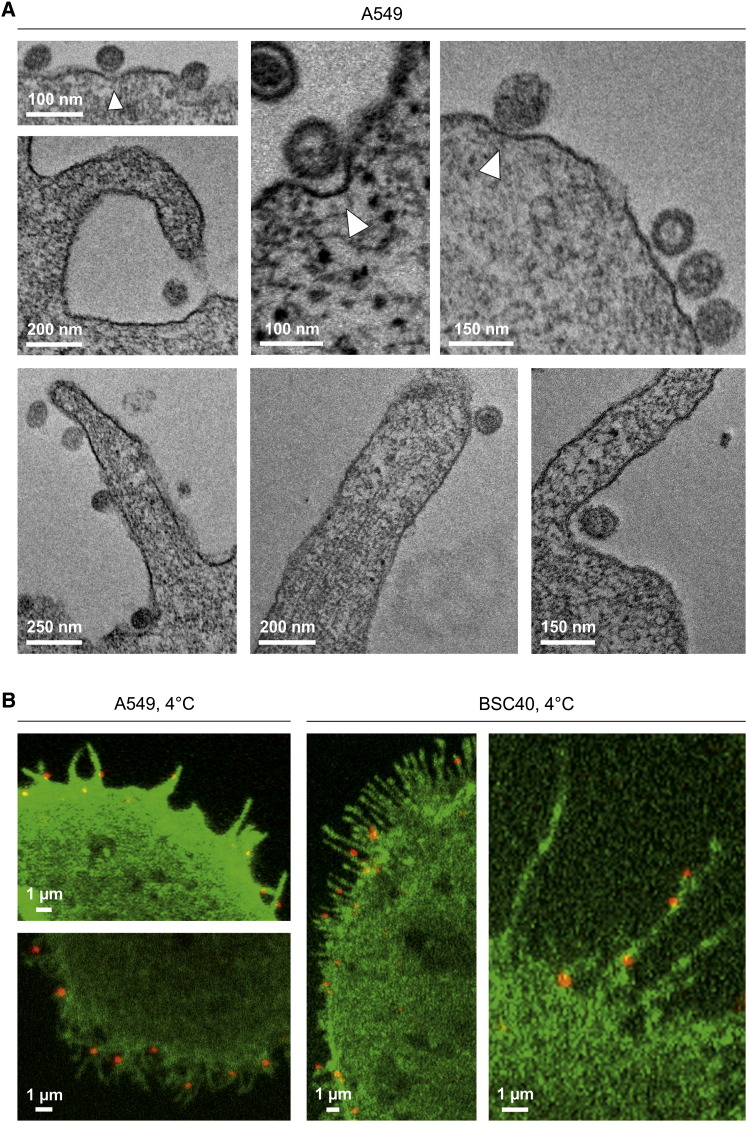
薄片电镜显示,与A549细胞表面结合的UUKV以单个颗粒的形式出现,病毒与质膜之间的距离为11.4±2.8 nm(n=30)( 图2 A) ●●●●。 在缺乏可见细胞质外套的浅质膜凹痕中可以看到一些( 图2 A、 白色箭头)。 大约一半与丝状伪足相关或位于其底部(分析的96个颗粒中有47个)。
图2。
UUKV与丝足类结合
(A) UUKV的EM与质膜相关。 将细胞暴露于病毒并进行薄片分析。 一些膜结合病毒与内陷有关(白色箭头)。
(B) UUKV-RED(moi~1)与表达PH-PLCΔ1EGFP的细胞结合,并通过共焦显微镜分析样品。 图片显示UUKV-RED与丝状足类有关。
对在质膜上表达荧光蛋白标记物(PH-PLCΔ1与增强型绿色荧光蛋白[EGFP]结合)的细胞进行荧光显微镜观察,证实了UUKV-RED与丝状足类的关联( 图2 B) ●●●●。 注意A549和BSC40细胞中的丝状伪足在长度和形状上不同。
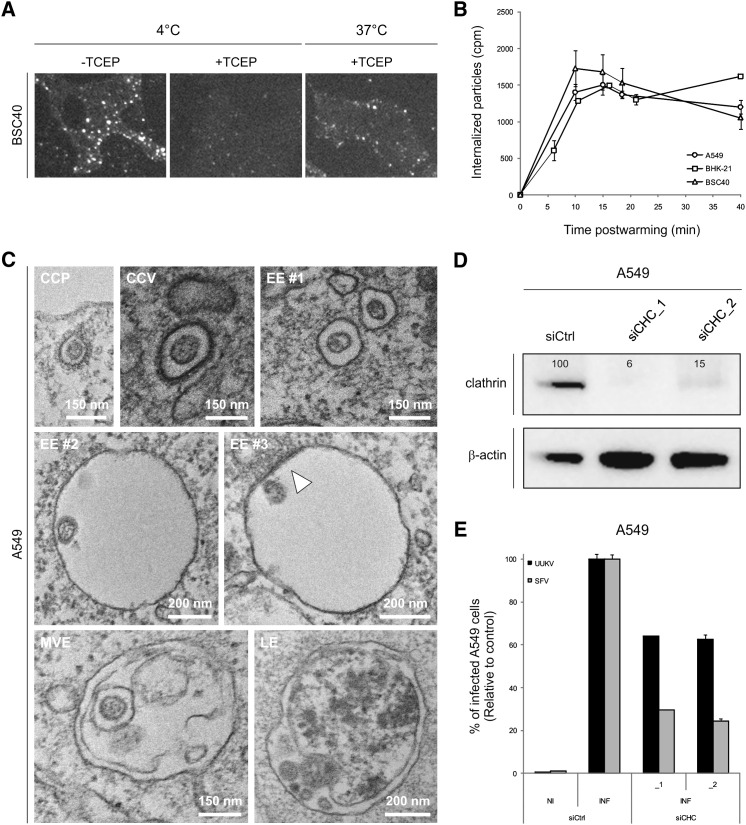
UUKV内化主要与氯氰菊酯无关 为了通过荧光显微镜分析UUKV内化,我们首先让UUKV-RED以相对较高的moi(~7.5)在冰上与BSC40细胞结合,然后在氯化铵(NH)存在下加热细胞 4 Cl)防止渗透。 40分钟后,将细胞放回冰上,以阻止进一步的内吞作用。 为了区分内化颗粒和表面结合颗粒,用三(2-羧乙基)膦(TCEP)在冰上处理细胞30分钟。 由于TCEP是一种不透膜的还原剂,它只去除了仍暴露在质膜上的UUKV-RED中的染料。 在升温前用TCEP处理的样品中,我们几乎没有观察到背景荧光( 图3 A[4°C,+TCEP]),而在升温后,内化病毒可被视为细胞内不同强度的荧光点( 图3 A[37°C,+TCEP])。 我们估计,25%的细胞结合颗粒在40分钟内被内吞。
图3。
UUKV进入主要与氯菊酯无关
(A) UUKV-RED(moi~7.5)与细胞结合,然后样品在NH存在下移动到37°C 4 Cl(50 mM)40分钟,以便内化。 随后用TCEP(一种膜不透性还原剂)处理细胞,以区分内部颗粒和外部颗粒,并用宽视野显微镜进行分析。
(B) 内部化时间进程 35 S-标记UUKV(moi~3)。 胰蛋白酶处理无法去除的部分被视为背景,并从其他值中减去。 误差条指示SD。
(C) 细胞在冰上暴露于UUKV,随后迅速加热至37°C,以使其内部化。 使用EM,病毒很少出现在CCP和CCV中,但通常出现在未涂层的小泡中(EE#1)。 UUKV也见于较大的内体结构(EE#2和#3)。 这些液泡有时与细胞溶质表面的电子致密结构有关(EE#3,白色箭头)。 在后期,病毒通常在MVE和可能对应于LE或自噬囊泡的结构中发现。
(D) western blotting检测CHC敲除效率。 CHC蛋白水平表示为用CHC siRNA(siCHC_1和_2)处理的细胞中CHC水平的百分比,标准化为用阴性对照siRNA处理的对照细胞中的β-actin和CHC水平。
(E) 用CHC-siRNAs处理的细胞被UUKV或SFV感染。 这些值被归一化为用阴性对照siRNA(siCtrl)处理的样本中的细胞数量和感染水平。 NI和INF分别用于非感染细胞和感染细胞。 误差条指示SD。
为了确定摄取动力学,使用了更定量的分析。 细胞在冰上培养 35 S标记颗粒。 清洗后,用冰上胰蛋白酶处理细胞,以去除表面结合的病毒。 在低温下结合后,90%以上的细胞相关放射性通过该程序被去除( 图S3 ). 相比之下,如果在胰蛋白酶处理之前将细胞加热到37°C 20分钟,大约三分之一的 35 胰蛋白酶无法接触到S标记颗粒( 图S3 ). 当分析一段时间内胰蛋白酶抵抗病毒的生成时,发现10分钟内已达到最大内化水平( 图3 B) ●●●●。 考虑到背景,我们可以确认25%的细胞结合颗粒被迅速内吞。
为了使用EM评估细胞内吞,将细胞暴露在高moi的冰上病毒中,并迅速转移到37°C以允许内吞。 2分钟后,病毒出现在直径约150 nm的光滑表面的囊泡中,通常位于质膜附近( 图3 C、 EE#1)。 在极少数情况下,可以看到病毒与网格蛋白包被的凹坑(CCP)和囊泡(CCV)有关( 图3 C) ●●●●。 10分钟后,在直径400–500 nm的经典内胚空泡中观察到UUKV( 图3 C、 EE#2和#3)。 其中一些在细胞溶质表面(EE#3)具有电子致密结构,其特征是含有氯氰菊酯的蛋白质簇和转运(ESCRT)复合物所需的内体分选复合物,是典型的早期内体(EE)( Sachse等人。, 2002 ). 30分钟后,病毒通常出现在多泡内体(MVE)和可能代表晚期内体(LE)的液泡中( 图3 C、 MVE和LE)。 未观察到病毒与限制膜或腔内小泡的融合。
为了进一步解决CME在感染中的潜在参与,我们在平行实验中使用两种不同的、非重叠的小干扰RNA(siRNAs)耗尽了克拉通重链(CHC)的A549细胞。 通过western blotting检测,每种siRNA使培养物中CHC蛋白水平降低85%–95%( 图3 D) ●●●●。 CHC-siRNA-处理的细胞仍能有效感染UUKV。 与转染对照siRNA的对照细胞相比,两种CHC siRNA的感染率仅下降35%( 图3 E) 。 作为评估CHC击倒有效性的对照,我们使用了Semliki Forest病毒(SFV),它只使用氯菊酯途径( Doxsey等人。, 1987 ). 与UUKV相比,SFV感染在这些细胞中受到强烈抑制,与对照组相比减少了75%-80%( 图3 E) 。 综上所述,结果表明,尽管在CCP和CCV中可以看到一些病毒颗粒,但大多数病毒颗粒是通过不涉及网格蛋白外壳的机制内吞的。
UUKV进入EE和LE EM研究表明,内化的病毒被转运到内体。 为了更好地确定这种病毒所采取的内吞途径,我们接下来确定病毒是否达到EE。在冰上的UUKV-RED(moi~10)与表达EGFP标记的EE标记物Rab5a(EGFP-Rab5a)的A549细胞结合后,温度迅速转移到37°C,持续30分钟。 共聚焦显微镜显示,UUKV与EGFP-Rab5a在加温5分钟后细胞质小泡中共定位(数据未显示)。 共定位病毒的数量在升温后10分钟达到最大值,此后减少,直到30分钟后不再检测到为止( 图4 A和4B)。 在活的BSC40细胞中,旋转圆盘共焦显微镜显示,UUKV-RED实际上随EGFP-Rab5a阳性小泡在细胞质中移动( 电影S1 ).
图4。
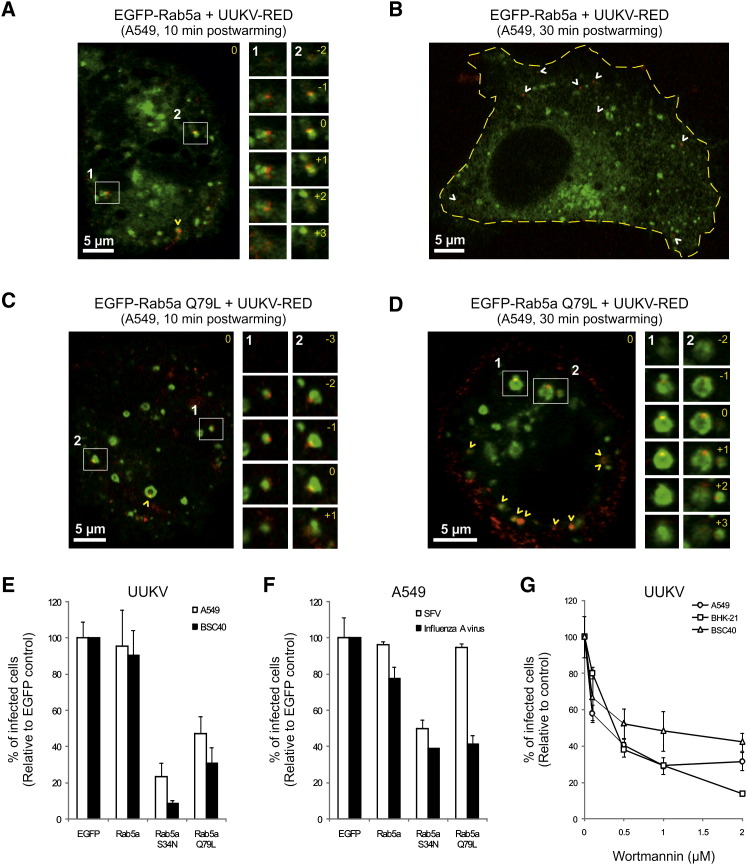
UUKV通过Rab5a-阳性EE进入内吞机制
(A–D)通过共焦显微镜将预结合UUKV-RED(moi~10)进入表达EGFP-Rab5a(A和B)或EGFP-Rab 5a Q79L(C和D)的细胞。 病毒在37°C下内化10分钟(A和C)或30分钟(B和D)。 显示了一个焦平面。 UUKV显示为红色,EE包含EGFP-Rab5a或Q79L显示为绿色。 UUKV和Rab5a阳性囊泡(白色数字和正方形)之间的关联放大倍数较高,显示在右侧边界上,以z叠加序列表示。 黄色数字表示堆栈在序列中与标记为0的原始平面相比的位置。 白色和黄色箭头分别表示非局域化和共局域化的内部化粒子。 黄色虚线划出质膜。
(E) EGFP-Rab5a WT、S34N和Q79L在细胞中瞬时表达。 这些细胞随后感染了UUKV,感染率为2。 使用FACS,根据EGFP信号的强度范围,在每个样本感染后7小时内选择一组细胞。 从该人群中,感染被量化并归一化为EGFP表达细胞。 误差条指示SD。
(F) EGFP-Rab5a WT、S34N和Q79L表达对SFV和甲型流感病毒感染的影响。 按照(E)中所述进行定量。 误差条指示SD。
(G) 用沃特曼预处理细胞并感染UUKV。 将数据归一化为忽略抑制剂的样品。 误差条指示SD。
也观察到UUKV的结球化,空泡中含有LE和溶酶体标记物Rab7a和LAMP-1(EGFP-Rab7a和EGFP-LAMP-1),但时间较晚。 暖化后20–30分钟,活细胞中的大肠杆菌化和与EGFP-Rab7a的协同运动发生( 图7 A和 电影S2 ). EGFP-LAMP-1的结肠化作用在30到40分钟之间最大( 图7 B) ,并观察到协调运动( 电影S3 ). 此时,大多数内化颗粒与EGFP-LAMP-1阳性囊泡相关。 请注意,一些颗粒位于小泡的中间,表明病毒尚未与限制膜融合( 图7 B) ●●●●。
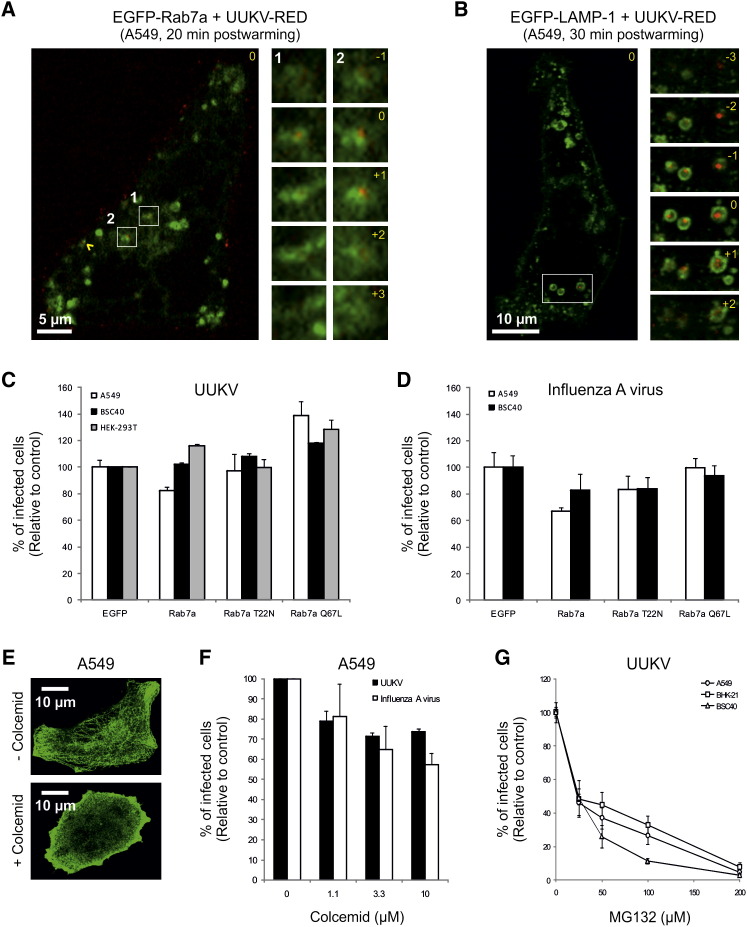
图7。
UUKV进入晚期内膜细胞
(A和B)通过共焦显微镜将预结合UUKV-RED(moi~10)进入表达EGFP-Rab7a(A)或EGFP-LAMP-1(B)的细胞。 病毒在37°C下内化20分钟(A)或30分钟(B)。 显示了一个焦平面。 UUKV为红色,LE为绿色,含有EGFP-Rab7a或EGFP-LAMP-1。 UUKV与Rab7a或LAMP-1阳性囊泡(白色数字和正方形)之间关联的放大倍数较高,显示在右边界上,为z叠加序列。 黄色数字表示堆栈在序列中的位置,与标记为0的原始平面相比。 黄色箭头显示共定位粒子。
(C和D)EGFP-Rab7a WT、T22N和Q67L表达对UUKV和甲型流感病毒感染的影响。 按照中所述进行感染和量化 图4 E.误差条表示SD。
(E) 细胞在冰上用秋水仙素(10μM)处理3小时,然后用抗α-微管蛋白抗体染色并用共焦显微镜分析。
(F和G)细胞用秋水仙素或MG132预处理,然后感染UUKV或甲型流感病毒。 将数据归一化为忽略抑制剂的样品。 误差条指示SD。
通过EE和传染性 为了确定感染性是否需要通过内体隔室,我们首先评估了UUKV在表达Rab5a组成活性突变体(EGFP-Rab5a Q79L)的细胞中的内化和感染。 如图所示,该突变体的表达导致EE增大 图4 C和4D( Stenmark等人。, 1994 ). LE的成熟和货物到溶酶体的运输受到影响( Hirota等人。, 2007 , 罗森菲尔德等人。, 2001 ). 在表达EGFP-Rab5a Q79L的A549和BSC40细胞中,我们发现与仅表达EGFP-Rab5a野生型或EGFP的细胞相比,UUKV感染减少了50%-70%( 图4 E) 。 与EGFP-Rab5a相比,与EGFP_Rab5a Q79L阳性囊泡共定位的病毒数量即使在30分钟后也显著增加( 图4 C和4D)。 此时,几乎所有内化颗粒都与巨大的EE相关,这与向LE和溶酶体的转运受阻相一致。
沃特曼是磷脂酰肌醇(PI)3-激酶(Rab5a的一个重要效应物)的抑制剂,已被证明可以诱导类似的、扩大的早期内吞囊泡的形成( Houle和Marceau,2003年 ). 当细胞用沃特曼预处理时,感染也被有效抑制( 图4 G) ●●●●。
Rab5a显性活性突变体(EGFP-Rab5a S34N)的表达,它取消了新形成EE的成熟( Stenmark等人。, 1994 )也导致两种细胞系的感染率大幅下降(80%-90%)( 图4 E) 。 对另一种晚穿透病毒甲型流感病毒也观察到类似的结果( 图4 F) ●●●●。 有趣的是,Rab5a S34N而不是Rab5aQ79L减少了SFV感染,这表明pH6.0到6.2之间的融合阈值的病毒可以融合在巨大的Rab5a-Q79L阳性EE中,而UUKV和流感a病毒不能融合( 图4 E和4F)。 总之,这些结果表明,感染进入途径包括通过Rab5a阳性内体,但生产性感染也需要运输到下游细胞器。
UUKV感染进入的低pH依赖性 为了测试内体液泡中的酸性pH值在UUKV感染中是否重要,将病毒添加到细胞中,并加入中和液泡pH值的试剂。溶酶体弱碱NH 4 氯和氯喹在所有三种细胞系中均诱导了对UUKV感染的剂量依赖性抑制( 图S4 A) ●●●●。 在这些实验中,我们确保培养基中的pH值不会降至pH~7.0以下,以确保药物的有效性( Mercer等人。, 2010 ).
两种H型液泡抑制剂 + -ATP酶(vATP酶)、巴非霉素A1和刀豆霉素B的结果相似( 图S4 B) ●●●●。 药物溶于乙醇或甲醇中,与二甲基亚砜不同,乙醇或甲醇对感染没有不良影响( 图S5 ). 我们使用四种不同的siRNA来耗尽这些质子泵的V1亚基A(vATPV1A),从而证实了vATP酶的参与。 经western blotting检测,vATPV1A蛋白水平降低了85%–95%( 图S4 C) ●●●●。 沉默导致了对UUKV感染的强烈抑制(从75%到95%)( 图S4 D) ●●●●。 总之,这些结果表明,UUKV感染依赖于液泡酸化。
低pH值是UUKV融合的充分必要条件 为了确定酸诱导步骤是否涉及膜融合,我们评估了UUKV介导细胞-细胞融合(“融合-无融合”)的能力,正如之前对其他包膜病毒所描述的那样( 怀特等人。, 1981 ). 简单地说,大量病毒在低温下与汇合的BHK-21细胞结合,并使用不同pH值的缓冲液对细胞进行加热。当缓冲液的pH值为5.4或更低时,观察到有五个或更多核的融合体的形成( 图5 A) ●●●●。
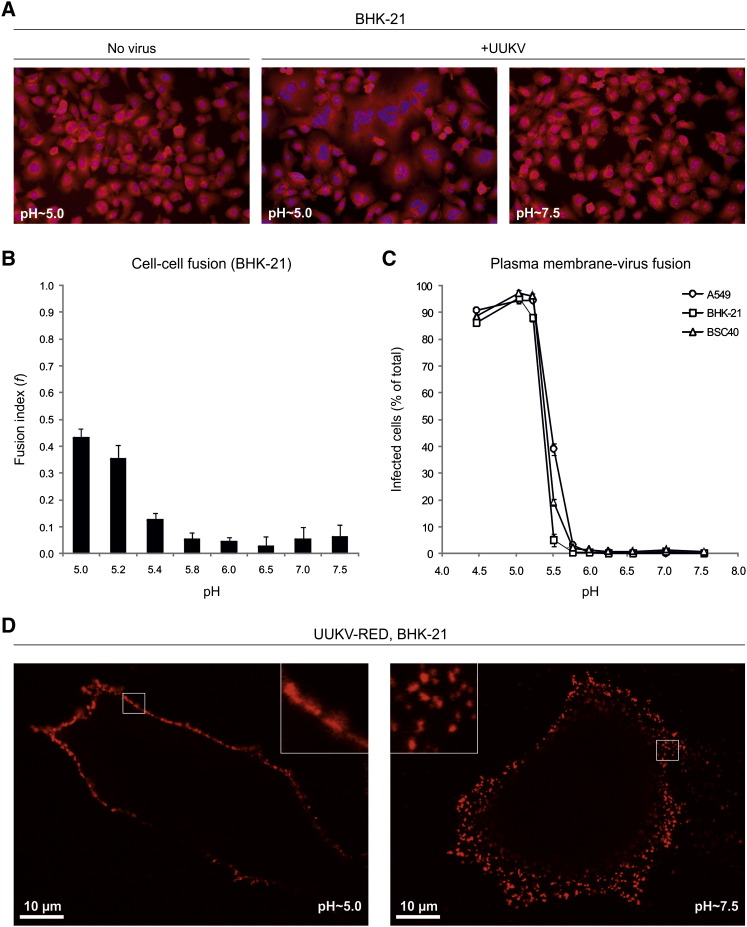
图5。
UUKV膜融合的pH阈值为5.4
(A) 将汇合的单层细胞暴露在冰上的UUKV(moi~1000)中,然后在37°C下用指定pH值的缓冲液处理5分钟。加热3小时后,分别用双苯甲酰亚胺和CellMask深红色对细胞核和细胞质进行染色。
(B) 显示(A)中获得的数据的量化。 融合指数如下所示 (f) = (1 − [ c(c) / n个 ]),其中 c(c) 是融合后字段中的细胞数 n个 核的数量。 错误条指示SD。
(C) 将细胞汇合单层暴露于冰上的UUKV(moi~5–30)中,在37℃下用不同pH值处理1.5分钟,然后在37℃和NH存在下培养18小时 4 Cl(50 mM)阻止内吞小泡进一步渗透。 感染由FACS测定。 错误条指示SD。
(D) 显示使用(C)中描述的协议,UUKV-RED(moi~2)与质膜在一个共焦平面内融合。 角部(白色方块)显示了较高放大倍数的质膜。
融合指数表示每个原始单核细胞融合事件的平均数,用以确定细胞间融合的程度( 图5 B)( 怀特等人。, 1981 ). 当显微镜视野中的所有细胞核都位于单个细胞中时,该指数达到1;当所有细胞都有一个细胞核时,该值为0。 pH~5.2及以下时,BHK-21细胞的融合指数达到0.4( 图5 B) ●●●●。
为了更准确地定义pH值阈值并将融合与感染联系起来,我们评估了UUKV与细胞质膜融合的能力,从而绕过了生产性感染期间内吞作用的需要,正如前面对SFV的描述一样( Helenius等人。, 1980 ). 简单地说,UUKV被允许与冰上的细胞结合,在具有不同pH值和NH的缓冲液中,温度迅速移动到37°C,持续1.5分钟 4 在剩余感染期添加中性pH的含氯培养基,以防止通过内体感染。 确认NH的添加 4 低H处理细胞后,Cl通过内吞病毒防止感染,细胞首先在pH~4.5下处理,然后在NH存在下暴露于UUKV 4 Cl.低pH处理的细胞与模拟处理的细胞一样被感染,NH 4 Cl在两种条件下都能完全抑制感染( 图S6 ).
如所示 图5 C、 旁路手术导致了有效的感染。 与病毒结合量相同的正常感染相比,感染水平实际上增加了一倍(数据未显示)。 原因可能是病毒的内吞作用效率低下。 有趣的是,在使用旁路方案时,通常未感染的raji细胞被感染。 当moi为10时,70%的raji细胞可以通过将病毒与质膜融合而感染。 在A549和BSC40细胞中,旁路的pH值为5.8及以下,而在BHK-21细胞中,所需的pH值略低。 在所有细胞系中,pH~5.4时达到50%的最大感染( 图5 C) ●●●●。
结果表明,pH值的降低足以触发病毒RNP通过质膜融合和感染性渗透到胞浆中。 显然,激活融合或感染该病毒不需要在内胚体隔室中进行额外的处理步骤。 旁路涉及病毒膜的融合,荧光标记糖蛋白G的扩散显示了质膜 N个 和G C类 酸化后进入BHK-21细胞的质膜( 图5 D) ●●●●。 相反,在中性pH条件下,荧光糖蛋白仍然是细胞表面的焦点。 观察到与质膜结合的高密度病毒是由于使用了相对较高的moi(~2)。
晚期内体室的酸激活渗透 为了确定内吞进入后需要酸步骤的时间,我们利用了这样一个事实,即当NH 4 将Cl添加到细胞外培养基中( Ohkuma和Poole,1978年 ). 在低温低moi(~1)条件下结合病毒后,A549细胞迅速转移到37°C和NH 4 加温后不同时间添加的Cl。 很明显,在所有三种细胞系中,感染渗透在5分钟延迟后开始,并在12分钟内达到一半最大水平( 图6 A) ●●●●。 显然,在内吞摄取后的5-30分钟内,个别病毒暴露于pH~5.4或更低的环境中是非同步的。
图6。
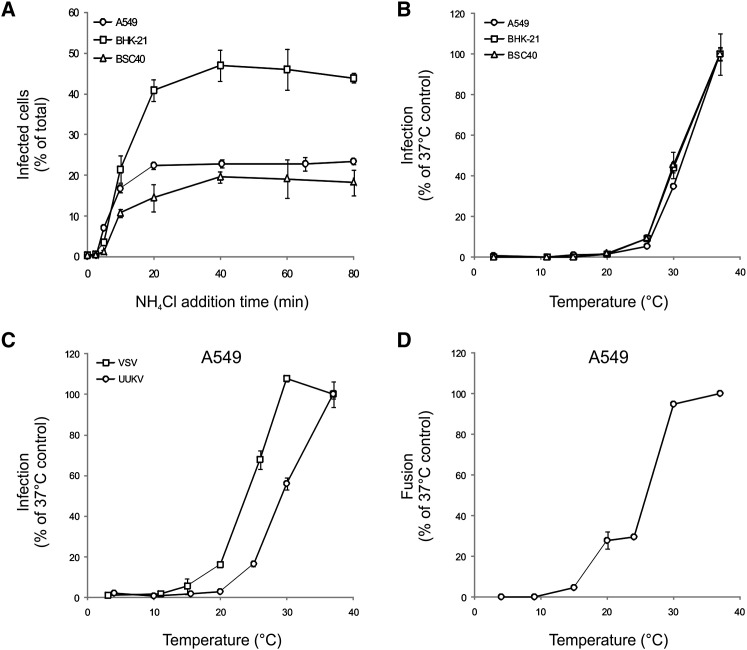
UUKV酸活化穿透在内化后40分钟内发生,且与温度有关
(A) 将细胞暴露于冰上的UUKV,然后转移到37°C以允许内化。 全日空航空公司 4 在不同时间添加Cl以阻止进一步渗透。 误差条指示SD。
(B) UUKV与冰上的细胞结合,将样品转移到不同的温度下1小时。然后在37°C的NH存在下培养受感染的细胞 4 Cl阻止进一步渗透。 误差条指示SD。
(C) 作为一种通过EE进入的原型病毒,VSV被用于(B)中描述的感染检测,并与UUKV进行了温度依赖性比较。 误差条指示SD。
(D) 使用以下描述的血浆膜病毒融合试验在指示温度下评估UUKV融合效率: 图5 C.误差条表示SD。
时间进程表明,LE可能发生穿透。 为了寻求这种可能性,我们确定了入境的温度依赖性,因为众所周知,从EE到LE的货物运输在温度低于20°C时受到限制( Dunn等人。, 1980 ). UUKV在低温下结合后,细胞迅速转移到不同温度下1小时 4 为防止进一步渗透,细胞随后在37°C下孵育,直至感染期结束。 在25°C及以下温度下,蛋白N在所有三种细胞系中的表达均受到强烈抑制( 图6 B) ●●●●。 与UUKV相反,由VSV感染,一种在EE中被酸激活的病毒( Johannsdottir等人。, 2009 )在15°C–20°C的温度下检测到( 图5 C) ●●●●。
为了检查融合过程是否受到温度的影响,我们使用旁路协议评估了UUKV融合的温度依赖性(见上文)。 在30°C时,融合与37°C时一样有效,而感染降低了一半( 图6 B–6D)。 在20°C时,融合仍然是37°C对照组的近30%,而通过正常途径的感染已无法检测到(图 6 B– 三 D) ●●●●。 正如预期的那样,病毒能够在昆虫宿主中复制,这表明融合并不是低温渗透的瓶颈。 这些病毒很可能在20°C及以下温度下没有感染,因为它们没有到达pH值足够低的隔间。
Rab7a是LE成熟和功能的主要组织者( Zhang等人。, 2009 ). 为了评估其在UUKV感染中的作用,我们感染了表达显性阴性或组成型活性突变体(分别为EGFP-Rab7a T22N或EGFP-Rab7a Q67L)的细胞。 在A549和BSC40细胞中,EGFP-Rab7a T22N的表达不能阻止UUKV感染,也不能阻止甲型流感病毒的感染( 图7 C和7D)。 然而,与A型流感病毒相比,EGFP-Rab7a Q67L在所有株系中促进了UUKV感染,感染率高达40%( 图7 C) ●●●●。
在某些细胞类型中,LE的成熟还取决于微管介导的内胚体向细胞核周区域的转运(综述于 Mercer等人。, 2010 )和蛋白酶体活性( Khor等人。, 2003 ). 对于UUKV和甲型流感病毒,秋水仙素治疗使感染率降低30%-40%( 图7 E和7F)。 MG132,一种蛋白酶体抑制剂,已知可将甲型流感病毒从晚期内体转移( Khor等人。, 2003 ),以剂量依赖的方式减少所有三种细胞系中的UUKV感染( 图7 G) 。 总之,这些数据表明,UUKV与甲型流感病毒相似,因为其进入依赖于LE的正常成熟。 它从EE运输到LE,其融合pH值与LE中的主要pH值一致。 它不能感染货物运输到内吞途径降解分支受阻的细胞。
讨论 在本研究中,我们开发了可靠和准确的检测方法来研究动物宿主细胞中的UUKV感染、内吞作用和膜融合,并应用荧光显微镜在其进入程序的各个阶段跟踪UUKV。 用硫代硫酸盐活化荧光染料或[ 35 S] 半胱氨酸和甲硫氨酸,我们利用了UUKV糖蛋白中异常大量的半胱氨酸和甲硫氨酸(分别为55和19),这是布尼亚病毒的典型特征。
无论使用何种细胞系,UUKV与细胞表面的结合都是特异性的,但效率低下。 电镜和荧光显微镜显示与丝状伪足和靠近丝状伪劣基底的质膜区域有优先关联。 这种相互作用在体内可能很重要,因为例如,树突状细胞对某些布尼亚病毒具有耐受性,具有许多树突和丝状伪足( Connolly-Andersen等人。, 2009 ). EM显示,约11nm的空间将质膜与病毒颗粒的膜分隔开,这与最近的冷冻-EM研究一致,该研究表明,尖峰糖蛋白从病毒包膜投射到10-15nm之间( Overby等人。, 2008 ). UUKV受体的身份尚待确定。
结合后,病毒发生内化。 它涉及大约四分之一的表面结合颗粒,占总输入病毒的不到2%。 虽然效率低,但速度快; 内吞阶段在10分钟内完成。如此多的结合病毒未能进入的原因尚不清楚,但对其他病毒如VSV也有类似的观察( Johannsdottir等人。, 2009 ).
据报道,CME对一些正布尼亚病毒、奈罗病毒和汉坦病毒的进入至关重要( Jin等人。, 2002 , Santos等人。, 2008 , Simon等人。, 2009年b ). 通过EM,我们可以在CCP和CCV中观察到一些UUKV颗粒,但这些非常罕见。 大多数位于质膜上的无涂层凹陷处,以及在无涂层的小细胞质小泡内吞后。 这些小泡可能代表CCV在一个不依赖于网格蛋白的途径中失去了其网格蛋白外壳或初级小泡。 与SFV相比,CHC敲低的边际效应可能反映了UUKV使用的内吞途径的多样性,或者网格蛋白在其他过程(如受体循环)中作用的差异。 总之,这些结果表明,大多数UUKV颗粒使用不依赖于网格蛋白的途径进入感染。 在内吞摄取后,在较大的囊泡中观察到病毒,EE、LE和MVE的形态表明,在内化后,病毒被导入经典的内体途径。
包膜病毒的渗透涉及病毒包膜和细胞膜之间的融合。 在大多数情况下,病毒糖蛋白被酸激活后,在内体中触发融合( Mercer等人。, 2010 ). UUKV共享这种渗透策略的第一个迹象是感染对提高空泡pH值的药物的敏感性 4 Cl,我们发现第一批病毒在细胞升温5分钟后达到了依赖酸的阶段,并且一半传入的感染性颗粒通过了NH 4 12分钟内出现Cl敏感性步骤。时间进程与从LE渗透的其他病毒类似,如淋巴细胞脉络膜脑膜炎病毒(LCMV)、甲型流感病毒和小型鼻病毒( Martin和Helenius,1991年 , Prchla等人。, 1994 , Quirin等人。, 2008 ). 这些病毒通过酸敏感步骤的半衰期通常为10-20分钟。相比之下,在EE中融合的病毒,如VSV或SFV,变成NH 4 5分钟内对氯不敏感,因为在酸活化后,氯的吸收几乎是瞬间发生的( Johannsdottir等人。, 2009 , Quirin等人。, 2008 ).
UUKV确实具有酸触发膜融合活性,这从两个方面得到了证明:通过外部添加的病毒颗粒诱导细胞间融合(“无融合”),以及结合病毒与细胞质膜的融合。 在这两种情况下,在pH值低于5.8时触发融合,最佳值为5.4。 这些是相对较低的pH值; 即,与甲型流感病毒相当,因此与LE的渗透性一致。 通过过度表达其他布尼亚病毒的糖蛋白,迫使其到达细胞表面,其他人“从内部”测量了细胞-细胞融合,发现融合体的形成发生在略高的pH值,即5.8–6.4,阈值约为6.0( Filone等人。, 2006 , Plassmeyer等人。, 2007 ). 糖蛋白G到底发生了什么 N个 和G C类 酸化后不清楚。 据报道,它们的生化特性发生了变化( Overby等人。, 2008 , Ronka等人。, 1995 ). 基于其他虫媒病毒糖蛋白的已知结构的计算建模,例如 黄病毒属 或 阿尔法病毒 ,建议G C类 可能负责 布尼亚病毒属 和 汉坦病毒 聚变( 加里和加里,2004年 , Tischler等人。, 2005 ).
UUKV介导的细胞-细胞和病毒-细胞融合证明,低pH值足以触发融合。 埃博拉病毒所观察到的内体蛋白质水解过程显然不需要( Kaletsky等人。, 2007 ). 结果还表明,RNP可以通过质膜以感染形式直接释放到胞浆中。酸激活发生在不到1.5分钟的时间内,与其他酸依赖性病毒观察到的pH触发动力学一致( Wessels等人。, 2007 ). 需要更多的功能研究来确定受体是否在UUKV融合中发挥作用。
从我们的数据中可以清楚地看出,与SFV和A型流感病毒一样,UUKV也依赖于经典内吞系统内的细胞内吞和膜转运进行感染。 抑制EE成熟和同型EE融合的Rab5a S34N的表达影响了所有三种病毒。 相比之下,Rab5a Q79L和沃特曼宁(wortmannin)可导致EE扩张并阻止LE正常成熟,但只影响晚期穿透病毒甲型流感病毒和UUKV。 最近有报道称,细小病毒和人鼻病毒血清2型(HRV2)也有类似的观察结果,这些病毒是晚期穿透的( Brabec等人。, 2006 , Harbison等人。, 2009 ). Rab5a Q79L对SFV感染没有不良影响,这表明巨大EE中的pH值低到足以介导这种早期穿透病毒的融合。 可以得出结论,UUKV通过Rab5a阳性EE,但要具有感染性,它必须到达酸性更强的下游细胞器,最有可能是晚期的内胚层。
其他观察结果支持UUKV的酸激活步骤发生在LE的观点。 一个是NH的时间 4 Cl-抑制步骤(20–40分钟),另一个步骤是在25°C以下观察到的抑制感染。 更直接的是,荧光共聚焦显微镜显示,Rab7a或LAMP-1阳性LE中的颗粒到达时间大致与酸活化时间一致。 对蛋白酶体抑制剂MG132的敏感性反映了对甲型流感和鼠冠状病毒的观察,这些病毒积聚在细胞溶质空泡中,无法感染( Khor等人。, 2003 , Yu和Lai,2005年 ). 还需要进一步的研究来确定泛素化和蛋白酶体在内体成熟中的作用。
与EE的Rab5一样,已知Rab7在晚期内吞室的形成和功能中起着关键作用( Zhang等人。, 2009 ). 它是LE成熟、内体运动以及与溶酶体融合的关键调节因子。 组成活性Rab7a构建物的表达显著增加了UUKV的感染性。 然而,鉴于许多迹象表明UUKV进入LE并利用其进行渗透,令人惊讶的是,非活性突变体Rab7 T22N对感染没有更显著的影响。 然而,还没有发现Rab7 T22N的表达影响其他晚穿透病毒(如LCMV)的感染( Quirin等人。, 2008 ). 对此可能有很多解释,例如Rab7的多种亚型的存在、突变体缺乏显性负效应、突变体Rabs的定位错误等( Bucci等人。, 2000 ). 显然,需要谨慎解释使用Rab7扰动剂的结果,并且需要在各种病毒系统和细胞系中仔细评估内体途径的扰动。
我们的结果表明,UUKV是一种晚期穿透病毒,因此是一组似乎利用LE和可能的内溶体进行穿透或转运的病毒的成员。 这些病毒包括甲型流感病毒、登革热病毒血清2型1株、HRV2、LCMV、犬和猫细小病毒、鼠和猴40多瘤病毒以及人乳头瘤病毒16( Brabec等人。, 2006 , Harbison等人。, 2009 , Mercer等人。, 2010 , Qian等人。, 2009 , Quirin等人。, 2008 , Sieczkarski和Whittaker,2003年 , van der Schaar等人。, 2008 ). 尽管它们使用不同的细胞表面受体、信号通路和主要的内吞机制,但大多数似乎都通过EE,从中它们被归类为内吞途径的降解分支。 EE中没有激活穿透作用。相反,它们与内吞的货物和腔内小泡一起移动到成熟的内体、LE、内溶酶体和深入细胞的溶酶体中。 通常,穿透发生在成熟的内体或LE中,但对于其中一些内体甚至不能排除较晚的隔室。 这些病毒与早期穿透病毒(如SFV和VSV)的主要区别在于,它们的激活pH阈值较低(5.4–5.8),因此穿透的半衰期较长(>10–15分钟)( Mercer等人。, 2010 ). 多瘤家族的病毒是例外,因为它们从晚期的内质体细胞器延续到内质网,在内质网发生渗透( Qian等人。, 2009 ). 与早期穿透病毒不同,晚期病毒对抑制LE正常成熟和货物运输进入内吞途径降解分支的处理敏感。 根据这里给出的结果,UUKV可以被自信地归类为这组有趣的病毒中的一员,其详细的细胞生物学仍然是未来工作的挑战。
实验程序 荧光显微镜 对于共聚焦显微镜,细胞在暴露于UUKV-RED之前被转染,然后用蔡司LSM510 Meta显微镜或旋转圆盘Visitech显微镜进行分析。 对于活细胞成像,在存在病毒的情况下进行分析。 对于基于TCEP的内化分析,使用蔡司Axiovert显微镜监测UUKV-RED的摄取。 为了区分内部颗粒和外部颗粒,使用50 mM TCEP(Pierce,补充50 mM Tris-HCl[pH~8.0]、125 mM NaCl、50 mM HEPES和1 mM MgCl)对样品进行三次处理 2 )固定前,在4°C下保持10分钟。
UUKV感染检测 细胞在37°C下暴露于UUKV(moi从1到10)1小时。 随后用培养基替换病毒上清液,并将细胞在37°C下培养指定时间(最多18小时)。 对于所有感染实验,感染细胞通过流式细胞仪进行定量,如 图S1 B和前面描述的( Quirin等人。, 2008 ). 对于抑制试验,细胞在37°C下用药物预处理30分钟(除秋水仙素外,在冰上3小时),然后在药物存在下暴露于UUKV(moi~2)1小时。 随后将UUKV暴露的细胞在37°C的培养基中培养6小时,并补充药物。 在我们未观察到对细胞活力有任何影响的浓度下使用药物。 对于基于siRNA的感染检测,在感染前1小时清洗转染细胞。 对于基于EGFP-Rabs的感染检测,转染细胞并在6小时后清洗。 转染细胞在转染后18小时暴露于病毒。
细胞-细胞和血浆膜病毒融合检测 如前所述进行细胞-细胞和质膜病毒融合测定( Helenius等人。, 1980 , 怀特等人。, 1981 ). 为了使荧光粒子在质膜(moi~2)处融合,在低pH处理后,将病毒结合细胞固定在中性pH条件下,然后如上所述通过共焦显微镜进行分析。
全日空航空公司 4 Cl添加时间进程 病毒结合(moi~1)在冰上同步。 病毒结合细胞迅速加热至37°C,NH 4 在指定时间(最多80分钟)添加Cl(50 mM)。 随后在37°C下培养细胞,并在暖班后7小时收获。
温度相关性 病毒结合(moi~1)在冰上同步。 病毒结合细胞在水浴中在指定温度下培养1小时,NH 4 然后添加Cl(50 mM)以阻止进一步渗透。 随后将细胞移到37°C,并在升温6小时后收获。
统计分析 这些数据代表了至少三个独立实验,并且给出的值是三倍±标准偏差(SD)的平均值。
致谢 这项工作得到了瑞士国家研究基金会(Swiss National Research Foundation)、欧洲研究委员会(ERC)高级研究员拨款苏黎世联邦理工学院(ETH Zurich)以及玛丽·居里(Marie Curie)在第七届欧洲共同体框架计划(7th European Community Framework Programme)内为P.-Y.L.提供的欧洲内部研究金的支持。 我们感谢F.Rey和J.Huiskonen对手稿的批判性阅读,感谢L.Burleigh和A.Smith对本文的校对。 我们还感谢苏黎世理工大学光学显微镜中心(LMC)的J.Kusch提供的帮助,以及J.Mercer提供的有益讨论。
补充信息 文件S1。 六幅图、一张表、补充实验程序和补充参考文献
电影S1 将UUKV-RED(moi~5)添加到表达EGFP-Rab5a的BSC40细胞中。 通过旋转圆盘共焦显微镜观察细胞。 在37°C的一个焦平面上以0.05 Hz的频率拍摄图像,持续时间不到10分钟。视频以15 Hz的频率显示。 一个粒子(红色)与EGFP-Rab5a阳性囊泡(绿色)一起移动。
电影S2 将UUKV-RED(moi~5)添加到表达EGFP-Rab7a的BSC40细胞中。 通过旋转圆盘共焦显微镜观察细胞。 在37°C下以0.05 Hz的频率拍摄图像,持续时间不到30分钟。视频以15 Hz的频率显示,对应于两个Z堆栈的最大投影。 暖化后约20分钟,一个颗粒(红色)与EGFP-Rab7a-阳性小泡(绿色)一起移动。
电影S3 将UUKV-RED(moi~5)添加到表达EGFP-LAMP-1的BSC40细胞中。 通过旋转圆盘共焦显微镜观察细胞。 在37°C下以0.07 Hz的频率拍摄40分钟的图像。 视频以15 Hz的频率显示,对应于四个Z堆栈的最大投影。 一个颗粒(红色)在20分钟内从质膜移动到EGFP-LAMP-1阳性囊泡(绿色),然后相互作用(长达40分钟)。
工具书类
Brabec M.、Blaas D.、Fuchs R.Wortmann延迟了人鼻病毒血清型2向晚期内吞室的转移。 生物化学。 生物物理学。 Res.Commun公司。 2006; 348:741–749. doi:10.1016/j.bbrc.2006.07.125。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Bucci C.、Thomsen P.、Nicoziani P.、McCarthy J.、van Deurs B.Rab7:溶酶体生物发生的关键。 分子生物学。 单元格。 2000; 11:467–480. doi:10.1091/mbc.11.2467。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Connolly-Andersen A.M.、Douagi I.、Kraus A.A.、Mirazimi A.克里米亚刚果出血热病毒感染人类单核细胞衍生的树突状细胞。 病毒学。 2009; 390:157–162. doi:10.1016/j.virol.2009.06.010。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Doxsey S.J.、Brodsky F.M.、Blank G.S.、Helenius A.通过抗网格蛋白抗体抑制内吞作用。 单元格。 1987; 50:453–463. doi:10.1016/0092-8674(87)90499-5。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Dunn W.A.、Hubbard A.L.、Aronson N.N.,Jr.低温选择性抑制125I-无唾液酸胎球蛋白被灌流大鼠肝脏异噬期间的胞饮小泡和溶酶体之间的融合。 生物学杂志。 化学。 1980; 255:5971–5978. [ 公共医学 ] [ 谷歌学者 ]
Filone C.M.、Heise M.、Doms R.W.、Bertolotti-Ciarlet A.使用α病毒复制子载体开发和鉴定裂谷热病毒细胞融合试验。 病毒学。 2006; 356:155–164. doi:10.1016/j.virol.2006.07.035。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Garry C.E.、Garry R.F.蛋白质组学计算分析表明,布尼亚病毒的羧基末端糖蛋白是II类病毒融合蛋白(β-萜烯)Theor。 生物医学模型。 2004; 1:10. doi:10.1186/1742-4682-1-10。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Harbison C.E.、Lyi S.M.、Weichert W.S.、Parrish C.R.。细小病毒感染细胞的早期步骤:细胞受体结合的宿主特异性差异,但类似的内体贩运。 J.维罗尔。 2009; 83:10504–10514. doi:10.1128/JVI.00295-09。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Helenius A.、Kartenbeck J.、Simons K.、Fries E.关于Semliki森林病毒进入BHK-21细胞的研究。 《细胞生物学杂志》。 1980; 84:404–420. doi:10.1083/jcb.84.2.404。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Hirota Y.、Kuronita T.、Fujita H.、Tanaka Y.Rab5活性在内涵体和溶酶体区室生物发生中的作用。 生物化学。 生物物理学。 Res.Commun公司。 2007; 364:40–47. doi:10.1016/j.bbrc.2007.09.089。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Houle S.、Marceau F.Wortmanin改变缓激肽B2受体的细胞内转运:磷脂酰肌醇3-激酶和Rab5的作用。 生物化学。 J.2003年; 375:151–158. doi:10.1042/BJ20030872。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Jin M.,Park J.,Lee S.,Park B.,Shin J.,Song K.J.,Ahn T.I.,Hwang S.Y.,Ahn.B.Y.,Anhn K.Hantaan病毒通过氯菊酯依赖性受体介导的内吞作用进入细胞。 病毒学。 2002; 294:60–69. doi:10.1006/viro.2001.1303。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Johannsdottir H.K.、Mancini R.、Kartenbeck J.、Amato L.、Helenius A.与水疱性口炎病毒进入相关的宿主细胞因子和功能。 J.维罗尔。 2009; 83:440–453. doi:10.1128/JVI.01864-08。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Kaletsky R.L.、Simmons G.、Bates P.埃博拉病毒糖蛋白的蛋白水解增强了病毒的结合性和传染性。 J.维罗尔。 2007; 81:13378–13384. doi:10.1128/JVI.01170-07。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Khor R.、McElroy L.J.、Whittaker G.R.在流感病毒进入宿主细胞期间,泛素-空泡蛋白分选系统是选择性需要的。 交通。 2003; 4:857–868. doi:10.1046/j.1398-9219.2003.0140.x。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Marsh M.,Helenius A.Semliki Forest病毒的吸附内吞作用。 分子生物学杂志。 1980; 142:439–454. doi:10.1016/0022-2836(80)90281-8。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Martin K.,Helenius A.传入流感病毒核衣壳进入细胞核的转运。 J.维罗尔。 1991; 65:232–244. doi:10.1128/jvi.65.1.232-244.1991。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Mercer J.、Schelhaas M.、Helenius A.通过内吞作用进入病毒。 每年。 生物化学评论。 2010年doi:10.1146/annurev-biochem-060208-104626。 2010年3月2日在线发布。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Ohkuma S.,Poole B.活细胞溶酶体内pH值的荧光探针测量以及各种试剂对pH值的扰动。 程序。 国家。 阿卡德。 科学。 美国1978年; 75:3327–3331. doi:10.1073/pnas.75.7.3327。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Overby A.K.、Pettersson R.F.、Grunewald K.、Huiskonen J.T.从Uukuniemi病毒的电子冷冻断层扫描了解bunyavirus结构。 程序。 国家。 阿卡德。 科学。 美国2008年; 105:2375–2379. doi:10.1073/pnas.0708738105。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Pettersson R.,Kaariainen L.非立方蜱传虫媒病毒Uukuniemi病毒的核糖核酸。 病毒学。 1973; 56:608–619. doi:10.1016/0042-6822(73)90062-7。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Plassmeyer M.L.、Soldan S.S.、Stachelek K.M.、Roth S.M.、Martin-Garcia J.、Gonzalez-Scarano F.拉克罗斯病毒糖蛋白的突变支持Gc(1066-1087)作为融合肽的作用。 病毒学。 2007; 358:273–282. doi:10.1016/j.virol.2006.08.050。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Prchla E.、Kuechler E.、Blaas D.和Fuchs R.从晚期内体中揭开人鼻病毒血清型2的外壳。 J.维罗尔。 1994; 68:3713–3723. doi:10.1128/jvi.68.6.3713-3723.1994。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Qian M.,Cai D.,Verhey K.J.,Tsai B.脂质受体将多瘤病毒从内溶酶体分类到内质网,从而引起感染。 《公共科学图书馆·病理学》。 2009; 5:e1000465。 doi:10.1371/journal.ppat.1000465。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Quirin K.、Eschli B.、Scheu I.、Poort L.、Kartenbeck J.、Helenius A.淋巴细胞脉络膜脑膜炎病毒利用一种新的内吞途径通过晚期内体进入感染。 病毒学。 2008; 378:21–33. doi:10.1016/j.virol.2008.04.046。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Ronka H.、Hilden P.、Von Bonsdorff C.H.、Kuismanen E.Uukuniemi病毒尖峰糖蛋白G1和G2的同二聚体关联。 病毒学。 1995; 211:241–250. doi:10.1006/viro.1995.1397。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Rosenfeld J.L.、Moore R.H.、Zimmer K.P.、Alpizar-Foster E.、Dai W.、Zarka M.N.、Knoll B.J.溶酶体蛋白在GTP-水解缺陷型rab5a表达期间重新分布。 细胞科学杂志。 2001; 114:4499–4508. doi:10.1242/jcs.114.24.4499。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Sachse M.、Urbe S.、Oorschot V.、Strous G.J.、Klumperman J.内体液泡上的双层网格蛋白涂层参与蛋白质向溶酶体的分选。 分子生物学。 单元格。 2002; 13:1313–1328. doi:10.1091/mbc.01-10-0525。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Santos R.I.、Rodrigues A.H.、Silva M.L.、Mortara R.A.、Rossi M.A.、Jamur M.C.、Oliver C.、Arruda E.Oropouche病毒进入HeLa细胞涉及氯氰菊酯,需要进行内体酸化。 病毒研究2008; 138:139–143. doi:10.1016/j.virusres.2008.08.016。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Schmaljohn C.,Nichol S.In:病毒学。 Fields K.D.,编辑。 Lippincott Williams&Wilkins; 费城:2007年。 布尼亚病毒科; 第1741-1788页。 [ 谷歌学者 ]
Sieczkarski S.B.、Whittaker G.R.对流感病毒和其他包膜病毒内吞的Rab5和Rab7的不同需求。 交通。 2003; 4:333–343. doi:10.1034/j.1600-0854.2003.0090.x。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Simon M.、Johansson C.、Lundkvist A.、Mirazimi A.克里米亚-刚果出血热病毒复制周期中的微管依赖和微管依赖步骤。 病毒学。 2009; 385:313–332. doi:10.1016/j.virol.2008.11.020。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Simon M.、Johansson C.、Mirazimi A.克里米亚-刚果出血热病毒的进入和复制依赖于网格蛋白、pH值和胆固醇。 《病毒遗传学杂志》。 2009; 90:210–215. doi:10.1099/vir.0.006387-0。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Stenmark H.,Parton R.G.,Steele-Motimer O.,Lutcke A.,Gruenberg J.,Zerial M.抑制rab5 GTPase活性可刺激内吞过程中的膜融合。 EMBO J.1994; 13:1287–1296. doi:10.1002/j.1460-2075.1994.tb06381.x。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Tischler N.D.、Gonzalez A.、Perez-Acle T.、Rosemblatt M.、Valenzuela P.D.汉坦病毒Gc糖蛋白:II类融合蛋白的证据。 《病毒遗传学杂志》。 2005; 86:2937–2947. doi:10.1099/vir.0.81083-0。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
von Bonsdorff C.H.,Pettersson R.Uukuniemi病毒的表面结构。 J.维罗尔。 1975; 16:1296–1307. doi:10.1128/jvi.16.5.1296-1307.1975。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
van der Schaar H.M.、Rust M.J.、Chen C.、van der Ende-Metselaar H.、Wilschut J.、Zhuang X.、Smit J.M.通过活细胞中的单粒子追踪分析登革热病毒的细胞进入途径。 《公共科学图书馆·病理学》。 2008; 4:e1000244。 doi:10.1371/journal.ppat.1000244。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Wessels L.、Elting M.W.、Scimeca D.、Weninger K.单个病毒颗粒与支撑脂质双层的快速膜融合。 生物物理学。 J.2007年; 93:526–538. doi:10.1529/biophysj.106.097485。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
White J.、Matlin K.、Helenius A.Semliki Forest的细胞融合、流感和水泡性口炎病毒。 《细胞生物学杂志》。 1981; 89:674–679. doi:10.1083/jcb.89.3.674。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Yu G.Y.,Lai M.M.在病毒进入期间,泛素蛋白酶体系统促进小鼠冠状病毒从内体转移到细胞质。 J.维罗尔。 2005; 79:644–648. doi:10.1128/JVI.79.1.644-648.2005。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Zhang M.、Chen L.、Wang S.和Wang T.Rab7:在膜贩运和疾病中的作用。 Biosci公司。 2009年代表; 29:193–209. doi:10.1042/BSR20090032。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
关联数据 本节收集本文中包含的任何数据引用、数据可用性声明或补充材料。
补充资料 文件S1。 六幅图、一张表、补充实验程序和补充参考文献
电影S1 将UUKV-RED(moi~5)添加到表达EGFP-Rab5a的BSC40细胞中。 通过旋转圆盘共焦显微镜观察细胞。 在37°C的一个焦平面上以0.05 Hz的频率拍摄图像,持续时间不到10分钟。视频以15 Hz的频率显示。 一个粒子(红色)与EGFP-Rab5a阳性囊泡(绿色)一起移动。
电影S2 将UUKV-RED(moi~5)添加到表达EGFP-Rab7a的BSC40细胞中。 通过旋转圆盘共焦显微镜观察细胞。 在37°C下以0.05 Hz的频率拍摄图像,持续时间不到30分钟。视频以15 Hz的频率显示,对应于两个Z堆栈的最大投影。 暖化后约20分钟,一个颗粒(红色)与EGFP-Rab7a-阳性小泡(绿色)一起移动。
电影S3 将UUKV-RED(moi~5)添加到表达EGFP-LAMP-1的BSC40细胞中。 通过旋转圆盘共焦显微镜观察细胞。 在37°C下以0.07 Hz的频率拍摄40分钟的图像。 视频以15 Hz的频率显示,对应于四个Z堆栈的最大投影。 一个颗粒(红色)在20分钟内从质膜移动到EGFP-LAMP-1阳性囊泡(绿色),然后相互作用(长达40分钟)。
Cell Host&Microbe的文章由提供 爱思维尔