引言 类风湿关节炎(RA)的特征是全身炎症状态,主要影响关节,也影响其他器官,如皮肤、眼睛、肺和心血管系统 1 RA患者分为两组:血清阳性型和血清阴性型。 类风湿因子(RF)和抗环瓜氨酸肽(抗CCP)抗体是血清阳性RA患者的特征 2 与血清阴性RA患者相比,血清阳性RA患者中存在抗CCP抗体与更持久的炎症、更大的侵蚀性关节损伤、更严重的临床表现和更糟糕的预后相关 三 RF参与疾病发展的情况尚不清楚; 然而,有人认为这种自身抗体增强了抗CCP的病理作用 4 这些自身抗体识别抗原后,形成的免疫复合物可以激活循环和关节中的单核吞噬细胞,促进炎症介质的分泌,如TNF-α、IL-6和IL-1β 5 这些细胞因子是RA全身炎症的生物标志物,有助于该病的免疫病理学,因为它们的阻断与临床改善和缓解相关 6 —— 8 .
了解哪些循环因素会导致RA患者的全身炎症,对于找到更有希望的干预和治疗方案至关重要。 RA患者的循环和滑液中检测到大量细胞外小泡(EV) 9 , 10 EVs在RA发病机制中的作用已开始阐明; 例如,这些囊泡表达自身抗原,如瓜氨酸肽(CP),形成IC,并参与miRNA的传递和成纤维细胞样滑膜细胞的激活 11 EV有助于细胞间通信,对免疫反应(主要是单核细胞和巨噬细胞)有广泛的影响,并诱导TNF-α、IL-6和IL-1β的产生 11 , 12 .
不同的细胞成分参与炎症的发展,包括中性粒细胞、肥大细胞、T和B淋巴细胞以及单核细胞/巨噬细胞。 这些细胞的激活导致产生细胞因子和炎症介质。 更具体地说,在RA中发现单核细胞/巨噬细胞被激活 13 —— 15 在RA中大量浸润滑膜 16 , 17 ,并产生TNF-α 17 在RA患者中已经表明,循环EV形成IC(EV IC) 10 , 18 中性粒细胞诱导白三烯生成 在体外 这表明这些小泡可能参与炎症过程。 我们认为EV可以激活循环中的单核细胞,并有助于RA的全身炎症过程,类似于在其他全身性自身免疫疾病中观察到的情况 19 然而,EV对单核细胞的影响以前并未与RA相关。 因此,我们评估了血清阳性RA患者的循环EV和单核细胞是否与全身炎症反应有关,并评估了EV和EV-IC在单核吞噬细胞中的直接作用。
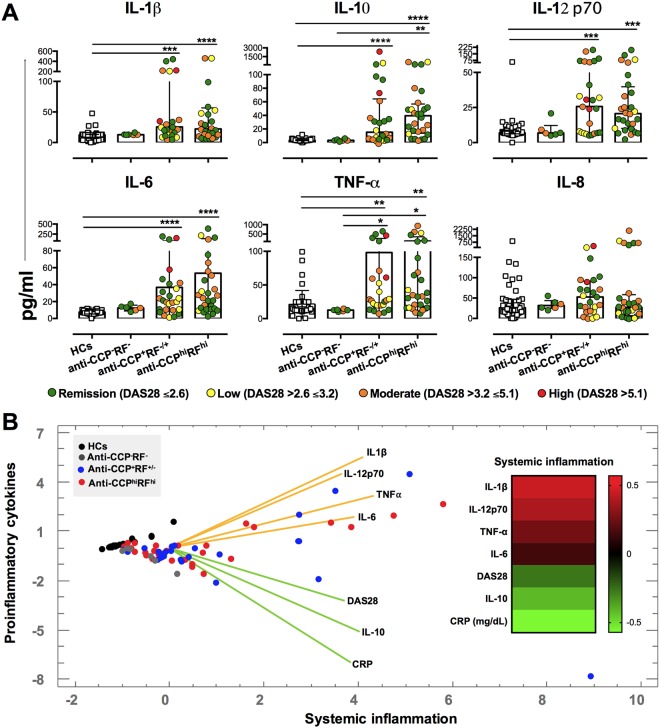
结果 血清阳性患者的全身炎症反应以高血清TNF-α、IL-6和IL-1β水平为特征 在不同的全身炎症过程中,血清细胞因子水平发生了变化。 测定血清细胞因子作为RA患者全身炎症状态的指标。 如图所示 1安培 根据疾病活动度评分(DAS)−28对患者进行疾病活动度分类,发现细胞因子浓度变化较大; 病情缓解或活动度低的患者血清细胞因子浓度升高或极低。 然而,当患者根据血清阳性进行分类时,抗CCP组 + 射频 +/− 和反CCP 你好 射频 你好 与健康对照组(HCs)相比,(血清阳性)患者的TNF-α、IL-6、IL12p70和IL-1β水平显著升高,但IL-8水平没有升高; 反CCP − 射频 − (血清阴性)患者没有表现出这种增加(图 1安培 ). 有趣的是,当我们评估其他系统性自身免疫性疾病(SADs)患者的细胞因子水平时,例如系统性红斑狼疮(SLE),我们没有发现与HCs相比,促炎性细胞因子血清浓度存在差异(数据未显示)。 这些发现表明,所有SAD患者的血清细胞因子浓度没有增加,可能是血清阳性RA患者的特征(抗CCP + 射频 +/− 和反CCP 你好 射频 你好 ).
图1。
血清阳性RA患者(抗CCP + 射频 +/− 和反CCP 你好 射频 你好 )与血清阴性患者和HC患者相比,血清细胞因子水平升高。 ( A类 )RA患者血清IL-1β、IL-10、IL-12p70、IL-6、TNF-α和IL-8水平(抗CCP − 射频 − ,反CCP + 射频 +/− 和反CCP 你好 射频 你好 )和HC。 患者根据DAS28缓解水平进行分类(DAS28≤2.6,绿点); 低活性(DAS28>2.6–≤3.2,黄点); 中等活性(DAS28>3.2–≤5.1,橙色圆点); 和高活性(DAS28>5.1,红点)。 通过Kruskal–Wallis检验和Dunn’s检验对各组进行比较 事后的,事后的 测试。 ( B类 )PCA对比血清阳性和血清阴性RA和HCs患者的促炎细胞因子(IL-1β、IL-12p70、IL-6和TNF-α)以及CRP、IL-10和DAS28变量。 主成分分析内部的热图(右)显示了成分2中每个变量(促炎细胞因子)的权重。
进行主成分分析(PCA),以确定血清阳性和血清阴性RA和HCs患者的血清细胞因子(IL-1β、IL-12p70、IL-6、TNF-α和IL-10)、C反应蛋白(CRP)和DAS28变量之间的相关性(图 1B年 ). PCA显示了两个成分,解释了65%的变异性,并使两组之间的变量得以分离:一组与包括大多数血清阳性患者的促炎细胞因子相关,另一组与CRP、IL-10、, DAS28与血清阳性/阴性无明显相关性。 HCs和反CCP − 射频 − 两组患者都没有根据这些变量进行定义,而是保持在一起。 利用每个变量的主成分分析得到的特征值,创建了一个热图。 热图显示,细胞因子IL-1β、IL-12p70、TNF-α和IL-6对血清阳性患者的定义优于DAS28和CRP(图 1B年 ).
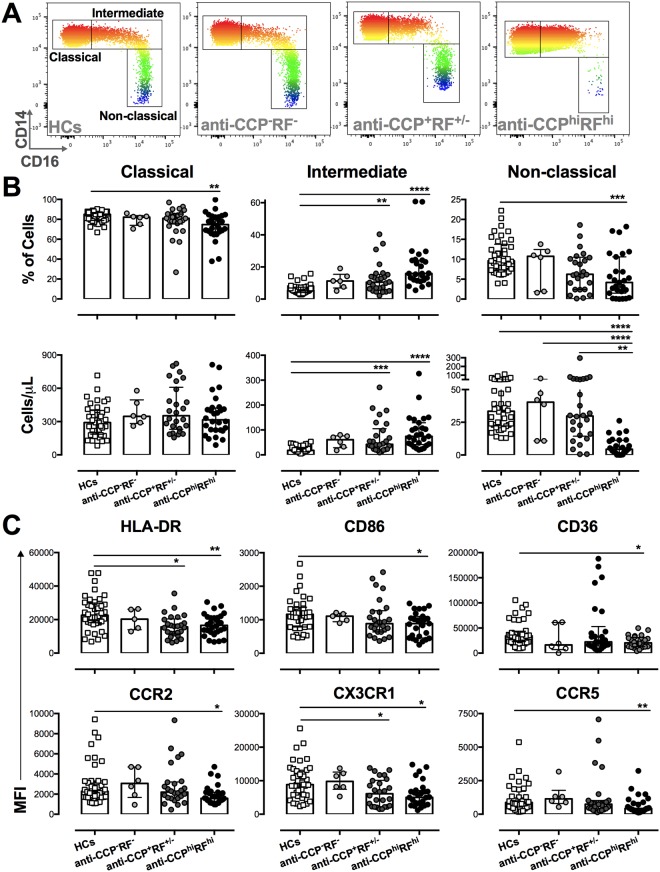
血清阳性RA患者中间单核细胞计数高 循环单核细胞亚群频率的改变 20 和激活总单核细胞产生促炎细胞因子 13 —— 15 已在RA患者中描述。 因此,我们评估了单核细胞亚群的数量、频率和表型是否与RA患者的血清阳性相关。 在抗CCP中观察到经典单核细胞比例下降 你好 射频 你好 患者,这没有反映在绝对计数中(图 2A、B ). 与HCs相比,血清阳性患者中中间单核细胞的比例和计数均显著升高。 此外,非经典单核细胞在抗CCP中的比例和数量均减少 你好 射频 你好 患者(图 2A、B ). 对中间单核细胞中与EV识别和单核细胞亚群迁移相关的受体的表达进行评估,因为这些细胞在血清阳性患者中的计数和频率受影响最大。 血清阳性患者HLA-DR和CX3CR1低表达,抗CCP患者CD86、CD36、CCR2和CCR5低表达 你好 射频 你好 将患者与HCs进行比较(图 2摄氏度 ). 与抗CCP相比,在血清阴性患者的所有单核细胞亚群中发现CD18的低表达 你好 射频 你好 患者和HC(未显示数据)。
图2。
血清阳性患者中间单核细胞计数高。 ( A类 )每个研究组1名个体的全血中CD45+HLA-DR+细胞上的单核细胞亚群(CD14++CD16-(经典)、CD14++CD16+(中间)和CD14+CD16++(非经典)单核细胞)的代表性CD14和CD16热图。 ( B类 )抗CCP经典、中间和非经典单核细胞的频率(上面板)和绝对计数(下面板) − 射频 − ,反CCP + 射频 +/− 和反CCP 你好 射频 你好 RA患者和HC。 ( C类 )抗CCP中间单核细胞上HLA-DR、CD86、CD36、CCR2、CX3CR1和CCR5的MFI − 射频 − ,反CCP + 射频 +/− ,反CCP 你好 射频 你好 RA患者和HC。 通过Kruskal–Wallis检验和Dunn’s检验对各组进行比较 事后的,事后的 测试。
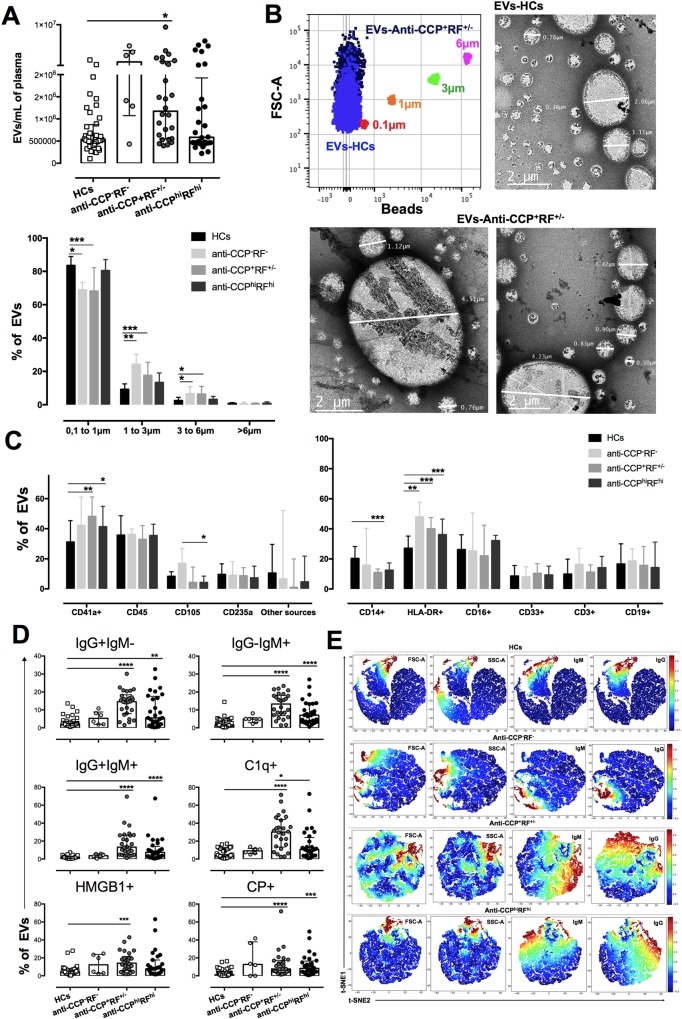
血清阳性患者的EV是血小板衍生、CPs+和形成IC 最近的报告表明EV在自身免疫性疾病中起着关键作用 21 , 22 因为对单核吞噬细胞和免疫系统的其他成分有不同的多效性作用 21 所有RA患者的EV计数均升高; 然而,只有反CCP + 射频 +/− 与HCs相比,患者表现出显著差异(图 3A级 ). 关于电动汽车规模的分销,反CCP − 射频 − 和反CCP + 射频 +/− 患者的0.1–1.0µm EV比例显著降低,1–3.0µm和3–6.0µm的EV比例升高(图 3A、B ). 还研究了EV表型以确定细胞来源。 血清阳性患者EV-CD41a+比例升高,抗CCP − 射频 − 与抗CCP组相比,该组EV-CD105+升高 你好 射频 你好 患者(图 3C公司 ). 考虑到约50%的EV来自白细胞(EV-CD45+),我们评估了不同的白细胞来源。 所有患者组EV-HLA-DR+频率均升高,EV-CD14+频率似乎降低,但差异仅在抗CCP方面具有统计学意义 + 射频 +/− 组(图 3C公司 ).
图3。
血清阳性患者和HC的循环EV在数量、细胞来源和表型上不同。 等离子电动汽车( A类 )反CCP中不同大小的计数(以上)和频率(以下) − 射频 − ,反CCP + 射频 +/− 和反CCP 你好 射频 你好 RA患者和HC; ( B类 )左(上),反CCP FSC-A电动汽车代表点图 + 射频 +/− 患者和HC,具有不同大小的太平洋蓝色珠子的强度。 右(上图),HC和反CCP电动汽车的代表性显微照片 + 射频 +/− 患者(如下)使用STEM。 ( C类 )左:来自不同细胞来源的循环EV的频率:血小板(CD41a)、白细胞(CD45)、内皮细胞(CD205)、红细胞(CD235a)和来自抗CCP的其他来源(评估分子的EV阴性) − 射频 − ,反CCP + 射频 +/− 和反CCP 你好 射频 你好 RA患者和HC。 右:抗CCP中不同白细胞来源循环EV的频率 − 射频 − ,反CCP + 射频 +/− 和反CCP 你好 射频 你好 RA患者和HC。 ( D类 )抗CCP抗体IgG+IgM-、IgG-IgM+、IgG+IgM+C1q+、HMGB1+和CP+阳性循环EV的频率 − 射频 − ,反CCP + 射频 +/− 和反CCP 你好 射频 你好 RA患者和HC。 通过Kruskal–Wallis试验和Dunn试验对研究组进行比较 事后的,事后的 测试。 ( E类 )电动汽车的集体t-SNE(1×10 5 )从每组分析并绘制的五个样本中得出(n=20)。 每个点代表单个EV,颜色表示在EV上分析和计算的每个给定标记的ArchSinh5转换表达值,从蓝色表示低表达到红色表示高表达的所有样本。
除了EV细胞来源外,还评估了参与RA生理病理学的EV成分。 血清阳性患者的EV-IC(IgG+IgM-、IgG-IgM+和IgG+IgM+EV-CPs)和EV-CPs+显著高于HCs患者。 反中共 + 射频 +/− EV-C1q+和EV-High-mobility group box 1(HMGB1)+频率高于其他组; 血清阴性患者的EVs与HCs相似(图 三维 ). RA患者EV-IC、EV-CPs+、EV-C1q+和EV-HMGB1+的细胞来源均为白细胞和血小板; 然而,血小板是血清阳性患者的主要来源(数据未显示)。 为了说明EV中IC含量的变化,随机选择RA和HCs患者每组的5名代表性个体,并进行t分布随机邻域嵌入(t-SNE)分析。 正如预期的那样,与HCs和血清阴性患者相比,血清阳性RA患者的水泡具有更高的频率,EV-IgM+和EV-IgG+的分布更广(图 第三方 ).
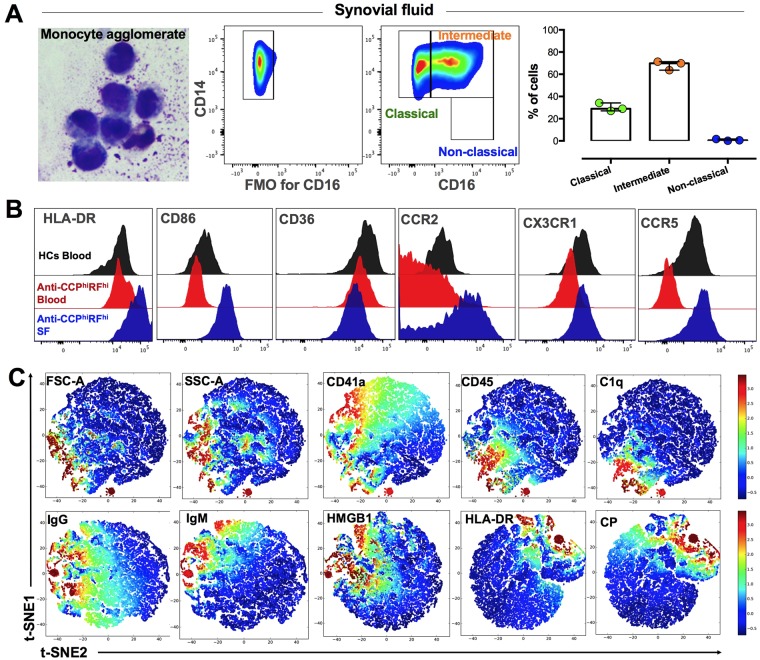
滑液和循环中的EV和单核细胞亚群具有一些共同特征 为了评估血清阳性患者循环中观察到的EV和单核细胞亚群表型是否也能在这些患者的滑液中发现,一种抗CCP的SF + 射频 +/− 和两个反CCP 你好 射频 你好 对患者进行评估。 大约20%的SF浸润细胞对应于单核细胞,引人注目的是,70%的这些细胞对应于中间单核细胞(图 4A级 ). 然而,与相同患者的循环细胞相比,SF的中间单核细胞中HLA-DR、CD86、CCR2、CX3CR1、CCR5和CD32的每细胞表达更高,而CD36、CD11b和FcμR的每细胞表现更低(图 4B类 和数据未显示)。 有趣的是,与HC相比,24小时培养的血清阳性RA患者的单核吞噬细胞的CD32表达更高,CD11b、CD36和FcμR表达更低(补充图 1 —— S1(第一阶段) ). 然后,患者SF中观察到的吞噬细胞一旦开始组织分化过程,就可以获得这种表型 23 .
图4。
血清阳性患者的EV和单核细胞在SF和血液中表现出一些相似的特征。 ( A类 )从左到右; 图为SF中抗CCP的单核细胞凝聚体 你好 射频 你好 病人。 抗CCP SF中CD45+HLA-DR+细胞上单核细胞亚群CD16伪彩色图的代表性CD14和FMO 你好 射频 你好 病人。 三名血清阳性患者SF中单核细胞亚群的频率。 ( B类 )HC(灰色)血液中中间单核细胞的HLA-DR、CD86、CD36、CCR2、CX3CR1和CCR5的代表性直方图 你好 射频 你好 患者(红色)和来自同一患者的SF(蓝色)。 ( C类 )电动汽车的总t-SNE(1×10 5 )对来自血清阳性RA患者的三份SF样本进行分析和绘图。 每个点表示单个EV,颜色表示在EV上分析和计算的给定参数的ArcSinh5转换表达式值,从蓝色表示低表达到红色表示高表达。
对于SF的EV以及与循环EV相似的EV,血小板和白细胞是这些囊泡的主要来源; 此外,规模较大(FSC-A)和复杂性较大(SSC-A)的EV是SF中主要形成IC的EV; 这些EV还含有不同比例的HMGB1、HLA-DR和CP(图 4摄氏度 ).
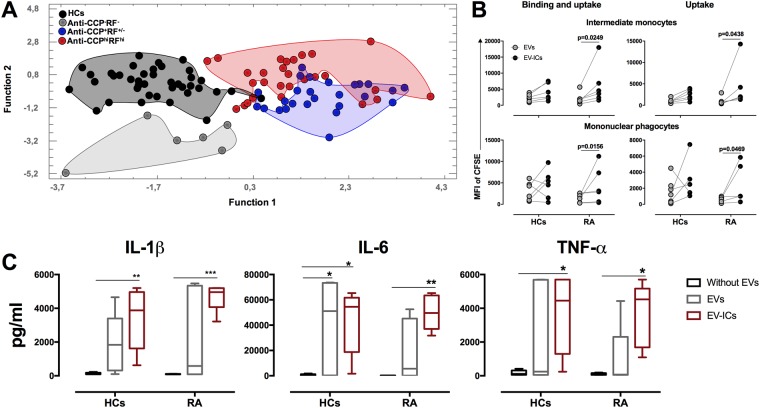
EV、中间单核细胞和促炎细胞因子可根据血清阳性率对RA患者进行鉴别 为了确定RA患者单核细胞亚群和EV中评估的变量与自身抗体水平和全身炎症相关,对患者和HC样本进行了判别分析。 包括23个预测变量,包括中间单核细胞计数和受体(CD16、CD64、CD32、CD86、HLA-DR、CCR2、CCR5、CX3CR1)、三个单核细胞亚群的CD18、细胞因子(IL-6、IL1β和TNF-α),以及IgG、IgM、HMGB1、CP、CD41a和HLA-DR阳性EV的频率。 四个研究组通过这些变量进行了显著区分(p<0.05),置信水平为95%。 然而,反CCP 你好 射频 你好 和反CCP + 射频 +/− 患者出现轻微重叠。 有趣的是,尽管HCs和反CCP − 射频 − 分离到同一侧,它们被相互排斥(图 5A级 )这表明EV和中间单核细胞与血清阳性患者的全身炎症密切相关。
图5。
EV、中间单核细胞和促炎细胞因子的变量可区分RA患者的血清阳性和血清阴性,而EV可诱导吞噬细胞单核激活。 ( A类 )对23个变量进行判别分析,包括中间单核细胞计数和受体MFI(CD16、CD64、CD32、CD86、HLA-DR、CCR2、CCR5、CX3CR1)、三个单核细胞亚群的CD18、血清促炎细胞因子(IL-6、IL1β和TNF-α)以及抗CCP抗体IgG、IgM、HMGB1、CP、CD41a和HLA-DR阳性EV的频率 − 射频 − (灰色圆圈云),反CCP + 射频 +/− (蓝色圆圈云)和反中共 你好 射频 你好 (红圈云)RA患者和HC(黑圈云)。 ( B类 )HCs和血清阳性患者培养24小时的中间单核细胞(如上)和单核吞噬细胞对EVs和EVs-IC的结合和摄取(左面板)以及摄取(右面板)(囊泡:细胞比3:1)。 采用Wilcoxon符号秩检验(n=7)对各组进行比较。 ( C类 )在存在或不存在EVs和EVs-IC的情况下培养120小时的HC和RA患者单核吞噬细胞上清液中IL-1β、IL-6和TNF-α的水平(3:1囊泡:细胞比)。 使用双向方差分析和Bonferroni’s进行组间比较 事后的,事后的 测试(n=7)。
血清阳性患者的EV诱导单核吞噬细胞产生促炎细胞因子 为了评估血清阳性患者的EV是否诱导与血清阳性患者检测到的全身炎症相关的细胞因子的产生,我们首先评估了这些囊泡的结合和内化。 RA患者24小时培养的中间单核细胞和单核吞噬细胞结合并内化的EV-IC水平高于未经补体处理的EV(图 5亿 ). 最后,我们发现,对于EVs(主要是EV-IC),RA患者和HCs的单核吞噬细胞上清液中积累了IL-1β、IL-6和TNF-α(图 5摄氏度 )这表明单核吞噬细胞在与EV相互作用后,可能导致血清阳性患者的全身炎症。
讨论 多项研究已经确定了几种反映RA全身炎症的循环细胞因子和趋化因子 24 , 25 然而,对造成这种情况的部件知之甚少。 我们观察到血清阳性RA患者血清细胞因子IL-1β、IL-12p70、IL-6和TNF-α水平较高; 相反,血清阴性和SADs患者的这些细胞因子水平没有升高。 血清阳性患者还表现出循环EVs对CD41a、IgG、IgM和CP的高阳性率,以及单核细胞亚群(主要是中间亚群)的计数、频率和受体表达发生改变。 这些变化在更接近HCs的血清阴性患者中未观察到。 实际上,血清阳性患者的EV-IC比EV更能诱导RA患者和HCs的单核吞噬细胞产生IL-1β、IL-6和TNF-α 在体外 。在RA患者的中间单核细胞和EV中观察到的任何一种变化都与DAS28评估的疾病活动性无关(图 S2系列 和数据未显示)。 因此,这些结果和判别分析表明,在RA中,血清阳性患者是那些主要表现为全身炎症的患者,这似乎可以部分解释为EVs对单核吞噬细胞的影响。 目前认为血清阳性和血清阴性是两种不同的RA实体,每种RA实体都有其自身的发病机制、病程和涉及的基因 26 .我们的结果与此假设一致,因为血清阳性患者的疾病更严重,预后更差 27 ,表现出明显的全身炎症。
根据RA患者的血清阳性状态,确定了不同的循环成分,如细胞因子、EV和单核细胞亚群。 一些研究分析了IL-17、IL-15 28 和IL-33 29 抗CCP阳性的细胞因子。 其他研究的重点是评估SF中的细胞因子; 哥梅斯·普埃尔塔 等 2013年 三 发现抗CCP+患者的细胞因子IL-1β、IL-10、IL-17和CCL20趋化因子水平高于血清阴性患者。 然而,尚不清楚这些患者的局部炎症过程和全身炎症过程之间是否存在关联。 最近的证据表明,细胞因子在抗瓜氨酸蛋白抗体(ACPA)阳性RA患者中发挥着重要作用。 据观察,滑膜ACPA阳性患者的SF中IL-6、IL-17和IL-8水平显著升高,RA患者的IL-8与中性粒细胞计数和不良临床表现呈正相关 30 另一项研究表明,破骨细胞暴露于ACPA后会优先释放IL-8,IL-8介导这些细胞的自分泌活化 31 虽然我们没有发现血清阳性患者与HCs和血清阴性患者的血清IL-8水平存在显著差异,但值得注意的是,我们评估了该细胞因子的血清浓度,而不是SF浓度。 因此,IL-8可能参与关节炎症而非全身炎症。 此外,值得注意的是,IL-8往往与RA中自身抗体的初始攻击有关,其中这种细胞因子似乎与诱导初始骨吸收有关,与血管翳形成和炎症疼痛相比,它与更高的神经病理性疼痛有关 32 , 33 .
我们的结果表明,循环细胞因子和DAS28之间的弱相关性表明,全身炎症过程并不总是与关节炎症相一致。 这表明仅根据DAS28的关节承诺将疾病归类为活动性疾病 2 不足以确定全身和非关节炎症患者。 此外,我们观察到,并非所有DAS28高的患者都表现出高水平的循环炎症细胞因子。 这可以用与全身炎症过程无关的关节疼痛的产生来解释,因为关节的感觉神经元可以在没有局部炎症、组织损伤或感染的情况下触发RA疼痛 34 此外,RA过程中经常会出现不可逆的破坏性关节损伤,即使炎症过程消退后仍会感到疼痛。 因此,DAS28是一个客观评分,可能会导致对疾病活动的高估,因为它可能会受到压痛关节计数参数的显著影响。 因此,仅在DAS28中对RA患者进行临床评估可能会导致对总疾病活动(关节和全身)的不准确反映。
此前已经证明 在体外 EV-ICs引起中性粒细胞产生白三烯-B4的显著上调 10 ; 然而,一些研究表明,单核细胞/巨噬细胞是炎症RA关节中促炎细胞因子和趋化因子的主要来源,包括TNF-α和IL-1β 35 在这里,我们观察到EV,尤其是RA患者的EV-IC,通过HCs和RA患者的单核吞噬细胞诱导IL-6、IL-1β和TNF-α的产生。 虽然关节中的炎症过程可能有助于循环细胞因子 36 我们的数据表明,这些介质的其他循环来源似乎存在于血清阳性患者中; 特别是,我们的数据支持EV-IC及其与单核细胞的相互作用可能是导致这种现象的原因。 然而,单核细胞是否是循环水平血清阳性患者促炎细胞因子的主要来源仍有待调查。
循环细胞因子和改变的EV能够影响远端组织的功能,包括脂肪、骨骼肌、肝脏和血管内皮 37 , 38 已有研究表明,细胞因子水平的长期升高,无论其大小或原因如何,都会产生一系列致动脉粥样硬化的改变,包括RA患者的胰岛素抵抗、血脂异常、血栓前效应、促氧化应激和内皮功能障碍 25 定义这些患者全身炎症的能力可以更好地确定治疗的类型和剂量,以防止与血清阳性RA相关的共病和/或避免疾病复发。 因此,评估血清细胞因子,以及EV和单核细胞中的一些变量,可能是患者随访的一个有希望的工具。 此外,在DAS28定义的缓解状态下识别RA患者的全身炎症,可以为RA的发病机制提供重要的见解,并可用于指导这些患者开始使用疾病修饰药物。
与之前的研究一致 9 , 10 我们发现血小板是RA患者最常见的EV来源; 此外,我们的研究表明,这主要发生在血清阳性患者中。 此外,这些患者循环中EV-IC+和EV-CP+的频率最高,这表明这些结构是RA患者循环和SF中IC、自身抗原和DAMP的重要来源,正如其他人之前提出的那样 10 , 18 , 21 , 22 在缺乏胶原受体糖蛋白(GP)VIa的RA小鼠模型中,血小板耗竭可减轻炎症性关节炎,产生较少数量的血小板衍生EV 体内 与对照组小鼠相比,脚踝厚度较小,骨骼和软骨侵蚀较差 9 ,这表明这些血小板衍生的小泡在关节炎的发病机制中具有重要作用。
在抗CCP+RF+/-患者与HCs中,观察到EV-CD14+显著降低。 CD14有两种形式; 由糖基磷脂酰肌醇尾(mCD14)和可溶性形式(sCD14)固定在膜上的形式 39 据描述,在炎症条件下,CD14可以从单核细胞膜释放到培养环境中 40 因此,在RA血清阳性患者的EVs中观察到的这种分子的减少频率可能是基于上述现象。 事实上,有报道称RA患者sCD14血水平升高 41 此外,在所有RA患者组中观察到EV-HLA-DR+的频率增加,以及血小板衍生EV的高频率。 虽然HLA-DR在健康人的血小板或血小板衍生EV中的表达尚未观察到,但以前在患有自身免疫性疾病(如急性特发性血小板减少性紫癜)的患者的血小板中也有描述 42 对类似患者的研究表明,血小板衍生EV也有HLA-DR表达 43 因此,RA患者EV-HLA-DR+的增加可能与EV-CD41a+中HLA-DR+的表达增加有关,也可能与白细胞来源有关。 需要进一步的实验来解决RA患者的这些假设。
与我们的结果类似,Nathalie Cloutier 等 . 10 据报道,RA患者的循环和SF EV在大小上高度异质,并且比HC的EV大。 然而,根据t-SNE图,在RA血清阳性患者中,EV大小的增加与IC的形成之间没有观察到明显的关联。 在这方面,值得一提的是,我们没有像之前报告的那样排除EV加总 44 事实上,值得注意的是,RA血清阳性患者的EV计数低于血清阴性患者。 虽然我们对这一发现没有明确的解释,但我们认为这些囊泡形成的IC可能会导致这些结构聚集 44 —— 46 ; IC激活和诱导血小板聚集 47 RA患者血液中血小板衍生EV的相当多频率为CD62P+和CD40L+(血小板活化标记物)( 维拉尔·维斯加J , 等 . 提交的手稿 ). 因此,IC是否能以类似血小板的方式促进EV的聚集尚不清楚。 需要更多的研究来证实这一假设。 此前,已证实RA患者SF中的EV通过抗CCP与瓜氨酸化自身抗原的相互作用形成IC 10 。虽然我们没有在这里详细探讨这一点,但我们的结果与此一致,因为t-SNE分析表明,一些EV-CP+也是IgG+和IgM+,主要发生在血清阳性患者中。
与我们的研究相一致,其他研究组已证明RA患者循环中中间单核细胞的增加 35 有趣的是,我们还发现这种增加主要存在于血清阳性患者的循环和SF中,与HC细胞相比,RA患者的中间单核细胞主要捕获EV-IC。 对RA血清阳性患者的其他单核细胞亚群进行了研究。 在最近的一项研究中,对两组循环单核细胞进行了评估 48 M1单核细胞被定义为CD14、CD68和CCR2阳性,而M2单核细胞核被定义为CD14、CX3CR1和CD163阳性。 作者证明,ACPA阳性RA患者的M1/M2比率较高。 此外,M1/M2比率与检测到的分化破骨细胞数量呈正相关 在体外 RA患者样本中。 此外,经脂多糖刺激后,M1单核细胞产生的IL-6浓度高于M2单核细胞核。 然而,由于没有研究M1和M2单核细胞中CD16的表达,因此目前无法将这些数据与我们的结果进行比较。
此前,在RA患者SF中发现的CD16+单核细胞与促炎细胞因子水平升高和关节破坏有关 17 , 49 RA患者的中间单核细胞频率与疾病活动评分呈负相关; 然而,在我们的研究中,我们没有发现这种关联(图 S2系列 相反,我们发现,在血清阳性患者中,中间单核细胞和EV的改变以及血清IL-6、TNF-α和IL-1β浓度的升高密切相关。 事实上,RA血清阳性患者的SF中中间单核细胞表现出比相同患者外周血中观察到的更显著的表型变化。 这表明关节中的中间单核细胞比其血液中的对应细胞参与程度更高,这可能与这些细胞到达该位置后的促炎激活或分化有关 50 此外,EVs还诱导单核吞噬细胞分泌IL1β、IL6和TNF-α。 此前,有人提出,单核细胞/巨噬细胞的靶向作用应该是抑制RA炎症和骨侵蚀的一种有效方法 35 考虑到所有这些方面,我们很容易推测,抑制单核细胞亚群,主要是中间亚群(例如,通过避免它们与EV的相互作用),可能会改善血清阳性RA患者的全身炎症过程。 实际上,抗TNF-α(inflixamab、adalimumab、etanercept等)和抗IL-6(tocilizumab、sarilumab、sirukumab等)生物治疗是有效的RA治疗方法 51 , 52 ,可能通过靶向循环EV的单核细胞促炎反应而部分有用。 鉴于在本研究中,生物治疗是一个排除变量,需要进一步调查以确定抗肿瘤坏死因子-α和抗白介素-6治疗的RA血清阳性患者是否EV和单核细胞改变较少,可能与较少的全身炎症有关。 然而,值得一提的是,本研究患者接受的治疗与观察到的EV和单核细胞亚群的变化无关(数据未显示)。
最后,我们的结果部分解释了血清阳性RA患者出现的全身炎症现象,EV和单核细胞亚群似乎在其中起作用。 血清阳性患者的特征是中间单核细胞数量增加,EV-ICs+和EV-CPs+以及促炎细胞因子IL-1β、IL-6和TNF-α的存在。 因此,这些循环成分的测量可能是一种有用的方法,可用于确定RA患者的全身炎症参数,而传统工具(如DAS28)无法对这些参数进行任何评估。
方法 试剂、材料和抗体 RPMI-1640培养基补充谷氨酸MAX、Dulbecco磷酸盐缓冲盐水(DPBS)和胎牛血清(FBS)购自Gibco-BRL(纽约州大岛)。 多聚甲醛购自Thermo Fisher Scientific,Inc.(宾夕法尼亚州匹兹堡)。 Histopaque®−1077、台盼蓝、青霉素和链霉素购自Cambrex-BioWhittaker(马里兰州沃克斯维尔)。 Annexin-V、Annexin-V结合缓冲液、裂解液、BD TM(TM) 人类炎症细胞计量珠阵列(CBA)和BD FACSFlow TM(TM) 从BD Pharmingen(加利福尼亚州圣地亚哥)购买。 无菌聚苯乙烯12×75-mm管购自BD Falcon(加利福尼亚州圣地亚哥)。 绝对计数珠取自Beckman Coulter(佛罗里达州Hialeah)。 从Polysciences,Inc.(宾夕法尼亚州沃林顿)获得了氟硅石校准等级尺寸范围工具包(直径为0.5μm、1.0μm、2.0μm、3.0μm和6.0μm的YG校准等级球体)、氟硅石YG微球(0.1μm)和氟硅石YG微球(0.2μm)。 玫瑰花九月人单核细胞浓缩鸡尾酒由STEMCELL Technologies(加拿大温哥华不列颠哥伦比亚省)提供。
从Beckman Coulter获得单克隆抗人MY4(CD14)-FITC(克隆322A-1)和MY4-RD1(克隆322A-1); 抗人CD16-V450(克隆3G8)、CD32-PE(克隆3D3)、CD36-APC(克隆CD38,也称NL07)、CD11b-PE(克隆D12)、CD18-APC(复制6.7)、FcμR-Alexa Fluor 647(克隆HM14-1)、CD41a-PE(克隆HIP8)、CD3-PE(克隆17A1)、CD33-PB(克隆WM53)、CD105-BV421(克隆266)、CD19-V450(复制HIB19)、CCR2-Alexa Furo 647(复制48607)的抗体 和CD45-PE-Cy7(克隆HI30)从BD Biosciences(加利福尼亚州圣地亚哥)获得。 单克隆抗人CX3CR1-PE(克隆号2A9-1)、CCR5-PE-Cy7(克隆号J418F1)、HLA-DR-APC-Cy7,克隆号L243,均来自BioLegend(加利福尼亚州圣地亚哥)。 从Abcam(加利福尼亚州旧金山)获得单克隆抗人C1q-FITC(克隆ab4223)、瓜氨酸一抗(克隆ab100932)和抗兔IgG H&L-Alexa Fluor 647-二级抗体(克隆ab150079)。 来自R&D Systems(明尼苏达州明尼阿波利斯)的人类HMGB1-APC抗体(克隆115603)。 F(ab') 2 与Alexa Fluor 488和F(ab')偶联的抗IgG片段 2 与Alexa Fluor 647偶联的抗IgM片段购自Jackson ImmunoResearch(宾夕法尼亚州西格罗夫巴尔的摩派克)。 抗人CD235a-APC(克隆HIR2)购自eBioscience(加利福尼亚州圣地亚哥)。
患者和对照组 60名RA患者,根据美国风湿病学会标准和欧洲风湿病联盟标准诊断 2 ,在圣维森特基金会医院大学风湿病学服务部(哥伦比亚麦德林HUSVF)招募; 她们的中位年龄为55岁,年龄在30至77岁之间,84%为女性。 患者分为三组:一组血清阴性[抗CCP − 射频 − ,(n=6)]和两个血清阳性[抗CCP + 射频 +/− (n=26)和反CCP 你好 射频 你好 (n=28)]; 没有一名患者接受过生物治疗。 作为对照,我们纳入了40名HC,中位年龄为46岁,年龄范围为25至77岁,其中85%为女性; 和60名SLE患者,中位年龄46岁,年龄范围25-77岁,85%为女性,仅用于血清细胞因子的测定 19 我们的研究是根据《赫尔辛基宣言》进行的。 安提奥基亚大学医学研究所和HUSVF伦理委员会批准了研究方案和知情同意书。 所有实验均按照良好临床实践和良好实验室实践进行,并符合安提奥基亚大学医学研究所的相关指南和规定。 所有患者和HC均提供了签署的知情同意书。
细胞因子、自身抗体和CRP测定 为了测定血清细胞因子IL-8、IL-6、IL-10、TNF-α、IL-1β和IL12p70,BD TM(TM) 根据制造商的说明使用人炎症性CBA。
根据制造商的说明,通过商业ELISA(Quanta-Lite RF-IgM、Quanta-Lite RF-IgG和Quanta-Liste CCP3-IgG;Innova Diagnostics,San Diego,CA)测定患者血清中的IgM和IgG RF以及IgG抗CCP。 据商业机构称,RF阳性结果>20 IU/mL,抗CCP阳性结果>10 IU/mL。 这些抗体在10至<250 IU/mL和≥250 IU/mL之间的结果被任意考虑为抗CCP的定义 + 射频 +/− 和反CCP 你好 射频 你好 组。
使用商用试剂盒试剂Dimension Flex定量测定CRP扩展范围和Dimension临床化学系统(均来自加利福尼亚州旧金山的McKesson)通过免疫比色法进行CRP定量。
单核细胞亚群分类 如前所述,单核细胞亚群是通过流式细胞术从全血和SF中确定的 19 , 53 :CD14++CD16−(经典)、CD14++CD16+(中间)和CD14+CD16++(非经典)单核细胞。 简言之,在室温黑暗中用抗人CD45、CD14、CD16和HLA-DR抗体对全血进行20分钟染色; 对每种抗体进行荧光减一(FMO)对照,并在FACS Canto上立即获得100000个细胞 TM(TM) II流式细胞仪,使用FACS DIVA软件(BD)。
单核细胞亚群免疫表型 如前所述,使用Ficoll密度梯度从血液和SF中获得单核细胞 19 使用针对CCR2、CX3CR1、CD64、CD36、CD86、CD11b、CD32、FcμR、CD18和HLA-DR的特异性抗体,在单核细胞亚群(基本组CD14、CD16和HLA-DR)上评估每个分子的表达。 使用基本面板对每个抗体进行FMO对照。 细胞被阻断(DPBS加1%牛血清白蛋白(BSA),0.01%NaN 三 和10%灭活FBS),并在4°C下染色30分钟,然后用洗涤缓冲液进行两次洗涤(DPBS加1%BSA和0.01%NaN 三 ). 立即通过流式细胞术获得50000个单核细胞。
电动汽车特性 循环EV和SF EV的分离和特征如我们之前所述 19 使用抗人CD41a-PE、CD45-PE-Cy7、CD105-BV421、CD33-PE、CD235a-APC、CD3-PE、CD19-V450、CD14FITC、CD16-BV450、HMGB1-APC、C1q-FITC和HLA-DR-APC-Cy7的单克隆抗体。 测量EV-IC,F(ab') 2 使用抗IgG Alexa Fluor-488和抗IgM Alexa Fluor-647片段。 为了通过流式细胞术评估EV上瓜氨酸肽的存在,使用了一种特定的一级抗体(兔多克隆抗人瓜氨酸肽抗体)和Alexa Fluor 647标记的二级抗体(抗兔IgG H和L-Alexa Fluor 647-二级抗体)。 如前所述,用参考珠评估EV大小和计数 19 通过扫描透射电镜(STEM)对RA和HCs患者的一些EV样本进行评估。 为此,用2.5%戊二醛将囊泡固定在镀铜碳STEM格栅上; 在40°C的栅格中干燥,并与乙酸铀酰和柠檬酸铅进行对比。 最后,在室温下干燥样品,并在Tecnai G2 F20显微镜(FEI公司,Hillsboro,OR)中进行评估。 使用Ultra Scan 1000XP-P相机记录图像(加利福尼亚州普莱森顿Gatan公司)。
EV-IC形成 从8名血清阳性RA患者的血浆低血小板中提取EV,并冷冻直至使用。 调理约1×10 6 将EV与15µg/mL纯化IgG(通过亲和层析从16名RA血清阳性患者的血浆中分离)混合并在37°C下孵育60分钟。 17000用1mL DPBS冲洗掉未结合抗体 克 持续60分钟。通过流式细胞术评估EV-形成(图 第3页 ).
单核细胞分离用于EV和EV-IC培养 根据制造商的说明,9月玫瑰红浓缩了循环单核细胞。 所有病例中CD14+单核细胞的纯度均大于90%。 据报道,培养24小时后,单核细胞亚群和吞噬细胞以1:3(细胞:EVs)的比例结合并摄取用2μM CFSE染色的EVs和EV-ICs 19 为了估计内化EV的细胞的平均荧光强度(MFI),在流式细胞仪上采集含有或不含有0.01%v/v台盼蓝的样品,以熄灭表面结合EV的绿色荧光。
约1.2×10 5 如前所述培养单核细胞 54 简单地说,细胞粘附在RPMI-1640-GlutaMAX中,其中含有0.5%灭活的自体血清耗尽的EV(iSA-f) 19 然后,在有或无EV和EV-IC的情况下,将细胞在含有10%iSA-f的RPMI-1640中培养120小时。 收集上清液并在−20°C下冷冻,直到CBA评估细胞因子。
数据分析 通过Kruskal–Wallis试验和Dunn’s试验对RA组患者和HC进行比较 事后的,事后的 测试(数据为中位数±四分位范围)。 使用ANOVA-II和Bonferroni对多个变量进行比较 事后的,事后的 测试(数据为平均值±标准偏差)。 统计显著性设为p≤0.05* p≤0.05,**p≤0.01,****p≤0.001,***p≤0.0001。 通过确定Spearman秩系数与95%置信区间进行关联。 为了说明EV的大小和含量的变化,应用t-SNE分析,将困惑度设置为100,并向下抽样至50000; 使用ACCENSE 0.0.5-beta软件,根据所选通道的表达对t-SNE图进行着色 55 使用FlowJo 10.2软件估计门控分析、细胞/EV频率和MFI。 使用GraphPad Prism 7.2版(GraphPad-Soft-ware Inc.,加利福尼亚州圣地亚哥)进行统计分析。 使用Statgraphics X64 Centurion XVI(Statpoint Technologies,Warrenton,VA,USA)进行多元判别分析和主成分分析。
致谢 C.Burbano是COLCIENCIAS博士奖学金的获得者(电话617-2013)。 作者感谢安提奥基亚大学(Universidad de Antioquia)“Sostenibilidad and Sistema Universityario de Investigaciones,CODI”(2013-05-42869836)和COLCIENCIAS项目(111565740575)的资助。 作者感谢Blanca Ortiz对ELISA过程的帮助,Janine Orejuela对收集临床数据的支持,以及Natalia Ortis和Johana Arboleda(Antioquia大学透射电子显微镜设备)对STEM程序的帮助。
作者贡献 C.B.和D.C.为数据的采集、分析和解释做出了贡献; 写了主要的手稿。 M.R.和G.V.对数据的分析和解释以及论文的起草做出了贡献。 C.M.-V.、A.V.-G.和L.C.对临床数据进行了采集和解释。 所有作者审查并批准了手稿的最终版本。
数据可用性 在本研究期间生成和/或分析的数据集可根据合理要求从相应作者处获得。
脚注 出版商备注: Springer Nature在公布的地图和机构关联中的管辖权主张方面保持中立。
电子辅助材料 补充信息 本文随附于10.1038/s41598-018-36335-x。
工具书类
1 McInnes IBSG。类风湿关节炎的发病机制。 北英格兰。 《医学杂志》2011; 365:2205–2219。 doi:10.1056/NEJMra1004965。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
2 阿莱塔哈,D。 等 类风湿关节炎分类标准:美国风湿病学院/欧洲风湿病防治联盟合作倡议。 安 . 大黄 . 数字化信息系统 .1580–1588,10.1136/年.2010.138461(2010年)。 [ 内政部 ] [ 公共医学 ]
3 Gómez-Puerta,J.A。 等 抗瓜氨酸肽/蛋白抗体阳性和阴性类风湿关节炎患者滑液细胞因子水平的差异,但滑液组织细胞浸润的差异不存在。 关节炎研究 . 疗法 . 15 (2013). [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ]
4 Conigliaro P等人。炎症性关节炎中的自身抗体。 自动immun。 2016年修订版; 15:673–683. doi:10.1016/j.autrev.2016.03.003。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
5 Szekanecz,Z.和Koch,A.巨噬细胞及其产物在类风湿性关节炎中的作用。 风湿病学的当前观点 19 (2007). [ 内政部 ] [ 公共医学 ]
6 Hennigan S,Kavanaugh A.白细胞介素-6抑制剂治疗类风湿关节炎。 疗法。 临床。 风险管理。 2008; 4:767–775. doi:10.2147/TCRM.S3470。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
7 Toussirot E,Wendling D.《TNF-α阻滞剂在类风湿关节炎中的应用:最新进展》。 专家操作。 药物治疗。 2007; 8:2089–2107. doi:10.1517/14656566.8.13.2089。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
8 Edalat,F.NIH公共访问。 40 ,1301–1315(2012年)。
9 Boyard E等。血小板通过胶原蛋白依赖性微粒的产生放大关节炎炎症。 科学。 2010; 327:580–3. doi:10.1126/science.1181928。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
10 Cloutier N等。微粒暴露自身抗原是形成有效炎症成分的基础:微粒相关免疫复合物。 EMBO分子医学2013; 5:235–249. doi:10.1002/emmm.201201846。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
11 Malda J、Boere J、van de Lest CHA、van Weeren PR、Wauben MHM。 细胞外囊泡-关节修复和再生的新工具。 自然评论。 风湿病学。 2016; 12:243–249. doi:10.1038/nrrheum.2015.170。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
12 Burbano,C.、Rojas,M.、Vásquez,G.和Castaño,D.在自身免疫反应中形成免疫复合物作为调节结构的微粒。 调解员影响力 . 2015 (2015年)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ]
13 Stuhlmüller B等。类风湿关节炎患者活化单核细胞中已知和新基因的鉴定。 大黄性关节炎。 2000; 43:775–790。 doi:10.1002/1529-0131(200004)43:4<; 775::AID-ANR8>; 3.0.CO; 2-7. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
14 Liote F、Boval-Boizard B、Weill D、Kuntz D、Wautier JL。 类风湿关节炎患者的血单核细胞活化:单核细胞粘附性增加、整合素表达和细胞因子释放。 临床。 实验免疫学。 1996; 106:13–19. doi:10.1046/j.1365-2249.1996.d01-820.x。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
15 Torsteinsdottir I,Arvidson NG,Hallgren R,Hakansson L.类风湿关节炎(RA)中单核细胞激活:整合素、Fcγ和补体受体表达增加以及糖皮质激素的作用。 临床。 实验免疫学。 1999; 115:554–560. doi:10.1046/j.1365-2249.1999.00817.x。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
16 Burmester GR等。炎症和非炎症关节疾病中滑膜的组织结构。 I.通过针对Ia和单核巨噬细胞抗原的单克隆试剂检测到的主要滑膜细胞群的定位。 风湿病。 国际1983年; 3:173–181. doi:10.1007/BF00541597。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
17 Kinne RW,Stuhlmuller B,Burmester G-R.类风湿关节炎滑膜细胞。 巨噬细胞。 关节炎研究与治疗。 2007; 9:224. doi:10.1186/ar2333。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
18 Nielsen CT等。系统性红斑狼疮患者细胞衍生血浆微粒IgG升高与自身抗体和补体激活有关。 大黄性关节炎。 2012; 64:1227–1236. doi:10.1002/art.34381。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
19 布尔巴诺,C。 等 系统性红斑狼疮患者单核细胞活化过程中血小板衍生微粒和微粒形成免疫复合物的潜在参与。 前部 . 免疫学 . 9 , (2018). [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ]
20 Rossol M、Kraus S、Pierer M、Baerwald C、Wagner U。CD14亮CD16+单核细胞亚群在类风湿性关节炎中扩张,并促进Th17细胞群的扩张。 大黄性关节炎。 2012; 第64:671–677页。 doi:10.1002/art.33418。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
21 Withrow J等。类风湿关节炎和骨关节炎发病机制中的细胞外囊泡。 关节炎研究与治疗。 2016; 18:286. doi:10.1186/s13075-016-1178-8。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
22 Pisetsky DS、Ullal AJ、Gauley J、Ning TC。作为风湿疾病介质和生物标记物的微粒。 风湿病。 (英国)2012年; 第51:1737–1746页。 doi:10.1093/rheumatology/kes028。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
23 Shi C,Pamer EG。感染和炎症期间单核细胞募集。 《自然免疫学评论》。 2011年; 11:762–774. doi:10.1038/nri3070。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
24 Scrivo R等。炎症性关节炎患者血清和滑液中白细胞介素-10家族细胞因子的分布揭示了其对全身和关节炎症的不同贡献。 临床。 实验免疫学。 2015; 179:300–308. doi:10.1111/cei.12449。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
25 Sattar N、McCarey DW、Capell H、McInnes IB。解释“高级”全身炎症如何加速类风湿关节炎的血管风险。 循环。 2003; 108:2957–2963. doi:10.1161/01.CIR.0000099844.31524.05。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
26 Ohmura K等人。抗瓜氨酸肽抗体阴性RA是一个基因独特的亚群:一项仅使用骨侵蚀性ACPA阴性类风湿性关节炎的权威性研究。 风湿病学(牛津)。 2010; 49:2298–2304. doi:10.1093/rheumatology/keq273。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
27 van der Woude D等人。ACPA同型曲线反映了类风湿关节炎的长期放射学进展。 大黄年鉴。 数字化信息系统。 2010; 69:1110–1116. doi:10.1136/ard.2009.116384。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
28 González-álvaro I等人。血清中白细胞介素15水平可能预测早期关节炎患者的严重病程。 公共科学图书馆一号。 2011年; 6:1–9. doi:10.1371/journal.pone.0029492。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
29 MU R等。类风湿关节炎患者血清白细胞介素33升高与自身抗体产生相关。 《风湿病学杂志》。 2010; 37:2006–2013. doi:10.3899/jrheum.100184。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
30 戈尔利诺,C.V。 等 类风湿关节炎患者滑膜抗瓜氨酸肽抗体水平与中性粒细胞反应之间的关系。 欧元 . J型 . 免疫学 .1563–1572,10.1002/eji.201847477(2018)。 [ 内政部 ] [ 公共医学 ]
31 Krishnamurthy A等。类风湿关节炎相关自身抗体介导的骨丢失背后新型趋化因子依赖性分子机制的鉴定。 大黄年鉴。 数字化信息系统。 2016; 75:721–729。 doi:10.1136/annrheumdis-2015-208093。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
32 Wigerblad G等。瓜氨酸化蛋白的自身抗体通过趋化因子依赖机制诱导关节疼痛,与炎症无关。 大黄年鉴。 数字化信息系统。 2016; 75:730–738. doi:10.1136/annrheumdis-2015-208094。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
33 Catrina AI、Svensson CI、Malmstrom V、Schett G、Klareskog L。类风湿关节炎中系统性自身免疫导致关节特异性疾病的机制。 自然修订版风湿病。 2017; 13:79–86. doi:10.1038/nrreum.2016.200。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
34 White FA,Jung H,Miller RJ。趋化因子与神经病理性疼痛的病理生理学。 程序。 国家。 阿卡德。 科学。 2007; 104:20151–20158. doi:10.1073/pnas.0709250104。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
35 Davignon J-L等。以单核细胞/巨噬细胞为靶点治疗类风湿关节炎。 风湿病学(牛津)。 2013; 52:590–598. doi:10.1093/风湿病学/kes304。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
36 McInnes IB.类风湿关节炎。 从长凳到床边。 大黄。 数字化信息系统。 临床。 北美,2001年; 27:373–387. doi:10.1016/S0889-857X(05)70207-6。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
37 Baron M,Boulanger CM,Staels B,Tailleux A.动脉粥样硬化中的细胞衍生微粒:生物标记物和药物调节靶点? J.细胞。 《分子医学》2012; 16:1365–1376. doi:10.1111/j.1582-4934.2011.01486.x。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
38 del Rincon ID、Williams K、Stern MP、Freeman GL、Escalante A.类风湿性关节炎队列中心血管事件的高发病率未被传统心脏风险因素解释。 大黄性关节炎。 2001; 44:2737–2745. doi:10.1002/1529-0131(200112)44:12<; 2737::AID-ART460>; 3.0.CO; 2-编号。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
39 Kirkland TN,Viriyakosol S.可溶性和膜结合CD14的结构-功能分析。 掠夺。 临床。 1998年生物研究; 397:79–87. [ 公共医学 ] [ 谷歌学者 ]
40 Bazil V,Strominger JL。 脱落是CD14对受刺激人单核细胞下调的机制。 免疫学杂志。 1991; 147:1567–1574。 [ 公共医学 ] [ 谷歌学者 ]
41 Mikuls TR等。类风湿关节炎中的可溶性CD14和CD14多态性。 《风湿病学杂志》。 2011年; 38:2509–2516. doi:10.3899/jrheum.110378。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
42 Boshkov LK,Kelton JG,Halloran PF。急性特发性血小板减少性紫癜血小板HLA-DR的表达。 英国血液学杂志。 1992; 81:552–557. doi:10.1111/j.1365-2141.1992.tb02991.x。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
43 Semple JW等。急性和慢性自身免疫性血小板减少性紫癜患者血清细胞因子水平的差异:与血小板表型和抗血小板T细胞反应性的关系。 鲜血。 1996; 87:4245–4254. [ 公共医学 ] [ 谷歌学者 ]
44 Gyorgy B等人。改进的流式细胞术评估揭示了关节疾病中不同的微泡(细胞衍生微粒)特征。 公共科学图书馆一号。 2012; 7:e49726。 doi:10.1371/journal.pone.0049726。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
45 Mustonen A-M等人首次在人体滑液中透明质酸包裹的细胞外小泡的体内检测和表征。 《矫形外科杂志》。 2016年决议; 34:1960–1968. doi:10.1002/jor.23212。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
46 Khlebtsov BN,Burygin GL,Matora LY,Shchyogolev SY,Khlebtshov NG。研究不溶性免疫复合物的方法。 生物化学。 生物物理学。 《学报》。 2004年; 1670:199–207. doi:10.1016/j.bbagen.2003.12005。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
47 Schattner M等人。用阳离子化人IgG制备的免疫复合物激活人血小板。 鲜血。 1993; 82:3045–3051. [ 公共医学 ] [ 谷歌学者 ]
48 岩本,N.M1和M2单核细胞在类风湿关节炎中的作用:M1/M2单核细胞失衡对破骨细胞生成的贡献。 8 , 1–10 (2018). [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ]
49 Iguchi T,Kurosaka M,Ziff M.类风湿滑膜中HLA-DR和单核/巨噬细胞染色细胞的电镜研究。 大黄性关节炎。 1986; 29:600–613. doi:10.1002/art.1780290504。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
50 Wynn TA、Chawla A、Pollard JW。 发展、体内平衡和疾病中的巨噬细胞生物学。 自然。 2013; 496:445–455. doi:10.1038/nature12034。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
51 Md Yusof MY,Emery P.在类风湿关节炎中靶向白细胞介素-6。 药物。 2013; 73:341–356. doi:10.1007/s40265-013-0018-2。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
52 Neovius M等人。类风湿关节炎患者使用TNF抑制剂的药物存活率阿达木单抗、依那西普和英夫利昔单抗的比较。 大黄年鉴。 数字化信息系统。 2015; 74:354–360. doi:10.1136/annrheumdis-2013-204128。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
53 Burbano C,Vasquez G,Rojas M。CD14+CD16++单核细胞对CD14++CD16−单核细胞的调节作用:系统性红斑狼疮单核细胞改变的可能解释。 风湿性关节炎。 (新泽西州霍博肯)2014年; 66:3371–3381. doi:10.1002/art.38860。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
54 Castaño D,García LF,Rojas M.结核分枝杆菌感染CD16+单核细胞的频率和细胞死亡增加。 肺结核。 2011年; 91:348–360. doi:10.1016/j.tube.2011.04.002。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
55 Shekhar K、Brodin P、Davis MM、Chakraborty AK。 基于非线性随机嵌入(ACCENSE)程序的细胞表达自动分类。 国家。 阿卡德。 科学。 2014; 111:202–207. doi:10.1073/pnas.1321405111。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
关联数据 本节收集本文中包含的任何数据引用、数据可用性声明或补充材料。
数据可用性声明 在本研究期间生成和/或分析的数据集可根据合理要求从相应作者处获得。