人巨细胞病毒(HCMV)在免疫反应受损或不成熟的多个患者群体中导致大量发病( 1 , 2 ). 器官移植或先天性感染期间的威胁导致HCMV疫苗的开发被列为最高优先事项( 三 ). 在不同的患者队列中研究了几种针对HCMV的疫苗(来自全病毒、DNA和病毒亚单位),总的来说,确定了以HCMV为目标的疫苗接种策略是一种可行的选择,具有重大的临床意义( 4 —— 10 ).
一个疫苗靶点是病毒糖蛋白B(gB),在三个第2阶段临床试验中,当使用MF59佐剂时,该蛋白已被证明具有部分保护作用( 6 , 9 , 11 ). gB蛋白是病毒进入所需的一种基本病毒成分( 12 , 13 )是体液免疫反应的主要靶点,包括中和作用( 14 —— 16 ). 传统上,中和抗体滴度被认为是评估疫苗的基准,因为这代表了一种有效的抗病毒机制。 然而,体液反应要复杂得多,产生的抗体在被感染细胞表面表达时可以结合病原体或目标抗原,从而引发多种下游效应。 这些抗体可以补充补体以促进病原体或受感染细胞的溶解,驱动抗体依赖性细胞毒性,促进病原体的吞噬作用,并调节适应性和先天性免疫反应的下游反应( 17 ). 在第二阶段的研究中,移植患者受到野生型HCMV的攻击,我们报告的数据显示,中和抗体反应与gB疫苗保护相关的证据有限( 9 ). 无法检测临床梅林中和的证据与之前的数据一致,该数据表明在经典的菌斑试验中抗体加补体对实验室菌株Towne没有影响( 9 ). 此外,我们提供证据表明,与自然感染的血清阳性者相比,疫苗接种在血清阴性者中诱导的针对gB的体液反应显示出明显的生物光谱。
结果 血清阴性疫苗接种患者的血清在单轮感染检测中不能中和HCMV感染。 注意,在本文中,术语“血清阴性”是指在接种gB/MF59疫苗或安慰剂之前血清阴性的患者。 我们使用高通量试验检测HCMV感染的中和证据,该试验通过计数立即早期(IE)阳性细胞来测量溶血感染的建立( 图1 ). 两种抗gB单克隆抗体(ITC88,一种抗AD-2抗体,被证明可以防止gB融合后结合[ 18 ]; 和2F12,一种针对gB未指定区域的商业单克隆抗体,以浓度依赖的方式抑制HCMV感染( 图1 一个 ). 接下来,我们在相同条件下测试了疫苗研究中的一组血清。 接种前,血清阴性个体的血清对HCMV感染没有影响。 重要的是,在评估接种后血清阴性血清时,在本试验中没有观察到抗HCMV活性的证据( 图1 B类 和 图S1 一个 —— 天 )即使在感染前将外源性补体添加到血清中( 图S2 ). 相反,血清阳性患者的血清在移植前对HCMV具有固有的中和活性( 图1 B类 和 图S1 E类 —— H(H) ),但接种疫苗后没有观察到中和能力增加的证据( 图1 B类 和 图S1 E类 —— H(H) ).
图1。
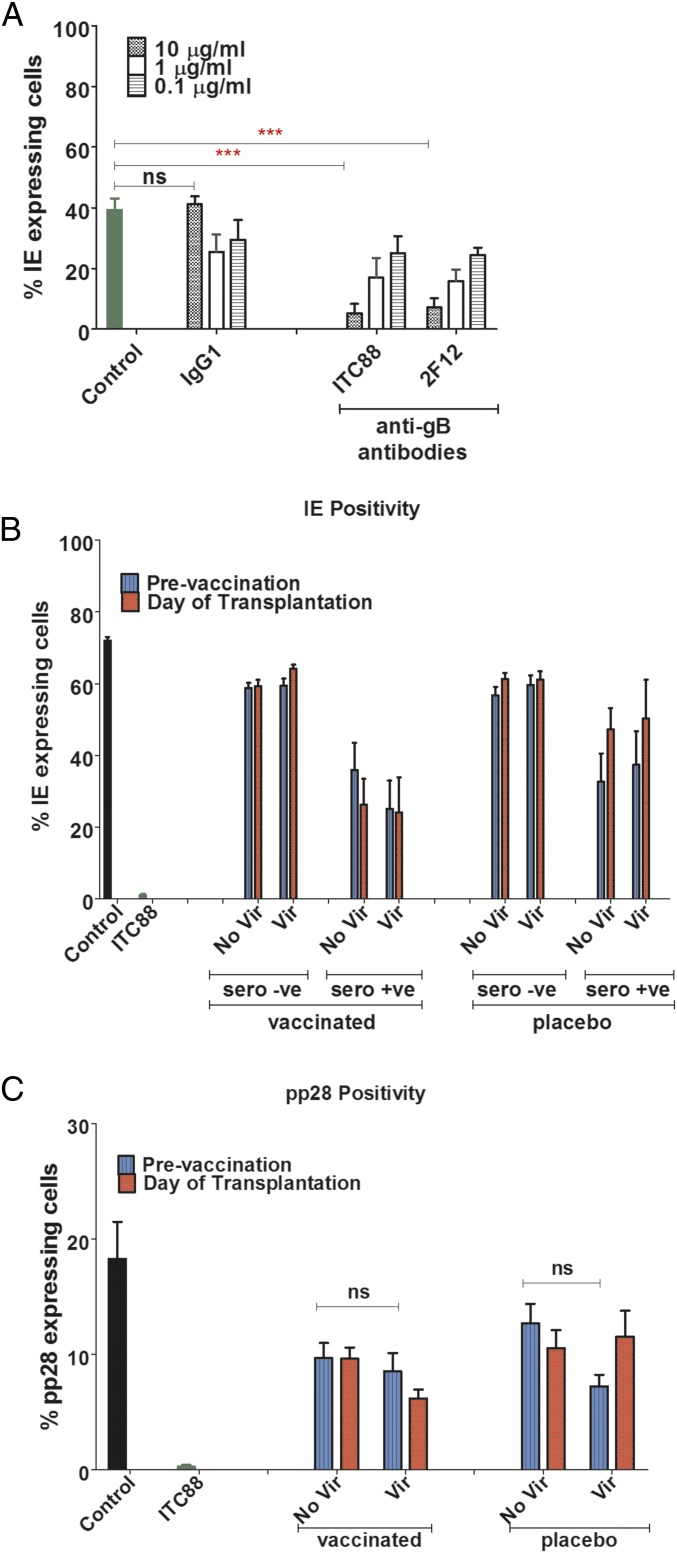
接种疫苗不会促进血清阴性的中和抗体反应。 ( 一个 )HCMV与不同浓度的抗gB单克隆抗体(ITC88和2F12)、IgG1同型对照或培养基孵育1h,然后用于感染HFF(MOI=0.5)。 IE阳性率为24hpi。 n个 = 3. ( B类 )HCMV与血清阳性或血清阴性患者的血清孵育1小时,这些患者的血清接种了gB或给予安慰剂,然后用于感染HFF(MOI=1)。 对接种疫苗前和移植当天(接种疫苗后)分离的血清进行分析。 IE阳性率为24 hpi,并进一步分层至病毒血症患者。 n个 = 3. ( C类 )HCMV与血清阴性患者的血清孵育1小时,这些患者的血清接种了gB或给予安慰剂,然后用于感染HFF(MOI=1)。 对移植当天(接种疫苗后)分离的血清流行情况进行分析。 对pp28阳性率进行120 hpi评分,并将其进一步分为出现病毒血症的患者。 n个 = 3.
为了解决血清阴性疫苗的血清中含有能够诱发流产/静止感染的抗体的可能性,如水痘感染的建议( 19 ),进行平行分析,测定pp28(病毒晚期基因)阳性( 图1 C类 ). 不出所料,在ITC88对照组中pp28阳性细胞很少( 图1 C类 )鉴于很少见到IE阳性细胞( 图1 B类 ). 相反,与IE数据一致,使用接种血清阴性的移植受者的血清,未观察到对pp28阳性的影响( 图1 C类 和 图S3 ).
接种血清阴性患者的血清不能抑制HCMV细胞相关梅林株在成纤维细胞单层中的传播。 我们的第一次检测通过测量接种后24小时内IE阳性细胞的数量(hpi)来测量血清限制大滴度无细胞病毒细胞感染的能力。 为了研究血清是否对细胞相关HCMV具有抗病毒活性,我们使用低感染多重性(MOI)接种的病毒传播试验评估了血清对HCMV在成纤维细胞培养物中生长的影响。 为了能够提出这个问题,我们利用了一种Merlin-IE2-GFP病毒,该病毒主要以细胞相关方式生长( 20 ). GFP与IE2动力学的表达允许实时成像和计数病毒的传播,因为我们实时观察感染细胞数量随时间的增加,从而监测病毒通过成纤维细胞单层的传播( 图2 一个 ). 首先,我们测量了ITC88限制这种细胞相关病毒传播的能力。 数据表明,ITC88对传播的影响最小,感染细胞的数量随着培养时间的增加而增加,这与细胞相关病毒对中和具有抵抗力相一致( 图2 B类 ). 重要的是,ITC88可以有效地限制以无细胞生长为主的高强度梅林菌株的传播,因此在该病毒传播试验中具有功能( 图2 C类 ). 在健康供者血清中也观察到类似的数据,其中血清阳性血清对IE2-GFP病毒传播的抵抗力要低得多,而健康供者的血清阴性血清则没有影响( 图2 天 ). 建立了检测的基线后,我们接下来分析了疫苗研究的血清。 数据显示,血清阳性血清的平均水平确实影响了Merlin-IE2-GFP的传播,其水平与天然血清阳性对照血清的水平相似( 图2 E类 和 图S4 一个 —— 天 ). 相反,血清阴性个体的血清在接种疫苗前后对病毒传播没有影响( 图2 E类 和 图S4 E类 —— H(H) ). 此外,数据还表明,接种血清阳性疫苗并没有增强疫苗接种前血清阳性血清对病毒传播的中度抑制作用( 图2 E类 和 图S4 一个 —— 天 ).
图2。
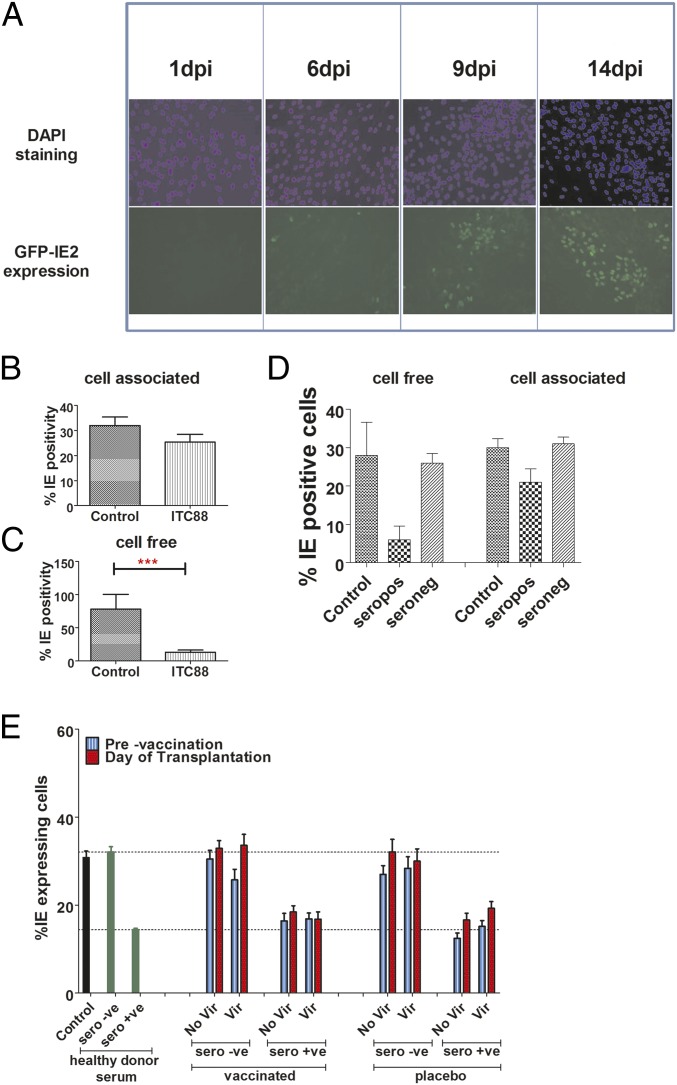
接种血清阴性的血清不能控制细胞相关HCMV在体外的传播。 ( 一个 )用Merlin-IE2-GFP感染HFF(MOI=0.01),监测感染进展2周。 显示感染后1、6、9和14天GFP表达的典型图像。 用DAPI对细胞进行复染,以显示细胞层。 ( B类 和 C类 )感染Merlin-IE2-GFP的HFF( B类 )或梅林( C类 )感染后2周,用ITC88(100μg/mL)和病毒扩散试验培养24 hpi。 用GFP(细胞相关)或IE免疫染色(无细胞)计算感染率。 n个 = 3. ( 天 )感染Merlin(无细胞)或Merlin-IE2-GFP(细胞相关)的HFF在无血清(对照)、血清阳性血清或血清阴性血清的情况下孵育24 hpi。 2周后,用GFP(细胞相关)或IE免疫染色(无细胞)计算感染率。 n个 = 3. ( E类 )将感染Merlin-IE2-GFP(细胞相关)的HFF与无血清(感染细胞)、健康供者血清阳性[HCMV(+)]血清或血清阴性[HCMV]血清孵育24 hpi。 或者,将HFF与给予gB疫苗或安慰剂的血清阳性或血清阴性患者的血清孵育。 分析移植当天(接种后)的血清流行情况。 2周后,用GFP(细胞相关)计算感染率。 n个 = 3. 患者进一步分为经历过病毒血症的患者和没有经历过病毒症的患者。
疫苗接种不会诱导能够促进可测量的ADCC反应的抗体库。 由于缺乏证据支持有效中和,我们研究了其他抗体效应机制。 ADCC涉及抗原表位的抗体识别和随后细胞效应器功能(例如自然杀伤(NK)细胞)的招募,以杀死受感染的细胞。 为了对我们的血清进行高通量筛选,以检测任何潜在的ADCC传播活性,我们在先前针对流感蛋白抗体的研究的基础上开发了一种体外检测方法( 21 ). 将重组疫苗gB固定化,并与健康献血者的外周血单个核细胞(PBMC)在血清中孵育。 然后,我们通过流式细胞术分析NK细胞,寻找CD107a表达的证据,CD107a是NK细胞脱颗粒的经典标志。 利用佛波醇12-肉豆蔻酸13-醋酸盐(PMA)/离子霉素(一种NK细胞脱颗粒的有效激活剂)对该试验进行验证,在这些激活剂存在的情况下,CD56+NK细胞上的CD107a表面表达显著上调( 图3 一个 ). 通过该试验,我们可以观察到健康供者血清阳性和血清阴性血清之间的CD107a表型差异( 图3 B类 和 图S5 一个 和 B类 ). 确定条件后,我们测试了纵向疫苗研究的血清。 在接种疫苗前后的血清阳性患者血清中都有明显的抗ADCC抗体证据( 图S5 C类 —— E类 ). 然而,没有证据表明疫苗接种增强了这些血清阳性个体原有的反应,也没有证据表明ADCC抗体水平与病毒血症保护相关( 图3 C类 和 天 ).
图3。
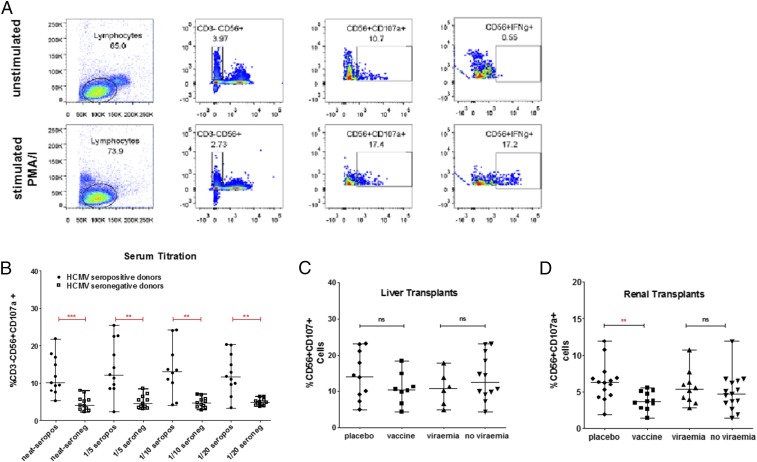
血清阳性者中未检测到针对gB的ADCC抗体反应增加。 ( 一个 )研究ADCC活动证据的门控策略。 然后对定义为CD56+CD3−的NK细胞进行CD107a表达或IFNg检测。 PMA/离子霉素作为阳性对照。 ( B类 )血清阳性和血清阴性供者健康供者血清的滴定,以确定其促进NK细胞CD107a表达的能力。 ( C类 和 天 )肝和肾器官移植时血清阳性受者ADCC反应的数据总结。 安慰剂和疫苗接种之间的比较,或病毒血症或无病毒血症之间的比较。 n个 = 3.
接下来,我们询问疫苗接种对血清阴性的影响是否明显。 正如预期的那样,在基线检查时,血清阴性样本中没有明显的ADCC效应(即流行率; 图4 一个 —— 天 ). 接种疫苗后的纵向样本分析表明,没有证据表明接种疫苗在移植前一直能诱发ADCC的抗gB抗体的可检测水平( 图4 一个 —— 天 ).
图4。
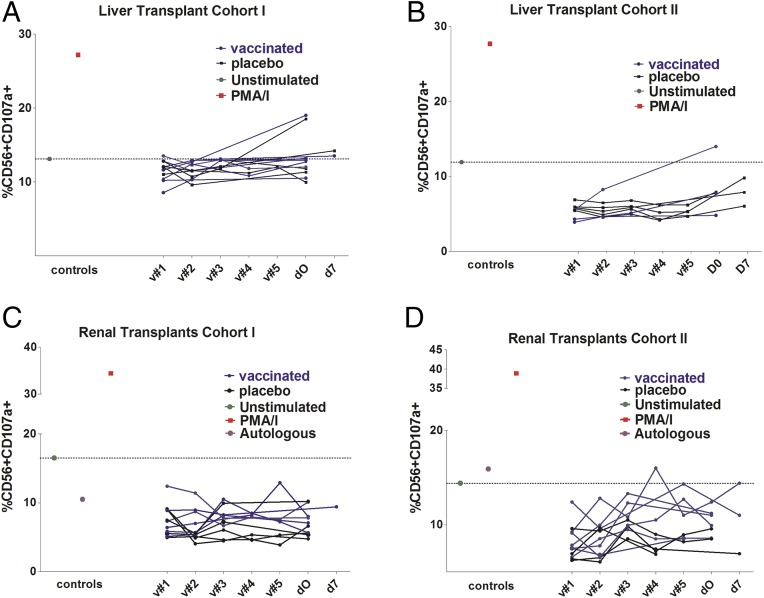
接种疫苗不会在血清阴性的情况下诱发针对gB的可检测ADCC抗体反应。 ( 一个 —— 天 )对多次就诊的纵向血清样本进行ADCC增殖活性分析。 样本为接种后或移植时(d0)或移植后7天(d7)的流行率(v#1)或1(v#2)、2(v#3)、6(v#4)和7(v#5)mo。 使用未刺激细胞或健康供者血清阴性血清显示基线阴性对照,PMA/离子霉素作为阳性对照。
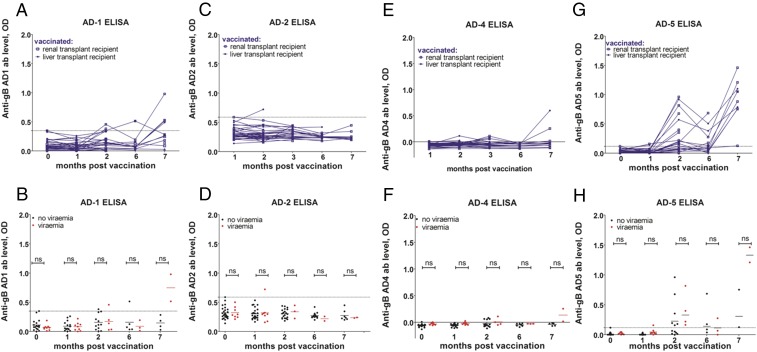
接种疫苗的个体对gB表位的独特抗体反应。 我们无法检测到血清阴性疫苗接受者中和或ADCC效应器功能与保护相关的证据,因此我们研究了HCMV关键抗原域(AD)的体液反应组成。 在一项对血清阳性个体的平行研究中,我们有证据表明,移植后病毒血症减少与抗AD-2抗体水平升高相关( 22 )与该表位被认为是抗体反应的重要靶点一致( 23 ). 因此,我们询问血清阴性疫苗接种是否诱导了针对已知gB抗原域的特异性抗体反应。 在接种前后对血清阴性血清的系列样本进行ELISA( 图5 ). 数据表明,接种疫苗对已知的ADs产生的反应有限,而对AD-2没有任何反应( 图5 C类 和 天 )或AD-4( 图5 E类 和 如果 ). 相反,在某些个体中观察到AD-1和AD-5反应,但这些与保护无关( 图5 一个 , B类 , G公司 、和 H(H) ). 因此,与血清阳性药物不同,gB的明确ADs不能与保护性直接相关。
图5。
疫苗接种诱导了与自然感染不同的表位反应模式。 ( 一个 —— H(H) )对接种后0个月或1、2、6和7个月的血清流行率进行ELISA。 接种疫苗代表背景。 抗AD1的ELISA ODs( 一个 ),AD2( C类 ),AD4( E类 )和AD5( G公司 )将显示响应。 或者,使用移植后结果对数据进行分层( B类 , 天 , 如果 、和 H(H) )评估反应对病毒血症的影响。 使用非参数Mann–Whitney测量统计显著性 U型 测试。 ns,无显著性。
讨论 使用基于HCMV关键病毒糖蛋白B的亚单位疫苗是抗gB抗体的有效诱导剂( 6 , 9 , 11 ). 此外,在实体器官移植受者的随机第2阶段试验中,这些抗体水平与病毒载量参数降低相关( 9 ). 这些数据支持这样一个概念,即诱导针对gB的强有力的体液反应是一种很好的预防HCMV疾病的策略。 然而,尽管对改善临床结果有了这样的认识,但保护的机制基础仍不完全清楚。
经典地,诱导有效的中和抗体反应被认为是评估任何疫苗策略的金标准( 18 , 24 ). 事实上,许多成功的疫苗接种计划都使用了这种疫苗( 24 ). 然而,在这项研究中,我们无法提供有力的中和抗体反应的支持证据来解释gB HCMV疫苗的成功。 数据显示,血清阳性移植受者的血清具有中和抗体,但通过接种gB/MF59疫苗,这些抗体没有被检测到增强。 最有可能的是,这些强有力的抗体是由抗gB和其他主要糖蛋白靶点(包括三聚体gH/gL/gO和五聚体复合物)组成的复合物( 25 ). 与这些作为中和靶点的糖蛋白一致的是,数据表明针对gH或五聚体复合物的单克隆抗体可以有效中和感染( 26 —— 28 ). 最近的研究表明,细胞相关HCMV的生长在很大程度上对Cytoctect(一种抗HCMV抗体的异质混合物)的活性具有抵抗力,可能是因为病毒的物理状态使其无法获得中和抗体( 20 )与之前的报告一致( 29 ). 我们在此提供的数据支持这些观察结果; HCMV Merlin-IE2-GFP株产生的少量无细胞病毒可以解释血清阳性血清对降低体外传播率的轻微影响。
因此,体内的双相生长模式(即无细胞和细胞相关)可能会证明,有效的HCMV疫苗可能依赖于多种体液效应器功能的诱导。 因此,虽然疫苗仍有诱导中和抗体反应的作用,但这些临床试验数据表明,尽管不能检测到与HCMV相关的有效中和反应,但针对HCMV的疫苗仍然有效, 它们增强了使用挑战模型评估疫苗接种策略的价值。 最近在小鼠身上进行的一项研究得出结论,接种AD-2无效,因为它的中和反应较差。 然而,AD-2疫苗是否对CMV挑战具有保护作用却一直没有得到解决( 30 ). 事实上,最近的一项研究表明,在小鼠巨细胞病毒攻击模型中,中和和非中和gB抗体反应均起作用( 31 ). 此外,这一概念可能并不局限于HCMV,因为对候选HIV疫苗的人类研究报告称,抗病毒体液反应的主要成分与ADCC相关( 32 , 33 ).
与急性病毒感染相比,HCMV在面对巨大的免疫反应时会在宿主的一生中持续存在( 33 ). HCMV编码多个免疫逃避基因,以促进宿主的终身生存和重新感染新宿主的能力,即使是那些对HCMV具有预先存在的自然免疫性的宿主。 这说明了HCMV与免疫反应的复杂相互作用,这种病毒在强大的免疫反应面前持续存在的能力可能会影响仅基于中和抗体诱导产生杀菌疫苗的能力。 简言之,血清阳性者的血清在体外具有强大的中和作用,但体内可能再次感染HCMV。 因此,我们调查了接种疫苗的患者血清增强抗体依赖性反应的能力。 NK细胞可以以抗体依赖的方式招募,以促进细胞毒性。 HCMV编码大量NK免疫逃避基因,这表明这是一种重要的功能相互作用( 34 ). 此外,HCMV血清阳性个体的NK细胞库由NK细胞亚群主导,这与NK细胞记忆有关( 35 ). 这些NK细胞亚群是HCMV的精英控制者,还是反映了病毒诱导的重编程仍然是一个重要的未决问题。 显然,根据我们的研究,血清阳性药物会激发抗gB反应,从而指导NK细胞介导的ADCC。然而,我们不能将疫苗的成功归因于此,因此,虽然存在促进ADCC的抗gB抗体,但我们无法提供证据来解释疫苗的保护作用。 促进ADCC反应的抗体的产生可能是在最初接触病原体或通过多次激活集中免疫反应后触发的。 疫苗显然不会将这些额外的暴露传递给免疫系统。 事实上,疫苗在没有其他致病基因编码功能的情况下传递gB,因此可能以独特的方式呈现gB。 这是否能使有效的抗HCMV反应比感染时更有效,这是疫苗研究需要解决的一个重要问题。 最后,重要的是避免暗示ADCC反应没有作用。 我们的数据表明,针对gB的ADCC反应无法检测(血清阴性疫苗)、增强(血清阳性疫苗)或与保护相关(血清阳性患者队列)。 然而,我们的数据并不排除ADCC对其他HCMV抗原的反应对于控制自然感染很重要。
虽然保护的机制相关性尚待确定,但很明显gB HCMV疫苗具有保护作用( 6 , 9 , 11 ). 有趣的是,表位分析指向一个令人兴奋的假设,即一个新的表位可能负责。 疫苗gB也通过furin裂解位点的丢失在跨膜域中被修饰,并被认为以融合后形式存在。所有这些差异可能导致gB的新表位出现,这些表位通常不暴露在病毒粒子中,但在进入过程中或HCMV感染的细胞中短暂暴露。 目前正在进行研究,以验证由gB疫苗形式呈现的新表位的假设。
总之,该人类挑战模型中的数据表明,gB疫苗的有效性是由一种机制决定的,而不是完全依赖于经典的中和生物活性。
材料和方法 该研究得到了伦敦大学学院研究伦理委员会的批准,所有样本在此接受调查的患者都出具了书面知情同意书( 9 ).
为了评估血清的中和能力,HCMV与血清预先孵育1 h,然后将整个样本用于感染人类胎儿成纤维细胞(HFF)。 或者,将病毒与抗gB抗体2F12(Abcam)或抗AD-2单克隆抗体ITC88孵育( 23 , 36 ). 24小时后,使用抗IE(Millipore;1:1000)和山羊抗鼠Alexafluor 568 nm(Life Technologies;1:1000。 或者,使用抗pp28抗体(Santa Cruz;1:1000)对固定在72 hpi的细胞进行染色,并用相同的二级抗体进行检测。 用DAPI(Sigma)对细胞核进行复染。 使用Hermes WiScan仪器和软件计算感染率。
要么是高攻击性梅林病毒(无细胞生长),要么是一种IE2-GFP病毒,这种病毒的生长主要与细胞相关(理查德·斯坦顿的礼物( 20 )]以0.01的MOI感染HFF。 在感染后1至14天,对细胞进行固定和染色以检测IE(Merlin)或观察GFP表达(IE2-GFP)。 用DAPI(Sigma)对细胞核进行复染。 使用Hermes WiScan仪器和软件计算感染率。
为了检测ADCC抗体,使用了来自血清阴性健康供体的总PBMC或纯化NK细胞(MACS NK-cell分离试剂盒II;Miltenyi Biotec)。 简单地说,96个平板涂有gB疫苗蛋白(0.75μg/孔),然后用PBS稀释的血清孵育。 将PBMC或NK细胞添加到微孔中,48小时后,收集细胞并对其进行CD3、CD56和CD107a表达染色(BD Biosciences),并通过流式细胞术进行计数。 PMA和离子霉素刺激作为阳性对照,健康血清阴性供者血清作为阴性对照。 此外,从血清阴性中分离出的流行性血清被用作基线阴性反应。
AD1、-2、-4和-5的ELISA已在前面描述( 15 ). AD1和AD2是非结构表位,并且已经确定这些肽被AD1和AD2抗体反应识别。 所用的重组AD4已被已知的AD4构象抗体识别,并且AD5抗原的结构已被证明与gB中的AD5具有相同的结构( 15 , 37 , 38 ). 简单地说,按照说明在PBS中稀释血清,然后用肽涂层96孔板培养。 健康血清阳性和血清阴性血清作为对照。 用HRP偶联的抗人IgG检测CMV抗体,并用3,3',5,5'-四甲基联苯胺底物进行可视化。 在450nm处测量OD。 第1次就诊(例如,血清阴性患者的患病率)被设定为背景/基线。
致谢 这项工作由欧洲联盟在FP7居里夫人行动下资助,拨款316655(VacTrain); Deutsche Forschungsgemeinschaft Grant MA 929/11-1; Wellcome Trust Grant WT/204870/Z/16/Z.M.B.R.获得了医学研究委员会奖学金(G:0900466)的支持。 gB/MF59的最初临床试验得到了国家过敏和传染病研究所拨款R01AI051355和赛诺菲·巴斯德的支持。
脚注
利益冲突声明:Sylvie Pichon是赛诺菲巴斯德的员工。 然而,出版这份手稿没有任何个人经济收益。
工具书类
1 Legendre C,Pascual M.提高面临巨细胞病毒感染风险的实体移植受者的预后:迟发性疾病和间接后果。 临床传染病。 2008; 46:732–740. doi:10.1086/527397。 [ DOI程序 ] [ 公共医学 ] [ 谷歌学者 ]
2 Griffiths P,Baraniak I,Reeves M。人类巨细胞病毒的发病机制。 病理学杂志。 2015; 235:288–297. doi:10.1002/path.4437。 [ DOI程序 ] [ 公共医学 ] [ 谷歌学者 ]
三。 Arvin AM、Fast P、Myers M、Plotkin S、Rabinovich R。国家疫苗咨询委员会预防巨细胞病毒病的疫苗开发:国家疫苗顾问委员会的报告。 临床传染病。 2004; 39:233–239. doi:10.1086/421999。 [ DOI程序 ] [ 公共医学 ] [ 谷歌学者 ]
4 Bernstein DI等。CMV血清阴性成人志愿者中巨细胞病毒α病毒复制子疫苗的随机、双盲、1期试验。 疫苗。 2009; 28:484–493. doi:10.1016/j.疫苗.2009.09.135。 [ DOI程序 ] [ 公共医学 ] [ 谷歌学者 ]
5 Plotkin SA等。Towne株减毒病毒疫苗在血清阴性肾移植受者中的多中心试验。 移植。 1994; 58:1176–1178. [ 公共医学 ] [ 谷歌学者 ]
6 Pass RF等。母体巨细胞病毒感染的疫苗预防。 《新英格兰医学杂志》,2009年; 360:1191–1199. doi:10.1056/NEJMoa0804749。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
7 Schleiss MR巨细胞病毒疫苗正在临床开发中。 J病毒错误。 2016; 2:198–207. [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
8 Adler SP等。原发性人类巨细胞病毒感染诱导的免疫可保护育龄妇女免受二次感染。 传染病杂志。 1995; 171:26–32. doi:10.1093/infdis/1171.1.26。 [ DOI程序 ] [ 公共医学 ] [ 谷歌学者 ]
9 Griffiths PD等。移植受者中使用MF59佐剂的巨细胞病毒糖蛋白-B疫苗:一项2期随机安慰剂对照试验。 柳叶刀。 2011; 377:1256–1263. doi:10.1016/S0140-6736(11)60136-0。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
10 Schleiss MR.VCL-CB01,一种可注射的双价质粒DNA疫苗,具有潜在的CMV疾病和感染保护作用。 当前操作摩尔热。 2009; 11:572–578. [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
11 Bernstein DI等。青少年女孩巨细胞病毒糖蛋白B(gB)疫苗的安全性和有效性:一项随机临床试验。 疫苗。 2016; 34:313–319. doi:10.1016/j.疫苗.2015.11.056。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
12 Isaacson MK、Juckem LK、Compton T.病毒进入和先天免疫激活。 当前顶级微生物免疫学。 2008; 325:85–100. doi:10.1007/978-3-540-77349-8_5。 [ DOI程序 ] [ 公共医学 ] [ 谷歌学者 ]
13 Isaacson MK,Compton T.人巨细胞病毒糖蛋白B是病毒进入和细胞间传播所必需的,但不是病毒粒子附着、组装或流出所必需的。 《维罗尔杂志》。 2009; 83:3891–3903. doi:10.1128/JVI.01251-08。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
14 Rasmussen L、Matkin C、Spaete R、Pachl C、Merigan TC。人类自然感染后对人巨细胞病毒糖蛋白gB和gH的抗体反应。 传染病杂志。 1991; 164:835–842页。 doi:10.1093/infdis/164.5.835。 [ DOI程序 ] [ 公共医学 ] [ 谷歌学者 ]
15 Pötzsch S等人B细胞全谱分析确定了人类巨细胞病毒糖蛋白B上的新抗原结构域,这些结构域是中和抗体的靶点。 《公共科学图书馆·病理学》。 2011; 7:e1002172。 doi:10.1371/journal.ppat.1002172。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
16 Banks T等。裂解的巨细胞病毒B糖蛋白羧基末端一半内的主要中和域图。 维罗尔将军。 1989; 70:979–985. doi:10.1099/0022-1317-70-4-979。 [ DOI程序 ] [ 公共医学 ] [ 谷歌学者 ]
17 Lu LL,Suscovich TJ,Fortune SM,Alter G.超越结合:抗体效应器在传染病中的作用。 Nat Rev免疫学。 2018年; 18:46–61. doi:10.1038/nri.2017.106。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
18 Kwong PD、Mascola JR、Nabel GJ。 广泛中和抗体和HIV-1疫苗的研究:开始的结束。 Nat Rev免疫学。 2013; 13:693–701. doi:10.1038/nri3516。 [ DOI程序 ] [ 公共医学 ] [ 谷歌学者 ]
19 Shiraki K等。水痘-带状疱疹病毒的中和抗gH抗体调节gH的分布并诱导基因调节,模拟潜伏期。 《维罗尔杂志》。 2011; 85:8172–8180。 doi:10.1128/JVI.00435-11。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
20 Murrell I等人。五聚体复合物驱动野生型人类巨细胞病毒的免疫隐蔽细胞间传播。 美国国家科学院院刊2017; 114:6104–6109. doi:10.1073/pnas.1704809114。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
21 Jegaskanda S等。在缺乏中和抗体的情况下,交叉反应性流感特异性抗体依赖性细胞毒性抗体。 免疫学杂志。 2013; 190:1837–1848. doi:10.4049/jimmunol.1201574。 [ DOI程序 ] [ 公共医学 ] [ 谷歌学者 ]
22 Baraniak I等人,MF59人巨细胞病毒糖蛋白-B疫苗的表位特异性体液反应:抗-D2水平与病毒血症保护相关。 传染病杂志。 2018年doi:10.1093/infdis/jiy102。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
23 Ohlin M、Sundqvist VA、Mach M、Wahren B、Borrebeck CA。用人单克隆抗体测定的人对巨细胞病毒gp58/116(gB)上表达的主要中和表位的免疫反应的精细特异性。 《维罗尔杂志》。 1993; 67:703–710. doi:10.1128/jvi.67.2.703-710.1993。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
24 Burton DR。抗体、病毒和疫苗。 Nat Rev免疫学。 2002; 2:706–713. doi:10.1038/nri891。 [ DOI程序 ] [ 公共医学 ] [ 谷歌学者 ]
25 Cui X,Meza BP,Adler SP,McVoy MA。巨细胞病毒疫苗无法诱导与自然感染相当的上皮进入中和抗体。 疫苗。 2008; 26:5760–5766. doi:10.1016/j.vaccine.2008.07.092。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
26 Fouts AE等。抗CMV gH/gL单克隆抗体MSL-109的中和活性机制。 美国国家科学院院刊,2014年; 111:8209–8214. doi:10.1073/pnas.1404653111。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
27 Manley K等人。人类巨细胞病毒通过将其结合到组装的病毒粒子中,从而逃脱自然产生的中和抗体。 细胞宿主微生物。 2011; 10:197–209. doi:10.1016/j.chom.2011.07.010。 [ DOI程序 ] [ 公共医学 ] [ 谷歌学者 ]
28 Kabanova A等。人类巨细胞病毒gHgLpUL128L亚单位疫苗的抗体驱动设计,选择性诱导有效的中和抗体。 美国国家科学院院刊,2014年; 111:17965–17970. doi:10.1073/pnas.1415310111。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
29 Jacob CL等。中和抗体无法抑制人巨细胞病毒的直接病毒细胞间传播。 病毒学。 2013; 444:140–147. doi:10.1016/j.virol.2013.06.002。 [ DOI程序 ] [ 公共医学 ] [ 谷歌学者 ]
30 Finnefrock AC等。针对人类巨细胞病毒糖蛋白B抗原域-2的肽结合疫苗的临床前评估。 Hum疫苗免疫疗法。 2016; 12:2106–2112. doi:10.1080/21645515.2016.1164376。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
31 Bootz A等。中和和非中和抗体对巨细胞病毒糖蛋白B的保护能力。 《公共科学图书馆·病理学》。 2017; 13:e1006601。 doi:10.1371/journal.ppat.1006601。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
32 Corey L等人,《疫苗预防HIV-1感染的免疫相关性》。 2015年《科学与运输医学》; 7:310伏。 doi:10.1126/scitranslmed.aac7732。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
33 Haynes BF等。HIV-1疫苗疗效试验的免疫相关性分析。 《N Engl J Med.2012》; 366:1275–1286. doi:10.1056/NEJMoa1113425。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
34 Jackson SE、Mason GM、Wills MR。人类巨细胞病毒免疫和免疫逃避。 病毒研究2011; 157:151–160. doi:10.1016/j.virusres.2010.10.031。 [ DOI程序 ] [ 公共医学 ] [ 谷歌学者 ]
35 Muntasell A、Vilches C、Angulo A、López-Botet M。人类NK细胞隔室对巨细胞病毒的适应性重组:宿主-猪相互作用的不同视角。 欧洲免疫学杂志。 2013; 43:1133–1141. doi:10.1002/eji.201243117。 [ DOI程序 ] [ 公共医学 ] [ 谷歌学者 ]
36 Reeves MB、Breidenstein A、Compton T。人巨细胞病毒激活ERK和髓细胞白血病-1蛋白与潜在感染细胞的存活相关。 美国国家科学院院刊2012; 109:588–593. doi:10.1073/pnas.1114966108。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
37 Wiegers AK,Sticht H,Winkler TH,Britt WJ,Mach M.人巨细胞病毒糖蛋白B抗原域5内中和表位的鉴定。 《维罗尔杂志》。 2015; 89:361–372. doi:10.1128/JVI.02393-14。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
38 Spindler N等。中和人抗体识别人巨细胞病毒糖蛋白B的结构基础。 《公共科学图书馆·病理学》。 2014; 10:e1004377。 doi:10.1371/journal.ppat.1004377。 [ DOI程序 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
关联数据 本节收集本文中包含的任何数据引用、数据可用性声明或补充材料。