介绍 代谢型谷氨酸(mGlu)受体属于G蛋白偶联受体(GPCR)大家族的C类。 mGlu受体定位于神经元和胶质细胞的突触和突触外部位,通过检测细胞外谷氨酸浓度来调节突触传递的强度。 mGlu受体参与学习和记忆等生理过程以及各种病理疾病。 尽管在最近的临床试验中普遍缺乏成功,但mGlu受体仍然是治疗各种神经精神疾病(如焦虑和抑郁)、神经发育疾病(如精神分裂症)和神经退行性疾病(如阿尔茨海默病和帕金森病)的有吸引力的药物靶点 1 。
mGlu受体根据序列同源性和G蛋白信号分为3类。 谷氨酸诱导的I组刺激(mGlu 1 和mGlu 5 )优先触发Gq激活,而II组(mGlu 2 和mGlu 三 )和III组(mGlu 4 和mGlu 8 )优先耦合到Gi/o 2 , 三 mGlu二聚体信号转导的分子基础尚不清楚,因为在活性和非活性状态下缺乏全长受体的结构。 mGlu受体是复杂的变构机器,谷氨酸活性可以被正变构调节剂(PAM)增强或被负变构调制器(NAM)抑制 4 此外,一些被称为激动剂-PAM(ago-PAMs)的化合物可以与变构结合位点结合,并在缺少谷氨酸等正构激动剂的情况下显示激动剂活性。
从分子角度来看,与大多数GPCR相比,mGlu和其他C类受体并不常见。 它们是必需的二聚体,二聚体对其功能至关重要 三 , 5 每个mGlu单体都包含一个大的胞外结构域(ECD),由捕蝇草结构域(VFT)和富含半胱氨酸结构域(CRD)组成。 VFT是一个双折叠结构,在形成正构结合位点的叶之间有一个裂缝。 CRD将VFT连接到七螺旋跨膜结构域(7TM),该结构域随后终止于C末端结构域。 已知一些变构调节剂与7TM结构域结合。 mGlu受体的C末端区域是非结构化的,尽管它对信号调制很重要 6 。
当考虑到功能选择性时,mGlu受体功能增加了额外的复杂性。 最近的研究报道了mGlu受体的有偏变构调节,尤其是mGlu 5 7 尽管这些研究由于只分析了下游效应器的变化而变得复杂。 mGlu信号 5 受体在HEK细胞或由激动剂3,4-二羟基苯二醇(DHPG)诱导的神经元中,在存在或不存在多种PAM的情况下,或通过单独使用ago PAM 8 ,诱导不同信号通路的激活 7 ,但通过Gq。 此外,激动剂诱导的mGlu 5 转染细胞中cAMP水平升高 9 尽管本研究中尚不清楚这是否是由mGlu直接激活Gs所致 5 配体依赖的功能选择性突出了mGlu的复杂性和多样性 5 信号转导。 它还强调了理解配体-受体相互作用的分子基础的重要性,以及这些分子如何驱动导致不同信号输出的构象变化。 开发针对变构结合位点的药物以实现功能选择性可能对减少副作用非常有益。 然而,由于对mGlu受体信号转导的结构基础缺乏了解,这仍然是一项具有挑战性的任务。
已经确定了C类GPCR的孤立结构域的结构,其中包括几种mGlu受体亚型、钙受体、GABA的VFT和ECD B类 受体和味觉受体 10 —— 14 此外,mGlu的7TM结构域的结构 1 和mGlu 5 已通过X射线晶体学测定 15 , 16 ,尽管它们都处于非活动状态。 全长mGlu受体的结构尚未确定。 因此,尚不清楚构象变化是如何从VFT传播到7TM的 17 , 18 以及如何实现功能选择性。 洗涤剂纯化的全长mGlu受体二聚体的功能特性对理解这些现象至关重要。
在这里,我们研究了人mGlu的表达、稳定性和纯化 5 野生型人mGlu 5 该受体在昆虫细胞中表达并纯化至均一性,为启动功能研究提供了足够的单分散受体。 纯化的受体具有功能,并在与内源性正构激动剂谷氨酸或合成的高亲和力ago-PAM VU0424465结合后激活G蛋白Gq。 最后,我们证明了VU0424465诱导mGlu 5 -HEK293细胞中的依赖性Gs激活以及洗涤剂结合Gs中的纯化受体。因此,纯化的功能性全长mGlu 5 本研究中产生的受体是其结构测定的第一步。
结果 定义最小人类mGlu 5 建造 C类GPCR的C端被认为是非结构化的 19 因此,为了最小化受体的灵活性,我们研究了保持Gq蛋白激活所需的C末端尾部的最小长度。 通过引入终止密码子设计了一系列C末端截断,该终止密码子将C末端从残基L865缩短到残基N832,对应于跨膜螺旋7(TM7)的细胞内末端。 然后,通过使用Cisbio IP-One®分析法测量磷脂酰肌醇(PI)分解,检查每个突变体的Gq激活(补充图 1 和 2 ). 数据显示mGlu的C端尾部 5 可截短至残基K851,而不会显著降低谷氨酸对Gq活化的效力。 进一步删除C-末端氨基酸残基会削弱Gq的激活。 尽管mGlu 5 -Δ851具有允许信号发送的C末端的最小长度,我们选择mGlu 5 -Δ856用于未来的工作,以确保有足够的长度来形成a类GPCR中观察到的螺旋8 20 突变体hmGlu 5 -ΔCter-A856具有pEC 50 谷氨酸为4.35±0.06(n=5),喹喹酯为7.34±0.18(n=6)(图 1安培 和补充 2 ). 这些值与全长野生型(WT)mGlu的值相似 5 pEC受体 50 谷氨酸的s为4.48±0.05(n=5),喹喹酯的s为7.51±0.15(n=5)(图 1B年 ). 截断结构(SNAP-mGlu)的热稳定性 5 -Δ856)和全长结构(SNAP-mGlu 5 -WT)也已确定。 两个构造都显示类似的明显T 米 值与先前出版的工作一致(WT,19.95±0.73°C(n=6); 微克葡萄糖 5 -Δ856 19.87±0.67°C(n=6); 图 1摄氏度 ) 16 因此,构造mGlu 5 -Δ856是一种全功能GPCR,具有人类mGlu二聚化和活化所需的所有结构特征 5 受体,并用于所有进一步的生化表征和纯化。
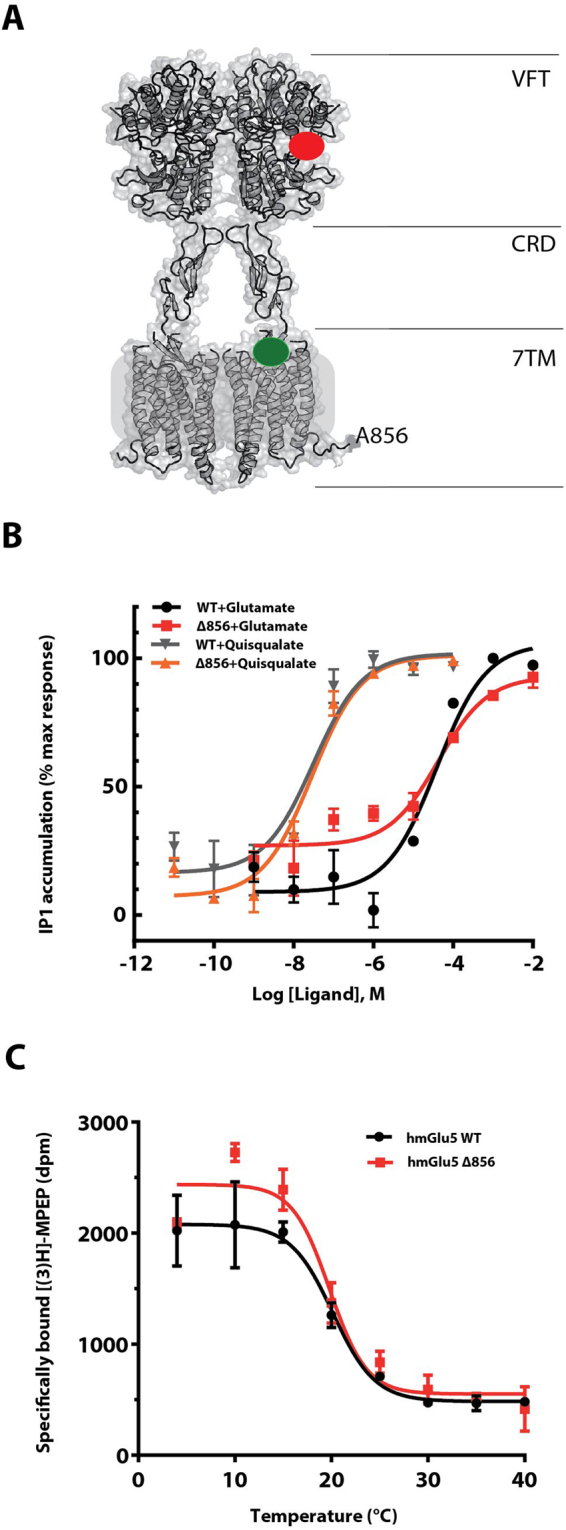
图1。
功能性C端截断SNAP-mGlu 5 受体二聚体。 ( A类 )人类mGlu的三维模型 5 受体在Ala856残基后截断。 截短受体由有效G蛋白信号传递所需的所有片段组成,包括维纳斯捕蝇草结构域(VFT)、富含半胱氨酸结构域(CRD)和七螺旋跨膜结构域(7TM)。 红色和绿色球体分别代表正构和变构结合位点。 ( B类 )瞬时转染SNAP-Tag全长人mGlu的HEK293细胞中谷氨酸和喹喹酯诱导的IP1生成 5 受体(黑色和灰色曲线)或SNAP-Tag C端mGlu 5 -Δ856受体(红色和橙色曲线)。 ( C类 )全长野生型mGlu的热稳定性 5 和mGlu 5 -Δ856 [ 三 H] -MPEP结合受体。 两种分析的数据点代表三个独立实验的平均值±SEM。
N-连接糖基化的表征 人类mGlu 5 氨基酸序列包含6个潜在的N-糖基化NX(S/T)共有位点,位于预计位于细胞外表面的受体区域。 其中五个站点位于大型VFT域中(图 2安培 )并且一个额外的位点在7TM的第二细胞外环(EL)中。 N-糖基化受体的异质性会阻碍其结晶,但N-糖基化对细胞表面功能性受体的表达也很重要。 我们探讨了这些位点对折叠良好受体的细胞表面表达的贡献。
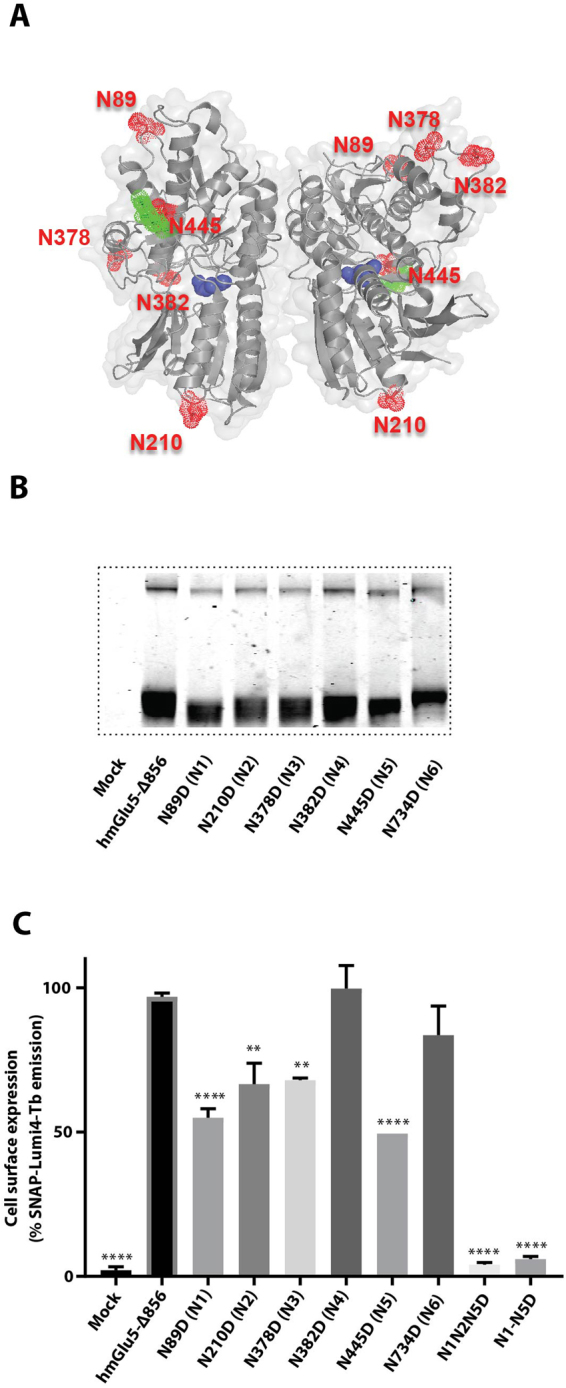
图2。
SNAP-mGlu的特性 5 -∆856 N-糖基化在HEK293细胞中的分布。 ( A类 )五mGlu 5 N-连接的糖基化位点在VFT(代码pdb 3LMK)的卡通结构(灰色)上突出显示为表面球体(红色)和糖部分(绿色)。 与VFT结合的谷氨酸分子中的原子表示为蓝色球体。 ( B类 )单体SNAP-mGlu的SDS-PAGE凝胶迁移 5 -Δ856和不同的N-糖基化突变体。 样品用还原剂(DTT)处理。 ( C类 )荧光标记SNAP-mGlu的细胞表面表达 5 -Δ856和使用SNAP-Lumi4Tb的不同N-糖基化突变体。 凝胶是重复至少两次的一个实验的代表。 表达谱是至少三个独立实验的代表。 邓内特的测试是其中的一部分 - 方差分析用于与hmGlu比较的方法 5 -Δ856设为参考水平。
SNAP-mGlu的六个突变体 5 -生成Δ856,其中每个天然N-糖基化位点从NxS/T突变为DxS/T。然后在HEK293细胞中瞬时表达这些结构,并用细胞免疫荧光标记细胞外SNAP标签。 然后使用合适的清洁剂从细胞中提取SNAP标记的受体,并通过SDS-PAGE分析未净化物质。 SNAP-mGlu 5 -Δ856受体在非还原条件下主要以二聚体(表观分子量180–200 kDa 三 ). 虽然单体和二聚体受体都可以在SDS-PAGE凝胶上看到,但我们的分析基于还原条件下形成的单体物种的凝胶迁移率变化(加上DTT),因为分子量的微小变化更为明显。 数据显示,当每个N-糖基化位点N1-N5发生突变时,单体受体的分子量略有下降(图 2B型 )表明它们参与WT受体的糖基化。 然而,定位于7TM结构域的N6位点突变似乎没有发生N-糖基化,因为该突变的表观分子量与野生型受体相似。
这些突变对SNAP-mGlu细胞表面表达的影响 5 -测定了五个N-糖基化位点突变体N1-N5的Δ856受体。 突变N1、N2、N3和N5会显著损害受体的细胞表面表达(图 2摄氏度 ). 只有突变N382D(N4)在细胞表面的表达水平没有降低,尽管表观分子量的降低表明该位点是N-糖基化的。 为了进一步减少受体上的N-聚糖数量,构建了一个突变体,其中三个糖基化位点(N1N2N5)发生突变,另一个突变型结合了所有5个突变的N-糖基化部位(N1-N5)。 SNAP标签荧光标记后,在细胞表面未检测到三重突变体(N1N2N5)或五重突变体(N1-N5)(图 2摄氏度 ). 总之,这些结果表明,在HEK293和Sf9细胞中,VFT中定位的所有5个N-糖基化位点都是N-糖基化的,并且至少4个位点的N-糖基化在确保受体的细胞表面表达方面起着关键作用。
mGlu的洗涤剂增溶和稳定性 5 -Δ856 GPCR的结构特征因其在洗涤剂中缺乏稳定性而变得复杂,因此难以在功能状态下纯化 21 因此,重要的是要确定一种能够保持mGlu的合适清洁剂 5 溶解后处于功能和稳定状态。 测量洗涤剂固体受体相对数量及其热稳定性的一种方法是使用放射性配体结合分析 22 为此,我们使用了“超级+”形式的放射性配体结合分析,该分析包括在进行洗涤剂溶解之前,使受体与放射性标记配体平衡(见材料方法部分) 22 , 23 这允许测定表观熔化温度(表观温度 米 )定义为50%的可溶性受体仍能与放射配体结合的温度。 表观T 米 是洗涤剂溶液中未净化受体稳定性的可靠指标。
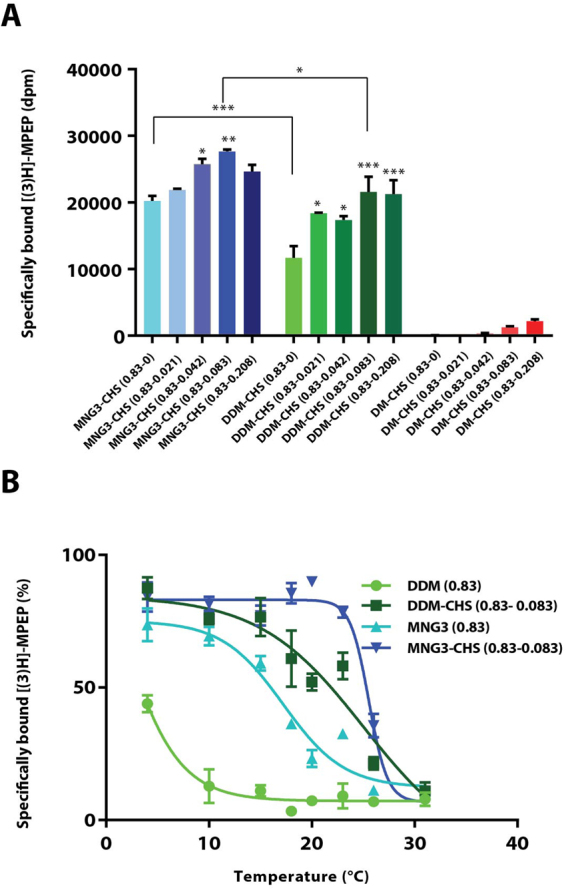
微克葡萄糖 5 -Δ856在昆虫细胞中表达,高亲和力放射性标记NAM[ 三 H] -结合7TM结构域的MPEP用于监测洗涤剂溶解后功能受体的百分比。 我们首先测试了两种温和的非离子洗涤剂,它们已成功用于许多GPCR的分离和纯化,即 n个 -十二烷基-β-D-麦芽糖苷(DDM)和麦芽糖-新戊二醇-3 24 (MNG3)。 此外,我们还测试了较短的烷基链同系物癸基-β-D-麦芽糖苷(DM)。 通过用胆固醇半琥珀酸酯(CHS)(一种用于进一步稳定GPCR的胆固醇衍生物)补充选定的洗涤剂,进一步优化了洗涤剂的溶解条件。 首次评估洗涤剂溶解mGlu的能力 5 以仍然可以绑定的功能形式[ 三 H] -4°C时的MPEP(图 3A级 ). 我们的结果清楚地表明,可溶性功能性mGlu的最高含量 5 -Δ856受体与MNG3结合,而DDM的效率低两倍。 然后用CHS补充洗涤剂,使最终浓度在0.04%至0.08%之间。 当MNG3添加CHS时,可溶性受体数量略有增加,在CHS为0.08%时达到最大产量。 添加CHS还显著提高了DDM中可溶性受体的数量。 我们发现0.08%的CHS浓度最适合溶解mGlu 5 受体二聚体。 微克葡萄糖 5 即使存在CHS,在DM中溶解后,受体也不稳定。
图3。
mGlu的洗涤剂增溶和热稳定性 5 -Δ856 [ 三 H] -昆虫细胞中的MPEP结合受体。 ( A类 )未净化mGlu的定量 5 -Δ856受体在4°C下用[ 三 H] -在一系列麦芽糖苷基洗涤剂中测定MPEP结合分析,这些洗涤剂包括月桂基麦芽糖新戊二醇-3(MNG3)、n-十二烷基-β-D-麦芽糖甙(DDM)和添加不同比例胆固醇半琥珀酸盐(CHS)的n-癸基-β-D麦芽糖肽(DM)。 ( B类 )mGlu的热稳定性 5 -Δ856 [ 三 H] -MPEP结合受体在四种不同条件下溶解; DDM(0.83%)、DDM-CHS(0.83–0.083%)、MNG3(0.83%)和MNG3-CHS(0.83–0.083%)。 两种分析的数据点( A、 B类 )表示三个独立实验的平均值±SEM。 邓内特的测试是其中的一部分 - 用方差分析法与MNG3-CHS(0.83-0)和DDM-CHS(083-0)分别作为MNG3和补充CHS的DDM的参考水平进行比较。
为了确定溶解和纯化的最佳洗涤剂,mGlu的热稳定性 5 绑定到[ 三 H] -在存在或不存在0.08%CHS的情况下,在0.8%MNG3和0.8%DDM中测定MPEP(图 第3页 ). 表观T 米 mGlu的 5 在MNG3中溶解的受体为18±0.3°C(n=3),但在DDM中该受体太不稳定,导致明显的T 米 待测量。 添加CHS显著提高了mGlu的稳定性 5 在两种洗涤剂中都有明显的T 米 DDM/CHS为21±1.5°C(n=3),表观温度为 米 在MNG3/CHS中为25±0.1°C(n=3)。 由于MNG3/CHS为[ 三 H] -MPEP结合mGlu 5 -Δ856,我们使用这些条件进行溶解和纯化。
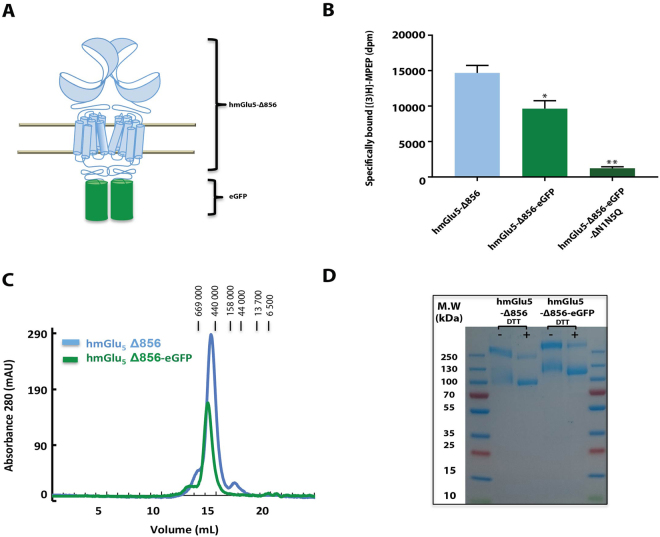
mGlu的表达与纯化 5 -来自Sf9细胞的Δ856 大规模生产mGlu 5 -Δ856是使用杆状病毒表达系统在Sf9细胞中进行的。 该系统用于表达迄今为止大多数结晶的GPCR,因为它通常具有良好的产率,并且可以进行翻译后修饰,如N-糖基化 25 .我们首先优化了mGlu的纯化 5 -Δ856在C端与eGFP熔断(图 4A级 ). 微克葡萄糖 5 -Δ856-eGFP显示出与野生型受体类似的药理学,使用[ 三 H] -MPEP结合分析(图 4B类 ). 对于HEK293细胞,糖基化对受体表达很重要。 我们测试了mGlu的表达 5 Sf9昆虫细胞中的ΔN1-N5突变体。 突变所有糖基化位点可消除受体表达(图 4B类 ). mGlu的纯化 5 -Δ856-eGFP在镍上实现 2+ -亲和柱后在MNG3/CHS中进行尺寸排除色谱(SEC)(图 4摄氏度 ). 纯化受体的凝胶过滤曲线(Superose 6增加,GE Healthcare)是对称的,这表明纯化受体是单分散的。 非还原性SDS-PAGE鉴定出一条表观分子量(MW)为~250kDa的主带和一条125kDa小带,这与mGlu的理论MW很好地对应 5 -eGFP二聚体(249568 Da)和单体(124784 Da)(图 4天 ). SDS-PAGE上蛋白质条带的同一性通过质谱法得到证实(补充图 4 ). 两条带都产生了15个与mGlu序列匹配的肽片段 5 -eGFP序列覆盖率为60%。 尽管SEC图谱没有显示出任何单体的存在,但SDS-PAGE观察到与单体相对应的一条小条带,这可能是由于SDS引起的离解所致。 与非还原样品相比,用还原试剂处理纯化样品以破坏二聚体增加了在125 kDa下迁移的单体物种的强度(图 4天 )。
图4。
二聚体mGlu的纯化 5 -在SF9细胞中产生∆856。 ( A类 )人类二聚体mGlu的卡通表示 5 带有融合蛋白eGFP(绿色)的受体(浅蓝色)取代856位的c末端结构域。 ( B类 )未净化mGlu的定量 5 受体使用[ 三 H] -MPEP结合分析,测定mGlu 5 -Δ856,mGlu 5 -Δ856-eGFP和mGlu 5 -Δ856-eGFP(N1-N5)。 邓内特的测试是其中的一部分 - 方差分析用于与mGlu比较的方法 5 -Δ856设为参考水平。 ( C类 )两种结构物的尺寸排除色谱图,mGlu 5 -Δ856(Ve=14.5毫升)和mGlu 5 -Δ856-eGFP(Ve=14.2 mL)使用叠加6增加。 ( D类 )考马斯蓝染色的mGlu SDS-PAGE凝胶 5 -Δ856和mGlu 5 -Δ856-eGFP。 所示凝胶是三个独立实验的代表。
我们最初仅将一个糖基化位点(N445)突变为该结构中的丙氨酸,因为mGlu的可用PDB结构中的糖部分很明显 5 VFT(3LMK)(图 2安培 ). 事实上,正如我们上面所证明的,由于表达水平的严重下降,不可能突变多个糖基化位点(图 2摄氏度 ). 用肽处理纯化的受体- N个 -葡萄糖苷酶F(PNGase F)过夜后再进行SEC,导致脱糖基化受体的纯化(补充图 4摄氏度 ). 最终产量为0.05 mg纯化mGlu 5 -获得了每升Sf9昆虫细胞培养物中的eGFP蛋白。 我们还纯化了另一个结构体mGlu 5 -Δ856,C端无eGFP(补充图 1摄氏度 )使用相同的方案,但包括额外的纯化步骤(使用抗FLAG标签抗体树脂的亲和层析)。 我们最终获得0.04 mg高纯度mGlu 5 -Δ856/升Sf9(图 4 ),这是进一步的特点 在体外 使用G蛋白活化分析。
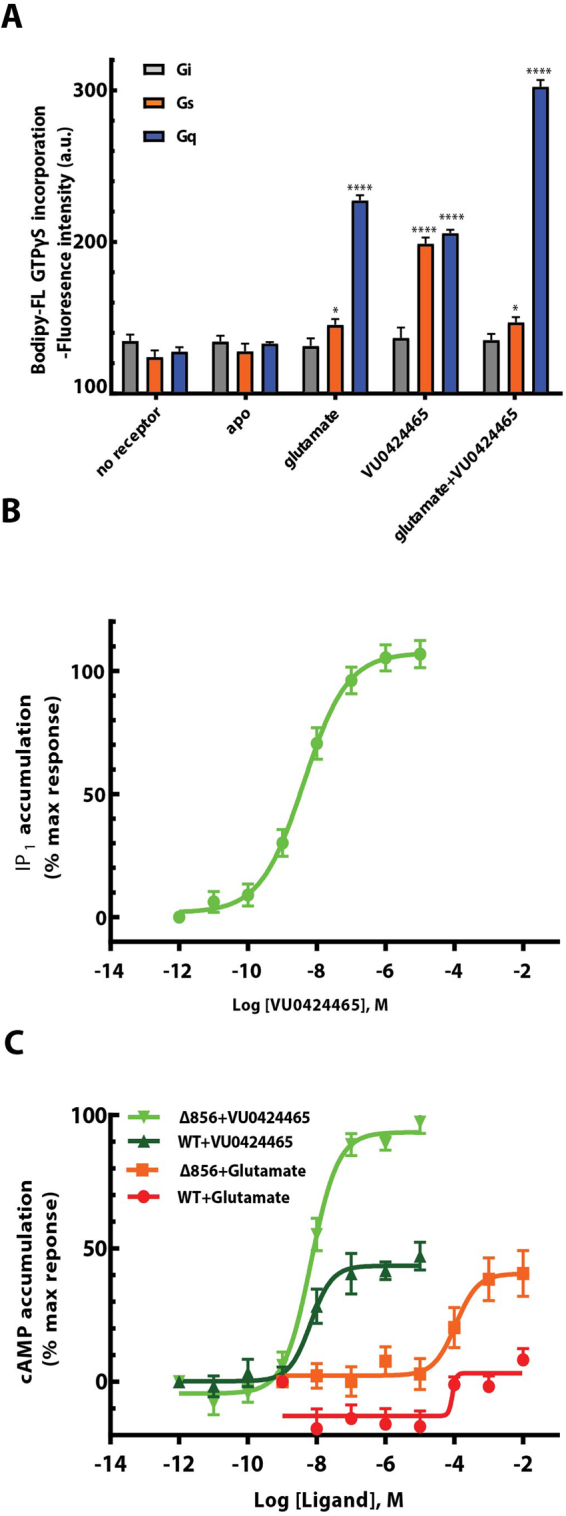
纯化mGlu的功能表征 5 受体 纯化mGlu 5 -使用荧光Body-FL GTPγS类似物测试Δ856激活纯化异三聚体G蛋白Gq的能力 26 .天然激动剂谷氨酸诱导Gα的募集和激活 q个 β 1 γ 2 与对照条件相比,Body-FL GTPγS荧光增加(图 5A级 ). ago-PAM VU0424465 27 产生类似谷氨酸的强烈反应,并显示pEC 50 在HEK293细胞中为8.53±0.13(n=4)(图 5亿 ). 这里制定的纯化方案排除了谷氨酸的存在,因此这些数据证实了VU0424465直接激活受体的能力。 最后,谷氨酸和VU0424465的组合使最大反应增加了30%,支持VU0444465的变构作用。
图5。
谷氨酸和VU0424465触发mGlu 5 -依赖性Gs和Gq激活。 ( A类 )通过配体活化诱导洗涤剂纯化受体进行GTPγS荧光结合实验。 荧光基线是根据不含任何配体的受体单独估算的。 数据点表示使用SEM进行的三次独立测量的平均值 - 方差分析法用于和载脂蛋白条件集作为参考水平进行比较。 ( B类 )微克葡萄糖 5 -使用IP单细胞检测试剂盒(Cisbio)在HEK293细胞和存在VU0424465和pEC的情况下测量依赖性Gq激活 50 为8.53±0.13(n=4)。 ( C类 )mGlu蛋白 5 -使用cAMP细胞检测试剂盒(Cisbio)分别在HEK293细胞和谷氨酸和VU0424465存在下测量依赖性Gs活化。 剂量-反应曲线显示VU0424465在截断mGlu处的正反应 5 -Δ856(浅绿色,pEC 50 8.17±0.11; n=4)和WT人类mGlu 5 (深绿色,pEC 50 7.80±0.50; n=3)曲线。 在截断的mGlu处观察到谷氨酸的激活较弱 5 -Δ856(橙色,pEC 50 3.86±0.20; n=3)和WT人mGlu 5 (红色,pEC 50 3.36±0.72; n=3)曲线。 数据点表示至少三个独立的SEM实验中三次测量的平均值。
我们还研究了纯化的mGlu的G蛋白选择性 5 -Δ856通过测试其激活纯化Gs和Gi的能力。我们无法测量谷氨酸或mGlu的VU0424464刺激对Gi的激活 5 -Δ856(图 5A级 ). 相反,观察到Gs的强烈激活,其荧光信号强度类似于VU0424464对Gq的激活所观察到的荧光信号强度。 通过在表达mGlu的HEK293细胞系中检测到VU0424465诱导的强烈cAMP剂量反应,我们证实了这一发现 5 -Δ856(图 5摄氏度 ). VU0424465显示pEC 50 与Gq激活(pEC)类似的Gs信号通路为8.17±0.11(n=4) 50 8.53±0.13(n=4))(图 5亿 ). 谷氨酸刺激纯化的mGlu 5 -Δ856仅诱导GsG蛋白的部分激活(图 5A级 ). 因此,在mGlu上检测到微弱但显著的cAMP生成 5 用pEC高浓度刺激受体 50 3.86±0.20(n=3)(图 5摄氏度 ). 我们还测试了WT人类mGlu 5 受体,包括激活GsG蛋白的完整c末端(图 5摄氏度 ). 对于VU0424465和谷氨酸这两种配体,与mGlu相比,cAMP的生成显著受损 5 -Δ856.令我们惊讶的是,谷氨酸和VU0424465的结合物与洗涤剂纯化的mGlu结合 5 -Δ856激活Gq,但不激活Gs。当mGlu 5 -Δ856被重组成膜状环境,如双核细胞、谷氨酸和与mGlu结合的VU0424465 5 -Δ856导致Gs的激活(补充图 5 ). 此外,在双细胞中重组的受体的Gq激活也显著增加。 因此,脂质很可能在mGlu中发挥关键作用 5 功能性和稳定性。
讨论 在这里,我们描述了生物化学特性和蛋白质工程,从而纯化出完整的功能性mGlu 5 受体二聚体。 纯化的mGlu 5 -Δ856包含其功能所需的所有结构域,经G蛋白活化试验验证,我们首次证明了人mGlu的直接偶联 5 纯化的受体包含ECD和7TM结构域,而C末端的尾部被缩短以减少非结构区域 19 从细胞内C末端结构域去除324个氨基酸(S857-L1180)不会损害Gq蛋白信号或受体稳定性(图 1 ). 事实上,所选结构仍然具有完整的功能 米 mGlu的 5 -20°C的Δ856与WT mGlu相同 5 这意味着C末端结构域不参与维持受体的整体折叠。
考虑纯化受体的同质性时,需要考虑的一个明显参数是 N个- 糖基化。 与许多其他真核细胞膜蛋白一样,mGlu 5 -Δ856需要翻译后 N个- 糖基化将功能受体运输到细胞表面,阻止所有糖基化位点的突变。 除VFT中N382和ECL2中N734的突变体外,单个N-糖基化位点的去除显著损害了细胞表面的表达(图 2摄氏度 ). 一种完全未糖基化的mGlu 5 受体突变体在HEK293或SF9细胞中表达时不能到达细胞表面(图 2摄氏度 和 4B类 ). 这一发现强调了保留N-糖基化对mGlu表达的重要性 5 -血浆中Δ856。 N-糖基化存在于其他C类GPCR上,其作用因受体而异。 例如,N-糖基化对GABA的细胞表面表达至关重要 B类 受体 28 而人类mGlu的N-糖基化 1 受体的表达或功能都不需要受体 29 。
mGlu的稳定性 5 -进一步研究了洗涤剂中的Δ856。 测试了几种洗涤剂维持mGlu的能力 5 -Δ856处于功能状态,包括MNG3 24 和DDM,两者均含有C12多不饱和疏水性脂肪族链,以及DM(已知对GPCR不太稳定的C10分子)。 MNG3是从质膜中提取受体的最佳洗涤剂,因为与DDM或DM相比,它赋予受体更高的稳定性。MNG3首次被证明在没有CHS的情况下具有稳定性。 单靠DDM不足以维持溶液中受体的折叠,必须辅以CHS才能对人mGlu进行功能性溶解 5 接收器(图 三 ). 进一步用CHS补充MNG3洗涤剂增加了表观T 米 在10:1 MNG3:CHS比率下,7°C(图 第3页 ). 毫不奇怪,较小的洗涤剂DM(C10)未能维持mGlu 5 处于功能状态。 这些数据表明mGlu 5 -Δ856在洗涤剂中稳定性较差。
mGlu 5 -Δ856-eGFP融合用于促进建立纯化方案,其方式与其他膜蛋白类似 30 ,并成功地生成了纯mGlu 5 受体二聚体(图 4 ). 非还原条件下的SDS-PAGE显示了一条强条带,该条带以mGlu的预期分子量迁移 5 -Δ856-eGFP二聚体。 每个VFT原聚体叶I中保守半胱氨酸残基之间的二硫键对二聚体至关重要 31 当mGlu 5 -Δ856用还原剂处理。 此外,观察到的SEC剖面是单分散的,相对分子量与二聚体一致(图 4摄氏度 )。
最后,我们研究了纯化的mGlu的功能 5 -Δ856通过其激活纯化G蛋白的能力。 谷氨酸或VU0424465刺激后异源三聚体G蛋白Gq的激活表明,纯化的受体功能齐全,并且处于天然构象(图 5 ). 这两种配体的结合进一步增加了Gq的活性,这表明VU0424465进一步稳定了谷氨酸结合诱导的活性构象,并突出了纯化的mGlu的变构性质 5 二聚体。 令人惊讶的是,这项研究还证明了mGlu的能力 5 将VU0424465绑定到7TM域后直接激活Gs 27 以前有报道称,I组mGlu受体在细胞检测中与Gs偶联 9 然而,没有明确的证据表明Gs与mGlu直接偶联 5 。
在这里,我们演示了洗涤剂纯化的mGlu的直接耦合 5 在表达mGlu的HEK293细胞中进一步证实的Gs受体 5 -Δ856受体(图 5摄氏度 ). 此外,受体C末端的长度直接影响配体、谷氨酸和VU0424465的Gs偶联。 然而,mGlu 5 -与Gq联轴器相比,Gs联轴器的效率要低得多(图 5 ). 纯化的mGlu 5 在谷氨酸和VU0424465存在下,受体二聚体仅有效激活Gq而不激活Gs。这表明它们是mGlu的不同活性构象 5 这在一定程度上支持了受体的G蛋白选择性 32 显然,Gs偶联的保守识别序列与Gq的不同,并将影响G蛋白偶联的强度 33 然而,很难推测mGlu 5 在缺乏结构数据的情况下直接与Gs或Gq相互作用的残基。 观察到的VU0424465诱导的Gs刺激可能是由于分子的高亲和力和强大能力稳定7TM的活性构象,而不依赖于受体二聚体的选择性四级构象,这一事实与观察到的谷氨酸的弱Gs激活相一致。 很容易假设,在缺乏谷氨酸的情况下,mGlu的7TM单位 5 受体二聚体的功能类似于a类GPCR 34 理论上,与高亲和力PAM VU0424465结合的7TM的活性构象可能不同于VU044465与谷氨酸共结合时诱导的活性构像。 因此,G蛋白选择性的分子决定因素需要更深入的表征,考虑到受体二聚体在采样单个7TM结构域的特定构象中的贡献。
总之,纯化的mGlu 5 受体是研究C类GPCR信号转导分子基础的极好工具。 我们证明mGlu 5 受体能够直接激活Gs,这在开发靶向mGlu的新药时应被视为一种替代性信号通路 5 事实上,VU0424465的强大而有效的作用强调了变构调节剂作用的系统表征的必要性,不仅在受体的主要信号级联上,而且在其他细胞途径上。 这些替代途径可能会增加药物的有益效果,或者相反,会导致有害的副作用。 mGlu选择性的进一步表征 5 不仅在异源表达系统中,而且在神经元中都需要G蛋白信号。 本文报道的研究结果可能对以mGlu为靶点的药物的未来发展具有指导意义 5 受体。 例如,VU0424465已被证明具有一些副作用,例如诱导小动物癫痫发作 27 这些不希望出现的效应与它的自传子活性有关,可能与化合物的偏倚信号特性有关 35 完整受体的高分辨率结构需要充分了解mGlu的结构特征 5 受体二聚体,其激活模式和破译其G蛋白偶联选择性。
方法 材料 氚化2-甲基-6-(苯乙炔基)吡啶盐酸盐[ 三 H] MPEP购自美国放射性标记化学品公司(ARC),谷氨酸购自Sigma Aldrich,quisqualate和MPEP购于Tocris。SF-900 II SFM和EX-CELL-420培养基中的Sf9细胞购自Simma Aldrich、lipofectamine 2000和Life Technologies的DMEM培养基。 洗涤剂是从Anatrace订购的。 SNAP-Lumi4-Tb和SNAP红从Cisbio Bioassays获得。 Body-FL GTPγS购自ThermoFisher。 (R) 如补充材料中所述,合成了-5-((3-氟苯基)乙炔基)-N-(3-羟基-3-甲基丁烷-2-基)吡啶酰胺(VU0424465)。
突变与细胞培养 FLAG SNAP标记的mGlu的所有单点突变 5 受体结构(Cisbio Bioassays)是使用快速改变策略(安捷伦技术)生成的,并通过测序(Eurofins Genomics)进行验证。 HEK293细胞在37°C的Dulbecco改良的Eagle’s培养基(DMEM)中培养,DMEM补充有10%的胎牛血清(FBS),加湿5%的CO 2 孵化器。 然后,根据制造商的方案,使用Lipofectamine 2000将HEK293细胞转染到一个预先涂有聚-dL-鸟氨酸的96-well板中。 DNA混合物包括40 ng mGlu 5 突变体,50 ng谷氨酸转运体EAAC1 cDNA,以避免细胞释放的分析介质中的谷氨酸产生任何影响,60 ng pRK6,以将最终DNA浓度调整到150 ng。
测量mGlu的细胞效应 5 G蛋白活化 根据制造商的建议(Cisbio Bioassays),分别使用IP-One和cAMP HTRF试剂盒在96个微孔板中测量转染细胞中的磷酸肌醇(IP)积累和环AMP。 转染48小时后,HEK293细胞在DMEM-Glutamax培养基(Life Technologies)中培养2小时,然后进行测量,以降低细胞外谷氨酸浓度。 取出介质后,SNAP-mGlu 5 -通过在提供的StimB缓冲液中添加稀释至所需浓度的配体(用于IP one试剂盒)或在补充有环核苷酸磷酸二酯酶抑制剂Ro-20–1724(50μM)(用于cAMP试剂盒)的DMEM培养基中添加配体来执行∆856激动剂刺激。 然后将细胞在37°C的加湿5%CO中培养30分钟 2 孵化器。 随后,通过添加IP1-d2或cAMP-d2结合物,然后分别添加铽隐式标记的抗IP1或抗cAMP抗体,对细胞进行裂解,这两种抗体均在所提供的裂解缓冲液中稀释。 在室温下孵育一小时后,在337 nm处激发后进行HTRF测量,延迟50微秒,使用PHERAstar FS(BMG Labtech)分别在620 nm和665 nm处测量铽隐式荧光和tr-FRET信号。 使用GraphPad Prism 7.0版(加利福尼亚州圣地亚哥的GraphPat软件)分析图形。 功能性浓度响应数据拟合为四参数方程。 pEC 50 数值表示为平均值±SEM。
洗涤剂固体化受体结合和热稳定性测量 转染48小时后,在室温下用NAM培养HEK293细胞1小时[ 三 H] 80 nM时的MPEP(≈K的五倍 D类 )在含有25 mM HEPES(pH 7.4)和400 mM NaCl的缓冲液中。 然后用0.83%(w/v)MNG3和0.042%(w/v)CHS在4℃下溶解膜1 h。 可溶性受体(SNAP-mGlu 5 -∆856),然后在4至40°C的不同温度下培养30分钟。 然后将样品在4°C下冷却5分钟,并按照之前的报告进行洗涤剂溶解的配体结合实验 22 与液体闪烁溶液混合后,使用MicroBeta液体闪烁计数器(Perkin-Elmer)定量结合放射性配体。 对于昆虫细胞表达,来自1 mL Sf9细胞培养物的颗粒表达mGlu 5 -∆856在室温下与100 nM(0.5µCi)的放射性汞合金孵育1小时[ 三 H] -结合缓冲液中的MPEP(ARC,inc)(25 mM HEPES(pH 7.4),400 mM NaCl)。 非特异性结合是在200 nM MPEP(Abcam)存在下通过竞争结合测定的。 通过添加0.83%(w/v)MNG3/0.083%(w/v)CHS并在4°C下再培养1小时,完成受体的溶解。 如前所述,通过凝胶过滤柱在批处理模式下快速过滤分离游离和结合的放射性配体分子 22 然后将可溶性受体在4至31°C的不同温度下培养30分钟。 然后将4mL闪烁溶液添加到洗脱溶液中,并使用液体闪烁计数器(Tri-Carb 2100TR,Packard)测量结合放射性。 计数的放射性值以每分钟崩解数(dpm)进行恢复。 通过总结合和非特异性结合之间的差异计算特异性结合。
监测mGlu 5 细胞表面表达 使用Lumi4-Tb标记的SNAP标签监测细胞表面SNAP标记蛋白表达的定量。 简单地说,用PBS清洗细胞一次,并在37°C下用100 nM的SNAP-Lumi4-Tb在Taglite缓冲液中培养1小时(Cisbio Bioassays)。 在荧光测量之前,细胞在PBS中清洗三次,以消除未结合的游离染料。 在PHERAstar FS(BMG Labtech)上施加50μs延迟后,在337 nm处激发45μs,在620 nm处发射,测量Lumi4-Tb荧光。
N-连接糖基化位点突变 首先预测了N-连接的糖基化位点(NX(S/T))(Protter软件),然后通过N残基对D的单一替换进行突变,形成六种不同的结构:N88D(N1)、N210D(N2)、N378D(N3)、N382D(N4)、N445D(N5)和N734D(N6)。 进一步将这些突变结合起来生成N89D/N210D/N445D(N1N2N5)和N89D/N210D/N378D/N382D/N445D结构体。 所有结构均通过测序确认(Eurofins Genomics)。 SNAP-mGlu公司 5 -∆856突变体在HEK293细胞系中表达,并使用SNAP-Red标记,如前一节所述。 然后使用0.83%(w/v)MNG3/0.083%(w/v)CHS在4°C下轻轻摇晃45分钟,从膜中提取蛋白质。 然后将溶液在4°C下以12000 g离心30 min,以清除细胞碎片。在37°C下加热5 min后,将20µL补充有10 mM二硫苏糖醇(DDT)还原试剂的上清液加载到4–20%三甘氨酸凝胶上。 扫描凝胶并荧光标记SNAP-mGlu 5 -∆856在远红色激发后可视化(奥德赛成像系统)。
生成mGlu 5 Sf9细胞表达优化构建体 专门用于Sf9细胞纯化优化的构建体是使用重叠PCR设计的,在截短的人mGlu的C末端具有eGFP融合蛋白 5 残基A856后的受体。 将该受体序列亚克隆到一个修饰的pFastBac1载体(Invitrogen)中,该载体被命名为pFastBac1,其中包含一个表达盒,该表达盒中含有一个GP64肽信号序列,该序列来自 苜蓿银纹夜蛾 N末端的核型多角体病毒(AcNPV杆状病毒)和TEV蛋白酶识别位点,以及受体C末端的eGFP序列和10×His标签。 使用相同的结构通过片段基因合成(Eurofins Genomics)生成突变的N-连接糖基化位点(NX(S/T))到Q(N89Q/N210Q/N378Q/N382Q/N445Q)。 设计用于大规模纯化的构建物分别包含GP64肽信号序列、FLAG(DYKDDDDK)和10×His标签,以及N末端的精确蛋白酶识别位点(LEVLFQGP),然后是人类mGlu 5 基因在A856处截断。 使用PCR将所有构建物亚克隆到pFastBac1中,引物对编码5′端的限制性位点BamH1和3′端的EcoR1,随后连接到载体中发现的相应限制性位点。
mGlu的纯化 5 Sf9细胞产生 所有设计的结构均使用Bac-to-Bac杆状病毒表达系统(Invitrogen)在EX-CELL 420培养基(Sigma-Aldrich)中生长的Sf9细胞中表达。 细胞以3-4×10的密度感染 6 每毫升含P2杆状病毒的细胞数。 培养物在27°C下生长,感染后48小时收集,然后在−80°C下保存,直至使用。 在含有25 mM HEPES(pH 7.4)、10 mM MgCl的裂解缓冲液中解冻冷冻细胞颗粒,破坏来自4 L培养物的昆虫细胞膜 2 、20 mM KCl和完整蛋白酶抑制剂鸡尾酒片(罗氏)。 在使用相同的裂解缓冲液以45000 rpm的转速进行两轮洗涤后,去除上清液,并使用含25 mM HEPES(pH 7.4)、10 mM MgCl的高盐缓冲液进行额外洗涤 2 20 mM KCl和1 M NaCl。 用添加了40%甘油的裂解缓冲液重新悬浮膜,然后将其储存在−80°C下。 将冲洗过的膜重新悬浮到含有10μM 2-甲基-6-(苯乙炔基)吡啶(MPEP,Abcam)、10 mM碘乙酰胺(Sigma)、完整蛋白酶抑制剂鸡尾酒片和额外蛋白酶抑制剂的缓冲液中; bestatin、leupetin、pefabloc和pepstatin(罗氏)。 然后将混合物在室温下培养1小时,然后溶解。 然后将膜溶解在含有25 mM HEPES缓冲液(pH 7.4)、0.4 M NaCl、10%甘油、0.5%(w/v)月桂基麦芽糖新戊二醇(MNG3,Anatrace)和0.05%(w/v)胆固醇半琥珀酸酯(CHS,Sigma)的缓冲液中,并在4°C下摇晃1.5小时。 然后通过45000 rpm离心1小时分离上清液,并补充10 mM咪唑(Sigma)。 对于mGlu 5 -∆856-eGFP构建,上清液加载到Ni上 2+ 柱(HisTrap HP,GE Healthcare),0.3 ml/min,4°C过夜。 粘合后,用20-30柱体积的洗涤缓冲液(25 mM HEPES(pH 7.4)、400 mM NaCl、10μM MPEP、10%(v/v)甘油、0.05(w/v)MNG3、0.005%(w/v)CHS和60 mM咪唑)洗涤树脂。 然而,对于mGlu 5 -∆856,上清液加载到钴上 2+ 树脂(泰龙超流,GE Healthcare),0.3 ml/min,4°C过夜。 然后用25 mM HEPES(pH 7.4)、400 mM NaCl、10μM MPEP、10%(v/v)甘油、0.05%(w/v)MNG3、0.005%(w/v)CHS和250 mM咪唑洗脱蛋白质。 洗脱的mGlu 5 -∆856蛋白与抗FLAG亲和树脂在4°C下孵育1小时,然后用10柱体积的洗涤缓冲液(25 mM HEPES(pH 7.4)、150 mM NaCl、10μM MPEP、0.01(w/v)MNG3、0.001%(w/v)CHS和2 mM钙)洗涤。 用含有0.01%MNG3、0.001%CHS、25 mM HEPES pH 7.4、0.15 M NaCl、10μM MPEP、0.2 mg/ml FLAG肽和2 mM EDTA的缓冲液洗脱蛋白质。 然后使用Vivaspin 20离心浓缩器100 kDa截止液(Sartorius)浓缩两种结构物的洗脱部分,以80000 rpm离心10分钟以消除聚集物,然后加载到尺寸排除色谱柱上(Superse 6增加,GE Healthcare)。 使用Vivaspin 6离心浓缩器100 kDa截止液(Sartorius)进一步浓缩洗脱部分,并使用双钦酸(BCA)分析测定蛋白质浓度。
质谱 通过Commassie蓝染色的SDS-PAGE凝胶评估蛋白质纯度,并通过质谱揭示条带的同一性。 SDS-PAGE凝胶显示出与SEC峰对应的两条带,将其切除并去除。 在25 mM NH中用10 mM TCEP降低蛋白质 4 HCO公司 三 溶液在56°C下培养30分钟,然后在室温下在20 mM碘乙酰胺中培养45分钟。 然后将凝胶片与20µl胰蛋白酶(Promega)溶液(19 ng/ul)孵育,在37°C下消化过夜。 然后用MALDI-TOF TOF质谱仪对所得碎片进行分析。
GTPγS结合 使用荧光Body-FL GTPγS类似物进行GTPγS-结合实验 26 N末端His-Tagged Gα 秒 表示为 大肠杆菌 并使用镍-硝基三乙酸亲和(Ni-NTA)色谱纯化 36 .Gα i2类 内部His-tag表达于 大肠杆菌 并如前所述进行纯化 37 .溶解他的 6 -标记的Gα q个 表示为 第9部分 细胞并使用Ni-NTA亲和层析纯化 38 最后,Gβ 1 是用他的 6 -标记的Gγ 2 在里面 9平方英尺 Ni-NTA色谱结合离子交换色谱从膜组分中纯化的细胞和Gβγ二聚体 38 使用配有Peltier控制温度装置的荧光分光光度计(Cary Eclipse,Varian)监测Body-FL GTPγS与G蛋白的关联,激发波长设置为500 nm,发射波长设置为511 nm。 反应条件为100 nM Gα 秒 β 1 γ 2 ,Gα q个 β 1 γ 2 或Gα i1号机组 β 1 γ 2 100 nM体-FL GTPγS和20 nM mGlu 5 洗涤剂中的受体或以2.8:1的比例重新配制成12%的DMPC:CHAPSO(双子叶)混合物。 在添加配体(最终浓度为10µM)后,在15°C下监测荧光10分钟。
统计分析 Dunnett检验作为单向方差分析的一部分,用于与定义的参考水平进行多次比较。 所有图形均使用GraphPad Prism 7.0版(GraphPad-software,San Diego,CA)进行分析。 统计显著性设置为一、二、三和四颗星,分别表示P<0.05、P<0.01、P<0.001和P<0.0001。
致谢 作者感谢劳伦特·普雷佐、朱莉·克尼泽夫、菲利普·伦达尔和西里尔·古德特的有益讨论,感谢克里斯·泰特对手稿的批判性阅读。 我们感谢Eric Trinquet(法国西斯比奥)为我们提供SNAP标签全长mGlu 5 表达质粒,以及IGF的Arpege和FFP平台。 Karine Rottier得到了FRM“ingenieur de Recherche”项目的支持,Chady Nasrallah得到了ATIP拨款(2014-2016)和蒙彼利埃大学博士后科学家项目(2016-2018)的支持。 Joan Font和Amadeu Llebaria感谢MINECO(PCIN-2013–017 C03-01和CTQ2014-57020-R)、加泰罗尼亚政府(2014SGR109和2014CTP0002)和ERANET神经元项目“LIGHTPAIN”的支持。 纪尧姆·勒本(Guillaume Lebon)对ATIP计划(2013-2016)、CNRS、INSERM和蒙彼利埃大学的支持表示感谢。
作者贡献 C.N.和G.L.设计了该项目。 C.N.、K.R.和R.M.进行了药理学表征、热稳定性测量、表达和纯化。 J.L.B.进行了G蛋白活化测量。 A.L.和J.F.合成了化合物VU0424465。 C.N.、K.R.、J.L.B.、G.L.分析了数据。 J.L.B.、V.C.和J.P.P.提供了一般性意见。 C.N.,G.L.用所有作者的贡献写了这份手稿。 G.L.监督了该项目。
脚注
电子补充材料
补充信息 本文随附于10.1038/s41598-018-22729-4。
出版商备注: Springer Nature在公布的地图和机构关联中的管辖权主张方面保持中立。
工具书类
1 Conn PJ、Christopoulos A、Lindsley CW。 GPCR的变构调节剂:一种治疗中枢神经系统疾病的新方法。 Nat Rev药物迪斯科。 2009; 8:41–54. doi:10.1038/nrd2760。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
2 Recasens M,Guiramand J,Aimar R,Abdulkarim A,Barbanel G.代谢性谷氨酸受体作为药物靶点。 当前药物目标。 2007; 8:651–681. doi:10.2174/138945007780618544。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
三。 Kniazeff J、Prezeau L、Rondard P、Pin JP、Goudet C.Dimers及其他:C类GPCR的功能谜题。 药物治疗学。 2011; 130:9–25. doi:10.1016/j.pharmthera.2011.01.006。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
4 Urwyler S.家族G-蛋白偶联受体的变构调节:从分子见解到治疗视角。 药理学修订版2011; 63:59–126. doi:10.1124/pr.109.002501。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
5 Kniazeff J等人。同二聚体mGlu受体的两个结合域的闭合状态是完全活性所必需的。 自然结构分子生物学。 2004; 11:706–713. doi:10.1038/nsmb794。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
6 Pin JP,Galvez T,Prezeau L.家族3/C G蛋白偶联受体的进化、结构和激活机制。 药物治疗学。 2003; 98:325–354. doi:10.1016/S0163-7258(03)00038-X。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
7 Sengmany K等人。代谢型谷氨酸受体5的偏向变构激动和调节:优化临床前神经科学药物发现的意义。 神经药理学。 2017; 115:60–72. doi:10.1016/j.neuropharm.2016.07.001。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
8 Rook JM等。偏倚mGlu5正变构调节剂在不增强mGlu6对NMDAR电流的调制的情况下提供体内疗效。 神经元。 2015; 86:1029–1040. doi:10.1016/j.neuron.2015.03.063。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
9 Joly C等。代谢型谷氨酸受体5型剪接变异体的分子、功能和药理特征:与mGluR1的比较。 神经科学杂志。 1995; 15:3970–3981. doi:10.1523/JNEUROSCI.15-05-03970.1995。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
10 Tsuchiya D,Kunishima N,Kamiya N,Jingami H,Morikawa K.与拮抗剂以及谷氨酸和Gd3+Proc Natl Acad Sci USA复合的代谢型谷氨酸受体配体结合核心的结构视图。2002; 99:2660–2665. doi:10.1073/pnas.052708599。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
11 Muto T,Tsuchiya D,Morikawa K,Jingami H。第II/III组代谢型谷氨酸受体胞外区域的结构。 美国国家科学院院刊2007; 104:3759–3764. doi:10.1073/pnas.0611577104。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
12 Kunishima N等。二聚代谢型谷氨酸受体识别谷氨酸的结构基础。 自然。 2000; 407:971–977. doi:10.1038/35039564。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
13 耿,Y。 等 人钙敏感受体配体激活的结构机制。 埃利夫 5 (2016). [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ]
14 Pin JP,Bettler B.mGlu和GABAB受体复合物的组织和功能。 自然。 2016; 540:60–68. doi:10.1038/nature20566。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
15 Wu HX,等。与变构调节剂结合的C类GPCR代谢性谷氨酸受体1的结构。 科学。 2014; 344:58–64. doi:10.1126/science.1249489。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
16 Dore AS等,C类GPCR代谢型谷氨酸受体5跨膜结构域的结构。 自然。 2014; 511:557–562. doi:10.1038/nature13396。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
17 Xue L,等。GPCR二聚体中主要配体诱导的七螺旋结构域界面重排。 自然化学生物。 2015; 11:134–140. doi:10.1038/nchembio.1711。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
18 Doumazane E等。阐明代谢型谷氨酸受体的激活机制和变构特性。 美国国家科学院院刊2013; 110:E1416–1425。 doi:10.1073/pnas.1215615110。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
19 Seebahn A等。第III组代谢型谷氨酸受体细胞内C末端结构域的结构特征。 FEBS信函。 2011; 585:511–516. doi:10.1016/j.febslet.2010.12.042。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
20 Venkatakrishnan AJ等。G蛋白偶联受体的分子特征。 自然。 2013; 494:185–194. doi:10.1038/nature11896。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
21 泰特美术馆。 纯化和结晶过程中膜蛋白不稳定性的实际考虑。 方法分子生物学。 2010年; 601:187–203。 doi:10.1007/978-1-60761-344-2_12。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
22 Magnani F等人。一种诱变和筛选策略,用于生成用于结构研究的最佳热稳定膜蛋白。 国家协议。 2016; 11:1554–1571. doi:10.1038/nprot.2016.088。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
23 Shibata Y等,《神经紧张素受体NTS1的热稳定化》。 分子生物学杂志。 2009; 390:262–277. doi:10.1016/j.jmb.2009.04.068。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
24 Chae PS等。用于膜蛋白溶解、稳定和结晶的麦芽糖-新戊二醇(MNG)双亲化合物。 自然方法。 2010; 7:1003–1008. doi:10.1038/nmeth.1526。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
25 杆状病毒感染细胞系统中Massotte D.G蛋白偶联受体过度表达:结构和功能研究的工具。 Biochim生物物理学报。 2003; 1610:77–89. doi:10.1016/S0005-2736(02)00720-4。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
26 McEwen DP,Gee KR,Kang HC,Neubig RR。荧光BODIPY-GTP类似物:实时测量核苷酸与G蛋白的结合。 分析生物化学。 2001年; 291:109–117. doi:10.1006/abio.2001.5011。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
27 Rook JM等。代谢型谷氨酸受体亚型5的正变构调节剂的独特信号特征决定了体内活性的差异。 生物精神病学。 2013; 73:501–509。 doi:10.1016/j.biopych.2012.09.012。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
28 Deriu D等。GABAB1b受体最小功能配体结合域的测定。 《生物化学杂志》2005; 386:423–431. doi:10.1042/BJ20040804。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
29 Mody N、Hermans E、Nahorski SR、Challiss RA。 衣霉素抑制人类1α-代谢型谷氨酸受体的N-连接糖基化:对细胞表面受体表达和功能的影响。 神经药理学。 1999; 38:1485–1492. doi:10.1016/S0028-3908(99)00099-4。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
30 Drew D等。基于GFP的酿酒酵母真核细胞膜蛋白过度表达和纯化优化方案。 国家协议。 2008; 3:784–798. doi:10.1038/nprot.2008.44。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
31 Romano C,Yang WL,OMalley KL。代谢型谷氨酸受体5是一种二硫键二聚体。 生物化学杂志。 1996; 271:28612–28616. doi:10.1074/jbc.271.45.28612。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
32 El Moustaine D等。代谢型谷氨酸受体二聚化在激动剂激活和G蛋白偶联中的不同作用。 美国国家科学院院刊2012; 109:16342–16347。 doi:10.1073/pnas.1205838109。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
33 Flock T等。GPCR-G-蛋白结合的选择性决定因素。 自然。 2017; 545:317–322. doi:10.1038/nature22070。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
34 Goudet C等。代谢型谷氨酸受体5的七叶结构域表现为视紫红质样受体。 美国国家科学院院刊2004; 101:378–383. doi:10.1073/pnas.0304699101。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
35 Sengmany K、Gregory KJ。 代谢型谷氨酸受体亚型5:分子药理学、变构调节和刺激偏向。 英国药理学杂志。 2016; 173:3001–3017. doi:10.1111/bph.13281。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
36 Greentree WK,Linder ME。大肠杆菌重组G蛋白α亚基的纯化。 方法分子生物学。 2004; 237:3–20. doi:10.1385/1-59259-430-1:3。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
37 Medkova M、Preininger AM、Yu NJ、Hubbell WL、Hamm HE。 G蛋白α(i1)的氨基末端螺旋在与Gbetagama亚基分离和激活后的构象变化。 生物化学。 2002; 41:9962–9972. doi:10.1021/bi0255726。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
38 Kozasa T.使用六组氨酸标记的α和β-γ亚基从Sf9昆虫细胞中纯化G蛋白亚基。 方法分子生物学。 2004; 237:21–38. doi:10.1385/1-59259-430-1:21。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
关联数据 本节收集本文中包含的任何数据引用、数据可用性声明或补充材料。