摘要 前列腺癌是目前美国男性最常见的非皮肤恶性肿瘤。 当肿瘤转移到骨组织时,这种疾病不再是可治愈的,通常采用雄激素消融术进行姑息性治疗。 然而,在转化为雄激素依赖性疾病后,目前还没有有效的治疗方法。 “T体”方法使用来自患者的基因重组淋巴细胞并表达嵌合受体基因,将T淋巴细胞和NK细胞的效应器功能与抗体识别预先定义的表面抗原的能力结合起来,具有高度特异性和非MHC限制性。 我们在这里展示了携带erbB2特异性嵌合受体的人淋巴细胞在SCID小鼠模型中对人前列腺癌BM病变的治疗效果,该模型对受体进行了调节,以允许过继转移细胞的归巢和持续功能。 使用低剂量辐射或环磷酰胺结合IL-2给药在骨髓内诱导基质细胞衍生因子-1的产生,增强了系统传递T小体的归巢,导致肿瘤生长和前列腺特异性抗原分泌减少,延长生存期,甚至治愈治疗小鼠。 这些临床前研究强烈支持T体方法对播散性前列腺癌具有治疗潜力的观点。
介绍 前列腺癌是美国男性最常见的恶性肿瘤,也是导致癌症死亡的第二大原因( 1 ). 骨是PC最常见的转移部位( 2 )骨转移是大多数转移性PC发病率的原因。 70%以上死于PC的患者检测到骨转移( 三 ). 转移性PC患者的中位生存期只有30个月( 4 ). 激素消融治疗是目前对这些患者的第一个标准治疗,激素依赖性疾病的难治状态通常在12-18个月内出现,之后大约一半的患者在6个月内死于疾病进展。 因此,非常需要扩展现有的治疗方法,以对抗播散性PC。“T体”方法,即用具有抗体特异性的嵌合受体重定向效应淋巴细胞,被认为有望用于癌症的过继免疫治疗( 5 – 7 ). 最近,我们证明了表达erbB2特异性嵌合受体(CRs)(称为T小体)的人淋巴细胞可以直接应用于局部限制的、成熟的PC异种移植物,从而导致肿瘤生长迟缓、前列腺特异性抗原(PSA)分泌减少和延长治疗动物的生存期( 8 ).
然而,优化T体方法用于晚期PC的系统治疗,必须克服几个缺点才能应用于临床。 免疫细胞过继转移的主要限制之一是缺乏将基因工程T细胞特异性运输到播散性肿瘤部位的能力。 将T细胞贩运到这些部位是一个复杂的多阶段过程,包括沿着内皮细胞在特定部位滚动和阻滞,然后靶组织外渗和渗透。 这些过程中的一个重要步骤是由组织分泌的趋化因子及其在T细胞膜上的相应受体之间的相互作用介导的( 9 ). 虽然肿瘤细胞可以分泌趋化因子,但在T细胞不表达适当的趋化因子表面受体的情况下,通常不会发生T细胞的定点贩运( 10 ).
最近,Brentjens等人( 11 )使用基因靶向人类T淋巴细胞在小鼠模型中根除全身B细胞肿瘤。 在该系统中,用抗CD19特异性CR转导的人PBL,然后在CD19存在下被激活和增殖 + CD80型 + “人工”抗原提呈细胞和IL-15在体内持续存在,并维持其功能足够长的时间,以消除其远处的肿瘤靶点。
在这里,我们吸取了人类造血干细胞移植的经验教训,以吸引T体到SCID小鼠的PC骨损伤中。 我们的方法是基于先前的证明,即人类造血细胞在先前接受全身照射(TBI)的SCID小鼠的骨髓中快速聚集( 12 – 14 )或环磷酰胺,增加骨髓基质细胞衍生因子-1(SDF-1)表达的治疗( 15 ). SDF-1是趋化因子CXC亚家族的成员,对T淋巴细胞和前B淋巴细胞具有强大的化学吸引力( 16 )表达SDF-1受体CXCR4( 17 ). SDF-1影响T细胞滚动和T细胞与活化内皮细胞的粘附强度( 18 )以及CD4的共刺激 + T细胞激活( 19 ).
因此,我们假设骨髓基质微环境中SDF-1的浓度增加,即PC骨转移所在的微环境,将增加全身给药T小体的归巢和滞留。 因此,我们建立了一个体内实验系统,以扩大T小体对转移癌的治疗范围。 我们在此证明,诱导骨髓中SDF-1表达的治疗可增强erbB2特异性人类T小体的归巢,从而抑制晚期PC的进展,甚至治愈。
结果 改善体外操纵淋巴细胞的迁移。 我们使用一种实验性临床前系统,在SCID小鼠中研究了人类T体治疗PC骨转移的能力,SCID小鼠在小鼠股骨中移植了人类PC异种移植物(图 1 ). 对这些小鼠进行治疗性(erbB2特异性)或对照性(2,4,6-三硝基苯酚特异性[TNP-特异性])人体T体的全身给药。 然而,我们第一次尝试消除这种骨转移失败,我们发现erbB2特异性T细胞几乎没有产生任何作用(数据未显示)。 因为之前发现相同的erbB2特异性T小体在肿瘤内给药后清除相同皮下PC异种移植物非常有效( 8 ),我们怀疑静脉注射后T体未能达到(足够数量)并有效排斥骨肿瘤。 用于激活人T细胞及其在IL-2中培养的体外条件,这是逆转录病毒转导和增殖所必需的( 20 ),已被证明下调参与淋巴细胞迁移的几个分子的表面表达,包括CXCR4( 17 , 21 ). 因此,我们研究了增加SDF-1(CXCR4配体)的水平是否会增强T小体向骨髓的迁移,从而消除表达相应靶抗原的骨肿瘤。 虽然T小体是人类起源的,SDF-1是由SCID小鼠产生的,但这两个物种的SDF-1分子之间几乎完全相同并具有交叉反应性( 22 , 23 ). 因为作为再生过程的一部分,SDF-1是为了应对组织损伤而产生的( 15 ),我们测试了提高其在骨骼中浓度的治疗方法的效果,如TBI和环磷酰胺( 15 ). 图 2 A表明,2 Gy剂量的亚致死剂量照射导致SCID BM中SDF-1表达增加。环磷酰胺(200 mg/kg,i.p.)也诱导BM中的SDF-1 mRNA表达水平增加(图 2 A) ●●●●。 因此,在全身给药携带CR的人淋巴细胞之前,使用2 Gy TBI或200 mg/kg环磷酰胺对小鼠进行预处理。 事实上,这些经过改造的淋巴细胞在该条件处理方案之后在更大程度上重新填充了小鼠骨髓。 人体T体向小鼠BM迁移的水平在TBI的12–24小时内达到峰值(图 2 B) ●●●●。 单次低剂量环磷酰胺也获得了类似的结果(数据未显示)。
图1。
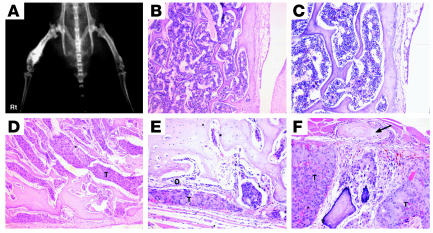
WISH-PC14诱导成骨细胞骨损伤。 将WISH-PC14单细胞悬浮液经转子注入SCID小鼠的右股骨。 ( A类 )肿瘤的X线表现。 ( B类 )对侧股骨的正常BM组织学。 放大倍数,×100。 ( C类 )与相同 B类 放大倍数,×200。 注意正常的骨小梁和骨膜。 ( D类 )WISH-PC14(T)占据右股骨的整个BM腔。 放大倍数,×100。 ( E类 )肿瘤细胞周围有成骨细胞活性(O)。 放大倍数,×200。 注意骨小梁增厚。 ( F类 )制备和放大与 E类 注意骨旁骨形成的骨膜反应(箭头)。
图2。
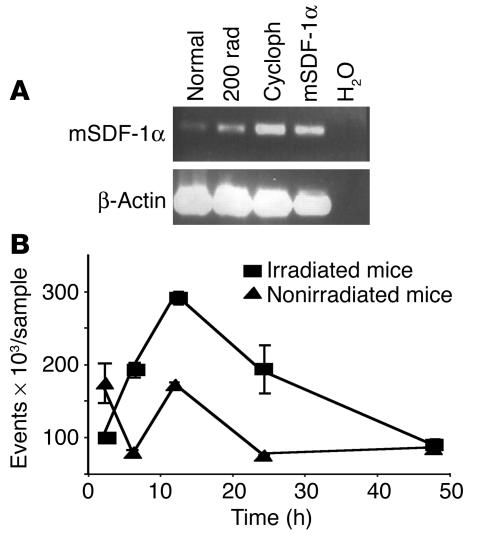
辐射和环磷酰胺对骨髓SDF-1 mRNA表达的影响以及随后人类T小体向小鼠骨髓的迁移( A类 和 B类 )SCID小鼠用2Gy照射或腹腔注射200mg/kg环磷酰胺,或不进行治疗。 ( A类 )治疗后24小时,制备mRNA并进行RT-PCR。 环磷酰胺; mSFF-1α,小鼠SDF-1α; 正常、未经治疗的小鼠。 H(H) 2 O用作阴性对照。 ( B类 )静脉注射给治疗小鼠后,人体T小体向BM迁移的动力学。 通过GFP上的FACS分析门控确定达到BM的T小体数量(事件)( n个 =每组3只小鼠; 实验至少重复了两次)。 在6小时和12小时时,受照受试者骨髓中累积的T小体数量明显大于未受照受者( P(P) =0.054和 P(P) 分别为0.011)。
为了测试工程化T细胞向骨髓的迁移增强是否是由于用低剂量TBI或环磷酰胺预处理后产生SDF-1所致,我们用抗CXCR4或对照抗体处理T体,包括人转铁蛋白受体(TfR)特异性单克隆抗体 (在淋巴细胞表面表达,与抗CXCR4单克隆抗体具有相同的同型)。 结果如图所示 三 表明抗CXCR4部分但显著( P(P) =0.003,与抗TfR相比)抑制T小体的特异性体内迁移。 在跨阱迁移试验中也获得了类似的结果,其中携带CR的淋巴细胞的迁移仅被抗CXCR4特异性抑制(图 4 ).
图3。
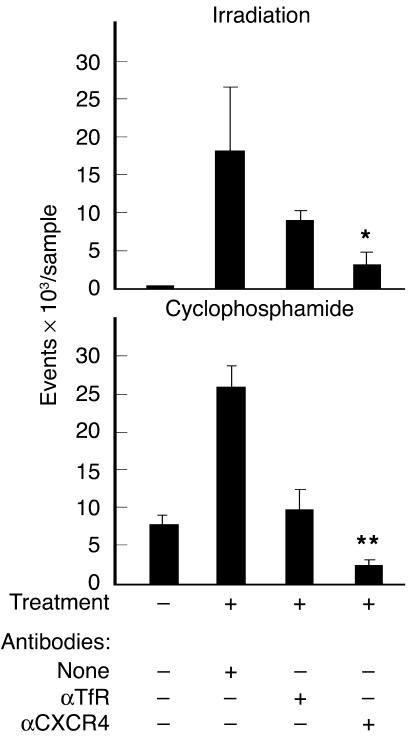
T小体向预处理小鼠骨髓的迁移部分由CXCR4介导。 SCID小鼠( n个 =每组3只小鼠)在静脉注射erbB2特异性CR淋巴细胞前24小时,用2 Gy TBI照射或注射200 mg/kg环磷酰胺。 将T小体与抗CXCR4单克隆抗体(αCXCR4)、不相关对照单克隆抗体抗人TfR(αTfR)或无抗体(无)在冰上预孵育30分钟,然后将其全身注射到小鼠体内。 24小时后,提取骨髓,通过FACS分析测定人淋巴细胞数量(辐射实验中检测GFP阳性T小体,环磷酰胺实验中检测CFSE标记细胞)。 两种受照小鼠的抗CXCR4治疗与对照治疗(抗TfR)显著不同(* P(P) =0.003)和环磷酰胺处理的小鼠(** P(P) =0.009),与无抗体治疗显著不同( P(P) =0.01和 P(P) 分别=0.0002)。
图4。
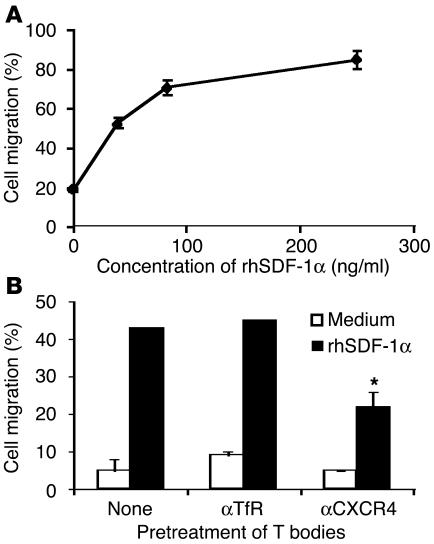
T小体向重组人SDF-1α(rhSDF-1)的跨阱迁移具有剂量依赖性,并受到抗CXCR4的抑制。 ( A类 和 B类 )T体的跨井运移。 ( A类 )T小体向rhSDF-1α浓度增加的方向迁移。 ( B类 )T小体在含有抗CXCR4或抗TfR的冰上预孵育30分钟,然后向含有rhSDF-1α(150 ng/ml)的培养基或单独培养基迁移1小时。 与抗-TfR或不治疗相比,抗-CXCR4显著抑制迁移(* P(P) =0.016和* P(P) 分别=0.019)。
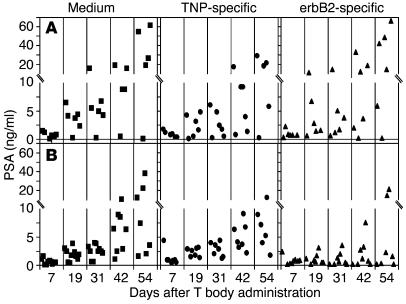
全身给药T体对PC BM病变的治疗效果。 在我们建立了改善SCID小鼠体内体外操纵人类淋巴细胞向骨内转移的方案后,我们测试了erbB2特异性人类淋巴细胞的治疗效果。 向携带已建立的股内PC(WISH-PC14)异种移植物的SCID小鼠全身给予T体的结果如图所示 5 – 5 在这组实验中,在静脉注射erbB2或TNP特异性人类T细胞体或培养基之前24小时,对小鼠进行照射(2 Gy TBI)或不照射。 如所有3个终点所示,血清PSA(图 5 ),骨射线照相术(图 6 )和动物生存(图 7 ),只有在用低剂量TBI预处理的小鼠中用抗erbB2 CR淋巴细胞治疗的组中才能获得特异性抗肿瘤效果。未受照射的小鼠组之间没有显著的统计差异(图 5 A) ; 然而,对于受照射的小鼠,用erbB2特异性T小体治疗的组与用TNP-特异性T小体治疗组或未治疗组之间的差异(仅给出培养基;图 5 B) 意义重大( P(P) =0.0145或 P(P) 分别为0.0455)。 无关T小体(TNP-特异性)或未经照射的小鼠均未产生治疗作用。 亚致死性TBI仅略微降低了骨髓中WISH-PC14异种移植物的生长速率(通过比较未受照小鼠和受照小鼠中对照[培养基处理]异种移生物的生长可以明显看出)。
图5。
erbB2特异性T小体全身治疗对WISH-PC14 BM损伤的影响取决于小鼠的预照射。 ( A类 和 B类 )携带已建立的骨内WISH-PC14异种移植物的SCID小鼠也未进行预处理( A类 )或用2 Gy TBI预处理( B类 )静脉注射erbB2或TNP-特异性CR淋巴细胞或培养基前24小时( n个 =每组10只小鼠)。 测定小鼠血清中的PSA水平。 方形、圆形和三角形分别代表注射到SCID受体小鼠体内的中型、TNP和erbB2特异性CR淋巴细胞。
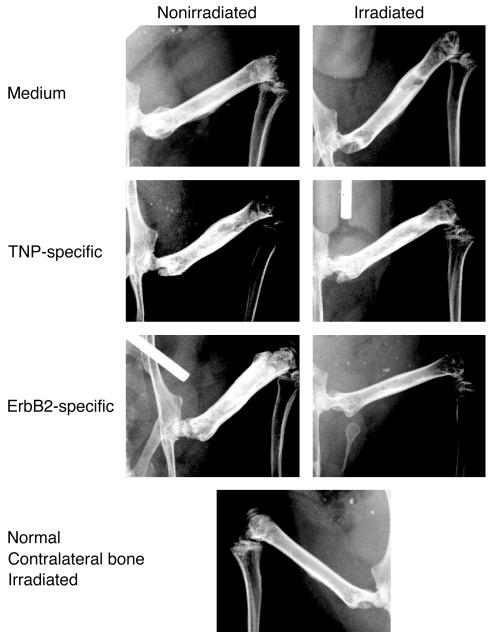
图6。
治疗后BM病变的放射照相。 治疗5周后对小鼠进行放射分析。 虽然在受照射和未受照射的小鼠对照组以及用erbB2特异性T小体治疗的未受照射动物中观察到肿瘤,但在用erbB2 CR淋巴细胞治疗的受照射动物上,在预照射和用erbB特异性T小体治疗5周后,没有明显的肿瘤放射学征象。
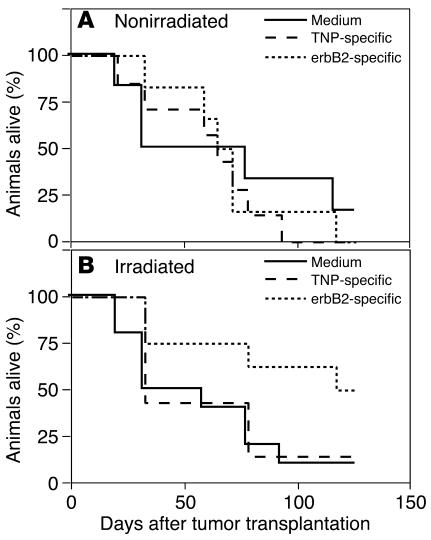
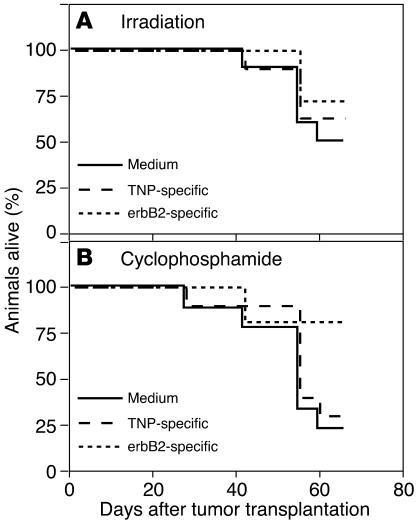
图7。
全身给予erbB2特异性人类淋巴细胞可延长PC-BM损伤小鼠的生存期。 ( A类 和 B类 )患有WISH-PC14骨损伤的SCID小鼠的生存数据( n个 =每组10只小鼠)用TNP或erbB2特异性CR淋巴细胞或培养基进行系统治疗( A类 )或使用( B类 )2 Gy TBI预处理。
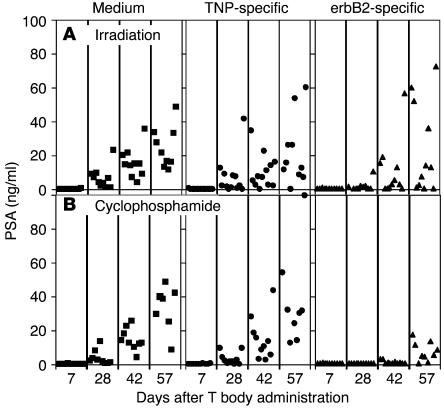
为了测试当荷瘤小鼠用环磷酰胺而不是照射预处理时,这种方法是否也有效,以及在另一种肿瘤异种移植物上测试这些效果,我们使用了雄激素依赖性和erbB2表达的PC异种移生物LuCaP 35。 在这个异种移植模型中( P(P) =0.037)仅在实验的第一个月内,用erbB2特异性T小体治疗的预照射组的肿瘤生长减少(如PSA分泌所示)(图 8 ). 然而,使用环磷酰胺进行预处理(图 9 )与非相关(TNP)特异性的对照细胞相比,erbB2特异性T小体具有更显著和持久的治疗作用( P(P) = 0.011). 此外,在用erB2特异性T体治疗的组中,35%(11只中的4只)的小鼠在治疗后2个月内保持低血清PSA水平(<5ng/ml)。
图8。
环磷酰胺预处理或照射增强了erbB2特异性CR淋巴细胞系统治疗LuCaP-35骨损伤的效果。 ( A类 和 B类 )用TBI预处理携带已建立的LuCaP-35骨内异种移植物的SCID小鼠( A类 )或环磷酰胺( B类 )静脉注射erbB2-特异性(三角形)或TNP-特异性(圆形)CR淋巴细胞或培养基(方形)前24小时( n个 =每组10只小鼠)。
图9。
erbB2特异性CR淋巴细胞全身治疗对LuCaP-35骨肿瘤小鼠生存的影响。 ( A类 和 B类 )携带LuCaP-35骨肿瘤SCID小鼠的生存数据( n个 =每组10只小鼠)用TNP或erbB2特异性CR淋巴细胞或培养基进行系统治疗,并用2 Gy TBI进行预处理( A类 )或环磷酰胺( B类 ).
讨论 表达预选肿瘤抗原特异性嵌合受体的转基因T细胞的开发克服了过继性细胞免疫治疗的几个关键障碍。 现在可以产生临床相关数量的肿瘤特异性自体淋巴细胞,携带各种亚型的CR( 8 , 11 , 20 ). 这些细胞对相同的非MHC和限制性抗原具有特异性,能够在预定靶点的刺激下协同工作。 已经构建了一个能够选择性识别不同肿瘤相关抗原的大量CR库( 10 , 24 – 39 )在实践中,人们可以用一组包含多种不同特异性和CR设计的T体来攻击给定的肿瘤。 这一武器库应该为癌症免疫治疗的主要缺点之一提供了一个可行的解决方案:选择性免疫压力导致逃逸变异体的再生( 7 , 40 , 41 ). 同样,三部分CR,如这些研究中使用的,具有额外的共刺激功能,如CD28和4-1BB( 20 , 42 , 43 ),它赋予程序化T细胞所需的特征,以抵消肿瘤宿主中常见的无能和凋亡信号( 7 ).
临床前模型和初步临床试验中观察到的T小体临床应用的障碍之一是体外操纵T小体对其肿瘤靶点的归巢效率低下。 显然,PBL衍生的基因修饰T细胞在体外激活、转导和长时间繁殖后,会改变其归巢特性,无法有效到达传播疾病的部位,从而无法持续维持其效应器功能。 这种模式是普遍的,与CR表达无关,因为非基因修饰的肿瘤浸润淋巴细胞(TIL)在临床试验中也屡次失败,无法证明患者在没有细胞清除治疗的情况下持续性和功能性植入( 44 – 46 ). 这一问题的一个表现是全身给药的体外操纵淋巴细胞被困在实验动物的肺部( 47 ). 为了克服这一主要局限性,并且为了优化T体方法对播散性癌症的系统治疗,我们在此表明,用低剂量TBI或环磷酰胺对受体进行预处理可以提高过继转移T体产生的治疗效果。 我们的数据表明,SDF-1–CXCR4相互作用至少参与了部分效应。 已有大量文献证明,作为组织再生过程的一部分,组织诱导剂(如环磷酰胺或TBI)诱导SDF-1的产生和分泌( 15 ). 众所周知,SDF-1是CXCR4表达的造血干细胞趋化性和趋化性的强大介质( 14 , 23 )以及成熟淋巴细胞,如NK和T细胞( 17 , 21 , 48 ). 作为适用于T体免疫治疗的晚期和不可治愈肿瘤靶点的模型,我们选择研究PC骨转移。 骨髓是PC转移的主要部位,导致了该病的大量发病率和死亡率。 在细胞表面表达的几种PC-相关抗原中( 49 – 52 ),我们选择靶向erbB2,因为它在高达80%的转移性PC上过度表达,并且随着雄激素依赖性的降低其表达增加( 53 – 55 ). 此外,erbB2的表达与前列腺癌的进展有关( 54 , 55 ). 我们在临床前研究中使用的两种异种移植物WISH-PC14( 8 )和LuCaP 35( 56 ),代表前列腺癌的侵袭性表型; WISH-PC14具有抗辐射性(数据未显示),而LuCaP 35是从转移淋巴结建立的,其生长独立于雄激素( 56 )而且抗辐射。 这些异种移植物在SCID小鼠中都不会自发转移到骨骼,但它们在注射到小鼠BM后会形成典型的PC骨损伤(图中WISH-PC14所示 1 ). 受体预处理加过继转移肿瘤特异性T细胞的联合方法被证明对两种PC异种移植物都有效(图 5 – 5 ).
在这两种预处理方法中,环磷酰胺更有效地创造了适当的条件,使携带CR的淋巴细胞在SCID小鼠中发挥其治疗作用。 低剂量环磷酰胺治疗后,大量细胞迁移至骨髓(图 2 和 三 ). 一种解释是,这两个过程是相互关联的; 即,在实验条件下,环磷酰胺在骨髓中诱导了更多的SDF-1生成,从而吸引了更多的治疗性T小体。 在使用的浓度下,小鼠淋巴细胞亚群对环磷酰胺的反应不同。 当效应器和辅助性T细胞耐药时,抑制性(或调节性)T细胞敏感( 57 ). 然而,在免疫缺陷SCID小鼠中,这种影响以及对淋巴细胞稳态的影响预计可以忽略不计。
在胰岛细胞瘤转基因小鼠模型中也进行了类似的观察,在该模型中,较高剂量的辐射通过增加粘附分子、细胞因子和趋化因子的表达来调节肿瘤微环境( 58 ). 作者认为,辐射引起的内皮细胞变化逆转了其非粘附表型,从而直接促进了白细胞与内皮细胞的相互作用。 在这种情况下,联合照射/过继转移诱导IFN-γ、TNF-α、血管抑制性趋化因子Mig和IP10的表达增强。 我们使用了免疫缺陷宿主这一事实并没有否定这种促炎机制也参与我们的模型的可能性。 的确,Ganss等人( 58 )结果表明,仅照射即可诱导促炎性事件,但未达到BM重建后激活内源性免疫所需的临界阈值,并且只有在随后输注激活的效应细胞后才会发生肿瘤排斥反应。 我们认为,在正常、免疫功能正常的受试者中,淋巴清除预处理(如本文所用的预处理)的总体效果是复杂的,包括改变体内平衡以允许移植外源性淋巴细胞、消除抑制细胞和诱导炎症环境, 其中包括吸引T淋巴细胞的趋化因子。
根据抗CXCR4部分阻断T小体向BM迁移的事实(图 三 )(以及跨阱实验中T体在SDF-1梯度上的迁移;见图 4 )并且辐射和环磷酰胺都增加了SDF-1的表达,我们认为至少部分治疗效果涉及CXCR4–SDF-1相互作用。 SDF-1不仅在吸引造血祖细胞进入骨髓中发挥关键作用( 12 – 14 , 18 , 23 )而且NK和NKT细胞也迁移到BM室( 17 ). 此外,一些研究报告了SDF-1激活T细胞:它是CD4的共刺激因子 + T细胞激活( 19 ),并且其在肿瘤部位的分泌(本例中为BM)促进了长寿命、肿瘤特异性细胞毒性T淋巴细胞反应的发展( 59 )导致肿瘤排异。 最近,Dudley等人证明,在过继转移肿瘤反应性T细胞之前,用环磷酰胺和氟达拉滨对转移性黑色素瘤患者进行非清髓性调节,对于功能性淋巴细胞克隆的持续重新繁殖以及将其运至转移部位至关重要。 该方案的使用使大量患者的肿瘤完全消退( 60 ). 尽管该研究中未确定其机制,但我们认为这些患者中SDF-1表达的增加与SCID小鼠中的表达方式类似。
理论上,癌症患者有意诱导SDF-1的一个担忧是,过度表达CXCR4的癌细胞也有可能导致不必要的迁移至骨骼( 61 ). 虽然大多数来源于普通实体肿瘤的细胞系不表达CXCR4( 62 ),最近报道CXCR4–SDF-1轴参与乳腺癌转移( 63 ). SDF-1在促进转移中的作用机制是复杂的。 在乳腺癌模型中( 63 ),抗CXCR4通过抑制CXCR4介导的增强癌细胞对组织的侵袭来减少转移。 类似地,横纹肌肉瘤( 62 )研究表明,SDF-1的作用主要涉及细胞与微环境的相互作用及其迁移,而非细胞增殖和存活。 然而,在人类结肠癌异种移植模型中( 64 )研究表明,CXCR4的激活在侵袭中并不起重要作用,而是导致微转移的产生。
总之,我们的研究结果表明,肿瘤特异性T细胞被SDF-1吸引,迁移到BM,在那里它们根除肿瘤细胞。 在患者中,SDF-1可能只对部分效应负责; 然而,我们的结果和最近发表的使用TIL进行黑色素瘤免疫治疗的临床研究( 60 )在过继转移肿瘤特异性T细胞之前,用无毒、低剂量辐射或环磷酰胺和氟达拉滨对癌症患者进行预处理是合理的。
方法 老鼠。 所有动物实验均由魏茨曼研究所动物护理和使用委员会批准。 将7-10周大的雄性小鼠(CB.17-SCID BEIGE;Charles River)饲养在魏茨曼科学研究所的无特定病原体(SPF)动物设施中。
肿瘤模型。 作为PC-BM病变的模型,我们使用WISH-PC14异种移植物( 8 )我们之前从一个晚期复发的原发性肿瘤经过明确的放射治疗和LuCaP 35异种移植(美国华盛顿州西雅图华盛顿大学医学院R.L.Vessella赠送的礼物)中建立的( 56 , 65 ). 这两种细胞系均过度表达erbB2,将PSA分泌到宿主血液中,具有抗辐射性,并诱导溶骨和成骨反应(参考文献。 65 和图 1 ). 用于肿瘤诱导,1×10 6 肿瘤细胞通过经粗隆途径直接接种到股骨。 在用氯胺酮和甲苯噻嗪(分别为127.5和4.5 mg/kg)全身麻醉镇静的小鼠中,进行了该手术和需要剖腹手术的腹腔微泵植入。 就WISH-PC14而言,SCID小鼠在肿瘤给药前接受皮下移植90天缓释睾酮丸(12.5mg/丸;美国创新研究)。
抗体。 抗ErbB2的N29单克隆抗体被用作构建CR的单链可变区(scFv)的来源( 66 ). 本实验室制备了兔抗N29独特型和鼠抗人TfR单克隆抗体(克隆V1-10)。 SP6标准立方英尺( 20 )(具有抗TNP特异性)作为对照。 如图所示,使用针对人类CXCR4的12G5单克隆抗体(R&D Systems Inc.) 三 和 4 .
CR基因及其在人淋巴细胞中的表达。 这个 CR公司 本研究中使用的基因为三重结构,其中单链抗体通过CD28胞外结构域(配体结合区从中被截断)与FcRIγ链的胞内部分相连( 20 ). 本研究中使用了来自2种单链抗体的CR:一种来自N29单克隆抗体的erbB2特异性受体,另一种来自Sp6单抗的TNP特异性受体。 将CR cDNA构建物克隆到pBullet载体中,随后进行内部核糖体进入位点序列和 GFP公司 基因( 20 ). 如前所述,使用含有载体的上清液,在逆转录酶上存在IL-2的情况下(FN-Takara Shuzo Ltd.),对来自健康供体的PBL进行转导,该PBL由抗CD3单克隆抗体和抗CD28单克隆抗体预激活( 20 ).
SCID小鼠PC异种移植的治疗。 荷瘤小鼠具有相似的肿瘤负荷(根据血清PSA水平确定),被随机分配到不同的实验组(通常在肿瘤注射后7-10天)。 在使用持续全身注射IL-2的实验中,将Alzelt微型渗透泵(Durcet Corp.)经腹腔移植。每个泵都装有重组人IL-2(R&D Systems Inc.),并设定为连续释放105单位/小时,持续1周。 当时,对小鼠进行照射(钴源2 Gy TBI)或接受环磷酰胺(200 mg/kg i.p.),或不使用上述任何一种方法进行预处理。 24小时后,5×10 7 将携带CR的淋巴细胞(T小体)注入尾静脉。 作为对照,同样注射了单独培养基(HBSS),以便在相同的实验条件下监测疾病的自然史。 随访包括定期血清PSA测定、骨损伤的连续X射线记录和动物生存监测。 对肿瘤负担高的小鼠实施安乐死。
半定量RT-PCR。 根据制造商的方案,使用TRI试剂盒(分子研究中心公司)从小鼠骨髓中分离出总RNA。 使用逆转录系统试剂盒(Promega Corp.)在42°C下对每个RNA样品(1μg)进行cDNA合成1小时。 在50μl反应混合物中进行PCR,该混合物含有5μl cDNA、1μl dNTP混合物(10mM;Promega Corp.)、小鼠SDF-1α引物(5′-GGACGCAAGGTCGTCGCCGTG-3′和3′-TTCATCTCCCACGGATGTCAG-5′;335bp)、5μl 10×NH 4 缓冲液,1.5μl 50-mM MgCl 2 溶液和5单位/反应样品的BIOTAQ DNA聚合酶(英国Bioline有限公司)。 使用小鼠β-肌动蛋白引物(5′-TCCTGTGGCATCCATGAAACTACATTCAATTCC-3′和3′-GTGAAAACGCAGCTCAGTAACAGTCCGCCTAG-5′;347bp)通过PCR确认所有cDNA样品的质量。 mSDF-1α表达的半定量分析是在65°C退火45秒的条件下,通过25个PCR周期完成的。
FACS分析。 通过对携带GFP-阳性CR的人淋巴细胞发出的绿色荧光进行门控,对BM衍生细胞进行FACS分析,以评估对BM的特异归巢。 为了避免因TBI或环磷酰胺的影响而产生的偏差,这种影响会减少小鼠细胞的数量,从而增加转导淋巴细胞的百分比,我们将所有BM细胞制剂调整到相同的体积,并在固定的时间段内计算人类细胞的数量(通过GFP表达门控)。
归位分析。 用于归航分析,5×10 7 TBI或环磷酰胺治疗24小时后,将人T小体静脉注射到小鼠体内,无论是否持续供应IL-2。 如图所示(见图 三 ),用抗人CXCR4单克隆抗体或抗人TfR对照单克隆抗体(3μg/10)在4°C下培养细胞30分钟 6 细胞),然后在不去除抗体的情况下静脉注射。 在不同的时间点处死小鼠,通过FACS回收BM细胞并分析是否存在上述人类细胞。 从未经处理的小鼠骨髓中获得的细胞作为对照。
T体的CFSE标记。 T小体用细胞内荧光染料CFSE(C-1157;分子探针)标记,方法是在室温下无血清培养8分钟,密度为10 7 5μM CFSE中的细胞/ml。 通过添加等量的冷FCS,CFSE加载停止。 细胞在完整的RPMI培养基中清洗两次( 67 ).
体外迁移试验。 如前所述,使用Costar Transwells(直径6.5 mm,孔径5 mm;康宁Costar)对CR转导的淋巴细胞进行趋化实验( 15 ). 含2×10的趋化缓冲液(RPMI 1640培养基和1%FCS) 5 将体积为0.1 ml的细胞以指定的浓度添加到上腔和0.6 ml趋化缓冲液中,包括或不包括SDF-1(R&D Systems Inc.)(见图 4 )被添加到底部腔室。 在显微镜下对1小时内迁移至跨孔底部室的细胞进行计数。 按照归巢试验所述,用抗体进行预孵育。
血清PSA测定。 使用两种化学发光免疫测定法(Immulite;Diagnostic Products Corp.)测定小鼠血清中的PSA水平:灵敏度为0.003 ng/ml的第三代PSA试剂盒(LKUP1)或灵敏度为0.03 ng/ml的LKPS1 PSA试剂箱。
统计分析。 使用JMP统计软件(SAS Institute Inc.)进行统计分析。 通过Dunnett试验分析血清PSA水平数据,确定不同治疗效果的显著性。 利用Fit模型进一步验证了实验期间不同治疗方法的疗效。 如有必要,使用单向方差分析测试对两种不同的个体治疗进行比较( 8 ). 生存实验采用Cox-Mantel-Rank检验进行分析。
致谢 感谢塔米·达农(Tami Danon)、萨拉·巴拉克(Sara Barak)和谢巴医学中心内分泌实验室团队的鼎力协助。 我们感谢前列腺癌基金会、美国陆军和欧盟的支持。 本研究得到了CaP-CURE基金会的资助,以及美国陆军前列腺癌研究计划(DAMD17-98-1-8507)和欧洲委员会生活质量计划(QLK3-1999-01262)的资助。
脚注
使用的非标准缩写: CR,嵌合受体; 前列腺癌; 前列腺特异性抗原; 单链可变区; SDF-1,基质细胞衍生因子-1; 全身照射; 转铁蛋白受体; 肿瘤浸润淋巴细胞; TNP,2,4,6-三硝基苯酚。
工具书类
1 Jemal A等人,《癌症统计》,2003年。 加州癌症杂志临床。 2003; 53:5–26. doi:10.3322/canjclin.53.1.5。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
2 Yonou H,等。在植入人类成人肺和骨的人源化非肥胖糖尿病/严重联合免疫缺陷小鼠中建立一种新的人类前列腺癌物种和组织特异性转移模型。 2001年癌症研究; 61:2177–2182. [ 公共医学 ] [ 谷歌学者 ]
三。 Whitmore WF.,Jr前列腺癌的自然史和分期。 乌洛尔。 临床。 北方。 1984年美国; 11:205–220. [ 公共医学 ] [ 谷歌学者 ]
4 新罕布什尔州侯赛因和克劳福德,D.1997。 转移性前列腺癌的雄激素剥夺策略。 在 泌尿生殖肿瘤学原理与实践。 D.Raghavan、H.I.Scher、S.A.Leibel和P.Lange,编辑。 利平科特-拉文。 美国宾夕法尼亚州费城591-597。
5 Eshhar Z.肿瘤特异性T体:临床应用。 癌症免疫学。 免疫疗法。 1997; 45:131–136. doi:10.1007/s002620050415。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
6 Ma,Q.Z.,Gonzalo-Daganzo,R.和Junghans,R.P.,2001年。 基因工程T细胞作为癌症的过继免疫治疗。 在 癌症化学疗法和生物反应调节剂,第20卷。 G.Giacone、R.Schilsky和P.Sond,编辑。 爱思唯尔科学。 英国牛津。 319–345. [ 公共医学 ]
7 Sadelain M,Riviere I,Brentjens R.用基因增强的T淋巴细胞靶向肿瘤。 Nat.Rev.癌症。 2003; 3:35–45. doi:10.1038/nrc971。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
8 Pinthus JH等。利用嵌合受体导向的人类淋巴细胞对已建立的前列腺肿瘤进行免疫基因治疗。 2003年癌症研究; 63:2470–2476. [ 公共医学 ] [ 谷歌学者 ]
9 Campbell JJ,Butcher EC。组织特异性和微环境特异性淋巴细胞归巢中的趋化因子。 货币。 操作。 免疫学。 2000; 12:336–341. doi:10.1016/s0952-7915(00)00096-0。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
10 Kershaw MH等。基因修饰T细胞对肿瘤血管上发现的血管生成激酶插入域相关受体(KDR)产生反应。 嗯,基因疗法。 2000; 11:2445–2452. doi:10.1089/10430340050207939。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
11 Brentjens RJ等。通过CD80和白细胞介素-15共同刺激的基因靶向人类T淋巴细胞根除全身B细胞肿瘤。 《国家医学》,2003年; 9:279–286. doi:10.1038/nm827。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
12 Cashman JD等。将正常人骨髓中的原始细胞移植到免疫缺陷小鼠中的多系造血再生的动力学证据。 鲜血。 1997; 89:4307–4316. [ 公共医学 ] [ 谷歌学者 ]
13 Kollet O等。将人CD34+CD38–/低CXCR4+干细胞和祖细胞快速高效地归巢至NOD/SCID和NOD/SCID/B2mnull小鼠的骨髓和脾脏。 鲜血。 2001; 97:3283–3291. doi:10.1182/血.v97.10.3283。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
14 Lapidot T,Kollet O。趋化因子SDF-1及其受体CXCR4在移植免疫缺陷NOD/SCID和NOD/SCID/B2mnull小鼠的人类干细胞归巢和再增殖中的重要作用。 白血病。 2002; 16:1992–2003. doi:10.1038/sj.leu.2422684。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
15 Ponomaryov T等。DNA损伤后诱导趋化因子基质衍生因子-1可改善人类干细胞功能。 临床杂志。 投资。 2000; 106:1331–1339. doi:10.1172/JCI10329。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
16 Bleul CC、Fuhlbrigge RC、Casasnovas JM、Aiuti A、Springer TA。 高效淋巴细胞趋化剂基质细胞衍生因子1(SDF-1)《实验医学杂志》,1996年; 184:1101–1109. doi:10.1084/jem.184.3.1101。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
17 Beider K等。CXCR4和IL-2参与人类NK和NK T细胞归巢和滞留到NOD/SCID小鼠的骨髓和脾脏。 鲜血。 2003; 102:1951–1958. doi:10.1182/bloud-2002-10-3293。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
18 Kantele JM,Kurk S,Jutila MA。持续暴露于基质细胞衍生因子-1α对T细胞滚动和与活化内皮细胞单层紧密粘附的影响。 免疫学杂志。 2000; 164:5035–5040. doi:10.4049/jimmunol.164.10.5035。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
19. Nanki T等。基质细胞衍生因子-1-CXC趋化因子受体4的相互作用在类风湿关节炎滑膜中CD4+T细胞的积聚中起着关键作用。 免疫学杂志。 2000; 165:6590–6598. doi:10.4049/jimmunol.165.11.6590。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
20. Eshhar Z、Waks T、Bendavid A、Schindler DG。 嵌合受体基因在人类T细胞中的功能表达。 免疫学杂志。 方法。 2001; 248:67–76. doi:10.1016/s0022-1759(00)00343-4。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
21 Jourdan P等人,IL-4诱导人T细胞上CXCR4的功能性细胞表面表达。 免疫学杂志。 1998; 160:4153–4157. [ 公共医学 ] [ 谷歌学者 ]
22. Shirozu M等。人基质细胞衍生因子1(SDF1)基因的结构和染色体定位。 基因组学。 1995; 28:495–500. doi:10.1006/geno.1995.1180。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
23. Peled A等。人类干细胞移植和NOD/SCID小鼠对CXCR4的再繁殖依赖性。 科学。 1999; 283:845–848. doi:10.1126/science.283.5403.845。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
24 Beecham EJ,Ortiz-Pujols S,Junghans RP。携带抗癌胚抗原嵌合免疫球蛋白T细胞受体的人类T淋巴细胞杀伤肿瘤细胞的动力学。 免疫学杂志。 2000; 23:332–343. doi:10.1097/00002371-200005000-00006。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
25 Haynes NM等。小鼠CTL对结肠癌的定向作用:含有TCR-zeta和FcεRI-gamma的单链可变结构域嵌合体的优越信号传递效率。 免疫学杂志。 2001; 166:182–187. doi:10.4049/jimmunol.166.1.182。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
26 Jensen M,Tan G,Forman S,Wu AM,Raubitschek A.CD20是scFvFc的分子靶点:zeta受体导向的T细胞:CD20+恶性肿瘤细胞免疫治疗的意义。 生物骨髓移植。 1998; 4:7583. doi:10.1053/bbmt.1998.v4.pm9763110。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
27 Hombach A等。一种抗CD30嵌合受体,在存在可溶性CD30的情况下,介导CD3-zeta-independent T细胞对霍奇金淋巴瘤细胞的激活。 1998年癌症研究; 58:1116–1119. [ 公共医学 ] [ 谷歌学者 ]
28 Finney HM,Lawson AD,Bebbington CR,Weir AN。嵌合受体通过单一基因产物在T细胞中提供初级和共刺激信号。 免疫学杂志。 1998; 161:2791–2797. [ 公共医学 ] [ 谷歌学者 ]
29 Hekele A等人,通过过继转移CD44v6特异性scFv:zeta嵌合体重编程的细胞毒性T淋巴细胞来抑制肿瘤的生长。 国际癌症杂志。 1996; 68:232–238. doi:10.1002/(SICI)1097-0215(19961009)68:2<232::AID-IJC16>3.0.CO; 2-摄氏度。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
30. Daly T等。用嵌合受体基因转导的T细胞识别人类结肠癌。 癌症基因治疗。 2000; 7:284–291. doi:10.1038/sj.cgt.7700121。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
31 Ren-Heidenreich L,Hayman GT,Trevor KT。嵌合T细胞受体修饰的初级淋巴细胞对EGP-2+肿瘤细胞的特异性靶向。 嗯,基因疗法。 2000; 11:9–19. doi:10.1089/10430340050016111。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
32 Hwu P,等。用由抗体可变区和Fc受体γ链组成的嵌合基因重定向的人淋巴细胞对卵巢癌细胞的裂解。 《实验医学杂志》,1993年; 178:361–366. doi:10.1084/jem.178.1.361。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
33 Weijtens ME、Willemsen RA、Valerio D、Stam K、Bolhuis RL。单链Ig/γ基因导向的人类T淋巴细胞产生细胞因子,特异性溶解肿瘤细胞,并具有循环溶解能力。 免疫学杂志。 1996; 157:836–843. [ 公共医学 ] [ 谷歌学者 ]
34 Weijtens ME、Willemsen RA、Hart EH、Bolhuis RL。逆转录病毒载体系统“STITCH”与优化的单链抗体嵌合受体基因结构相结合,可在人类T淋巴细胞中高效进行基因转导和表达。 基因疗法。 1998; 5:1195–1203. doi:10.1038/sj.gt.3300696。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
35 Yun CO、Nolan KF、Beecham EJ、Reisfeld RA、Junghans RP。通过嵌合抗GD3免疫球蛋白T细胞受体将T淋巴细胞靶向黑色素瘤细胞。 肿瘤。 2000; 2:449–459. doi:10.1038/sj.neo.7900108。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
36 Reinhold U等。受体移植的T细胞对黑色素瘤细胞的特异性裂解通过针对受体的scFv结构域的抗独特型单克隆抗体增强。 J.投资。 皮肤病。 1999; 112:744–750. doi:10.1046/j.1523-1747.1999.00586.x。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
37 Mezzanzanica D等人。由肿瘤特异性抗体的可变区域组成的嵌合受体基因的转移可赋予T细胞抗碳水化合物的特异性。 癌症基因治疗。 1998; 5:401–407. [ 公共医学 ] [ 谷歌学者 ]
38 Willemsen RA等。用肿瘤特异性嵌合单链和双链TCR移植原代人类T淋巴细胞。 基因疗法。 2000; 7:1369–1377. doi:10.1038/sj.gt.3301253。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
39 龚MC等。前列腺特异性膜抗原基因靶向的癌症患者T细胞特异性地溶解前列腺癌细胞并释放细胞因子以响应前列腺特异性薄膜抗原。 肿瘤。 1999; 1:123–127. doi:10.1038/sj.neo.7900018。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
40 Bander NH等。前列腺癌中MHC I类和II类的表达以及干扰素-α和-γ的调节。 前列腺。 1997; 33:233–239. doi:10.1002/(sici)1097-0045(19971201)33:4<233::aid-pros2>3.0.co; 2-i。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
41 Sanda MG等。人类前列腺癌中缺陷抗原处理的分子特征。 J.国家。 1995年癌症研究所; 87:280–285. doi:10.1093/jnci/87.4.280。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
42 Croft M.通过OX40、4-1BB和CD27协同刺激T细胞。 细胞因子生长因子修订版2003; 14:265–273. doi:10.1016/s1359-6101(03)00025-x。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
43 Maus MV等。通过表达T细胞受体、CD28和4-1BB配体的人工APC体外扩增多克隆和抗原特异性细胞毒性T淋巴细胞。 自然生物技术。 2002; 20:143–148. doi:10.1038/nbt0202-143。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
44 Rosenberg SA等。用自体肿瘤浸润淋巴细胞和白细胞介素2治疗转移性黑色素瘤患者。 J.国家。 1994年癌症研究所; 86:1159–1166. doi:10.1093/jnci/86.15.1159。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
45 Yee C等。黑色素瘤抗原特异性免疫治疗后黑素细胞的破坏:T细胞介导白癜风的直接证据。 《实验医学杂志》,2000年; 192:1637–1644. doi:10.1084/jem.192.11.637。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
46 Dudley ME等人。克隆的黑色素瘤反应性T淋巴细胞的过继转移用于治疗转移性黑色素瘤患者。 免疫学杂志。 2001; 24:363–373. doi:10.1097/00002371-200107000-00012。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
47 Kjaergaard J等。不同给药途径下淋巴因子活化杀伤T细胞在荷瘤动物体内的生物分布和肿瘤定位。 癌症免疫学。 免疫疗法。 2000; 48:550–560. doi:10.1007/PL00006673。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
48 Rossi D,Zlotnik A.趋化因子及其受体的生物学。 每年。 免疫学评论。 2000; 18:217–242. doi:10.146/annrev.immunol.18.1.217。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
49 刘华,等。前列腺特异性膜抗原胞外区的单克隆抗体也与肿瘤血管内皮细胞发生反应。 1997年癌症研究; 57:3629–3634. [ 公共医学 ] [ 谷歌学者 ]
50 Reiter RE等。前列腺干细胞抗原:前列腺癌中过度表达的细胞表面标记物。 程序。 国家。 阿卡德。 科学。 美国1998年; 95:1735–1740. doi:10.1073/pnas.95.4.1735。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
51 Su ZZ,et al.表面-上皮掩蔽和表达克隆确定了人前列腺癌肿瘤抗原基因PCTA-1是半乳糖凝集素基因家族的成员。 程序。 国家。 阿卡德。 科学。 美国1996年; 93:7252–7257. doi:10.1073/pnas.93.14.7252。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
52 Hubert RS等。STEAP:一种前列腺特异性细胞表面抗原,在人类前列腺肿瘤中高度表达。 程序。 国家。 阿卡德。 科学。 美国1999年; 96:14523–14528. doi:10.1073/pnas.96.25.14523。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
53 Lyne JC等。neu分化因子/海红细胞蛋白及其受体复合物在前列腺癌中的组织表达及其对前列腺癌细胞的体外生物学效应。 癌症科学杂志。 美国1997年; 3:21–30. [ 公共医学 ] [ 谷歌学者 ]
54 Craft N等。雄激素依赖性肿瘤中雄激素依赖型前列腺癌细胞通过两步过程克隆生长的证据。 1999年癌症研究; 59:5030–5036. [ 公共医学 ] [ 谷歌学者 ]
55 Signoretti S等人。人类前列腺癌中Her-2-neu的表达和雄激素非依赖性的进展。 J.国家。 2000年癌症研究所; 92:1918–1925. doi:10.1093/jnci/92.23.1918。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
56 Corey E等,LuCaP 35:前列腺癌向雄激素非依赖性进展的新模型。 前列腺。 2003; 55:239–246. doi:10.1002/pros.10198。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
57. Gomez GG、Hutchison RB、Kruse CA。癌症的化学免疫治疗和化疗免疫治疗。 癌症治疗。 2001年修订版; 27:375–402. doi:10.1053/ctrv.2001.0222。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
58 Ganss R、Ryschich E、Klar E、Arnold B、Hammerling GJ。 T细胞治疗和炎症触发相结合可诱导血管重塑和肿瘤根除。 2002年癌症研究; 62:1462–1470. [ 公共医学 ] [ 谷歌学者 ]
59 Dunussi-Joannopoulos K等人。趋化因子基质细胞衍生因子1(SDF-1)的有效免疫调节活性:SDF-1在肿瘤部位的局部分泌作为T细胞化学吸引剂并介导T细胞依赖性抗肿瘤反应。 鲜血。 2002; 100:1551–1558. [ 公共医学 ] [ 谷歌学者 ]
60 Dudley ME等。用抗肿瘤淋巴细胞克隆性重新填充后患者的癌症退化和自身免疫。 科学。 2002; 298:850–854. doi:10.1126/science.1076514。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
61 Geminder H等。CXCR4及其配体CXC趋化因子基质细胞衍生因子-1在神经母细胞瘤骨髓转移发展中的可能作用。 免疫学杂志。 2001; 167:4747–4757. doi:10.4049/jimmunol,167.8.4747。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
62 Libura J等。CXCR4-SDF-1信号在横纹肌肉瘤细胞中活跃,并调节运动、趋化性和粘附。 鲜血。 2002; 100:2597–2606. doi:10.1182/bloud-2002-01-0031。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
63 Muller A等。趋化因子受体在乳腺癌转移中的作用。 自然。 2001; 410:50–56. doi:10.1038/35065016。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
64 Zeelenberg IS,Ruuls-Van Stalle L,Roos E.结肠癌微转移的生长需要趋化因子受体CXCR4。 2003年癌症研究; 63:3833–3839. [ 公共医学 ] [ 谷歌学者 ]
65 Corey E等人。骨前列腺癌模型的建立和表征:人类前列腺癌细胞的椎体内注射。 前列腺。 2002; 52:20–33. doi:10.1002/pros.10091。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
66 Stancovski I等人。ERBB2受体单克隆抗体对抗肿瘤生长作用的机制方面。 程序。 国家。 阿卡德。 科学。 美国1991年; 88:8691–8695. doi:10.1073/pnas.88.19.8691。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
67 Jung S等。体内CD11c+树突状细胞的缺失会取消外源性细胞相关抗原对CD8+T细胞的启动作用。 免疫。 2002; 17:211–220. doi:10.1016/s1074-7613(02)00365-5。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]