介绍 癌症的发展和转移是一个多步骤的过程,包括肿瘤的局部生长和侵袭,然后扩散到远处并在远处重建。 肿瘤转移的能力是癌症患者死亡率的主要决定因素。 因此,阐明肿瘤转移所必需的分子途径是癌症生物学的首要任务,并为开发抗转移癌症治疗的新治疗靶点提供了基础。
转录因子NF-κB通过其诱导编码细胞因子、细胞因子受体和细胞粘附分子的基因表达的能力,最初被发现并研究为免疫和炎症功能的主要激活物,最近被认为与细胞增殖和肿瘤发生的控制有关(参考文献。 1 ). NF-κB转录因子以异二聚体或同源二聚体的形式与DNA结合,该二聚体由小鼠和人类中五种可能的亚基(RelA/p65、c-Rel、RelB、p50和p52)组成。 这些蛋白质的特征是其Rel同源结构域,该结构域介导DNA结合、二聚化以及与抑制剂κB(IκB)蛋白质的相互作用。 尽管Rel/p65和p50亚单位普遍表达,但p52、c-Rel和RelB亚单位在特定分化细胞类型中的功能更为重要(参考文献综述)。 2 ). 在大多数未经刺激的细胞中,NF-κB二聚体是不活跃的,因为它与IκB蛋白结合,掩盖了NF-κ的核定位序列,从而将其保留在细胞质中并阻止DNA结合。 几个IκB蛋白参与NF-κB活性的控制,其中三个蛋白(IκB-α、Iκ-Bβ和IκB/ε)以刺激依赖的方式充当负调节因子。 例如,通过促炎细胞因子如TNF-α和IL-1刺激细胞,导致位于蛋白质N末端结构域的两个丝氨酸残基的IκB磷酸化(参考文献。 三 , 4 ). IκB的磷酸化导致附近赖氨酸残基的泛素化,这代表26S蛋白酶体降解的信号。 IκB蛋白的降解导致NF-κB的释放,允许核移位并结合到靶基因调控区域的同源DNA基序。 因此,诱导了这些基因的转录,这些基因参与免疫和炎症反应、凋亡调节以及细胞生长控制(参考文献中综述)。 三 , 4 ). NF-κB活化的关键步骤是高分子量IκB激酶(IKK)复合物对IκB的磷酸化。 该复合物包括两种激酶蛋白,IKK-1和IKK-2(分别称为IKK-α和IKK-β),以及一种称为NF-κB基本调节剂(NEMO;也称为IKKγ)的调节成分(参考文献综述)。 4 ).
过去几年积累了大量证据表明NF-κB活性与肿瘤发生有关(参考文献中综述)。 1 , 2 ). 通过鉴定c-Rel的病毒同源物v-Rel作为引起鸡侵袭性肿瘤的禽逆转录病毒的转化癌基因,初步表明异常NF-κB活性与癌症之间的联系( 5 ). 此外,致癌病毒,如人类T细胞白血病病毒I或EB病毒,作为转化过程的一部分激活NF-κB( 6 , 7 ). NF-κB基因的转位 NF公司- κ B2/第52页 和IκB家族成员 Bcl-3型 在一些淋巴肿瘤中观察到。 8 ). 高水平的NF-κB被证明对霍奇金淋巴瘤肿瘤细胞的转化表型至关重要( 9 )在一些霍奇金淋巴瘤病例中检测到编码IκBα的基因突变( 10 ). 与此同时,组成性核NF-κB活性已成为许多其他人类白血病、淋巴瘤和实体瘤的标志(参考文献综述)。 2 , 8 ). 此外,包括Ha-Ras和Bcr-Abl在内的几种癌蛋白已知可激活NF-κB并依赖NF-κB介导其转化活性(参考文献综述)。 1 ). 尽管核因子-κB在人类肿瘤发病机制中的确切作用尚待确定,但抑制凋亡显然非常重要,因为抑制核因子-kb B会使许多肿瘤细胞对死亡诱导刺激敏感,包括化疗药物(参考文献综述)。 1 , 2 ).
NF-κB是否以及如何调节侵袭性反应,如上皮-间充质转化(EMT)和转移,目前尚不清楚。 越来越多的证据表明,EMT代表了晚期肿瘤进展的重要体外相关性( 11 —— 15 ). 按最初定义( 16 )EMT涉及上皮细胞向成纤维细胞、迁移细胞和更多恶性细胞的去分化,显示出一个深刻改变的间充质基因表达程序( 17 , 18 ). EMT也发生在胚胎发育过程中,受信号通路的精细相互作用调节( 12 , 13 , 15 , 16 ). 在包括EpH4乳腺上皮细胞在内的几种上皮细胞模型中,致癌Ras保护细胞免受TGF-β诱导的细胞周期阻滞和凋亡,从而克服TGF-?在早期肿瘤发生中的抑瘤作用。 此外,致癌Ras与TGF-β协同诱导EMT,这是一种通过自分泌TGF-( 19 —— 23 )并导致细胞迁移和运动,这对肿瘤的进展和转移至关重要(参考文献综述)。 15 ). EMT和转移所需的Ras下游效应器通路最近被确定为Raf/MEK/MAPK通路,而PI3K/Akt信号过度激活可保护TGF-β诱导的细胞凋亡( 17 ). 在这些模型系统中,转移潜能与上皮性肿瘤细胞接受EMT的能力密切相关( 15 ).
在这项研究中,我们表明NF-κB在Ras转化的乳腺上皮细胞EMT的诱导中起着重要作用。 NF-κB活性的丧失消除了TGF-β诱导的凋亡对这些细胞的保护作用,但也积极抑制了EMT基因程序,从而阻断了EMT。 相反,在缺乏TGF-β的情况下,NF-κB活性的增加在这些Ras转化细胞中诱导了EMT。 此外,NF-κB在维持EMT后的间充质状态方面也发挥着重要作用,因为其抑制可导致EMT逆转。 在小鼠中,抑制NF-κB活性大大降低了Ras转化的EpH4细胞的转移潜力。 我们的研究结果表明,NF-κB信号通路对小鼠乳腺癌模型的EMT和转移至关重要,并提示抑制NF-κ的治疗可能是控制肿瘤侵袭和转移的有效策略。
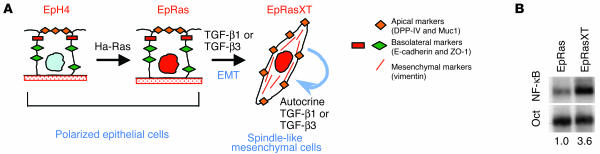
结果 EMT期间NF-κB信号的上调。 EpRas细胞代表致癌、完全极化、Ha-Ras转化的EpH4乳腺上皮细胞,它们在肿瘤和胶原凝胶中对TGF-β进行EMT反应,在这两种情况下都会产生间充质样细胞(EpRasXT细胞)。 EpRasXT细胞的特点是具有纺锤状形态和间充质标记蛋白的获得,这是一种通过自分泌TGF-β环在体内外稳定的表型(参考文献。 19 , 20 ; 参见图 1 A) ●●●●。 我们想确定NF-κB是否在EMT过程中发挥作用。 因此,我们通过电泳迁移率测定(EMSA)分析了指数增长的EpRas和EpRasXT细胞的全细胞提取物。 我们在EpRas细胞中检测到一些NF-κB DNA-结合活性,即使没有已知的NFκB诱导物的刺激,我们也始终观察到EpRasXT细胞中NF-κ的B DNA结合活性增加了3-4倍(图 1 B) ●●●●。
图1。
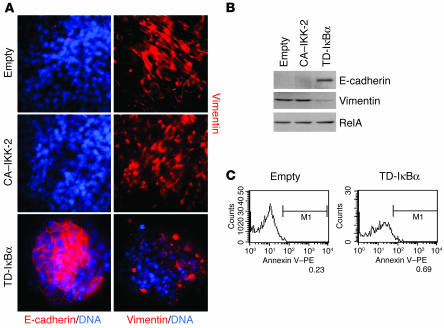
在EMT期间诱导NF-κB活性。 ( A类 )示意图说明了我们研究中使用的细胞类型中发现的形态和上皮/间充质标记物的重新分布或表达。 将未转化的EpH4乳腺上皮细胞稳定地转染Ha-Ras癌基因,产生转化的上皮性EpRas细胞,经TGF-β处理后进行EMT,从而通过自分泌TGF-?环进一步稳定间充质性EpRasXT细胞。 DPP-IV,二肽基肽酶IV; ZO-1,闭塞带1。 ( B类 )指数生长的EpRas和EpRasXT细胞的全细胞提取物(6μg)的EMSA使用NF-κB特异性探针(上面板)和八聚体特异性探针作为对照。 量化的相对DNA结合水平显示在EMSA下方。 使用不同的蛋白质提取物制剂获得了类似的数据(另请参见图 2 A) ●●●●。
基于这些观察结果,我们接下来询问NF-κB靶基因在间充质EpRasXT细胞中的诱导程度是否与其上皮对应物EpRas细胞相同。 为了解决这个问题,我们重新分析了先前报告的表达谱数据,其中我们对多聚体结合mRNA进行了微阵列分析,以确定EpRasXT与EpRas细胞中差异表达的基因(参考文献中的表2和表3)。 18 ). 有趣的是,在EMT期间上调的75个注释基因中,有13个之前被描述为NF-κB靶基因(表 1 ). 在间充质EpRasXT细胞中,编码NF-κB调节细胞因子/趋化因子的几个基因( 白介素-11 , JE/MCP-1 、和 KC/Gro1公司 ),蛋白酶( 基质金属蛋白酶-13 , 组织蛋白酶B , 基质金属蛋白酶2 、和 组织蛋白酶Z ),荷尔蒙( 胆囊收缩素 和 胎盘增殖素2 )和转录因子 统计-1 ,以及β 2 -微球蛋白 表达水平高于上皮细胞。 此外,NF-κB先前已被证明直接调节两个EMT标记基因 波形蛋白 和 tenascin C (表 1 ). 此外, bcl-3 ,NF-κB活性的调节因子( 24 )以前被确定在人类乳腺癌中表达( 25 ),同样在EpRasXT细胞中诱导( 18 ). 相反,在EpRasXT细胞中下调的基因中,只有一个基因( 凝血酶敏感蛋白1 )已建议由NF-κB调节(参考。 26 ; 参考文献中审查。 27 ). 因此,表达谱分析结果清楚地表明,NF-κB靶基因在间充质EpRasXT细胞中的表达丰富,与NF-κ的活性增加一致。
表1。 EMT期间EpRas/EpRasXT细胞对中NF-κB调节基因的诱导
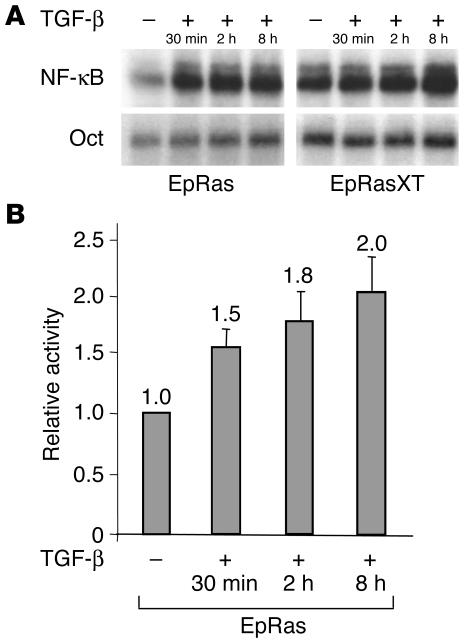
TGF-β在EMT期间诱导NF-κB活性。 根据TGF-β信号传导对EpRas细胞EMT的诱导至关重要的观察( 19 , 20 )以及TGF-β可以调节某些上皮细胞中NF-κB活性的报道( 28 ),我们试图测试TGF-β是否能影响EpRas和EpRasXT细胞中的NF-κB活性。 为了描述用TGF-β1刺激后NF-κB DNA结合活性的变化,我们在TGF-α1存在的情况下培养EpRas和EpRasXT细胞,并用EMSA监测NF-kb B DNA-结合活性的水平。 在EpRas细胞中,我们在30分钟内观察到NF-κB DNA结合活性的3-4倍诱导,而在Ep拉斯特细胞中我们观察到TGF-β无反应(图 2 A) ●●●●。 鉴于EpRasXT细胞本身产生TGF-β,其结果并不令人惊讶。 此外,用NF-κB依赖的荧光素酶报告子(3xκB.luc)瞬时转染EpRas和EpRasXT细胞。 用TGF-β1刺激EpRas细胞导致在2-8小时内NF-κB转录激活活性增加约2倍(图 2 B) ,而在EpRasXT细胞中没有发现增加(数据未显示)。 因此,TGF-β刺激导致EpRas细胞中功能活性NF-κB的诱导,而不影响EpRasXT细胞中增加的NFκB活性。
图2。
TGF-β诱导EpRas细胞NF-κB活性。 ( A类 )用TGF-β1(5 ng/ml)刺激EpRas和EpRasXT细胞达指定时间。 使用NF-κB特异性探针(上图)和八聚体特异性探针(下图)作为对照,对全细胞提取物(6μg)进行EMSA。 ( B类 )NF-κB转录活性。 用3xκB.luc或β-珠蛋白-TATA报告子构建瞬时转染EpRas细胞三次。 转染后20小时,用TGF-β1(5ng/ml)处理细胞指定的时间。 然后,测定提取物的荧光素酶活性,并根据Renilla荧光素酶的表达进行归一化。 显示3xκB.luc和β-珠蛋白-TATA的比率。 未刺激的空载体感染的EpRas细胞的表达水平被用作参考荧光素酶活性,并被任意设置为1。 平均值和标准偏差代表了两个独立的实验,共进行了三次。 条形图表示标准偏差。
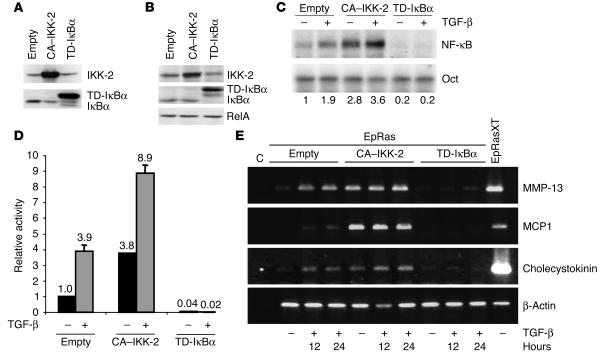
NF-κB对EMT至关重要。 为了研究IKK/IκBα/NF-κB信号模块在EMT和转移调控中的作用,我们利用逆转录病毒基因转移在EpRas细胞中表达该通路的显性干扰突变体。 使用表达 反式 -显性(TD)IκBα蛋白(TD-IκBβ,其中位于32和36位的丝氨酸残基突变为丙氨酸残基,形成不可降解的阻遏物),是一种组成活性(CA)IKK-2蛋白(CA–IKK-2,其中激活环中的两个丝氨酸残端突变为磷酸谷氨酸残基), 或空矢量控制。 当逆转录病毒共同作用增强GFP时,免疫荧光显微镜观察到稳定感染的细胞。 通过Western blot检测TD-IκBα和CA–IKK-2在φNX产生系细胞和稳定感染的EpRas细胞中的表达(图 三 、A和B)。 该分析显示,与内源性对应物相比,突变蛋白的过度表达很强。 如之前在另一个细胞系统中观察到的( 29 ),高水平外源性TD-IκBα的存在导致内源性IκBβ表达减少,很可能是由于NF-κB活性受到抑制。 EMSA分析EpRas细胞中TD-IκBα和CA–IKK-2表达对NF-κB DNA结合活性的影响。 在感染TD-IκBα的EpRas细胞中,未观察到NF-κB DNA结合活性,无论细胞是未受刺激还是受TGF-β刺激(图 三 C) 、TNF-α或PMA(未显示数据)。 相比之下,感染CA–IKK-2的细胞在未刺激状态下表现出2到3倍的DNA结合活性(与未刺激的EpRas对照细胞相比),并且与TGF-β处理的EpRas对照细胞相比较,在TGF-α刺激后,NF-κB活性的诱导大约高出2倍。 用3xκB.luc瞬时转染这些细胞和随后的荧光素酶检测显示,与未经刺激或TGF-β处理的EpRas对照细胞相比,感染CA–IKK-2的未经处理的Ep Ras细胞的荧光素酶活性诱导为3到4倍,用TGF-, 分别。 相反,在用TGF-β治疗前后,表达TD-IκBα的EpRas细胞中NF-κB转录活性几乎被完全抑制(图 三 D) ●●●●。 此外,与EMT相关的NF-κB调节靶基因子集的RT-PCR分析(表 1 ) ( 18 )在TGF-β诱导的EMT前后用EpRas突变体进行。 该分析表明 基质金属蛋白酶-13 , MCP-1型 、和 胆囊收缩素 在没有TGF-β的情况下,在CA–IKK-2–表达EpRas细胞中 MCP-1型 ,这甚至与EpRasXT细胞中的表达水平相当),并且在TGF-β的存在下这些基因的表达略强( 胆囊收缩素 和 基质金属蛋白酶-13 )而在TD-IκBα表达细胞中,这些基因的表达和TGF-β诱导的上调几乎完全被阻断(图 三 E) ●●●●。 基于这些结果,NF-κB激活了转化生长因子β诱导的EMT基因程序中的至少一部分基因。
图3。
EpRas细胞中NF-κB活性的调节。 ( A类 和 B类 )优势干扰突变体在ΦNX产生细胞中的表达水平( A类 )和稳定感染的EpRas细胞( B类 )通过全细胞提取物的Western blot分析,使用IκBα和IKK特异性抗体CA-IKK-2、内源性IKK-2(与CA–IKK-2结合)、TD-IκBβ和内源性IκBα进行测定。 使用p65/RelA特异性抗体评估等载量( B类 ,底部面板)。 ( C类 )EMSA使用NF-κB特异探针(上面板)和八聚体特异探针(下面板)作为负载控制,对稳定感染的EpRas突变体的提取物进行分析,这些提取物未经处理(-)或用TGF-β(5 ng/ml)刺激2小时(+)。 显示了量化的相对DNA结合水平。 ( D类 )用3xκB.luc或β-珠蛋白TATA报告基因构建体瞬时转染稳定感染的细胞,一式三份。 24小时后,用TGF-β(5 ng/ml,持续4小时)处理细胞(+)或不处理细胞(-)。 根据Renilla荧光素酶的表达(如图所示 2 B) ●●●●。 显示3xκB.luc和β-珠蛋白-TATA的比率。 未刺激空载体转染的EpRas细胞的表达水平用作参考,并任意设置为1。 条形图表示标准偏差。 ( E类 )用TGF-β(5 ng/ml)刺激EpRas突变体和EpRasXT细胞达到指定的时间,并进行RT-PCR分析,以检测其转录表达 基质金属蛋白酶-13 , MCP-1型 , 胆囊收缩素 、和β -肌动蛋白 ,如方法中所述。 C、 控制(水); 空的EpRas细胞感染空载体控制。
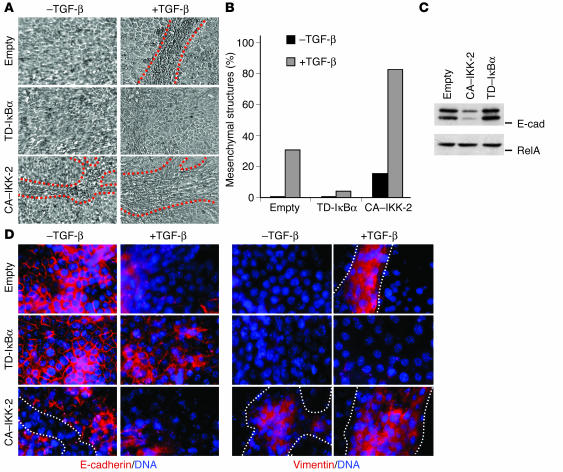
然后我们询问NF-κB活性的这种调节是否影响EpRas细胞进行EMT的能力。 在允许上皮极化的多孔支架(过滤器)上,感染空载体(如未感染细胞)的EpRas细胞显示出完全极化的上皮表型,上皮标记物E-cadherin的基底外侧质膜表达,但间充质标记物vimentin不表达(图 4 ,A–D)。 用TGF-β处理这些EpRas细胞5天后,产生了纺锤形、波形蛋白阳性的细胞链,这些细胞仅弱表达E-钙粘蛋白(图 4 、A、B和D)。 在不含TGF-β的TD-IκBα表达细胞中,与EpRas对照细胞相比,未观察到表型变化或标记表达变化(图 4 ,A–D)。 然而,在用TGF-β治疗后,由于细胞死亡,这些TD-IκBα-过表达且NF-κB活性被阻断的EpRas细胞中有相当一部分迅速从多孔支架上脱落。 其余的细胞几乎完全不能进行EMT(图 4 A) ●●●●。 TGF-β处理的TD-IκBα表达的EpRas细胞缺乏纺锤状间充质细胞链,这些细胞在感染病毒的空EpRas对照培养物中大量存在(图 4 、A和B)。 同样的细胞未能上调波形蛋白,并保留了高水平的E-cadherin,E-cadherin部分重新分布到细胞质,这表明极性有所丧失(图 4 D) ●●●●。 令人惊讶的是,即使在没有TGF-β的情况下,CA–IKK-2–过度表达的EpRas细胞NF-κB活性也能以相当高的速度进行EMT(图 4 、A和B)。 细胞在多孔支架上生长6天后,我们观察到梭形E-钙粘蛋白阴性和波形蛋白阳性细胞链,它们覆盖了总表面积的10%以上(图 4 、A、B和D)。 当我们通过Western免疫印迹分析这些细胞的大量培养物时,我们观察到E-cadherin水平显著降低(图 4 C) ●●●●。 与这些观察结果一致,我们注意到TGF-β处理后CA–IKK-2表达细胞的EMT较对照EpRas细胞增强,如胞质(去极化)或无E-cadherin表达的纺锤形细胞百分比更高以及波形蛋白表达强(图 4 、A、B和D)。 重要的是,当CA-IKK-2和TD-IκBα转基因导入V12S35Ras细胞时,获得了非常相似的结果。 这些细胞代表另一个单基因转化细胞系,该细胞系独立于原始EpH4细胞生成,并由不同致癌Ras的效应突变体转化,该效应突变体诱导ERK/MAPK过度激活,但不诱导PI3K信号( 17 ). 我们观察到TD-IκBα表达细胞中的EMT受到抑制,并且在CA–IKK-2–表达V12S35Ras细胞中没有TGF-β的情况下,自发EMT的发生率相当高,发生频率甚至高于CA–IK-2–表示EpRas细胞(参见补充图1;补充材料可从 http://www.jci.org/cgi/content/full/114/4/569/DC1 ). 因此,NF-κB在EMT调节中的作用并不局限于单个细胞系。
图4。
表达TD-IκBα的EpRas细胞不能进行EMT,而CA–IKK-2的表达在缺乏TGF-β的情况下驱动EMT(多孔支持物分析)。 表达空载体对照、TD-IκBα或CA–IKK-2的EpRas细胞在有(+)或无(-)TGF-β(5 ng/ml;第2-7天)的多孔支架上培养7天。 ( A类 )显示培养细胞的照片; 具有纺锤形间充质细胞链的区域由红色虚线表示。 原始放大倍数,×100。 ( B类 )量化由间充质干细胞覆盖的多孔支架上的面积,作为相对于粘附细胞覆盖的总面积的百分比(培养物显示为 A类 ; 第6天)。 ( C类 )表达空载体、TD-IκBα或CA–IKK-2且未经TGF-β处理的EpRas细胞中的E-cadherin水平通过E-cadherin-特异性抗体的Western blot分析测定(E-Cad;上面板)。 随后用p65/RelA特异性抗体(下面板)剥离和重制印迹,以证明负载量相等。 ( D类 )如图所示,在有或无TGF-β(5 ng/ml;第2-7天)的情况下,将细胞培养在多孔支架上7天。 如方法所述,用DAPI反染DNA(蓝色)对细胞进行E-cadherin或vimentin免疫染色(红色)。 间充质细胞、E-钙粘蛋白阴性细胞和波形蛋白阳性细胞的区域用白色虚线勾勒出来,对应于 A类 (红色虚线)。 原始放大倍数,×400。
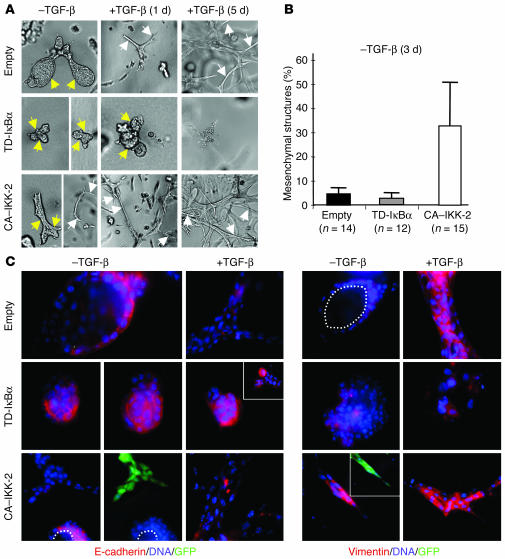
用于分析上皮细胞行为和可塑性的更具生理学意义的培养系统是三维无血清I型胶原凝胶培养( 15 ). 在这些培养物中,完全极化的EpRas对照细胞形成管状和肺泡结构,管腔较大(图 5 A) ●●●●。 这些细胞显示E-钙粘蛋白的基底外侧膜(极化)表达,但没有波形蛋白表达(图 5 C) ●●●●。 添加TGF-β1后,EpRas对照细胞进行EMT,如纺锤形和迁移表型、E-钙粘蛋白丢失和治疗6天后波形蛋白的从头表达所示(图 5 、A和C)。 未经处理的TD-IκBα细胞与对照的EpRas细胞相似,它们形成上皮结构(管腔的管状结构),并显示基底侧E-cadherin染色,无波形蛋白表达。 尽管存在这种相似性,TD-IκBα上皮结构看起来更紧密,尺寸更小(图 5 、A和C)。 用TGF-β治疗后,表达TD-IκBα的EpRas细胞形成的上皮结构保留了E-cadherin的表达(图 5 C) ,但迅速分解(图 5 、A和C)。 只有极少数结构(约0.5%)在分解前形成无序的细胞链(数据未显示)。 相反,未经处理的表达CA–IKK-2的细胞NF-κB活性增加,形成了两种结构。 而大部分带有管腔的上皮管状结构是明显的(图 5 A) ,大量结构由无序的细胞链组成,具有纺锤状细胞形态,类似于TGF-β处理的对照EpRas细胞(图 5 、A和B)。 有趣的是,在与对照组EpRas细胞相似的上皮结构中(E-cadherin阳性和vimentin阴性),有很大比例的CA–IKK-2表达缺失或下调,如低水平的协同调节GFP表达所示(图 5 C、 底部)。 相反,未经处理的CA–IKK-2表达细胞产生的间充质结构为E-cadherin阴性,表达vimentin,并显示出较强的GFP染色,表明转基因表达较高(图 5 C) ●●●●。 因此,即使在没有TGF-β的情况下,高水平的CA–IKK-2表达似乎也能促进EMT。 正如预期的那样,TGF-β治疗诱导剩余的上皮细胞CA–IKK-2表达的EpRas细胞快速形成间叶结构,表达波形蛋白,但不表达E-cadherin(图 5 、A和C)。 我们还确定了强NF-κB激活剂(如TNF-α)是否会诱导EMT。 事实上,我们在TNF-α处理的EpRas胶原凝胶培养物中观察到少量间充质结构表达波形蛋白,即使没有TGF-β(补充图2)。 总之,活化的NF-κB通路加上Ras足以引起EMT,而抑制NF-κ的B活性可以阻止EMT,导致胶原蛋白中形成的结构解体。
图5。
EpRas细胞中表达的TD-IκBα可预防EMT,而CA–IKK-2在缺乏TGF-β的情况下诱导EMT(胶原凝胶分析)。 将表达空载体对照、TD-IκBα或CA–IKK-2的EpRas细胞接种到胶原凝胶中,允许其形成结构3-5天,不进行诱导处理(-),或通过添加TGF-β(+)诱导其进行EMT 5-6天。 ( A类 )左柱,无TGF-β培养7天; 中柱,无TGF-β培养5天,加TGF-β处理(5 ng/ml)1天; 右柱,无TGF-β培养5天,加上TGF-α治疗(5 ng/ml)5天。 图中显示了具有管腔(黄色箭头)或扩张弦的代表性管状结构以及具有间充质形态的侵袭性细胞束(白色箭头)的照片。 原始放大倍数,×100。 ( B类 )间充质结构的量化(参见中的白色箭头 A类 对于CA–IKK-2,–TGF-β培养),在没有TGF-。 下图, n个 表示所分析的胶原蛋白凝胶的数量。 条形图表示分析单个胶原蛋白凝胶时获得的标准偏差。 ( C类 )对胶原凝胶结构进行染色,以检测上皮标记物E-cadherin(第一和第二列)或间充质标记物vimentin(第三和第四列)。 最下面一行,左起第二行(CA–IKK-2–表达细胞,–TGF-β):E-cadherin染色结构的GFP表达(绿色)。插图,左起的第三个面板,中间一行(TD-IκBα-表达细胞,+TGF-?):E-钙粘蛋白染色的分解结构。插图,右起的第二个面板,最下面一排 :波形蛋白染色结构的GFP表达(绿色)。 原始放大倍数,×400。
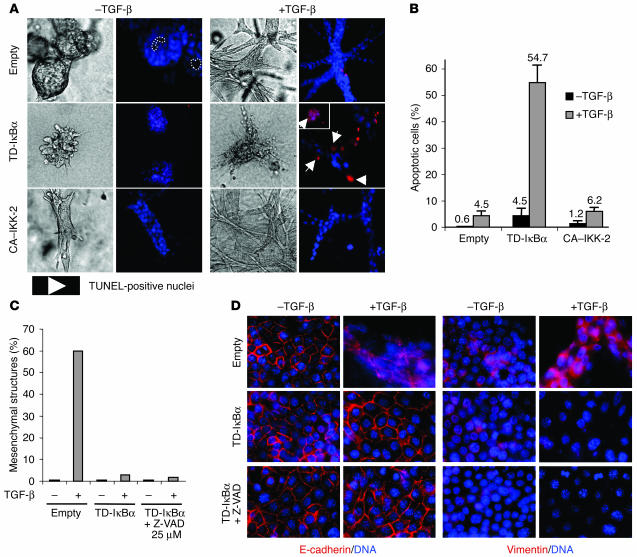
NF-κB是保护TGF-β诱导的细胞凋亡和直接促进EMT所必需的。 先前的实验表明,NF-κB在与Ras联合诱导EMT时,至少可以部分替代TGF-β。 接下来,我们讨论了NF-κB抑制与EMT预防相关的机制性后果。 因为我们观察到TGF-β治疗后TD-IκBα表达结构迅速解体,所以我们评估了它们在这些条件下的凋亡反应。 允许EpRas对照细胞以及表达TD-IκBα和CA–IKK-2的衍生物在胶原凝胶中形成器官型结构3天。 然后用TGF-β诱导他们进行EMT或不治疗。 经TGF-β处理的TD-IκBα表达的EpRas结构显示凋亡导致细胞解体,如原位TUNEL染色所示(图 6 A) ●●●●。 如图所示 6 B、 大约55%的细胞为TUNEL阳性,因此在TGF-β治疗6天后出现凋亡。 此外,即使在没有TGF-β的情况下,TD-IκBα细胞与对照EpRas细胞相比,诱导凋亡的能力也略有提高(4.5%对0.6%),这可能解释了胶原凝胶中表达TD-I kbα的细胞形成的上皮结构较小的原因。 最后,表达CA–IKK-2的EpRas细胞显示出较低的凋亡水平,与EpRas对照细胞相当。 然后我们询问是否观察到表达TD-IκBα的EpRas细胞在接受EMT时失败(图 4 和 5 )这完全是由于抑制了这些细胞中NF-κB的抗凋亡功能。 将EpRas对照细胞和表达TD-IκBα的衍生物培养在多孔支架上。 用25μM细胞透性caspase抑制剂苄氧羰基-Val-Ala-Asp-氟甲基酮(Z-VAD-FMK)处理表达TD-IκBα的EpRas细胞,强烈抑制这些细胞(在多孔支架和胶原凝胶上)中TGF-β诱导的凋亡;图 6 B) ,达到与EpRas对照细胞相当的水平(未显示数据)。 重要的是,用TGF-β刺激4天后,在这些Z-VAD-FMK处理的TD-IκBα表达的EpRas细胞中既没有观察到间充质结构(如TGF- 6 、C和D)。 值得注意的是,由于TGF-β治疗后出现大量凋亡细胞,在表达TD-IκBα的EpRas培养物中检测到小面积的不规则结构(数据未显示)。 Z-VAD-FMK阻断细胞凋亡时未观察到这些现象。 总之,Ras转化细胞在EMT期间需要NF-κB信号传导来保护其免受TGF-β诱导的凋亡。 此外,NF-κB作为EMT程序的直接调节器发挥着额外的作用,因为阻断凋亡并不能恢复表达TD-Iκβα的EpRas细胞对TGF-β进行EMT反应的能力。
图6。
抑制EpRas细胞中的NF-κB活性可导致细胞凋亡并防止EMT。 ( A类 )将表达空载体对照、TD-IκBα或CA–IKK-2的EpRas细胞接种到胶原凝胶中,让其形成结构3天,并用TGF-β治疗6天或不治疗。 对胶原培养物进行原位TUNEL染色(红色)和DAPI染色(蓝色,表示活细胞)。 图中还显示了TUNEL染色前拍摄的同一实验胶原蛋白凝胶的光学显微镜图像。 箭头表示TUNEL阳性核。 插图,右中面板:另一个具有TUNEL阳性细胞核的结构。 原始放大倍数,×200。 ( B类 )根据胶原凝胶结构定量TUNEL阳性细胞 A类 在三到六个随机选择的区域中,对至少300个细胞的细胞核进行TUNEL染色。 使用2到3个胶原蛋白凝胶的平均值计算凋亡指数和标准偏差。 在2–3个胶原凝胶(每个凝胶至少300个细胞)中评估的每种细胞类型的凋亡细胞平均百分比显示在条形图上。 ( C类 )表达空载体对照或TD-IκBα的EpRas细胞在有或无25μM Z-VAD-FMK(Z-VAD;第0-5天)和/或TGF-β(5 ng/ml;第1-5天)的多孔支架上培养5天。 间充质链覆盖的多孔支架上面积的量化显示为与粘附细胞覆盖的总面积的百分比(在第4天,经过或不经过TGF-β治疗3天后)。 ( D类 )在有或无TGF-β(5 ng/ml;第1-5天)的情况下,在多孔支架上培养所示细胞(有或无25μM Z-VAD-FMK;第0-5天)5天。 在多孔支架上培养5天后,对细胞进行E-cadherin或vimentin(红色)的免疫染色,以及DNA(蓝色)的DAPI复染。 原始放大倍数,×400。
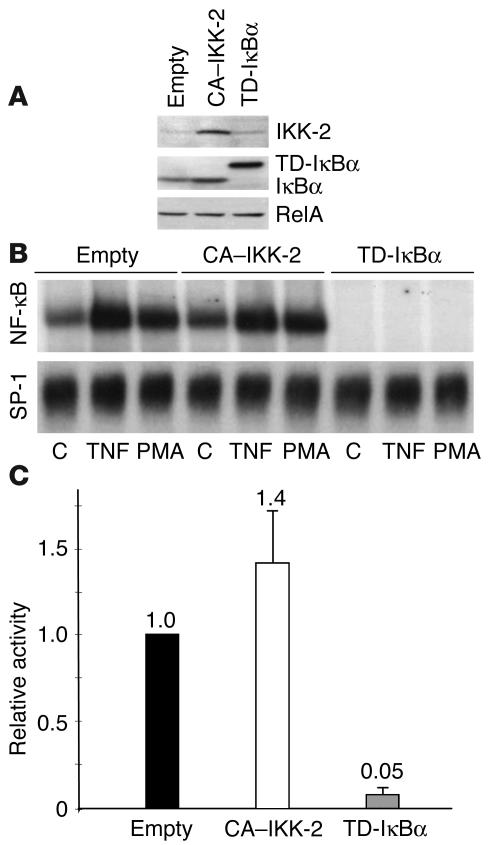
抑制间充质EpRasXT细胞NF-κB活性可导致EMT逆转。 接下来,我们研究了NF-κB活性的干扰是否也会影响已完成EMT的间充质EpRasXT细胞。 EpRasXT细胞再次被表达TD-IκBα或CA–IKK-2的逆转录病毒或GFP-空对照载体稳定感染。 通过蛋白质印迹分析评估的转基因表达如图所示 7 A.EMSA在未经治疗和TNF-α或PMA刺激的表达TD-IκBα的EpRasXT细胞中显示出NF-κB DNA结合活性的完全抑制。 在未经处理的细胞中,CA–IKK-2的表达仅导致NF-κB活性中度(不到2倍)增强(图 7 B) ●●●●。 用3xκB.luc瞬时转染和随后的荧光素酶检测显示,在表达TD-IκBα的EpRasXT细胞中,NF-κB反式激活活性被强烈阻断,而感染CA–IKK-2的EpRasXT细胞的荧光素酶活性中度增加。
图7。
逆转录病毒表达的TD-IκBα和CA–IKK-2对EpRasXT细胞NF-κB活性的影响。 ( A类 )在稳定感染的EpRasXT细胞中,通过使用IκBα-和IKK特异性抗体对全细胞提取物进行Western blot分析,确定显性干扰突变体与内源性表达野生型突变体的表达水平。 显示了CA–IKK-2/内源性IKK-2(整合)、TD-IκBα和内源性IκBβ的蛋白带。 通过剥离和重制带有p65/RelA抗体的印迹来评估平均负荷(底部面板)。 ( B类 )未对稳定感染的EpRasXT细胞进行治疗(对照),或用TNF-α(TNF;40 ng/ml)刺激1小时,或用PMA(50 ng/ml)刺激1个小时。 然后,以NF-κB特异性探针(上面板)或Sp-1特异性探针作为负荷对照,评估NF-κ子B DNA结合活性。 ( C类 )中描述的EpRasXT衍生物中的NF-κB转录活性 A类 和 B类 通过荧光素酶分析测定,如图所示 三 D.空载体转染的EpRasXT细胞的表达水平用作参考荧光素酶活性,并任意设置为1。 平均值显示在条形图上方。
为了测试TD-IκBα是否能够逆转EMT,我们在多孔支架上培养表达TD-I激酶Bα、CA–IKK-2或对照载体的EpRasXT细胞。 正如预期的那样,表达CA–IKK-2–和对照载体–的EpRasXT细胞显示出间充质、纺锤状表型,并表达高水平的波形蛋白,但没有E-cadherin(图 8 、A和B)。 然而,有趣的是,大量TD-IκBα表达细胞恢复到上皮表型,其中细胞形成紧密结构,在质膜上恢复了显著的E-cadherin表达,并且几乎完全失去了波形蛋白的表达,如免疫荧光所示(图 8 A) 和Western blot分析(图 8 B) ●●●●。 在不同培养条件下获得了类似的结果(数据未显示)。 表达TD-ⅠκBα的EpRasXT细胞在多孔支架上培养时没有明显的细胞死亡迹象(例如,细胞核浓缩、细胞解体和从多孔支架上脱落)。 膜联蛋白V染色(图 8 C) 以及TD-IκBα表达的EpRasXT细胞的细胞周期分析(数据未显示),这些细胞已恢复为上皮表型,表明恢复的上皮细胞仍然存活且健康。 这些结果表明,维持经过EMT的Ras转化细胞的间充质表型需要NF-κB活性。
图8。
抑制间充质EpRasXT细胞NF-κB活性可导致EMT逆转。 表达空载体对照、TD-IκBα或CA–IKK-2的EpRasXT细胞在多孔支架上培养6天。 ( A类 )对细胞进行E-钙粘蛋白(红色;左栏)或波形蛋白(红色;右栏)的免疫染色,并对DNA进行复染(蓝色;在顶部和中间面板中省略,右栏)。 原始放大倍数,×200。 ( B类 )用E-钙粘蛋白和波形蛋白特异性抗体分别通过Western blot分析测定E-钙黏蛋白和波状蛋白水平。 随后用p65/RelA特异性抗体剥离和重制印迹,以显示相等的负载(底部面板)。 ( C类 )感染TD-IκBα表达病毒或对照病毒的EpRasXT细胞生长在多孔支架上,以使TD-I k Bα细胞中的EMT逆转。 通过annexin V染色和FACS分析鉴定凋亡细胞。
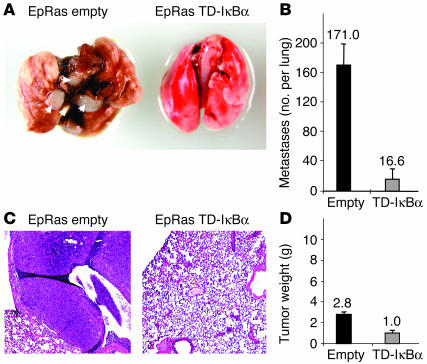
NF-κB是体内EpRas细胞转移潜能所必需的。 EpRas细胞对内源性TGF-β的体内EMT反应( 19 ). 在尾静脉注射培养的EpRas细胞(S.Grünert和H.Beug,未发表数据)或从EpRas-诱导的原发性乳腺肿瘤中重新培养的细胞后,TGF-β诱导的EpRas细胞EMT与它们形成肺转移的能力密切相关( 17 ). 由于NF-κB活性被发现对EMT的诱导和维持都至关重要,我们试图确定NFκB信号是否也是Ras和TGF-β在体内诱导转移潜能所必需的,以及抑制NF-κ的B是否会消除这种转移能力。 通过将培养细胞注射到裸鼠尾静脉,检测表达TD-IκBα的EpRas细胞和EpRas对照细胞的转移潜能。 注射EpRas对照细胞的小鼠因多次大转移而迅速死亡(平均在尾静脉注射后3-4周),而注射表达TD-IκBα的EpRas细胞的小鼠在注射EpRas对照细胞后死亡时看起来很健康。 通过组织学分析,注射NF-κB活性被阻断的EpRas细胞的小鼠肺重量减少了2倍(与相同年龄的对照小鼠相比;数据未显示),并且只有少数小(微)转移(平均数为每肺16.6个转移), 相比之下,注射EpRas对照细胞的动物每肺平均转移171.0个(图 9 ,A–C)。 为了验证表达TD-IκBα的EpRas细胞仍然能够以与EpRas对照细胞相似的方式形成原发性肿瘤,我们将上述细胞类型(在每种情况下,来自用于尾静脉注射的同一批次)注射到裸鼠的乳腺脂肪垫中。 3周后,EpRas对照细胞和表达TD-IκBα的EpRas细胞均形成肿瘤,其大小主要不同(图 9 D) ●●●●。 总之,抑制NF-κB活性强烈影响体内EpRas细胞的转移潜能,而对原发性肿瘤的形成影响不大。
图9。
抑制NF-κB活性可防止EpRas细胞的转移。 ( A类 )将感染空GFP载体(empty)或TD-IκBα的EpRas细胞(每次注射5×105个细胞)注入裸鼠(每种细胞类型4只动物)的尾静脉,并分析小鼠是否存在肺转移。 注意,注射了EpRas细胞的小鼠肺部出现了大的转移性结节(白色箭头),这些细胞已经感染了空载体(EpRas-empty;left)。 ( B类 )肺部转移类似于 A类 在连续切片中进行定量,以确定每个肺的平均转移数(每个细胞类型四个肺)。 ( C类 )注射了感染空载体或TD-IκBα的EpRas细胞的小鼠肺部苏木精和伊红染色。 注意,注射了感染空载体的EpRas细胞的小鼠出现了大的转移。 原始放大倍数,×10。 ( D类 )相同的细胞在 A类 —— C类 将(每注射部位2×105个细胞;每只动物4个注射部位)注射到裸鼠(每种细胞类型3只动物)的脂肪垫中,3周后测定每只小鼠的肿瘤总重量。 显示肿瘤的平均总重量。
讨论 NF-κB信号的激活越来越被认为是肿瘤发生的关键机制,并被认为主要通过赋予转化细胞抗凋亡的能力发挥作用。 在本报告中,我们使用一个特性良好的体外/体内乳腺癌发生联合模型(EpRas)来确定NF-κB在上皮可塑性和转移调节中的功能。 首先,我们发现NF-κB活性需要与致癌Ras一起发挥作用,以有效保护乳腺上皮细胞免受TGF-β诱导的凋亡,这是这些细胞向侵袭性、转移性肿瘤表型进行EMT的先决条件。 其次,在缺乏TGF-β的情况下,NF-κB可以在Ras转化细胞中部分诱导EMT,这表明NF-kb B信号可以介导对诱导EMT至关重要的TGF-α信号的重要方面。 第三,NF-κB活性对细胞保持间充质状态是必要的,因为其抑制会导致EMT逆转; 最后,NF-κB信号对Ras转化的上皮细胞在体内的转移是必需的,这与其在体外调节肿瘤进展的至少这三个不同方面的基本作用是一致的。
NF-κB是肿瘤进展的不同方面所必需的。 我们观察到NF-κB的抗凋亡作用在晚期肿瘤发生(EMT)中起着关键作用,这与文献中的许多报道一致。 事实上,NF-κB正向调节过多的抗凋亡基因( 30 )在乳腺癌、前列腺癌、结直肠癌和卵巢癌以及某些形式的白血病和淋巴瘤中发现了构成性NF-κB活性(参考文献。 2 ). 在许多人类肿瘤衍生的细胞系中,包括霍奇金病的恶性Reed-Sternberg细胞,抑制NF-κB,诱导自发凋亡和/或使细胞对TNF-α或抗癌药物的杀伤敏感( 30 ). 一些研究表明,抑制NF-κB导致肿瘤细胞对癌症治疗的敏感性增加,即诱导凋亡。 例如,在小鼠异种移植模型中,将重组TD-IκBα传递到化疗耐药肿瘤,通过使其对拓扑异构酶I抑制剂CPT-11的化疗治疗敏感,从而诱导肿瘤退化( 31 , 32 ). 我们的结果清楚地确立了NF-κB作为EMT基因程序的重要调节器的关键作用,该调节器超越了其在细胞凋亡保护中的既定功能。 这是基于几条证据。 首先,NF-κB的激活足以在相当比例的上皮性EpRas细胞中诱导EMT。 其次,NF-κB的抑制导致EMT的阻断(在有效抑制细胞凋亡的条件下)。 第三,NF-κB是TGF-β诱导基因程序中内源性基因子集激活的关键因素。 最后,NF-κB阻断可以部分逆转EMT,从而产生存活的健康上皮细胞。
在这里,我们首次证明,据我们所知,NF-κB在Ras转化的乳腺上皮细胞EMT的诱导和维持中发挥因果作用,介导侵袭/转移肿瘤表型。 这些发现为NF-κB在晚期乳腺肿瘤发生和转移中的作用提供了机制上的见解。 我们关于NF-κB在未刺激的EpRas和EpRasXT细胞中可检测到或进一步升高的基线活性的观察结果,与证明乳腺癌中NF-κ子B因子组成性激活的报告一致( 33 , 34 ). 抑制诱导人乳腺癌细胞凋亡的NF-κB活性( 34 )或导致致瘤性降低( 35 ). 此外,小鼠乳腺肿瘤病毒 c-rel公司 –转基因小鼠发生不同组织学的迟发性乳腺肿瘤( 36 ). 有趣的是,Romieu-Mourez等人在研究中发现的一些肿瘤是梭形细胞癌,这是一种可能由EMT产生的肿瘤类型( 12 , 22 ).
最近的研究表明,NF-κB调节参与肿瘤扩散和转移的多个基因的表达,包括编码MMPs、, 白介素-8 , 血管内皮生长因子 、和 CXCR4系列 ( 37 , 38 ). 我们已经报道了在EpRas细胞EMT期间诱导的几个NF-κB靶基因,如编码各种MMPs和组织蛋白酶家族成员、趋化因子/细胞因子、tenascin-C等(见表 1 和图 三 E) ,可能有助于我们在研究中观察到的NF-κB依赖性转移能力。 在人前列腺癌细胞中也有报道通过阻断NF-κB活性抑制转移( 37 ),在人类黑色素瘤细胞中( 39 )和在小鼠肺泡癌细胞中( 40 ). 总之,我们的工作和其他人的工作清楚地表明了NF-κB信号在多肿瘤模型系统中肿瘤进展和转移的重要性。 然而,值得注意的是,虽然NF-κB在许多细胞类型中有助于肿瘤发生,但其在角质形成细胞中的IκBα介导的抑制最近被证明是Ras介导诱导类似鳞状细胞癌的侵袭性表皮肿瘤所必需的( 41 ). 然而,TGF-β信号通路在致瘤性Ras/IκBα肿瘤中的作用尚未得到研究。
NF-κB在肿瘤进展过程中Ras-和TGF-β依赖性信号通路的协同作用中的作用。 Janda等人之前的研究( 17 )在EpH4/EpRas模型中,使用Ras突变体,专门激活Raf/MEK/Erk途径(S35Ras)或PI3K/Akt途径(C40Ras),研究Ras信号通路对上皮可塑性的影响。 此外,阻断Ras、MEK1或PI3K的特异性抑制剂被用于干扰EpRas细胞中EMT的诱导或维持( 17 ). 这两种方法都表明,Raf/MEK/Erk通路的Ras依赖性信号与TGF-β信号结合是EMT所必需的( 17 ). 相反,C40诱导的PI3K/Akt信号通路保护EpH4细胞免受TGF-β诱导的凋亡,但未能诱导EMT。 在体内,只有能够激活Raf/MEK/Erk通路(S35Ras)的Ras突变体,而不是C40Ras突异体能够产生转移,这与这些突变体诱导EMT的潜力密切相关( 17 ). 许多报道表明,致癌Ras刺激NF-κB依赖性转录,并且NF-κB是Ras介导的转化所必需的(参考文献综述)。 1 ). 一些证据表明,NF-κB与PI3K/Akt共同作用于一条通路,导致抑制转化生长因子β诱导的Ras转化乳腺上皮细胞凋亡。 首先,在表达TD-IκBα的EpRas细胞和用特异性PI3K抑制剂处理的EpRas细胞中,TGF-β依赖性凋亡诱导率非常相似( 17 ). 其次,Akt已在几种细胞系统中被证明可以刺激上调NF-κB活性的信号通路。 重要的是,PDGF诱导的抗凋亡信号需要Akt诱导的NF-κB转录活性( 42 ). 一些报道表明,IKK活性与Akt刺激NF-κB转录活性的能力有关( 42 —— 44 )而其他人发现PI3K或Akt也可以通过靶向NF-κB p65亚单位的信号通路刺激NF-κ的B活性( 45 ). 我们的发现是,调节NF-κB活性在EpRas细胞和V12S35细胞中具有相同的作用,这与PI3K/Akt信号可能是NFκB活动上游的解释一致。 总之,需要进一步的实验来阐明NF-κB如何精确地介导EpRas细胞系统中的Ras依赖性效应。
我们观察到,TGF-β依赖性EMT诱导至少部分依赖于NF-κB活性,这提出了这些信号通路如何协作的问题。 如我们的研究所观察到的,TGF-β诱导NF-κB活性和靶基因转录与Arsura等人的观察结果一致( 28 )在肝上皮细胞中。 转化生长因子-β可以通过转化生长因子β1活化激酶1(TAK1)以Smad依赖的方式发出信号。 有趣的是,TAK1已被证明直接磷酸化IKK复合物以响应TGF-β治疗,促进NF-κB活化( 28 ). 此外,一些Smad蛋白作为TGF-β信号传导的主要应答者,可以通过与NF-κB亚单位的物理相互作用,通过κB位点刺激转录,从而发挥转录辅激活剂的作用( 46 ). 进一步分析这两条通路在何种水平上交叉,以消除TGF-β在诱导细胞凋亡中的经典功能,以及它们如何协同增强TGF-?在诱导EMT中的作用,将是非常重要的。 最近发现了一个潜在的新交叉点。 TGF-β通过Smad蛋白与FoxO转录因子协同作用的机制诱导细胞周期抑制剂p21CIP1的转录( 47 ). 已经描述了三种策略来克服这种细胞周期抑制。 第一种是Fox转录因子家族的另一个成员,即FoxG1对FoxO功能的抵消( 47 ). 第二种是通过PI3K/Akt途径使FoxO蛋白失活,导致FoxO蛋白质重新定位到细胞质( 48 ). 第三,在乳腺肿瘤中,已经观察到IKK-2的上调,并且IKK-2被证明可以直接磷酸化FoxO蛋白并在功能上使其失活( 49 ).
总之,我们的研究在体外/体内联合模型系统中对乳腺癌进展的几个方面对NF-κB的需求进行了功能解剖。 它确定NF-κB是EMT过程的关键调节器,EMT过程本身是转移的关键先决条件。 进一步明确NF-κB参与乳腺癌和其他恶性肿瘤侵袭和转移的机制将为药物研发提供重要靶点,这将为抗转移癌治疗带来新的治疗方法。
方法 细胞和细胞培养。 EpRas和EpRasXT细胞的起源和培养条件已在前面描述( 19 , 20 ). 前面描述了表达TD-IκBα、CA–IKK-2的φNX双嗜性逆转录病毒产生细胞和亲本载体的产生和培养条件,以及通过内部核糖体进入位点与GFP–zeocin抗性融合基因的表达耦合( 29 ).
用φNX产生细胞上清液逆转录病毒感染EpRas和EpRasXT细胞。 如前所述,EpRas和EpRasXT细胞被表达显性干扰突变体的亲本载体或逆转录病毒感染( 29 ). 简言之,在感染前24小时,将EpRas和EpRasXT细胞接种在6孔板中,密度为2×105个细胞/孔,将φNX细胞接种在密度为3×106个细胞/10-cm的板中。 对于感染,获取φNX细胞上清液,并通过0.45μm过滤器过滤,并向滤液中添加5μg/ml聚brene(Sigma-Aldrich,St.Louis,Missouri,USA)。 此后,从EpRas和EpRasXT细胞中取出培养基,并用含有逆转录病毒的φNX细胞上清液替换。 培养板在750℃下离心 克 2h后,去除上清液并用培养基替换。 然后,48小时后,通过荧光显微镜(Improvision,Heidelberg,Germany)监测感染效率,并用浓度为1500μg/ml(EpRas)和1700μg/ml的zeocin筛选感染细胞。
NF-κB分析。 如前所述,进行免疫印迹分析以监测显性干扰NF-κB突变体的蛋白表达水平( 29 )使用对IκBα(sc-371;Santa Cruz Biotechnology,Santa Cruz,California,USA)、IKK-2(sc-7607;Santa Cruz Biotechnology)和RelA(sc-372;Santa Cruz Biotechnology)特异性的抗体。
用EMSA测定NF-κB DNA结合活性。 采用“冻融”方法制备全细胞提取物,并按照前面所述进行EMSA( 29 ). 在所有情况下,将全细胞提取物与含有Igκ增强子共有NF-κB位点、八聚体特异性位点(5′-ATGAAAT-3′)或Sp-1特异性位点(5′-ATTCGATCGGCGGGGCGAGC-3′)的放射性标记的双链寡核苷酸在室温下孵育20分钟, 然后通过天然4%聚丙烯酰胺凝胶电泳从游离寡核苷酸中分离出形成的DNA蛋白复合物。
通过稳定转染EpRas和EpRasXT亲本和逆转录病毒转染的克隆以及3xκB荧光素酶报告子(3x kb B.luc)和β-珠蛋白-TATA,以及随后的荧光素素酶活性测定,测量NF-κB反式激活活性的调节。 简而言之,在单纯疱疹病毒胸苷激酶启动子的控制下,用10μg 3xκB.luc报告质粒和100 ng胸苷激酶Renilla荧光素酶报告子转染细胞。 通过在无血清培养基中以1:2.5的比例(lipofectamine 2000;Invitrogen,Carlsbad,California,USA)将DNA和脂质体混合物培养细胞4小时,进行转染。 在开始转染后的20–28小时,使用Lumat LB 9507光度计(德国巴德·威尔德巴德Berthold Technologies)测定荧光素酶活性。
半定量RT-PCR。 如前所述提取总RNA并进行半定量RT-PCR( 29 ). 鼠标 基质金属蛋白酶-13 用引物5′-CACTCCAAGGACCAGGCCC-3′(正)和5′-GCTGAGGGGCAGGCCAGAA-3′(反义;28个周期)扩增; 鼠标 MCP-1型 用引物5′-CGGCTGGAGCATCCACGTGTG-3′(正)和5′-GTCTGACTCCTTCTTGGG-3′扩增(反义;28个周期); 鼠标 胆囊收缩素 用引物5′-CGCAGCCGGTCCCTGCAGAA-3′(正)和5′-CACATCCCATAGTCCCGG-3′(反义;28个周期)扩增; 和小鼠β -肌动蛋白 用引物5′-GGTTCAGAAGACTCCTATGTG-3′(有义)和5′-AAGGCAACATGCACAGCTTC-3′(反义;28个循环)扩增。
多孔支架上生长细胞的标记分析。 细胞接种在多孔支架上(细胞培养插入物;孔径为0.4μm;BD,加利福尼亚州圣何塞,美国),EpRas细胞密度为0.5×105个细胞/孔,Ep拉斯特细胞密度为1×105个/孔。 在一些实验中,以指定的浓度培养细胞(见图 6 C) 广谱半胱天冬酶抑制剂Z-VAD-FMK(美国明尼苏达州明尼阿波利斯研发系统公司)。 每隔一天,每次更换培养基时都会提供新鲜抑制剂。 细胞培养5-7天,然后对其中一个细胞进行免疫荧光染色(参考文献中详细描述)。 17 )用多克隆兔抗E-钙粘蛋白(610182;1:500稀释;BD)、单克隆抗鼠波形蛋白(Vim-13.4;V-2258;1:500;Sigma-Aldrich)和Cy3-结合驴抗鼠IgG作为二级抗体(1:1000稀释;Jackson ImmunoResearch Laboratories),或在含有20 mM HEPES、25%甘油、, 0.42 M氯化钠,1.5 mM氯化镁 2 和0.2 mM EDTA,并使用E-cadherin、vimentin和RelA特异性抗体进行Western免疫印迹分析(如上所述)。 免疫荧光染色采用DAPI(0.1 ng/ml)进行核复染。 使用Metamorph软件(EpRas cells;Universal Imaging Corp.,Philadelphia,Pennsylvania,USA)在蔡司Axioplan 2(美国纽约州桑伍德蔡司)上使用MicroMAX相机(美国新泽西州特伦顿Roper Scientific)或荧光显微镜(Improvision)采集数字图像 使用OpenLab 3.0.2和3.0.3软件(EpRasXT单元;Improvision)。
胶原蛋白凝胶培养、标记物分析和凋亡检测。 如前所述,对EpRas细胞及其衍生物进行无血清三维培养( 17 , 19 ). 2-5天后将TGF-β1(5 ng/ml;R&D Systems)添加到培养物中,然后每隔一天与新鲜培养基一起提供,共5-7天。 如Janda等人所述,进行原位免疫荧光分析以分析E-cadherin和vimentin表达的三维结构( 17 ). 使用以下抗体:多克隆兔抗E-钙粘蛋白(610182;1:500稀释;BD)、单克隆抗小鼠波形蛋白(Vim-13.4;V-2258;1:500倍稀释;Sigma-Aldrich)和Cy3-结合山羊抗小鼠IgG作为二级抗体(1:3000稀释;Jackson ImmunoResearch Laboratories)。 在所有情况下,DAPI(0.1 ng/ml)用于核复染。
对于TUNEL分析,根据制造商的说明,将胶原蛋白凝胶固定在PBS中4%的多聚甲醛中,用PBS洗涤三次,并用原位细胞死亡检测试剂盒TMR红(2156792;美国印第安纳州印第安纳波利斯罗氏诊断公司)对凋亡细胞核进行染色。 DAPI(0.1 ng/ml)用于核复染。
使用Micromorph软件,在蔡司Axioplan 2上使用MicroMAX相机采集免疫荧光染色和TUNEL染色胶原凝胶的数字图像。 为了定量TUNEL测定,对每个胶原凝胶中至少三个区域的300多个细胞进行计数,并从两个胶原凝胶中测定平均凋亡指数。
膜联蛋白V染色。 表达TD-IκBα或空载体的XT细胞在孔径为0.4μm(BD)的细胞培养插入物上生长4天。 将细胞从过滤器上刮下,在冰冷的PBS中洗涤两次,并以1×106个细胞/ml的密度重悬于结合缓冲液(BD)中。然后,将1×105个细胞用5μl藻红蛋白偶联的膜联蛋白V(BD)染色15分钟,用PBS洗涤两次,并通过流式细胞术(FACSCalibur,BD)进行分析。
肿瘤发生和转移检测。 所有动物研究均已获得分子病理学研究所审查委员会的批准。 使用Athymic MF1裸鼠进行乳腺和尾静脉注射,6至10周龄雌性小鼠的乳腺注射用每20μl PBS有20万个细胞(肿瘤发生试验),尾静脉注射用每0.5 ml PBS有50万个细胞。
在肿瘤发生试验中,当对照动物的肿瘤直径达到约1.0–1.5 cm时(平均为乳腺注射后3周),或者如果肿瘤发生溃疡或小鼠表现出明显的发病率,则处死小鼠。 然后,将肿瘤切除并收集在PBS中,并测定每只动物的总肿瘤重量(从每只小鼠的四个注射部位)。
对于转移检测,每天检查小鼠体重减轻和呼吸困难情况,以检测大规模肺转移。 当对照组小鼠开始死于肺转移时(平均在尾静脉注射后3-4周),处死整个实验的小鼠。 肺被切除并收集在PBS中,并测定肺重量。
为了进行转移试验的组织学分析,在石蜡包埋和切片之前,将肺浸泡在10%中性缓冲福尔马林中。 对5μm厚的切片进行苏木精-伊红染色和组织学评估。 通过收集连续肺切片、选择相距约0.3 mm的切片以及计算转移病灶数来确定每个肺的转移总数,并校正出现在多个切片上的大转移病灶的影响。
致谢 我们感谢M.Jechlinger提供EpRas和EpRasXT细胞; B.Anic和G.Litos提供了出色的技术援助; K.Stangl和P.Garin-Chesa为组织学提供帮助; 分子病理研究所生物光学系支持免疫荧光显微镜; 以及K.Scharffetter-Kochanek、P.Petzlbauer、C.Hoeller、S.Maschler和M.Herlyn的科学讨论和有用评论。 这项工作的部分资金来自奥地利基因组研究(GEN-AU)项目(M.A.Huber)和德国科学基金会(DFG SFB497/B1 to B.Baumann;SFB451/A9 to T.Wirth)。
脚注
使用的非标准缩写: 苄氧羰基-Val-Ala-Asp-氟甲基酮(Z-VAD-FMK); 成分活性(CA); 电泳迁移率测定(EMSA); 上皮-间充质转化; IκB激酶(IKK); 抑制剂κB(IκB); NF-κB必需调节剂(NEMO); 转化生长因子-β1-活化激酶1(TAK1); 超显性(TD)。
工具书类
1 Orlowski RZ,Baldwin Jr.AS。NF-κB作为癌症的治疗靶点。 《2002年摩尔医学趋势》; 8:385–389. doi:10.1016/s1471-4914(02)02375-4。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
2 Karin M,Cao Y,Greten FR,Li ZW。癌症中的NF-κB:从无辜的旁观者到罪魁祸首。《国家癌症评论》。 2002; 2:301–310. doi:10.1038/nrc780。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
3 Ghosh S、May MJ、Kopp EB。 NF-κB和Rel蛋白:免疫反应的进化保守介质。 每年。 免疫学版。 1998年; 16:225–260. doi:10.1146/annurev.immuniol.16.1.225。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
4 Karin M,Ben-Neriah Y.磷酸化遇到泛素化:NF-κB活性的控制。 每年。 免疫学评论。 2000; 18:621–663. doi:10.1146/annurev.immuniol.18.1.621。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
5 Gilmore TD.多种突变有助于逆转录病毒癌蛋白v-Rel.癌基因的致癌性。 1999; 18:6925–6937. doi:10.1038/sj.onc.1203222。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
6 Cahir-McFarland ED、Izumi KM、Mosialos G.Epstein-Barr病毒转化:潜在膜蛋白1介导的NF-κB活化的参与。 致癌物。 1999; 18:6959–6964. doi:10.1038/sj.onc.1203217。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
7 太阳SC,巴拉德DW。 HTLV-1的tax转化蛋白对NF-κB的持续激活:劫持细胞IκB激酶。 致癌物。 1999; 18:6948–6958. doi:10.1038/sj.onc.1203220。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
8 Rayet B,Gelinas C.人类癌症中的异常rel/nfkb基因和活性。 致癌物。 1999; 18:6938–6947. doi:10.1038/sj.onc.1203221。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
9 Bargou RC等。构成核因子-κB-RelA激活是霍奇金病肿瘤细胞增殖和存活所必需的。 临床杂志。 投资。 1997; 100:2961–2969. doi:10.1172/JCI119849。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
10 Cabannes E、Khan G、Aillet F、Jarrett RF、Hay RT。霍奇金病中IκBα基因的突变表明IκBα具有肿瘤抑制作用。 致癌物。 1999; 18:3063–3070. doi:10.1038/sj.onc.1202893。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
11 Boyer B,Valles AM,Edme N.上皮-间充质转化的诱导和调节。 生物化学。 药理学。 2000; 60:1091–1099. doi:10.1016/s0006-2952(00)00427-5。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
12 Thiery JP。肿瘤进展中的上皮-间充质转变。 Nat.Rev.癌症。 2002; 2:442–454. doi:10.1038/nrc822。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
13 Thiery JP。发育和病理中的上皮-间充质转变。 货币。 操作。 细胞生物学。 2003; 15:740–746. doi:10.1016/j.ceb.2003.10006。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
14 Petersen OW等。人类乳腺癌中的上皮细胞向间充质细胞转化可以提供非恶性基质。 美国病理学杂志。 2003; 162:391–402。 doi:10.1016/S0002-9440(10)63834-5。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
15 Grünert S、Jechlinger M、Beug H。不同的细胞和分子机制有助于上皮的可塑性和转移。 自然修订版分子细胞生物学。 2003; 4:657–665。 doi:10.1038/nrm1175。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
16 Hay ED.上皮-间充质转化概述。 《安娜特学报》。 (巴塞尔)。 1995; 154:8–20. doi:10.1159/000147748。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
17 Janda E等。Ras和TGFβ协同调节上皮细胞可塑性和转移:Ras信号通路的分离。 《细胞生物学杂志》。 2002; 156:299–313. doi:10.1083/jcb.200109037。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
18 Jechlinger M等。肿瘤进展中上皮可塑性的表达谱。 致癌物。 2003; 22:7155–7169. doi:10.1038/sj.onc.1206887。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
19 Oft M等。TGF-β1和Ha-Ras协同调节上皮肿瘤细胞的表型可塑性和侵袭性。 基因发展1996; 10:2462–2477. doi:10.1101/gad.10.19.2462。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
20 Oft M,Heider KH,Beug H.TGFβ信号传导对癌细胞的侵袭和转移是必要的。 货币。 《生物》1998; 8:1243–1252. doi:10.1016/s0960-9822(07)00533-7。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
21 Lehmann K等。Raf诱导TGFβ生成,同时阻断其凋亡但非侵袭性反应:一种导致上皮细胞恶性程度增加的机制。 基因开发2000; 14:2610–2622. doi:10.1101/gad.181700。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
22 Oft M、Akhurst RJ、Balmain A.转移是由H-ras和Smad2水平的顺序升高驱动的。 自然细胞生物学。 2002; 4:487–494. doi:10.1038/ncb807。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
23 Gotzmann J等。通过TGF-β1和Ha-Ras的协同作用,肝细胞转化为成纤维细胞表型:向侵袭性迈进的步骤。 J.细胞。 科学。 2002; 115:1189–1202. doi:10.1242/jcs.115.6.1189。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
24 Dechend R等。Bcl-3癌蛋白在NF-κB/Rel和核共同调节因子之间起到桥梁作用。 致癌物。 1999; 18:3316–3323. doi:10.1038/sj.onc.1202717。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
25 Cogswell PC、Guttridge DC、Funkhouser WK、Baldwin Jr.AS。人类乳腺癌中NF-κB亚基的选择性激活:NF-κ的B2/p52和Bcl-3的潜在作用。 致癌物。 2000; 19:1123–1131. doi:10.1038/sj.onc.1203412。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
26 Adolph KW,Liska DJ,Bornstein P.人类血小板反应蛋白2基因(THBS2)启动子和转录起始位点的分析。 基因。 1997; 193:5–11. doi:10.1016/s0378-1119(97)00070-x。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
27 Pahl HL公司。 Rel/NF-κB转录因子的激活物和靶基因。 致癌物。 1999; 18:6853–6866。 doi:10.1038/sj.onc.1203239。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
28 Arsura M等。TGF-β1通过TAK1/IKK激酶途径瞬时激活NF-κB抑制AP-1/SMAD信号和凋亡:在肝肿瘤形成中的意义。 致癌物。 2003; 22:412–425. doi:10.1038/sj.onc.1206132。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
29 Huber MA等。IKK-2/IκBα/NF-κB通路在成纤维细胞CCR3和eotaxin-1的调节中起着关键作用。 IκBα缺陷小鼠皮炎的关键环节。 生物学杂志。 化学。 2002; 277:1268–1275. doi:10.1074/jbc。 M109358200。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
30 Kucharczak J,Simmons MJ,Fan Y,Gelinas C.生存与否:NF-κB是Rel/NF-κ·B调控细胞凋亡的答案。 致癌物。 2003; 22:8961–8982. doi:10.1038/sj.onc.1207230。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
31 Wang CY,Cusack Jr.JC,Liu R,Baldwin Jr.AS。诱导性耐药的控制:通过抑制NF-κB增加凋亡来增强抗肿瘤治疗。 《国家医学》,1999年; 5:412–417. doi:10.1038/7410。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
32 Cusack Jr.JC,Liu R,Baldwin Jr.AS。结直肠癌细胞对7-乙基-10-[4-(1-哌啶基)-1-哌啶基团]-羰基氧喜树碱(CPT-11)诱导的化学耐药性,异种移植模型通过抑制核因子-κB活化而被克服。 癌症研究2000; 60:2323–2330. [ 公共医学 ] [ 谷歌学者 ]
33 Nakshatri H、Bhat-Nakshatra P、Martin DA、Goulet Jr.RJ、Sledge Jr.GW。乳腺癌向激素依赖性生长发展过程中NF-κB的组成性激活。 分子细胞。 生物.1997; 17:3629–3639. doi:10.1128/mcb.17.7.3629。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
34 Sovak MA等。核因子-κB/Rel异常表达与乳腺癌发病机制。 临床杂志。 投资。 1997; 100:2952–2960. doi:10.1172/JCI119848。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
35 Romieu-Mourez R等。IKK激酶和蛋白激酶CK2在乳腺癌核因子-κB活化中的作用。 2001年癌症研究; 61:3810–3818. [ 公共医学 ] [ 谷歌学者 ]
36 Romieu-Mourez R等。小鼠乳腺肿瘤病毒c-rel转基因小鼠发生乳腺肿瘤。 分子细胞。 生物.2003; 23:5738–5754. doi:10.1128/MCB.23.16.5738-5754.2003。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
37 Huang S、Pettaway CA、Uehara H、Bucana CD、Fidler IJ。 阻断人前列腺癌细胞NF-κB活性与抑制血管生成、侵袭和转移相关。 致癌物。 2001; 20:4188–4197. doi:10.1038/sj.onc.1204535。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
38 Helbig G等。NF-κB通过诱导趋化因子受体CXCR4的表达促进乳腺癌细胞的迁移和转移。 生物学杂志。 化学。 2003; 278:21631–21638。 doi:10.1074/jbc。 M300609200。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
39 Huang S、DeGuzman A、Bucana CD、Fidler IJ。 核因子-κB活性与裸鼠中人类黑色素瘤细胞的生长、血管生成和转移相关。 临床。 癌症研究2000; 6:2573–2581. [ 公共医学 ] [ 谷歌学者 ]
40 Andela VB,Schwarz EM,Puzas JE,O'Keefe RJ,Rosier RN.肿瘤转移和核因子kappa B对促转移和抗转移因子的相互调节.癌症研究2000; 60:6557–6562. [ 公共医学 ] [ 谷歌学者 ]
41 Dajee M等。NF-κB阻断和致癌Ras触发侵袭性人类表皮瘤形成。 自然。 2003; 421:639–643. doi:10.1038/nature01283。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
42 罗马什科娃JA,马卡洛夫SS。 NF-κB是AKT在抗凋亡PDGF信号传导中的靶点。 自然。 1999; 401:86–90. doi:10.1038/43474。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
43 Kane LP,Shapiro VS,Stokoe D,Weiss A.通过Akt/PKB激酶诱导NF-κB。 货币。 生物学1999; 9:601–604. doi:10.1016/s0960-9822(99)80265-6。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
44 Ozes ON等。肿瘤坏死因子激活NF-κB需要Akt丝氨酸-三氢嘌呤激酶。 自然。 1999; 401:82–85. doi:10.1038/43466。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
45 Madrid LV、Mayo MW、Reuther JY、Baldwin Jr.AS.Akt通过利用IκB激酶和激活有丝分裂原活化蛋白激酶p38来刺激NF-κB的RelA/p65亚单位的反式激活潜能。 生物学杂志。 化学。 2001; 276:18934–18940. doi:10.1074/jbc。 M101103200。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
46 Lopez-Rovira T、Chalaux E、Rosa JL、Bartrons R、Ventura F。NF-κB与Smads的相互作用和功能合作。 junB启动子的转录调控。 生物学杂志。 化学。 2000; 275:28937–28946. doi:10.1074/jbc。 M909923199。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
47 Seoane J,Le H-V,Shen L,Anderson SA,Massague J。Smad和叉头通路在神经上皮和胶质母细胞瘤细胞增殖控制中的整合。 单元格。 2004年; 117:211–223. doi:10.1016/s0092-8674(04)00298-3。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
48 Brunet A等。Akt通过磷酸化和抑制叉头转录因子促进细胞存活。 单元格。 1999; 96:857–868. doi:10.1016/s0092-8674(00)80595-4。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
49 Hu MC-T等。IκB激酶通过抑制叉头FoxO3a促进肿瘤发生。 单元格。 2004年; 117:225–237. doi:10.1016/s0092-8674(04)00302-2。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
50 Lilienbaum A,Duc Dodon M,Alexandre C,Gazzolo L,Paulin D。人类T细胞白血病病毒I型tax蛋白对人类波形蛋白基因激活的影响。 J.维罗尔。 1990; 64:256–263. doi:10.1128/jvi.64.1.256-263.1990。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
51 Li X等人IKKα、IKKβ和NEMO/IKKγ均为NF-κB介导的炎症反应程序所需。 生物学杂志。 化学。 2002; 277:45129–45140. doi:10.1074/jbc。 M205165200。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
52 Katsel PL,Greenstein RJ。大鼠胆囊收缩素基因启动子上重叠AP-2/NF-κB反应元件的鉴定。 生物学杂志。 化学。 2001; 276:752–758. doi:10.1074/jbc。 M007553200。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
53 Ueda A等。NF-κB和Sp1调节人类单核细胞趋化蛋白-1基因的转录。 免疫学杂志。 1994; 153:2052–2063. [ 公共医学 ] [ 谷歌学者 ]
54 Liacini A等。关节软骨细胞中MAP激酶、AP-1和NF-κB转录因子介导TNF-α诱导基质金属蛋白酶-13基因表达。 实验细胞研究2003; 288:208–217. doi:10.1016/s0014-4827(03)00180-0。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
55 Mettouchi A等。c-Jun诱导的转化过程涉及tenascin-c表达的复杂调控。 分子细胞。 生物学1997; 17:3202–3209. doi:10.1128/mcb.17.6.3202。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
56 田斌,Brasier AR。核因子κB依赖性基因网络的鉴定。最新进展。 霍姆。 2003年决议; 58:95–130. doi:10.1210/rp.58.1.95。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
57 Philip S、Bulbule A、Kundou GC。 骨桥蛋白通过核因子-κB介导诱导小鼠黑色素瘤细胞膜型1基质金属蛋白酶,刺激肿瘤生长和前基质金属蛋白酶-2的激活。 生物学杂志。 化学。 2001; 276:44926–44935. doi:10.1074/jbc。 M103334200。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
58 Israel A等。TNF通过诱导NF-κB样增强子结合活性来取代构成因子,从而刺激小鼠MHC I类基因的表达。 EMBO J.1989; 8:3793–3800. doi:10.1002/j.1460-2075.1989.tb08556.x。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
59 Israel A,Yano O,Logeat F,Kieran M,Kourilsky P。两种纯化因子与小鼠MHCⅠ类基因增强子中的相同序列结合:其中一种是诱导畸胎瘤细胞分化的阳性调节因子。 核酸研究1989; 17:5245–5257. doi:10.1093/nar/17.13.5245。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
60 Bitko V,Velazquez A,Yang L,Yang YC,Barik S.人类呼吸道合胞病毒对多种细胞因子的转录诱导需要NF-κB的激活,并被水杨酸钠和阿司匹林抑制。病毒学。 1997; 232:369–378. doi:10.1006/viro.1997.8582。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
61 Ohmori Y、Fukumoto S、Hamilton TA。 两个结构不同的kappa B序列基序协同控制LPS诱导的小鼠巨噬细胞KC基因转录。 免疫学杂志。 1995; 155:3593–3600。 [ 公共医学 ] [ 谷歌学者 ]
关联数据 本节收集本文中包含的任何数据引用、数据可用性声明或补充材料。