介绍 动脉粥样硬化是一种渐进性疾病,由血管树中受到血流紊乱和许多系统因素(包括高脂血症、吸烟和糖尿病)影响的区域的生物力学力量引发( 1 , 2 ). 随着时间的推移,血管壁对脂质的吸收导致动脉粥样硬化斑块的逐渐积聚。 一旦形成,斑块继续扩大,导致管腔直径逐渐受限,血流受到影响。 在某些情况下,斑块破裂会导致血管内血栓形成,从而导致动脉血供完全和突然中断。 斑块的积聚、生长和破裂都与全身和血管壁炎症有关( 三 – 5 ). 尽管有大量数据表明血管壁炎症与动脉粥样硬化进展有关,但炎症诱导动脉粥样硬化疾病进展的机制仍不清楚( 4 )虽然通过抗炎治疗阻止疾病进展的努力在临床试验中失败了( 三 ).
最近的研究表明,内皮-间充质转化(EndMT)在许多与炎症相关的病理条件中的发生率很高,例如心肌梗死( 6 ),脑海绵状畸形( 7 ),门脉高压( 8 ),肺动脉高压( 9 )和血管移植失败( 10 , 11 )除其他外。 EndMT的特征是正常内皮细胞(EC)表型发生变化,呈现间充质细胞(成纤维细胞、平滑肌细胞[SMCs])的形状和特性,包括增殖和迁移增强; 分泌细胞外基质蛋白,如纤维连接蛋白和胶原; 以及各种白细胞粘附分子的表达。
TGF-β已被确定为推动EndMT进展的核心因素( 12 , 13 )但导致其信号激活的过程仍不明确。 我们以前曾报道过,通过敲除关键细胞内信号介质FGF受体底物2α(FRS2α)诱导内皮细胞FGF介导的信号转导减少( 10 )或内皮中的主要FGF受体(FGF受体1[FGFR1])( 14 )激活TGF-β信号传导,导致EndMT。
FGFR1生物学的不寻常特征是,FGFR1在内皮细胞中的表达受到某些炎症刺激的影响,包括IFN-γ、TNF-α和IL-1β,这些炎症刺激诱导其表达显著降低( 10 ). 由于这些正是动脉粥样硬化斑块中发现的炎症介质,我们开始研究EndMT在动脉粥样硬化中的发生和作用。
细胞培养和小鼠模型的研究表明,振荡流体剪切应力和可溶性炎症介质均降低FGFR1的表达和信号传导,并促进TGF-β信号和EndMT。 此外,对人类冠状动脉的分析表明,内皮细胞FGFR1的表达、TGF-β信号的增加以及EndMT的出现与动脉粥样硬化的严重程度之间存在着强烈的相关性。 总之,这些发现指出了生物力学和可溶性炎症刺激减少保护性内皮细胞FGFR1信号从而驱动EndMT和动脉粥样硬化斑块进展的机制。
结果 炎症细胞因子、剪切应力和EndMT。 炎症和剪切应力在动脉粥样硬化病变的发展和进展中起着重要作用。 先前的研究已确定FGFR1表达是TGF-β诱导的EndMT的关键调节因子( 14 )并证明某些炎症细胞因子可以降低FGFR1水平,从而减少FGF信号( 10 ). 为了测试FGF信号、FGFR1表达和细胞因子的减少程度之间的联系,我们首先研究了FGFR1或其关键细胞内信号介质FRS2α表达的减少、TGF-β信号的激活和EndMT的出现之间的关系。 当暴露于递增剂量的FGFR1或FRS2αshRNA-编码慢病毒时,HUVEC表现出靶基因表达的剂量依赖性下降,TGF-β信号转导介质SMAD2(p-SMAD2)的磷酸化增加,以及EndMT标记物胶原蛋白1、波形蛋白和SM22α的出现( 补充图1 ; 见补充材料中完整的未经编辑的斑点; 本文的在线补充材料; 数字对象标识: 2017年10月17日/JCI82719DS1 ).
接下来用增加浓度的IFN-γ、TNF-α或IL-1β处理HUVECs。 所有3种细胞因子均诱导FGFR1表达减少和EndMT标记物增加( 补充图2 ; 见补充材料中完整的未经编辑的印迹),与上述shRNA-介导的FGF信号抑制观察到的结果类似。 为了更全面地描述这种反应,用3种细胞因子的最佳剂量单独或联合治疗HUVEC。 联合使用IFN-γ、TNF-α和IL-1β时,细胞因子诱导的FGFR1表达减少最为显著( 补充图3B ; 请参阅补充材料中完整的未经编辑的斑点)。 就其本身而言,这些细胞因子均未诱导血管内皮细胞钙粘蛋白(VE-cadherin)或VEGFR2等内皮标志物的表达减少。 然而,细胞因子组合大大降低了这些蛋白的表达( 补充图3B ; 请参阅补充材料中完整的未经编辑的斑点)。 同样,当3种细胞因子中的任何2种存在时,作为EndMT诱导的关键步骤,TGF-β受体1(TGF-?1)表达的增加最为显著( 补充图3A ). 最后,体外诱导EC中的EndMT导致间充质标志物(ZEB2、SLUG、SNAIL、波形蛋白和胶原1)、平滑肌标志物(SM22α)、白细胞粘附分子(ICAM-1和VCAM-1)、单核细胞趋化蛋白1(MCP-1)和促炎蛋白纤溶酶原激活物抑制物-1(PAI-1)显著上调 以及保护性蛋白内皮NOS(eNOS)的丧失( 补充图3B ; 请参阅补充材料中完整的未经编辑的斑点)。 有趣的是,IFN-γ、TNF-α或IL-1β治疗并不影响原发性人类SMC中FGFR1的表达( 补充图4、B和D ; 请参阅补充材料中完整的未经编辑的斑点)。
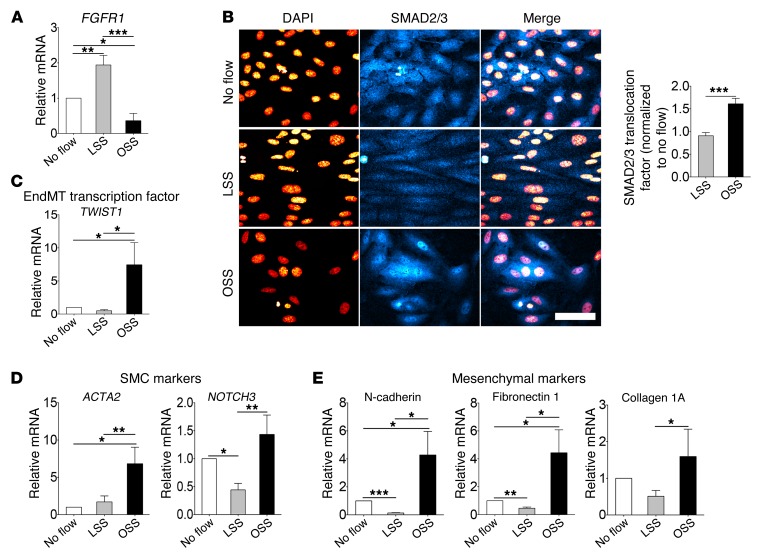
动脉粥样硬化斑块优先发生在以振荡剪切应力(OSS)为特征的动脉区域,而高层流剪切应力则具有动脉粥样硬化保护作用。 因此,我们研究了OSS和LSS对HUVEC中FGFR1表达和TGF-β信号转导的影响。 当暴露在16小时的OSS中时,HUVEC表现出显著降低 FGFR1号机组 表达,而暴露于LSS的类似时间增加了表达( 图1A ). SMAD2/3染色显示这些蛋白向暴露于OSS的HUVEC细胞核的易位增加,而不是LSS,这一发现与OSS激活TGF-β信号一致( 图1B ). 此外,OSS(而非LSS)诱导转录因子mRNA水平显著增加 扭转1 ( 图1C ),据报道与TGF-β信号传导有关( 11 , 15 ). 与EndMT程序的激活一致,SMC标记的表达增加( ACTA2公司 ,编码平滑肌α-肌动蛋白,以及 槽口3 ) ( 图1D )和间充质标记物(N-钙粘蛋白、纤维连接蛋白1和胶原1A)( 图1E ).
图1。 体外剪切应力下调FGFR1表达并上调TGF-β信号转导。
( A类 和 B类 )HUVEC受到12达因/cm的影响 2 LSS或1±4达因/厘米 2 OSS持续16小时。 FGFR1号机组 通过以下方法检测SMAD2/3的表达和核转位( A类 )qRT-PCR和( B类 )免疫荧光染色。 qRT-PCR结果的条形图代表了4个独立实验(* 对 <0.05** 对 < 0.01; *** 对 < 0.001; 使用Newman-Keuls事后检验进行多重比较校正的单因素方差分析)。 SMAD2/3核转位图像代表了3个独立实验(*** 对 < 0.001; 未配对双尾学生的 t吨 测试)。 比例尺:50μm。 ( C类 – E类 )HUVEC受到12达因/cm的影响 2 LSS或1±4达因/厘米 2 OSS持续48小时。 用qRT-PCR检测EndMT标记基因的表达。 qRT-PCR结果的条形图代表了4个独立实验(* 对 <0.05** 对 < 0.01; 使用Newman-Keuls事后检验进行多重比较校正的单因素方差分析)。
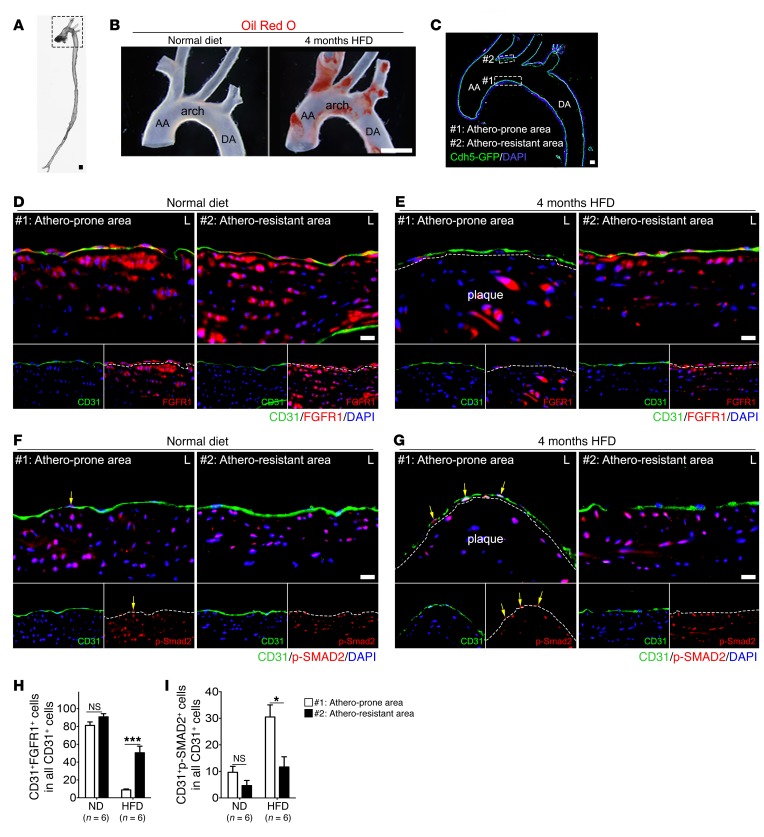
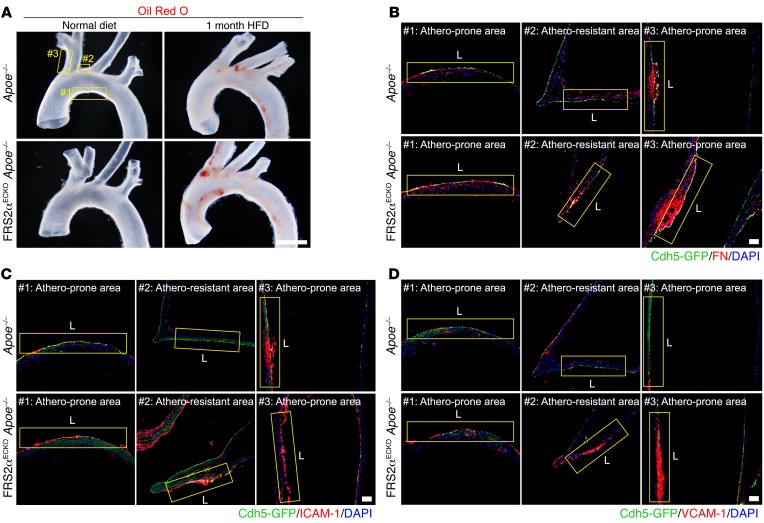
动脉血管树的某些部位存在扰动剪应力,例如主动脉弓和分支起源部位的较小曲率,而其他部位存在保护动脉粥样硬化的线性剪应力(包括主动脉弓的较大曲率)( 图2,A–C ). 事实上,经过4个月的高脂肪饮食(HFD), 阿波 –/– 小鼠在动脉粥样硬化区有广泛的病变,但在动脉粥样硬化保护区没有( 图2B ). 正常饮食小鼠主动脉切片的免疫细胞化学检查显示内皮细胞FGFR1的表达没有任何差异( 图2、D和H )或p-SMAD2水平( 图2、F和I )在动脉粥样硬化和动脉粥样硬化保护区之间。 然而,HFD 4个月后,与动脉粥样硬化保护的内皮相比,动脉粥样硬化内皮中FGFR1的表达显著降低,p-SMAD2水平显著升高( 图2,E和G–I ).
图2。 剪切应力下调体内FGFR1的表达,上调TGF-β信号转导。
( A类 )整个小鼠主动脉。 比例尺:1 mm( B类 )油红O染色主动脉弓断面的代表性显微照片 阿波 –/– 正常饮食16周后的小鼠( n个 =3)或HFD( n个 = 3). 比例尺:4 mm( C类 )高倍图像 A类 纵切面显示主动脉弓。 AA,升主动脉; DA,降主动脉。 比例尺:160μm。 ( D类 – G公司 )主动脉弓CD31(绿色)、FGFR1(红色)和p-SMAD2(红色)的免疫荧光染色 阿波 –/– 正常饮食16周后的小鼠( n个 =6)或HFD( n个 = 6). 动脉粥样硬化预防区用#1表示,而动脉粥样硬化抵抗区用#2表示。 黄色箭头表示EC表达p-SMAD2。 细胞核用DAPI(蓝色)染色。 L、 管腔。 比例尺:10μm。 ( H(H) 和 我 )表达FGFR1和p-SMAD2的管腔EC数量的量化(NS,与#1相比不显著* 对 与#1相比<0.05*** 对 与#1相比<0.001; 未配对双尾学生的 t吨 测试)。
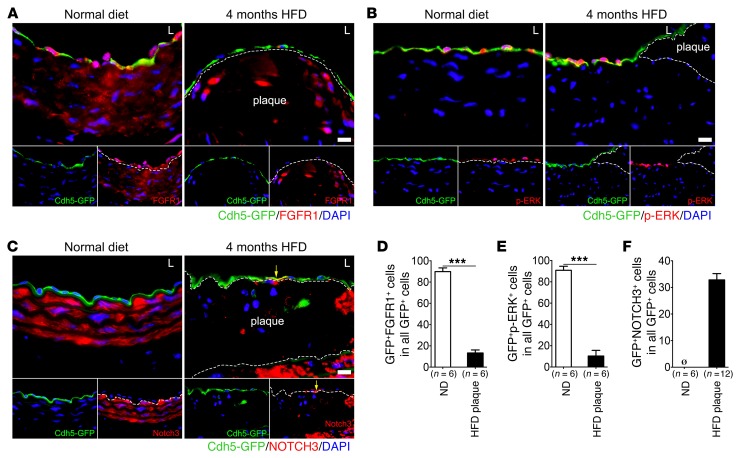
EndMT在小鼠动脉粥样硬化中的作用。 为了建立内皮细胞FGF信号缺失与动脉粥样硬化之间的因果关系,我们接下来研究了HFD对内皮细胞命运图中内皮细胞的影响 毫吨/毫克 记者 阿波 –/– 老鼠( Cdhr5-CreER公司 T2段 mT/mG载脂蛋白 –/– 老鼠)。 16周的HFD导致管腔EC中FGFR1的表达显著降低( 图3,A和D ). 为了检测FGFR1水平降低对功能的影响,对正常饮食和HFD的小鼠全身注射FGF2。 FGF2注射15分钟后主动脉中p-ERK表达的免疫细胞化学分析表明,与正常饮食小鼠血管段正常内皮细胞相比,斑块中p-ERK的表达显著减少( 图3、B和E ). 与内皮FGF信号的减少一致,在HFD小鼠中,超过三分之一的管腔内皮细胞表达EndMT标记物NOTCH3,而在维持正常饮食的小鼠中,这种标记物几乎不存在( 图3、C和F ).
图3。 小鼠动脉粥样硬化模型中FGF信号活性和EndMT程度。
( A类 )大鼠主动脉FGFR1的免疫荧光染色 Cdh5-CreER公司 T2段 mT/mG载脂蛋白 –/– 小鼠(每组6只)。 比例尺:10μm。 ( B类 ) Cdh5-CreER公司 T2段 mT/mG载脂蛋白 –/– HFD治疗16周后的小鼠( n个 =6)或正常饮食( n个 =6)静脉注射FGF2(每只小鼠1μg),通过免疫荧光染色测定p-ERK激活。 比例尺:10μm。 ( C类 )主动脉和斑块切片中NOTCH3的免疫荧光染色 Cdh5-CreER公司 T2段 mT/mG载脂蛋白 –/– 小鼠(正常饮食, n个 = 6; HFD、, n个 = 12). 比例尺:10μm。 ( D类 – F类 )表达FGFR1、p-ERK和NOTCH3的管腔内皮细胞数量的量化(*** 对 与正常饮食相比<0.001; 未配对双尾学生的 t吨 测试)。 黄色箭头表示表示NOTCH3的EC。 Ø,未检测到。
为了进一步研究内皮细胞FGF信号在动脉粥样硬化病变发展中的作用,我们制作了内皮细胞命运定位基因编码pan-FGFR适配器分子FRS2α的可诱导内皮特异性缺失的小鼠 阿波 –/– 背景使用 Cdh5-CreER公司 T2段 驾驶员( 16 ). Cdh5-CreER公司 T2段 毫吨/毫克 小鼠与 Frs2a公司 飞行/飞行 鼠标,生成 Cdh5-CreER公司 T2段 mT/mG Frs2a 飞行/飞行 线路(此处指定为FRS2α ECKO公司 老鼠)。 然后将这些老鼠交给 阿波 –/– 背景,生成 Cdh5-CreER公司 T2段 mT/mG载脂蛋白 –/– Frs2a公司 飞行/飞行 小鼠(FRS2α ECKO公司 阿波 –/– 老鼠)和 Cdh5-CreER公司 T2段 mT/mG载脂蛋白 –/– Frs2a公司 佛罗里达州/+ 室友控制( 补充图5A ). 出生后注射三苯氧胺,FRS2α的命运定位和FRS2β切除效率 ECKO公司 阿波 –/– 小鼠主动脉免疫细胞化学检测( 补充图5B )和蛋白质印迹( 补充图5C ; 请参阅补充材料中完整的未经编辑的斑点)。 FRS2α中的体重、总胆固醇、甘油三酯和高密度脂蛋白胆固醇水平 ECKO公司 阿波 –/– 小鼠与 阿波 –/– HFD 16周前后的小鼠( 补充图5、D和E ).
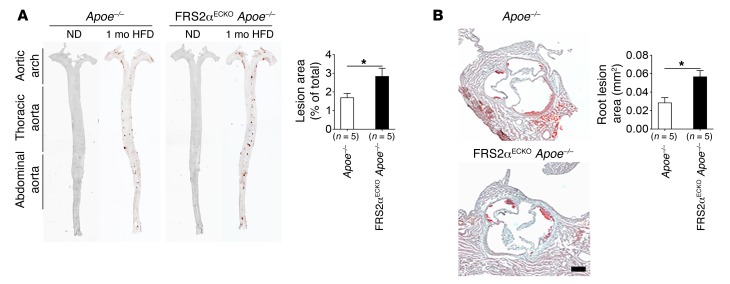
HFD 4周后对主动脉弓、胸主动脉、腹主动脉和主动脉根部的检查显示FRS2α中有更广泛的动脉粥样硬化病变 ECKO公司 阿波 –/– 小鼠与 阿波 –/– 老鼠( 图4 ). 此外,FRS2α ECKO公司 阿波 –/– 主动脉显示动脉粥样硬化斑块病变增加,纤维连接蛋白沉积,ICAM-1和VCAM-1在动脉粥样硬化易感区和抵抗区的表达升高,这在 阿波 –/– 老鼠( 图5 ).
图4。 内皮FGF信号抑制对HFD 4周后小鼠动脉粥样硬化的影响。
阿波 –/– 和FRS2α ECKO公司 阿波 –/– 将小鼠置于HFD上,4周后进行检查。 ( A类 )主动脉显微照片 阿波 –/– 和FRS2α ECKO公司 阿波 –/– 12周龄的小鼠在用油红O染色后进行面部准备(每组5只小鼠)并量化损伤面积。 所有数据显示为平均值±SD(* 对 与相比<0.05 阿波 –/– ; 未配对双尾学生的 t吨 测试)。 ( B类 )油红O染色主动脉根部横截面的代表性示例(每组5只小鼠)和主动脉根部病变区域的量化。 比例尺:200μm。 平均值±标准差(* 对 与相比<0.05 阿波 –/– ; 未配对双尾学生的 t吨 测试)。
图5。 FRS2α动脉粥样硬化的早期发病 ECKO公司 阿波 –/– 老鼠。
阿波 –/– 和FRS2α ECKO公司 阿波 –/– 将小鼠置于HFD上,4周后进行检查。 ( A类 )HFD 4周前后主动脉弓油红O染色动脉粥样硬化病变的代表性显微照片(每组5只小鼠)# 1和#3表示动脉粥样硬化预防区,而#2表示动脉粥样硬化抵抗区。 比例尺:4 mm( B类 – D类 )Fibronectin(FN)、ICAM-1和VCAM-1区域的纵向截面对应于来自 A类 在里面 阿波 –/– 和FRS2α ECKO公司 阿波 –/– 小鼠(每组5只)。 细胞核用DAPI(蓝色)染色。 比例尺:16μm。
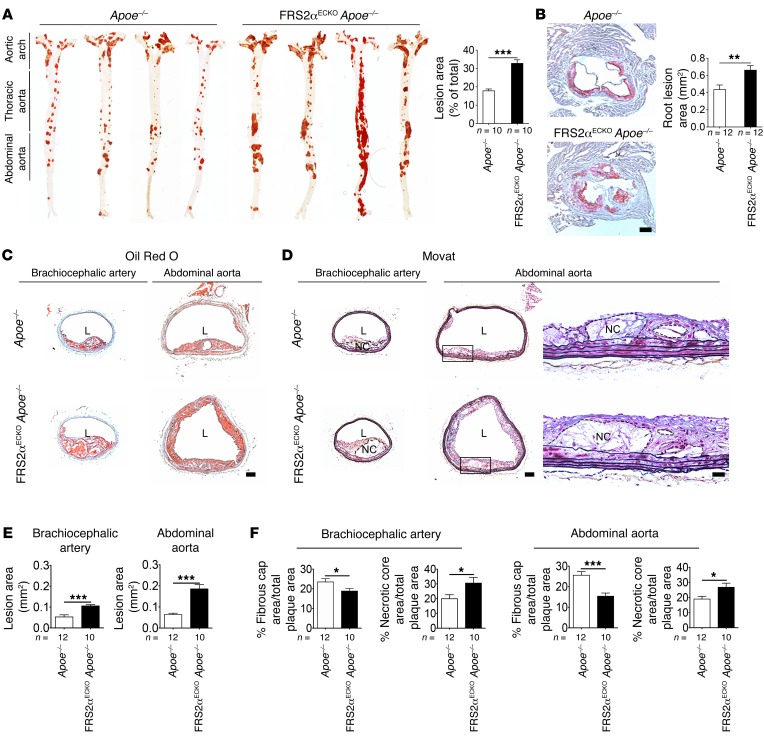
HFD 16周后,FRS2α ECKO公司 阿波 –/– 小鼠出现广泛的动脉粥样硬化斑块,累及主动脉弓、胸主动脉和腹主动脉、主动脉根部和头臂动脉( 图6,A–C ). 主动脉中的总斑块负荷比 阿波 –/– 小鼠(17.82% 阿波 –/– FRS2α中为32.79% ECKO公司 阿波 –/– ) ( 图6A ). 主动脉根部、头臂动脉和腹主动脉的病变面积增加同样显著( 图6、B、C和E ). 对腹主动脉的组织学检查显示,双基因敲除动物的腹主动脉环周斑块非常广泛,覆盖了正常情况下从未观察到的抗动脉粥样硬化区域 阿波 –/– 老鼠( 图6D ). 此外,坏死核心的尺寸显著增加,纤维帽的尺寸减小( 图6、D和F ),具有脆弱斑块的典型特征。
图6。 内皮FGF信号抑制对HFD 4个月后小鼠动脉粥样硬化的影响。
( A类 )主动脉显微照片 阿波 –/– 和FRS2α ECKO公司 阿波 –/– 小鼠(24周龄)在4个月HFD后,用油红O染色并量化损伤区域后,在面部准备中(每组10只小鼠)。 所有数据显示为平均值±SD(*** 对 <0.001与 阿波 –/– ; 未配对双尾学生的 t吨 测试)。 ( B类 )用油红O染色的主动脉根部横截面的代表性示例和主动脉根部病变面积的量化(每组12只小鼠)。 比例尺:200μm。 平均值±标准偏差(** 对 与相比<0.01 阿波 –/– ; 未配对双尾学生的 t吨 测试)。 ( C类 和 D类 )油红O型或运动染色的头臂动脉和腹主动脉的代表性图像 阿波 –/– 和FRS2α ECKO公司 阿波 –/– 老鼠( 阿波 –/– 老鼠, n个 = 12; FRS2α ECKO公司 阿波 –/– 老鼠, n个 = 10). 比例尺:100μm。 方框区域显示的病变的高放大率图像显示在右侧。 比例尺:50μm。 NC,坏死核心。 注意FRS2α中的周向斑块 ECKO公司 阿波 –/– 老鼠。 ( E类 )病变面积测量(*** 对 <0.001与 阿波 –/– ; 未配对双尾学生的 t吨 测试)。 ( F类 )头臂动脉和腹主动脉纤维帽和坏死区范围的量化 坡(poe) –/– 和FRS2α ECKO公司 阿波 –/– 老鼠(* 对 <0.05*** 对 <0.001与 阿波 –/– ; 未配对双尾学生的 t吨 测试)。
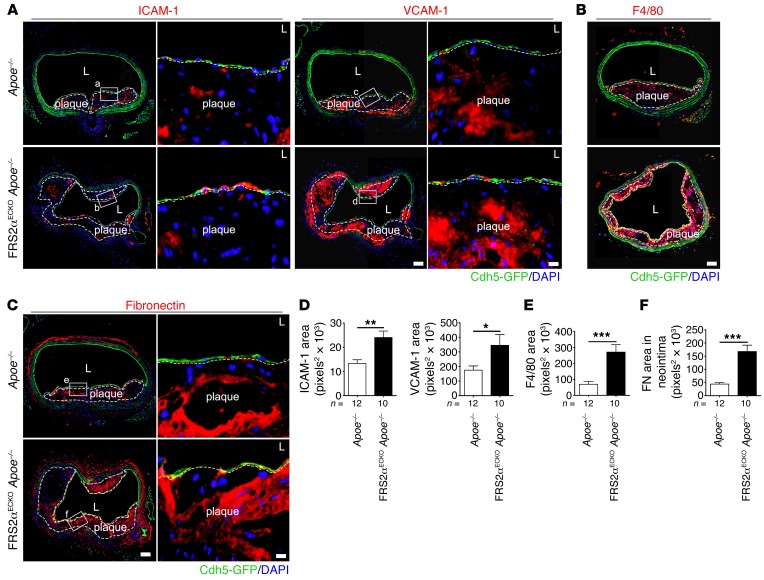
免疫细胞化学显示ICAM-1和VCAM-1的广泛周向表达以及单核细胞/巨噬细胞的募集( 图7、A、B、D和E ). 此外,FRS2α的动脉粥样硬化病变 ECKO公司 阿波 –/– 小鼠的TGF-β信号激活(p-SMAD2)、平滑肌α-actin和NOTCH3表达以及大量胶原和纤维连接蛋白沉积被强烈染色( 补充图6 和 图7、C和F ),EndMT的所有标记。 头臂动脉检查也有类似结果( 补充图7 ).
图7。 内皮细胞FGF信号抑制对小鼠炎症和EndMT标记基因表达的影响。
( A类 – C类 )用抗ICAM-1、抗VCAM-1、F4/80和抗纤维连接蛋白抗体对动脉粥样硬化斑块进行组织学分析( 阿波 –/– 老鼠, n个 = 12; FRS2α ECKO公司 阿波 –/– 老鼠, n个 = 10). 注意FRS2α中的周向斑块 ECKO公司 阿波 –/– 老鼠。 细胞核用DAPI(蓝色)复染。 比例尺:62μm(低倍图像); 10μm(高倍图像)。 方框区域的高分辨率图像显示在右侧。 ( D类 – F类 )F4/80、ICAM-1、VCAM-1和纤维连接蛋白面积的测量(* 对 <0.05** 对 < 0.01; *** 对 <0.001与 阿波 –/– ; 未配对双尾学生的 t吨 测试)。
EndMT在人类动脉粥样硬化中的作用。 为了研究人类动脉粥样硬化中的EndMT,使用免疫荧光显微镜检查左冠状动脉主干( 补充图8A )冠状动脉正常(定义为无新生内膜)、轻度冠状动脉疾病(CAD)(内膜-中膜[I/M]比值,<0.2,I级斑块)、中度CAD(I/M比值,0.2-1.0,II级斑块)或重度CAD(I/M>1.0,III级和IV级斑块)患者中( 补充图8B ).
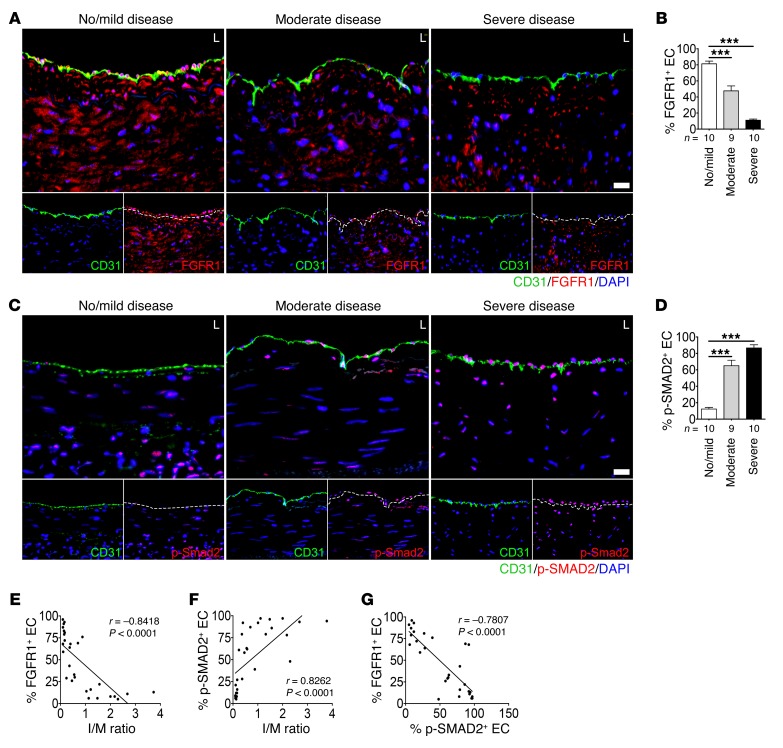
无/轻度CAD患者81%的管腔内皮细胞显示FGFR1表达,而中度CAD患者下降至管腔内皮的47.6%,重度CAD患者下降到11.1%( 图8,A和B ). 在相同的样本中,p-SMAD2是TGF-β信号传导激活的标志物,随着疾病的严重程度而逐渐增加( 图8、C和D ). I/M比率与表达FGFR1的内皮细胞数量之间存在强烈的反线性关系( 第页 = –0.84, 对 < 0.0001 图8E )与表达p-SMAD2的内皮细胞数量呈同样强的正相关( 第页 = 0.83, 对 < 0.0001, 图8F ). 最后,FGFR1表达与TGF-β信号转导呈负相关( 第页 =–0.78, 对 < 0.0001, 图8G ).
图8。 人冠状动脉内皮细胞FGFR1表达和SMAD2磷酸化。
免疫细胞化学分析( A类 )FGFR1和( C类 )p-SMAD2在无/轻度冠心病患者左主干内皮细胞中的表达( n个 =10),中等( n个 =9),严重( n个 =10)CAD。 CD31(绿色)和FGFR1(红色)或p-SMAD2(红色)免疫荧光染色的代表性图像。 细胞核用DAPI(蓝色)染色。 比例尺:16μm。 ( B类 和 D类 )FGFR1的百分比 + EC或p-SMAD2 + 管腔中的EC(*** 对 <0.001,与无/轻度疾病相比; 使用Newman-Keuls事后检验进行多重比较校正的单因素方差分析)。 ( E类 和 F类 )FGFR1或p-SMAD2和I/M比率的散点图。 相应的斯皮尔曼相关系数( 第页 )FGFR1或p-SMAD2与I/M比和 对 显示值。 ( G公司 )FGFR1和p-SMAD2散点图。 相应的斯皮尔曼相关系数( 第页 )FGFR1和p-SMAD2与 对 显示值。
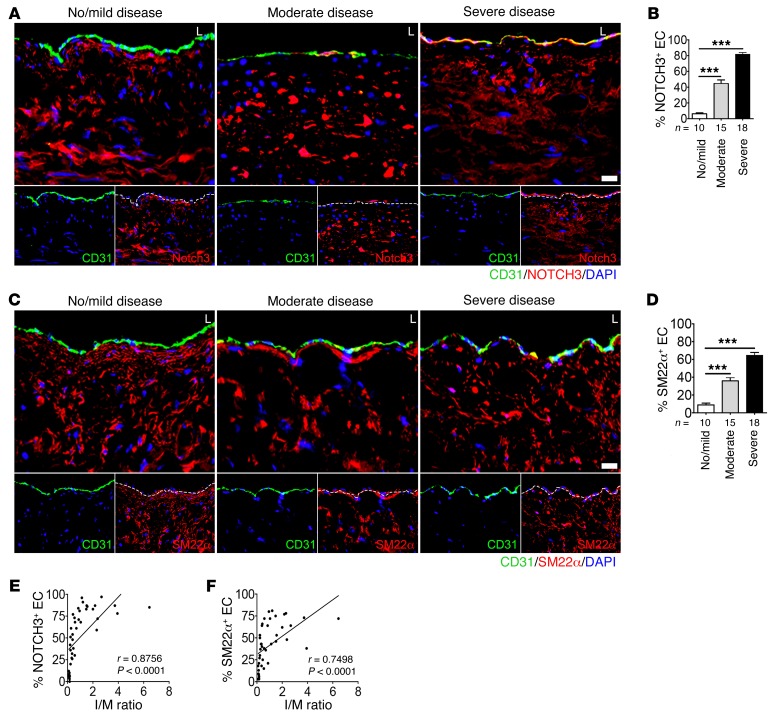
接下来,我们在该患者队列中检测了EndMT标记物NOTCH3和SM22α。 虽然在没有疾病的情况下,基本上没有管腔冠状动脉内皮细胞表达这些蛋白,但随着疾病的严重程度,其患病率显著增加,严重CAD患者左主干的几乎所有内皮细胞都显示出强染色( 图9,A–D ). 对整个患者队列的定量分析表明,当转化内皮细胞的患病率接近35%时,表达NOTCH3和SM22α的内皮细胞数量与I/M比率之间有很强的相关性( 第页 分别=0.88和0.75; 对 < 0.0001, 图9,E和F ).
图9。 平滑肌标记物在人冠状动脉内皮中的表达。
无/轻度患者的左主冠状动脉( n个 =10),中等( n个 =15),严重( n个 =18)评估CAD。 ( A类 和 C类 )左主冠状动脉CD31(绿色)、NOTCH3(红色)和SM22α(红色)免疫荧光染色的代表性图像。 细胞核用DAPI(蓝色)染色。 比例尺:16μm。 ( B类 和 D类 )NOTCH3的百分比 + EC或SM22α + 管腔中的EC(*** 对 <0.001,与无/轻度疾病相比; 使用Newman-Keuls事后检验进行多重比较校正的单因素方差分析)。 ( E类 和 F类 )NOTCH3散点图 + EC或SM22α + 管腔中的EC和I/M比率。 相应的斯皮尔曼相关系数( 第页 )NOTCH3之间 + EC或SM22α + 管腔内皮细胞和I/M比率以及 对 显示值。
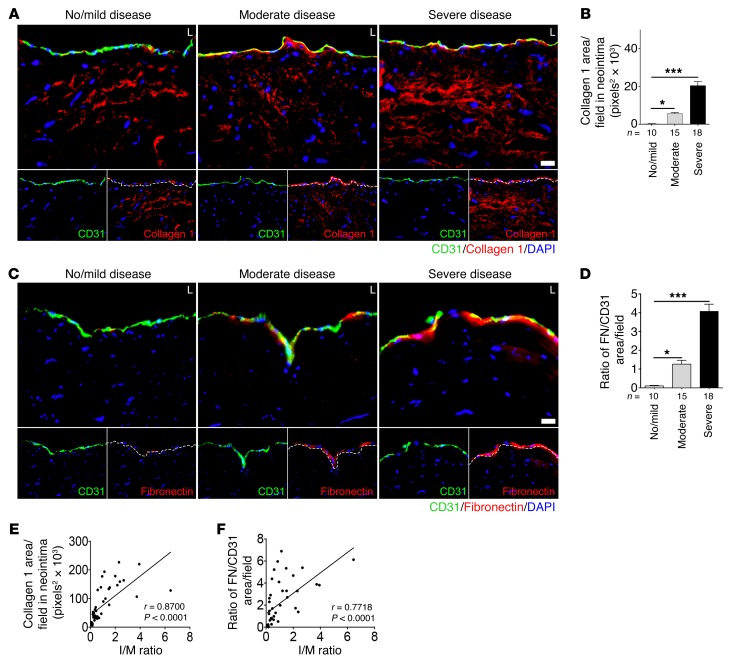
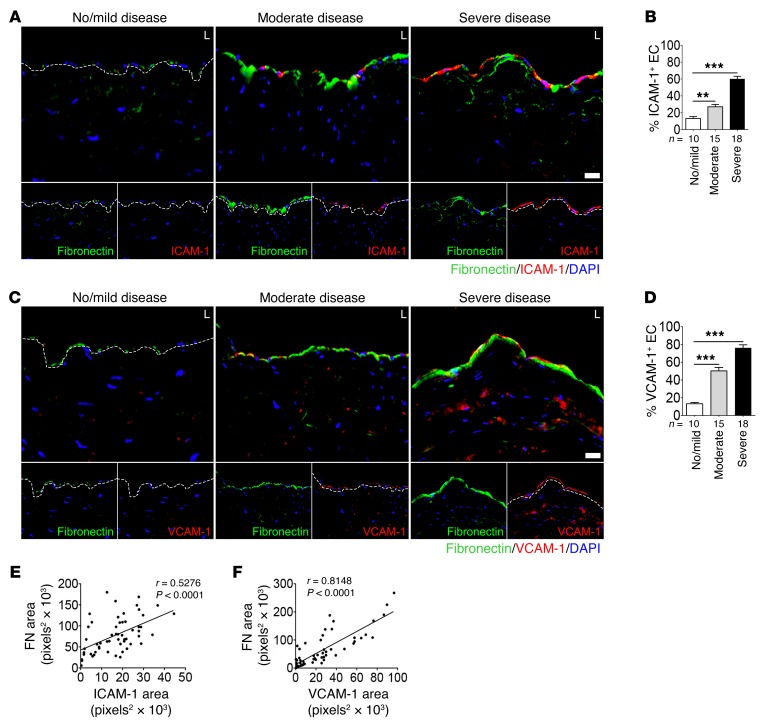
细胞外基质蛋白胶原和纤维连接蛋白是上皮-间充质转化和EndMT的公认标志物,在动脉粥样硬化斑块进展中起重要作用。 ECs在该患者群体中的表达也与I/M比率的增加密切相关( 图10,A–D )胶原蛋白和纤维连接蛋白的内皮表达增加与疾病严重程度之间有很强的线性关系( 图10,E和F ). 此外,免疫染色显示,随着CAD严重程度的增加,管腔内皮细胞ICAM-1和VCAM-1的表达增加( 图11,A–D ). 纤维连接蛋白沉积的增加与ICAM-1和VCAM-1的表达密切相关( 图11,E和F ). 这些观察结果建立了CAD严重程度与内皮细胞FGFR1表达缺失之间的关系,以及内皮细胞TGF-β信号的激活与EndMT程度之间的关系。
图10。 人冠状动脉内皮细胞间充质标记物的表达。
无/轻度患者的左主冠状动脉( n个 =10),中等( n个 =15),严重( n个 =18)评估CAD。 ( A类 和 C类 )患者左主冠状动脉CD31(绿色)、胶原蛋白1(红色)和纤维连接蛋白(红色)免疫荧光染色的代表性图像。 细胞核用DAPI(蓝色)染色。 比例尺:16μm。 ( B类 )测量每个场新生内膜中的胶原蛋白1面积(* 对 <0.05,中度疾病与非/轻度疾病的比较*** 对 <0.001比较严重疾病与无/轻度疾病; 使用Newman-Keuls事后检验进行多重比较校正的单因素方差分析)。 ( D类 )管腔内每个场纤维连接蛋白面积与CD31面积的比值(* 对 <0.05,中度疾病与非/轻度疾病的比较*** 对 <0.001比较严重疾病与无/轻度疾病; 使用Newman-Keuls事后检验进行多重比较校正的单因素方差分析)。 ( E类 和 F类 )每视野新生内膜中胶原蛋白1面积的散点图、管腔中纤维连接蛋白面积与CD31面积的比值以及I/M比值。 相应的斯皮尔曼相关系数( 第页 )每个场新生内膜中的胶原蛋白1面积与每个场纤维连接蛋白面积与CD31面积的比值以及I/M比值与 对 显示值。
图11。 人冠状动脉内皮细胞间充质和炎症标记物的表达。
无/轻度患者的左主冠状动脉( n个 =10),中等( n个 =15),严重( n个 =18)评估CAD。 ( A类 和 C类 )患者左冠状动脉主干纤维连接蛋白(绿色)、ICAM-1(红色)和VCAM-1(红)免疫荧光染色的代表性图像。 细胞核用DAPI(蓝色)染色。 比例尺:16μm。 ( B类 )ICAM-1的百分比 + 管腔中的EC(** 对 与无/轻度疾病相比,<0.01*** 对 <0.001比较中度疾病与无/轻度疾病*** 对 <0.001比较严重疾病与无/轻度疾病)。 ( D类 )VCAM-1的百分比 + 管腔中的EC(*** 对 <0.001比较中度疾病与无/轻度疾病*** 对 <0.001比较严重疾病与无/轻度疾病; 使用Newman-Keuls事后检验进行多重比较校正的单因素方差分析)。 ( E类 和 F类 )腔中每个场的纤连蛋白面积、ICAM-1和VCAM-1面积散点图。 相应的斯皮尔曼相关系数( 第页 )纤维连接蛋白面积与ICAM-1和VCAM-1面积之间 对 显示值。
讨论 这项研究的结果表明,EndMT是引发动脉粥样硬化的因素(如炎症和剪切紊乱)与导致斑块形成的组织重塑之间的联系。 起始事件是OSS和血管壁炎症诱导的保护性内皮细胞FGF信号输入的丢失。 这导致内皮TGF-β信号的激活和EndMT的诱导。 一旦诱导,EndMT通过增加纤维连接蛋白(一种已知的致动脉粥样硬化ECM蛋白)的沉积促进斑块进一步生长( 17 , 18 )以及增加粘附分子(如ICAM和VCAM)的内皮表达,从而进一步促进循环单核细胞和白细胞的募集并诱导新间充质细胞的形成,导致新内膜扩张。
许多观察结果支持这一假设。 首先,当暴露于OSS或某些炎症介质时,内皮细胞下调FGFR1表达并激活TGF-β信号。 第二,内皮特异性FGF信号输入中断的小鼠发展为EndMT,当交叉到 阿波 –/– 背景。 第三,对不同程度动脉粥样硬化患者左主干冠状动脉的分析表明,冠状动脉内皮细胞FGFR1的表达程度、p-SMAD2信号的出现以及EndMT与患者CAD严重程度之间存在强烈的负相关。 综上所述,这些结果在炎症、剪切应力、保护性内皮细胞FGF信号输入的丢失和EndMT的诱导之间建立了联系,EndMT反过来在动脉粥样硬化病变的发展和生长中起着重要作用。
我们观察到动脉粥样硬化病变中内皮细胞FGFR1表达下降与EndMT程度之间的强烈相关性,这与之前内皮细胞FGF信号的保护作用的证明一致( 10 , 14 ). 调节内皮细胞FGFR1表达的两个关键因素,即剪切应力紊乱和血管壁炎症,也是众所周知的动脉粥样硬化危险因素( 1 , 5 ). 然而,扰动剪切应力与内皮细胞FGFR1表达之间的联系以前还没有报道。 在本研究中,我们表明,体外培养的内皮细胞暴露于OSS,而非动脉粥样硬化保护性LSS,会导致FGFR1表达减少,p-SMAD2增加。 有趣的是,在体内,正常饮食小鼠的动脉粥样硬化保护和动脉粥样硬化内皮细胞中的内皮细胞FGFR1水平没有差异。 然而,HFD诱导了动脉粥样硬化内皮中FGFR1水平的显著降低。
炎症是动脉粥样硬化的重要组成部分。 过去十年的研究证明,动脉粥样硬化病变中存在单核细胞衍生的巨噬细胞、T细胞、B细胞和其他免疫介质( 19 – 21 ). 这种炎症环境被认为是由多种因素综合作用的结果,包括机械因素,如剪切应力的扰动( 2 )脂质引起血管壁的变化。 关于前者,许多研究将扰动的剪切应力与内皮细胞产生纤维连接蛋白联系起来( 17 , 22 ),一种公认的上皮向间充质转化的标志物( 23 , 24 ). 纤连蛋白在促进内皮细胞炎症信号传导中起主要作用( 2 , 21 )在小鼠身上进行的多项研究表明,纤维连接蛋白在促进动脉粥样硬化中具有因果作用( 18 , 25 ). 因此,EndMT产生的纤维结合蛋白似乎是该过程促进炎症和动脉粥样硬化的机制之一。
同时,动脉粥样硬化形成过程中脂质负载巨噬细胞中胆固醇结晶的形成可激活炎症小体,从而促进前IL-1β转化为活性细胞因子( 26 ). 巨噬细胞M1亚群在动脉粥样硬化病变中的优势( 27 )提供了炎症存在的进一步证据,因为这些巨噬细胞被认为来源于单核细胞,以应对IFN-γ的刺激。 后者可能是由人类皮损中的T细胞产生的,其Th1分泌谱包括IFN-γ和TNF-α( 4 ). γ-干扰素在动脉粥样硬化中的致病作用通过其诱导病变进展的能力得到进一步证明( 28 , 29 )而其缺乏导致病变大小显著减小,同时不影响整体脂质状况( 30 ). 同样,在人类动脉粥样硬化病变中也发现自然杀伤细胞的激活( 19 ),导致IFN-γ和TNF-α的分泌。 因此,动脉粥样硬化富含炎症介质,并表现出各种炎症途径慢性激活的证据。
虽然炎症和动脉粥样硬化之间的联系已被明确确立,但这种联系的分子基础仍不清楚。 我们建议EndMT提供一个这样的潜在链接。 持续的炎症以及干扰的剪切应力降低了内皮细胞FGFR1的表达,导致TGF-β信号的激活,从而诱导EndMT。 后者负责许多致动脉粥样硬化的后果,包括粘附分子的增加表达,如ICAM-1和VCAM-1,从而促进炎症细胞的进一步流入; 细胞外基质的沉积,如纤维连接蛋白,会加剧炎症,从而加速动脉粥样硬化的生长; 最后,新的间充质细胞的出现,在新生内膜中产生SMC和成纤维细胞,进一步促进斑块扩张。 接受EndMT的内皮细胞的促炎表型建立了一个前馈回路,进一步加剧炎症并导致斑块持续增长。 抑制这一过程可能是阻止动脉粥样硬化进展的关键步骤。
最近,炎症的减轻已成为新的抗动脉粥样硬化疗法发展的关键目标。 抑制炎症特定方面的各种尝试,包括IL-1β-中和抗体(CANTOS)( 31 ),充其量是模棱两可的。 然而,EndMT的新兴生物学表明,针对单个炎症途径的方法可能会失败,因为斑块中发现的任何“三大”细胞因子——IFN-γ、IL-1β和TNF-α——都可以诱导EndMT,从而导致动脉粥样硬化疾病进展。 相反,恢复有效的内皮FGF信号和/或抑制内皮TGF-β信号可能有效阻止疾病进展。 后者指出了内皮生物学的复杂性,因为平滑肌TGF-β信号传导与动脉粥样硬化的减少有关( 32 , 33 )并可能解释TGF-β在动脉粥样硬化中作用的模糊性( 34 ).
总之,由动脉粥样硬化的炎症成分诱导的EndMT可增强动脉粥样硬化病变的炎症环境,并导致动脉粥样硬化斑块的进行性生长。 旨在控制这一过程的干预措施将测试其在动脉粥样硬化进展中的作用,如果成功,可能会提供有效的新方法来逆转这种疾病的自然病史。
方法 细胞培养和试剂。 HUVEC(第5-10代;CC-2517,Lonza)在内皮基础培养基-2中培养,补充EGM-2MV BulletKit(CC-3202,Lonsa),或在M199中培养,添加ECGS,补充20%FBS(Sigma-Aldrich), 我 -谷氨酰胺(Gibco)和青霉素/链霉素(Gibco.)。 人冠状动脉平滑肌细胞(HCASMC)(C-017-5C)、培养基(M231-500)和补充剂(SMGS,S-007-25;SMDS,S-008-5)购自Life Technologies。 细胞在37°C、5%CO下生长 2 在Medium 231(Life Technologies)中添加平滑肌生长补充剂(SMGS含有4.9%FBS、2 ng/ml FGF2、0.5 ng/ml EGF、5 ng/ml肝素、2μg/ml IGF-1和0.2μg/ml BSA)。 为了进行SMC分化,HCASMC与含有平滑肌分化补充剂的培养基231(含有1%FBS和30 g/ml肝素的SMDS)孵育8天。 对于不同的细胞因子治疗,在完全生长培养基或分化培养基中用人IFN-γ(300-02,PeproTech)、人TNF-α(300-01A,PeproTech)或人IL-1β(200-01B,Peproech)处理HUVEC或HCASMC。
流体剪切应力。 将HUVECs接种在涂有10μg/ml纤连蛋白的组织培养塑料载玻片上,并在补充有20%FBS、ECGS、100mg/l肝素和青霉素/链霉素的M199培养基中生长至汇合。 刺激前4小时,细胞在补充有8%FBS的M199培养基中饥饿。 然后将滑块夹在平行板流动室中,并以12达因/厘米的速度剪切 2 (层流)或1±4达因/厘米 2 (振荡流)16或48小时。 然后在PBS中清洗细胞,并进一步处理以进行免疫染色或mRNA提取。
SMAD2/3易位分析。 细胞用4%甲醛固定15分钟,然后用1%Triton X-100渗透15分钟。 渗透后,用StartingBlock Blocking Buffer(Thermo Fisher Scientific)封闭细胞15分钟,并在4°C下用在StartingBlocking Buffer(1:500,Cell Signaling)中稀释的SMAD2/3一级抗体培养过夜。 经过3个清洗步骤后,用DAPI和Alexa Fluor 647结合二级抗体(1:500,分子探针)在室温下在StartingBlock Blocking Buffer中稀释2小时,对细胞进行检测。 然后用Fluoromount-G安装介质(Southern Biotech)安装细胞。 然后用安装在装有电动载物台(Prior Scientific)的Perkin Elmer旋转圆盘共焦显微镜上的×20物镜拍摄50张图像。 然后使用前面描述的专用MATLAB函数分析图像( 35 ). 简单地说,图像的掩模是使用自适应直方图均衡化算法与强度和大小阈值相结合来制作的。 通过提取细胞核的掩模(由DAPI图像确定),将其拟合为椭圆,并确定流动方向与椭圆长轴之间的角度,计算细胞方向。 根据拟合椭圆的偏心率测量核偏心率。 取转录因子染色掩模(SMAD2/3),计算细胞核内染色面积和染色强度的乘积,再除以总染色面积和总染色强度的积,计算核移位。 这产生了一个我们称之为易位因子的无单位度量,在完全核易位的细胞中等于1,在没有易位的电池中等于0。
慢病毒的产生。 人FGFR1 shRNA慢病毒构建物购自Sigma-Aldrich,人FRS2αshRNA慢毒构建物购于Open Biosystems。 为了生产shRNA慢病毒,使用X-tremeGENE 9 DNA转染试剂(06365787001,Roche)将携带对照、FGFR1和FRS2αshRNA的3.7μgΔ8.2、0.2μg VSVG和2.1μg pLKO.1共转染到293T细胞中。 48小时后,收集培养基,用0.45-μm过滤器(PN4184,PALL Life Sciences)清除,并与聚丁烯(5μg/ml)(H9268,Sigma-Aldrich)混合,然后应用于细胞。 培养6小时后,用新鲜培养基替换含病毒培养基。 使用QuickTiter慢病毒滴度试剂盒(慢病毒相关HIV p24,VPK-107,Cell Biolabs)偷笑病毒上清液。
RNA分离和定量实时PCR。 将细胞悬浮在TRIzol试剂(15596018,Invitrogen)中,并根据制造商的说明分离总RNA(74134,QIAGEN)。 使用iScript cDNA合成试剂盒(170-8891,Bio-Rad)进行逆转录。 通过混合等量cDNA、iQ SYBR Green Supermix(170-8882,Bio-Rad)和SABiosciences(一家QIAGEN公司)(FGFR1[PPH00372F]、VE-cadherin[PPH00668F]、N-cadherin[PPPH00636F]、eNOS[PPH01298F]、TGF-βR1[PPH00237C]、PAI-1[PPH00215F])的基因特异性引物,使用Bio-Rad CFX94进行定量实时PCR(qRT-PCR) 、ICAM-1[PPH00640F]、VCAM-1[PPH00623E]、MCP-1[PPH00192F]、ZEB2[PPH09021B]、Slug[PPH02475A]和Snail[PPH02459A])或以下用于检测mRNA的引物: 扭转1 、actggcctgcaaaaccatag和tgcattaccatggtcct; ACTA2公司 、gccacagctctctctct和tgaattccagccat; 槽口3 、ctcatccgaaacctctac和tcttccaaccctctac; 纤维连接蛋白1、gttgtccggctctcc和agtgtcagggttgcctcca; 胶原蛋白1A、tgtggcccagaactggt和caggagtcagctggatgg。 所有反应均在25μl反应体积内进行,一式两份。 个体信使核糖核酸的表达与内源性β-肌动蛋白的表达相关。 PCR扩增包括在95°C下进行10分钟的初始变性步骤,然后在95°C下进行46次PCR循环15秒和60°C下进行30秒。
用于蛋白质免疫检测的抗体。 我们使用以下抗体进行免疫印迹(IB)、免疫荧光(IF)或免疫组织化学(IHC; IHC),p44/42 MAPK(ERK1/2)(Thr202/Tyr204)(4370,细胞信号;IHC( 14 )、FRS2α(ab10425,abcam;IHC),FRS2(sc-8318,Santa Cruz;IB),GAPDH(2118,细胞信号;IB, NOTCH3(5276,细胞信号;IB),NOTCH三(ab23426,abcam;IHC),PAI-1(612024,BD;IB 465/467 )(3101,细胞信号;人类石蜡样品的IHC),p-SMAD2(Ser 465/467 )(AB3849,Millipore;IHC用于小鼠石蜡样品),p-SMAD2(Ser 465/467 )(3108,细胞信号;IB),SMAD2(3122,细胞信号;IB),SMAD2/3(8685,细胞信号;IF),平滑肌α-肌动蛋白(A2547,Sigma-Aldrich;IB),平滑肌α-肌动蛋白-别藻蓝蛋白(IC1420A,研发系统;IHC),转化生长因子-βR1(3712,细胞信号;IB),转化生长因子-βR1(sc-398,Santa Cruz;IB),β-微管蛋白(T7816,Sigma-Aldrich;IB), VCAM-1(NBP1-47491,Novus Biologicals;IHC用于人体组织),VCAM-1,(ab19569,abcam;IHC-用于小鼠组织),VC AM-1(3540-1,Epitomics;IB),VE-cadherin(sc-6458,Santa Cruz;IB;),VEGFR2(2479,Cell Signaling;IB。
小鼠的产生。 Frs2a公司 飞行/飞行 之前描述过老鼠( 36 ). Frs2a公司 飞行/飞行 老鼠被杂交到 罗莎26 荧光报告器 毫吨/毫克 报告行(JAX SN:007676),然后交叉到C57BL/6 阿波 –/– 鼠标(JAX SN:002052)。 Frs2a公司 飞行/飞行 阿波 –/– 毫吨/毫克 用表达Cre重组酶的小鼠在 加拿大存托凭证5 发起人(德国穆斯特马普研究所R.H.Adams赠送)。 阿波 –/– 和FRS2α ECKO公司 阿波 –/– 雄性小鼠喂食西方饮食(40%千卡%脂肪,1.25%胆固醇,0%胆酸)4或16周(产品 D12108号 ,研究饮食),从8周大开始。 他们的体重和血脂状况与 阿波 –/– 老鼠( 补充图5、D和E ). 使用以下引物进行PCR基因分型分析: Frs2a公司 飞行/飞行 (5′-GAGTGGCTGTGATTGGAGAGGCAGG-3′和5′-GGCACAGTGTCGACACATG-3′), 毫吨/毫克 (5′-CTCTGCTGCCTCCTGGCTTCTT-3′,5′-CGAGGCGGATACACAGCAATA-3′和5′-TCAATGGGCGGTGT-3′), Cdh5-CreER公司 T2段 (5′-GCTGCATTACCGGTCGATGCAACGA-3′和5′-GTGGCAGAGGCAACACCATT-3′), 阿波 (5′-GCCTAGCGCGAGGAGCCG-3′,5′-GTGACTGGAGCTCTGCAGC-3′,和5′-GCGCCCCGACTGCCT-3′)。
免疫组织化学染色。 使用Microm低温恒温器(用于冷冻块)或石蜡切片机(用于石蜡块)以5μm的间隔进行切片。 对于冷冻组织切片,将载玻片在–20°C的丙酮中固定10分钟。 对于石蜡切片,将载玻片在二甲苯中脱蜡,在柠檬酸盐缓冲液(10mM,pH 6.0)中煮沸20分钟用于抗原回收,并再水合。 用PBS清洗3次后,在4°C的加湿室中用封闭溶液(10%BSA和PBS中的马血清)稀释的一级抗体培养组织切片过夜。 切片用Tris缓冲盐水冲洗3次; 与适当的Alexa Fluor 488–、Alexa Fuor 594–或Alexa Fluor 647–结合二级抗体在室温下在封闭溶液中稀释1:1000培养1小时; 再次清洗3次,并用带DAPI的ProLong黄金安装试剂安装在载玻片上( 第36935页 ,生命科技)。 所有免疫荧光显微照片均使用Axiovert 200M显微镜系统(卡尔蔡司显微成像)采集。 使用Velocity软件捕获图像,并使用ImageJ软件(NIH)进行量化。
动脉粥样硬化病变的组织学分析。 对动物实施安乐死,并用4%多聚甲醛(18814,Polysciences Inc.)经左心室灌注固定5分钟。 使用油红O染色分析位于主动脉、主动脉根部、头臂动脉和腹主动脉的病变。 为了测量主动脉中的病变,解剖整个主动脉,包括升弓、胸段和腹段,轻轻清洁外膜组织,并用油红O(O0625,Sigma-Aldrich)染色,如前所述( 37 ). 使用ImageJ软件(NIH)量化表面病变面积。 为了测量主动脉根部的病变,切除心脏和近端主动脉,并切除心室的顶点和下半部分。
血脂分析。 血清是在9391通过血液离心2分钟获得的 克 在4°C下保存,并在-80°C下储存,直到进行每次分析。 在耶鲁小鼠代谢表型中心测量总胆固醇、甘油三酯和HDL胆固醇水平。
蛋白质印迹分析。 用HNTG裂解缓冲液(20 mM HEPES[PH7.4],150 mM NaCl,10%甘油,1%Triton X-100,1.5 mM MgCl)裂解细胞 2 ,1.0 mM EGTA),含有完整的无EDTA的微型蛋白酶抑制剂(11836170001,罗氏)和磷酸酶抑制剂(04906837001,罗氏。 使用Tris/Glycin/SDS流动缓冲液(161-0772,Bio-Rad)在标准TGX预铸凝胶(567-1084,Bio-Rad)上溶解每个样品中的20μg总蛋白,转移到硝化纤维素膜(162-0094,Bio-Read)上,然后用各种抗体进行探测。 使用SuperSignal West Pico化学发光基板(34080,Thermo Fisher Scientific)进行化学发光测量。
患者人数。 人冠状动脉取自移植受体或尸体器官供体的移植心脏。
标本采集。 研究人员随时待命于手术组,并在移植时采集心脏。 为了尽量减少体外伪影,在手术室中切除了约5至20毫米的左主冠状动脉段( 补充图8A )并立即作为冰冻切片进行处理( n个 =43)在最佳切割温度介质中(樱花Finetek USA Inc.),当长度足够时,另加一段( n个 =29)也固定在福尔马林中,用于随后的包埋、切片和染色。 尽管某些抗体(FGFR1和p-SMAD2)对石蜡包埋标本的检测更为理想,但大多数分析都是在冷冻标本中进行的。
组织学和形态计量学分析。 左主冠状动脉切片用H&E和Movat染色。 每个区块一个截面的数字H&E和Movat照片以最终放大倍数×40进行投影。 使用ImageJ软件(NIH)进行形态计量分析。 如中所述 补充图8B ,测量内膜和中膜厚度。 I/M厚度与斑块分期的比率( 38 )用于分级动脉粥样硬化的严重程度。 我们平均了每个样本4个不同区域的这些参数的结果,以获得平均值。 I/M比值小于0.2的左主冠状动脉被视为无疾病或轻度疾病; I/M比值在0.2到1之间的患者被视为中度疾病; I/M比值大于1或钙化的患者被视为患有严重疾病。
统计。 所有图形都是使用GraphPad Prism软件创建的,统计分析是使用Graph Pad Primm计算的。 使用双尾学生的 t吨 测试。 对于多重比较,使用了纽曼-凯尔斯检验的单因素方差分析。 采用皮尔逊秩相关检验进行变量间的相关分析。 A类 对 小于0.05的值被认为是显著的。 所有结果都得到了至少3个独立实验的证实。 误差线代表平均值±SEM。
研究批准。 耶鲁大学动物护理和使用委员会审查并批准了所有涉及动物的实验。 耶鲁大学机构审查委员会和新英格兰器官银行批准了与人体受试者相关的程序。 手术患者同意放弃同意,已故器官捐赠者的书面知情同意书由其家属提供。
作者贡献 P-YC、LQ、GL、GT、MAS和MS设计研究; P-YC、LQ、NB、MB、TA和GL进行研究; P-YC、LQ、GL、GT、NB和MS分析数据; P-YC和MS撰写了手稿。
致谢 我们感谢Robert Friesel(缅因州医学中心研究所)提供FGFR1抗体,感谢Ralf Adams(马克斯普朗克研究所) Cdh5-CreER公司 T2段 老鼠。 我们感谢丽塔·韦伯(Rita Webber)和妮可·科普兰(Nicole Copeland)保持了本研究中使用的小鼠群体。 这项工作得到了NIH拨款R01 HL053793(给M.Simons)和P01 HL107205(给M.Simons和M.A.Schwartz)的支持。 血脂谱由耶鲁小鼠代谢表型中心核心设施(NIH拨款U24 DK059635)进行。
脚注
参考信息: 临床研究杂志 . 2015; 125(12):4514–4528. doi:10.1172/JCI82719。
参考文献
1 Conway DE,Schwartz MA。动脉粥样硬化中的流动依赖性细胞机械传导。 细胞科学杂志。 2013; 126(第22部分):5101–5109。 doi:10.1242/jcs.138313。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
2 Hahn C,Schwartz MA。血管生理学和动脉粥样硬化形成中的机制转导。 Nat Rev Mol细胞生物学。 2009; 10(1):53–62. doi:10.1038/nrm2596。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
三。 Libby P、Ridger PM、Hansson GK。 动脉粥样硬化生物学翻译的进展和挑战。 自然。 2011; 473(7347):317–325. doi:10.1038/nature10146。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
4 Libby P、Lichtman AH、Hansson GK。 动脉粥样硬化相关的免疫效应机制:从小鼠到人类。 豁免权。 2013; 38(6):1092–1104. doi:10.1016/j.immuni.2013.06.009。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
5 塔巴斯一世、加西亚-卡德纳G、欧文斯GK。 动脉粥样硬化细胞生物学的最新见解。 细胞生物学杂志。 2015; 209(1):13–22. doi:10.1083/jcb.201412052。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
6 Zeisberg EM等。内皮细胞向间充质细胞的转化导致心脏纤维化。 2007年《国家医学》; 13(8):952–961. doi:10.1038/nm1613。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
7 Maddaluno L等人EndMT有助于脑海绵状畸形的发生和发展。 自然。 2013; 498(7455):492–496。 doi:10.1038/nature12207。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
8 Kitao A等。通过转化生长因子-β1/Smad激活的内皮细胞向间充质细胞转化与特发性门静脉高压患者的门静脉狭窄相关。 《美国病理学杂志》。 2009; 175(2):616–626. doi:10.2353/ajpath.2009.081061。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
9 Piera-Velazquez S,Li Z,Jimenez SA。内皮-间充质转化(EndoMT)在纤维化疾病发病机制中的作用。 《美国病理学杂志》。 2011; 179(3):1074–1080. doi:10.1016/j.ajpath.2011.06.001。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
10 Chen PY等。FGF通过控制let-7 miRNA的表达来调节TGF-β信号和内皮-间充质转化。 细胞报告2012; 2(6):1684–1696. doi:10.1016/j.celrep.2012.10.021。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
11 Cooley BC等。TGF-β信号转导介导静脉移植重建过程中的内皮-间充质转化(EndMT)。 2014年《科学与运输医学》; 6(227):doi:10.1126/scitranslmed.3006927。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
12 Medici D、Shore EM、Lounev VY、Kaplan FS、Kalluri R、Olsen BR。血管内皮细胞转化为多能干样细胞。 《国家医学》,2010年; 16(12):1400–1406. doi:10.1038/nm.2252。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
13 van Meeteren LA,ten Dijke P.TGF-β对内皮细胞可塑性的调节。 《细胞组织研究》2012; 347(1):177–186. doi:10.1007/s00441-011-1222-6。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
14 Chen PY,Qin L,Tellides G,Simons M.成纤维细胞生长因子受体1是内皮细胞TGFβ信号的关键抑制剂。 科学信号。 2014; 7(344):doi:10.1126/scisignal.2005504。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
15 Ten Dijke P、Egorova AD、Goumans MJ、Poelmann RE、Hierck BP。 TGF-β信号在内皮-间充质转化中的作用:剪应力和初级纤毛的作用。 科学信号。 2012; 5(212):doi:10.1126/scisignal.2002722。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
16 Pitulescu ME,Schmidt I,Benedito R,Adams RH。新生血管中的诱导基因靶向和小鼠视网膜血管生成分析。 国家协议。 2010; 5(9):1518–1534. doi:10.1038/nprot.2010.113。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
17 Feaver RE、Gelfand BD、Wang C、Schwartz MA、Blackman BR。动脉粥样硬化血液动力学调节纤维连接蛋白沉积,产生维持内皮炎症的正反馈。 Circ Res.2010; 106(11):1703–1711. doi:10.1161/CIRCRESAHA.109.216283。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
18 Rohwedder I等。血浆纤维连接蛋白缺乏阻碍动脉粥样硬化进展和纤维帽形成。 EMBO Mol Med.2012; 4(7):564–576。 doi:10.1002/emmm.201200237。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
19 Lahute C,Herbin O,Mallat Z,Tedgui A.动脉粥样硬化中的适应性免疫:机制和未来的治疗靶点。 Nat Rev Cardiol公司。 2011; 8(6):348–358. doi:10.1038/nrcardo.2011.62。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
20 Libby P.动脉粥样硬化中的炎症。 动脉硬化血栓血管生物学。 2012; 32(9):2045–2051. doi:10.1161/ATVBAHA.108.179705。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
21 Li X,Derode N,Mallat Z。炎症小体在心血管疾病中的作用。 《分子医学杂志》(柏林)2014; 92(4):307–319. doi:10.1007/s00109-014-1144-3。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
22 Gelfand BD等。血管内皮中β-catenin和T细胞特异性转录因子信号的血流动力学激活调节纤维连接蛋白的表达。 动脉硬化血栓血管生物学。 2011; 31(7):1625–1633。 doi:10.1161/ATVBAHA.11227827。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
23 Jung HY,Fattet L,Yang J.分子途径:将肿瘤微环境与转移中的上皮-间充质转化联系起来。 《临床癌症研究》2015; 21(5):962–968. doi:10.1158/1078-0432.CCR-13-3173。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
24 Scanlon CS、Van Tubergen EA、Inglehart RC、新泽西州D'Silva。 鳞状细胞癌上皮-间充质转化的生物标志物。 牙科研究杂志2013; 92(2):114–121. doi:10.1177/0022034512467352。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
25 Tan MH,Sun Z,Opitz SL,Schmidt TE,Peters JH,George EL。小鼠选择性剪接纤维连接蛋白EIIIA结构域的缺失可减少动脉粥样硬化。 鲜血。 2004; 104(1):11–18. doi:10.1182/bloud-2003-09-3363。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
26 Duewell P等人。NLRP3炎性体是动脉粥样硬化形成所必需的,并被胆固醇晶体激活。 自然。 2010; 464(7293):1357–1361. doi:10.1038/nature08938。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
27 Stoger JL等。人类动脉粥样硬化中巨噬细胞极化标记物的分布。 动脉粥样硬化。 2012; 225(2):461–468. doi:10.1016/j.动脉粥样硬化.2012.09.013。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
28 Gupta S、Pablo AM、Jiang X、Wang N、Tall AR、Schindler C.IFN-γ增强ApoE基因敲除小鼠的动脉粥样硬化。 临床投资杂志。 1997; 99(11):2752–2761. doi:10.1172/JCI119465。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
29 Tellides G等人。干扰素-γ在缺乏白细胞的情况下引发动脉硬化。 自然。 2000; 403(6766):207–211. doi:10.1038/35003221。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
30 Whitman SC、Ravisankar P、Daugherty A.IFN-γ缺乏对载脂蛋白E-/-小鼠的动脉粥样硬化形成产生性别特异性影响。 《干扰素细胞因子研究杂志》,2002年; 22(6):661–670. doi:10.1089/10799900260100141。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
31 Everett BM等人,《心血管消炎试验的原理和设计:动脉粥样硬化血栓的炎症假设测试》。 《美国心脏杂志》2013; 166(2):199–207.e15。 doi:10.1016/j.ahj.2013.03.018。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
32 Lutgens E等。转化生长因子-β在斑块进展过程中调节炎症和纤维化之间的平衡。 动脉硬化血栓血管生物学。 2002; 22(6):975–982. doi:10.1161/01.ATV.0000019729.39500.2F。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
33 Mallat Z,Tedgui A.转化生长因子β在动脉粥样硬化中的作用:新见解和未来展望。 当前Opin Lipidol。 2002; 13(5):523–529。 doi:10.1097/00041433-200210000-00008。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
34 Toma I,McCaffrey TA。 转化生长因子-β与动脉粥样硬化:动脉粥样硬化与动脉粥样硬化保护相互交织的方面。 《细胞组织研究》2012; 347(1):155–175. doi:10.1007/s00441-011-1189-3。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
35 Baeyens N等。Syndecan 4是血流和动脉粥样硬化保护信号中内皮细胞对齐所必需的。 美国国家科学院院刊2014; 111(48):17308–17313. doi:10.1073/pnas.1413725111。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
36 Lin Y,Zhang J,ZhangY,Wang F.Frs2α条件空等位基因的产生。 起源。 2007; 45(9):554–559. doi:10.1002/dvg.20327。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
37 Huang Q等。AIP1通过限制高脂血症诱导的炎症和血管内皮功能障碍来抑制动脉粥样硬化。 动脉硬化血栓血管生物学。 2013; 33(4):795–804. doi:10.1161/ATVBAHA.113.01220。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
38 Virmani R、Kolodge FD、Burke AP、Farb A、Schwartz SM。冠状动脉猝死的教训:动脉粥样硬化病变的综合形态学分类方案。 动脉硬化血栓血管生物学。 2000; 20(5):1262–1275. doi:10.1161/01.ATV.20.5.1262。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
关联数据 本节收集本文中包含的任何数据引用、数据可用性声明或补充材料。