摘要 积极利用谷氨酰胺对肿瘤细胞增殖至关重要。 谷氨酰胺水解是谷氨酰胺利用的第一步和限速步骤,由谷氨酰胺酶(GLS)催化。 ErbB2的激活是乳腺癌的主要原因之一,乳腺癌是许多国家妇女第二常见的死亡原因。 然而,ErbB2信号是否影响乳腺癌细胞中谷氨酰胺酶的表达尚不清楚。 在本研究中,我们发现MCF10A-NeuT细胞系在mRNA和蛋白水平上都高于其亲本MCF10A细胞系GLS1的表达,并且ErbB2的敲除降低了MCF10A-NeuT的GLS1表达。 我们进一步表明,在这些细胞中,ErbB2介导的GLS1上调与c-Myc表达无关。 此外,PI3K-Akt和MAPK通路的激活都不足以上调GLS1的表达。 有趣的是,抑制NF-κB可阻断ErbB2刺激的GLS1表达,而刺激NF-κ的B足以提高MCF10A细胞中GLS1的水平,这表明NF-κ子B的PI3K-Akt-非依赖性激活可上调ErbB2-阳性乳腺癌细胞中的GLS1。 最后,敲除或抑制GLS1可显著降低GLS1水平较高的乳腺癌细胞的增殖。 综上所述,我们的数据表明,ErbB2激活通过PI3K-Akt-非依赖性NF-κB通路促进乳腺癌细胞中GLS1的表达,从而确定另一种刺激GLS1表达的致癌信号通路,从而促进肿瘤细胞中谷氨酰胺的利用。 这些发现,如果通过体内模型验证,可能有助于确定癌症预防和治疗的新生化靶点。
关键词: 乳腺癌、ErbB2、谷氨酰胺酶、谷氨酰胺、GLS1、核因子κB
谷氨酰胺水解活性是许多肿瘤的主要生化特征。 通过谷氨酰胺水解,谷氨酰胺被用来满足高增殖细胞的生物合成、能量和还原需求[ Reitzer等人,1979年 ; Turowski等人,1994年 ; DeBerardinis等人,2008年 ; Levine和Puzio-Kuter,2010年 ; Meng等人,2010年 ; Dang等人,2011年 ; Shanware等人,2011年 ]. 谷氨酰胺分解是谷氨酰胺酶(GLS)催化谷氨酰胺转化为谷氨酸的过程,谷氨酰胺酶包括两种亚型:GLS1和GLS2。 特别是,据报道GLS1在非肝组织和肿瘤中广泛表达[ Aledo等人,2000年 ]. 此外,GLS1过度表达与细胞增殖和肿瘤生长相关[ de la Rosa等人,2009年 ]而肝脏亚型GLS2参与尿素循环[ Gomez-Fabre等人,2000年 ].
癌基因通过各种信号通路促进肿瘤形成和调节细胞生长[ Borrello等人,2008年 ]. 细胞代谢过程提供能量、构建块和还原当量,以支持细胞生存和增殖,形成包括增殖和恶性转化在内的所有细胞活动的生化基础。 癌基因作为致癌转化的启动子和细胞生长的调节器,不仅可以促进细胞周期的进展,而且可以通过营养物质的重新规划利用来协调恶性转化。 谷氨酰胺分解不仅提供ATP和还原当量,而且是氮合成代谢的基本机制[ 汤普森等人,2008年 ; Gao等人,2009年 ; Meng等人,2010年 ]. 作为代谢转化过程的一部分,肿瘤启动癌基因可能通过提高GLS的表达促进谷氨酰胺的利用。 作为一种癌基因,c-Myc已被证明能增强人类肿瘤细胞中GLS1的表达; 然而,其他致癌基因是否调节GLS1的表达并协调谷氨酸分解与肿瘤细胞增殖仍不明确。
乳腺癌是女性第二大死亡原因[ Rana等人,2010年 ]占美国女性癌症诊断总数的26%[ Dizdar和Altundag,2009年 ]. 大约15-20%的乳腺癌表现出ErbB2的过度表达和/或扩增[ Baselga和Swain,2009年 ; Guarneri等人,2010年 ]. ErbB2的过度表达促进与其他ErbB蛋白形成ErbB2-同源二聚体或异源二聚体,导致下游信号通路的激活,如MAPK/Erk、PI3K-Akt或核因子κB(NF-κB),共同促进细胞生存、增殖和肿瘤发生[ Slamon等人,1987年 ; Yarden和Sliwkowski,2001年 ; 乔多什,2011年 ]. 此外,不稳定激活的ErbB2信号传导也会导致ER阳性乳腺癌对内分泌治疗的耐药性,导致不良结果[ Ertel等人,2010年 ]. 然而,ErbB2信号是否以及如何参与肿瘤发生过程中谷氨酰胺的利用尚不清楚。
在本研究中,我们报告了ErbB2激活上调GLS1表达。 我们还表明,这种上调机制由NF-κB途径控制,而不是由c-Myc控制。 最后,我们表明ErbB2增加的谷氨酰胺酶活性对乳腺癌细胞的快速增殖很重要。
材料和方法 细胞系和细胞培养 MCF10A和NeuT转化的MCF10A(MCF10A-NeuT)由R.Pestell博士(宾夕法尼亚州费城Kimmel癌症中心)慷慨提供。 在补充有马血清(5%)、胰岛素(10µg/ml)、EGF(20 ng/ml)、氢化可的松(0.5µg/ml)和霍乱毒素(100 ng/ml)的DMEM/F12(50:50)(Mediatech,Inc.,Manassas,VA)中培养MCF10A和MCF10A-NeuT细胞。 MCF10A和MCF10A-NeuT细胞的增殖检测培养基为DMEM/F12(50:50)(Mediatech,Inc.),补充有马血清(5%)、胰岛素(10µg/ml)、氢化可的松(0.5µg/ml)和霍乱毒素(100 ng/ml)。 SK-BR-3和MDA-MB-453细胞来自ATCC,并保存在补充有10%胎牛血清的DMEM(Mediatech,Inc.)中。 所有细胞均在37°C下在含5%二氧化碳的加湿培养箱中培养。
抗体和试剂 小鼠抗c-ErbB2单克隆抗体购自Calbiochem(Gibbstown,NJ); 小鼠抗谷氨酰胺酶单克隆抗体购自马萨诸塞州剑桥市Abcam; 小鼠抗-Myc单克隆抗体购自Santa Cruz Biotechnology(加州圣克鲁斯); 兔抗活性Erk和总Erk1/2多克隆抗体购自Promega(威斯康星州麦迪逊); 兔抗磷酸化Akt(Ser473)、总Akt和p65多克隆抗体来自Cell Signaling(Danvers,MA); 小鼠抗α-微管蛋白单克隆抗体来自Sigma-Aldrich(密苏里州圣路易斯)。 PD98059和LY294002购自Sigma-Aldrich。 这两种药物均在二甲基亚砜中稀释,并作为库存保存在−20°C。 核因子-κB抑制剂BAY 11-7082和核因子-激酶B活化剂佛波醇-12-吡啶-13-醋酸盐(PMA)购自EMD Chemicals,Inc.(新泽西州吉布斯敦)。 两种药物均在二甲基亚砜中稀释,并作为库存保存在−20°C。 TNF-α和双-2-(5-苯基乙酰氨基-1,3,4-噻二唑-2-基)乙基硫醚(BPTES)购自Sigma-Aldrich。 TNF-α在无菌PBS中稀释。BPTES在DMSO中稀释。 药学级曲妥珠单抗(Herceptin)购自Genentech(加利福尼亚州旧金山)。 用20ml供应的注射用抑菌水(USP)重新配制曲妥珠单抗,其中含有1.1%的苯甲醇作为防腐剂。 每小瓶的最终曲妥珠单抗溶液浓度为21mg/ml。当药物作用于细胞时,使用不同的浓度,如文本或图表所示。
siRNA敲除试验 ErbB2、GLS1、c-Myc、p65和对照siRNA购自Ambion(德克萨斯州奥斯汀)。 转染前,3×10 5 细胞接种到六孔板中。 第二天早上,使用lipofectamine 2000转染试剂(Invitrogen,Carlsbad,CA)用ErbB2、GLS1、c-Myc、p65或对照siRNA转染细胞。 转染6小时后,将Opti-MEM(Invitrogen,Grand Island,NY)改为常规培养基。 第三天,使用对照或靶向siRNA再次转染细胞。 转染后24小时,收集全细胞裂解物并制备用于Western blotting分析。
血浆和瞬时转移 过表达MEK的控制载体或质粒[ Sang等人,2003年 ]或Akt-Myr[ Ahmed等人,1997年 ]用于瞬时激活MEK/MAPK和/或PI3K-Akt信号通路。 转染前,将MCF10A细胞接种到10 cm培养皿中; 当细胞达到约70%的融合时,按照制造商的方案使用Lipofectamine 2000进行转染。 转染后24小时,收集全细胞裂解物进行Western blotting分析。
RNA提取和qRT-PCR 将MCF10A和MCF10A-NeuT细胞培养24 h,然后用冰镇PBS洗涤两次。使用RNeasy Mini Kit(加利福尼亚州巴伦西亚,恰根)提取总RNA。 使用纳米滴分光光度计(Nanodrop Technologies,Montchanin,DE)在260/280 nm处测定RNA浓度。 根据制造商手册(纽约州格兰德岛Invitrogen),使用SuperScript II逆转录酶逆转录每个样品中的2µg总RNA,总体积为20µl。 通过β-actin的PCR扩增证实了cDNA的质量。 cDNA(1:50稀释)用于定量分析,使用预先设计和验证的GLS1和GLS2 TaqMan探针(加利福尼亚州福斯特市应用生物系统)。 PCR检测按以下方案进行:在50°C下2分钟后,在95°C下变性10分钟,在95℃下变性40个周期15 s,在60°C下退火1分钟并延伸。 PCR反应体积为10µl,包含4.5µl 1:50稀释cDNA、5µl TaqMan 2×Universal PCR Master Mix NoAmpErase UNG(Applied Biosystems)、0.5µl预先设计和验证的基因特异性TaqMan-gene Expression Assay Mix。 β-肌动蛋白的RNA水平用于使RNA负载正常化。 使用StepOne™Software v2.1(Applied Biosystems)从收集的数据(阈值循环数,简称Ct)进行相对定量(RQ)研究。
西部地块 使用含有6.6M尿素、10mM Tris-HCl、1%SDS、5mM DTT、1%Triton X-100、10%甘油和1×蛋白抑制剂混合物的尿素裂解缓冲液收集全细胞裂解物。 使用Bio-Rad蛋白质分析试剂盒I测定蛋白质浓度。将等量的总蛋白质加载到微型蛋白TGX预制凝胶(Bio-RadHercules,CA)上,并进行电泳。 将分离出的蛋白质转移到PVDF膜(Bio-Rad)上,在TBST缓冲液(50mM Tris,pH 8.0,150mM NaCl,0.2%吐温-20)中用5%的无脂奶粉封闭,并用合适的抗体进行检测。 使用化学发光系统(伊利诺伊州罗克福德的Thermo Scientific)对色带进行可视化。 在含有62.5mMTris-HCl、pH 6.7、2%十二烷基硫酸钠和100mM 2-巯基乙醇的缓冲液中,在50°C下将蛋白质印迹剥离1 h,在TBST缓冲液中洗涤4-6次,并在需要时进行再验证。 使用Quantity One(Bio-Rad)进行蛋白质印迹定量; 软件自动分析谱带。 通过减去检测到的强度×mm来计算信号 2 背景。 对照组的信号被任意设置为1.00,而治疗组的信号表示为与对照组相比的倍数。
免疫荧光染色 将MCF10A和MCF10A-NeuT细胞接种在八个室玻片中(BD Biosciences)。 用TNF-α和PMA处理MCF10A细胞6h,然后在室温下用4%多聚甲醛固定15min。 用PBS冲洗三次后,用含有5%山羊血清和0.3%Triton X-100的PBS培养细胞1小时以进行阻断,然后在含有1%BSA和0.3%Triton X-100的稀释的PBS初级抗体中培养细胞2小时。在PBS中冲洗三次, 细胞与荧光结合的山羊抗兔或小鼠二次抗体孵育。 然后通过共聚焦显微镜(Fluoview 1000;Olympus)观察细胞。
细胞增殖试验 对于GLS1敲除:用对照或GLS1 siRNA转染MCF10A-NeuT、SK-BR-3和MDA-MB-453细胞24小时。第二天,在96周的平板上再次分离细胞,一式三份。 使用CyQUANT测定细胞数量 ® NF细胞增殖检测试剂盒(Invitrogen,Grand Island,NY),电镀后6小时,该数字设置为第0天。 通过将第1天、第3天和第5天的细胞数除以第0天,计算每个细胞系的每个条件下的“数字倍数”。 对于BPTES处理:将MCF10A、MCF10A-NeuT、SK-BR-3和MDA-MB-453细胞以3×10的密度一式三份接种在96孔板中 三 每个孔的细胞数。 第二天,用不同浓度的BPTES(0、5、10、20µM)处理这些细胞。 在治疗后第0、1、3和5天使用CyQUANT检测细胞数量 ® NF细胞增殖检测试剂盒(Invitrogen,纽约州格兰德岛)。
统计分析 对于定量PCR和细胞增殖分析结果,RQ或细胞数值由学生分析 t吨 测试。 P(P) 值<0.05为显著。
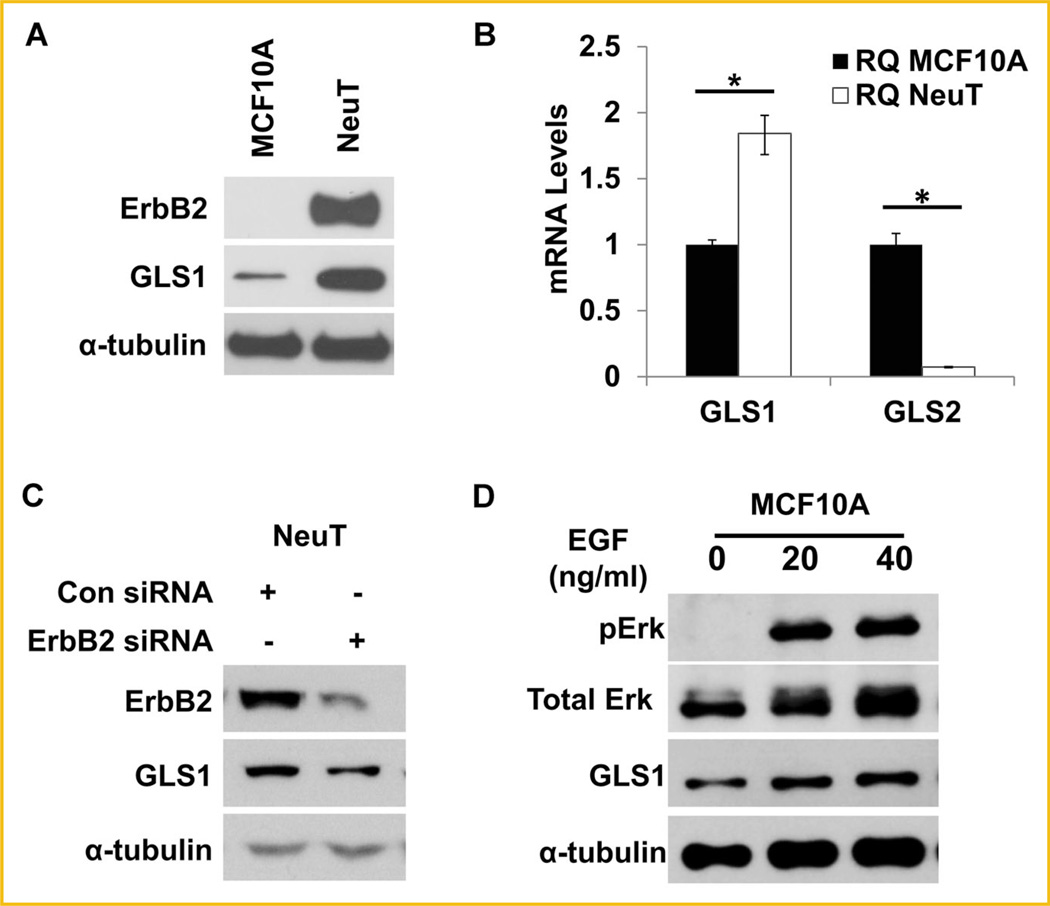
结果 ErbB2激活上调MCF10A细胞GLS1表达 癌基因和肿瘤抑制剂被提议用于调节葡萄糖和谷氨酰胺代谢[ Li等人,2012年 ; Qie等人,2012 ; Yin等人,2012年 ]. ErbB2作为一种导致大部分乳腺癌的癌基因,尚未研究其在乳腺癌细胞谷氨酰胺利用中的潜在作用。 为了探讨ErbB2激活是否在细胞致癌和代谢转化过程中对谷氨酰胺利用的调节中发挥作用,我们使用了非肿瘤性乳腺上皮细胞系MCF10A和转化的MCF10A-NeuT细胞系MCF1 0A-Neu T作为实验模型。 我们首先通过Western blotting比较了这对匹配细胞系中的GLS1蛋白水平,发现NeuT转化细胞显著增加了GLS1蛋白质( 图1A ). 实时qRT-PCR定量mRNA水平还显示,与MCF10A细胞相比,MCF10A-NeuT细胞中GLS1 mRNA水平升高,而GLS2 mRNA含量降低( 图1B ). 为了确定ErbB2激活是否与MCF10A-NeuT细胞中GLS1表达增加有关,我们使用ErbB2-siRNA敲除MCF10A-NeuT中的ErbB2,发现ErbB2-敲除降低了这些细胞中GLS2的表达( 图1C ). 为了进一步证实ErbB2激活正向调节GLS1,我们用EGF处理MCF10A细胞,EGF是一种天然生长因子,通过不同的机制结合并激活ErbB2。 EGF的作用通过Erk的磷酸化来表示( 图1D ). 正如预期的那样,EGF治疗增加了GLS1的表达( 图1D ),证实了配体介导的ErbB2通路激活也提高了GLS1水平。
图1。
ErbB2激活在mRNA和蛋白质水平上调GLS1的表达。 A: 对从MCF10A-NeuT及其亲本细胞系MCF10A制备的总细胞裂解物进行Western blotting分析。 同时检测ErbB2和GLS1,并使用α-微管蛋白作为负荷对照。 B: 实时PCR定量分析GLS mRNA水平。 从MCF10A和MCF10A-NeuT细胞中分离出总RNA样本,并反转录到cDNA。 通过qRT-PCR(ΔRQ)测定GLS1和GLS2在mRNA水平的表达。 所示误差条为标准偏差* P(P) < 0.05. C: ErbB2敲除降低MCF10A-NeuT细胞中GLS1的水平。 对照组和ErbB2特异性siRNA转染MCF10A-NeuT细胞。 制备转染后20小时的细胞裂解物,并用Western blots进行分析。 D: EGF处理后GLS1表达。 用指定剂量的EGF处理MCF10A。 处理后6小时收集细胞。 Western blot检测GLS1,pErk作为ErbB2信号通路激活的指标。
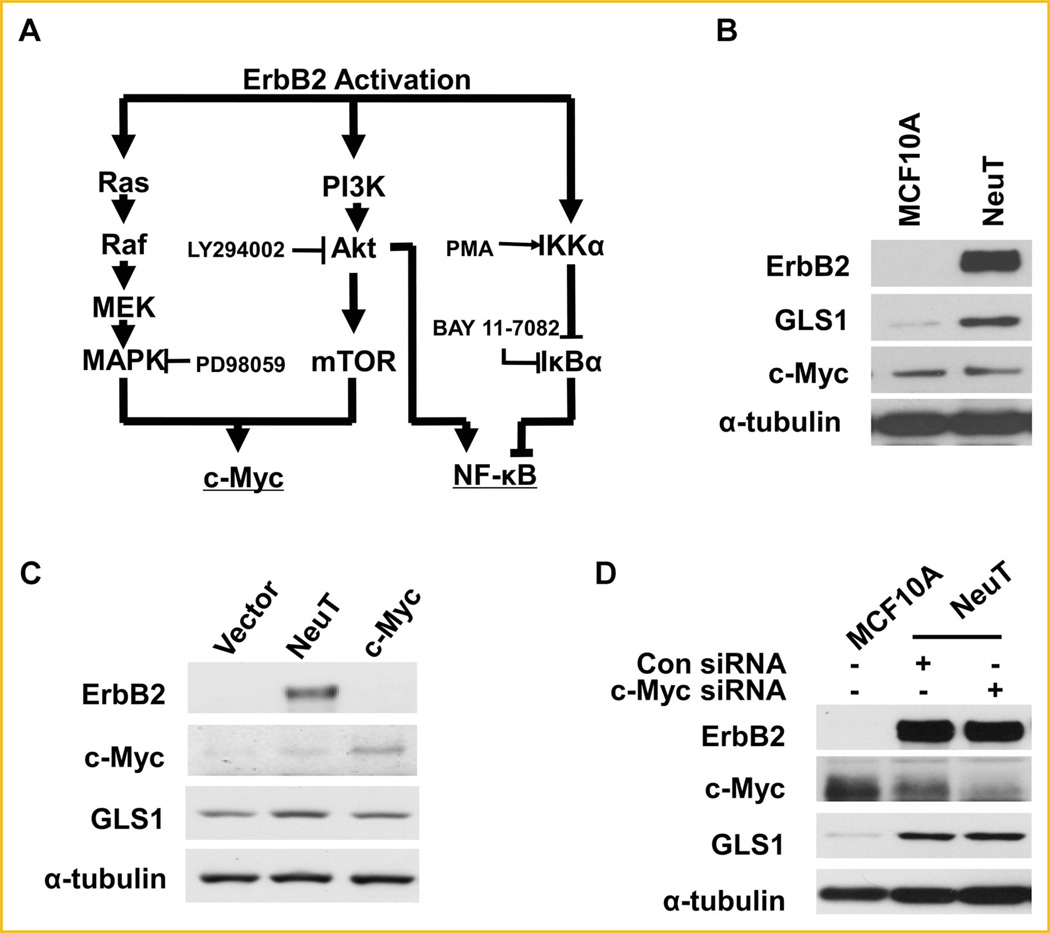
GLS1上调不涉及MCF10A-NEUT细胞中c-Myc的诱导 已有研究表明,c-Myc通过抑制miR-23a/b表达上调GLS1的表达[ Gao等人,2009年 ]. 据报道,ErbB2激活可激活MAPK和PI3K信号通路,共同增强c-Myc的表达,如图 图2A [ Neve等人,2000年 ]. 接下来我们询问ErbB2是否通过c-Myc诱导上调GLS1表达。 为了解决这个问题,我们通过Western blotting测定了MCF10A和MCF10A-NeuT细胞中的c-Myc水平。 我们发现,虽然MCF10A-NeuT转化细胞增加了GLS1,但与亲代MCF10A细胞相比,c-Myc表达水平没有受到影响( 图2B ). 为了进一步探讨c-Myc在MCF10A中GLS1表达中的作用,我们检测了稳定过度表达c-Myc的MCF10A细胞系中GLS1的水平。 Western blot显示MCF10A细胞中c-Myc的稳定过表达并没有增强GLS1的表达( 图2C ). 最后,c-Myc基因敲除并没有降低MCF10ANeuT细胞中GLS1的水平( 图2D ). 综上所述,这些数据表明c-Myc不太可能是MCF10A中GLS1的主要调节器,表明ErbB2激活可能通过与c-Myc不同的途径上调GLS1。
图2。
ErbB2增强的GLS1表达不涉及c-Myc。 A: ErbB2及其下游信号通路。 MAPK/Erk和PI3K/Akt通路是ErbB2激活的两条关键信号通路。 ErbB2可通过MAPK/Erk或PI3K/Akt或两者诱导c-Myc表达。 此外,ErbB2激活通过诱导IKK刺激NF-κB通路,而IKK与PI3K无关。 图中显示了所研究信号通路的抑制剂和激活剂。 PD98059是MAPK/Erk抑制剂; LY294002是Akt抑制剂; BAY 11-7082是一种NF-κB抑制剂; PMA是NF-κB激活剂。 (B) ErbB2不上调MCF10A-NeuT细胞中c-Myc的表达。 Western blotting分析测定MCF10A和MCF10A-NeuT细胞中ErbB2、GLS1和c-Myc的蛋白水平。 C: MCF10A细胞中稳定过度表达C-Myc未能上调GLS1。 D: c-Myc敲除不影响MCF10A-NeuT细胞中GLS1的表达。
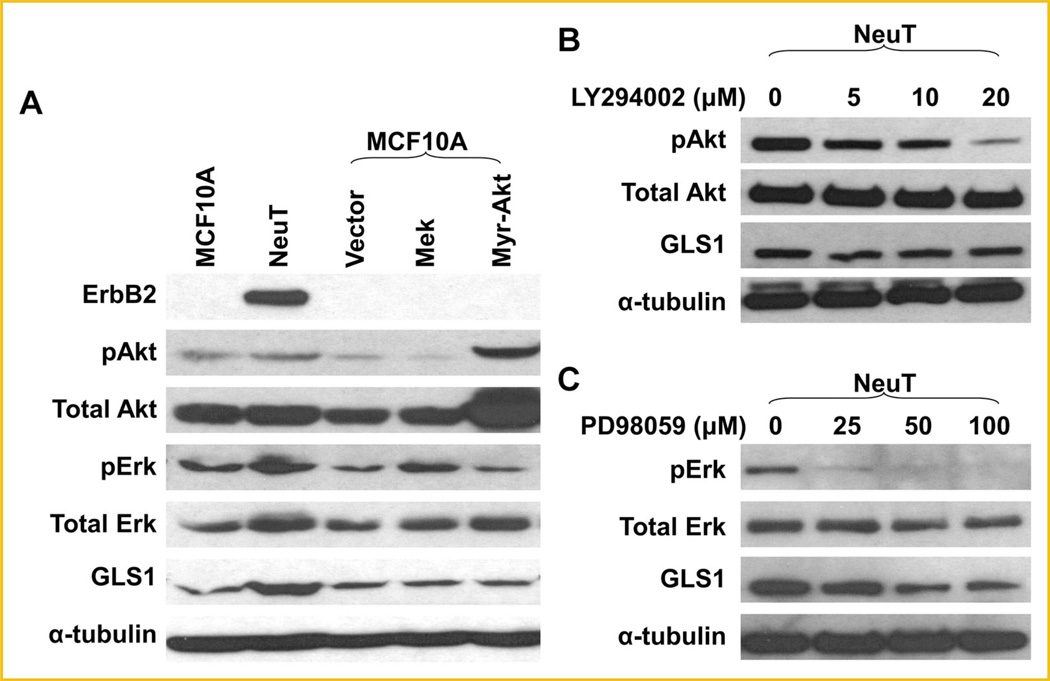
激活PI3K-AKT或MAPK/ERK不足以诱导GLS1表达 ErbB2激活通过激活MAPK/Erk和PI3k-Akt信号通路增强细胞存活、细胞周期进展和细胞增殖( 图2A ) [ Baselga和Swain,2009年 ]. 毫不奇怪,我们发现MCF10A-NeuT细胞的磷酸化MAPK/Erk和磷酸化Akt水平高于MCF10A细胞( 图3A ). 为了确定介导ErbB2诱导的GLS1上调的信号通路,我们继续研究PI3K-Akt或MAPK/Erk通路的激活是否足以刺激GLS1表达。 我们在MCF10A细胞中过度表达了MEK(Erk的上游激活激酶)和Myr-Akt(Akt的组成活性形式)。 我们观察到,无论哪种情况,GLS1水平都没有受到影响( 图3A ). 此外,用PI3K抑制剂LY294002处理细胞可抑制MCF10A NeuT细胞中Akt磷酸化,但不能抑制GLS1的表达( 图3B ). 然而,MAPK抑制剂PD98059抑制了MCF10A-NeuT细胞中Erk磷酸化和GLS1的表达( 图3C )提示维持GLS1表达需要MAPK信号的基础水平。 综上所述,这些结果表明,虽然GLS1表达似乎需要足够的MAPK信号,但仅激活MAPK或PI3K-Akt通路并不足以诱导MCF10A细胞中GLS1的表达。
图3。
激活PI3K-Akt或MAPK/Erk不足以增强GLS1的表达。 A: 用空载体瞬时转染MCF10A细胞中GLS1的表达,以及表达MEK或Myr-Akt的质粒。 蛋白质印迹显示MAPK/Erk或Akt途径的激活不足以上调GLS1。 B: 抑制PI3K通路并不抑制GLS1的表达。 在细胞收获和Western blotting分析之前,用0、5、10和20mM LY294002处理MCF10A-NeuT细胞24小时。 磷酸化Akt被检测为PI3K通路抑制的指示物。 C: 用0、25、50和100 mM PD98059处理MCF10A-NeuT细胞24小时。Erk激活和GLS1表达均受到抑制。
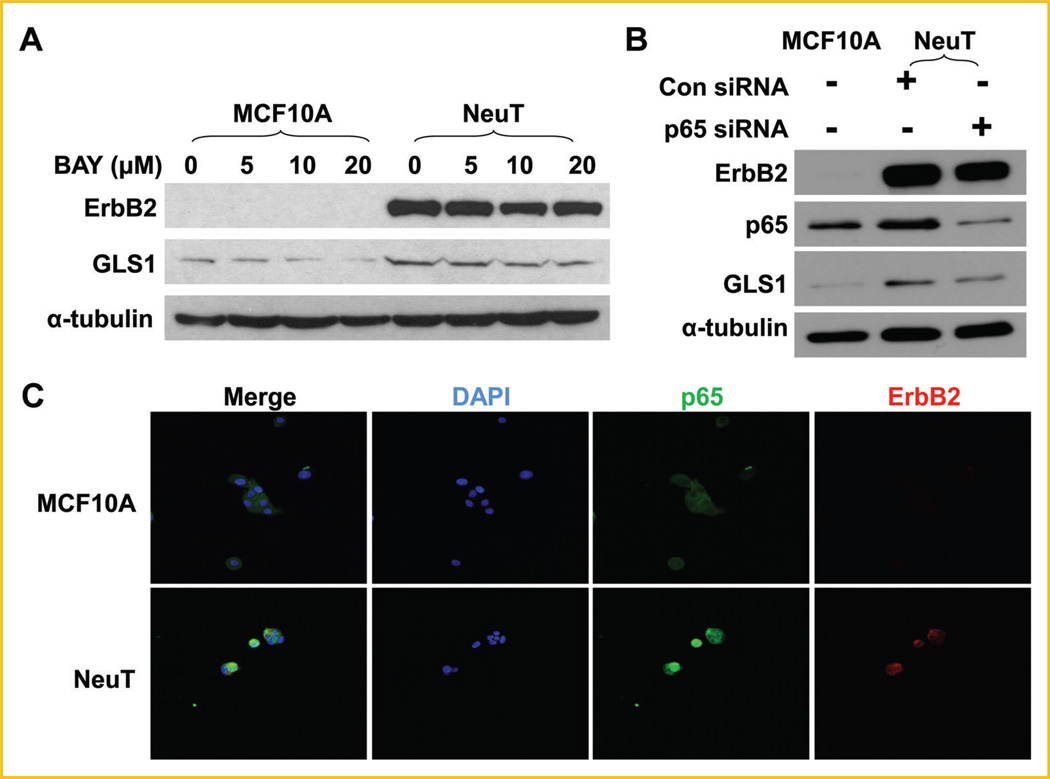
ErbB2通过激活NF-κB信号通路上调GLS1表达 除了MAPK和PI3K-Akt途径外,NF-κB被证明是ErbB2信号传导的介导者( 图2A ) [ Galang等人,1996年 ; Pianetti等人,2001年 ; Liu等人,2009年 ; Merkhofer等人,2010年 ]. 此外,最近的研究表明p65诱导GLS1的表达[ Wang等人,2010年 ; Rathore等人,2012年 ]. 因此,我们接下来测试NF-κB激活是否与ErbB2诱导的GLS1上调有关。 BAY 11-7082通过阻断IκB-α的磷酸化而选择性和不可逆地抑制NF-κB的活化,但不影响组成性IκBα的磷酸化合[ Pierce等人,1997年 ]. 我们用BAY 11-7082处理MCF10A和MCF10A-NeuT细胞,发现BAY 11-70 82降低了两种细胞系中GLS1的表达( 图4A ). 此外,用siRNA敲低p65可降低MCF10ANeuT细胞中GLS1的表达( 图4B ). 核移位是NF-κB活化的指标。 为了检测NeuT转化是否导致NF-κB活化,我们对p65进行免疫荧光染色以追踪其亚细胞定位。 我们发现MCF10A-NeuT的细胞核p65水平高于其亲本细胞系MCF10A( 图4C ). 综上所述,这些数据表明ErbB2激活促进p65激活,这是增强GLS1表达所必需的。
图4。
NF-κB通路参与MCF10A-NeuT细胞中GLS1的表达。 A: 用0、5、10和20mM的BAY 11-7082(BAY)处理MCF10A和MCF10A-NeuT细胞24 h,通过Western blotting分析测定GLS1的表达。 B: p65敲除下调MCF10A-NeuT细胞中的GLS1。 C: p65在MCF10A NeuT细胞中的核定位。 将MCF10A和MCF10A-NeuT细胞培养在八孔室玻片中,固定并染色p65、ErbB2和DNA(DAPI)。
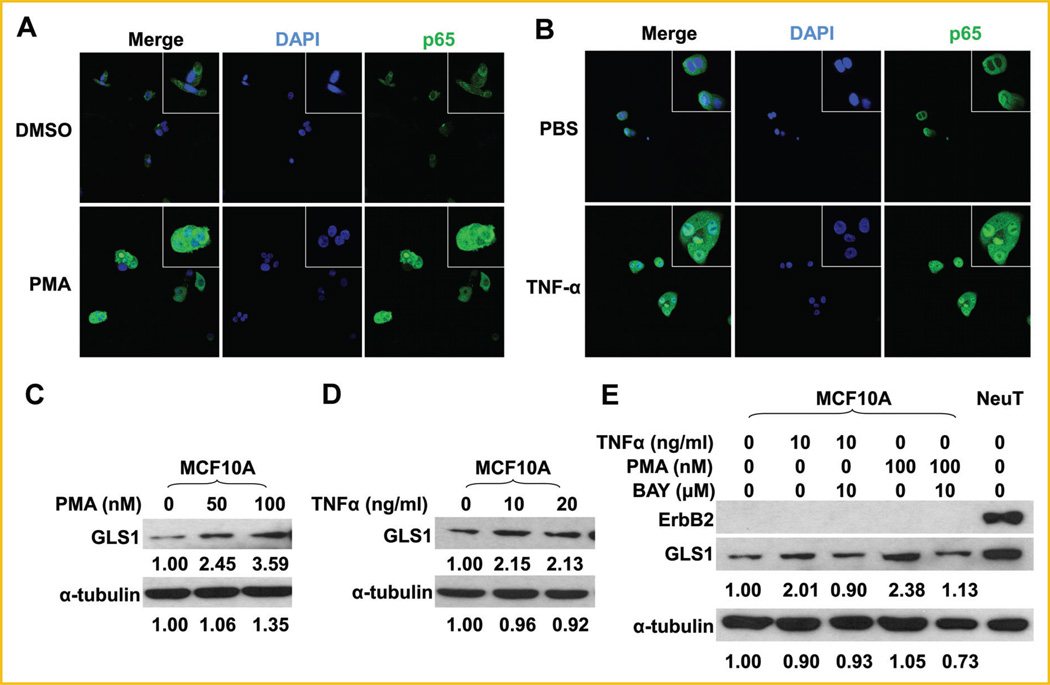
NF-κB的激活足以上调MCF10A细胞中GLS1的表达 为了解决NF-κB活化是否足以增强GLS1表达,我们接下来用两种研究良好的NF-κ子B活化剂PMA或TNF-α处理MCF10A细胞[ Conant等人,1994年 ]. 免疫荧光染色证实,PMA或TNF-α激活MCF10A细胞中的p65,如其核定位所示( 图5A、B ). NF-κB的两种激活剂均增强MCF10A细胞中GLS1的表达( 图5C、D )通过使用NF-κB抑制剂BAY 11-7082对MCF10A细胞进行预处理而消除( 图5E ). 综上所述,这些结果表明NF-κB激活足以增强MCF10A细胞中GLS1的表达。
图5。
激活p65足以上调MCF10A细胞中的GLS1。 A: 用100 nM的PMA在DMSO或DMSO中单独处理MCF10A细胞6小时,然后对p65进行免疫荧光染色。 B: 用20 ng/ml TNF-α在PBS或单独PBS中处理MCF10A细胞6 h,然后对p65进行免疫荧光染色。 C: MCF10A细胞用DMSO中的0、50或100nM PMA处理6小时。通过蛋白质印迹测定GLS1的表达。 D: 用0、10和20 ng/ml的TNF-α处理MCF10A细胞6 h,用Western blots检测GLS1的表达。 E: 用10mMof BAY 11-7082处理MCF10A细胞18小时,然后用10ng/ml TNF-α或100nM PMA再处理6小时。收集全细胞裂解物用于蛋白质印迹分析。 印迹下的数字是每个检测到的条带的量化; 对照组的GLS1或α-微管蛋白设置为1.00,并将治疗组与对照组进行比较。
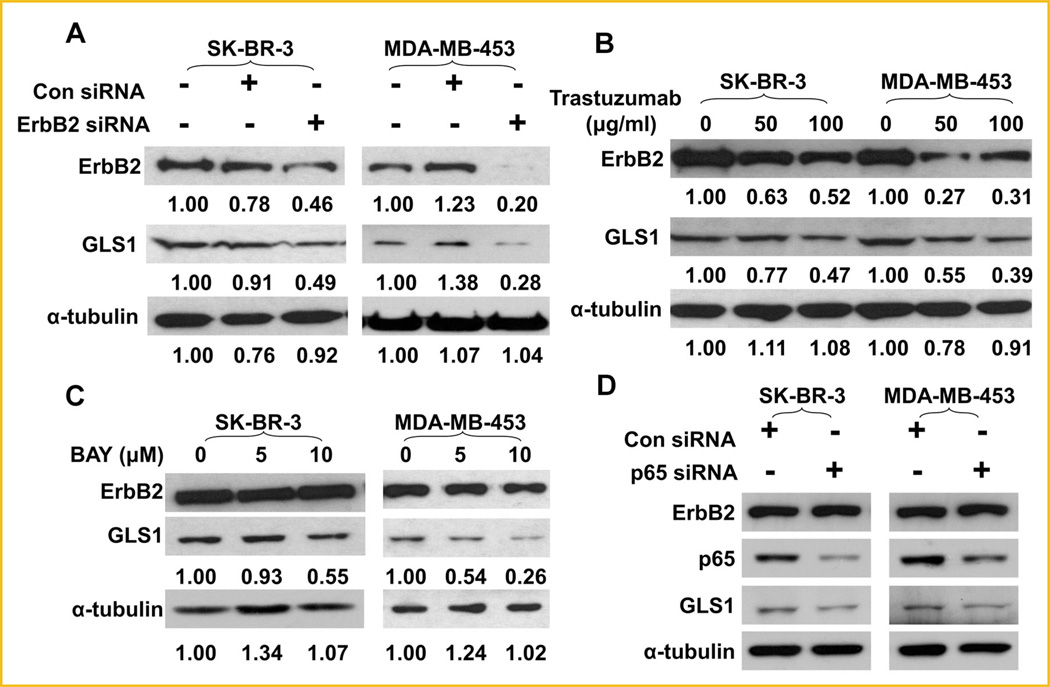
人乳腺癌细胞中GLS1的ErbB2依赖性表达 为了进一步探索ErbB2激活在调节人类乳腺癌细胞中GLS1表达中的作用,我们检测了ErbB2阳性SK-BR-3和MDA-MB-453细胞中GLS1的水平,并证实了这两种细胞系中GLS1的高水平(补充数据,图S1)。 我们使用ErbB2 siRNA敲低了SK-BR-3和MDA-MB-453细胞中ErbB2的表达,并观察到ErbBB2敲低显著降低了这些细胞中GLS1的表达( 图6A ). 曲妥珠单抗是一种重组人源化IgG 1 直接结合ErbB2胞外结构域并抑制其激活的单克隆抗体[ 戈登堡,1999 ]. 为了排除与siRNA敲除相关的潜在非靶向效应,我们还使用曲妥珠单抗治疗SK-BR-3和MDA-MB-453细胞。 我们发现曲妥珠单抗治疗降低了SKBR-3和MDA-MB-453细胞中的GLS1水平( 图6B ). 我们还注意到曲妥珠单抗导致ErbB2减少,这是以前研究中报道的现象[ Raja等人,2008年 ; 巴黎等,2010年 ]. 重要的是,BAY 11-7082和p65敲除也降低了SK-BR-3和MDA-MB-453细胞中GLS1的表达( 图6C、D ),证实p65是ErbB2诱导GLS1表达的关键介质。 综上所述,这些数据表明ErbB2增强、NF-κB介导的GLS1表达可能是某些乳腺癌细胞的共同特征,而不是仅适用于MCF10A细胞系的特殊发现。
图6。
抑制ErbB2下调人类乳腺癌细胞中GLS1的表达。 A: ErbB2的敲除下调SK-BR-3和MDA-MB-453细胞中GLS1的水平。 转染后24小时,用Western blots检测SK-BR-3和MDA-MB-453细胞中ErbB2和GLS1的蛋白水平。 B: 曲妥珠单抗抑制GLS1的表达。 用曲妥珠单抗(50或100 mg/ml)处理SK-BR-3和MDA-MB-453细胞24小时。通过Western blotting测定ErbB2和GLS1的蛋白质水平。 印迹下的数字是每个检测到的条带的量化; 对照组的ErbB2、GLS1或α-微管蛋白设置为1.00,治疗组与对照组进行比较。 C、 D:抑制或敲低p65可降低ErbB2阳性乳腺癌细胞中GLS1的表达。 SK-BR-3和MDA-MB-453细胞中的NF-κB活性受到5和10mM BAY 11-7082处理细胞或siRNA敲除的抑制。 通过Western blotting分析监测GLS1表达水平和p65敲除效应。
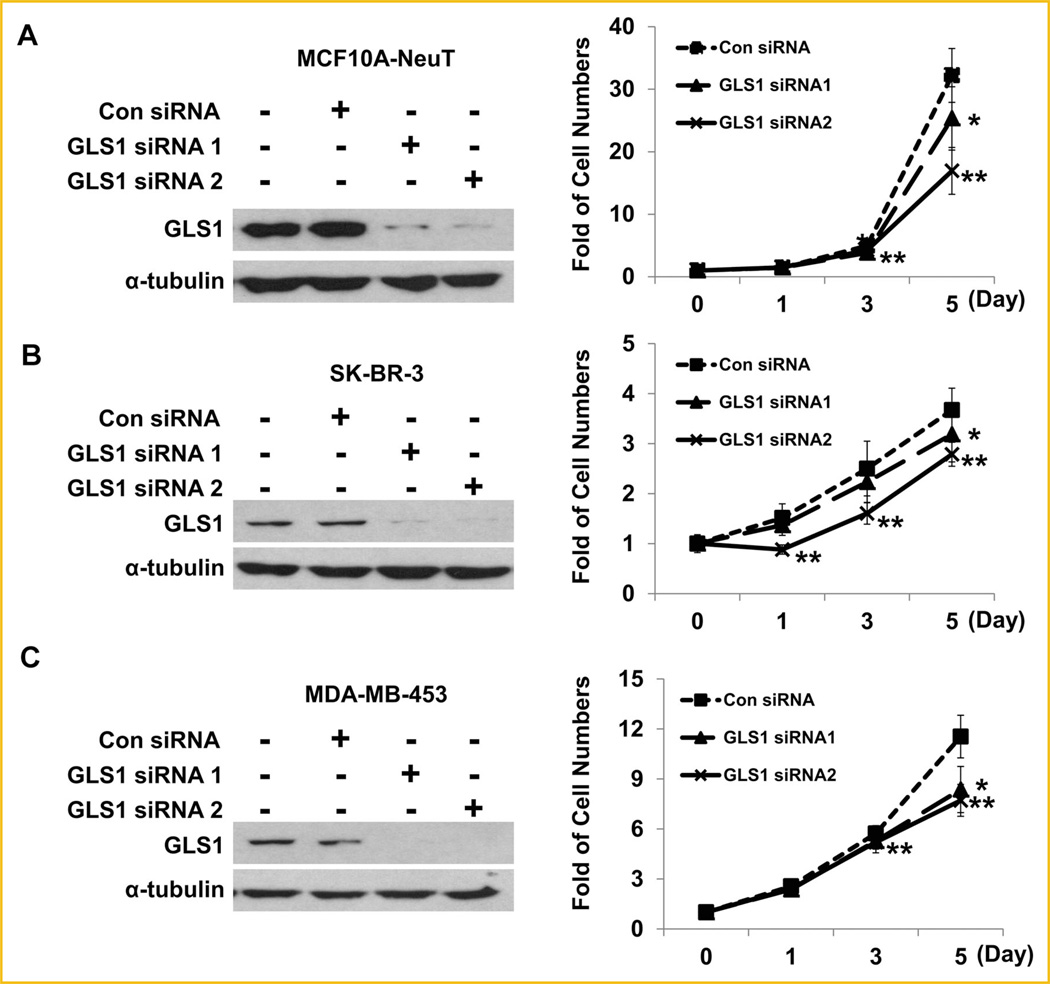
GLS1敲除抑制乳腺癌细胞增殖 在生化方面,一些代谢酶可以过度表达,因此增加表达可能不会影响代谢动力学和细胞过程。 为了确定ErbB2增强的GLS1表达水平是否有助于乳腺癌细胞增殖,我们使用了两种不同的GLS1-siRNA来降低GLS1水平。 通过Western blotting在MCF10A-NeuT、SK-BR-3和MDA-MB-453细胞中证实GLS1敲除( 图7A –C,左侧面板)。 细胞增殖分析显示GLS1敲除显著抑制细胞生长速率( 图7A–C ,右侧面板)。 这些数据表明,ErbB2激活引起的GLS1表达增加确实促进了细胞增殖率。
图7。
GLS1敲除可降低MCF10A-NeuT、SK-BR-3和MDA-MB-453细胞的增殖率。 A–C:Western blots显示了MCF10A-NeuT(A)、SK-BR-3(B)和MDA-MB-453(C)细胞中两种不同GLS1 siRNA的敲除作用(左侧面板)。 MCF10A-NeuT、SK-BR-3和MDA-MB-453细胞的细胞增殖曲线如右图所示* P(P) GLS1 siRNA1组与对照siRNA组的差异<0.05** P(P) GLS1 siRNA2组与对照siRNA组的差异<0.05。
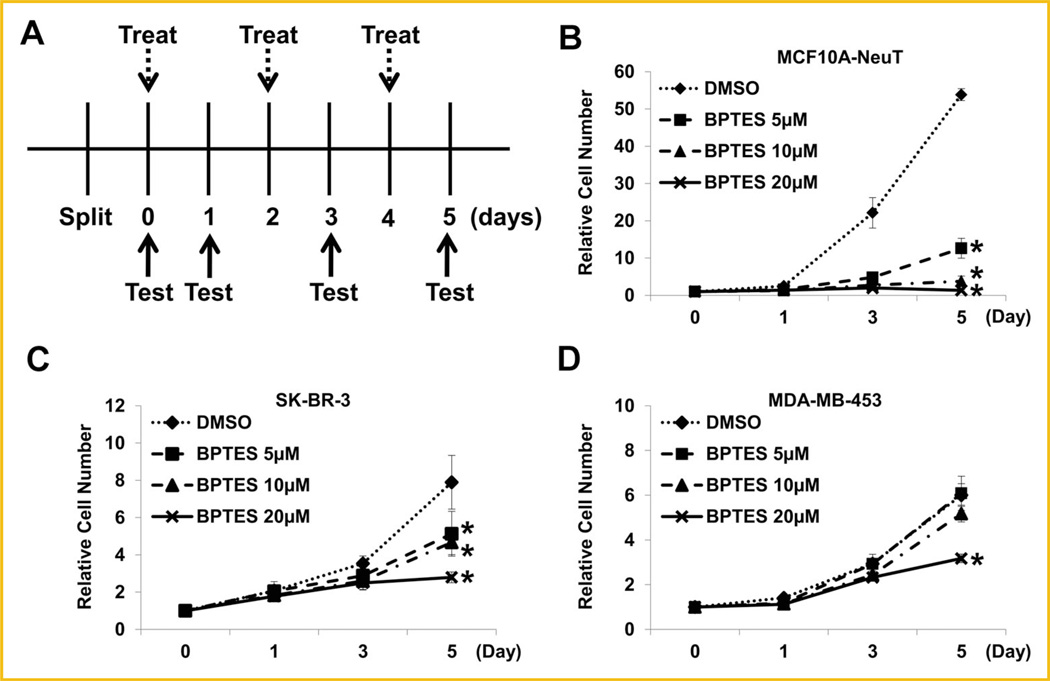
GLS1抑制剂抑制乳腺癌细胞增殖 BPTES被用作抑制GLS1活性的抑制剂[ Robinson等人,2007年 ; Le等人,2012年 ]. 为了进一步证实GLS1活性在乳腺癌细胞增殖中的作用,我们还检测了BPTES对ErbB2阳性乳腺癌细胞株的影响。 治疗计划如所示 图8A 对不同方案下细胞生长曲线的分析表明,BPTES治疗(≥5µM)显著抑制MCF10A-NeuT细胞增殖( 图8B ). 高浓度(20µM)的BPTES也抑制了两种ErbB2阳性乳腺癌细胞系SK-BR-3和MDA-MB-453( 图8C、D ). 这些数据为GLS1活性增强可能促进乳腺癌细胞增殖提供了额外证据。
图8。
小分子化合物BPTES抑制ErbB2阳性人类乳腺癌细胞的增殖。 A: BPTES治疗示意图。 使用的BPTES浓度为:0、5、10和20mM。 治疗:更换含有指定浓度BPTES的培养基。 测试:细胞数测定。 B–D:BPTES对MCF10A-NeuT细胞(B)、SK-BR-3细胞(C)和MDA-MB-453细胞(D)增殖率的影响。
讨论 谷氨酰胺分解和Warburg效应是肿瘤细胞最显著的两个代谢特征,代表着氮和碳源利用的改变,以促进代谢转化。 Warburg效应定义了肿瘤细胞线粒体氧化磷酸化向糖酵解的转变[ Vander Heiden等人,2009年 ; Dang,2010年 ],促进涉及碳代谢产物的增殖生物合成。 谷氨酰胺在生物体内被认为是一种非必需氨基酸,因为它可以在许多组织中合成。 尽管谷氨酰胺在所有氨基酸中的血清浓度最高,但在高度增殖的肿瘤细胞中,谷氨酰胺的需求可能会超过其供应[ DeBerardinis和Cheng,2010年 ]. 谷氨酰胺在支持肿瘤细胞生存和增殖方面的重要性已得到充分证明[ Kita等人,2007年 ; Yueva等人,2007年 ; Gao等人,2009年 ]. 培养基中缺乏谷氨酰胺通常会导致氨基酸缺乏应激、内质网应激,最终导致生长停滞和细胞死亡[ Qie等人,2012年 ]. 除了作为碳源外,谷氨酰胺还被证明是主要的氮源[ Meng等人,2010年 ]. 事实上,谷氨酰胺是谷氨酸的主要前体; 谷氨酰胺和谷氨酸都参与多种含氮生物分子的生物合成[ Meng等人,2010年 ]. 值得注意的是,增殖细胞需要积极合成氮基、谷胱甘肽、鸟氨酸、多胺和其他非必需氨基酸。 由于大多数类型的细胞不能有效地吸收谷氨酸,谷氨酰胺对这些细胞通过谷氨酰胺水解维持其细胞内谷氨酸水平至关重要。 有人提出,“谷氨酸-α-酮戊二酸循环”在维持细胞内非必需氨基酸库的动态平衡以支持生物合成过程中起着重要作用[ Meng等人,2010年 ]. 代谢途径分析表明,快速增殖的细胞需要增加丝氨酸、天冬氨酸和甘氨酸的合成; 谷氨酸是其生物合成的主要氨基供体。 因此,作为快速增殖的细胞,肿瘤细胞要求增加谷氨酰胺的供应和利用,限制谷氨酰胺的利用可能会抑制肿瘤细胞的增殖[ Reitzer等人,1979年 ; Turowski等人,1994年 ; DeBerardinis等人,2008年 ; Levine和Puzio-Kuter,2010年 ; Meng等人,2010年 ; Dang等人,2011年 ; Shanware等人,2011年 ].
Myc是第一个通过重新编程与谷氨酰胺代谢相关的基因表达促进谷氨酰胺利用的癌基因,包括谷氨酰胺转运体和GLS1[ 汤普森等人,2008年 ]. 尤其是,谷氨酰胺水解率与GLS1水平相关。 ErbB2激活是乳腺癌细胞的重要致癌途径。 在这项研究中,我们发现ErbB2的激活与乳腺癌细胞中GLS1水平的增加有关。 ErbB2敲低降低了NeuT转化的乳腺上皮细胞和两种ErbB2阳性的人类乳腺癌细胞系中GLS1的表达,证实了ErbB2激活和GLS1表达之间的联系。 总之,我们的数据表明一种新的致癌信号通路可能促进谷氨酰胺在致瘤过程中的利用。
ErbB2在机械上激活了几个下游信号通路。 两条主要的下游途径是MAPK/Erk和PI3K-Akt途径[ 海恩斯和莱恩,2005年 ; 海恩斯和麦克唐纳,2009年 ]. 据报道,在其他实验环境中,ErbB2激活这两条通路可诱导c-Myc的表达[ Olayioye等人,2000年 ]; 然而,我们的结果显示,与MCF10A细胞相比,MCF10A-NeuT细胞中的c-Myc没有明显上调。 更重要的是,在MCF10A细胞中过度表达c-Myc并没有增强GLS1的表达。 为什么c-Myc状态不影响GLS1在该细胞系中的表达仍不清楚。 我们还评估了MAPK/Erk和PI3K/Akt通路在GLS1上调中的作用。 我们的结果表明,PI3K-Akt途径不参与这一过程; 与先前的报告一致,谷氨酰胺水解独立于PI3K-Akt的激活[ 汤普森等人,2008年 ]. 抑制MAPK/Erk通路可降低MCF10A-NeuT细胞中GLS1的表达,但MEK的过度激活未能诱导GLS1上调,这表明需要足够的MAPK/Erk信号传导,但不足以刺激肿瘤细胞中谷氨酰胺的利用。
我们和其他人已经证明ErbB2激活NF-κB信号传导[ Galang等人,1996年 ; Pianetti等人,2001年 ; Liu等人,2009年 ; Merkhofer等人,2010年 ]. ErbB2如何激活NF-κB尚不清楚。 Pianetti等人[2001] 据报道,ErbB2通过PI3K-Akt激活NF-κB,其可被PTEN抑制,并由钙蛋白酶而非IκB复合物介导。 Merkhofer等人[2010] 据报道,NF-κB的ErbB2激活需要IKKα以PI3K-Akt非依赖性的方式进行。 我们在这里报道的结果支持NF-κB的PI3K-Akt非依赖性激活,其潜在的分子机制尚待阐明。
NF-κB介导的GLS1调控的精确作用模型也尚不明确。 最近有报道称NF-κB通过抑制miR-23a以c-Myc依赖的方式调节谷氨酰胺代谢[ Rathore等人,2012年 ]. 独立研究表明,抑制剂或siRNA抑制NF-κB可降低癌细胞中的GLS1[ 埃里克森和塞里昂,2010年 ; Wang等人,2010年 ]. 这些最近的独立研究提供了额外的证据来支持我们的发现,即NF-κB介导ErbB2信号传导并上调GLS1表达,如补充图S2所示。 然而,我们发现ErbB2敲除并不影响miR-23a/b水平(数据未显示)。 此外,生物信息学分析显示没有证据支持NF-κB可能直接与GLS1启动子/增强子相互作用。 众所周知,NF-κB是一种多效性转录因子,控制大量与细胞生存、增殖、凋亡和免疫反应相关的基因的表达[ 斯利瓦斯塔瓦和拉马纳,2009年 ]. 据报道,NF-κB活化促进葡萄糖摄取,触发氧化磷酸化向糖酵解的转换,从而增强肿瘤发生[ 川内等人,2008 ; Jin等人,2010年 ]. NF-κB是否通过间接代谢链接增强GLS1的表达尚待研究。
我们还研究了GLS1活性对ErbB2阳性细胞增殖的影响。 BPTES是GLS1的非竞争性抑制剂,抑制GLS1活性并导致细胞谷氨酸消耗[ 库尼等人,1976年 ; Lebedeva等人,1986年 ]. BPTES治疗降低ErbB2阳性人乳腺癌细胞的肿瘤细胞增殖。 这些表明,GLS1活性增强不仅是ErbB2介导的恶性转化的副作用,而且是其重要组成部分。 因此,如果体内研究进一步证实,我们的数据可能表明NF-κB信号通路和GLS1活性都是ErbB2阳性乳腺癌预防和治疗的潜在靶点。
由于代谢转化是致癌信号通路引起恶性转化的生化基础,因此需要注意的是ErbB2-NF-κB轴可能仅代表调节谷氨酰胺利用的这些途径之一; 除c-Myc和ErbB2外,其他致癌信号通路也可能影响GLS1的表达和谷氨酰胺的利用。 此外,基于乳腺癌细胞系的这些发现尚待体内肿瘤模型进一步验证。 然而,我们已经证明,ErbB2的激活通过NF-κB上调GLS1的表达,谷氨酰胺酶表达的增加促进了细胞培养中ErbB2阳性乳腺癌细胞的增殖。 因此,如果通过体内模型验证,谷氨酰胺的利用可能被探索为预防和治疗乳腺癌的一个新的生化靶点。
致谢 我们感谢R.Pestell博士(K.C.C.,T.J.U.)提供MCF10A和MCF10A-NeuT细胞系,M.Reginato博士(DUCOM)提供初始研究和有益讨论所需的细胞裂解液,K.L.Guan博士(UCSD)提供pCMV。 MEK1质粒和P.N.Tsichlis博士(塔夫茨大学医学院)提供Akt-Myr质粒。 Clarissa Chu是德雷克塞尔大学资助的STAR学者。
资助方:NCI、美国国立卫生研究院(NIH); 拨款编号:R01-CA129494; 赠款赞助商:德雷克塞尔大学。
缩写
阿克特 v-akt小鼠胸腺瘤病毒癌基因同源物
ERBB2号机组 v-erb-b2红细胞白血病病毒癌基因同源物2
GLS公司 谷氨酰胺酶
HER2型 人表皮生长因子受体2
MAPK/Erk公司 丝裂原活化激酶样蛋白
c-Myc公司 v-myc骨髓细胞瘤病病毒癌基因同源物(禽)
核因子-κB B细胞kappa轻多肽基因增强子的核因子
PI3K系列 磷脂酰肌醇-4,5-二磷酸3-激酶
定量RT-PCR 定量逆转录聚合酶链反应
脚注
支持信息
其他支持信息可以在出版商的网站上找到本文的在线版本。
参考文献
Ahmed NN、Grimes HL、Bellacosa A、Chan TO、Tsichlis PN。通过Akt蛋白激酶转导白细胞介素-2抗凋亡和增殖信号。 美国国家科学院院刊1997; 94:3627–3632. doi:10.1073/pnas.94.8.3627。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Aledo JC、Gomez-Fabre PM、Olalla L、Marquez J.两个人类谷氨酰胺酶基因座的鉴定和两个相关基因的组织特异性表达。 哺乳动物基因组。 2000; 11:1107–1110. doi:10.1007/s003350010190。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Baselga J,Swain SM。新的抗癌靶点:重访ERBB2和发现ERBB3。 Nat Rev癌症。 2009; 9:463–475. doi:10.1038/nrc2656。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Borrello MG,Degl’Inocenti D,Pierotti MA。炎症与癌症:肿瘤驱动的联系。 癌症快报。 2008; 267:262–270. doi:10.1016/j.canlet.2008.03.060。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
乳腺癌:现状与未来展望。 2011年乳腺癌研究; 13:113. doi:10.1186/bcr3045。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Conant K、Atwood WJ、Traub R、Tornatore C、Major EO。 与HIV-1 LTR结合的p50/p65 NF-κB的增加不足以增加人类原代星形胶质细胞中的病毒表达。 病毒学。 1994; 205:586–590. doi:10.1006/viro.1994.1685。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Cooney DA、Jayaram HN、Milman HA、Homan ER、Pittillo R、Geran RI、Ryan J、Rosenbluth RJ.DON、CONV和DONV-III。药理学和毒理学研究。 生物化学药理学。 1976; 25:1859–1870. doi:10.1016/0006-2952(76)90190-8。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
谷氨酸水解:为癌细胞提供碳或氮,还是两者兼而有之? 细胞周期。 2010; 9:3884–3886. doi:10.4161/cc.9.13302。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Dang CV,Hamaker M,Sun P,Le A,Gao P。癌细胞代谢的治疗靶向性。 《分子医学杂志》(柏林)2011; 89:205–212. doi:10.1007/s00109-011-0730-x。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
de la Rosa V、Campos-Sandoval JA、Martin-Rufian M、Cardona C、Mates JM、Segura JA、Alonso FJ、Marquez J.哺乳动物组织中的一种新型谷氨酰胺酶亚型。 神经化学国际2009; 55:76–84. doi:10.1016/j.neuint.2009.02.021。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
DeBerardinis RJ,Cheng T.Q的下一篇:谷氨酰胺在代谢、细胞生物学和癌症中的多种功能。 致癌物。 2010; 29:313–324. doi:10.1038/onc.2009.358。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
DeBerardinis RJ、Sayed N、Ditsworth D、Thompson CB。 一砖一瓦:新陈代谢和肿瘤细胞生长。 2008年通用操作技术开发; 18:54–61. doi:10.1016/j.gde.2008.02.003。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Dizdar O,Altundag K。转移性乳腺癌的新兴药物。 专家操作紧急药物。 2009; 14:85–98. doi:10.1517/14728210802625671。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
埃里克森·JW,Cerione RA。 谷氨酰胺酶:调节癌细胞代谢的热点? Oncotarget公司。 2010; 1:734–740. doi:10.18632/onctarget.208。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Ertel A、Dean JL、Rui H、Liu C、Witkiewicz AK、Knudsen KE、Knudsen ES。乳腺癌RB途径破坏:与疾病亚型、疾病特异性预后和治疗反应的差异性关联。 细胞周期。 2010; 9:4153–4163. doi:10.4161/cc.9.20.13454。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Galang CK、Garcia-Ramirez J、Solski PA、Westwick JK、Der CJ、Neznanov NN、Oshima RG、Hauser CA。癌基因Neu/ErbB-2增加ets、AP-1和NF-kappaB-依赖的基因表达,并抑制ets激活阻止Neu-mediated细胞转化。 生物化学杂志。 1996; 271:7992–7998. doi:10.1074/jbc.271.14.7992。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Gao P、Tchernyshyov I、Chang TC、Lee YS、Kita K、Ochi T、Zeller KI、De Marzo AM、Van Eyk JE、Mendell JT、Dang CV.c-Myc对miR-23a/b的抑制增强了线粒体谷氨酰胺酶的表达和谷氨酰胺代谢。 自然。 2009; 458:762–765. doi:10.1038/nature07823。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Goldenberg MM.Trastuzumab,一种重组DNA衍生的人源化单克隆抗体,一种治疗转移性乳腺癌的新药物。 临床治疗学。 1999; 21:309–318. doi:10.1016/S0149-2918(00)88288-0。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Gomez-Fabre PM、Aledo JC、Del Castillo-Olivares A、Alonso FJ、Nunez De Castro I、Campos JA、Marquez J.人类乳腺癌细胞谷氨酰胺酶的分子克隆、测序和表达研究。 《生物化学杂志》2000; 345(第2部分):365-375。 [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Guarneri V、Barbieri E、Dieci MV、Piacentini F、Conte P.HER2阳性乳腺癌的抗-HER2新辅助和辅助治疗。 《癌症治疗》2010年修订版; 36(增刊3):S62–S66。 doi:10.1016/S0305-7372(10)70022-0。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Hynes东北,Lane HA。 ERBB受体与癌症:靶向抑制剂的复杂性。 Nat Rev癌症。 2005; 5:341–354. doi:10.1038/nrc1609。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Hynes NE、MacDonald G.ErbB受体和癌症中的信号通路。 当前操作细胞生物学。 2009; 21:177–184. doi:10.1016/j.ceb.2008.12.010。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Jin HC、Liu X、Wang X、Zhang J、Lam EKY、Shin VY、Cheng ASL、Yu J、Chan FKL、Sung JJY。 Warburg效应重温:糖酵解和胃癌发生之间的表观遗传联系。 致癌物。 2010; 29:442–450. doi:10.1038/onc.2009.332。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Kawauchi K、Araki K、Tobiume K、Tanaka N。p53通过IKK-NF-kappaB途径调节葡萄糖代谢并抑制细胞转化。 自然细胞生物学。 2008; 10:611–618. doi:10.1038/ncb1724。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Kita K,Suzuki T,Ochi T.二苯胂酸(一种化学战剂降解产物)对人肝癌细胞中谷氨酰胺酶C的下调作用。 毒理学应用药理学。 2007; 220:262–270. doi:10.1016/j.taap.2007.01.009。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Le A、Lane AN、Hamaker M、Bose S、Gouw A、Barbi J、Tsukamoto T、Rojas CJ、Slusher BS、Zhang H、Zimmerman LJ、Liebler DC、Slebos RJ、Lorkiewicz PK、Higashi RM、Fan TW、Dang CV。通过TCA循环促进B细胞增殖和存活的葡萄糖非依赖性谷氨酰胺代谢。 单元格元数据。 2012; 15:110–121. doi:10.1016/j.cmet.2011.12.009。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Lebedeva ZI、Kabanova EA、Berezov TT.6-二唑-5-氧代-L-诺亮氨酸和氮杂丝氨酸作为谷氨酰胺(天冬酰胺)酶的亲和力抑制剂。 生物化学国际1986; 12:413–420. [ 公共医学 ] [ 谷歌学者 ]
Levine AJ,Puzio-Kuter AM。癌基因和抑癌基因对癌症代谢开关的控制。 科学。 2010; 330:1340–1344. doi:10.1126/science.1193494。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Li W,Tai Y,Zhou J,Gu W,Bai Z,Zhow T,Zhong Z,McCue PA,Sang N,Ji JY,Kong B,Jiang J,Wang C.通过靶向SREBP1和脂肪生成抑制子宫内膜肿瘤生长。 细胞周期。 2012; 11:2348–2358. doi:10.4161/cc.20811。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Liu M、Ju X、Willmarth NE、Casimiro MC、Ojeifo J、Sakamaki T、Katiyar S、Jiao X、Popov VM、Yu Z、Wu K、Joyce D、Wang C、Pestell RG。 核因子-kappaB增强体内ErbB2诱导的乳腺肿瘤发生和新生血管生成。 《美国病理学杂志》。 2009; 174:1910–1920. doi:10.2353/ajpath.2009.080706。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Meng M,Chen S,Lao T,Liang D,Sang N.氮合成代谢是谷氨酰胺分解在增殖细胞中的重要性的基础。 细胞周期。 2010; 9:3921–3932. doi:10.4161/cc.9.13139。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Merkhofer EC、Cogswell P、Baldwin AS。Her2激活NF-kappaB并通过涉及IKKalpha的经典途径诱导侵袭。 致癌物。 2010; 29:1238–1248. doi:10.1038/onc.2009.410。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Neve RM、Sutterluty H、Pullen N、Lane HA、Daly JM、Krek W、Hynes NE。致癌ErbB2对乳腺癌细胞G1细胞周期调节因子的影响。 致癌物。 2000; 19:1647–1656. doi:10.1038/sj.onc.1203470。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Olayioye MA、Neve RM、Lane HA、Hynes NE。ErbB信号网络:发育和癌症中的受体异二聚体。 EMBO J.2000; 19:3159–3167. doi:10.1093/emboj/19.13.3159。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Paris L、Cecchetti S、Spadaro F、Abalsamo L、Lugini L、Pisanu ME、Iorio E、Natali PG、Ramoni C、Podo F。磷脂酰胆碱特异性磷脂酶C的抑制下调乳腺癌细胞质膜上HER2的过度表达。 2010年乳腺癌研究; 12:R27。 doi:10.1186/bcr2575。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Pianetti S、Arsura M、Romieu-Mourez R、Coffey RJ、Sonenshein GE。Her-2/neu过度表达通过PI3-激酶/Akt途径诱导NF-kappaB,该途径涉及钙蛋白酶介导的IkappaB-α降解,可被肿瘤抑制因子PTEN抑制。 致癌物。 2001; 20:1287–1299. doi:10.1038/sj.onc.1204257。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Pierce JW、Schoenleber R、Jesmok G、Best J、Moore SA、Collins T、Gerritsen ME。细胞因子诱导的IkappaBalpha磷酸化和内皮细胞粘附分子表达的新型抑制剂在体内表现出抗炎作用。 生物化学杂志。 1997; 272:21096–21103. doi:10.1074/jbc.272.34.21096。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Qie S,Liang D,Yin C,Gu W,Meng M,Wang C,Sang N.谷氨酰胺消耗和葡萄糖消耗通过独特的基因表达重编程触发生长抑制。 细胞周期。 2012; 11:3679–3690. doi:10.4161/cc.21944。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Raja SM、Clubb RJ、Bhattacharyya M、Dimri M、Cheng H、Pan W、Ortega-Cava C、Lakku-Reddi A、Naramura M、Band V、Band H。Trastuzumab和17-AAG的联合诱导ErbB2过表达乳腺癌细胞中泛素化和溶酶体途径依赖的ErbB_2降解和细胞毒性增强。 癌症生物治疗。 2008; 7:1630–1640. doi:10.4161/cbt.7.10.6585。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Rana A、Rangasamy V、Mishra R。雌激素如何刺激乳腺癌。 未来Oncol。 2010; 6:1369–1371. doi:10.2217/fon.10.112。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Rathore MG、Saumet A、Rossi JF、de Bettignies C、Tempe D、Lecellier CH、Villalba M。NF-kappaB成员p65通过miR-23a控制谷氨酰胺代谢。 国际生物化学与细胞生物学杂志。 2012; 44:1448–1456. doi:10.1016/j.biocel.2012.05.011。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Reitzer LJ、Wice BM、Kennell D。谷氨酰胺而非糖是培养HeLa细胞的主要能量来源的证据。 生物化学杂志。 1979; 254:2669–2676. [ 公共医学 ] [ 谷歌学者 ]
Robinson MM,McBryant SJ,Tsukamoto T,Rojas C,Ferraris DV,Hamilton SK,Hansen JC,Curthoys NP.双-2-(5-苯基乙酰氨基-1,2,4-噻二唑-2-基)乙基硫醚(BPTES)生物化学杂志2007抑制大鼠肾脏型谷氨酰胺酶的新机制; 406:407–414. doi:10.1042/BJ20070039。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Sang N,Stiehl DP,Bohensky J,Leshchinsky I,Srinivas V,Caro J.MAPK信号通过其对p300的影响上调低氧诱导因子的活性。 生物化学杂志。 2003; 278:14013–14019. doi:10.1074/jbc。 M209702200。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Shanware NP、Mullen AR、DeBerardinis RJ、Abraham RT。谷氨酰胺:在肿瘤生长和应激抵抗中的多效性作用。 《分子医学杂志》(柏林)2011; 89:229–236. doi:10.1007/s00109-011-0731-9。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Slamon DJ、Clark GM、Wong SG、Levin WJ、Ullrich A、McGuire WL。 人类乳腺癌:复发和存活与HER-2/neu癌基因扩增的相关性。 科学。 1987; 235:177–182. doi:10.1126/science.3798106。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Srivastava SK,Ramana KV。聚焦分子:核因子-kappaB。 Exp-Eye Res.2009; 88:2–3. doi:10.1016/j.exer.2008.03.012。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Thompson CB、Wise DR、DeBerardinis RJ、Mancuso A、Sayed N、Zhang XY、Pfeiffer HK、Nissim I、Daikhin E、Yudkoff M、McMahon SB。Myc调节刺激线粒体谷氨酰胺分解并导致谷氨酰胺成瘾的转录程序。 美国国家科学院院刊2008; 105:18782–18787. doi:10.1073/pnas.0810199105。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Turowski GA、Rashid Z、Hong F、Madri JA、Basson MD。谷氨酰胺调节人类结肠癌细胞株的表型并刺激其增殖。 1994年癌症研究; 54:5974–5980. [ 公共医学 ] [ 谷歌学者 ]
Vander Heiden MG、Cantley LC、Thompson CB。 了解Warburg效应:细胞增殖的代谢需求。 科学。 2009; 324:1029–1033. doi:10.1126/science.1160809。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Wang JB、Erickson JW、Fuji R、Ramachandran S、Gao P、Dinavahi R、Wilson KF、Ambrosio AL、Dias SM、Dang CV、Cerione RA。 靶向线粒体谷氨酰胺酶活性抑制致癌转化。 癌细胞。 2010; 18:207–219. doi:10.1016/j.ccr.2010.08.009。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Yarden Y,Sliwkowski MX,《解开ErbB信号网络》,《Nat Rev Mol Cell Biol》。 2001; 2:127–137. doi:10.1038/35052073。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Yin C,Qie S,Sang N.癌细胞碳源代谢及其调控。 真核生物基因实验关键评论。 2012; 22:17–35. doi:10.1615/critreveukargeneexpr.v22.i1.20。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Yueva M、Zamboni N、Oefner P、Sachidanandam R、Lazebnik Y。谷氨酰胺而非葡萄糖缺乏会诱导人类细胞中MYC依赖性凋亡。 细胞生物学杂志。 2007; 178:93–105. doi:10.1083/jcb.200703099。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]