摘要 雷帕霉素(mTOR)的机制靶点在多种癌症中过度激活,使其成为引人注目的药物靶点; 然而,mTOR抑制对癌症代谢重编程的影响尚不完全清楚。 在这里,通过整合多形性胶质母细胞瘤(GBM)细胞系、临床前模型和临床样本的代谢和功能研究,我们证明谷氨酰胺代谢的代偿性上调促进了对mTOR激酶抑制剂的耐药性。 GBM细胞的代谢组学研究表明,mTOR激酶抑制剂治疗后谷氨酰胺酶(GLS)和谷氨酸水平升高。 此外,这些mTOR抑制剂依赖性代谢改变在GBM异种移植物模型中得到了证实。 mTOR抑制剂治疗后GLS的表达以α-酮戊二酸依赖(α-KG-依赖)的方式促进GBM存活。 mTOR激酶和GLS的基因和/或药理学联合抑制在荷瘤小鼠中导致大规模协同肿瘤细胞死亡和生长抑制。 这些结果强调了谷氨酰胺代偿代谢在促进mTOR抑制剂耐药性中的关键作用,并表明合理的联合治疗有可能抑制耐药性。
介绍 与正常细胞相比,大多数癌细胞消耗葡萄糖的速度惊人地高,并以乳酸的形式分泌出大部分葡萄糖衍生碳,而不是将其完全氧化,这种现象称为Warburg效应( 1 ). 除了葡萄糖,氨基酸还可以进入三羧酸(TCA)循环,因为它们的分解代谢导致TCA循环中间体的产生。 谷氨酰胺在细胞生长和能量代谢中具有重要作用,TCA循环和葡萄糖是碳源( 2 , 三 ). 谷氨酰胺分解代谢的前2个反应是由谷氨酰胺酶(GLS)调节的谷氨酰胺转化为谷氨酸,以及由谷氨酸脱氢酶(GDH)催化的谷氨酸转化为α-酮戊二酸(αKG)。 随后发生酶反应,生成天冬氨酸、苹果酸、丙酮酸、柠檬酸、丙氨酸和乳酸,以支持线粒体呼吸和三磷酸腺苷(ATP)的生成( 4 ). 谷氨酸还可以参与谷胱甘肽的合成,帮助调节细胞的抗氧化状态。 人们普遍认为,癌细胞倾向于将谷氨酰胺作为能量来源,这种现象在许多癌症中都已观察到。 许多研究表明,通过阻止这些关键酶的活性来抑制谷氨酰胺分解,可以显著抑制癌细胞的生长和增殖( 5 – 7 ). 因此,GLS已成为恶性胶质瘤治疗干预的一个有吸引力的靶点。
雷帕霉素(mTOR)的机制靶点是一种蛋白激酶,它通过磷脂酰肌醇3-激酶(PI3K)途径与细胞能量和营养状态整合生长因子受体的致癌信号,激活促进肿瘤生长和生存的下游信号通路( 8 ). 因此,mTOR已成为PI3K驱动癌症的重要分子靶点。 mTOR通过两种不同的复合物,mTOR复合物1(mTORC1)和mTOR复合物2(mTORC2),通过经典的PI3K途径介导细胞生长和增殖,并可能介导肿瘤细胞存活( 9 ). 特别是,mTORC1独特地通过PI3K整合生长因子和代谢信号,通过S6K1整合下游信号,突出了其作为癌症靶点的价值( 10 ). 我们之前已经证明,mTOR是EGFR突变、PTEN缺乏的多形性胶质母细胞瘤(GBM)下游信号传导的关键效应器,介导对EGFR酪氨酸激酶抑制剂的耐药性( 11 ). 然而,变构mTOR抑制剂雷帕霉素的临床失效是由AKT激活引起的,导致了负反馈的丢失,这与mTORC1作为PI3K/AKT信号负调节器的稳态调节作用是一致的( 12 ). 此外,我们证明mTORC2通过AKT和mTORC1诱导的信号通路介导雷帕霉素耐药( 13 ). 这些结果突出了阻断mTORC1和mTORC2的mTOR激酶抑制剂在GBM治疗中的作用( 14 ). 此外,揭示mTOR激酶抑制的分子和代谢反应为确定新的药物靶点和mTOR靶向治疗的耐药机制提供了宝贵的见解。
在此,我们对GBM细胞系、体内异种移植物模型和临床样本进行了综合分析,以检查谷氨酰胺代谢在mTOR靶向治疗反应中的重要性。 我们证明,与正常脑组织相比,GLS在大量临床GBM样本中高度表达,这表明GLS是治疗干预的一个有吸引力的靶点。 有趣的是,mTOR靶向治疗影响谷氨酰胺的利用,并导致谷氨酰胺碳向TCA循环输送的途径发生改变,GLS的表达增加。 用RNA干扰或化合物968抑制剂抑制GLS表达,该化合物已被证明可阻断癌细胞中的GLS活性( 7 , 15 – 17 ),使表达EGFRvIII的GBM细胞对mTOR靶向治疗敏感。 mTOR和GLS联合抑制显示出协同抑制体内肿瘤生长。 GBM细胞需要GLS以α-KG依赖的方式存活mTOR抑制。 这些结果表明,mTOR信号的抑制足以改变GBM细胞的代谢特征,并表明我们认为GLS在促进获得性抗mTOR靶向治疗方面的一种以前未被认识的功能, 表明需要结合mTOR靶向治疗来抑制谷氨酰胺分解。
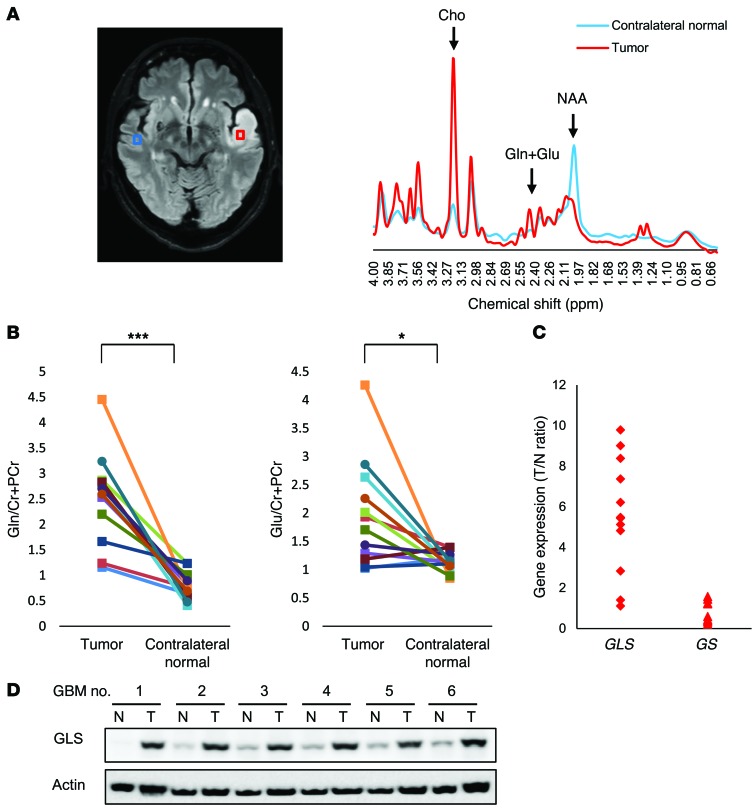
结果 GBM患者原位谷氨酰胺代谢和GLS表达。 在培养的大多数哺乳动物细胞中,葡萄糖和谷氨酰胺被大量分解代谢,提供碳、氮和自由能,并减少支持细胞生长和分裂所需的当量( 1 , 18 ). 有氧糖酵解(也称为Warburg效应)和谷氨酰胺分解是癌症的核心特征,是癌细胞所必需的。 为了探讨细胞内代谢的临床意义,我们检测了几个GBM患者肿瘤组织和邻近正常脑组织中的葡萄糖和谷氨酰胺代谢。 一名68岁男性左侧颞叶出现GBM,其磁共振波谱(MRS)显示胆碱显著升高,胆碱明显降低 N个 -乙酰基- 我 -与对侧正常大脑相比,肿瘤中的天冬氨酸(NAA)峰值( 图1A ). NAA/胆碱比值降低是预测胶质瘤恶性程度增加的常见标志( 19 ). 然而,在这项研究中最重要也是最本质的变化是,与MRS显示的对侧正常大脑相比,肿瘤中的谷氨酰胺和谷氨酸水平增加( 图1A ). 随后对12名GBM患者进行配对比较发现,肿瘤中谷氨酰胺和谷氨酸水平相对于对侧正常脑组织显著升高,这表明谷氨酰胺代谢强烈参与GBM细胞的代谢重编程( 图1B ). 在统计学上,肿瘤中的葡萄糖和乳酸水平也高于对侧正常脑组织,这表明GBM细胞中存在众所周知的有氧糖酵解现象( 补充图1、A和B ; 本文的在线补充材料; 数字对象标识: 10.1172/JCI78239DS1 ). 接下来,为了确定谷氨酰胺代谢在GBM细胞中是如何受到影响的,我们检测了12名GBM患者的肿瘤样本和正常脑组织中GLS(谷氨酰胺-谷氨酸转换酶)的表达以及谷氨酰胺合成酶(GS)的水平。 基因表达分析表明 GLS公司 与 GS公司 水平( 图1C )这表明谷氨酰胺分解代谢率较高,可能存在从谷氨酰胺到谷氨酸的代谢通量。 从6名GBM患者的手术样本中获得的裂解物的免疫印迹分析证实,相对于正常脑组织,肿瘤组织中GLS的表达增加( 图1D ). 总之,这些发现表明谷氨酰胺也是GBM细胞的主要营养素,GLS可能是GBM治疗的代谢基因的良好靶点。
图1。 GBM患者的肿瘤中谷氨酰胺和谷氨酸水平以及GLS表达升高。
( A类 )针对68岁GBM患者肿瘤(红色)和对侧正常脑(蓝色)区域的谷氨酰胺和谷氨酸的MRS研究。胆碱、谷氨酰胺和麸胺酸复合物以及NAA的峰值分别约为3.22、2.4和2.0 ppm的化学位移。 Cho,胆碱; Cr,肌酸; 谷氨酰胺; 谷氨酸、谷氨酸。 ( B类 )12例GBM患者肿瘤和对侧正常脑区MRS研究中的谷氨酰胺和谷氨酸水平。 根据肿瘤和对侧正常脑VOI的肌酸和磷酸肌酸计算谷氨酰胺和谷氨酸的相对水平* P(P) < 0.05; *** P(P) <0.001,根据双尾学生 t吨 测试。 ( C类 )关键酶的mRNA水平包括 GLS公司 和 GS公司 在12名GBM患者中,谷氨酰胺和谷氨酸之间存在差异。 相对水平 GLS公司 和GS表示为肿瘤/正常大脑(T/N)的表达比率。 ( D类 )6例GBM患者肿瘤切除后获得的肿瘤和正常脑组织中GLS染色的免疫印迹分析。另见 补充图1 .
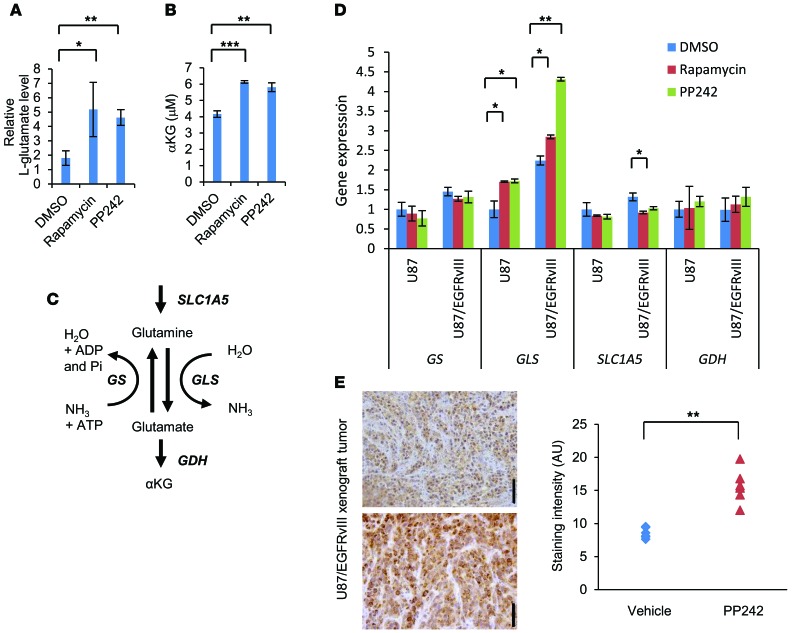
在体外和体内,由于mTOR抑制剂的作用,GBM中GLS和细胞内谷氨酸水平升高。 在刺激葡萄糖吸收和利用的EGFR/PI3K途径中,mTOR在引导可用氨基酸进入蛋白质合成中具有明确的作用。 谷氨酰胺摄取似乎对脂质合成和碳供应也至关重要,以运行TCA循环。 我们在U87胶质瘤细胞系中过度表达EGFR-激活突变(EGFRvIII),这已被证明可以增加mTORC1和mTORC2信号( 20 , 21 ). 通过对用mTOR抑制剂(雷帕霉素或PP242)处理48小时的U87和U87/EGFRvIII细胞进行气相色谱-质谱(GC/MS)分析,我们确定了91种代谢物,其水平随着变构mTOR抑制物雷帕霉素或者ATP-竞争性mTOR抑制物PP242的反应而显著变化( 图2 和 补充表1 ). 我们之前已经证明,雷帕霉素对体内模型和使用该药物治疗的患者的GBM细胞系中的mTORC2信号具有最小活性,而PP242同时阻断GBM细胞中的mTORC1和mTORC1信号( 12 , 13 , 22 ). 各治疗组代谢物变化的主成分分析(PCA)表明,这三个组有明显的聚类或明显的分离( 补充图2,A和B ). 关键的差异代谢物是谷氨酸(谷氨酸)、天冬氨酸、柠檬酸(或异柠檬酸)和琥珀酸( 补充图2B ). 特别是,一些谷氨酰胺水解和TCA循环的中间产物在mTOR抑制剂的治疗下表现出增加,增加了谷氨酰胺有效代谢的可能性( 补充图2C ). 事实上,在U87/EGFRvIII模型中,两种mTOR抑制剂均显著抑制葡萄糖消耗、乳酸生成和细胞增殖,但没有增加细胞死亡( 补充图3,A和B ). 与Csibi等人的研究结果一致( 23 ),细胞内 我 -U87和U87/EGFRvIII细胞中的谷氨酸升高,使其能够在mTOR靶向治疗中存活( 图3A ). 此外,我们发现mTOR抑制处理后,细胞内αKG、ATP和氨水平升高或至少保持不变,表明谷氨酰胺代谢的代偿性增加( 图3B 和 补充图4,A和B ). 这些结果表明GBM细胞可能对mTOR抑制剂产生耐药性。 接下来,为了确定mTOR信号的抑制如何影响代谢途径,我们用mTOR抑制剂处理U87和U87/EGFRvIII细胞,以测试糖酵解和谷氨酸解途径中关键酶的基因表达( 图3C ). 值得注意的是,mTOR抑制剂处理U87/EGFRvIII和较小程度的U87细胞导致 GLS公司 ( 图3D ). 特别是在2种GLS变体中( 7 , 15 ),较长肾脏型谷氨酰胺酶的表达( KGA公司 )mRNA显著增加,而短谷氨酰胺酶C的表达( 通用汽车公司 )mTOR抑制剂治疗后mRNA下降( 补充图4C ). 葡萄糖转运蛋白1( 葡萄糖转运蛋白1 ),丙酮酸脱氢酶激酶1( PDK1系列 )和乳酸脱氢酶A( LDHA公司 )雷帕霉素或PP242治疗后水平降低,与mTOR抑制糖酵解的作用一致( 补充图4D ). 最后,为了确定是否可以在体内检测到GLS表达,以应对mTOR靶向治疗,我们在治疗5天后分析了异种移植模型中表达EGFRvIII的肿瘤组织。 PP242处理后, GLS公司 与对照组相比,表达显著升高( 图3E ). 用另一种mTOR激酶抑制剂CC214治疗后也发现了类似的结果( 22 ) ( 补充图5 ).
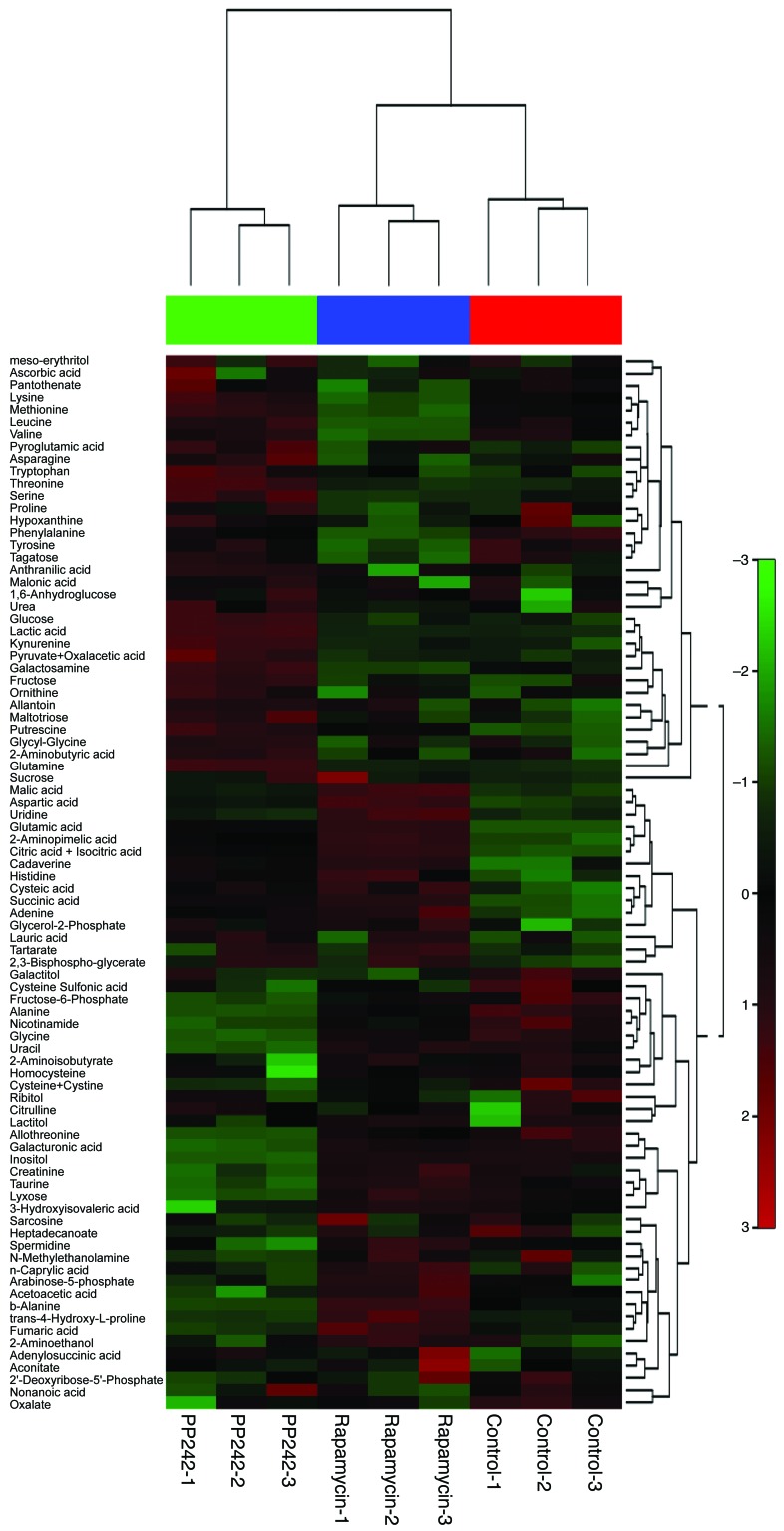
图2。 比较代谢组学确定谷氨酸是一种潜在的代谢物,可促进对mTOR抑制剂治疗的耐药性。
经1 nM雷帕霉素、1μM PP242和对照二甲基亚砜处理48小时的U87/EGFRvIII GBM细胞中差异表达的代谢物2D层次聚类的热图表示。 每列代表一个治疗组,每行代表一种代谢物。
图3。 GLS蛋白和谷氨酸水平的代偿性升高使GBM细胞能够存活于mTOR抑制剂治疗。
( A类 和 B类 )细胞内水平 我 -谷氨酸盐( A类 )和αKG( B类 )用1 nM雷帕霉素、1μM PP242或对照DMSO处理U87/EGFRvIII GBM细胞48小时。 数据表示3个独立实验的平均值±SEM* P(P) < 0.05; ** P(P) < 0.01; *** P(P) <0.001,根据双尾学生 t吨 测试。 ( C类 )示意图显示了本研究中针对的谷氨酰胺分解酶。 二磷酸腺苷; Pi,磷酸盐。 ( D类 )mRNA水平 GS公司 , GLS公司 ,溶质结合载体家族A1( SLC1A5型 )、和 GDH公司 在U87和87/EGFRvIII细胞中。 用1 nM雷帕霉素、1μM PP242或对照DMSO处理细胞48小时。 数据表示3个独立实验的平均值±SEM* P(P) < 0.05; ** P(P) <0.01,根据双尾学生 t吨 测试。 ( 电子 )用PP242治疗的EGFRvIII表达U87的异种移植物获得的GLS免疫组织化学图像( n个 =2)或控制DMSO( n个 =2)持续5天。 组织用苏木精复染。 比例尺:50μm。 从每组的6个独立图像中测量相对染色强度** P(P) <0.01,根据双尾学生 t吨 测试。 另请参见 补充图2-5 和 补充表1 .
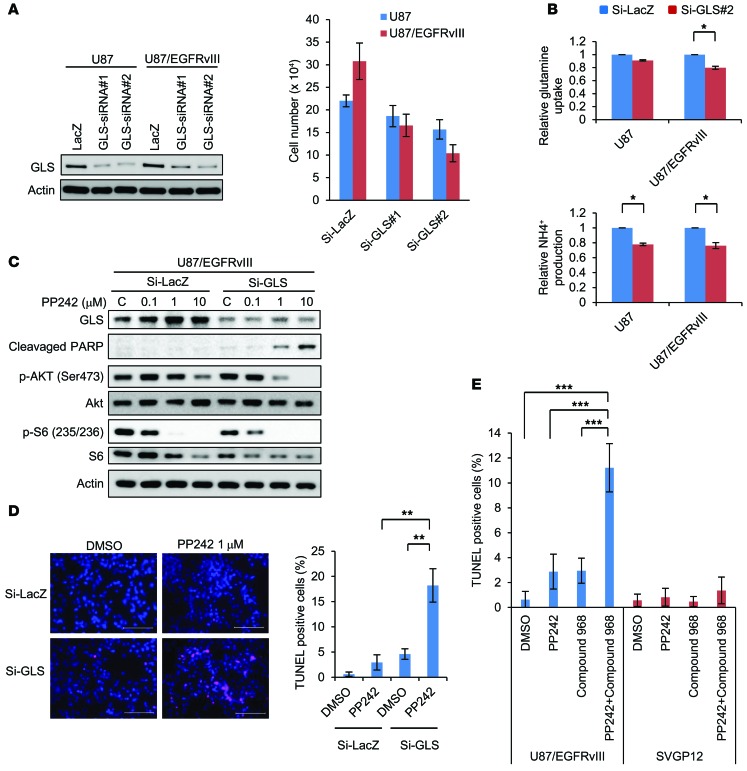
GLS抑制使GBM细胞对mTOR靶向治疗敏感。 由于PP242相对于雷帕霉素对GBM细胞中两种mTOR复合物的活性增强,我们主要使用PP242进行进一步的功能分析( 12 , 13 , 24 , 25 ). 在确认GLS在针对GBM的mTOR靶向治疗中的特定作用之前,我们测试了谷氨酰胺的可用性是否影响PP242介导的细胞死亡。 TUNEL分析表明,谷氨酰胺剥夺显著提高了U87/EGFRvIII GBM细胞对PP242介导的细胞死亡的敏感性,这一点已由多聚ADP核糖聚合酶(PARP)裂解分析和TUNEL染色证实( 补充图6,A和B ). 接下来,我们在U87/EGFRvIII GBM细胞中诱导siRNA-介导的GLS敲除,并评估其对PP242反应的影响。 siRNA转染导致GLS基因缺失,抑制了所有受试GBM细胞(U87MG和U87/EGFRvIII)的增殖,增强了EGFRvIII表达肿瘤细胞的抗增殖作用( 图4A ). GLS敲除被证实可抑制谷氨酰胺摄取和NH4 + 通过U87和U87/EGFRvIII GBM细胞中GLS的酶活性产生谷氨酰胺( 图3C 和 图4B ). 值得注意的是,GLS的敲除显著逆转了mTOR靶向治疗耐药性,有效地使U87-EGFRvIII细胞对PP242介导的细胞死亡敏感,如PARP阳性和TUNEL阳性细胞所示( 图4、C和D ). 接下来,为了评估GLS的药理抑制可用于使GBM对mTOR靶向治疗敏化的可能性,我们测试了GLS抑制剂化合物968对调节细胞对PP242的反应的作用。 化合物968以剂量依赖性的方式减少谷氨酰胺的摄取和谷氨酰胺分解代谢副产物(如氨)的分泌,抑制GLS活性( 补充图7A ). 在GLS活性受到抑制后,化合物968以剂量依赖的方式显著抑制GBM细胞增殖( 补充图7B ). 在TUNEL染色测定中,化合物968显著增强了PP242介导的表达EGFRvIII的GBM细胞的细胞死亡,尽管PP242和化合物968单独都不能促进广泛的肿瘤细胞死亡( 图4E 和 补充图8B ). 化合物968还增加了经PP242处理的EGFRvIII表达的GBM细胞的PARP裂解( 补充图8A ). 重要的是,化合物968和PP242的联合治疗并未导致正常人类星形胶质细胞(SVGP12)的显著细胞死亡( 图4E 和 补充图8C ),表明正常星形胶质细胞具有不同于GBM细胞的特征,并且GLS抑制在选择性地使GBM细胞对mTOR靶向疗法敏感方面具有潜在的临床用途。 为了测试化合物968和PP242对GBM患者衍生肿瘤细胞的作用,我们从GBM患者建立了原代培养细胞(KMG02),EGFR/PI3K轴(p-EGFR[Y1068]、p-AKT[S473]和p-S6[S235/236])以及GLS呈阳性染色( 补充图9A ). TUNEL分析显示化合物968显著增强PP242介导的KMG02细胞死亡( 补充图9B ). 化合物968还增加了PP242处理的KMG02细胞的PARP裂解( 补充图9C ). 综上所述,这些结果证明了GLS在通过GBM细胞中的谷氨酰胺代谢介导mTOR激酶抑制剂耐药性中以前未知的作用。
图4。 GLS抑制使GBM细胞对mTOR靶向治疗敏感。
( A类 )用2种GLS siRNA和干扰对照siRNA构建物转染U87和U87/EGFRvIII细胞24小时,并换成10%FBS培养基2天。 细胞数表示3个独立实验的平均值±SEM。 ( B类 )谷氨酰胺相对摄取量和NH4 + 对照GLS敲除U87和U87/EGFRvIII细胞的产量。 数据表示3个独立实验的平均值±SEM* P(P) <0.05,根据双尾学生 t吨 测试。 ( C类 )使用U87/EGFRvIII细胞的指示抗体进行免疫印迹分析,该抗体带有针对GLS的siRNA结构,或使用PP242或对照DMSO处理2天的对照LacZ。 GLS、p-AKT(Ser473)和AKT的图像是使用相同的细胞裂解液从另一个凝胶中获得的。 ( D类 )TUNEL染色的U87/EGFRvIII GBM细胞的代表性图像。 用抗GLS的siRNA转染细胞,并用1μM PP242或DMSO处理对照LacZ 2天。 用ImageJ软件对TUNEL阳性细胞进行定量。 数据表示每组3个独立图像的平均值±SEM** P(P) <0.01,根据双尾学生 t吨 测试。 比例尺:100μm。 ( 电子 )用1μM PP242和/或1μM化合物968处理2天的U87/EGFRvIII和SVGP12细胞的TUNEL染色。 用ImageJ软件对TUNEL阳性细胞进行定量。 数据表示每组3个独立图像的平均值±SEM。 Tukey-Kramer诚实显著性检验用于多重比较检验*** P(P) < 0.001. 另请参见 补充图6–9 .
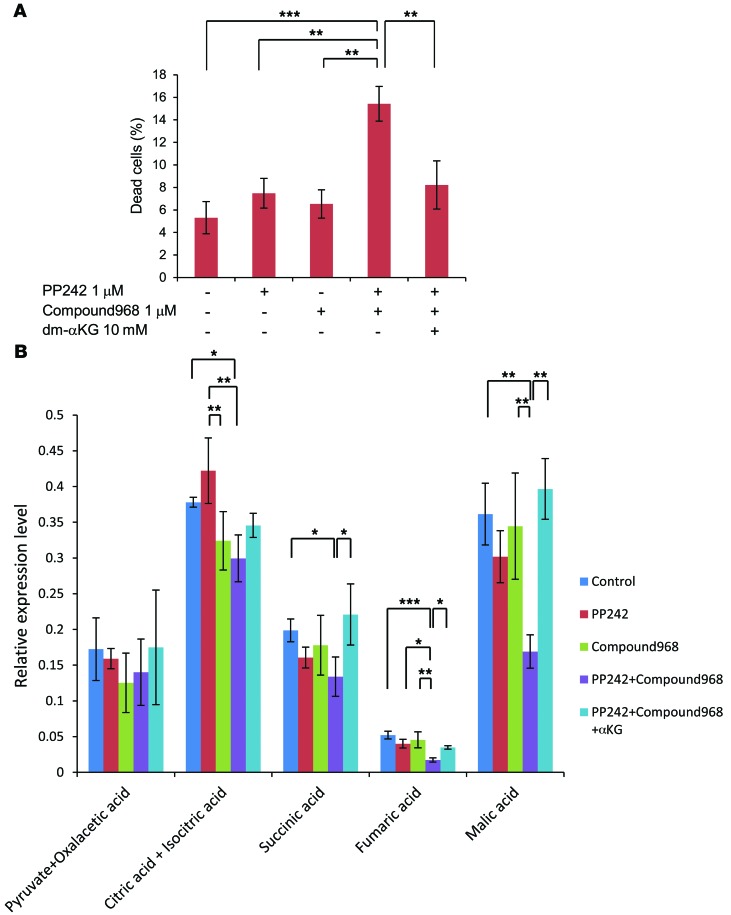
GBM细胞需要GLS以α-KG依赖的方式存活mTOR抑制。 为了确定GLS介导mTOR靶向治疗耐药的下游机制,我们检测了αKG作为下游代谢物的参与。 有趣的是,αKG的类似物二甲基αKG(dm-αKG)明显挽救了mTOR和GLS抑制处理的U87/EGFRvIII GBM细胞的活性( 图5A )表明凋亡抵抗是通过αKG介导的,而αKG是TCA循环所必需的。 为了确定TCA循环中的代谢变化,我们使用PP242和化合物968处理的U87/EGFRvIII GBM细胞,在含有dm-αKG的培养基中,通过GC/MS分析细胞内代谢产物。 综合代谢组分析表明,经PP242和化合物968联合处理的细胞中TCA循环代谢物显著减少,包括柠檬酸和异柠檬酸、琥珀酸、富马酸和苹果酸。 重要的是,dm-αKG挽救了TCA循环中αKG的直接下游代谢产物琥珀酸、富马酸和苹果酸水平的下降,这是对mTOR和GLS联合抑制的反应,但αKG上游代谢产物柠檬酸和异柠檬酸的水平没有显着挽救( 图5B ). 这些结果增加了葡萄糖和谷氨酰胺代谢协同调节癌症代谢重编程的可能性,并且GLS可能通过α-KG-依赖性补体驱动氧化TCA循环,使GBM细胞能够存活于mTOR抑制。
图5。 作为对mTOR抑制的反应,GLS以αKG依赖的方式促进GBM细胞存活。
( A类 )代谢物dm-αKG(10 mM)经1μM PP242和1μM化合物968处理3天后,对U87/EGFRvIII细胞的存活能力进行了测试。 通过台盼蓝排除法计算细胞死亡。 数据表示3个独立实验的平均值±SEM。 Tukey-Kramer诚实显著性检验用于多重比较检验** P(P) < 0.01; *** P(P) < 0.001. ( B类 )GC/MS分析针对用1μM PP242和/或1μM化合物968与正常DMEM或DMEM与dm-αKG(10 mM)处理24小时的U87/EGFRvIII细胞中TCA循环相关代谢物、丙酮酸和草酰乙酸、柠檬酸和异柠檬酸、琥珀酸、富马酸和苹果酸。 数据表示3个独立实验的平均值±SEM。 Tukey-Kramer诚实显著性检验用于多重比较检验* P(P) < 0.05; ** P(P) < 0.01; *** P(P) < 0.001.
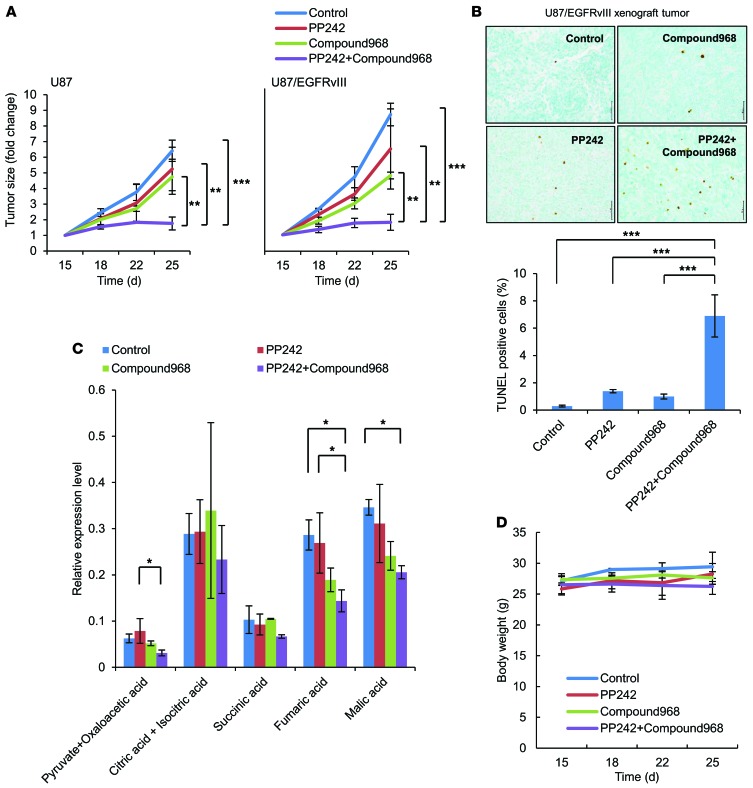
在异种移植模型中,GLS和mTOR联合抑制会导致GBM细胞死亡并阻止肿瘤生长。 为了确定体内GLS抑制是否使GBM细胞对mTOR激酶抑制剂敏感,我们分析了化合物968与PP242结合对U87和U87/EGFRvIII GBM异种移植物中肿瘤细胞代谢物、细胞死亡和肿瘤大小的影响。 将小鼠分为4个治疗组,通过腹腔注射PP242(5 mg/kg)、化合物968(5 mg/kg/kg)或PP242和化合物968的组合(5 mg/kg.)治疗15天。 仅化合物968或PP242可使肿瘤大小减小约20%-50%( 图6A )而没有显著的细胞凋亡诱导。 重要的是,化合物968和PP242的联合治疗使U87/EGFRvIII和U87异种移植模型的肿瘤缩小了约80%( 图6A ). 在U87/EGFRvIII异种移植模型的免疫组织化学分析中,化合物968在PP242治疗中导致凋亡细胞增加6倍( 图6B ). 重要的是,体内整体代谢分析表明,联合使用PP242和化合物968治疗的EGFRvIII表达的GBM肿瘤中的某些TCA循环代谢物显著减少( 图6C )表明mTOR信号和谷氨酰胺代谢在促进GBM细胞的TCA循环中起着重要作用。 最重要的是,在整个实验过程中,这种治疗对小鼠的体重没有明显影响( 图6D ). 最后,为了确定药物对正常器官和运动功能的不良影响,对非肿瘤小鼠进行15天的类似治疗,并在旋转棒装置上进行测试( 26 , 27 ). 整个治疗过程中未观察到对体重的明显影响,整个治疗后运动功能也未出现恶化( 补充图10A和B ). 在PP242、化合物968单独或联合用药的小鼠中,细胞形态没有显著差异,大脑(皮层和海马)、肝脏和肾脏中也没有诱导死亡细胞( 补充图11-13 ). 综上所述,这些结果表明,GLS抑制可以逆转体内mTOR靶向治疗耐药性,并通过调节肿瘤生物能量和分子合成与PP242协同作用,诱导肿瘤细胞死亡( 图7 ). 这些结果还表明,该药物组合的细胞毒性作用在肿瘤组织中增强,而不是在正常组织中。
图6。 在体内,mTOR和GLS抑制均显示协同抑制肿瘤生长。
( A类 )每只小鼠皮下注射1×10 6 U87(左侧)和U87/EGFRvIII(右侧)单元。 通过腹腔注射PP242(5 mg/kg)和/或化合物968(5 mg/kg.)治疗荷瘤小鼠。 对照组接受等量的二甲基亚砜。 植入15天后开始治疗。 在指定的时间点测量5只小鼠每个异种移植的肿瘤体积(折叠变化)。 数据表示3个独立实验的平均值±SEM** P(P) < 0.01; *** P(P) < 0.001. ( B类 )U87/EGFRvIII异种移植物样本的代表性图像,采用TUNEL染色(棕色细胞)评估凋亡细胞。 用ImageJ软件对TUNEL染色进行定量。 数据表示每组3个独立图像的平均值±SEM*** P(P) < 0.001. 比例尺:50μm。 ( C类 )针对U87/EGFRvIII异种移植物样品中TCA循环相关代谢物、丙酮酸和草酰乙酸、柠檬酸和异柠檬酸、琥珀酸、富马酸和苹果酸的GC/MS分析。 数据表示每组3个独立异种移植物的平均±SEM* P(P) < 0.05. ( D类 )每天腹腔注射PP242和/或化合物968对各组小鼠体重变化的影响。 Tukey-Kramer诚实显著性检验用于多重比较检验。 另请参见 补充图10–13 .
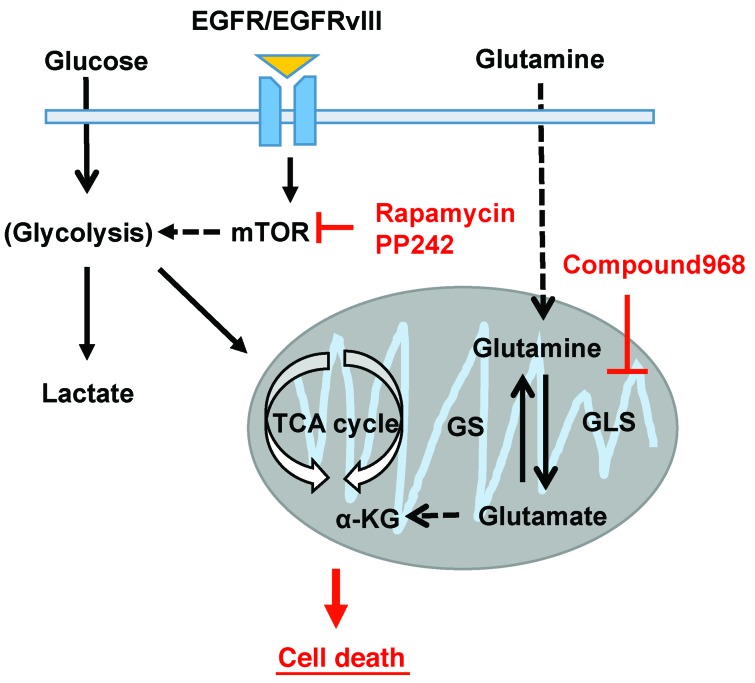
图7。 mTOR和GLS抑制都会减弱TCA循环的能量生成,导致GBM中的细胞死亡。
mTOR激酶抑制剂治疗GBM细胞后,GLS和谷氨酸水平升高。 结合mTOR激酶抑制剂和GLS抑制剂为GBM患者提供了合理的治疗策略。
讨论 癌细胞增殖和肿瘤发生与代谢重编程有关( 18 ). 由受体酪氨酸激酶或Ras启动的常见致癌信号转导途径参与PI3K/AKT信号传导,直接刺激糖酵解代谢( 28 ). 除了这种称为Warburg效应的有氧糖酵解外,谷氨酰胺代谢在癌症中的参与作为开发新的癌症治疗药物的潜在途径受到了越来越多的关注。 我们的研究表明,通过mTOR靶向治疗对PI3K信号的药理学损伤可以通过增加GLS活性增强谷氨酰胺代谢,从而导致谷氨酰胺依赖性GBM细胞。 代谢改变被认为是大多数癌症进展、生存和耐药性的关键因素,有助于设计有效的分子抑制剂和治疗GBM患者的策略。
癌细胞吸收和代谢葡萄糖和谷氨酰胺的程度远远超过了合成代谢大分子合成中对这些分子的需求( 4 , 29 ). 我们已经证明,谷氨酰胺、谷氨酸和GLS水平在GBM样本中经常升高,包括在体内成像的患者中。 由于PI3K信号通路与生长控制和代谢重编程密切相关,mTOR信号通路刺激特定的代谢途径,包括糖酵解、磷酸戊糖途径的氧化臂和从头合成脂质( 10 )mTOR信号可能在调节谷氨酰胺代谢中发挥重要作用。 谷氨酰胺可以通过促进亮氨酸的摄取来调节mTORC1途径( 30 )通过促进mTORC1组装和溶酶体定位( 31 , 32 )这表明谷氨酰胺既是mTORC1的信号,又是促进蛋白质翻译的来源。 最近的一项研究进一步强调了mTORC1和谷氨酰胺代谢之间的功能联系,表明mTORC2的抑制通过上调SIRT4表达来抑制GDH活性,从而降低谷氨酰胺代谢( 23 ). 我们发现GBM细胞通过提高GLS表达来增加谷氨酰胺代谢,以响应mTOR靶向治疗,我们的数据可能表明了不同的途径,因为本研究中使用的GBM细胞能够抵抗mTOR抑制,而之前的论文中使用的细胞则不能( 23 ). 尽管在我们的研究中,mTOR抑制治疗后GDH水平没有改变,但我们发现氨、细胞内谷氨酸、αKG和ATP水平升高或至少保持不变,这与谷氨酰胺代谢增加一致。 这些结果还表明,至少在一些GBM细胞中,mTOR激酶抑制的抵抗可能是一种潜在机制。
我们之前已经表明,EGFRvIII,GBM中最常见的EGFR突变,通过上调c-MYC激活Warburg效应,重新编程细胞代谢以驱动肿瘤生长,并且我们已经确定了互补的mTORC1和mTORC2依赖性途径。 mTORC1通过MYC相互作用蛋白MAX的剪接调节c-MYC活性,mTORC2通过FOXO-乙酰化依赖机制控制其水平来调节MYC活动( 20 , 21 ). 这里的结果强调了mTOR介导的谷氨酰胺代谢调控的重要性,表明GBM细胞通过增加GLS表达来提高谷氨酸水平,从而适应mTOR抑制剂。 当mTOR抑制导致糖酵解缺陷时,这可能是TCA中间体损失的必要补偿。 然而,还需要进一步的研究来测试该模型,并探索其他途径作为GLS表达和活性介质的潜在作用。
这些结果还揭示了针对分子靶向治疗和/或某些代谢应激的代谢重编程。 在葡萄糖限制下,人类癌症中高表达的GLUT1水平驱动了KRAS途径突变的获得( 33 )TCA循环也可以重新编程并完全由谷氨酰胺驱动,生成柠檬酸盐,这种柠檬酸盐仅由特定类型的癌细胞中的谷氨酰胺碳组成( 34 ). AKT抑制通过增加GDH活性刺激谷氨酰胺代谢( 6 ). 抑制线粒体丙酮酸代谢可增加谷氨酸依赖性缺乏,促进αKG的还原代谢,为脂质合成提供柠檬酸( 35 ). 癌细胞依赖谷氨酰胺代谢并不奇怪( 4 ). 重要的是,我们的数据表明,通过α-KG-依赖性恢复维持TCA循环可能与促进GBM存活和对mTOR靶向治疗的耐药性有关。 这些发现可能对将mTOR激酶抑制剂与GLS抑制剂结合应用于GBM患者和其他可能的mTOR活化癌症患者具有重要意义。
方法 详细方案见补充实验程序。
细胞系。 如前所述获得U87、U87-EGFRvIII和U87-EGFR等基因GBM细胞系( 36 ). U251、LN229、T98和A172人GBM细胞系和SVGP12人星形胶质细胞(ATCC)在补充有10%FBS(生物工业)和100U/ml青霉素和链霉素(Nacalai Tesque)的DMEM(Nacalai Tesque)中在湿润的5%CO中培养 2 37°C培养箱。
抗体和试剂。 获得的抗体针对以下抗体:EGFR(细胞信号,目录2232)、p-EGFR Tyr1068(细胞信号学,目录2236)、p-AKT Ser473(细胞信号化,目录4060)、AKT(细胞信号传导,目录9272)、p-S6 Ser235/236(细胞信号传递,目录4858)、S6(细胞信号传播,目录2217)、PARP(细胞信号转导,目录9542)、, 裂解PARP(Cell Signaling,目录5625)、GLS(Abcam,目录ab60709)、GLS1(Sigma-Aldrich,目录HPA036223)、GLS2(Simma-Aldrich,目录HPA38608)、β-actin(Ambion)和EGFR/EGFRvIII混合抗体(Novocastra)。 所用试剂为雷帕霉素(LC Laboratories)、PP242(Chemdea)、GLS抑制剂(化合物968,Calbiochem)和dm-αKG(Sigma-Aldrich)。
RNA提取和实时PCR。 使用mirVana miRNA分离试剂盒(Applied Biosystems)提取细胞系、肿瘤样本和正常脑组织的总RNA。 使用高容量cDNA逆转录试剂盒(Applied Biosystems)从20 ng总RNA合成第一链cDNA。 按照制造商的说明,使用TaqMan基因表达分析(Applied Biosystems)对3μl稀释cDNA进行实时PCR。 所有反应均一式三份。 18S核糖体RNA作为内源性对照。 采用应用生物系统7500实时PCR系统(Applied Biosystems)通过ΔΔCt法获取并分析定量mRNA表达数据。 本研究使用了以下使用FAM-MGB染料进行的TaqMan基因表达分析:SLC2A1(SMID:Hs00892681_m1)、LDHA(SMID:Hs00855332_g1)、PDK1(SMID:Hs01561850_m1)、SLC1A5(SMID:Hs01056542_m1),GLS(SMID:%s00248163_m1 SMID:Hs03989560_s1), 18S(SMID:Hs99999901_s1)。
质粒和siRNA转染。 使用全血清中的Lipofectamine RNAiMAX(Invitrogen)将siRNA转染到GBM细胞系中,24小时后改变培养基。 专门针对GLS(目录L-004548-01-0005)的On-TARGETplus SMARTpool siRNAs(Thermo Scientific,Dharmacon Division)和非靶向siRNA对照池在10 nM下使用。
基于免疫组织化学染色和图像分析的评分。 石蜡包埋组织切片取自神户大学医院的病理组织学和组织核心设施。 玻片用苏木精复染以显示细胞核。 染色强度由2名病理学家和/或2名不知道分子分析结果的神经肿瘤学家独立评分。 定量图像分析是用软成像系统软件进行的,该软件在靶向药物的临床试验中已被证明可用于测量GBM样本中的药物特异性作用( 11 , 12 ).
代谢物测量。 使用BioProfile 400分析仪(Nova Biomedical)测量培养细胞培养基中的葡萄糖、乳酸、谷氨酰胺、谷氨酸和铵。 细胞在各种条件下的新鲜培养基中培养,48小时后测量培养基中的代谢物浓度,并将其归一化为每个样本中的细胞数。
我 -谷氨酸水平。
将培养细胞或snap冷冻组织样品溶解并用磷酸盐缓冲液均质。 细胞内 我 -按照制造商的说明测量谷氨酸水平(Yamasa 我 -谷氨酸检测试剂盒)。
GC/MS分析。 如前所述,提取并衍生生物样品中的代谢物,并进行了一些修改( 37 , 38 ). 根据之前报告中描述的方法,使用GC/MSQP2010 Ultra(岛津公司)和熔融石英毛细管柱(CP-SIL 8 CB低渗/MS;30 m×0.25 mm内径,0.25μm膜厚;安捷伦公司)进行GC/MS分析( 39 , 40 ). 结果数据以CSV格式文件导出,并使用内部分析软件进行分析(AI输出)。 该软件使用内部代谢物库进行峰值识别和量化。 将所有数据归一化为内标物2-异丙基苹果酸的峰高。 为了评估代谢组学实验中的技术差异,每个样品都被提取、衍生化并在3个重复中进行测量。
MRS研究。 对新诊断或复发的GBM患者进行术前MRI和MRS检查。使用3T MRI/MRS扫描仪(飞利浦医疗系统公司阿奇耶娃)获取MR波谱数据。 使用8通道头部MRI线圈接收信号,使用正交体MRI线圈传输射频(RF)脉冲。 使用双回波PRESS序列获得了单轴定位MR谱。 MRS采集参数如下:1.5×1.5×1.5 cm 三 ,TR/TE=2000/35 ms,128个平均值,1024个复点用于光谱数据。 感兴趣的体积(VOI)定位于实体肿瘤的代表性区域,由董事会认证的神经放射学家或技术人员确定。 作为对照,还将体素放置在大脑对侧(非肿瘤侧)的同一解剖位置,以获得控制光谱。 使用用户依赖的拟合程序(由Steven Provencher开发的LCModel)获得以mM/l VOI绝对单位表示的浓度估计值[ http://s-provencher.com/pages/lcmodel.shtml ]),它基于单个代谢物的模型光谱库( 41 , 42 ). 对胆碱(3.22 ppm)、NAA(2.0 ppm)、葡萄糖(3.44 ppm)、乳酸(1.33 ppm)、谷氨酰胺(2.45 ppm)和谷氨酸(2.35 ppm)水平进行定量。 还计算了总肌酸(肌酸加磷酸肌酸,3.0 ppm)的代谢物比率,明确假设该水平在正常和许多病理状态下是稳定的( 43 ).
Xenograft模型。 将U87和U87-EGFRvIII细胞植入免疫缺陷BALB/cAJcl-nu/nu小鼠(Clea Japan)进行皮下异种移植研究。 对于皮下植入,将培养的指数生长的肿瘤细胞进行胰蛋白酶化,通过台盼蓝排除计数,并在1×10的条件下重新悬浮 6 细胞/100μl,置于Dulbecco的PBS和Matrigel(BD Biosciences)溶液中。 通过测量每个皮下肿瘤的垂直直径,用卡尺监测肿瘤生长。 每天腹腔注射PP242(5 mg/kg)和/或GLS抑制剂(5 mg/kg/kg)和生理盐水治疗肿瘤。 采取适当措施将动物的不适感降至最低,并在肿瘤植入和给药过程中使用适当的无菌手术技术。 对濒死或有坏死肿瘤的动物实施安乐死。
统计学。 结果显示为平均值±SEM。PCA使用商用SIMCA-P Plus软件12.0.1版(Umetrics)进行。 Tukey Kramer诚实显著性检验用于多重比较检验。 与双尾学生进行了其他比较 t吨 测试,除非另有说明。 统计显著性定义为 P(P) < 0.05.
研究批准。 胶质瘤组织取自神户大学神经外科的常规临床治疗程序。 在手术过程中切除组织样本和外周脑组织,并立即在液氮中冷冻以进行后续研究。 每位患者或其法定监护人提供书面知情同意书,同意将所有临床数据和切除的组织标本用于研究目的。 本研究得到神户大学伦理委员会的批准(批准号:1497,用于胶质瘤患者的GC/MS和MRS研究;1579,用于胶质细胞瘤样本的使用)。 根据实验动物资源委员会的标准,所有小鼠均在神户大学规定的无病原体条件下繁殖和饲养。 所有实验均获得神户大学动物保护和使用委员会的批准。
致谢 我们要感谢神户大学脑瘤转化资源部的所有成员,感谢他们对生物标本和生物储存的支持。 我们还要感谢Izumi Takayama(神户大学医学研究生院放射肿瘤学系)帮助进行TUNEL分析,Yukiko Takeuchi(神户学院医学研究生学院循证实验医学部)帮助进行GC/MS分析, 以及Ryosuke Doi和Mitsuharu Endo(神户大学医学研究生院生理与细胞生物学系)帮助进行ATP检测。 K.Tanaka得到了科学研究援助基金(KAKENHI)(24791501)和武田科学基金会的部分支持。 T.Sasayama、K.Hosoda和E.Kohmura也得到了科学研究补助金(KAKENHI)的部分支持(分别为25462258、24592126和25293309)。 P.S.Mischel得到了路德维希癌症研究所(Ludwig Institute for Cancer Research)的支持,并获得了国家神经疾病和中风研究所(NS73831)、国家癌症研究所、Ben and Catherine Ivy基金会和Defeat GBM Research Collaborative(国家脑瘤学会的子公司)的资助。
脚注
参考信息: 临床研究杂志 . 2015; 125(4):1591–1602. doi:10.1172/JCI78239。
工具书类
1 Vander Heiden MG、Cantley LC、Thompson CB。 了解Warburg效应:细胞增殖的代谢需求。 科学。 2009; 324(5930):1029–1033. doi:10.1126/science.1160809。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
2 Buchakjian MR、Kornbluth S.《驱动船舶的引擎:细胞增殖和死亡的代谢导向》。 Nat Rev Mol细胞生物学。 2010; 11(10):715–727. doi:10.1038/nrm2972。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
三。 Lunt SY,Vander Heiden MG.有氧糖酵解:满足细胞增殖的代谢要求。 Ann Rev细胞开发生物学。 2011; 27:441–464. doi:10.1146/annurev-cellbio-092910-154237。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
4 Wise DR,Thompson CB。 谷氨酰胺成瘾:癌症的新治疗靶点。 生物化学科学趋势。 2010; 35(8):427–433. doi:10.1016/j.tibs.2010.05.003。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
5 Seltzer MJ等。谷氨酰胺酶的抑制优先减缓IDH1突变的胶质瘤细胞的生长。 2010年癌症研究; 70(22):8981–8987. doi:10.1158/008-5472.CAN-10-1666。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
6 Yang C、Sudderth J、Dang T、Bachoo RM、McDonald JG、DeBerardinis RJ。胶质母细胞瘤细胞需要谷氨酸脱氢酶才能在葡萄糖代谢或Akt信号受损时存活。 2009年癌症研究; 69(20):7986–7993. doi:10.1158/0008-5472.CAN-09-2266。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
7 王建军,等。靶向线粒体谷氨酰胺酶活性抑制致癌转化。 癌细胞。 2010; 18(3):207–219. doi:10.1016/j.cr.2010.08.009。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
8 癌症基因组图谱研究N.综合基因组特征定义了人类胶质母细胞瘤基因和核心途径。 自然。 2008; 455(7216):1061–1068. doi:10.1038/nature07385。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
9. Guertin DA,Sabatini DM。确定mTOR在癌症中的作用。 癌细胞。 2007; 12(1):9–22. doi:10.1016/j.ccr.2007.05.008。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
10 Duvel K等,mTOR复合物下游代谢基因调控网络的激活1。 分子细胞。 2010; 39(2):171–183. doi:10.1016/j.molcel.2010.06.022。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
11 Mellinghoff IK等。胶质母细胞瘤对EGFR激酶抑制剂反应的分子决定因素。 《新英格兰医学杂志》,2005年; 353(19):2012–2024. doi:10.1056/NEJMoa051918。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
12 Cloughesy TF等。雷帕霉素对复发性PTEN缺乏性胶质母细胞瘤患者的一期试验抗肿瘤活性。 《公共科学图书馆·医学》2008; 5(1):e8。 doi:10.1371/journal.pmed.0050008。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
13 Tanaka K等。癌基因EGFR信号激活mTORC2-NF-κB通路,促进化疗耐药。 癌症发现。 2011; 1(6):524–538. doi:10.1158/2159-8290.CD-11-0124。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
14 Yang H,Rudge DG,Koos JD,Vaidialingam B,Yang HJ,Paveletich NP.mTOR激酶结构、机制和调节。 自然。 2013; 497(7448):217–223. doi:10.1038/nature12122。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
15 Katt WP、Ramachandran S、Erickson JW、Cerione RA。 二苯并菲类药物作为谷氨酰胺酶C和癌细胞增殖的抑制剂。 摩尔癌症治疗。 2012; 11(6):1269–1278. doi:10.1158/1535-7163.MCT-11-0942。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
16 Huang W等。谷氨酰胺通过抗酸性在癌细胞生长中的作用。 2013年细胞研究; 23(5):724–727. doi:10.1038/cr.2013.15。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
17 Simpson NE,Tryndyak副总裁,Pogribna M,Beland FA,Pogripny IP。 通过抑制谷氨酰胺代谢来修改代谢敏感的组蛋白标记会影响基因表达并改变癌细胞表型。 表观遗传学。 2012; 7(12):1413–1420. doi:10.4161电子邮箱22713。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
18 Ward PS,Thompson CB公司。 新陈代谢重编程:即使是沃伯格也没有预料到的癌症标志。 癌细胞。 2012; 21(3):297–308. doi:10.1016/j.ccr.2012.02.014。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
19 Poptani H,Gupta RK,Roy R,Pandey R,Jain VK,Chhabra DK.用体内质子磁共振波谱表征颅内肿块病变。 AJNR美国神经放射杂志。 1995; 16(8):1593–1603. [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
20 Babic I等人。EGFR突变诱导的Max选择性剪接有助于脑癌糖酵解肿瘤的生长。 单元格元数据。 2013; 17(6):1000–1008. doi:10.1016/j.cmet.2013.04.013。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
21 Masui K等。mTOR复合物2通过FoxO乙酰化和c-Myc上调控制胶质母细胞瘤中的糖酵解代谢。 单元格元数据。 2013; 18(5):726–739. doi:10.1016/j.cmet.2013.09.013。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
22 Gini B等人mTOR激酶抑制剂CC214-1和CC214-2优先阻断EGFRvIII激活的胶质母细胞瘤的生长。 2013年临床癌症研究; 19(20):5722–5732. doi:10.1158/1078-0432.CCR-13-0527。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
23. Csibi A等。mTORC1途径通过抑制SIRT4刺激谷氨酰胺代谢和细胞增殖。 单元格。 2013; 153(4):840–854. doi:10.1016/j.cell.2013.04.023。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
24 Sarbassov DD等。长期雷帕霉素治疗抑制mTORC2组装和Akt/PKB。 分子细胞。 2006; 22(2):159–168. doi:10.1016/j.molcel.2006.03.029。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
25. Efeyan A,Sabatini DM。mTOR与癌症:一条通路中的多个环路。 当前操作细胞生物学。 2010; 22(2):169–176. doi:10.1016/j.ceb.2009.10.007。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
26 罗德里格斯TB、Granado N、Ortiz O、Cerdan S、Moratalla R。谷氨酸能和多巴胺能神经递质系统之间的代谢相互作用通过D(1)多巴胺受体介导。 神经科学研究杂志2007; 85(15):3284–3293. doi:10.1002/jnr.21302。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
27 Hamm RJ、Pike BR、O'Dell DM、Lyeth BG、Jenkins LW。 旋转试验:评估其在评估创伤性脑损伤后运动障碍方面的有效性。 神经创伤杂志。 1994; 11(2):187–196. doi:10.1089/neu.1994.11.187。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
28 Kroemer G,Pouyssegur J.肿瘤细胞代谢:癌症的致命弱点。 癌细胞。 2008; 13(6):472–482. doi:10.1016/j.cr.2008.05.005。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
29 DeBerardinis RJ、Lum JJ、Hatzivassiliou G、Thompson CB。 癌症生物学:代谢重组刺激细胞生长和增殖。 单元格元数据。 2008; 7(1):11–20. doi:10.1016/j.cmet.2007.10.002。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
30. Nicklin P等。氨基酸的双向运输调节mTOR和自噬。 单元格。 2009; 136(3):521–534. doi:10.1016/j.cell.2008.11.044。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
31 Duran RV等。谷氨酰胺水解激活Rag-mTORC1信号。 分子细胞。 2012; 47(3):349–358. doi:10.1016/j.molcel.2012.05.043。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
32 Kim SG等。代谢应激通过调节TTT-RUVBL1/2复合物控制mTORC1溶酶体定位和二聚化。 分子细胞。 2013; 49(1):172–185. doi:10.1016/j.molcel.2012.10.003。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
33 Yun J等。葡萄糖缺乏有助于肿瘤细胞中KRAS途径突变的发展。 科学。 2009; 325(5947):1555–1559. doi:10.1126/science.1174229。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
34 Le A等。通过TCA循环促进B细胞增殖和存活的葡萄糖非依赖性谷氨酰胺代谢。 单元格元数据。 2012; 15(1):110–121. doi:10.1016/j.cmet.2011.12.009。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
35. Hitosugi T等。线粒体丙酮酸脱氢酶激酶1的酪氨酸磷酸化对癌症代谢很重要。 分子细胞。 2011; 44(6):864–877. doi:10.1016/j.molcel.2011.10.015。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
36 Wang MY,等。雷帕霉素抑制的哺乳动物靶点促进PTEN缺乏和PTEN完整的胶质母细胞瘤细胞对表皮生长因子受体激酶抑制剂的反应。 2006年癌症研究; 66(16):7864–7869. doi:10.1158/008-5472.CAN-04-4392。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
37 Yoshie T等。大肠癌中APC基因突变对代谢产物的调节。 癌症科学。 2012; 103(6):1010–1021. doi:10.1111/j.1349-7006.2012.02262.x。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
38 Wise DR等。低氧促进α-酮戊二酸盐的异柠檬酸脱氢酶依赖性羧化为柠檬酸盐,以支持细胞生长和存活。 美国国家科学院院刊2011; 108(49):19611–19616. doi:10.1073/pnas.111773108。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
39 Yoshida M等人。使用气相色谱-质谱法通过代谢组分析诊断胃肠疾病。 胃肠病学杂志。 2012; 47(1):9–20. doi:10.1007/s00535-011-0493-8。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
40 Nakamizo S等人,基于GC/MS的神经胶质瘤患者脑脊液(CSF)代谢组学分析。 神经瘤杂志。 2013; 113(1):65–74. doi:10.1007/s11060-013-1090-x。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
41 校准器SW。 使用LCModel对体内局部1H光谱进行自动定量。 核磁共振生物识别。 2001; 14(4):260–264. doi:10.1002/nbm.698。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
42. Andronesi OC等。通过体内光谱编辑和2D相关磁共振波谱检测IDH突变胶质瘤患者中的2-羟基戊二酸。 《科学与运输医学》,2012年; 4(116):116ra4。 doi:10.1126/scitranslmed.3002693。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
43 Tartaglia MC等。多发性硬化症病变前正常白质中胆碱增加。 神经学杂志。 2002; 249(10):1382–1390. doi:10.1007/s00415-002-0846-6。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
关联数据 本节收集本文中包含的任何数据引用、数据可用性声明或补充材料。