摘要
为了刺激不受调控的增殖,癌细胞改变代谢以支持大分子生物合成。细胞培养研究揭示了不同的致癌突变和营养物质如何影响代谢。葡萄糖和谷氨酰胺是使用的主要燃料在体外; 然而,最近的研究表明,利用其他氨基酸以及脂类和蛋白质对癌细胞也很重要。肿瘤代谢的早期研究正在将这些发现转化为整个肿瘤的生物学,并表明除了营养物质的可用性之外,还存在额外的复杂性体内全身代谢和肿瘤异质性也会影响肿瘤细胞的代谢,而成功地靶向肿瘤治疗需要了解体内肿瘤代谢。
关键词:癌症代谢、肿瘤代谢、细胞增殖、营养物质可用性
了解癌症代谢的研究
近年来,对癌细胞代谢适应机制的研究取得了巨大进展。研究使用在体外培养系统通过描述癌细胞如何利用现有的代谢程序来促进增殖和存活,从而对营养利用和代谢途径的调控产生了重要的见解。检查肿瘤代谢体内引入了新的复杂性,但采取这一步骤对于深入了解整个动物生理学如何影响营养物质的可用性以及理解肿瘤异质性的作用以及组织中不同细胞类型之间的相互作用至关重要。获得这一认识对于开发利用代谢途径和改进患者治疗的新疗法至关重要。在这篇综述中,我们首先讨论了主要从细胞培养研究中获得的对癌细胞代谢的当前认识,然后重点关注使用患者和小鼠模型进行实验时产生的新见解,目的是强调每种实验环境的优势和局限性,并提请注意关键的未回答问题。
使用细胞培养定义增殖代谢
癌症的定义是转化细胞的无限制增殖。在培养物中建立细胞系从肿瘤中选择生长最快的恶性克隆,同时失去不分裂和缓慢增殖的癌细胞以及作为原始肿瘤组织一部分的任何其他细胞类型(图1A). 举例来说,一个克隆具有5%的增殖优势,几乎可以在不到65代的时间内完全消除第二个克隆(图1B). 因此,从本质上讲,细胞培养选择相对均匀的癌细胞群体,生成清洁的系统,用以研究特定致癌突变对代谢程序的贡献以及细胞增殖的潜在代谢需求。常见致癌因素Ras公司和Myc公司两者都促进与恶性转化相关的细胞自主代谢变化,即代谢底物转向合成代谢途径(见词汇表)。致癌Ras增加葡萄糖和谷氨酰胺的消耗[1,2]而Myc通过转录程序增强谷氨酰胺吸收和分解代谢相关基因的表达,从而增强谷氨酰胺代谢(见词汇表)[三,4]. Myc还将谷氨酰胺分解增加与葡萄糖代谢变化联系起来[5],可以直接控制参与有氧糖酵解的基因的表达[6]. 其他关键癌症基因的突变也会影响新陈代谢。p53缺失促进葡萄糖摄取和代谢[7,8],可以影响细胞对葡萄糖的利用[9]. 在所有情况下,与癌症相关的基因改变都伴随着有利于合成代谢的代谢改变,使营养物质的获取和利用能够满足增加的ATP(见词汇表)需求,并产生快速细胞分裂所需的核苷酸、脂质和蛋白质[10].
图1。
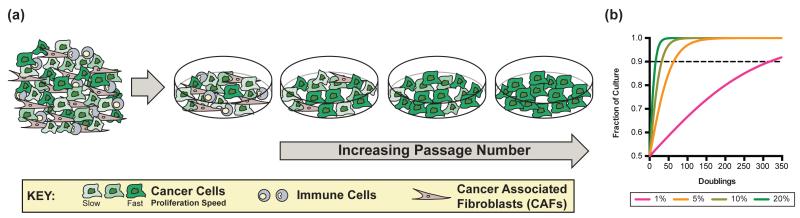
在培养基中建立肿瘤衍生细胞系会选择人群中增殖最快的克隆,而不分裂和增殖较少的细胞在连续传代时会丢失。细胞培养的这一不可避免的结果如图所示(A类)以肿瘤细胞系生成为例。面板(B类)显示了一个模型,该模型演示了如果克隆具有所示的增殖优势,克隆需要多少倍细胞才能接管培养群体(关键;增殖优势表示为比控制倍增时间快%)。该模型假设两个不同的克隆在相同密度下进行竞争,其中一个克隆具有固定的优势,随着时间的推移而保持不变。我们进一步定义了一个克隆,其代表了超过90%的培养群体,即已经接管了培养物。这一阈值是在317次倍增后达到的,其中增殖优势为1%,64次倍增为5%,32次倍增10%,只有16次倍增20%。模型的其他详细信息包含在补充材料中。
增殖细胞和非增殖细胞之间的代谢差异受到的审查较少。利用哺乳动物原代成纤维细胞和淋巴细胞进行的研究表明,与增殖细胞相比,静止细胞有利于分解代谢[5,11] (图2). 维持体内平衡需要营养物质分解以生成ATP,以及NADPH生成以应对氧化还原应激[11,12]. 静止细胞也努力平衡脂肪酸和蛋白质降解与合成[11]这一发现与这些非增殖细胞的细胞质量没有增加相一致。然而,这些培养的细胞仍然依赖葡萄糖和谷氨酰胺,而许多分化的哺乳动物组织使用其他营养物质[13]. 例如,心脏可以消耗脂肪酸、葡萄糖、酮或氨基酸来支持电活动和持续机械收缩所需的大量ATP[14]虽然大脑几乎完全依赖于葡萄糖代谢,但只有在葡萄糖不可用时才转换为酮类[15]. 因此,将培养中的专门静止细胞系统的研究推广到生物体完整组织中的不同细胞类型时需要谨慎。
图2。
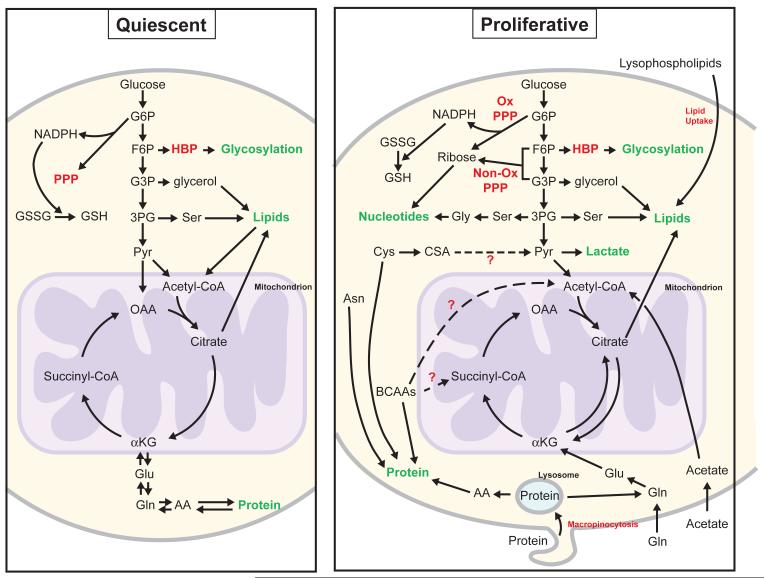
/B> 静止代谢和增殖代谢之间的差异。在静态代谢(左)中,细胞平衡分解代谢和合成代谢过程,如脂肪生成和β-氧化,或蛋白质合成和降解。在增殖代谢(右)中,合成代谢过程有利于生物量的净生产。红色标签表示代谢途径未详细显示。绿色标签表示代表分解代谢途径起点和/或合成代谢途径终点的大分子(或蛋白质修饰,如糖基化)。折断的箭头表示尚未进行广泛调查的已确定营养素的潜在命运。线粒体以紫色表示,以说明区室化反应。缩写:AA=氨基酸,Asn=天门冬氨酸,αKG=α-酮戊二酸,BCAAs=支链氨基酸,CSA=半胱氨酸亚磺酸,Cys=半胱胱氨酸,F6P=果糖-6-磷酸,Gln=谷氨酰胺,Glu=谷氨酸,Gly=甘氨酸,GSH=还原谷胱甘肽,GSSG=氧化谷胱甘苷,G3P=甘油醛-3-磷酸,G6P=葡萄糖-6-磷酸,HBP=己糖胺生物合成途径,NADPH=还原烟酰胺腺嘌呤二核苷酸磷酸,OAA=草酰乙酸,ox=氧化,PPP=戊糖磷酸途径,Pyr=丙酮酸,Ser=丝氨酸,3PG=3-磷酸甘油酯。
然而,培养中增殖细胞和非增殖细胞的不同代谢表型表明,这些状态具有不同的代谢需求。大致上,增殖细胞有利于生物量的产生,而非增殖细胞有助于生物量的维持。与理解肿瘤代谢相关,并非所有癌细胞在许多实体肿瘤中都能活跃增殖[16]以及连续传代癌细胞系的机制选择对抗静止或较缓慢增殖的癌细胞(图1B),限制了迄今为止对这些肿瘤细胞群的研究。重要的是要认识到,对培养的癌细胞代谢的研究未能捕捉到增殖较少的肿瘤细胞的代谢表型。
葡萄糖和谷氨酰胺:增殖代谢的主要底物在体外
葡萄糖
除了吸收更多的葡萄糖外,培养物中增殖的癌细胞对葡萄糖的代谢与非增殖细胞不同,将葡萄糖衍生的大部分丙酮酸转化为乳酸,而不是通过三羧酸(TCA)循环将其氧化。Otto Warburg首先描述了一项观察结果,对于大多数正常细胞来说,在缺氧条件下,葡萄糖向乳酸的转化增加是有利的,而癌细胞即使在氧气充足的情况下也表现出这种表型[17]. 这种代谢表型被称为有氧糖酵解或Warburg效应,它是癌细胞的一个被广泛研究的特征[10].
通过糖酵解增加的葡萄糖流量(见词汇表)被认为促进代谢物分流到合成大分子的分支途径(见词汇)[10]. 例如,葡萄糖-6-磷酸通过戊糖磷酸途径(PPP)的氧化臂代谢产生NADPH和核糖-5-磷酸,这是新细胞生成的两个关键成分。NADPH对于管理氧化还原应激和还原性生物合成反应至关重要,而5-磷酸核糖是从头开始核苷酸合成[18]. 此外,一些癌细胞依赖下游糖酵解中间产物流入PPP的非氧化臂以生产核糖-5-磷酸(图2) [19,20]. 葡萄糖代谢也有助于核苷酸碱基的生成,在某些情况下,减慢这种生成可以限制增殖[21].
将糖酵解的另一产物果糖-6-磷酸转移到己糖胺生物合成途径(HBP)中,为蛋白质和脂质的糖基化提供了必要的底物,这是一种丰富的修饰,与肿瘤进展的几个方面有关[22]. 致癌K-ras和磷脂酰肌醇3-激酶(PI3K)/Akt途径激活被认为是通过HBP的葡萄糖流量的重要驱动因素[20,23]将这些信号通路直接与葡萄糖代谢的这一方面联系起来。因此,HBP作为一个整合中枢,确保持续的有丝分裂信号和增殖只在有利的条件下发生。
葡萄糖代谢的几个分支点为从头开始脂肪生成在分裂细胞中生成新的脂质膜。葡萄糖碳氧化为柠檬酸盐可以生成胞浆乙酰辅酶A,用于合成脂肪酸和甾醇。糖酵解产物也有助于形成两种不同的脂质头组。甘油醛-3-磷酸可进一步代谢为甘油-3-磷酸,形成三酰甘油酯和膜磷脂的甘油成分[18]. 神经酰胺和其他相关结构和信号脂质的合成需要丝氨酸,丝氨酸的来源之一是糖酵解产生的3-磷酸甘油酸[18]. 有趣的是,在一些癌症中发现了编码磷酸甘油酸脱氢酶(PHGDH)的基因扩增,PHGDH是催化葡萄糖丝氨酸生物合成途径的初始步骤的酶[24,25]. 虽然在扩增细胞系中敲除PHGDH会损害增殖,但外源性丝氨酸无法挽救这种效应,这表明通过这一途径的流量以不仅仅是丝氨酸产生的方式促进增殖。
谷氨酰胺
在细胞培养中,谷氨酰胺是仅次于葡萄糖的第二大消耗营养素[26]. 谷氨酰胺是两种血浆中最丰富的氨基酸[27]以及培养基,其消耗量与核苷酸和蛋白质合成的需求量相比过大[28,29]. 由于很少有葡萄糖衍生的碳进入TCA循环,谷氨酰胺氧化使细胞能够补充TCA循环中间体,用于生物合成反应[1,29]. 与糖酵解对应物一样,TCA代谢物也是合成代谢过程所必需的,以维持细胞增殖[18]. 例如,核苷酸和蛋白质合成所必需的几种非必需氨基酸,例如天冬氨酸和谷氨酸,可以从TCA循环中间产物中衍生出来。谷氨酰胺也是培养中增殖细胞氮的主要来源,这对从头开始核苷酸和氨基酸合成[29]. 促进谷氨酰胺吸收和利用的致癌突变确保了转化细胞持续和充足的氮供应。提取氮和进一步代谢谷氨酰胺碳的确切机制可能有所不同,因为Myc增加的细胞株支持谷氨酰胺分解(见词汇表),氮以氨的形式释放,而突变的K-ras则支持氮转氨为α-酮酸[三,4,30].
作为癌细胞营养素的其他氨基酸
虽然细胞培养中营养利用的大部分研究都集中在葡萄糖和谷氨酰胺的命运上,但癌细胞体内能够获得其他营养物质,包括支持增殖的氨基酸。例如,尽管许多癌细胞合成丝氨酸和甘氨酸从头开始最近的研究表明,从培养基中摄取这些营养素也很重要。对NCI-60细胞系的废培养基进行分析发现,甘氨酸水平与增殖率相关[26]. 这一发现可能反映了增殖过程中丝氨酸耗竭和氨基酸使用[31]因为在增殖最快的细胞中丝氨酸摄取量显著增加,几乎是甘氨酸摄取量的8倍[32]. 虽然丝氨酸和甘氨酸可以通过丝氨酸羟甲基转移酶(SHMT)相互转化,但这种相互转化的方向性可以对增殖细胞产生深远的影响。特别是,在没有甘氨酸的情况下,丝氨酸可以为核苷酸生物合成提供必要的细胞内甘氨酸和一碳单位,而甘氨酸不能补偿所有细胞中的无丝氨酸条件[31].
当丝氨酸水平较低时,过量的甘氨酸消耗一个碳单位和碳块从头开始核苷酸合成,阻止增殖[31]. SHMT的线粒体亚型(SHMT2)可能在这一块中起着关键作用,因为它从丝氨酸中生成叶酸,用于细胞系中的核苷酸生物合成[33,34]这种酶与甘氨酸裂解系统的活性相协调可以影响血管化不良肿瘤的增殖[35]. 像谷氨酰胺一样,细胞也会吸收超过蛋白质合成所需的丝氨酸。甘氨酸并非总是如此,这一发现与丝氨酸产生一些用于制造蛋白质的甘氨酸相一致[36]. 然而,DNA合成速率与甘氨酸摄取直接相关[36]与直接纳入13C-甘氨酸从培养基进入核苷酸的嘌呤骨架[26]. 因为葡萄糖代谢对核苷酸合成也很重要[21],了解葡萄糖衍生丝氨酸和甘氨酸相对于外源氨基酸的使用将非常重要。甘氨酸也有助于谷胱甘肽的合成,这在p53缺失细胞中至关重要[32]. 因此,虽然这些研究强调了可用的细胞外和新合成的丝氨酸和甘氨酸的独特贡献,但它们也强调了代谢环境如何影响细胞中的通路流量,并伴随着对增殖和生长的影响。确定是什么调节丝氨酸和甘氨酸的相互转化,以及如何调节这些氨基酸在不同代谢过程中的使用,是该领域的一个重要未决问题。
谷氨酰胺以外的氨基酸的分解代谢也可能导致肿瘤进展。例如,支链氨基酸转氨酶1(BCAT1)的表达对异柠檬酸脱氢酶(IDH)野生型胶质瘤的生长和进展是必要的[37]. 这些野生型IDH胶质瘤是脑肿瘤的一个独特亚群,与IDH获得性功能突变患者相比,其临床预后较差[38]. 支链氨基酸(BCAA)是血清中丰富的氨基酸[27] (表1),BCAT1的表达可能使BCAA成为TCA循环的额外碳源[37]. 然而,在这类胶质瘤以及其他癌症中,BCAA分解对癌细胞代谢的贡献需要进一步的表征。
表1。
在几项研究中报告的标准组织培养基中也发现了血浆/血清中的营养水平。还显示了不同标准培养基配方中相同营养素的浓度以进行比较。所有浓度均以μM为单位。
|
血浆/血清
|
媒体
|
| 人类 |
鼠标 |
BME公司 |
MEM公司 |
DMEM公司 |
RPMI公司 |
Blau等人
阿尔。一[100] |
阿尔布里顿b条
[101] |
麦克梅纳米
等。c(c)[102] |
纽加德
等。d日
[103] |
Pitkanen等人。e(电子)[104] |
Stein和
摩尔(f)
[27] |
Wuu等人
阿尔。克[105] |
阿尔布里顿小时
[101] |
男性40-
59岁 |
雌性
40-59岁 |
| 丙氨酸 |
146-494 |
449 |
320 |
367.3 |
406 |
347 |
383 |
243.7 |
662 |
|
|
|
|
| 精氨酸 |
28-96 |
132 |
68 |
115.3 |
128 |
99 |
86.6 |
25.5 |
55.7 |
100 |
600 |
400 |
1149 |
| 天门冬氨酸 |
32-92 |
|
|
16.5 |
65 |
58 |
43.9 |
77 |
|
|
|
|
379 |
| 天冬氨酸盐 |
2-9 |
|
|
17 |
18 |
22.5 |
9.1 |
|
|
|
|
150 |
| 胱氨酸 |
24-54 |
58.3 |
|
|
|
|
49.1 |
23.2 |
33 |
50 |
100 |
200 |
208 |
| 谷氨酸盐 |
6-62 |
54.4 |
<20 |
81.2 |
66 |
45 |
47.6 |
19.5 |
224.3 |
|
|
|
136 |
| 谷氨酰胺 |
466-798 |
|
450 |
561 |
556 |
568 |
261.8 |
|
1000 |
2000 |
4000 |
2055 |
| 甘氨酸 |
147-299 |
240 |
235 |
328.4 |
262 |
315 |
205 |
168.7 |
253 |
|
|
400 |
1334 |
| 组氨酸 |
72-108 |
90.2 |
88 |
81.9 |
107 |
96 |
74.1 |
65.5 |
103.1 |
50 |
200 |
200 |
97 |
| 异亮氨酸 |
46-90 |
122 |
57 |
149 |
74 |
58 |
67.9 |
95.1 |
114.4 |
200 |
400 |
800 |
382 |
| 亮氨酸 |
113-205 |
145 |
79 |
151 |
121 |
129 |
121.8 |
183 |
200 |
400 |
800 |
382 |
| 赖氨酸 |
135-243 |
205 |
143 |
|
232 |
203 |
186 |
182.9 |
438 |
200 |
400 |
800 |
219 |
| 蛋氨酸 |
13-37 |
33.5 |
28 |
27.6 |
33 |
26 |
25.5 |
17.1 |
67 |
50 |
100 |
200 |
101 |
| 苯丙氨酸 |
46-74 |
84.8 |
56 |
61.6 |
67 |
60 |
50.9 |
55.5 |
145.3 |
100 |
200 |
400 |
91 |
| 脯氨酸 |
97-297 |
|
142 |
158.1 |
|
|
205 |
131.1 |
156 |
|
|
|
174 |
| 丝氨酸 |
89-165 |
|
85 |
116.7 |
132 |
155 |
107 |
117.9 |
|
|
|
400 |
285 |
| 苏氨酸 |
92-180 |
168 |
135 |
|
148 |
142 |
117 |
97.1 |
294 |
200 |
400 |
800 |
168 |
| 色氨酸 |
25-65 |
53.9 |
21 |
|
54 |
51 |
54.4 |
126.4 |
102.8 |
20 |
50 |
80 |
24 |
| 酪氨酸 |
37-77 |
82.8 |
70 |
67.1 |
80 |
62 |
56.8 |
54.2 |
138 |
100 |
200 |
400 |
110 |
| 缬氨酸 |
179-335 |
239 |
174 |
235.3 |
267 |
204 |
246 |
176.4 |
367 |
200 |
400 |
800 |
171 |
| 葡萄糖 |
|
4996我
|
|
5578我
|
|
|
|
|
|
5500 |
5500 |
25000 |
11100 |
| 丙酮酸盐 |
27-160 |
136 |
|
90 |
|
|
|
|
|
|
|
1000 |
|
对患者源性胶质瘤样本代谢物的检测表明,半胱氨酸的部分分解代谢和半胱氨酸亚磺酸(CSA)的积累与肿瘤分级的增加有关[39]. 虽然大多数涉及半胱氨酸代谢的癌症研究都集中于半胱氨酸对谷胱甘肽的贡献[40,41],阻断半胱氨酸分解代谢到CSA独立抑制肿瘤生长[39]. CSA在这些肿瘤中的最终命运尚待确定。
支持增殖的额外氨基酸的分解代谢是一个有趣的主题;然而,现有数据表明,大多数氨基酸主要用于分裂细胞中的蛋白质合成[36,42]. 当其他营养物质受到限制时,氨基酸的分解可能对维持ATP和细胞氧化还原状态以支持细胞生存更为重要。与此断言一致,MYC公司诱导脯氨酸分解代谢向合成代谢的转变以支持增殖[43].
清除大分子、还原性TCA助熔剂和醋酸盐
除了葡萄糖和游离氨基酸的代谢外,癌细胞还可以分解细胞外蛋白,以补充其在某些遗传和环境条件下的营养需求。致癌的Ras公司表达刺激大胞饮作用,这一过程使细胞外物质能够不依赖于网格蛋白的吸收[44]. 然后,一些细胞外物质可以被输送到溶酶体,在那里蛋白质被降解,以提供可以进入中央碳代谢的氨基酸[45]. 当谷氨酰胺或必需氨基酸受到限制时,这个过程允许培养的肿瘤细胞增殖[45,46]药物抑制大胞饮作用可以减缓异种移植瘤的生长[45]. 了解肿瘤细胞在其环境中对细胞外物质代谢的依赖程度体内是一个活跃的研究领域。
细胞外脂质也可以是癌细胞的重要燃料。在细胞培养中,葡萄糖为从头开始脂质合成。在两种致癌情况下Ras公司然而,溶血磷脂的表达或缺氧也会导致脂肪酸蓄积[47]. 这种摄取补偿了在两种条件下观察到的通过丙酮酸脱氢酶(PDH)的葡萄糖碳流量的减少[1,48]. 低氧也会改变谷氨酰胺碳进入TCA循环的命运,因为它有利于还原代谢而非氧化代谢,从而成为脂肪酸合成中乙酰辅酶a的来源[48-50],部分用于补偿葡萄糖对柠檬酸盐的贡献减少[51].
其他碳源也可用于脂质合成。最近的数据表明,尽管醋酸盐在细胞培养基和血清中的含量相对较低,但它也有助于脂肪酸合成和TCA循环代谢[52-54]. 醋酸盐通过乙酰辅酶A合成酶(ACSS)的作用转化为乙酰辅酶B,ACSS2对至少某些肿瘤类型的生长至关重要体内[55]..
位置、位置、位置
许多研究表明,癌细胞在培养过程中可以利用多种燃料,这表明尽管遗传和环境背景有利于某些底物的使用,但仍存在代谢灵活性。这表明肿瘤中癌细胞的新陈代谢将受到营养物质可用性的严重影响,并揭示了细胞培养的潜在局限性,因为它不一定模拟组织中的营养条件。改变培养条件以保持恒定的营养水平是一种用于产生洞察力的方法[56]然而,标准细胞培养基中含有超过血浆营养水平四倍的营养物质,不同营养物质的比例也与发现的不同体内(方框1和表1). 还有其他营养素,包括醋酸盐,它们存在于血液中,但没有添加到标准培养基中(表2). 在缺氧或低水平特定营养素中培养细胞可能会提供信息,但在大多数情况下,这些扰动伴随着培养基中其他营养素的超生理水平,无法模拟低灌注的现实。由于对肿瘤环境建模的最佳方法尚不明确,研究肿瘤代谢的努力体内这对于下一步了解癌症代谢至关重要。
方框1。细胞培养基的开发。
早期细胞培养基需要补充大量血清,以便详细调查生长需求在体外仍然不切实际。1955年至1956年,哈里·伊格尔及其同事首次概述了特定的氨基酸、维生素、盐和其他营养素,这些营养素使两种细胞系(成年小鼠成纤维细胞和HeLa细胞)能够持续培养,只需添加少量血清[28,108,109]. 这些研究为最初的标准化培养基配方奠定了基础,该配方后来被称为基本中型鹰(BME)(表1). 这些研究中有两个观察结果。首先,谷氨酰胺被认为是与其他氨基酸分离的,并且相当于葡萄糖,作为培养物中增殖的需要。第二,虽然支持生长的最佳氨基酸浓度是根据经验确定的,但浓度故意保持在Albritton报告的生理范围附近[101,108].
Eagle及其同事在接下来的几年里进行了额外的工作,开发了最低限度的基本媒体(MEM)[110]. 这种培养基可以培养更多的细胞系,其BME中的氨基酸含量增加了两倍或更多(表1). 这些变化旨在更加符合培养的人类细胞中总蛋白的氨基酸组成[110]. 1960年,玛格丽特·沃格特(Marguerite Vogt)和雷纳托·杜尔贝科(Renato Dulbecco)在研究多瘤病毒与胚胎细胞之间的相互作用时,进一步修改了MEM,使其氨基酸和维生素的浓度达到鹰(Eagle)描述的四倍[111]. 这种培养基,现在被称为DMEM(Dulbecco改良的Eagle培养基),它还含有五倍于血液中正常浓度的葡萄糖(表1),已成为当今使用的标准文化媒体。
乔治·摩尔(George Moore)和罗斯韦尔公园纪念研究所(RPMI)的同事们以类似于伊格尔(Eagle)过去十年的研究的方式,开展了类似的工作,主要关注正常和转化血细胞培养基的开发。这项工作催生了一系列类似的媒体,包括RPMI 1640[112]最初设计用于培养正常初级白细胞,现已成为现代组织培养的另一个主力。RPMI与DMEM的主要区别在于添加的氨基酸数量(表1).
自这些早期研究以来,已经进行了许多额外的修改,以生成专门的培养基,尽管这些修改在很大程度上都是基于Eagle和Moore的开创性和艰苦的工作,在大多数情况下,主要差异在于添加了新的生长因子和激素。现在可以在完全确定的(无血清)培养基中培养一些细胞,但营养成分仍然基于经典配方。
表2。
未添加到标准组织培养基中的代谢产物的血浆/血清水平可能是体内组织的营养来源。所有列出的代谢物在至少90%的对照患者中均可检测到,所有浓度均以μM为单位。所有值均来自Hoffman等人[106],除非另有说明。
| 营养物 |
平均 |
范围一
|
| 乳酸 |
1700 |
700–3300 |
| 乙醇酸盐 |
27 |
9–42 |
| 2-羟基丁酸酯 |
54 |
8–80 |
| 3-羟基丁酸酯b |
180 |
22–170 |
| 3-羟基丁酸酯 |
20 |
4–48 |
| 甘油酸盐 |
10 |
未注明日期:24 |
| 焦谷氨酸盐 |
51 |
13–161 |
| 乙酰乙酸b条
|
21 |
未注明日期:86 |
| 2-氧代-3-甲基-n个-戊酸盐 |
18 |
8–31 |
| 2-氧异丙酸盐 |
28 |
编号:58 |
| 月桂酸酯 |
12 |
2–37 |
| 异柠檬酸盐 |
6 |
未注明日期–10 |
| 柠檬酸盐 |
190 |
30–400 |
| 醋酸盐[107] |
51 |
2–99 |
| 甘油三酯 |
|
450–1710 |
研究细胞的代谢需求体内增加了许多生物和实验复杂性。营养物质可用性体内在器官内和跨器官的细胞类型之间可能会有所不同。例如,肝脏的结构导致氧和营养物质在肝细胞区域的梯度[57]. 肿瘤也有微血管中断引起的葡萄糖和氧气可用性梯度,导致肿瘤和邻近正常组织的营养吸收不同[58-61]. 此外,代谢产物的稳态调节以及多种组织和细胞类型参与确定营养水平体内为实验目的而使营养水平的操作复杂化[32].
正常组织中营养物质可用性的差异可能决定了这些组织使用的代谢程序。有趣的是,这些程序似乎限制了肿瘤细胞的代谢储备体内试验。对22种人类肿瘤类型和正常组织的代谢基因的表达分析表明,与其他组织的肿瘤相比,肿瘤的表达模式更接近其起源组织的表达模式[62]. 原组织甚至限制了相同致癌因子在不同组织中的作用Myc公司-与谷氨酰胺代谢相关的不同表型的肝癌和肺癌[63]. 更为复杂的是,由同一组织中不同致癌基因驱动的肿瘤也可能表现出不同的代谢程序[63]. 因此,尽管某些中枢代谢途径(如核苷酸生物合成)的上调与组织类型和驱动因子突变无关,但其他途径的使用是异质的,可能反映了癌症起源的组织和对可用营养素的适应[62].
肿瘤细胞还与正常宿主组织发生代谢相互作用,对癌症发病机制产生深远影响。例如,肥胖和糖尿病等全身代谢改变影响许多癌症的发展和进展,包括胰腺癌[64-67]. 胰腺癌反过来会改变全身代谢,导致许多患者新发糖尿病和恶病质,肿瘤可以分泌改变全身代谢率的因子[68-72],. 考虑到营养供应的变幻莫测体内,这些全身代谢相互作用表明肿瘤可能会积极地努力控制其环境,从而为其生长创造有利条件[73]. 为此,早期胰腺癌可导致全身蛋白质周转增加,并在诊断前多年伴随氨基酸释放[74].
肿瘤的代谢异质性
肿瘤细胞之间的另一个本质区别在体外和体内当每个细胞在体外必须增殖或在传代时丢失,体内在任何给定的时间,只有一小部分肿瘤细胞在活跃分裂[16]. 已经观察到胶质母细胞瘤细胞中细胞周期标记物的表达谱存在显著的细胞间差异,这与整个肿瘤的可变增殖相一致[75]. 同样的研究也发现低氧相关基因表达与肿瘤内O2梯度,为代谢程序的肿瘤内异质性提供证据[75]. 丙酮酸激酶活性要求的差异也表明,增殖和非增殖肿瘤细胞对葡萄糖的使用不同,葡萄糖的代谢方式会影响细胞增殖的能力体内[16].
营养物质可用性和代谢表型的空间异质性允许肿瘤内不同细胞群之间的代谢合作。例如,缺氧癌细胞释放的乳酸可以作为邻近正常氧细胞生长的氧化燃料[76,77]. 也有人提出,肿瘤细胞可能在癌相关成纤维细胞(CAF)中诱导类似的代谢表型,诱导它们释放乳酸、二肽和酮体,以促进肿瘤氧化代谢[78-80]. 与非恶性肿瘤基质细胞的代谢相互作用也可以直接影响疾病进展、转移和氧化还原状态。卵巢肿瘤经常转移到网膜,部分是由于网膜脂肪细胞释放脂肪因子而引起的[81]. 一旦到达目的地,脂肪细胞向肿瘤细胞的直接脂质转移支持癌细胞增殖,因为脂肪细胞上调脂肪分解,与肿瘤细胞中β-氧化增加相一致[81]. 在慢性淋巴细胞白血病中,骨髓基质细胞对胱氨酸的代谢产生半胱氨酸,以支持肿瘤细胞中谷胱甘肽的合成[82]. 使用基于质谱的组织中代谢物空间分布评估的新方法可能有助于进一步了解[83,84],尽管还需要开发更多的新方法来阐明肿瘤组织中不同细胞类型之间的复杂相互作用。
肿瘤代谢测定体内
癌症代谢研究体内已经发现,与细胞培养模型一致,大多数肿瘤相对于周围正常组织增加了营养吸收。医生利用这一点使用[18F] -2-脱氧葡萄糖正电子发射断层扫描(FDG-PET),这是一种有助于癌症分期和衡量治疗反应的方法[85,86]. [18F] -谷氨酸和谷氨酰胺类似物也正在作为肿瘤显像剂进行研究[87,88],按原样[11C] -醋酸盐[89]这些药物可能有助于追踪FDG-PET阴性肿瘤[88]. 迄今为止,PET示踪剂(见术语表)在提供营养吸收以外的信息方面受到了限制,因为通过这种成像方法无法区分下游代谢中的标记物种。然而,通过组织取样评估了谷氨酰胺并入蛋白质和转化为谷氨酸的情况[88].
放射性同位素和稳定同位素都被用于研究癌症代谢表型体内[90]. 虽然早期的研究仅限于全身代谢的研究,但他们证实了葡萄糖氧化增加[91,92],蛋白质周转[93]和脂肪分解[94]在肿瘤患者中。最近的研究将稳定同位素示踪剂的使用与核磁共振(NMR)光谱或质谱(MS)相结合,以确定组织中不同营养素的确切命运。在一个例子中,[U-13C] 葡萄糖发现Warburg效应体内可能不是通用的,因为Myc公司-驱动性肝肿瘤显示葡萄糖-乳酸转换增加,而遇见-驾驶者没有[63]. NMR光谱的使用也可以提供对活体动物肿瘤代谢动态变化的见解[95],尽管即使使用超极化方法来提高灵敏度,但迄今为止追踪到的代谢物的多样性也是有限的[96].
比较组织中的营养素命运体内,可以使用实现稳定同位素示踪剂的稳态等离子体富集的方法[16,97]. 注射[U-13C] FDG-PET阳性颅内肿瘤患者体内的葡萄糖显示,虽然葡萄糖如预期那样被代谢为乳酸,但大量葡萄糖也通过TCA循环被氧化[98]. 葡萄糖也被发现有助于从头开始脑肿瘤中谷氨酰胺合成的研究[98]. 将标记的葡萄糖输注到原位人类胶质母细胞瘤移植小鼠体内,进一步证实了葡萄糖进入TCA循环的流量以及葡萄糖产生谷氨酰胺的量高于预期[97]. 在研究其他体内需要建立模型来了解脑癌是否在代谢表型或小鼠和人类肿瘤之间的相似性方面代表一个独特的病例(方框2),结果表明营养素的使用体内与大多数细胞系中观察到的情况不同。
方框2。新陈代谢的种间差异。
十多年前,Rangarajan和Weinberg在讨论用老鼠模拟人类癌症时,吟诵道:“老鼠不是小人物”[113]. 然而,小鼠仍然是研究癌症的有力工具,因为它们易于进行基因操作,世代相对较短,并且与人类有许多生理相似性。然而,存在重要的物种特异性差异。小鼠自发性癌症的自然病史和组织光谱与人类不同[113]. 引入组织特异性的原癌基因改变是建立器官肿瘤发生模型的有力工具,虽然这些改变通常再现了人类疾病的许多病理特征,但也存在差异,包括小鼠肿瘤细胞之间的遗传异质性小得多。此外,啮齿类动物的代谢率高出7倍[114]可能在组织如何响应人类癌症中发现的基因变化和改变的信号通路方面发挥作用。
不同哺乳动物对营养物质的处理也可能存在显著差异。虽然小鼠和大鼠通常用于研究2型糖尿病,但从葡萄糖调节转录因子到胰岛素分泌机制,再到葡萄糖处理的初级组织,啮齿动物在各个水平上的葡萄糖代谢都与人类不同[115]. 毫不奇怪,氨基酸在蛋白质合成需求和组织中单个氨基酸的相对分解代谢方面也表现出物种特异性差异[116,117]. 大量营养素(见词汇表)处理上的这些差异可能是由于哺乳动物的饮食成分差异很大。当不同物种被用作研究新陈代谢及其对疾病影响的研究工具时,未能解释这些代谢差异可能会影响研究结果的可翻译性[115].
尽管有这些警告,但从人类癌症的小鼠模型中可以获得重要的见解,并为研究癌症代谢提供了强有力的工具体内试验。人类和小鼠在早期胰腺癌引发的支链氨基酸(BCAAs)中都有相同的升高,在小鼠中研究这种表型的能力发现,氨基酸水平的变化反映了蛋白质周转的增加[74]. 同样,对小鼠人脑胶质母细胞瘤葡萄糖代谢的详细研究显示,与在胶质母细胞癌患者肿瘤中观察到的表型几乎相同[97,98]. 考虑到术中研究的复杂性,以获得对人类肿瘤的代谢洞察力体内与动物研究结果的一致性表明,通过使用小鼠模型进行更容易控制的实验,可以获得对人类疾病的真正机制性见解。对每个物种的表型发现进行仔细验证,可以提高对小鼠表型进行机械解剖的可能性,从而为改善患者护理提供信息。
结束语
对培养中癌症代谢的研究提高了我们对增殖代谢需求的理解。体外细胞培养将继续允许研究单个细胞类型的代谢特征以及谨慎的遗传和环境操作的影响。事实上,许多细胞类型之间代谢共生的例子都是通过培养系统来定义的[77,79-82]. 然而,要继续从文化体系中获得洞察力,对上述局限性有更深入的认识是很重要的(方框3). 来自的有限数据体内研究表明,整个动物体内的癌症代谢可能与培养中观察到的不同。这种差异是否反映了构成肿瘤主体的低增殖癌细胞群的代谢表型尚待确定,但研究体内将有助于研究这些细胞以及不适合细胞培养的癌症类型。研究体内对于探测可能对患者预后产生重大影响的肿瘤-宿主组织相互作用也很重要[70]. 最后,了解不同组织中与肿瘤生长相关的代谢变化的能力也将受益于癌症代谢的研究体内并告知我们对转移的理解[99]. 最重要的是,体内研究将有助于指导在相关临床环境中更有效地针对那些有助于肿瘤进展的代谢变化。
方框3。未决问题。
长期培养如何形成癌细胞的代谢依赖性?
在多种癌症类型中,半胱氨酸、醋酸盐、BCAA和蛋白质等不同代谢底物相对于葡萄糖和谷氨酰胺的重要性是什么?
非增殖肿瘤细胞与增殖肿瘤细胞的代谢需求有何不同,能否开发条件来研究培养中的这些非增殖细胞?
“不可培养”肿瘤细胞群的代谢表型是什么?
肿瘤细胞与肿瘤内和远处组织中的正常细胞群之间的代谢关系是什么?能否开发系统来研究这些共生关系体内?
起源组织和肿瘤生长的组织部位如何影响癌细胞的代谢表型体内?
癌症模型如何忠实地再现在人类癌症中观察到的代谢变化?
致谢
我们感谢Vander Heiden实验室的所有成员在编写本手稿的整个过程中进行了深入的讨论和反馈,特别感谢A.M.Hosios和D.Y.Gui协助生成了培养增殖模型,感谢S.M.Davidson就新陈代谢进行了讨论体内我们感谢R.J.Debrardinis、A.M.Hosios和W.J.Israelsen为编制血浆营养值所做的贡献。我们也感谢审稿人花时间和周到的评论来改进我们的手稿。由于篇幅有限,我们很遗憾无法引用许多优秀的论文。J.R.M.得到F30 CA183474的支持。M.G.V.H.感谢Burroughs Wellcome基金会、Lustgarten基金会、美国癌症研究协会和NCI的支持。
词汇表框
- 合成代谢:
需要输入能量以在细胞中合成新大分子的生化反应。
- 列车自动防护系统:
三磷酸腺苷。电池的主要能源货币。
-
分解代谢的:
通过氧化各种营养物质为细胞提供能量的生化反应。
-
通量:
每单位时间通过代谢途径的代谢产物流动速率。
- 谷氨酰胺分解:
TCA循环中谷氨酰胺的氧化代谢。
- 大分子:
构成细胞大部分结构的大型聚合物,包括DNA、蛋白质和脂质
- 大量营养素:
描述大量所需营养素的一般术语,如碳水化合物、蛋白质和脂肪。
- NADPH公司:
还原烟酰胺腺嘌呤二核苷酸磷酸。细胞内氧化还原反应的辅因子,主要用作还原反应的电子源。它对于许多合成代谢反应和应对活性氧物种非常重要。
- 静态:
非营利性。
- 示踪剂:
代谢物的一种版本,其中一个或多个原子被该原子的不同同位素版本所取代,从而可以使用质谱或核磁共振光谱来追踪差异。如果使用的同位素具有放射性,也可以使用放射性检测方法。
脚注
披露M.G.V.H.是Agios Pharmaceuticals的顾问和科学顾问委员会成员,该公司致力于以癌症代谢为目标,以获得治疗益处。
出版商免责声明:这是一份未经编辑的手稿的PDF文件,已被接受出版。作为对客户的服务,我们正在提供这份早期版本的手稿。手稿在以最终可引用的形式出版之前,将经过编辑、排版和校对结果证明。请注意,在制作过程中可能会发现可能影响内容的错误,适用于该期刊的所有法律免责声明均适用。
关联数据
本节收集本文中包含的任何数据引用、数据可用性声明或补充材料。




