摘要 肝脏在损伤后再生的能力是独特的,在此过程中,肝细胞通过细胞粘附复合物主动分裂并建立细胞-细胞接触。 在这里,我们证明了α-连环蛋白(一种公认的粘附成分)的缺失会显著破坏肝脏再生。 使用部分肝切除模型,我们发现α-catenin击倒小鼠的再生肝明显大于对照再生肝,细胞大小和增殖增加。 这种增殖增加与YAP激活增加相关,这与Hippo/YAP途径中的α-catenin有关。 此外,α-catenin敲除小鼠表现出类似临床胆汁淤积症的表型,胆小管急剧改变,胆汁成分水平升高,并有黄疸和炎症迹象。 再生能力受损是肌动蛋白细胞骨架结构紊乱的结果,导致顶端微绒毛丧失,胆管内腔扩张,以及紧密连接处漏水。 这项研究阐明了α-连环蛋白在肝脏再生中的一种新的重要作用。
肝病在世界范围内普遍存在,美国统计数据显示,十分之一的人患有某种形式的肝病,如脂肪肝、丙型肝炎或肝癌 1 据报道,肝病也是欧盟第五大死亡原因,至少占六分之一 2 虽然有一些特定的治疗方法可用于治疗肝病,但存活率主要取决于肝脏的再生潜力。 与其他器官不同,肝脏具有通过再生而非疤痕形成从损伤中恢复的独特能力 三 有鉴于此,过去几十年来,为了将治疗策略应用于临床,人们对肝脏再生进行了广泛研究。 研究肝脏再生的最典型范例是在啮齿类动物中使用部分肝切除术,这会导致肝脏特异性再生反应 4 在肝再生过程中,不同的细胞内和细胞外信号被刺激,从而激活静止的肝细胞重新进入细胞周期并增殖,恢复肝体质量比。 随后肝脏结构的重塑适应了细胞数量的增加,并将肝脏恢复到再生前的正常状态 5 .
在肝再生过程中,新形成的肝细胞通过连接复合体的组装形成高度极化的索。 粘附连接是连接形成的第一个关键事件,由钙粘蛋白-钙调素复合体启动。 经典的钙粘蛋白是跨膜糖蛋白,通过亲同性相互作用确保细胞间粘附,并通过α-连环蛋白间接连接到皮质肌动蛋白细胞骨架。 α-肌动蛋白是一种具有两个肌动蛋白结合域的机械传感器和机械传感器 6 羧基末端结构域可以直接与肌动蛋白微丝结合(如果α-catenin受到力诱导的跨信息作用) 7 , 8 , 9 或EPLIN(上皮蛋白在肿瘤中丢失) 10 ,用作肌动蛋白束丝。 需要通过在C末端产生肌动蛋白力来揭开中央结构域的神秘面纱,从而可以接触到维酮结合,进而促进肌动蛋白微丝的组装 6 。因此,当两个站点协同工作时,粘合强度最大化 11 通过EPLIN和vinculin锚定肌动蛋白丝,以调节细胞骨架对细胞外信号的反应 12 .
最近出现了几项研究,证明了α-连环蛋白的新作用。 据报道,α-连环蛋白不仅仅是一种连接蛋白,而是在粘附过程中控制肌动蛋白细胞骨架组织的分子开关 7 , 13 此外,消融小鼠表皮中的α-连环蛋白会导致鳞状细胞癌的缺陷,包括过度增殖和细胞极性不规则 14 α-catenin的这种抗增殖作用已经通过使用靶向大脑的条件α-catentin敲除小鼠得到证实 15 以及将α-catenin与Hippo通路联系起来的研究 16 此外,还强调了α-连环蛋白在微管调节中的作用 17 .
以前的工作对肝脏中的增殖是由肝干细胞还是成人肝细胞引起的存在争议,但一项结论性研究表明99%的新肝细胞来源于先前存在的成人肝细胞 18 因此,研究α-连环蛋白在现有肝细胞中的敲除作用,以及它如何影响增殖和新的细胞-细胞接触的形成,可能有助于阐明α-连环素在肝再生过程中的作用。
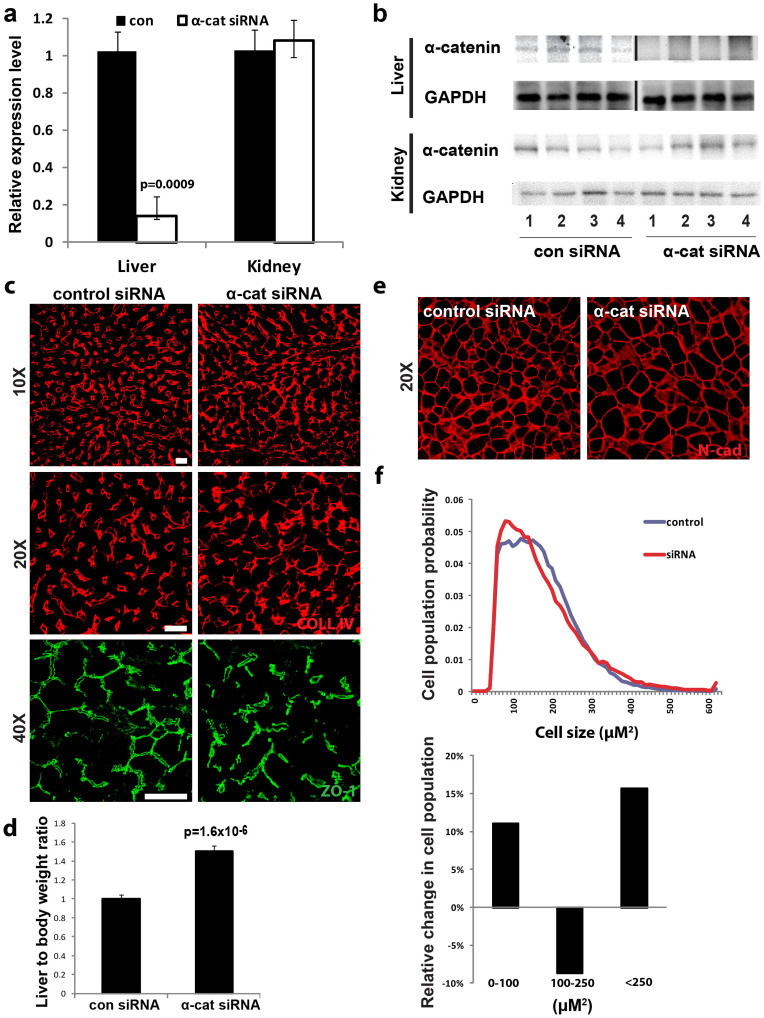
结果 要确定 体内 α-catenin在肝脏再生中的意义,通过将α-catentin siRNA封装在脂质纳米粒(LNPs)中并修饰以特异性靶向肝脏,实现对该基因的肝脏特异性敲除 19 , 20 , 21 , 22 。作为对照器官的肝脏和肾脏是从长期注射siRNA-LNP的小鼠中获得的( 图S1A ). 然后对这些组织进行转录水平分析,以确保敲除和特异性。 与对照siRNA注射的肝脏相比,α-catenin siRNA注射肝脏中的α-catentin表达显著降低,而对照器官(肾脏)的转录水平在两组之间没有任何变化( 图1A ). 同样,通过蛋白质印迹和免疫组织荧光测定,我们观察到蛋白质水平相应降低( 图1B , 图S1B–C )后者显示α-catenin在整个组织中均匀沉默,主要在肝细胞中。
图1。 肝脏中α-连环蛋白的特异性敲除导致肝功能单位发生重大改变。
(A) 注射α-catenin siRNA-类固醇颗粒(LNP)的小鼠在肝脏中的α-catentin转录水平(每组n=6)表现出特定的下调,但在肾脏中没有(每组n=4)。 (B) 肝脏α-catenin蛋白水平相应下降(每组n=6)。 所示凝胶图像经过裁剪,呈现简洁。 (C) 用针对IV型胶原(红色;10倍和20倍)和闭塞带(ZO)-1(绿色;40倍放大)的抗体对再生的肝组织进行免疫标记。 在α-catenin siRNA-处理的肝脏中,用IV型胶原标记的窦状突是曲折的和无组织的。 ZO-1免疫标记的胆管排列在一个有组织的管状结构网络中,而在α-catenin-siRNA注射的肝脏中观察到该网络中断。 BC的管腔也扩大了。 (D) 收获后,对肝脏进行解剖和称重。 α-catenin-siRNA注射的肝脏比对照肝脏大50%。 (E) 用N-钙粘蛋白对肝切片细胞膜进行免疫标记(红色;20倍放大),结果显示α-catenin siRNA注射的肝脏中的一些细胞明显较大。 (F) 对实验肝脏的细胞大小进行了统计分析。 顶部:计算并显示了单元格的概率分布图。 底部:计算了对照组和α-catenin siRNA细胞群之间的差异,并用siRNA和对照组之间的百分比变化表示。 这表明,与对照肝脏相比,α-catenin siRNA注射的肝脏在大小细胞组分中的富集程度更高(对照组:n=8,α-cat:n=11)。 比例尺,50µm。
肝脏由肝细胞索组成的功能单元和肝细胞索之间的血管组成,肝细胞索形成胆管。 血管网形成窦状结构,这些窦状结构是排列在肝细胞基底外侧膜上的有序、间隔良好的管状血管。 在顶膜上,胆小管排列在一个由紧密连接密封的有序的小管网络中。 肝细胞质膜的极化对于转运蛋白的定位至关重要,而转运蛋白对肝细胞功能至关重要。 为了研究α-连环蛋白在肝脏结构形成和维持中的作用,我们选择了一个成熟的肝脏再生模型(部分肝切除术),以考察其重复性和有效性 4 ( 图S1A ). 在手术条件下,三分之二的肝脏被切除,再生的肝叶在七天后收获; 这段时间足以使肝组织再生70%以上 4 有趣的是,我们发现α-连环蛋白敲低的肝脏表现出极为紊乱的表型。 在击倒小鼠中,肝索断裂与肝细胞肥大和增生相关。 肥大的肝细胞因颗粒或“毛玻璃”深嗜酸性细胞质和增大的细胞核而增大,主要见于门脉周围和中环区,较少见于中央静脉周围( 图S2 ). 敲除肝脏中的窦状体高度弯曲、紊乱且间距不均。 ZO-1免疫标记显示胆总管网状结构也严重紊乱,正常分支的网状结构被畸形、断开的结构所取代,管腔扩大( 图1C ). 为了确定这种结构紊乱是由于肝细胞中α-catenin的特异性敲除所致,我们沉默了AML12细胞中的α-catentin,AML12是一种小鼠肝细胞系,已知其具有典型的肝细胞特征,如过氧化物酶体和胆管样结构。 α-catenin的敲除导致ZO-1标记的中断,这与观察到的情况类似 体内 ( 图S3A ). 类似地,当α-catenin在分离的原代肝细胞中沉默时,如观察到的那样,胆管显示出扩大的管腔 体内 ( 图S3B ). 我们还注意到敲除肝脏中的肝脏肿大,在物理和细胞水平上都有肿大,并且肝体重比增加了60%( 图1D ). 经过更仔细的检查,我们发现敲除的肝脏具有更大比例的肝细胞( 图1E ). 对细胞大小的进一步分析显示,敲低肝脏中的细胞大小有很大变化,比中值大小(100-250µm)更小和更大的细胞比例明显更高,这导致中值大小与对照相比相应降低( 图1F ). 肝细胞大小的这种不均匀反映了肝脏的普遍组织混乱,因为肝细胞通常大小均匀,以维持血管沿着肝细胞索的有序排列。 在形态学水平上,我们的结果表明,α-catenin的敲除破坏了肝脏再生机制,导致肝脏结构严重紊乱。
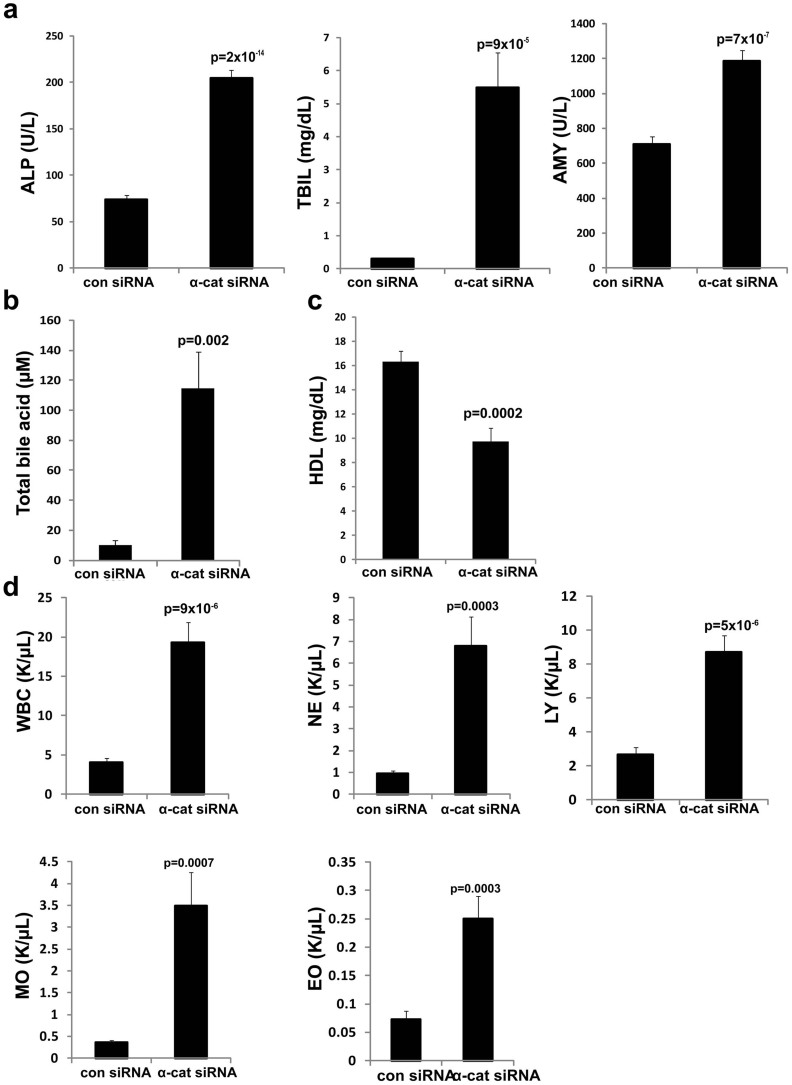
为了进一步研究这种无组织化对肝脏代谢的影响,从这些小鼠的血液样本中测定了几种肝酶。 有趣的是,α-catenin击倒小鼠的碱性磷酸酶(ALP)和总胆红素(TBIL)水平显著升高。 临床上,这些变化表明胆汁流动中断,表现为人类胆汁淤积症( 图2A ). 淀粉酶(AMY)水平也升高,这可能发生在胆汁运输受阻后( 图2A ). 一组小鼠也出现黄疸症状,皮肤呈黄色色素沉着,这与胆红素水平升高一致(数据未显示)。 由于胆汁流动中断意味着胆汁酸在血液循环中积聚,我们接下来评估了血浆中的总胆汁酸(TBA)水平。 正如预期的那样,我们发现α-catenin击倒小鼠的血清TBA水平比对照小鼠增加了10倍,符合胆汁淤积样表型( 图2B ). 此外,由于胆汁通常分泌到胃中以重新吸收脂质,如果胆汁流动受阻,预计脂质含量会降低。 事实上,α-catenin击倒小鼠的高密度脂蛋白(HDL)水平显著降低( 图2C ). 最后,进行血液学分析以评估炎症迹象。 在击倒小鼠中,包括所有细胞亚型(中性粒细胞、淋巴细胞、单核细胞和嗜酸性粒细胞)在内的总白细胞计数升高,与炎症反应一致( 图2D ).
图2。 α-catenin击倒小鼠的血液化学显示体内胆汁淤积。
在肝脏收获时对小鼠的血液样本进行血液化学分析,并测量与肝功能相关的几个标记物。 (A) α-catenin siRNA注射组的碱性磷酸酶(ALP)水平显著升高。 高ALP水平在临床上与胆管功能障碍有关。 与对照组相比,siRNA注射组的总胆红素(TBIL)含量也升高,这表明胆汁生成和流动障碍。 α-catenin注射组的淀粉酶(AMY)水平也显著升高,这在临床上与胆汁流动中断有关(对照组:n=17,α-cat:n=21)。 (B) α-catenin注射组的总胆汁酸(TBA)水平也升高,这表明血液中TBA的积累很高。 (C) α-catenin注射组的高密度脂蛋白(HDL)水平显著降低,对应于胆汁转运受阻(con:n=9,α-cat:n=10)。 (D) siRNA注射小鼠的白细胞总数(WBC)显著升高,表明有炎症反应。 此外,白细胞群中的不同亚群均显著升高,包括中性粒细胞(NE)和单核细胞(MO)、淋巴细胞(LY)和嗜酸性粒细胞(EO)。 K/µl:千/微升血液(con:n=17,siRNA:n=21)。
为了确定α-catenin敲除的效果是否与再生过程有关,在未进行部分肝切除的情况下沉默α-catentin的表达。 观察到明显更温和的表型。 胆管的分支结构部分消失,管腔略微扩大( 图S4A ). α-catenin击倒小鼠的碱性磷酸酶和淀粉酶水平显著升高( 图S4B–C ),但我们测量到总胆红素水平没有显著变化( 图S4D ). 此外,α-catenin击倒小鼠的肝脏重量没有显著增加( 图S4E ).
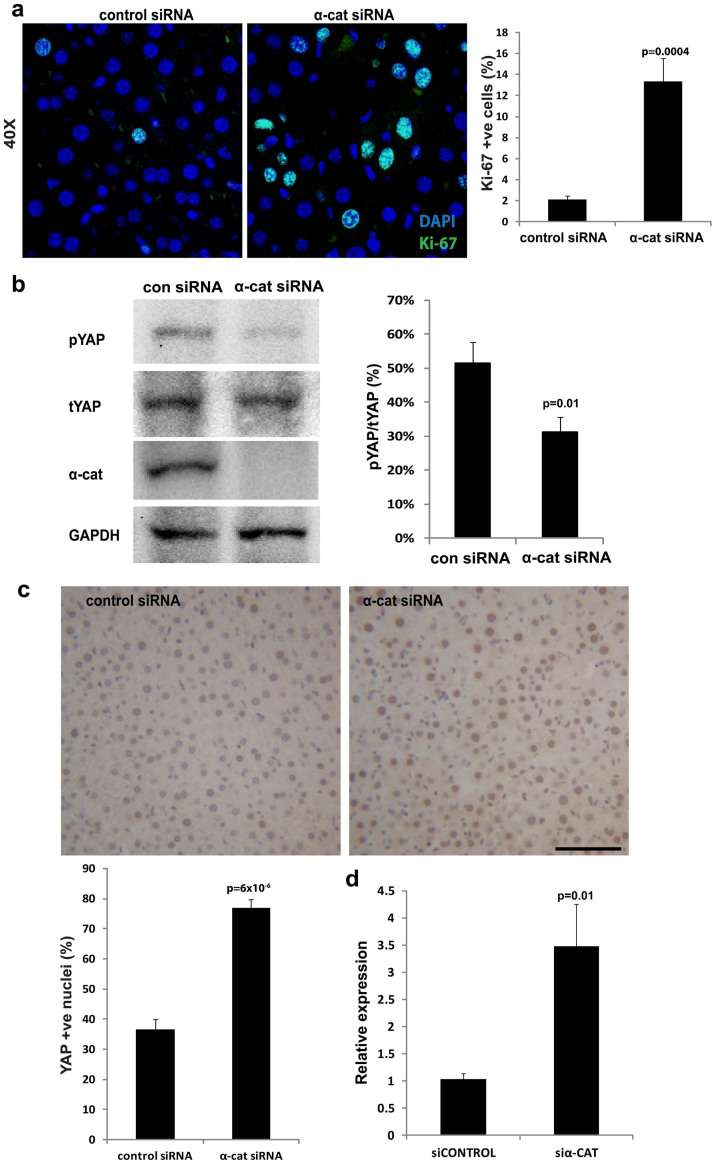
接下来,我们试图了解α-catenin的丢失是如何导致这些缺陷的。 观察到的肝脏大小增加可能是由于肝细胞大小增加或细胞数量增加。 因此,我们生成了一个肝脏模拟模型,以计算仅由细胞大小增加引起的假设肝脏大小增加。 该分析表明,观察到的细胞大小增加只能解释肝质量增加1.3%的原因( 图S5 ). 因此,为了确定肝脏大小的增加是否是由于增殖引起的,用增殖标记物Ki67对再生的肝脏切片进行免疫标记。 与对照切片相比,敲除肝切片显示Ki67阳性染色的程度要高得多。 定量分析Ki67阳性细胞的百分比表明,与对照组相比,α-catenin击倒肝脏中Ki67标记细胞的数量增加了6倍(分别为13.37%和2.1%)( 图3A ).
图3。 肝脏大小的增加是由于YAP激活导致肝细胞增殖增加所致。
(A) 用抗Ki67抗体(绿色)和DAPI(蓝色)对肝切片的细胞核进行免疫标记。 左:对照组和α-catenin敲除肝脏切片的代表性图像。 比例尺,50µm。 右图:然后计算α-catenin敲除和对照肝脏中Ki67阳性细胞占所有核阳性细胞的百分比。 与对照肝相比,α-catenin敲除的肝表现出更高的增殖水平(%)(分别为13.37%和2.1%)。 (B) 对肝脏裂解物进行磷酸化(p)YAP和总(t)YAP的印迹,在α-catenin敲除的肝脏中磷酸化YAP与总YAP的比率(百分比)显著降低(每组n=9)。 所示凝胶图像经过裁剪,代表了在相同实验条件下运行的凝胶。 (C) 用抗YAP抗体(棕色)对肝切片的细胞核进行免疫标记。 上图:对照组和α-catenin敲除肝脏切片的代表性图像。 比例尺,50µm。 左下图:计算α-catenin敲除和对照肝脏的YAP阳性(+ve)细胞核百分比(每组n=7)。 (D) 结缔组织生长因子(CTGF)是YAP的一个重要下游转录靶点,对其基因表达水平进行了评估。 CTGF在α-钙蛋白敲除的肝脏中显著上调(对照组n=7,α-钙素组n=10)。
以前的报告已经将肝脏中的增殖增加与Hippo-YAP途径联系起来。 此外,α-catenin已被确定为Yap1的物理相互作用物,Yap1是河马途径中的一个重要参与者 16 为了探索这种可能的联系,我们进行了western blotting以确定YAP磷酸化的任何变化,这是一种干扰其核定位的翻译后修饰。 有趣的是,α-连环蛋白敲除导致磷酸化YAP百分比持续下降(作为总YAP的一个功能),因此支持此途径参与细胞增殖( 图3B ). 鉴于磷酸化/活化的YAP转位到细胞核以激活下游转录靶点,我们接下来试图通过量化YAP阳性细胞核的百分比来确定YAP核转位的百分比。 α-catenin击倒的肝脏显示YAP阳性细胞核的百分比几乎翻了一番,证实了YAP信号确实通过α-catening的丢失而增强( 图3C ). 磷酸化YAP占总YAP的百分比从52%下降到32%,约下降40%。 YAP阳性核百分比的增加从37%增加到78%,略高于增加的两倍。 考虑到这两个结果是从不同类型的化验中获得的,考虑到化验的不同性质导致的预期差异水平,我们认为结果是惊人的一致。 此外,我们检测了结缔组织生长因子(CTGF)的表达水平,CTGF是YAP的一个重要下游靶点( 图3D ). 我们发现,α-catenin击倒的肝脏中CTGF显著上调,证实了YAP信号通路的参与。
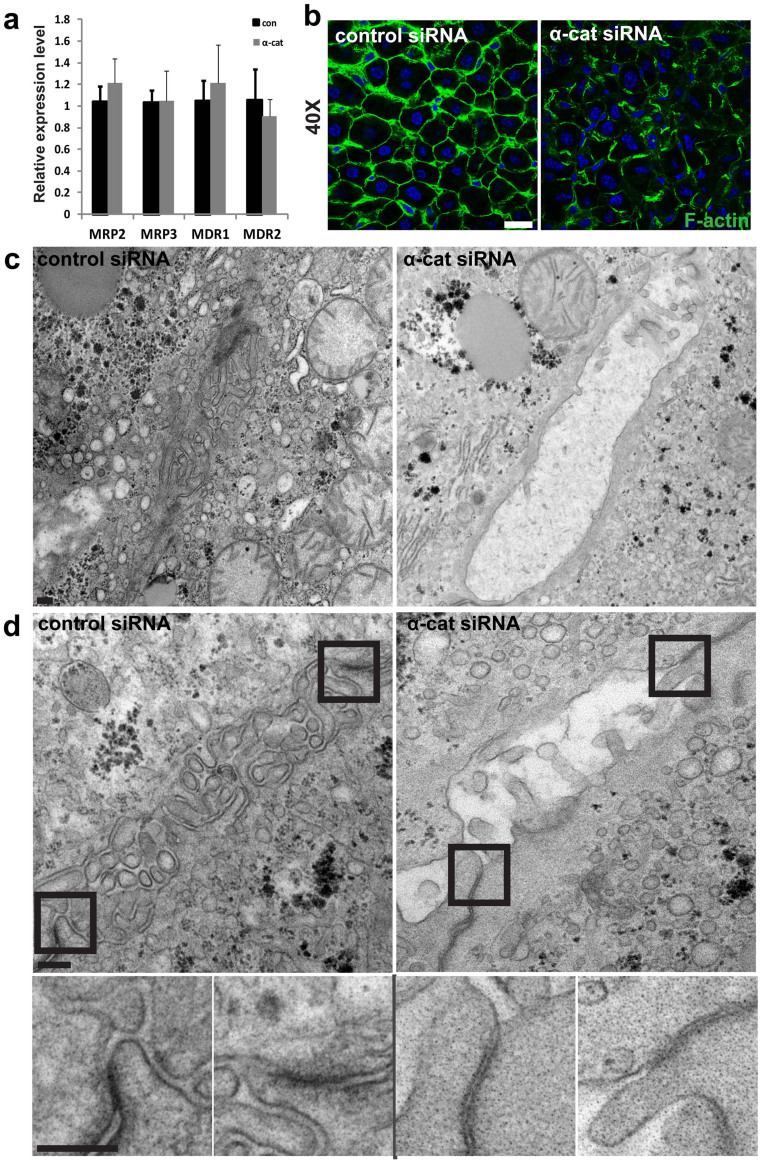
在胆汁淤积的临床病例中,观察到患者的胆汁流动障碍与关键胆汁转运蛋白表达水平的改变或细胞骨架的改变有关,而细胞骨架的变化又导致紧密连接处漏水,无法充分封闭胆道 23 虽然本例中胆管网络的破坏指向后一种理论,但我们仍然检测了胆汁淤积相关的四种不同转运体的表达,以排除这种可能性 24 : 多药耐药相关蛋白-2 ( Mrp2型 ), Mrp3型 , 多药耐药基因-1 ( Mdr1号机组 也称为P-糖蛋白多药转运蛋白(Pgp)或ABCB1),以及 Mdr2公司 正如预期的那样,这些蛋白的表达水平没有显著变化,这表明胆汁流动的中断并不涉及胆汁转运蛋白的变化( 图4A ). 大多数人和动物的胆汁淤积性肝病都与肝细胞骨架的变化有关,包括在心包域中积聚无组织的肌动蛋白纤维束。 这反过来又导致顶端微绒毛的损失和小管膜的收缩性减弱,这可能导致紧密连接的渗漏 24 已知α-连环蛋白与皮质肌动蛋白丝结合; 因此,我们用指骨肽染色法研究肌动蛋白丝的定位。 在对照肝脏中,肌动蛋白束以有组织的周周模式勾勒出细胞膜的外围,而在敲除的肝脏中,则肌动蛋白丝严重扭曲、畸形,不能连续排列在细胞皮层上( 图4B ).
图4。 肌动蛋白细胞骨架紊乱引起的胆管破裂导致微绒毛丧失和胆管管腔扩张。
(A) 在α-catenin敲除的肝脏中测量了四种重要胆汁转运蛋白的实时表达,即多药耐药相关蛋白-2(Mrp2)、Mrp3、多药耐药基因-1(Mdr1,也称为P-糖蛋白多药转运蛋白(Pgp)或ABCB1)和Mdr2,并与对照肝脏进行了比较。 未观察到任何蛋白质的显著变化。 (B) 肝脏切片用指骨肽进行免疫标记,以染色F-actin(绿色)和DAPI(蓝色),并通过共焦显微镜进行可视化。 代表性染色显示,在对照肝脏中,肌动蛋白微丝沿细胞外围排列,呈有组织的周膜模式,但在α-catenin敲除的肝脏中,微丝严重扭曲和畸形。 比例尺,20µm。 (C-D)在α-catenin击倒和对照肝脏上进行的典型电子显微镜图像。 (C) 如图所示,控制BC由充满微绒毛的管腔组成。 引人注目的是,α-catenin击倒小鼠的BC内腔扩张增加,微绒毛严重缺乏。 (D) 放大的插图(最下面一行)显示了密封BC的紧密连接。 在对照肝脏中,紧密连接的标志是两个膜融合成一个特征性的较暗的单层膜。 相比之下,α-catenin击倒的肝脏中BC侧的膜没有融合,紧密连接区域显示出两个分离的质膜。 比例尺,0.2µm。
我们假设,如果肌动蛋白丝的这种结构紊乱确实干扰了微绒毛和小管膜的收缩性,那么胆管的形态就会改变。 引人注目的是,电子显微镜显示α-catenin击倒的肝脏中的胆管腔高度扩张,表明肝脏标本的收缩能力减弱。 此外,与对照肝脏相比,微绒毛的比例严重降低( 图4C ). 在对照肝脏中,紧密连接处有一个明显的较暗区域,该区域由两个并置的膜双层组成。 相反,在α-catenin击倒的肝脏中,在胆管两侧的质膜之间观察到一个间隙,表明紧密连接的完整性受到损害( 图4D ). 因此,α-catenin的丢失导致肌动蛋白丝的紊乱,导致顶端微绒毛的丢失和胆管扩张,并伴有紧密的漏泄连接,进而导致胆汁流动中断。
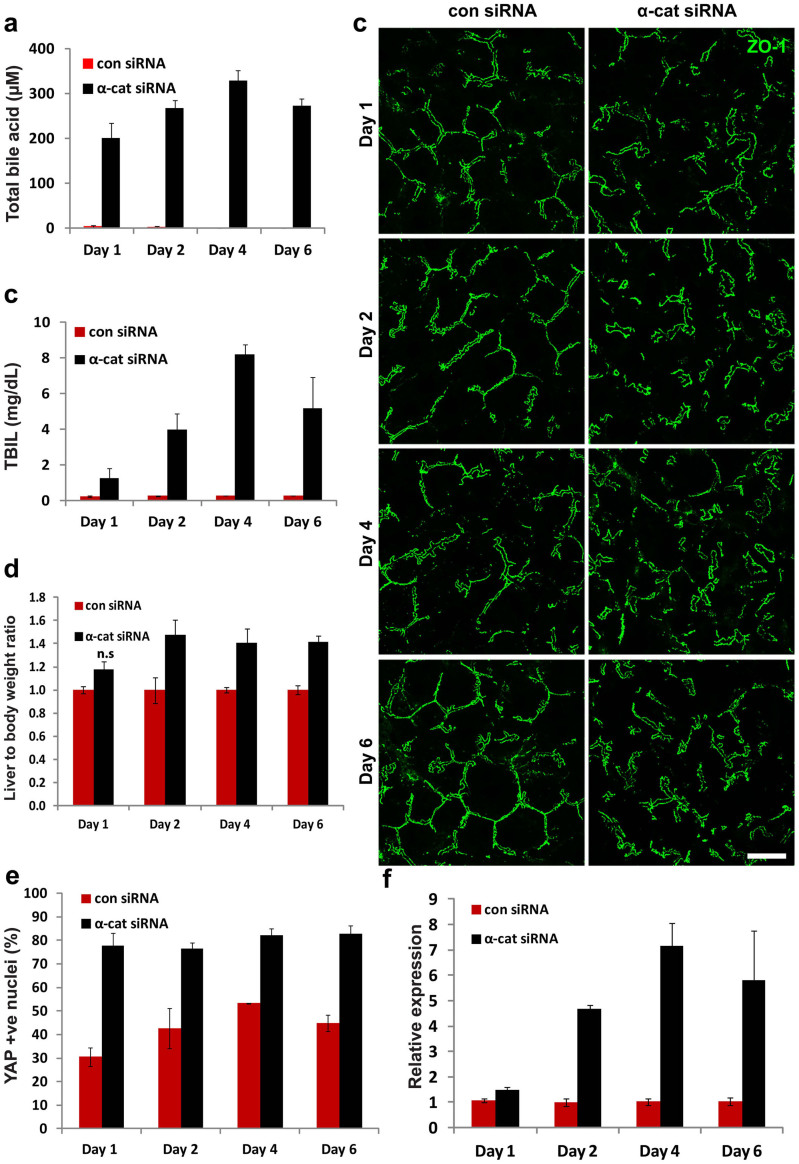
最后,研究α-catenin缺失引起的缺陷的时间轴是有意义的。 因此,在部分肝切除术后的不同时间点(术后1、2、4和6天)检查α-catenin敲除的肝脏和血样。 手术后第1天,这些小鼠血液中的TBA和TBIL水平显著升高,在第4天达到峰值( 图5A-B ). 相关地,从术后第1天开始,胆总管结构紊乱,观察到管腔扩大,一直持续到第6天( 图5C ). α-catenin击倒小鼠的肝体重比从第1天开始逐渐增加,尽管只有在手术后第2天才观察到显著上调( 图5D ). 此外,在α-catenin击倒的肝脏中,早在第1天,YAP的核免疫标记就显著升高,并持续到第6天( 图5E ). 此外,CTGF的表达在第1天和第2天之间显著上调,这与肝细胞增殖的峰值相对应( 图5F ). 总之,这些结果表明,α-catenin的存在在整个肝脏再生过程中至关重要,α-catanin的丢失会导致再生过程中的慢性和持续性缺陷。
图5。 α-catenin在肝脏再生的整个过程中都是必需的。
对注射α-catenin-siRNA-类固醇颗粒(LNP)的小鼠进行手术,并在手术后1、2、4、6天进行血液和肝脏分析。 (A) α-catenin siRNA-LNP注射小鼠的总胆汁酸从第1天开始显著增加,第4天达到峰值。 (B) 总胆红素水平(TBIL)从第1天开始相应增加,第4天再次达到峰值。 (C) 手术后第1天,注射α-catenin-siRNA-LNP的小鼠胆道结构的ZO-1染色(绿色)被破坏,并持续到第6天。 (D) 仅从第2天起,总肝体重比显著增加(除第6天外,每个时间点n=3;对照组n=2)。 除第6天外,所有配对组均具有显著的p值(不显著)。 比例尺,20µm。 (E) 用抗YAP抗体(棕色)对肝切片的细胞核进行免疫标记。 然后计算每个时间点α-catenin击倒和对照肝脏的YAP阳性(+ve)细胞核百分比。 在每个时间点测量到显著差异(p<0.05)。 (F) 结缔组织生长因子(CTGF)的基因表达。 从第2天起,CTGF显著上调。 在每个时间点测量到显著差异(p<0.05)。
讨论 最近发现,α-钙调素除了作为钙粘蛋白和肌动蛋白微丝之间的连接物外,还发挥其他功能 13 , 25 在这项研究中,我们揭示了α-catenin缺失对肝脏再生的过多影响。 再生的α-catenin敲除的肝脏明显大于对照再生的肝脏,其增大与肝细胞增殖增加有关。 以前在其他系统中也观察到α-catenin丢失导致细胞增殖增加。 小鼠表皮中α-catenin的消融导致类似鳞状细胞癌表型的缺陷,包括过度增殖和细胞极性改变 14 超增殖与细胞粘附和Wnt信号转导无关,但与Ras/MAPK通路有关。 此外,大脑中α-连环蛋白的条件性敲除也会导致过度增殖,这是由于α-连环素可能参与了Hedgehog通路 15 先前的一项研究也证实了β-catenin/Wnt信号在正常肝再生早期的参与。 由于β-连环蛋白降解减少,其核定位增加,这被认为是导致再生过程中观察到的增殖增加的原因 26 除这些途径外,α-catenin也被证明对Yap1有负调节作用 16 α-catenin的沉默导致YAP重新定位到细胞核,与TEAD转录因子相互作用以诱导增殖。 更重要的是,YAP的过度表达会显著增加小鼠的肝脏质量 27 ,这与我们在这里的发现类似。 值得注意的一点是,Ki67阳性细胞百分比增加约6倍与肝脏重量增加50%相关,这与他们的研究报告显示Ki67阳性的细胞百分比增加近4倍与肝脏质量增加30%相关,从而加强了我们的数据。 我们的结果还表明,α-catenin通过不同的信号通路作为增殖的负调控因子。 微环境决定了α-catenin与不同途径之间的相互作用程度,这是非常合理的。 在我们的研究中,我们发现增殖的增加与Hippo-YAP途径有关。 再生肝脏中α-catenin的丢失伴随着YAP的激活、其核转位的增加以及CTGF的表达增加,CTGF是对细胞生长重要的直接YAP下游靶点 28 值得注意的是,YAP核转位和CTGF表达的增加发生在再生的前两天,对应于肝细胞的增殖高峰期。 因此,根据之前的研究,我们的结果表明,a-catenin的丢失导致YAP激活增加,进而导致增殖增加。
肝脏再生后,肝体质量比持续恢复 三 , 5 我们观察到α-catenin击倒的肝脏的肝体质量比更大,这可能意味着α-catening在这一主调控中发挥作用。 肝肿大存在于许多疾病中,如肝硬化、脂肪肝和胆汁流动障碍。 因此,在本例中观察到的肝肿大可能预示着肝损伤或功能失常。 以前,β-catenin的激活或失调已被证明在结肠和卵巢肿瘤中上调mTOR通路 29 , 30 然而,在我们的研究中,细胞大小的增加并不是由于mTOR通路的上调,因为我们没有观察到磷酸化S6激酶水平的任何变化(数据未显示)。 我们也没有观察到α-catenin击倒后β-catenin-核易位的显著变化,也没有观察出多倍体的显著增加,这可能导致细胞肥大(数据未显示)。 因此,我们研究中细胞大小的增加更可能是由于肌动蛋白微丝的失调,这可能导致细胞大小的改变,也许是通过渗透压的改变 31 .
正常的胆汁形成和流动对体内平衡非常重要。 胆汁的产生对于脂肪的消化、脂类和脂溶性维生素的吸收以及胆红素(循环红细胞的副产物)的排泄至关重要。 我们发现,在我们的α-连环蛋白敲低小鼠中,包括TBIL、TBA、ALP和AMY在内的各种血浆成分水平升高,这表明胆汁流存在缺陷。 临床上,TBA和TBIL水平升高 善意的 胆汁淤积的指标,如黄疸,我们在α-catenin击倒小鼠的一个子群中观察到。 胆汁淤积症发生在各种病理学中,如原发性肝硬化、酒精性肝病、胆管肿瘤和肝炎,其特征是胆汁流动受阻,因此经常与肝肿大、炎症和血脂水平降低有关。 在这些α-catenin敲除的再生肝中观察到的表型是临床胆汁淤积的特征,并观察到肝小管紊乱、肝肿大、肝酶升高、胆汁盐和炎症。 在胆汁淤积状态下,血浆高密度脂蛋白胆固醇降低通常伴随着血浆胆固醇升高; 然而,在我们的α-catenin击倒小鼠中,只有HDL受到影响。 高密度脂蛋白的减少可能源于TBA的增加,TBA本身激活高密度脂素启动子区的抑制性FXR元件 32 .FXR增加胆固醇酯转移蛋白(CETP)活性,将胆固醇从HDL转移到非HDL颗粒 33 虽然总胆固醇没有显著增加,但非HDL颗粒增加,尽管不明显。
再生的α-catenin敲除的肝脏的窦状和胆管网络在周管区显示肌动蛋白束紊乱,窦状结构扭曲且紊乱。 此外,胆管管腔扩张,微绒毛消失,紧密连接完整性受损。 一种假设是,α-连环蛋白的丢失相当于缺乏控制肌动蛋白丝的分子开关 13 导致肌动蛋白细胞骨架断裂,进而对胆管产生扰动。 α-catenin是粘附连接中肌动蛋白聚合的中央调节器,作为机械传感器和换能器响应局部施加到该质膜亚结构域的力。 此外,主要位于紧密连接胞质域的闭塞带-1(ZO-1)也可以与α-连环蛋白相互作用,局部控制肌动蛋白聚合 34 因此,α-catenin的缺失导致ZO-1的失活也就不足为奇了。 肌动蛋白微丝动力学的任何破坏都会影响紧密连接的稳定性,紧密连接本身严重依赖于粘附连接的完整性 35 全长α-连环蛋白的缺乏在很大程度上影响了粘附强度,并阻止了细胞加倍中接触面积的扩大 36 在这些细胞骨架改变后,再生肝脏中的胆管可能会出现异常扩张的管腔,并伴有微绒毛丢失和漏水紧密连接。 值得注意的是,这些细胞骨架的变化与许多人类和动物的胆汁淤积性疾病有关 37 ,并已被证明会导致顶端微绒毛丧失和胆小管收缩能力减弱 38 此外,实验性诱导大鼠胆汁淤积导致封闭胆道的紧密连接中断 39 紧密连接处通透性的增加可能导致细胞旁通透性增加,胆汁成分回流到血浆中。 根据这一假设,我们观察到TBA和TBIL水平急剧增加。 此外,胆汁淤积性疾病,如原发性胆汁性肝硬化和胆管炎,也与炎症有关。 在我们的研究中,我们测量了敲低小鼠的总白细胞计数的升高,这表明存在炎症反应。
有趣的是,最近一项关于肝脏中β-catenin条件缺失的研究也导致胆管异常和肝内胆汁淤积 40 尽管与此处描述的表型相比,其严重程度较低。 如前所述,β-连环蛋白易位与α-连环素丢失相关的趋势不明显。 因此,很有意思的是,我们的系统中α-catenin丢失的影响与其在细胞粘附中的作用无关。 在肝脏中表达的E-cadherin的作用,基于看似矛盾的报道尚不清楚。 在单层培养的肝细胞中,E-cadherin被证明对维持扩展的胆管网络很重要 41 在β-catenin条件性肝特异性敲除小鼠中,未观察到紧密连接形态或胆管外观的变化 42 总之,这些研究中缺乏类似的严重表型,这进一步证明了α-连环蛋白在细胞粘附中众所周知的作用并不是观察到的表型的关键作用。
正常稳态肝脏中α-catenin表达的沉默引起了更温和的表型,BC形态和肝酶略有改变,但肝质量没有改变, 这表明,α-catenin在再生期的快速增殖和新结构形成期间,而不是在肝脏衰老期间,尤其重要。 事实上,α-连环蛋白的存在似乎对正常肝再生至关重要,并且是必要的,其丢失似乎会严重且持续地影响这一过程。 我们观察到,在不同时间点收获的所有α-连环蛋白敲低的肝脏中,细胞增殖和胆管缺陷增加。 α-连环蛋白敲低导致肝脏严重肿大的显著表型,部分归因于肝肿大,部分归因于增殖增加和胆管形成的严重缺陷,这些变化模拟了胆汁淤积的临床状况。 与已知的相互作用伙伴相比,α-catenin在受影响时表现出相对温和的表型,在与正常肝功能、肝再生和胆汁淤积相关的众多信号通路中似乎很重要。 通过了解α-连环蛋白在这些过程中的作用,我们可以阐明相关的病理学,并制定前瞻性的相应治疗方案。
方法 注射siRNA-醇脂质 动物协议由新加坡A*STAR动物护理和使用机构委员会批准,并符合国家卫生研究院指南和公法。 所有实验均按照这些批准的动物方案进行。 siRNA靶向转录物 α-钙调素 由Axolabs(德国Kulmbach)合成。 引入2’OMe修饰的核酸碱基和dTsdT 3’悬链(’s’表示硫代磷酸连接)来增加siRNA 体内 稳定性,并抑制免疫刺激。 siRNAs被配制成脂质纳米粒(LNP),优先靶向肝脏,平均粒径约为60–80 nm 43 , 44 , 45 , 46 为了确保每个基因在mRNA和蛋白质水平上的显著敲除,9至11周龄Balb/cByJ雌性小鼠通过尾静脉注射LNP,剂量为0.5 mg/kg体重,每5天注射一次,持续20天,第27天再注射一次。
肝部分切除术 如前所述,在第25天对动物进行了部分肝切除术 4 解剖的肺叶用10%中性缓冲福尔马林固定或在干冰上新鲜冷冻。 新鲜组织也被冷冻以进行蛋白质和RNA分析。 手术后7天,处死小鼠并采集肝脏进行分析。
细胞培养 AML12细胞购自ATCC(美国弗吉尼亚州马纳萨斯),并根据ATCC推荐的条件进行培养。 使用Lipofectamine 2000(Life Technologies)和ON-TARGETplus小鼠α-catenin siRNA(Thermo Fisher Scientific)进行转基因,
肝细胞的分离、接种和培养 采用两步原位胶原酶灌注法从雄性Wistar大鼠分离肝细胞。 根据新加坡国立大学IACUC委员会批准的IACUC协议处理动物。 当产量大于108个细胞/只大鼠时,通过台盼蓝排斥试验检测肝细胞的存活率大于90%。 将新鲜分离的大鼠肝细胞(20万)接种到24孔板上,并在0.5 ml William’s E培养基中培养,该培养基补充有2 mM L-谷氨酰胺、1 mg/ml BSA、0.3μg/ml胰岛素、100 nM地塞米松、50μg/ml亚油酸、100单位/ml青霉素和100 mg/ml链霉素,全部购自Aldrich Sigma。 细胞与5%CO孵育 2 温度37°C,湿度95%。 培养3小时后,去除未附着的细胞。 每天更换培养基。 细胞接种24小时后,向每个孔中添加0.25 mL 0.5 mg/mL中性胶原蛋白,并在37°C下培养3小时。 胶原蛋白凝胶化后加入新鲜培养基。
免疫组织化学 福尔马林固定的组织要么嵌入Tissue-Tek(Sakura Finetek Europe B.V,荷兰)中,要么嵌入石蜡中并相应切片。 新鲜冷冻切片在−20°C的乙醇中固定30分钟。石蜡切片被脱蛋白,再水化,并使用柠檬酸钠缓冲液进行抗原回收。 用2.5%牛血清白蛋白(美国密苏里州圣路易斯市Sigma-Aldrich)和0.3%Triton X-100(英国普尔市VWR)封闭切片2小时,然后在4°C下用一级抗体溶液培养过夜,然后用适当的二级抗体培养1.5小时 h.然后用DAPI对载玻片进行染色,并用Vectashide(Vectorlabs,加利福尼亚州伯灵盖姆,美国)固定载玻片。 使用的抗体包括兔抗N-钙粘蛋白(ab18203;Abcam,美国马萨诸塞州剑桥市)、兔抗抗原IV(ab6586;Abcam)、兔抗病毒YAP1(sc-15407;Santa Cruz,Dallas,TX,USA)、大鼠ZO-1(DSHB,美国爱荷华州爱荷华市)、兔子抗Ki67(ab15580;Abcan)和卵磷脂-AF488(A12379;Life Technologies,Carlsbad,CA,USA。 用AF546缀合的和AF488缀合的二级抗体(Life Technologies)检测一级抗体。 使用荧光显微镜(CTR6000;Leica,Wetzlar,德国)或共焦显微镜(LSM700;Zeiss,Oberkochen,德国)进行成像。
免疫荧光和图像采集 肝细胞或AML12细胞在4%多聚甲醛(PFA)中固定30分钟,并在TBST中渗透30分钟(TBS中0.2%Triton-X)。 在TBST中用1%的BSA封闭渗透性细胞4小时,并在室温黑暗中用生殖器肽-Alexa 488(生命技术)培养1小时。 用DAPI(Sigma-Aldrich)染色后,将细胞安装在安装介质中(DAKO,Carpindia,CA,USA)。 在尼康A1R共焦显微镜上,用100×NA1.4油透镜获得了共焦显微图像的三维叠加。
血液化学分析 麻醉下使用21-G针通过心脏穿刺采集血液。 在A*STAR分子细胞生物学研究所组织病理学部门使用自动化方法对血液学小组(HEMAVET 950FS,Thermo Fisher Scientific,Waltham,MA,USA)和血清标记物和酶的血液化学小组(VETSCAN VS2,Abaxis,Union City,CA,USA。 使用Diazyme(美国加利福尼亚州波韦市)的商用试剂盒分析血清中的总胆汁酸水平,每个样品测试三次。 分别使用Biovision(加州山景城,美国)、Wako Chemicals(弗吉尼亚州里士满)和Stanbio(德克萨斯州博恩)的商用试剂盒测定血浆中的磷脂、甘油三酯和总胆固醇水平,
Ki67和YAP定量 每个样本都用抗Ki67抗体和DAPI进行双重标记,并在40倍放大镜下拍摄总共20张图像。 同样,每个样品都用抗YAP标记,并在20倍放大率下拍摄图像。 使用ImageJ软件(NIH,Bethesda,MD,USA)量化每个区域中Ki67阳性或YAP阳性细胞核的数量。 然后将Ki67阳性或YAP阳性核的总数除以总核数,计算Ki67阳性核或YAP正核的百分比。
统计测试和量化 所有p值均采用双尾分布的非配对t检验计算,假设方差不相等。 对于细胞大小量化和肝脏模拟模型,用膜标记物标记细胞,以可视化细胞轮廓。 使用旋转核增强膜信号,并将图像转换为二值图像。 应用距离变换公式,将局部最大值设置为单元的中心。 基于这个细胞中心,进化广义Voronoi图 47 , 48 方法对细胞进行分割。 根据分割结果,为每个条件创建概率分布函数。 为了确定肝脏大小的增加是否是由于细胞大小的增加,进行了数值模拟。 通过考虑每组100万个细胞并生成每个细胞的概率密度函数,为对照细胞和siRNA注射细胞创建了模拟模型。
RNA提取和第一链cDNA合成 根据制造商的方案,使用Qiagen RNeasy迷你试剂盒(荷兰Venlo的Qiangen)从冷冻小鼠肝脏和单层细胞中提取RNA。 使用Superscript III逆转录酶试剂盒(Life Technologies)进行第一链cDNA合成。
实时PCR 使用实时PCR结合SYBR绿色检测或Taqman基因表达分析来确认敲除并评估来自细胞培养物和组织样本的各种基因的表达水平,使用以下引物进行:E-cadherin F:CAG CCT TCT TTT CGG AAG ACT, R:GGT AGA CAG CTC CCT ATG ACT G.α-catenin F:TCT CTA CTG CCA GCT CAA C,R:AAG CCA TCC CCT GTG ACT TCT。 MRP2 F:GTG TGG ATT CCC TTG GGC TTT,R:CAC AAC GAA CAC CTG CTT GG MRP3 F:CTG GGT CCC CTG CAT CTA C,R:GCC GTC TTG AGC CTG GAT AAC MDR1:Quantitect引物QT01051988,MDR2:Quantitect-primers QT00164010(荷兰文洛市齐根)。 CTGF:Mm01192932_g1,ACTIN:Mm00487499(生命科技)。 每次运行中都包含适当的非模板控制。
电子显微镜 将肝组织样品固定在pH 7.4的0.1 M磷酸盐缓冲液中,该缓冲液含有4%PFA、2.5%GA和0.2%苦味酸,然后再固定在pH 7.6、包含1%四氧化锇和1.5%铁氰化钾的0.1 M碳酸钠中。 然后将样品脱水,用2%乙酸铀酰和75%乙醇进行染色,用丙酮渗透并嵌入树脂中。 然后修剪这些块以去除多余的树脂。 使用超微切片机制作0.5µm的半薄切片,用亚甲蓝和硼砂染色。 在确定感兴趣的区域后,将每个样品修剪至小于3mm的区域。切割90nm的超薄切片,并用150目铜栅收集。 然后用重金属染色、醋酸铀酰(10分钟)和柠檬酸铅(8分钟)对网格进行染色,以形成对比。 在Jeol 1220 TEM上进行了观察和图像采集(日本东京)。
蛋白质印迹 将肝组织在冰上均匀化5秒,然后在含有2 mM/ml Na的RIPA缓冲液中溶解 三 VO(旁白) 4 和1x蛋白酶抑制剂鸡尾酒(Sigma-Aldrich)在4°C下保持20分钟。 使用SDS-PAGE分离整个组织裂解物并转移到PVDF膜上。 所使用的主要抗体是Alpha-catenin(610194;BD Biosciences,San Jose,CA,USA)、GAPDH(ab9485;Abcam)、Yap(4912;Cell Signaling,Danvers,MA,USA;和磷光体Yap-Ser127(4911;Cell信号)。
作者贡献 K.J.H.设计了实验,进行了实验并撰写了论文。 N.T.协助动物实验并进行了western blots。 J.W.E.O.协助了实验。 Q.L.和V.V.进行了涉及原代大鼠肝细胞的实验。 L.L.Y.提供了该研究的初步数据。 H.Y.、R.B.、J.E.D.、D.G.A.和V.K.制定并提供了siRNA-LNP。 W.Y.对细胞大小和肝脏模拟模型进行了统计分析。 Y.G.C.和B.H.B.进行了电子显微镜检查。 R.S.对血清样本进行了脂质分析。 J.P.T.为研究提供了建议和指导,并编辑了论文。
致谢 我们感谢本研究所组织病理学系的血液分析和组织学工作。这项工作得到了科学技术研究署(A*STAR)的支持。
工具书类
A.L.肝脏健康基金会。 提高公众对肝脏健康的认识< http://www.liverfoundation.org/downloads/alf_download_29.pdf > (2009). 已访问7 第个 2014年7月。 [ 谷歌学者 ]
肝脏E.A。 f.t.S.o.事实和数字。 肝脏:生命的关键< http://old.easl.eu/eu_facts.asp > (2009). 已访问7 第个 2014年7月。 [ 谷歌学者 ]
Huang J.和Rudnick D.A。 阐明肝脏再生的代谢调节。 美国病理学杂志。 184309–32110.1016/j.ajpath.2013.04.034(2014)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Mitchell C.和Willenbring H。 一种可重复且耐受性良好的小鼠2/3部分肝切除方法。 《国家协议》。 3、1167–1170、10.1038/nprot.2008.80(2008)。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
米哈洛普洛斯·G·K。 肝脏再生。 J.细胞。 生理学。 213286–300,10.1002/jcp.21172(2007)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Yonemura S.、Wada Y.、Watanabe T.、Nagafuchi A.和Shibata M。 α-儿茶酚胺作为一种张力传感器,可诱导粘附连接的发育。 自然细胞。 生物。 12、533–542、10.1038/ncb2055(2010)。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
汉森S.D。 等。 alphaE-catenin肌动蛋白结合域改变肌动蛋白丝的构象并调节成核和分解因子的结合。 分子生物学。 单元格 24、3710–3720、10.1091/mbc。 E13-07-0388(2013)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
博尔吉N。 等。 E-钙粘蛋白处于构成肌动蛋白生成的张力下,该张力在细胞间接触时在外部拉伸时增加。 程序。 国家。 阿卡德。 科学。 美国 10912568–12573,10.1073/pnas.1204390109(2012)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Hong S.、Troyanovsky R.B.和Troyanovsky S.M。 与F-actin的结合引导钙粘蛋白簇的组装、稳定性和运动。 《细胞生物学杂志》。 201、131–143、10.1083/jcb.201211054(2013)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Abe K.和Takeichi M。 EPLIN介导钙粘蛋白-连环蛋白复合物与F-actin的连接,并稳定环向肌动蛋白带。 程序。 国家。 阿卡德。 科学。 美国 105、13–19、10.1073/pnas.0710504105(2008)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
托马斯·W·A。 等。 α-钙粘蛋白和vinculin协同促进高E-cadherin粘附强度。 生物学杂志。 化学。 288、4957–4969、10.1074/jbc。 M112.403774(2013年)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Pokutta S.、Drees F.、Takai Y.、Nelson W.J.和Weis W.I。 α-胡萝卜素的l-afadin和肌动蛋白结合位点的生化和结构定义。 生物学杂志。 化学。 277、18868–18874、10.1074/jbc。 M201463200(2002)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Drees F.、Pokutta S.、Yamada S.、Nelson W.J.和Weis W.I。 α-catenin是一种分子开关,结合E-钙粘蛋白-β-catenin并调节肌动蛋白纤维组装。 单元格 123、903–915、10.1016/j.cell.2005.09.021(2005)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Vasioukhin V.、Bauer C.、Degenstein L.、Wise B.和Fuchs E。 皮肤中α-胡萝卜素条件消融后上皮极性增生和缺陷。 单元格 104, 605–617 (2001). [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Lien W.H.、Klezovitch O.、Fernandez T.E.、Delrow J.和Vasioukhin V。 alphaE-catenin通过调节刺猬信号通路控制大脑皮层大小。 科学类 3111609–1612,10.1126/science.1121449(2006)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Schlegelmilch K.公司。 等。 Yap1作用于α-钙调素下游以控制表皮增殖。 单元格 144、782–795、10.1016/j.cell.2011.02.031(2011)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Shtutman M。 等。 α-胡萝卜素在微管调节中的信号功能。 细胞周期 7, 2377–2383 (2008). [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
马拉托Y。 等。 小鼠肝内稳态和再生中成熟肝细胞的命运追踪。 临床杂志。 投资。 121、4850–4860、10.1172/JCI59261(2011)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
阿金克A。 等。 脂质体siRNA制剂的开发,用于全身给药到肝脏。 摩尔-热。 17、872–879、10.1038/mt.2009.36(2009)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
博戈拉德·R·L。 等。 以整合素为靶点的纳米颗粒形成的siRNA抑制小鼠肝癌的进展。 国家公社 5,3869,10.1038/ncomms4869(2014)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
斯派克T。 等。 肝细胞中β1整合素的敲除和敲除通过抑制生长因子信号传导损害肝再生。 国家公社。 53862,10.1038/ncomms4862(2014)。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Wolfrum C.公司。 等。 亲脂性siRNA体内传递的机制和优化。 自然生物技术。 251149–115710.1038/nbt1339(2007)。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Zollner G.和Trauner M。 胆汁淤积的分子机制。 维恩。 Wochenschr医学博士。 156、380–385、10.1007/s10354-006-0312-7(2006)。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Trauner M.、Meier P.J.和Boyer J.L。 胆汁淤积症的分子发病机制。 北英格兰。 医学杂志。 339、1217–1227、10.1056/NEJM199810223391707(1998)。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Maiden S.L.和Hardin J。 alpha-catenin的秘密生命:形态发生中的兼职。 《细胞生物学杂志》。 195、543–552、10.1083/jcb.201103106(2011)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Monga S.P.、Pediaditakis P.、Mule K.、Stolz D.B.和Michalopoulos G.K。 大鼠肝脏再生中调节生长过程中WNT/β-连环蛋白途径的变化。 肝病学 33、1098–1109、10.1053/jhep.2001.23786(2001)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
董杰(Dong J.)。 等。 果蝇和哺乳动物通用尺寸控制机制的阐明。 单元格 130、1120–1133、10.1016/j.cell.2007.07.019(2007)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
赵B。 等。 TEAD介导YAP依赖性基因诱导和生长控制。 基因开发 1962-1971年,10.1101/gad.1664408(2008)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
坦瓦尔P.S。 等。 雷帕霉素的哺乳动物靶点是Wnt/beta-catenin和PTEN失调的小鼠卵巢子宫内膜样腺癌的治疗靶点。 PLOS一号 6,e20715,10.1371/journal.pone.0020715(2011)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Fujishita T.、Aoki K.、Lane H.A.、Aoki-M.和Taketo M。 抑制mTORC1通路可抑制ApcDelta716小鼠肠息肉的形成并降低死亡率。 程序。 国家。 阿卡德。 科学。 美国 105、13544–13549、10.1073/pnas.0800041105(2008)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
蒂内夫兹·J·Y。 等。 皮层张力在气泡生长中的作用。 美国国家科学院程序 106、18581–18586、10.1073/pnas.0903353106(2009)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
克劳代尔·T。 等。 胆汁酸活化核受体FXR通过负FXR反应元件抑制载脂蛋白A-I转录。 临床杂志。 投资。 109、961–971、10.1172/JCI14505(2002)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
戈蒂埃T。 等。 Farnesoid X受体激活增加人类和转基因小鼠中胆固醇酯转移蛋白的表达。 《脂质研究杂志》。 54、2195–2205、10.1194/jlr。 M038141(2013)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Yonemura S.公司。 粘附连接处的钙粘附素-肌动蛋白相互作用。 货币。 操作。 单元格。 生物。 23、515–522、10.1016/j.ceb.2011.07.001(2011)。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Huang R.Y.、Guilford P.和Thiery J.P。 上皮-间充质转化过程中细胞粘附和极性的早期事件。 细胞科学杂志。 125,4417–4422,10.1242/jcs.099697(2012年)。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Engl W.、Arasi B.、Yap L.、Thiery J.P.和Viasnoff V。 肌动蛋白动力学调节粘附连接处E-cadherin的机械敏感性固定。 Nat细胞生物学 16、587–594、10.1038/ncb2973(2014)。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Phillips M.J.、Poucell S.和Oda M。 胆汁淤积的机制。 实验室投资。 54, 593–608 (1986). [ 公共医学 ] [ 谷歌学者 ]
安德森·J·M。 连接处漏与胆汁淤积:密切相关。 胃肠病学 110, 1662–1665 (1996). [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Rahner C.、Stieger B.和Landmann L。 大鼠肝内外胆汁淤积症后紧密连接损伤的结构-功能相关性。 胃肠病学 110, 1564–1578 (1996). [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Yeh T.H.是的。 等。 肝特异性β-catenin基因敲除小鼠出现胆管异常、胆汁分泌缺陷和肝内胆汁淤积。 肝病学 52、1410–1419、10.1002/hep.23801(2010)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Terry T.L.和Gallin W.J。 胎牛血清和钙粘蛋白功能破坏对肝细胞间胆小管形成的影响。 实验细胞研究。 214642–65310006/excr.1994.1302(1994)。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Battle文学硕士。 等。 肝细胞核因子4alpha在发育中的肝脏上皮转化过程中调控细胞粘附蛋白的表达。 程序。 国家。 阿卡德。 科学。 美国 103、8419–8424、10.1073/pnas.0600246103(2006)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
爱K.T。 等。 用于低剂量体内基因沉默的类脂质材料。 程序。 国家。 阿卡德。 科学。 美国 107、1864–1869、10.1073/pnas.0910603106(2010)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
阿金克A。 等。 以内源性和外源性配体为基础的机制靶向递送RNAi疗法。 摩尔-热。 18、1357–1364、10.1038/mt.2010.85(2010)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
弗兰克·卡梅内茨基M。 等。 针对PCSK9的治疗性RNAi可大幅降低啮齿动物的血浆胆固醇和非人灵长类动物的低密度脂蛋白胆固醇。 程序。 国家。 阿卡德。 科学。 美国 105、11915–11920、10.1073/pnas.0805434105(2008)。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
齐格勒A。 等。 Rab5是体内内溶酶体系统生物发生所必需的。 自然 485465-47010.1038/nature11133(2012)。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Yu W.、Lee H.K.、Hariharan S.、Bu W.和Ahmed S。 用于精确细胞图像分割的进化广义Voronoi图。 细胞计量学A 77、379–386、10.1002/cyto.a.20876(2010)。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Yu W.、Lee H.K.、Hariharan S.、Bu W.和Ahmed S。 基于拓扑依赖图像分割的神经突起生长定量测量。 细胞计量学A 75、289–297、10.1002/cyto.a.20664(2009)。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
关联数据 本节收集本文中包含的任何数据引用、数据可用性声明或补充材料。