介绍
调节性T细胞(Tregs)对自我耐受至关重要(1). 在移植的实验模型中,Tregs在建立移植耐受性方面是必要的,并且在某些实验条件下是足够的(2——5). 已有三项I期试验对Treg细胞治疗移植物抗宿主病(GvHD)的安全性进行了评估,所有试验均显示出最小的毒性,并提示可能的疗效(6——8). Treg治疗儿童新发1型糖尿病的一期试验也显示疾病进展较慢,无严重不良事件(9). 这些发现启发了许多人考虑将Treg疗法应用于实体器官移植,以便将免疫抑制降至最低或取消。
同种异体抗原反应Tregs(arTregs)在诱导移植实验模型耐受方面比多克隆扩增Tregs更有效(10——12). 我们估计,PolyTregs对人类有效所需的Tregs数量为数十亿,而arTregs则少了10倍(13). 报道了几种选择性扩增人类arTreg的方法(12,14——16),并且没有一个在符合良好生产规范(GMP)的条件下证明扩张。在本研究中,我们报告了一种用于制造临床级人类arTreg的稳健工艺。
方法
细胞
正常献血者同意捐献全血。或者,从加州大学旧金山分校血液中心获得来自正常供体的未经鉴定的脱水产品。如前所述分离外周血单个核细胞(PBMC)(17)并使用新鲜或冷冻保存后的CryoStor CS10冷冻介质(BioLife Solutions,Bothell,WA)。脾脏来自经研究同意的尸体器官捐赠者。所有程序均由加州大学旧金山分校和伦敦国王学院当局批准。
CD40L刺激B细胞(CD40L-sBc)的产生
使用未接触的B细胞富集试剂盒(Invitrogen,Carlsbad,CA)从PBMC或脾脏富集B细胞,并按照所述与辐照的3T3-CD40L细胞(40 Gy)培养(21). 辐照CD40L-sBc(30 Gy)并用于刺激Tregs或在CryoStor CS10中冷冻保存直至使用。对于符合GMP的扩增,使用CliniMACS上的CD19阳性选择纯化B细胞(Miltenyi Biotech,Auburn,CA),在补充有10%人类AB血清(Valley Biomedical,Winchester,PA)、GMP级IL-4(Miltenye)的含转铁蛋白的X-VIVO15培养基(Lonza,Walkersville,MD)中用辐照过的K562-CD40L细胞(100 Gy)刺激B细胞和环孢霉素A(宾夕法尼亚州北威尔士Teva Pharmaceuticals)。
混合淋巴细胞反应(MLR)
标记有1.25µM羧基荧光素琥珀酰亚胺酯(CFSE;Invitrogen)的应答者PBMC用辐照的异基因CD40L-sBc(每个PBMC 2 sBc)或辐照的异遗传PBMC(每个应答者5个刺激物)刺激。84-96小时后收集培养物,并用CD3(克隆SK7)、CD4(克隆SK3)、CD8(克隆SK1)、固定活性染料FOXP3(克隆206D)和HELIOS(克隆22F6)抗体染色。在Fortessa(BD Biosciences)上进行流式细胞术,并使用FACSdiva(BD生物科学)或FlowJo软件(Treestar、Ashland、or)进行分析。
Treg扩展
使用BD FACSAria II(BD Biosciences)基于CD4表型分离Tregs+CD127型lo/−CD25细胞+和PolyTreg展开如前所述(17). 临床依从性筛选利用了诺埃尔·华纳(BD Biosciences)生成和提供的GMP单克隆抗体。对于arTreg扩增,培养物保存在补充有谷氨酸MAX(Invitrogen)、青霉素/链霉素和2%人AB血清的OpTmizer培养基(Invit罗gen)中,或保存在含有10%人AB血的X-VIVO15培养基中。将荧光活化细胞分选(FACS)纯化的Tregs与CD40L-sBc以4:1 sBc/Treg的比例混合。用300 IU/ml人IL-2维持培养至第9天或第11天,然后用新辐照的sBc或GMP级抗CD3和抗CD28涂层(抗CD3/CD28)珠以4:1 sBc/T细胞或1:1珠/T细胞的比例重新刺激细胞。培养物在3天后喂食,并在重新刺激后的第5天收获。使用台盼蓝排除法评估细胞的活性。
流式细胞术
采用以下三种流式细胞仪检测扩增Tregs的表型:(1)CD8(克隆SK1)、CD4(克隆SK3)、CD3(克隆SK7)和CD19(克隆SJ25C1);(2) CD4、CD62L(克隆SK11)、CD27(克隆L128)和FOXP3(克隆206D;BioLegend,加利福尼亚州圣地亚哥);以及(3)CD4、CD25(克隆2A3)、HELIOS(克隆22F6;BioLegend)和FOXP3。对于一些实验,如前所述,评估了扩增arTregs产生干扰素γ(IFNγ)(22). CD40L-sBc用HLA-DR(克隆G46-6)、CD80(克隆L307.4)、CD86(克隆2331)和CD19(克隆HIB19)抗体染色。染色细胞在FACSCalibur或AccuriC6(BD Biosciences,San Diego,CA)上进行分析。除非另有说明,所有抗体均来自BD Biosciences。
Treg特异性分析
扩张的Tregs用1.25µM CFSE标记,并用异体或自体CD40L-sBc、抗CD3/CD28珠刺激,或在含有30 IU/mL IL-2的培养基中保持未刺激状态。72小时后,收集细胞,用抗CD4和碘化丙啶染色,并在AccuriC6上进行分析。
TCRβ储备分析
基因组DNA提取自0.25×106至1×106新隔离的Tregs和体外扩展了PolyTregs和arTregs。DNA被提交给Adaptive Biotechnologies(西雅图,WA)进行调查级TCRβ测序。使用自适应生物技术开发的算法对测序数据进行分析,包括确定克隆性指数和曲目相似性。
体外抑制试验
滴定数的膨胀Tregs与3×10混合4三份来自Treg供体的PBMC,置于V型底部96个平板中。用来自sBc或第三方供体的辐照PBMC刺激细胞7天,并加入三[H] 胸腺嘧啶核苷在培养的最后16-20h用于测量增殖。不含Tregs的培养物用作对照。
Treg-特异性去甲基化区域(TSDR)甲基化检测
0.5×10的基因组DNA6根据既定方案,使用Epiontis GmbH(德国柏林)的授权试剂对扩增的Tregs进行分析(23). 去甲基化TSDR的百分比计算为:[非甲基化DNA平均拷贝数/(非甲基化平均拷贝数+甲基化DNA的平均拷贝数)]×100。对于雌性Tregs,将上述计算的百分比乘以2,以校正X染色体失活。
皮肤移植的人性化小鼠模型
在知情同意的情况下,从手术患者处获得未经确认的人类皮肤。将皮肤移植到8至12周龄的BALB/c.Rag2上−/−γc−/−小鼠移植6周后,给受体小鼠注射10×106HLA-匹配的CD25缺失PBMC。一些小鼠联合注射2×106PolyTregs或arTregs。PBMC注射6周后对移植物进行组织学分析。在这些实验的总持续时间内,每4-5天腹腔注射100µg抗小鼠Gr1(Bio X Cell,西黎巴嫩,NH),以耗尽小鼠粒细胞。所有程序都是按照机构准则进行的。用5%多聚甲醛固定人皮肤移植物的冰冻切片,并用抗人抗原ki67(cat.#ab15580;Abcam,Cambridge,MA)、CD45(clone HI30;eBioscience)、CD3(cat.#A0452;Dako,Carpenteria,CA)、FOXP3(clone 259D/C7;eBios)、involucrin(clone SY5)和CD31(cat.#1ab28364;Abcam)的抗体染色,然后用适当的荧光结合二级抗体孵育,并用带有4-6-二氨基-2-苯基吲哚(DAPI;Invitrogen)的Prolong Gold防褪色试剂固定。免疫荧光结果的定量评估是通过计数一个对治疗条件一无所知的个体所形成的四到六个非重叠场来完成的。
统计
使用GraphPad Prism 5.00版(GraphPad Software,San Diego CA)进行统计分析。
结果
CD40L-sBc是arTregs的有效刺激物
使用单向MLR,我们发现CD40L-sBc在刺激CD4增殖方面明显强于PBMC+T细胞,CD8+T细胞和CD4+FOXP3公司+HELIOS公司+特雷格斯(图1A和B). 为了确定增殖是否是对CD40L-sBc上表达的同种异体抗原的反应,我们比较了自体CD40L-s Bc和同种异体CD40L-s-Bc对应答者不同程度HLA错配的刺激能力。我们发现CD4应答频率较高的趋势+传统T细胞(Tconv)和Tregs具有更多HLA-DR失配和更高的CD8应答频率+HLA-AB失配较多的T细胞(图1C). 这些结果表明CD40L sBc是有效的异基因刺激因子,并促使我们探索CD40L sBc在arTregs选择性扩增中的作用。
图1。CD40L-sBc能有效刺激T细胞增殖。
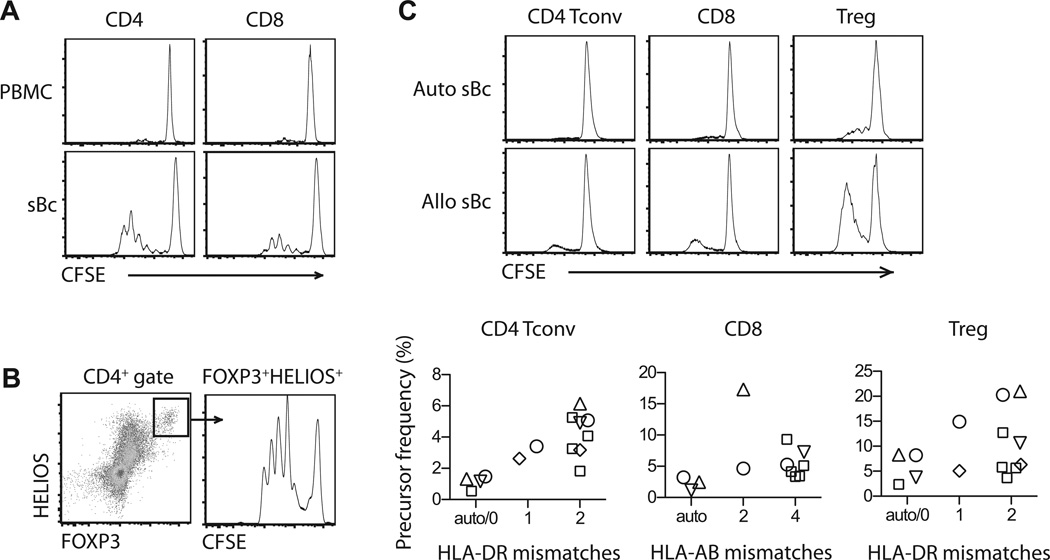
比较来自同一供体的(A和B)PBMC和CD40L-sBc在单向MLR中刺激同种反应性T细胞增殖的能力。MLR前用CFSE标记应答者PBMC,第4天采集培养物进行流式细胞术分析。CD4的典型CFSE稀释曲线+和CD8+T细胞(A)和CD4+FOXP3公司+HELIOS公司+图中显示了Tregs(B)。这些数据代表了至少10个独立实验。(C) 比较具有不同程度HLA失配的自体CD40L-sBc和异基因CD40L-s Bc与应答细胞刺激CD4增殖的能力+Tconv,CD8型+T细胞和Treg细胞。每个符号代表相同的响应者。结果15种不同刺激器和应答器组合的面积总结。CD40L-sBc、CD40L-刺激的B细胞;CFSE,羧基荧光素琥珀酰亚胺酯;MLR,混合淋巴细胞反应;外周血单个核细胞;Tconv,常规CD4+T细胞;Treg,调节性T细胞。
GMP兼容CD40L表达细胞的产生
与GMP相容的人CD40L表达细胞系KT64.CD40L。HLADR0401(缩写为K-CD40L)是为了制造临床级arTregs而产生的。我们使用慢病毒转导在骨髓白血病细胞系K562中表达CD40L,K562已被用作癌症疫苗和人工抗原呈递细胞,用于临床应用(24——27). 额外的CD64和HLADR0401基因用于其他应用,不会干扰sBc的CD40L刺激。在第0天和第7天用K-CD40L细胞进行两轮刺激,并持续供应IL-4,导致纯化的B细胞扩增10至50倍(图2A). 与新分离的B细胞相比,CD40L-sBc表达的HLA-DR、CD80和CD86水平显著升高(图2B和C)与它们刺激T细胞的增强效力一致。
图2。使用K-CD40L细胞生成CD40L-sBc。
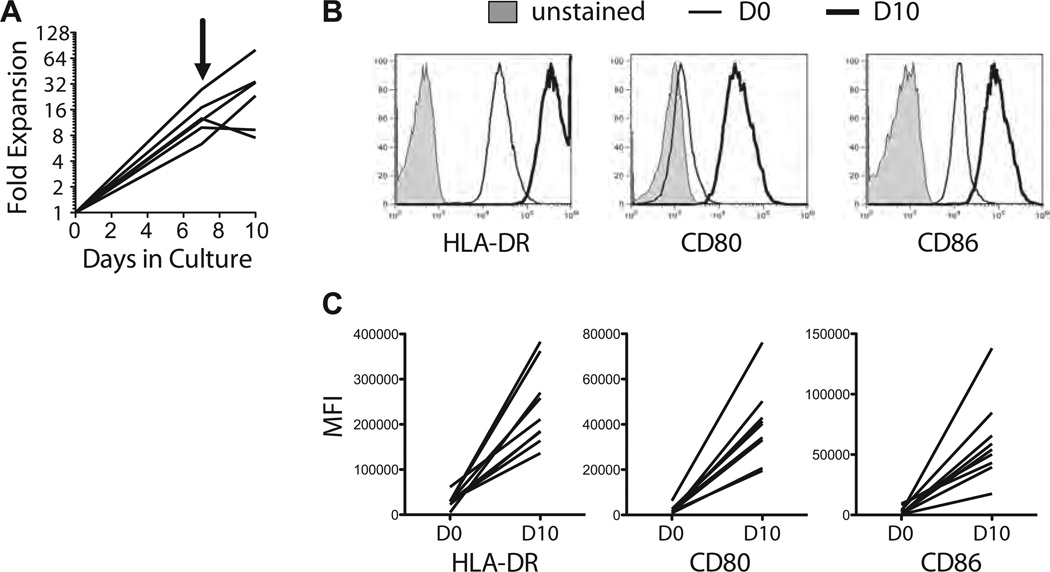
(A) 在10天的培养中显示纯化的B细胞的扩增。箭头指示重新模拟的时间。(B和C)使用流式细胞术比较新鲜分离的B细胞和第10天CD40L-sBc中HLA-DR、CD80和CD86的表达。样本叠加直方图如(B)所示,总结独立实验结果的图表如(C)所示。数据是六个独立实验的总结。CD40L-sBc、CD40L-刺激的B细胞;K-CD40L、CD40L表达细胞系;KT64.cd40升。HLADR0401;MFI,平均荧光强度。
CD40L-sBc强烈诱导arTreg扩增
我们以前报道过FACS纯化CD4的多克隆扩增+CD127型lo/−CD25细胞+Tregs使用两轮刺激(第0天和第9天)和抗CD3/CD28珠(17). 为了扩大arTregs,我们比较了CD40L-sBc和原发性CD40L-s Bc刺激以及抗CD3/CD28再刺激的两轮刺激。CD40L-sBc的两次刺激导致Tregs扩张50-300倍(图3A)与CD40L-sBc在再刺激过程中被珠子取代时的结果类似(图3B). Tregs的两种扩张方式都对用于扩张的sBc反应强烈(图3C). 为了便于标准化和实施,我们决定使用珠子重新模拟进行arTreg扩展。
图3。使用CD40L-sBc选择性扩增arTregs。
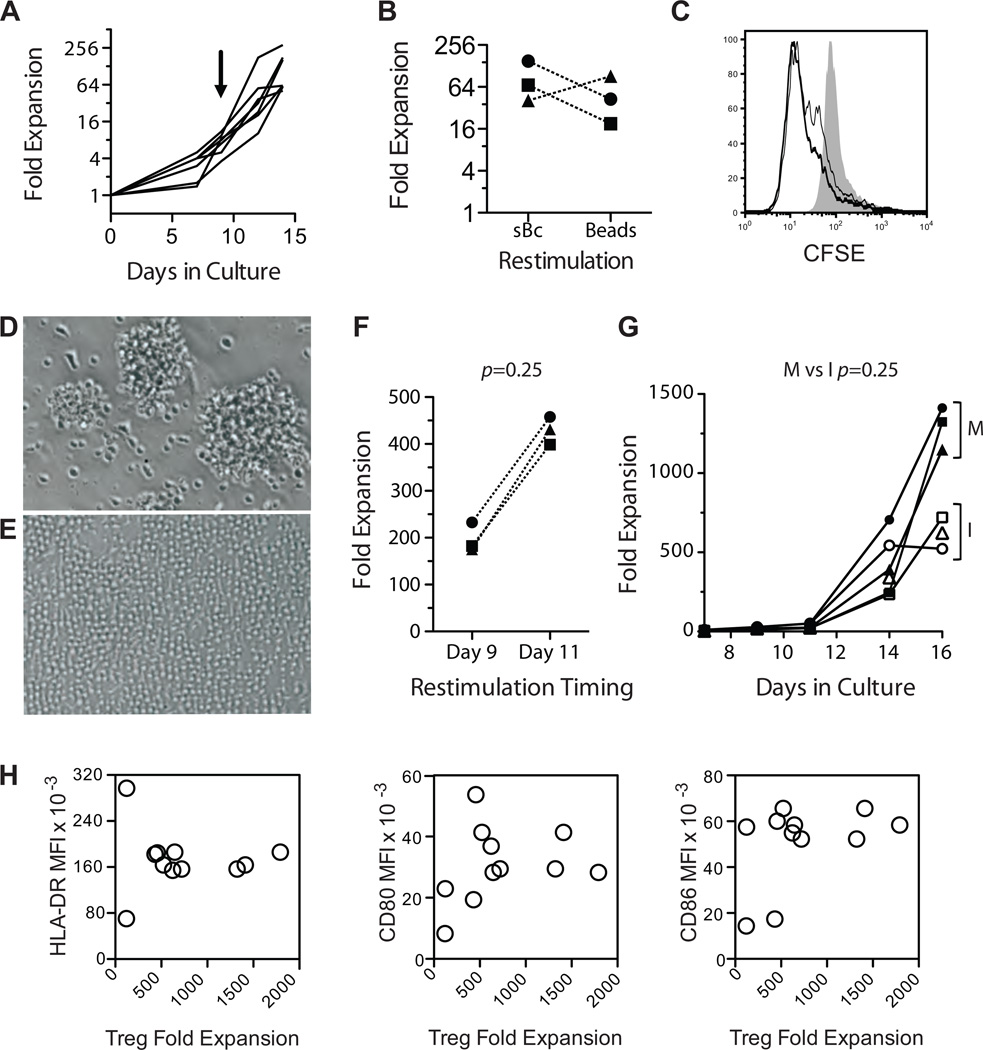
(A) 在第0天和第9天,使用异基因sBc刺激FACS纯化的Tregs。在六个独立实验中,显示了Treg在14天培养中的折叠扩展。箭头指示重新模拟的时间。(B) 用CD40L-sBc刺激Tregs 9天,然后分离培养物,其中一半用同一供体的CD40L-s Bc重新刺激,另一半用抗CD3和抗CD28涂层珠重新刺激。显示了三种独立配对培养物在第14天的折叠扩展(第页=0.75,Wilcoxon配对签名秩检验)。(C) 扩增Tregs的同种异体反应性是通过在用相同的用于扩增的CD40L-sBc(粗线)、抗CD3和抗CD28涂层珠(细线)或同基因CD40L-s Bc(阴影直方图)重新刺激前用CFSE标记扩增Treg来确定的。(D和E)主要刺激后第9天(D)和第11天(E)出现Treg培养物。数据表示来自至少10种独立文化的结果。(F) 用CD40L-sBc刺激Tregs 9或11天,然后用抗CD3和抗CD28涂层珠重新刺激。在重新刺激5天后收获培养物,并比较三对培养物的总折叠扩张(第页=0.25,Wilcoxon配对签名秩检验)。(G) 用CD40L-sBc刺激Tregs 11天,然后用Invitrogen(开放符号)或Miltenyi Biotec(封闭符号)的抗CD3和抗CD28涂层珠重新刺激。显示了三种配对培养物中细胞随时间的膨胀。采用Wilcoxon配对符号秩检验比较第16天总折叠扩张的差异(第页= 0.25). (H) XY散点图显示了arTreg扩增与不同CD40L-sBc制剂上表达的HLA-DR、CD80和CD86的平均荧光强度(MFI)的相关性。这些数据是11种独立arTreg培养基的摘要。arTregs、arTreg、同种抗原反应Tregs;CD40L-sBc、CD40L-刺激的B细胞;CFSE,羧基荧光素琥珀酰亚胺酯;荧光活化细胞分选;Tregs,调节性T细胞。
FACS纯化后,一单位血液平均产生500万Tregs。通过50到300倍的扩张,我们将能够生产2.5亿到15亿arTreg,这可能低于我们估计的有效剂量(13). 因此,我们探索了改善arTreg扩展的条件。CD40L-sBc刺激的Tregs在刺激后第9天继续聚集并爆发(图3D)这表明Tregs仍处于激活状态,如果此时重新刺激,可能会经历激活诱导的细胞死亡。将再刺激推迟到第11天,此时细胞似乎休息得更充分(图3E)整体扩张持续改善(图3F). 抗CD3/CD28珠的来源也影响Treg扩增的速率(图3G). 相反,我们发现CD40L-sBc上HLA-DR、CD80和CD86表达的变化与arTreg扩增无关(图3H)这表明,只要达到阈值,CD40L-sBc的效力与这些分子的绝对量并不严格相关。总的来说,通过优化再刺激时间和再刺激试剂,arTregs通常会扩大100到1600倍。
arTregs的体外特性
高通量TCR测序用于比较新分离Treg和各种扩增Treg的序列。arTregs的多样性低于新分离的Tregs和PolyTregs(表1)与使用CD40L-sBc刺激的选择性扩张相一致。arTreg基因库仍然多样化,前10个克隆的累积频率不到总基因库的7%,克隆性指数非常低。我们发现,在初次CD40L-sBc刺激和额外抗CD3/CD28珠再刺激后,Tregs之间有85%的TCR序列相似性(图4A). 一贯地,arTregs通过两轮CD40L-sBc或初级CD40L-s Bc扩增,二次珠状再刺激在TCRβ使用方面具有93%的相似性(图4B). 这些结果表明,多克隆再刺激并没有明显改变arTreg基因库。最后,使用两种不同的异基因CD40L-sBc扩增同一个体的Tregs,它们的TCR谱几乎没有重叠(图4C),证明了使用该方案的同种抗原选择性Treg扩增和非反应细胞的有效耗竭。
表1。
利用高通量TCRβ链测序对Tregs进行TCR序列分析
| 1°刺激 |
2°刺激 |
n个 |
%独特的读数 |
前10个克隆的频率(%) |
克隆性1
|
| 无 |
无 |
5 |
10.23 ± 5.39 |
1.77 ± 0.96 |
0.037 ± 0.007 |
| 聚 |
聚 |
三 |
11.36 ± 2.09 |
1.37 ± 0.71 |
0.036 ± 0.018 |
| 分配 |
无 |
2 |
5.87 ± 1.45 |
6.41 ± 2.09 |
0.122 ± 0.016 |
| 分配 |
分配 |
2 |
2.34 ± 1.31 |
5.76 ± 1.82 |
0.133 ± 0.025 |
| 分配 |
聚 |
4 |
3.12 ± 1.39 |
6.86 ± 2.27 |
0.127±0.027 |
图4。使用高通量TCRβ链测序进行Treg TCR储备分析。
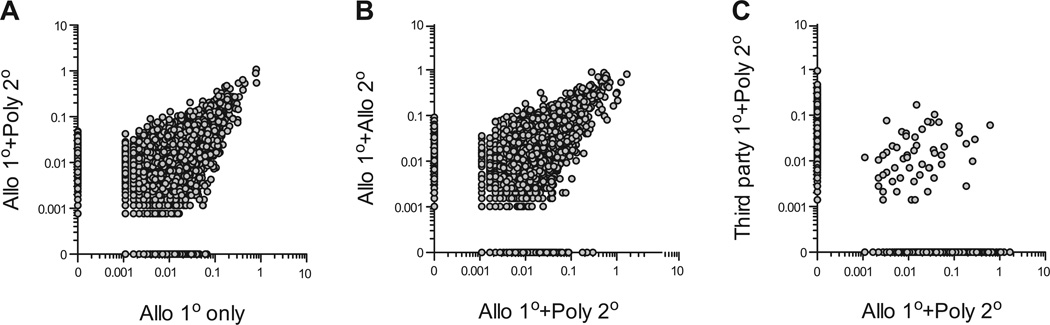
(A) 使用xy散点图比较Tregs在初次CD40L-sBc(Allo)刺激(x轴)或CD40L-s Bc(Allo)刺激和抗CD3/28珠(Poly)再刺激(y轴)后TCRβ链的使用情况,显示两个样本之间85%的相似性。每个圆圈代表一个独特的TCRβ链核苷酸序列,x轴和y轴上的数据点出现在一个样本中,但在另一个样本上没有。这些数据代表了两个独立实验的结果。(B) 使用xy散点图比较Tregs在初次CD40L-sBc刺激和抗CD3/CD28珠再刺激(x轴)后以及在两轮同种异体抗原刺激(y轴)后TCRβ链的使用情况,显示两个样本之间93%的相似性。这些数据代表了两个独立实验的结果。(C) 从一个供体纯化的Tregs被分成两个相等的部分,并用来自两个不同异基因B细胞供体(Allo和Third party)的CD40L-sBc进行初级刺激,然后进行多克隆再刺激。两种arTreg制剂对TCRβ链使用情况的比较显示有2%的重叠。相似的CD40L-sBc、CD40L-刺激的B细胞;Treg,调节性T细胞。
通过该方案扩展的Tregs平均存活率>95%,CD3+CD4细胞+CD8污染最小+T细胞和CD19+B细胞(图5A和表2). 大多数CD4+T细胞为FOXP3+HELIOS公司+和共同表达的CD27和CD62L(图5B和表2)与类似扩张的Tconv细胞表达的模式不同(图5B). 大多数扩张的Tregs已去甲基化TSDR(图5C,表2)TCR或有丝分裂刺激后不产生IFNγ(图5D). 这些结果表明arTreg是稳定的体外扩张并没有像我们之前报道的那样导致IFNγ表达增加(22). 为了确定扩增Tregs的反应性,我们用来自同一供体的CD40L-sBc重新刺激第16天采集的Tregs。平均87.5%(范围72.5%–95.2%)的同种抗原扩增Tregs在相同sBc的再刺激下增殖,类似于使用抗CD3/CD28珠诱导的增殖(平均88.8%,范围73.6%–96%),表明绝大多数Tregs对CD40L-sBc表达的同种抗原反应(图5E和F)。
图5。表型、同种抗原反应性和在体外Tregs的功能随着CD40L-sBc的增加而增强。
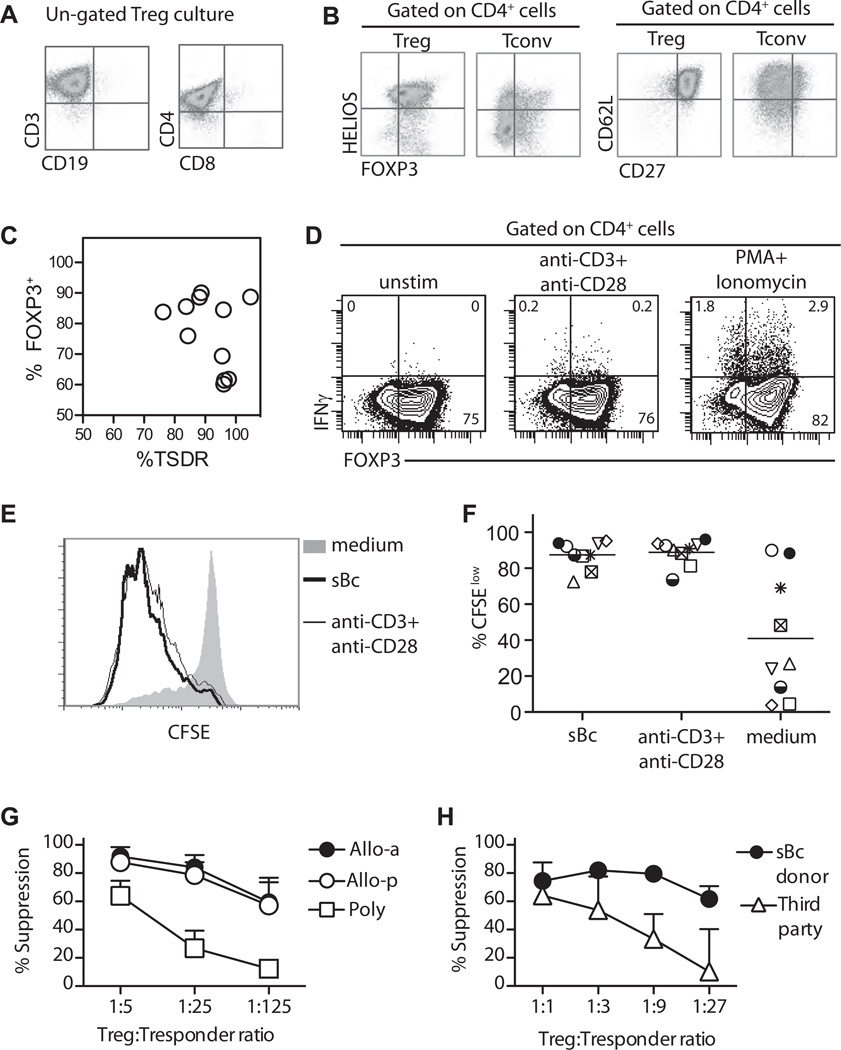
(A和B)流式细胞术检测未经修饰的(A)和CD4门控的(B)Treg培养物。数据代表了至少14个独立实验。(C) 来自11个独立培养物的去甲基化TSDR和FOXP3的百分比之间的相关性。(D) 4小时后arTregs表达IFN-γ在体外刺激。(E) 在第11天,通过原代异基因sBc刺激和多克隆再刺激扩增的Tregs的同种异体反应性测定如下:图3B。显示了叠加直方图的示例。(F) 如(C)所述,对七种独立文化进行了分析。每个符号代表一种独立的Treg文化。(G) 以下内容的摘要在体外图中显示了Tregs通过两轮异基因CD40L-sBc刺激(闭合圆,Allo-a,n=3)、异基因sBc初级刺激后多克隆再刺激(开放圆,Allo-p,n=8)或两轮多克隆刺激(开放方形,Poly,n=5)扩大的抑制。应答者是Treg供体的PBMC,刺激者是sBc供体的PBMC。所示数据是在三到八个独立实验中观察到的平均值±SEM抑制。采用双向方差分析(ANOVA)和Bonferroni多重比较检验确定差异的统计显著性。不同Tregs组在1:5比例下的抑制作用没有显著差异。与Allo-a Tregs相比,PolyTregs的抑制作用显著降低(第页1:25比例下<0.001,以及第页<0.01(1:125比例),或与Allo-p Tregs相比(第页1:25比例下<0.0001,以及第页<0.001,比例为1:125)。Allo-a和Allo-p Tregs在所有比率上都没有显著差异。(H) 显示了CD40L-sBc对sBc供体(闭合圈)或第三方供体(开放三角形)PBMC刺激的Tregs的抑制作用。所示数据是在六个独立实验中观察到的平均值±SEM抑制。采用双向方差分析和Bonferroni多重比较检验来确定差异的统计显著性。受sBc和第三方供体刺激的1:1和1:3比率抑制没有显著差异。与第三方供体刺激的抑制相比,sBc供体以1:9和1:27的比例刺激的抑制显著降低(第页在1:9的比例下<0.001,以及第页<0.001,比例为1:27)。arTregs、arTreg、同种抗原反应Tregs;CD40L-sBc、CD40L-刺激的B细胞;CFSE,羧基荧光素琥珀酰亚胺酯;γ干扰素;外周血单个核细胞;PolyTregs,多克隆扩增Tregs;Tconv,常规CD4+T细胞;Tregs,调节性T细胞;TSDR,Treg-特异性去甲基区。
表2。
|
CD3(CD3)+
|
CD4细胞+
|
FOXP3公司+
|
TSDR公司 |
HELIOS公司+
|
CD62L型+CD27型+
|
CD8(CD8)+
|
CD19型+
|
| 平均值 |
97.1 |
97.1 |
83 |
94 |
88.2 |
85.4 |
0.5 |
0.2 |
| 标准偏差 |
2.6 |
1.9 |
10.8 |
15.5 |
6.6 |
6.4 |
0.2 |
0.2 |
| N个 |
14 |
14 |
14 |
10 |
14 |
10 |
14 |
14 |
与表型和增强的同种异体抗原识别一致,扩增的arTregs在激活时具有高度抑制性在体外与CD40L-sBc来自同一供体的PBMC(图5G). arTregs在抑制MLR方面的效力是PolyTregs的5到25倍(图5G)与之前的报道一致,同种异体反应Tregs的效力增加了5到32倍(12,14,28——30). 用CD40L-sBc或抗CD3/CD28珠重新刺激扩增的arTreg具有相同的抑制活性(图5G)证明多克隆再刺激并没有改变其同种反应性或抑制活性在体外此外,当受相关PBMC刺激时,arTregs的抑制作用是受第三方细胞刺激时的9–27倍(图5H). 总之,我们的结果表明,CD40L-sBc扩增的Tregs对用于扩增的B细胞表达的同种抗原具有增强的反应性和抑制活性。
arTregs在体内保护同种异体皮肤方面表现优异
使用我们最近描述的同种异体免疫介导的人类同种异体皮肤移植损伤模型(12),我们比较了arTregs和PolyTregs的效力。BALB/c.图2−/−γc−/−用HLA-DR0401的人皮肤移植小鼠+供体在过继移植耗尽CD25的异基因PBMC前+单独的细胞或与同基因Treg的不同制剂以5:1的效应细胞/Treg的比例组合。PBMC供体为HLA-DR0401−使用HLA-DR0401对这些捐赠者的arTreg进行扩增+CD40L-sBc。对移植物进行监测,直到排斥反应或PBMC重建后6周,然后收集移植物进行组织学分析。单独或联合使用PBMC或Tregs的小鼠的人类白细胞在脾脏中的植入水平相似(图6A). 在这些实验期间,所有小鼠的体重都保持稳定,表明缺乏GvHD(图6B),与我们之前关于该模型的报告一致(31)。
图6。PolyTregs和arTregs抑制皮肤移植损伤体内在一个人性化的小鼠模型中。
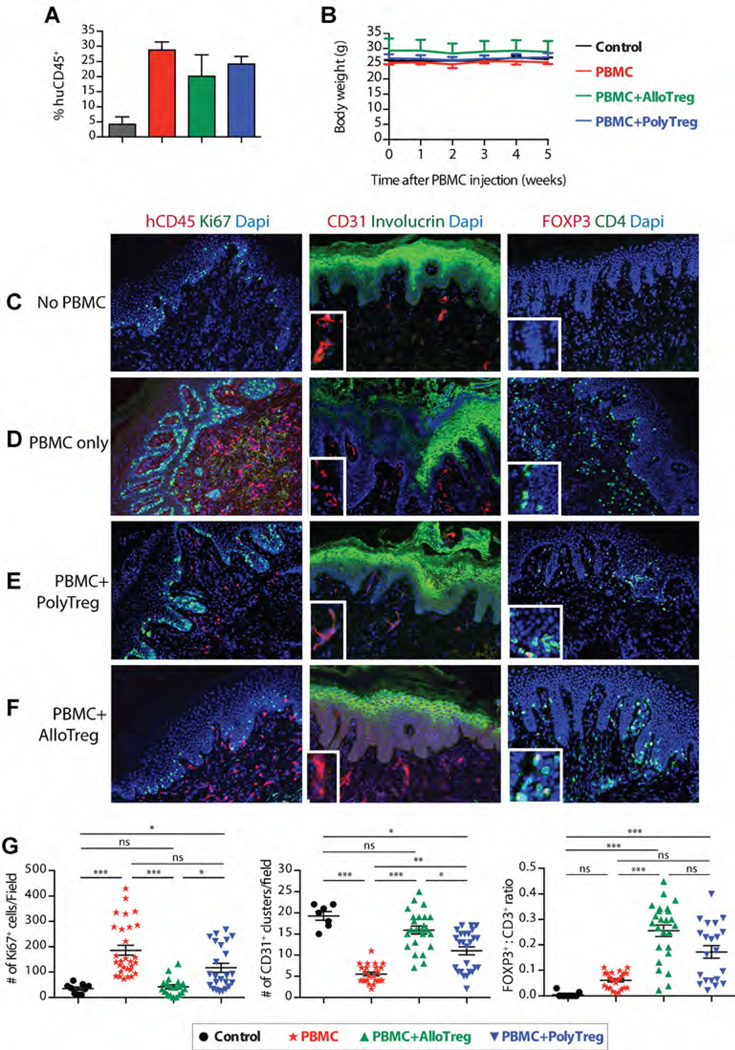
BALB/c.图2−/−γc−/−用人类皮肤移植小鼠,并用与皮肤供体同种异体的PBMC重建。(A) 实验结束时测定了PBMC的重建,表明联合输注Tregs不会显著改变PBMC重建的程度。(B) BALB/c.Rag2的体重−/−γc−/−对四个实验组的小鼠进行评估,以确定总体健康状况,证明PBMC输注不会诱发GvHD。(C–F)使用三色免疫荧光显微镜评估皮肤移植损伤,并显示具有代表性的结果。(G) 通过计算每个移植体的每个染色点的四至六个高倍视野来分析免疫荧光显微图像。然后比较四个实验组的定量结果。采用Kruskal–Wallis检验和Dunn多重比较后验的单向方差分析来确定差异的统计显著性(*第页<0.05, **第页<0.01, ***第页<0.001). arTregs、arTreg、同种抗原反应Tregs;移植物抗宿主病;外周血单个核细胞;PolyTregs,多克隆扩增Tregs;Tregs,调节性T细胞。
与没有PBMC对照动物的皮肤移植物相比(图6C),PBMC单独组的移植物显示强烈的人类CD45+单个核细胞浸润,伴随着角质形成细胞增殖增加、总苞蛋白丢失和血管减少,如聚集的CD31减少所示+真皮中的细胞(图6D). 这些变化揭示了由异基因人类白细胞介导的活跃炎症和真皮-表皮完整性丧失。所有这些炎症参数都通过共同注射PolyTregs而降低,这与FOXP3的增加有关+单元格(图6E). 此外,arTreg组的皮肤移植物几乎完全不受移植物损伤的组织学特征的影响,除了FOXP3的浸润外,与对照组的移植物没有区别+单元格(图6F). 组织学结果的定量分析显示Ki67显著降低+角质形成细胞和CD31增加+细胞簇,与显著较高的FOXP3相关+至CD3+与PolyTreg组相比,arTreg治疗小鼠移植物中的细胞比率(图6G). 这些结果表明,arTregs在保护同种异体移植物方面的疗效有所提高体内。
讨论
在体外在将Treg疗法应用于人类时,扩张一直是一大挑战(13). 通过用有效的抗原CD40L-sBc刺激高度纯化的Tregs,我们能够在16天内实现100到1600倍的扩增。扩充后的特雷格乐队有不同的TCR曲目;保留的Treg特异性表型丰富了同种抗原反应性,并且在抑制同种免疫反应方面更有效在体外和体内与扩展的PolyTregs相比。促成该方案成功的关键参数是培养开始时Tregs的纯度、CD40L-sBc的效力和再刺激条件。
在未添加抗CD28激动剂抗体的情况下,幼稚B细胞未能诱导Tregs扩增(30)与Treg扩展依赖于CD28的协同模拟的概念一致(32). 我们发现,用CD40L刺激B细胞可诱导CD80和CD86表达增加近20倍,这可能是其作为Treg刺激剂效力的基础。使用B细胞的一个优点是与树突状细胞相比,B细胞相对丰富且易于扩增。在活体供体移植的环境中,我们估计器官供体的100毫升外周血将产生足够的CD40L-sBc,以扩大5×106Tregs是从1 U血液中纯化出来的,经过200倍的扩增后可以产生10亿arTregs。对于已故供体移植,供体脾可以用作CD40L-sBc的来源,而无需事先纯化B细胞,因为B细胞的丰度很高(数据未显示)。我们的结果表明,在短期培养中使用符合GMP的试剂大规模生产高纯度和有效的arTregs是可行的。以前的报告显示Tregs可以从尿毒症移植前患者中扩展(33,34). 目前的工作重点是应用该方案扩大从移植前患有终末期器官疾病的患者中分离的Tregs,以实现计划中的两项肝脏和肾脏移植的I期试验。我们认为,Treg在移植中的疗效取决于Treg产品的数量和质量,以及Treg输注和辅助免疫抑制的时间(5,13)。
致谢
本研究得到了尼古拉斯家族、加州大学旧金山分校外科、JDRF、加州大学洛杉矶分校CTSI、NIH(R34 AI095135,P30DK063720)和英国心脏基金会的研究资金支持。MW是基因泰克研究生奖学金的获得者,NS是医学研究委员会(MRC)临床研究奖学金的接受者。该研究还得到了国家健康研究所(NIHR)、盖伊生物医学研究中心、圣托马斯NHS基金会信托基金会和伦敦国王学院的资助。所表达的观点是作者的观点,不一定是NHS、NIHR或卫生部的观点。作者感谢MRC移植中心的支持。
缩写
- arTreg公司
同种抗原反应Tregs
- CD40L-sBc
CD40L刺激的B细胞
- CFSE公司
羧基荧光素琥珀酰酯
- DAPI公司
4-6-二氨基-2-苯基吲哚
- 直流
树突状细胞
- FACS公司
荧光激活细胞分选
- 药品GMP
良好制造规范
- GvHD公司
移植物抗宿主病
- INFγ
干扰素γ
- MLR公司
混合淋巴细胞反应
- 多溴联苯胺
外周血单个核细胞
- PolyTregs公司
多克隆扩增Tregs
- Tconv公司
常规CD4+T细胞
- 特雷格
调节性T细胞
- TSDR公司
Treg-特异性去甲基区
脚注
作者贡献
ALP、NS、AM、ML、MW、GLS、ET、MAM、WL、A Lares、KL和A Laing进行了实验并分析了数据。RIL、JLR和JAB为研究提供了关键建议和审查。QT和GL指导了这项研究,并与ALP和NS一起撰写了手稿。
披露
本手稿的作者有利益冲突需要披露,如美国移植杂志JAB和QT是两项调节性T细胞治疗专利的共同发明者。JAB已收到BD Biosciences的试剂和设备,以支持开发调节性T细胞治疗。
工具书类
-
1Sakaguchi S.自然产生Foxp3-表达CD25+CD4+调节性T细胞,对自身和非自身免疫耐受。自然免疫学。2005年;6:345–352. doi:10.1038/ni1178。[内政部] [公共医学] [谷歌学者]
-
2Wood KJ,Sakaguchi S.移植耐受中的调节性T细胞。Nat Rev免疫学。2003;3:199–210. doi:10.1038/nri1027。[内政部] [公共医学] [谷歌学者]
-
三。Walsh PT、Taylor DK、Turka LA、Tregs和移植耐受性。临床投资杂志。2004;114:1398–1403. doi:10.1172/JCI23238。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
4Waldmann H,Adams E,Cobbold S.重新编程免疫系统:作为利用耐受机制的范例的共受体阻断。免疫学评论2008;223:361–370. doi:10.1111/j.1600-065X.2008.00632.x。[内政部] [公共医学] [谷歌学者]
-
5唐清,蓝石JA,康士明。移植中的CD4(+)Foxp3(+)调节性T细胞治疗。分子细胞生物学杂志。2011;4:11–21. doi:10.1093/jmcb/mjr047。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
6Trzonkowski P、Bieniaszewska M、Juscinska J等。人类体外扩增CD4+CD25+CD127-T调节细胞治疗移植物抗宿主病患者的首次临床结果。临床免疫学。2009;133:22–26。doi:10.1016/j.clim.2009.06.001。[内政部] [公共医学] [谷歌学者]
-
7Brunstein CG、Miller JS、Cao Q等。用脐血移植成人体内扩增T调节细胞的输注:安全性和检测动力学。鲜血。2010;117:1061–1070. doi:10.1182/bloud-2010-07-293795。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
8Di Ianni M、Falzetti F、Carotti A等。Tregs在HLA同源移植中预防GVHD并促进免疫重建。鲜血。2011;117:3921–3928. doi:10.1182/bloud-2010-10-311894。[内政部] [公共医学] [谷歌学者]
-
9Marek-Trzonkowska N、Mysliwiec M、Dobyszuk A等。CD4+CD25highCD127-调节性T细胞的给药可保护儿童1型糖尿病的β细胞功能。糖尿病护理。2012;35:1817–1820年。doi:10.2337/dc12-0038。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
10Sanchez-Fueyo A、Sandner S、Habicht A等。CD4+CD25+调节性T细胞功能在同种异体免疫中的特异性。免疫学杂志。2006;176:329–334. doi:10.4049/jimmunol.176.1.329。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
11Tsang JY,Tanriver Y,Jiang S,等。通过TCR基因转移对CD4+CD25+Tregs的间接异体特异性有利于小鼠移植耐受。临床投资杂志。2008;118:3619–3628。doi:10.1172/JCI33185。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
12Sagoo P、Ali N、Garg G、Nestle FO、Lechler RI、Lombardi G。具有同种抗原特异性的人类调节性T细胞比多克隆调节性T淋巴细胞更能有效抑制同种免疫皮肤移植损伤。2011年《科学与运输医学》;3 doi:10.1126/scitranslmed.3002076。83岁42岁。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
13Tang Q,Lee K。移植的调节性T细胞治疗:我们需要多少细胞?当前手术器官移植。2012;17:349–354. doi:10.1097/MOT.0b013e328355a992。[内政部] [公共医学] [谷歌学者]
-
14Peters JH、Hilbrands LB、Koenen HJ、Joosten I.从CD4(pos)CD25(high)T细胞体外生成人类同种抗原特异性调节性T细胞用于免疫治疗。《公共科学图书馆·综合》。2008;3:e2233。doi:10.1371/journal.pone.0002233。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
15Koenen HJ,Fasse E,Joosten I.基于CD27/CFSE的高抑制性同种抗原特异性人类调节性T细胞体外筛选。免疫学杂志。2005年;174:7573–7583. doi:10.4049/jimmunol.174.12.7573。[内政部] [公共医学] [谷歌学者]
-
16Banerjee DK、Dhodapkar MV、Matayeva E、Steinman RM和Dhodapkar KM。骨髓瘤患者在体外和注射细胞因子成熟DC后通过人类树突状细胞(DC)扩增FOXP3高调节性T细胞。鲜血。2006;108:2655–2661. doi:10.1182/bloud-2006-03-011353。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
17Putnam AL、Brusko TM、Lee MR等。1型糖尿病患者调节性T细胞的扩增。糖尿病。2009;58:652–662. doi:10.2337/db08-1168。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
18Novak EJ、Liu AW、Nepom GT、Kwok WW。MHC II类四聚体可识别肽特异性人类CD4(+)T细胞对甲型流感抗原的增殖反应。临床投资杂志。1999;104:R63–R67。doi:10.1172/JCI8476。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
19Parry RV,加利福尼亚州朗布里,左侧范登伯格,瑞士六月,莱利JL。CD28和可诱导共刺激蛋白Src同源性2结合域对人CD4 T淋巴细胞中磷脂酰肌醇3-激酶、Bcl-xL和IL-2的表达有明显的调节作用。免疫学杂志。2003;171:166–174。doi:10.4049/jimmunol.171.1.166。[内政部] [公共医学] [谷歌学者]
-
20Suhoski MM、Golovina TN、Aqui NA等。构建人工抗原提呈细胞以表达多种共刺激分子。分子热学。2007;15:981–988. doi:10.1038/mt.sj.6300134。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
21Zand MS、Bose A、Vo T等。用于重复监测T细胞和B细胞同种异体反应性的供体细胞的可再生来源。《美国移植杂志》。2005年;5:76–86. doi:10.1111/j.1600-6143.2003.00637.x。[内政部] [公共医学] [谷歌学者]
-
22McClymont SA、Putnam AL、Lee MR等。健康受试者和1型糖尿病患者中人类调节性T细胞的可塑性。免疫学杂志。2010;186:3918–3926. doi:10.0409/jimmunol.103099。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
23Wieczorek G、Asemissen A、Model F等。FOXP3的定量DNA甲基化分析是一种计算外周血和实体组织中调节性T细胞的新方法。2009年癌症研究;69:599–608. doi:10.1158/0008-5472.CAN-08-2361。[内政部] [公共医学] [谷歌学者]
-
24Ye Q,Loisiou M,Levine BL,等。工程化人工抗原提呈细胞促进肿瘤浸润淋巴细胞的直接高效扩增。《运输医学杂志》2011;9点31分。doi:10.1186/1479-5876-9-131。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
25Butler MO、Friedlander P、Milstein MI等。利用体外培养的CD8+T细胞建立人类抗肿瘤记忆。2011年《科学与运输医学》;3 doi:10.1126/scitranslmed.3002207。80ra34。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
26Smith BD、Kasamon YL、Kowalski J等。K562/GM-CSF免疫治疗可降低甲磺酸伊马替尼残留病慢性粒细胞白血病患者的肿瘤负担。《临床癌症研究》2010;16:338–347. doi:10.1158/1078-0432.CCR-09-2046。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
27Borrello IM、Levitsky HI、Stock W等。分泌粒细胞巨噬细胞集落刺激因子(GM-CSF)的细胞免疫疗法结合自体干细胞移植(ASCT)作为急性髓细胞白血病(AML)血液的缓解后治疗。2009;114:1736–1745. doi:10.1182/bloud-2009-02-205278。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
28Veerapathran A,Pidala J,Beato F,Yu XZ,Anasetti C.直接或间接呈现的同种抗原特异性人类Tregs的体外扩增。鲜血。2011;118:5671–5680. doi:10.1182/bloud-2011-02-337097。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
29Tran GT、Hodgkinson SJ、Carter NM等。白细胞介素-5(IL-5)促进抗原特异性CD4+CD25+T调节细胞的诱导,抑制自身免疫。鲜血。2012;119:4441–4450. doi:10.1182/bloud-2011-12-396101。[内政部] [公共医学] [谷歌学者]
-
30Chen LC,Delgado JC,Jensen PE,Chen X.使用异基因B细胞直接扩增人类同种异体特异性FoxP3+CD4+调节性T细胞用于治疗应用。免疫学杂志。2009;183:4094–4102. doi:10.4049/jimmunol.0901081。[内政部] [公共医学] [谷歌学者]
-
31Ali N、Flutter B、Sanchez Rodriguez R等。NOD-scid IL-2Grammanull小鼠的异种移植物抗宿主病表现为T效应记忆表型。《公共科学图书馆·综合》。2012;7:e44219。doi:10.1371/journal.pone.0044219。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
32Golovina TN、Mikheeva T、Suhoski MM等。CD28协同刺激对人类T调节的扩展和功能至关重要。免疫学杂志。2008;181:2855–2868年。doi:10.4049/jimmunol.181.4.2855。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
33Berglund D、Korsgren O、Lorant T、Schneider K、Tufveson G、Carlsson B。等待肾移植的尿毒症患者CD4+CD25+FoxP3+调节性T细胞和Tr1细胞的分离、扩增和功能评估。转导免疫。2012;26:27–33. doi:10.1016/j.trim.2011.09.003。[内政部] [公共医学] [谷歌学者]
-
34Berglund D、Karlsson M、Biglarnia AR等。从等待肾移植的尿毒症患者中获取调节性T细胞用于临床试验。临床实验免疫学。2013;173:310–322. doi:10.1111/cei.12112。[内政部] [PMC免费文章] [公共医学] [谷歌学者]








