摘要 早期哺乳动物胚胎利用组蛋白H3赖氨酸27三甲基化(H3K27me3)使基本发育基因保持在抑制染色质状态。 随着分化的进行,H3K27me3以一种独特的方式被去除,以激活发育基因表达的谱系特异性模式。 早期胚胎染色质环境的这些快速变化被认为依赖于H3K27脱甲基酶。 我们采用小鼠遗传学方法去除了 6千马克 基因家族, Utx公司 ( 丹麦马克6a ,X连锁基因)和 Jmjd3号机组 ( Kdm6亿 ,常染色体基因)。 男性胚胎因活性H3K27脱甲基而无效 6千马克 基因家族可以存活到足月。 在妊娠中期,胚胎表现出适当的模式和激活 霍克斯 基因。 这些雄性胚胎保留Y染色体UTX同源物UTY,由于Jumonji-C结构域催化位点的突变,UTY不能去甲基化H3K27me3。 缺乏所有酶解KDM6去甲基化的胚胎干细胞在分化过程中表现出全球H3K27me3水平的典型下降。 这些ES细胞的维甲酸分化显示H3K27me3的丢失和H3K4me3的增加 霍克斯 启动子和其他转录因子,并诱导类似于控制细胞的表达。 一小部分基因表现出与启动子H3K4me3减少和一些低水平H3K27me3积累相关的表达减少。 最后, Utx公司 和 Jmjd3号机组 突变的小鼠胚胎成纤维细胞(MEFs)显示H3K27me3从几种 霍克斯 基因和转录因子。 我们的结果表明,在没有主动去甲基化的情况下,早期胚胎H3K27me3阻遏可以通过 6千马克 基因家族。
作者摘要 H3K27me3在胚胎初期抑制发育基因。 KDM6家族由UTX和JMJD3组成,是已知的唯一能去甲基化H3K27me3的蛋白质,推测它们在哺乳动物早期发育中催化抑制性染色质的快速去除。 然而,我们报告称,男性胚胎携带两种基因的突变 Utx公司 和 Jmjd3号机组 存活至足月,妊娠中期表现正常。 我们利用几种细胞培养模型证明,在缺乏活性KDM6去甲基化的情况下,H3K27me3从受抑制的启动子中丢失。 我们的数据表明,KDM6 H3K27me3去甲基化在早期胚胎中不是必需的,H3K17me3从发育基因中丢失是通过新的机制发生的。
介绍 哺乳动物胚胎在整个发育过程中会经历细胞规格和基因表达程序的剧烈变化。 组蛋白的翻译后修饰促进了这些变化,组蛋白提供了一种表观遗传机制来协调谱系特异性转录谱的启动和维持,这些转录谱可以通过多个细胞分裂遗传。 在胚胎干细胞和其他多能干祖细胞中,关键的发育基因保持在静止状态。 二价表观遗传特征定义了这一大类基因。 这些启动子通过组蛋白H3赖氨酸27三甲基化(H3K27me3 [1] —— [4] 已在ES细胞、早期胚胎、谱系祖细胞和生殖系中鉴定出双价启动子 [4] —— [15] 通过规范或分化,这些二价启动子可以分解为单价H3K4me3活性状态或H3K27me3抑制状态。 在许多细胞培养模型系统中,组蛋白去甲基化酶需要去除H3K27me3以促进基因激活,这表明H3K17me3去甲基化在胚胎发育中至关重要 [16] —— [30] .
H3K27me3脱甲基酶是组蛋白脱甲基酶KDM6,Jumonji-C(JmjC)结构域家族的成员。 三种KDM6蛋白JMJD3(KDM6B,由常染色体基因编码)、UTX(KDM5A,X染色体)和UTY(Y染色体)都共享一个非常保守的JmjC组蛋白去甲基化结构域 [31] 在这个蛋白家族中,JMJD3和UTX脱甲基H3K27三甲基和二甲基残基,而人类UTY的催化活性大大降低 [27] , [31] —— [34] 小鼠UTY虽然与X染色体同源UTX保持82%的相似性,但由于其JmjC结构域的催化活性位点发生突变,不会去甲基化H3K27me3 [31] .
UTX和JMJD3分别参与细胞培养中的早期胚胎规范事件 [17] —— [19] , [22] , [32] 导致H3K27me3脱甲基酶在早期胚胎分化事件中发挥作用的假设。 然而,小鼠诱变表明情况并非如此,因为缺乏个别脱甲基酶的胚胎可以存活到足月。 Jmjd3号机组 −/− 纯合子因新生儿呼吸缺陷而表现出出生后死亡 [35] . Utx公司 −/年 半合子男性可以活到成年,并显示出正常的寿命 [31] 相反,使H3K27甲基化的多梳抑制复合物2(PRC2)的突变导致早期胚胎发育基因的早熟表达和原肠胚形成停滞 [36] —— [39] . Utx公司 −/− 纯合雌性和 Utx公司 负极 ; 尤蒂 负极 半合子男性都是妊娠中期致死的,发育迟缓,胚胎心脏发育缺陷 [31] 因此,UTX/UTY缺失导致的妊娠中期心血管死亡是由于这些蛋白的脱甲基酶非依赖性功能所致。 目前尚不清楚KDM6家族是否存在早期胚胎脱甲基酶依赖性功能,因为JMJD3和UTX之间可能存在一些冗余。
为了研究KDM6家族在早期胚胎发育中的作用,我们产生了旨在消除发育中小鼠胚胎中所有KDM6 H3K27me3脱甲基酶活性的突变。 男性 Utx公司 −/年 ; Jmjd3号机组 −/− 没有KDM6 H3K27去甲基化的胚胎存活至足月。 中产阶级 Utx公司 −/年 ; Jmjd3号机组 −/− 胚胎表现正常,具有胚胎第10.5天(E10.5)胚胎的特征。 我们利用几个模型系统(类胚体、维甲酸、小鼠胚胎成纤维细胞)证明,在没有活性KDM6去甲基化的情况下,H3K27me3可以从被抑制基因的启动子中去除。 我们的结论是,KDM6脱甲基酶对早期胚胎发育不是必需的,而H3K27me3的阻遏作用可以在KDM6脱甲作用不活跃的情况下减轻。
结果 缺乏KDM6去甲基化的小鼠胚胎存活至足月,并显示正常的早期胚胎表型 为了去除小鼠胚胎中的H3K27去甲基化酶活性,我们在这两种细胞中产生了突变等位基因 Utx公司 和 Jmjd3号机组 我们之前描述了 Utx公司 佛罗里达州 外显子3两侧带有loxP位点的等位基因 [31] .Cre介导的外显子3缺失( Utx公司 Δ )在编码序列中创建了移码,UTX蛋白为空。 我们现在描述一个靶向等位基因, Jmjd3号机组 tm1标记 ( Jmjd3号机组 佛罗里达州 )将loxP位点5′整合到外显子14,将3′整合到第20外显子( 图S1A )。 经Southern印迹、PCR基因分型和RT-PCR验证( 图S1B、S1C和S1D ),Cre介导的这部分编码序列的删除( Jmjd3号机组 Δ )去除了JmjC催化H3K27脱甲基酶结构域( 图S1A )。 与已发表的报告类似, Jmjd3号机组 Δ/Δ 纯合子幼崽出生时死于呼吸系统缺陷( 图S1E ). Jmjd3号机组 Δ/Δ 纯合胚胎在妊娠中期表现正常( 图S1F ); 然而,一些表型在胚胎发育后期出现,将在其他地方描述。 同时 Jmjd3号机组 Δ/Δ 断奶时未观察到纯合子幼崽,它们在E18.5时很容易恢复( 图1A ).
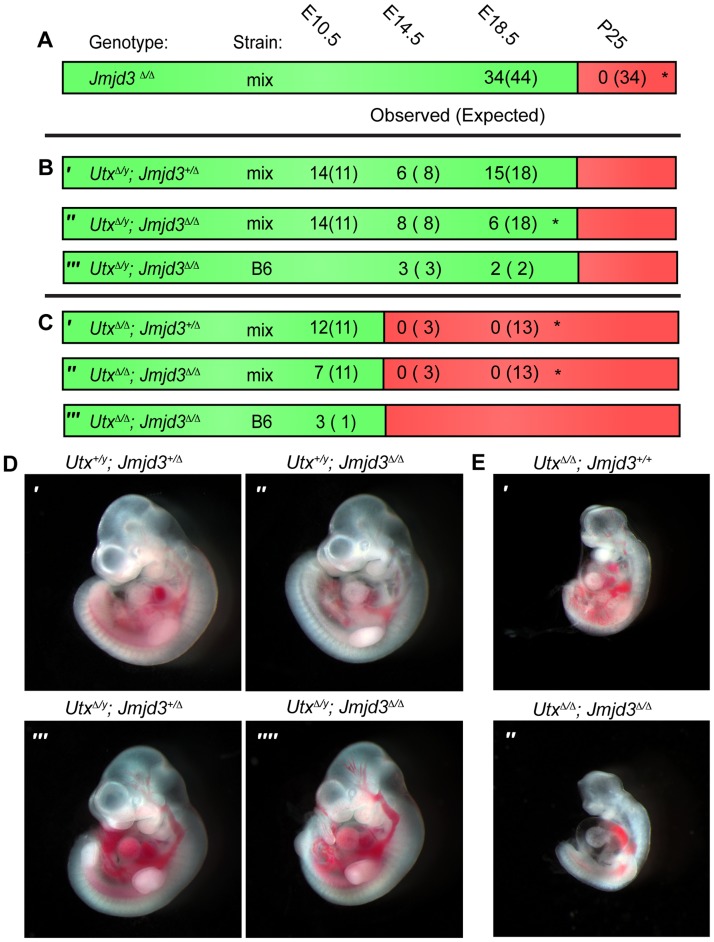
图1。 Utx公司 和 Jmjd3号机组 突变表型。
(A–C)在胚胎(第10.5、14.5或18.5天)或出生后(第25天,断奶)时间点观察到的和预期的(括号内)指示基因型数量。 数据包括 Jmjd3号机组 Δ/Δ (A) , Utx公司 Δ/ 年 ; Jmjd3号机组 +/ Δ (B′), Utx公司 Δ/ 年 ; Jmjd3号机组 Δ/Δ (B〃和B′〃), Utx公司 Δ/Δ ; Jmjd3号机组 +/ Δ (C′),和 Utx公司 Δ/Δ ; Jmjd3号机组 Δ/Δ (C〃和C〃)基因型。 绿色区域表示生存能力,红色区域表示致命性。 Mix表示混合遗传背景,B6已回交至C57BL6超过5代。 与χ确定的预期等位基因频率的显著偏差 2 p值为:(A)*<0.001,(B)*=0.005,和(C)*<0.00。 (D,E)胚胎第10.5天(D)雄性的图像 Utx公司 +/年 ; Jmjd3号机组 +/Δ (D′), Utx公司 +/年 ; Jmjd3号机组 Δ/Δ (D〃), Utx公司 Δ/ 年 ; Jmjd3号机组 +/ Δ (D〃), Utx公司 Δ/ 年 ; Jmjd3号机组 Δ/Δ (D〃〃)胚胎和(E)雌性 Utx公司 Δ/Δ (E′)和 Utx公司 Δ/Δ ; Jmjd3号机组 Δ/Δ (E〃)胚胎,B6背景。
我们接下来试图推导 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 所有KDM6 H3K27去甲基化都会丢失的胚胎,同时保留野生型UTY的去甲基化酶非依赖性功能。 类似 Utx公司 −/年 仅突变 [31] ,两者都是 Utx公司 Δ/年 ; Jmjd3号机组 +/Δ 和 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 胚胎存活至E18.5( 图1B′和1B〃 )。 然而,观察到的 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 相对于预期孟德尔频率的胚胎。 预期基因型频率 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 胚胎是在E14.5时获得的,因此在 Utx公司 和 Jmjd3号机组 在胚胎发育后期。 妊娠中期,所有男性组合 Utx公司 和 Jmjd3号机组 突变与对照组基本上没有区别( 图1D ). Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 胚胎表现出E10.5胚胎的正常特征,如正常大小和体节数(35-40),突出的前肢和后肢芽,发育的鳃弓(包括将鳃弓1分离为上颌和下颌部分, 图1D〃〃 )。 作为 Utx公司 −/年 出生后死亡在C57BL6/J(B6)背景下更为明显 [31] ,我们交叉了 Utx公司 Δ 和 Jmjd3号机组 Δ 等位基因。 在B6背景上, Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 胚胎在E14.5和E18.5时间点都能存活( 图1B〃 )。 鉴于母体UTX在果蝇胚胎中的沉积有助于早期发育中的去甲基化活性 [40] ,我们测试了UTX和JMJD3母体库的缺失是否会增强小鼠表型。 Utx公司 fl/Δ ; Jmjd3号机组 fl/Δ ; 瓦萨 Cre公司 雌性小鼠(卵母细胞缺失 Utx公司 和 Jmjd3号机组 )与 Utx公司 飞行/飞行 ; Jmjd3号机组 fl/Δ ; 瓦萨 Cre公司 雄性小鼠(精子携带缺失 Utx公司 和 Jmjd3号机组 )和结果E10 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 胚胎( 图S2A ')已完全重组 Utx公司 和 Jmjd3号机组 floxed等位基因( 图S2B )并复制了从 Utx公司 +/Δ ; Jmjd3号机组 +/Δ 杂合母亲( 图1D〃〃 ).
Utx公司 和 Jmjd3号机组 通过定量RT-PCR确认敲除( 图S3A )和E10.5处, Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 胚胎没有发生改变 霍克斯 H3K27me3的表达水平或全球水平升高( 图S3B 、C、D)。 E10.5的H3K27me3免疫荧光比较 Utx公司 +/年 ; Jmjd3号机组 +/Δ 和 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 在同一张玻片上切片的胚胎显示心脏心肌内H3K27me3水平相似( 图S3E )和脊髓近端ISL1阳性运动神经元( 图S3F )。 然而,来自这些胚胎的小鼠胚胎成纤维细胞(MEFs)H3K27me3水平略有升高,但具有统计学意义( 图S3G,H )。 总的来说,在没有KDM6 H3K27去甲基化的情况下,胚胎可以通过原肠胚形成存活下来,并在E10.5呈现正常模式。 值得注意的是 Utx公司 Δ/Δ ; Jmjd3号机组 +/Δ 和 Utx公司 Δ/Δ ; Jmjd3号机组 Δ/Δ 雌性胚胎与 Utx公司 Δ/Δ 纯合突变,因为这些胚胎在E10.5后都是致命的( 图1C )表现出类似的发育迟缓特征( 图1E )。 此外,UTX和JMJD3去甲基化的母亲缺失对表型严重性没有贡献( 图S2A ″). 综合起来,我们的数据表明 发送(Utx/U) 是上位的 Jmjd3号机组 ,主要在后期发育阶段发挥作用。
没有KDM6 H3K27me3去甲基化的ES细胞具有女性特异性分化缺陷 我们建立了ES细胞分化模型来研究在没有UTX和JMJD3的情况下H3K27me3去甲基化的时间过程。 我们利用了 CAGGCre-ER公司 添加三苯氧胺诱导等位基因重组的转基因系统 [41] 在接受他莫昔芬治疗(+TX)2天后, Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 男性或 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 雌性ES株表现出floxed外显子完全缺失和内源性蛋白丢失( 图S4A和S4B )。 140-KD背景波段存在于 图S4B和 不会迷失在 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES+TX。确保这不是一种替代方案 Utx公司 我们分析了其在 Utx公司 GT1/年 胚胎干细胞 [31] ,任何替代产品都应该被基因捕获。 尽管 Utx公司 GT1/年 ES细胞确实陷阱 Utx公司 阻止跨JmjC域表达的转录物( 图S4C )它不会影响背景带的水平( 图S4B )表明这些确实是非特异性带。 此外,带有第二个独立UTX抗体的western blot产生了一个干净的blot,其中没有UTX带 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES+TX样本( 图S4D ).
我们诱导了类胚体(EB)分化,如 图2A .培养4天, Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 +TX EB看起来与未经处理的对照组相同( 图2B ). Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 雌性EB+TX较小,外胚层紊乱,细胞突出或脱落( 图2B )。 与聚集EB分化相比,悬滴EB分化在规定的滴体积内利用较小的起始ES细胞数,但仍产生相似的EB表型( 图S5A )。 随着分化的进展,类胚体的全球H3K27me3水平呈现特征性下降 [32] , [42] 从EB中提取组蛋白以确定该过程是否在没有UTX和JMJD3去甲基化的情况下发生。 相对于ES细胞中H3K27me3的整体水平,所有EB,甚至 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 女性EB+TX显示H3K27me3降低( 图3C )。 荧光定量western blotting证实雄性和雌性+TX EB都表现出H3K27me3水平的丢失( 图S5B、C )。 因此,在没有所有KDM6的情况下,早期EB分化事件与H3K27me3水平的下调一致。
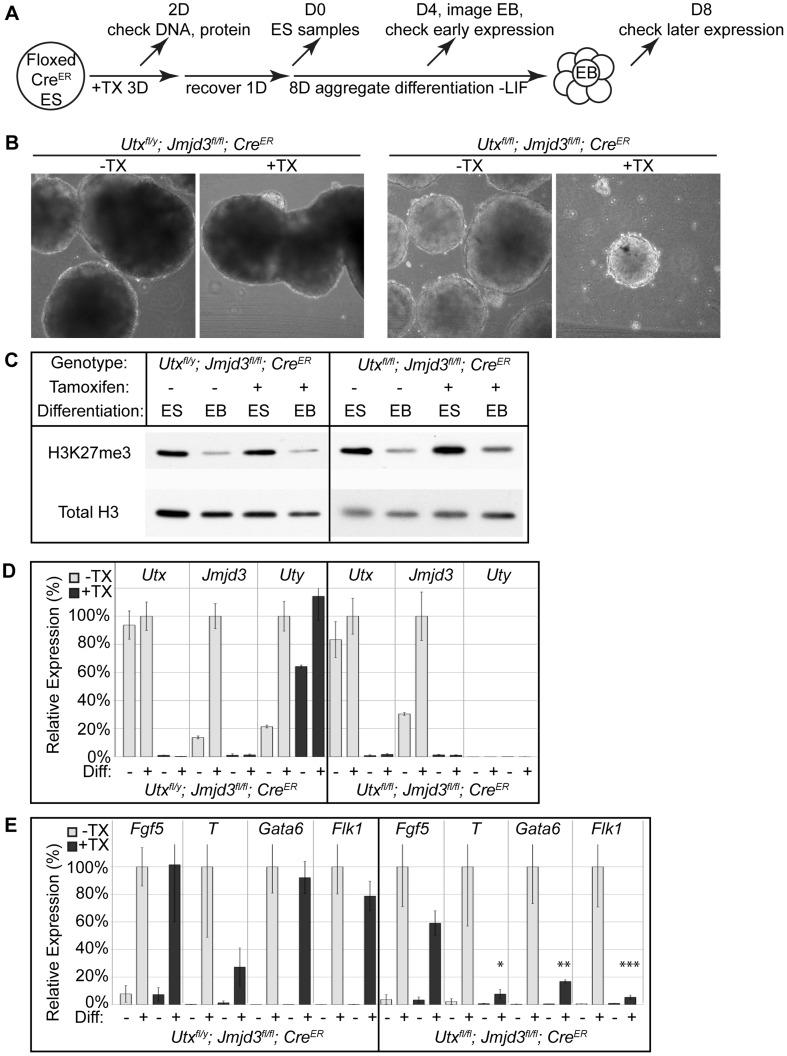
图2。 男女EB分化 Utx公司 和 Jmjd3号机组 突变ES细胞系。
(A) Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 或 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞系未经处理(−TX)或用三苯氧胺处理3天(+TX),然后在聚合悬浮培养(EB)中分化。 (B) 第4天EB的图像。 (C) 组蛋白提取自 Utx公司 飞行/年 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 或 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞(分化ES)或第4天EB(分化EB。 (D) 定量RT-PCR Utx公司 , Jmjd3号机组 ,或 尤蒂 从第0天开始 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 或 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞(分化−)或第8天EB(分化+)未经治疗(−TX,浅灰色)或预处理三苯氧胺(+TX,黑色)。 RT-PCR交叉删除 Utx公司 和 Jmjd3号机组 外显子。 N=每次处理3个样品。 所有样本均相对于单个雄性或雌性品系中的−TX分化+进行了标准化。 (E) 定量RT-PCR Fgf5型 (EB第4天), Brachyury T公司 ( T型 ,EB第4天), Gata6公司 (EB第8天),或 法兰1 (EB第8天)从 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 或 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞(Diff−)或指示的EB时间点(Diff+)未经治疗(−TX,浅灰色)或用三苯氧胺(+TX,黑色)预处理。 所有样本均相对于单个雄性或雌性品系中的−TX分化+进行了标准化。 表达显著降低(T检验p值*=0.02,**=0.005,***=0.006,N=3个样本/次)。
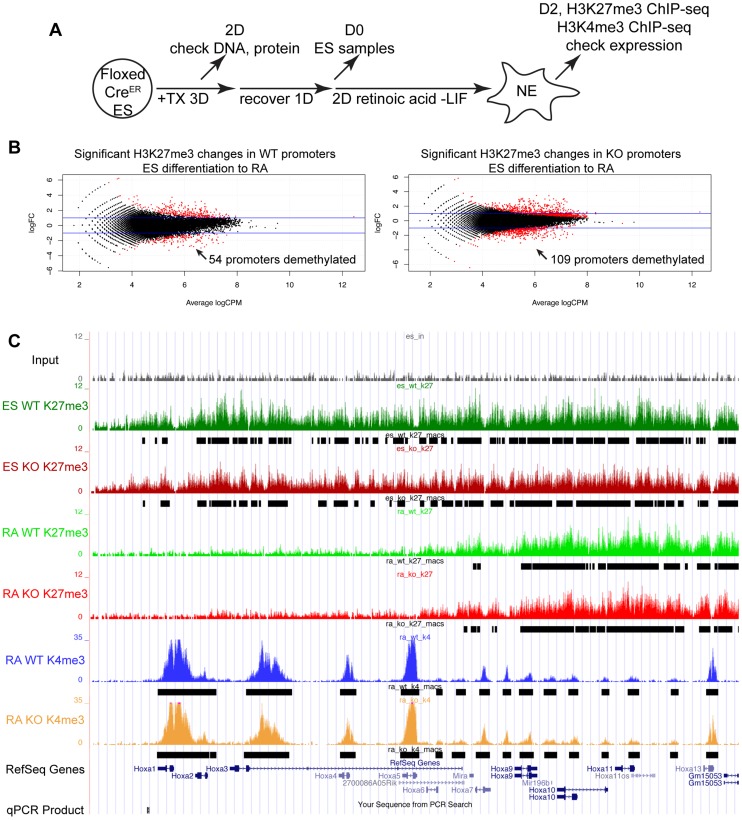
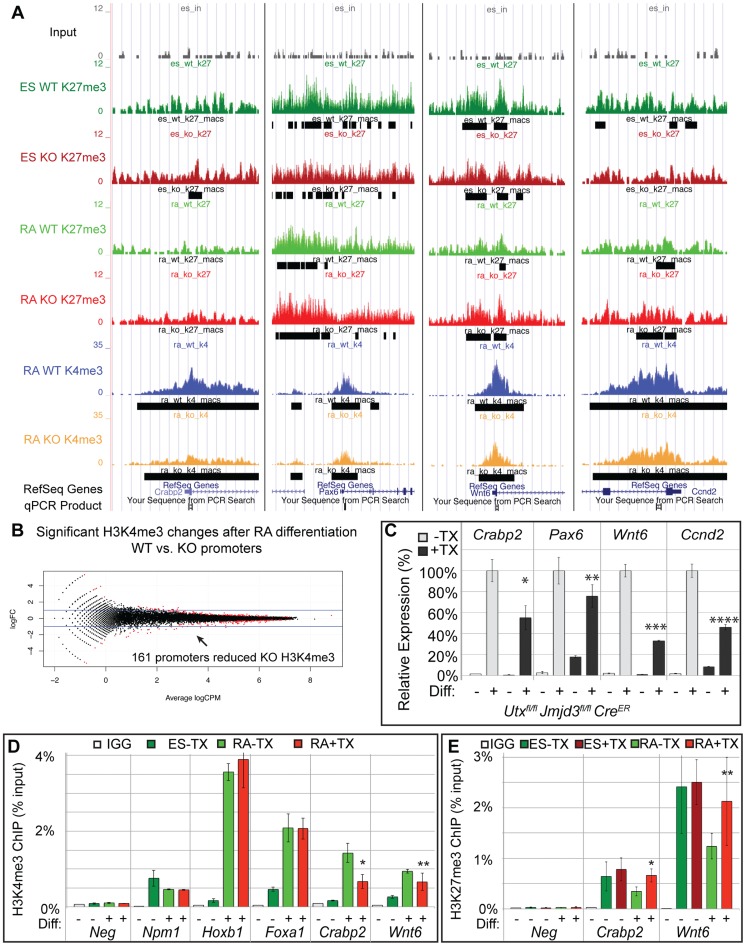
图3。 在没有KDM6去甲基化的情况下,近端Hox基因显示RA治疗后H3K27me3丢失。
(A) Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞未经处理(WT)或用TX预处理3天(KO),恢复,并通过2天的维甲酸处理分化为神经表皮。 在D0 ES细胞和D2 RA处理的细胞上进行H3K27me3和H3K4me3 ChIP-seq。 (B) 通过edgeR比较ES和RA处理细胞中所有启动子(+/-1 KB)的标准化序列读数,以确定在任一WT中H3K27me3降低的启动子( Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 −TX)或KO( Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 +TX)小区。 对数倍变化(logFC)是根据每百万次读取的平均日志计数(平均logCPM)绘制的。 在该图中,54个WT和109个KO启动子在RA处理下表现出H3K27me3降低(logFC阴性,FDR<0.05,ES细胞中确定的H3K17me3 MACS峰值)。 (C) UCSC基因组浏览器查看ChIP-seq的轨迹 草酸铂 集群。 图中所示为输入(黑色)、WT ES H3K27me3 ChIP(深绿色)、KO ES H3G27me3 ChIP(深红色)、WT-RA H3K17me3 ChIP(浅绿色)、KI RA H3K24me3 ChIP(浅红色)、WI RA H3Ch4me3 ChIP。 底部标注了ChIP-qPCR检测的RARE区域。
跨缺失外显子的RT-PCR证实,即使在培养8天后,野生型 Utx公司 和 Jmjd3号机组 表情缺失 尤蒂 TX处理细胞的表达没有减少( 图2D )。 男性 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 EBs+TX显示原始外胚层的正常激活( Fgf5型 表达),中胚层( 法兰1 )和内胚层( Gata6公司 , 图2E )。 相反, Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 雌性EBs+TX启动分化并诱导原始外胚层( Fgf5型 ),但未能指定中胚层(Brachyury T型 ,如图所示 T型 ),中胚层( 法兰1 )和内胚层( Gata6公司 , 图2E ). Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 将ES+TX电镀以获得突变克隆的单细胞集落,该突变ES系在数周内的组成性繁殖不会影响细胞分化为EB的能力( 图S5D、E )。 总的来说,EB分化严重不足 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 +TX细胞不能重现 Utx公司 Δ/Δ ; Jmjd3号机组 Δ/Δ 雌性胚胎( 图1E〃 ).
ES细胞H3K27me3的去除和基因激活不需要KDM6脱甲基酶 为了研究KDM6在H3K27me3脱甲基中的作用,我们利用ES细胞的维甲酸(+RA)分化。 作为 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 EB+TX似乎能够启动外胚层规范,可以在此细胞模型中研究RA向神经-外胚层谱系的分化,其中KMD6成员的所有活性去甲基化都已被移除。 我们使用了中概述的2天RA分化时间过程 图3A .H3K27me3 ChIP在4个WT ES个体重复上进行( Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 西班牙−德克萨斯州),KO ES( Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES+TX),重量RA( Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 RA−TX)和KO RA( Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 RA+TX)。 每组4个重复中的两个合并在一起,每组产生的2个重复进行高通量测序。 H3K4me3 ChIP-seq也在WT RA和KO RA的2个重复上进行。 ChIP-seq(MACS)算法的基于模型的分析确定了各组中H3K27me3和H3K4me3的富集峰,edgeR统计分析软件确定了WT(WT ES vs.WT RA)和KO(KO ES vs KO RA)RA分化中经历H3K17me3去甲基化的基因。 总的来说,1044个WT ES启动子(转录起始位点:TSS+/-1KB)和1141个KO ES启动子都显示出H3K27me3峰值。 在这些启动子中,945和1055(WT和KO)也有RA H3K4me3峰,表明这些启动子大多数是二价的。
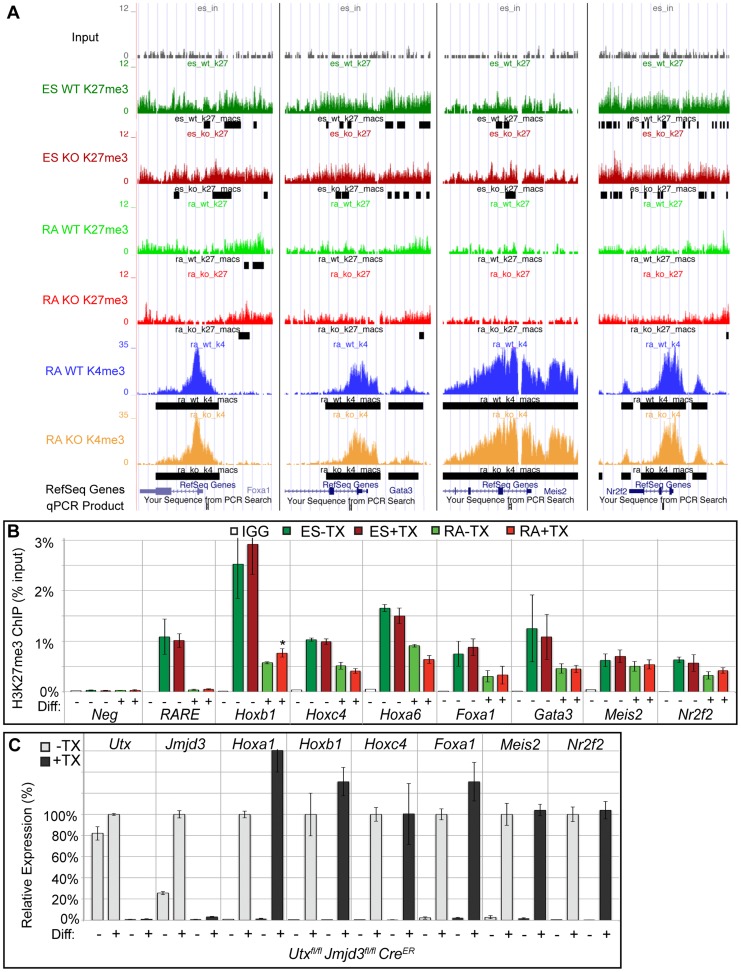
EdgeR鉴定出54个WT启动子(来自50个独特基因,一些具有替代启动子)和109个KO启动子( 图3B 和 表S1 )两个数据集中有许多基因重叠。 许多 霍克斯 基因在WT和KO-RA分化中都丢失了H3K27me3。 H3K27me3和H3K4me3 ChIP-seq的轨迹上传到UCSC基因组浏览器。 随着RA分化 草酸铂 群集( 图3C )来自 霍克萨1 通过 霍克斯6 WT和KO细胞从ES向RA分化时H3K27me3广泛丢失。 组蛋白谱的这种改变与近端H3K4me3的大峰值相关 草酸铂 启动子,显示基因激活事件。 H3K27me3也从近端大量丢失 霍克斯布 ( Hoxb1-Hoxb6型 ), 霍克斯 ( Hoxc4-Hoxc6型 ), 和Hoxd ( Hoxd1-Hoxd4型 )集群( 图S6A、B、C )。 除了 霍克斯 基因,许多其他转录因子,如 福克斯1 , 加塔3 , 梅斯2 、和 编号2f2 KO-RA治疗中证实启动子H3K27me3缺失( 图4A 和 表S1 )。 H3K27me3 ChIP-qPCR证实了在没有KDM6脱甲基的情况下H3K17me3的丢失( 图4B )。 值得注意的是,所有测试的基因在RA分化时都表现出类似的H3K27me3的WT和KO损失。 仅限 霍克斯b1 与WT RA相比,KO RA的H3K27me3略有显著增加,但总体上 霍克斯b1 与KO ES相比,KO RA中H3K27me3的表达量明显减少。此外,RT-PCR表达分析证实,H3K17me3缺失的基因可有效诱导RA KO细胞的转录激活( 图4C ). Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 将ES+TX电镀以获得突变克隆的单细胞集落,该突变ES系在数周内的组成性繁殖不会影响细胞激活转录的能力( 图S5F )。 H3K27脱甲基酶与H3K4甲基转移酶的MLL复合物家族有物理关联。 该复合物的两个成员(ASH2L和RBBP5)在KO细胞中以正常水平表达( 图S7A )。 在没有去甲基化的情况下,H3K27me3缺失的一种替代解释是PRC2 H3K27甲基化复合物在分化细胞中下调或以非甲基化酶依赖的方式从靶向启动子中移位。 而EZH2 H3K27甲基转移酶在RA分化细胞中保持高表达( 图S7B )在没有KDM6去甲基化的情况下,蛋白质从H3K27me3缺失的启动子中转移()。 总之,被抑制的基因可以证明H3K27me3的丢失,并在没有KDM6的情况下启动表达。
图4。 在没有KDM6去甲基化的情况下,一些发育基因在RA治疗中表现出H3K27me3丢失。
(A) UCSC基因组浏览器视图 福克斯1 , 加塔3 , 梅斯2 、和 编号2f2 图中所示为Input(黑色)、WT ES H3K27me3 ChIP(深绿色)、KO ES H3G27me3 ChIP(深红色)、WT-RA H3K17me3 ChIP(浅绿)、KO-RA H3C27me3 ChIP(浅红)、WT-RA H3K4me3 ChIP。 底部标注了ChIP-qPCR检测的区域。 (B) 通过ChIP-qPCR验证H3K27me3损失。 H3K27me3的ChIP Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞(深绿色和红色,Diff−)或RA治疗2天后(浅绿色或红色,Diff+)未经治疗(绿色)或用三苯氧胺(红色)预处理。 IgG控件ChIP显示为白色条。 H3K27me3阴性基因座的定量PCR( Slc2a8系列 发起人, 阴性 )用于与 霍克斯 一种簇状视黄酸反应元件( 罕见 ), 霍克斯b1 , 霍克斯4 , 霍克斯6 , 福克斯1 , 加塔3 , 梅斯2 、和 编号2f2 发起人。 N=每次处理4个样品。 所有测试的基因在WT和KO细胞中均表现出去甲基化,只有Hoxb1在KO-RA治疗中表现出轻微但显著的增加(p值=0.03)。 (C) 定量RT-PCR Utx公司 , Jmjd3号机组 ,并指示 霍克斯 基因, 福克斯1 , 梅斯2 、和 编号2f2 从 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞(Diff−)或RA治疗2天后(Diff+)未经治疗(−TX,浅灰色)或预先用他莫昔芬(+TX,黑色)治疗。 N=每次处理3个样品。 所有样本均相对于−TX分化+RA治疗进行了归一化。 未检测到基因在KO-RA细胞中的表达显著降低。
KDM6的缺失减少了H3K4me3调节基因的一小部分中H3K4甲基化和转录激活 对WT RA和KO RA细胞的H3K4me3 ChIP-seq进行MAC分析,确定在19140和19367个各自的启动子处出现富集峰(TSS+/-1KB)。 WT RA与KO RA的EdgeR比较发现161个启动子(147个基因)在KO H3K4me3中表现出显著降低(FDR<0.05)( 图5B , 表S2 )。 其中大多数是整个峰值强度范围内的小褶皱变化。 在这161个启动子中,只有27个(26个基因)具有ES WT或KO H3K27me3峰值,因此大多数基因不受H3K27甲基化的调控。 一些表现出KO H3K4me3减少并具有H3K27me3峰值的基因如 图5A RT-PCR证实,几个KO H3K4me3减少的基因表达减少( 螃蟹2 , 第6页 , 重量6 , 抄送2 , 图5C )。 在KO RA样本中,几个基因被表示为经历了正常的H3K27me3丢失和基因激活( 霍克斯b1 , 福克斯1 )经历了与ES细胞状态相关的正常KO RA H3K4me3上调( 图5D )。 然而,ChIP-qPCR确实证实了ChIP-seq中的基因在RA KO H3K4me3中存在缺陷( 螃蟹2 , 重量6 , 图5D )。 我们接下来研究了KO RA H3K4me3受影响的基因是否与H3K27me3的增加相关。 ChIP-qPCR 螃蟹2 和 重量6 证明KO RA H3K27me3增加至ES可比水平( 图5E ).
图5。 一组基因表现出H3K4me3减少,UTX和JMJD3丢失。
(A) UCSC基因组浏览器视图 螃蟹2 , 第6页 , 重量6 、和 抄送2 图中所示为Input(黑色)、WT ES H3K27me3 ChIP(深绿色)、KO ES H3G27me3 ChIP(深红色)、WT-RA H3K17me3 ChIP(浅绿)、KO-RA H3C27me3 ChIP(浅红)、WT-RA H3K4me3 ChIP。 底部标注了ChIP-qPCR检测的区域。 (B) 在WT上执行H3K4me3 ChIP-seq( Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 −TX)或KO( Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 +TX)细胞经RA处理。 通过edgeR比较RA处理细胞中所有启动子(+/-1 KB)的标准化序列读数,以确定KO细胞中H3K4me3减少的启动子。 对数倍变化(logFC)是根据每百万次读取的平均日志计数(平均logCPM)绘制的。 在该图中,161个KO启动子在RA处理后表现出H3K27me3减少(负logFC,FDR<0.05,并且在WT RA细胞中鉴定出H3K4me3 MACS峰)。 (C) 定量RT-PCR Crabp2型 , 第6页 , 重量6 、和 抄送2 从 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞(Diff−)或RA治疗2天后(Diff+)未经治疗(−TX,浅灰色)或预先用他莫昔芬(+TX,黑色)治疗。 N=每次处理3个样品。 所有样本均相对于−TX分化+RA治疗进行了归一化。 表达显著减少(p-vale=*0.01,**0.03,***0.001,****0.004)。 (D) 通过ChIP-qPCR验证KO-RA细胞中H3K4me3的减少。 H3K4me3的ChIP Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞(深绿色,Diff−)或RA治疗2天后(浅绿色或红色,Diff+)未经治疗(绿色)或用他莫昔芬(红色)预处理。 IgG控件ChIP显示为白色条。 H3K4me3阴性基因座(基因沙漠地区, 阴性 )用于与 Npm1号机组 (阳性对照),显示正常KO基因激活的基因( Hoxb1、Foxa1 )和KO H3K4me3减少的基因( Crabp2,重量6 )。 仅限 螃蟹2 和 重量6 证明KO-RA治疗减少(p值=*0.01,**0.07)。 (E) H3K27me3的ChIP 螃蟹2 和 重量6 相对于阴性对照(Slc2a8)。 这两个基因均显示RA KO细胞中H3K27me3增加(浅红色条,p值=*0.003,**0.03)。
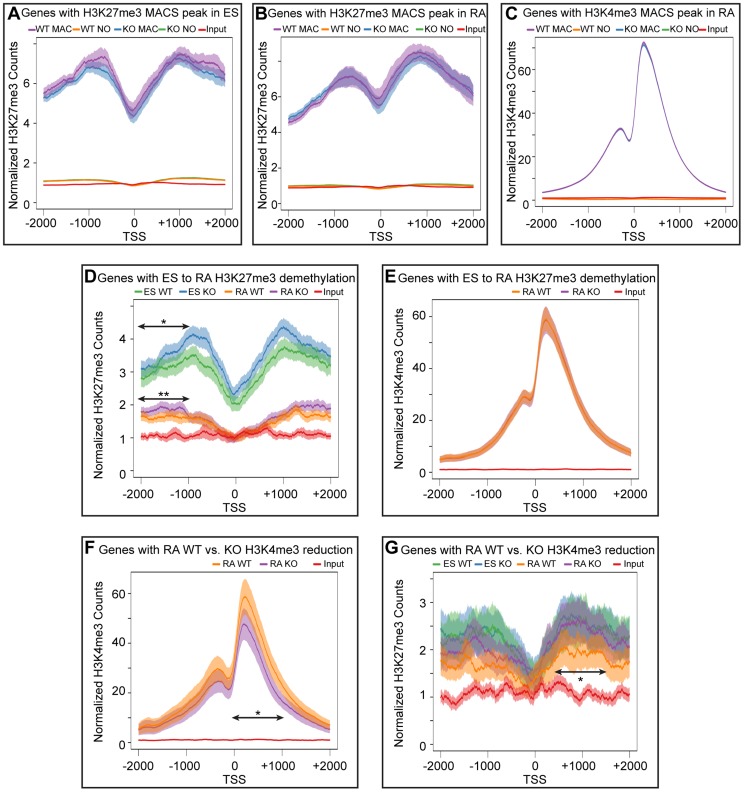
对分类基因亚群的Meta分析显示,在没有KDM6去甲基化的情况下,H3K27me3发生低水平变化 为了更好地分析H3K27me3和K3K4me3的分布,我们进行了一项荟萃分析,以检查这些组蛋白修饰在所有启动子中的总体分布,以及相应的MACS峰。 这些元分析( 图6A-G )以平均归一化读取计数为中心绘制95%置信区间。 ES细胞和RA分化细胞在启动子中都有广泛的K27me3分布,在TSS附近有下降( 图6A、B )。 TSS下游H3K4me3富集达到峰值( 图6C )H3K27me3和H3K4me3的WT和KO剖面之间有非常紧密的重叠。 RA分化后H3K27me3显著降低的基因,在WT和KO的ES和RA样本之间的相对H3K26me3序列读数有明显差异( 图6D )。 在比较WT RA和KO RA时,TSS附近有非常紧密的重叠(+/-1 KB); 然而,TSS上游(−2 KB至−1 KB)KO RA在每个基因的平均H3K27me3水平上表现出显著富集。 同一地区WT ES与KO ES的比较也表明H3K27me3水平显著升高( 图6D )。 虽然这些KO启动子的H3K27me3升高,但H3K4me3分布完全重叠( 图6E ),进一步支持该基因类别在KO-RA细胞中有效激活转录的数据( 图4C )。 因此,随着RA的分化,KO细胞可以在特定启动子处经历H3K27me3的显著降低,尽管TSS上游有少量H3K26me3积累,但转录没有受到影响。
图6。 H3K27me3和H3K4me3在雌性KDM6 WT和KO启动子中分布的荟萃分析。
(A) 荟萃分析绘制了所有具有H3K27me3 MACS峰的雌性KDM6 WT和KO ES启动子相对于所有没有MACS峰的启动子的标准化H3K27me3序列读数和相应的95%置信区间。 基因分布跨越转录起始位点上游的−2000碱基对到下游的+2000碱基对。 (B) 对所有具有H3K27me3 MACS峰值的WT和KO RA启动子进行标准化H3K17me3序列读取,而对所有没有MACS峰的启动子进行检测。 (C) 对所有具有H3K4me3 MACS峰值的WT和KO RA启动子进行标准化H3K4me3序列读取,而对所有没有MACS峰的启动子进行检测。 (D) 经标准化的H3K27me3序列读取edgeR识别的启动子,以经历RA分化的H3K27me3缺失。 图中显示了ES WT和KO与RA WT和GO的对比。 虽然WT和KO-RA计数都有很大下降,但在−1000到−2000年间,KO-ES和KO-RA分别相对于WT-ES和WT-RA略有升高(所有给定启动子的平均值T检验,p值=* 0.036,**0.019)(E)标准化H3K4me3序列读取edgeR识别的启动子,以经历RA分化的H3K27me3丢失。 图中显示了RA WT和KO。 (F) 通过edgeR识别的启动子读取标准化的H3K4me3序列,以在KO RA中相对于WT RA经历H3K4me3缺失。 图中显示了RA WT和KO。 KO RA在0到+1000之间显著降低(p值=*0.009)。 (G) 经标准化的H3K27me3序列读取edgeR识别的启动子,在KO RA中相对于WT RA出现H3K4me3缺失。 图中显示了ES WT和KO与RA WT和GO的对比。 在+500到+1500之间,KO RA相对于WT RA显著升高(p值=*0.040)。
对KO RA细胞中显示H3K4me3减少的启动子的Meta分析证实,该数据集在TSS下游的H3K4me3中显著不足( 图6F )。 该数据集的H3K27me3图谱显示,在WT ES到WT RA的分化过程中,这些基因没有发生显著的K3K27me3丢失( 图6G )。 然而,RA KO相对于RA WT的H3K27me3有一个小而显著的升高,从TSS+0.5 KB到+1.5 KB。 因为从图表中识别一小部分数据用于统计分析相当于樱桃采摘,而且并非没有偏见,所以我们使用edgeR对WT RA和KO RA H3K27me3水平进行了全基因组比较。 WT RA与KO RA的全基因组交叉比较没有发现任何启动子(TSS+/-1 KB)显示KO H3K27me3显著增加。 我们还比较了所有KO RA H3K27me3 MACS峰(峰中心+/-0.5 KB),包括在TSS中未发现的峰,以便在WT RA上进行归一化序列读取富集。 该分析确定了74个KO RA H3K27me3 MACS峰(共4504个MACS峰),这些峰在WT的序列读取中富集( 表S3 )。 这些峰值位于64个独特基因的不同附近; 然而,由于TSS H3K4me3水平降低,这些基因中只有7个表现出转录受损( 表S3 )。 总的来说,随着KDM6去甲基化的丧失,一小部分基因的H3K4me3略有减少,转录也减少,其中一部分基因升高了H3K27me3。
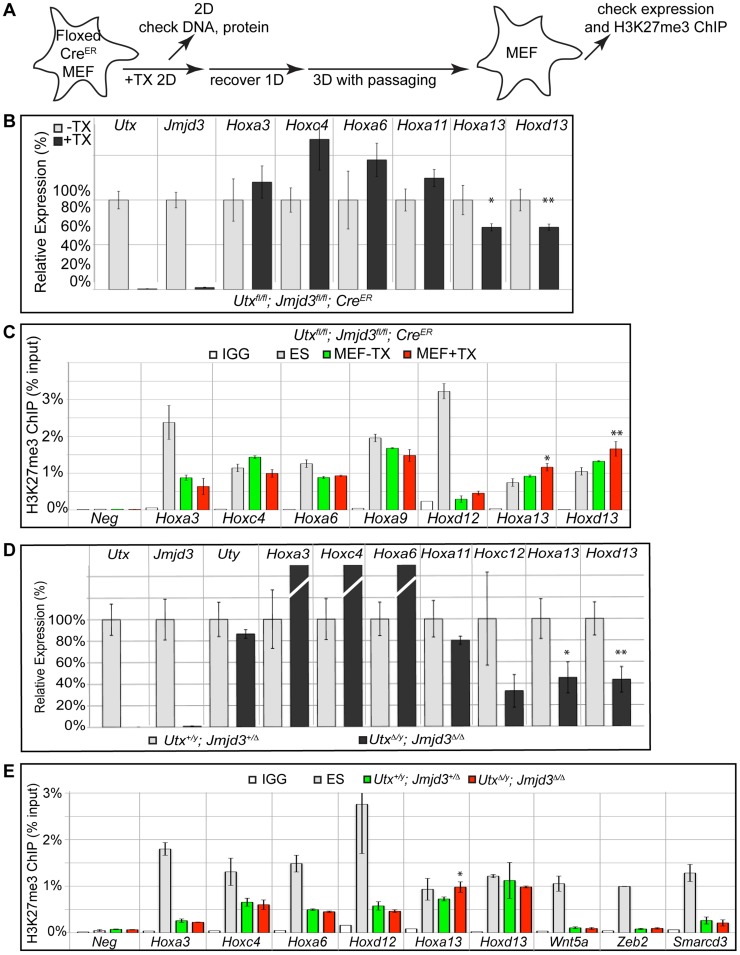
MEF表现出启动子对H3K27me3的KDM6独立损失 为了检测分化的初级组织中H3K27me3阻遏物的丢失,我们利用小鼠胚胎成纤维细胞(MEFs)。 从E13.5培养原代MEF Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 胚胎和三苯氧胺治疗 图7A 相对于ES细胞,代表小组 霍克斯 基因( 霍克萨3 , 霍克斯4 , Hoxa13州 和 霍克斯13 )MEF表达水平升高( 图S8A )。 三苯氧胺治疗后 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 MEF大幅放缓,而无Cre的MEF继续激增。 无论如何, Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 MEFs+TX在很大程度上没有减少 霍克斯 相对于未处理对照的表达( 图7B )。 只有最远端的基因 霍克斯 A和D集群( Hoxa13州 和 霍克斯13 )在UTX和JMJD3缺失的情况下,表达轻微但显著降低。 霍克斯 H3K27甲基化 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 MEFs+TX与它们的表达谱相匹配,因为少数远端基因表现出轻微的表达缺陷( Hoxa13州 和 霍克斯13 )H3K27me3也显著增加( 图7C ).
图7。 RT-PCR和H3K27me3 ChIP Utx和Jmjd3 突变MEF。
(A) MEF TX治疗示意图。 (B) 来自的指示基因的定量RT-PCR Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 小鼠胚胎成纤维细胞(MEF)未经处理(−TX,浅灰色)或预处理TX(+TX,黑色)。 大幅减少 霍克斯 显示表达(T检验p值*=0.05,**=0.02,N=3个样本/处理)。 (C) H3K27me3的ChIP Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 MEF未经处理(绿色)或用TX预处理(红色)。 IgG控制ChIP用白色条表示,ES细胞的H3K27me3 ChIP用浅灰色条表示。 H3K27me3阴性基因座的定量PCR( Slc2a8系列 发起人, 阴性 )用于与 霍克斯 发起人。 显示了MEF+TX相对于−TX的显著H3K27me3积累(T检验p值*=0.01,**=0.04,每次处理N=3个样本)。 (D) 来自的指示基因的定量RT-PCR Utx公司 +/年 ; Jmjd3号机组 +/Δ (浅灰色条)或 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ MEF(黑色条)。 大幅减少 霍克斯 显示了表达(T检验p值*=0.01,**=0.003,N=3个独立的MEF系/治疗)。 (E) H3K27me3的ChIP Utx公司 +/年 ; Jmjd3号机组 +/Δ (绿色条)或 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ MEF(红色条)。 IgG控制ChIP用白色条表示,ES细胞的H3K27me3 ChIP用浅灰色条表示。 H3K27me3阴性基因座的定量PCR( Slc2a8系列 发起人, 阴性 )用于与 霍克斯 基因和其他指示转录因子。 H3K27me3大量累积 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ MEF相对于 Utx公司 +/年 ; Jmjd3号机组 +/Δ 显示MEF(T检验p值*=0.02,N=3个样本/次)。
原代MEF也从E13.5培养 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 胚胎在建立和维持H3K27脱甲基状态中的功能测定。 类似于瞬态TX引起的KDM6损耗, Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ MEF显著降低了更多远端组织的表达 霍克斯 基因( Hoxa13州 , 霍克斯13 , 图7D )相对于 Utx公司 +/年 ; Jmjd3号机组 +/Δ 控制。 H3K27me3的ChIP Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ MEF只显示了 Hoxa13州 而其他 霍克斯 基因未受影响( 图7E )。 值得注意的是,有几个 霍克斯 与ES细胞相比,基因显示H3K27me3水平显著降低( 霍克萨3 , 霍克斯4 , 霍克斯6 , 霍克斯12 )在控制和 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ MEF公司( 图7E )。 一些近端Hox基因实际上显示KO MEF增加 霍克斯 表达式( 霍克萨3 , 霍克斯4 和 霍克斯6 ),但这可能是这些细胞生长速度下降的伪影,因为这些基因的H3K27me3谱不受影响。 此外,一些其他转录因子( Wnt5a型 , Zeb2公司 , Smarcd3型 )也表现出H3K27me3几乎完全丧失,即使在整个胚胎发育过程中所有的KDM6去甲基化酶都被去除了。 值得注意的是,即使H3K27me3总蛋白水平,这些基因也会失去局部的H3K17me3( 图S3G,H )和EZH2水平( 图S8B、C )升高(H3K4me3水平未受影响, 图S8C )。 因此,H3K27me3抑制基因可以在没有KDM6脱甲基酶的情况下建立清除该抑制染色质的启动子状态。
讨论 H3K27脱甲基酶领域存在巨大的二分法。 H3K27me3会导致整个早期胚胎中的基因抑制,但催化其去除的酶对雄性胚胎的生存能力并不是必需的。 这些发现出乎意料,因为许多基因对早期胚胎原肠胚形成事件至关重要 [43] —— [52] 在开发过程中经历H3K27me3去抑制 [4] , [53] , [54] 包括但不限于GATA、TGF-β/BMP、WNT、FGF和T-box转录因子网络。 细胞培养模型系统表明UTX和JMJD3在激活这些途径中发挥作用 [17] —— [19] , [22] , [32] 。我们现在演示 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 缺乏所有KDM6去甲基化的胚胎显著存活至足月,并在妊娠中期表现正常。 Utx公司 Δ/Δ ; Jmjd3号机组 Δ/Δ 胚胎(缺乏UTY的脱甲基酶非依赖性功能)通过原肠胚形成存活,尽管体积较小,但可以发育E10.5特征。 因此,KDM6对于减轻早期胚胎原肠胚形成所需基因的H3K27me3阻遏作用并不重要。
即使在单个细胞和生物体模型中,也有几项研究产生了相互矛盾的报告。 据报道,UTX介导的H3K27去甲基化在细胞重编程和生殖细胞发育中起作用 [55] ,但还活着 Utx公司 突变雄性小鼠可以生育 [31] , [56] 据报道,UTX对于雄性ES细胞分化中生殖层标记的适当表达至关重要 [19] , [56] 然而,分化缺陷可以通过UTY或催化无效的UTX形式得到很大程度的缓解 [32] , [57] .UTX对于高效 霍克斯 H3K27me3脱甲基和基因激活 [27] , [29] , [30] , [57] , [58] 然而,Utx阴性男性ES细胞可以在很大程度上清除 霍克斯 H3K27me3并显示正常转录激活 [56] 这些报告中的差异可能是由于细胞类型、遗传背景、ES细胞克隆的内在生长差异、差异JMJD3冗余或差异UTY表达的差异[如已报道的那样 [31] , [32] , [56] , [59] 我们利用突变诱导等位基因来比较相同ES细胞克隆中具有相同生长速率和遗传背景的整个KDM6家族的控制和敲除。 与中期妊娠的正常外观相似 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 胚胎中,KDM6突变雄性ES细胞能正常分化为所有EB胚层。 KDM6去甲基化无效的突变雌性ES细胞表明,H3K27me3的全球水平(有EB分化)和H3K17me3的局部水平从近端显著降低 霍克斯 簇和其他转录因子的启动子(RA分化)。 虽然在RA KO细胞中这些启动子上游有低水平的显著H3K27me3积累,但这些基因大部分被清除,并经历了正常的转录激活,与 Utx公司 男性淘汰研究 [56] . Utx公司 和 Jmjd3号机组 突变MEFs显示H3K27me3轻度积聚,仅在细胞的最远端区域表达减少 霍克斯 集群。 类似地,斑马鱼UTX功能的丧失会导致远端的中度缺陷 霍克斯 表达 [27] EZH2蛋白水平在 6千马克 MEF突变,可能是远端改变的原因 霍克斯 基因调控。 相对于ES细胞, Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ MEF显示了几个Hox基因和发育转录因子的启动子H3K27me3的显著降低。 因此,在没有KDM6 H3K27去甲基化的情况下,H3K27me3损失可以在发育情况下启动和维持。
我们的研究提出了关于H3K27me3早期胚胎切除的有趣问题。 到目前为止,只有UTX和JMJD3证明有能力去甲基化H3K27me3。 另一种JmjC蛋白不太可能去甲基化H3K27me3。 包括JHDM1D和PHF8在内的KDM7家族能够去甲基化H3K9和H3K27二甲基残基,但不能去甲基化三甲基残基 [60] , [61] PHF8活性位点不能在空间上容纳三甲基残基 [62] 相反,UTX将H3K27me3定位在离活性位点更远的位置,以正确定位较大的残基修饰 [63] 此外,UTX氨基酸Y1135与甲基H3K27me3键合,对去甲基化至关重要 [31] , [63] 该残基在KDM7家族中不保守。 该位置的酪氨酸对于H3K9和H3K36三甲基脱甲基酶的KDM4家族成员是保守的。 然而,这一蛋白质家族有一个深口袋内的催化核心,H3K27下游的残基编码的灵活性不足以适应活性位点的这种修饰 [64] 一个新的蛋白质家族可能利用不同的化学性质主动去甲基化H3K27me3。
或者,早期胚胎中的H3K27me3可以被被动机制取代,因为组蛋白可以在每个细胞周期内多次翻转 [65] PRC复合物在DNA复制过程中与染色质保持结合,并与分裂细胞中的复制叉结合,以在新并入的子链组蛋白上直接甲基化H3K27me3 [66] —— [68] 因此,在H3K27me3替代的被动模型中,复制过程中PRC2复合物的置换允许纳入未甲基化的H3K27。 以类似的方式,小鼠植入前胚胎和生殖系中的DNA甲基化可以通过被动的复制依赖机制,通过DNA甲基转移酶从复制位点转移来消除 [69] , [70] .
KDM6系列在开发中的作用尚不明确。 被动去除H3K27me3可能在快速分裂的细胞中占主导地位,例如在早期胚胎中。 活性H3K27me3脱甲基可能对快速响应特定环境或发育线索更为重要,尤其是在更为静态的细胞群体中。 或者,H3K27去甲基化酶可能起到微调转录活性的作用,而不是促进剧烈的基因诱导,从而促进基因表达的准确稳健的时间和空间模式。 因此,UTY与广泛的染色质和转录机制相关,可以促进适当的基因表达输出 [31] 在这个意义上,KDM6成员可能编码一个阅读器功能,以招募转录复合物来抑制基因和/或取代PRC2,而无需主动去甲基化。 UTX和JMJD3催化域中的点突变进一步强调了KDM6家族的脱甲基酶独立作用 [32] , [71] , [72] 展望未来,需要进行分析染色质修饰因子之间串扰的遗传实验和哺乳动物胚胎内的结构/功能分析,以确定KDM6家族在胚胎发育中的特定功能。
材料和方法 老鼠 所有小鼠实验程序均获得北卡罗来纳大学动物护理和使用委员会的批准。 这个 Utx公司 佛罗里达州 描述了等位基因 [31] Jmjd3号机组 tm1标记 ( Jmjd3号机组 佛罗里达州 )通过靶向E14 ES细胞获得等位基因。 这个 Jmjd3号机组 通过BAC重组产生靶向结构,将LoxP位点插入内含子13,将FRT-Neomycin-FRT-LoxP盒插入 Jmjd3号机组 成功靶向后,通过电穿孔pCAGG-FLP构建物去除新霉素盒。 产生的结果 Jmjd3号机组 +/飞行 将ES细胞注射到C57BL/6J胚泡中。 结果嵌合体与CD1雌性交配以评估种系传播,并保持在混合CD1背景或回交到C57BL/6J。 Utx公司 Δ 和 Jmjd3号机组 Δ 等位基因是通过将floxed等位基因与 瓦萨克里 限制生殖系Cre活性的转基因 [73] 然后将这些后代交配以繁殖 Utx公司 Δ 和 Jmjd3号机组 Δ 等位基因。 为了在 Utx Jmjd3公司 遗传互作杂交, Utx公司 +/Δ ; Jmjd3号机组 +/Δ 雌性小鼠与其中一种交配 Utx公司 飞行/飞行 ; Jmjd3号机组 fl/Δ ; 瓦萨克里 或 Utx公司 +/年 ; Jmjd3号机组 fl/Δ ; 瓦萨克里 男性。 从卵黄囊样本中对胚胎进行PCR基因分型 Utx公司 或 Jmjd3号机组 并通过PCR基因分型方案进行性别鉴定 Utx公司 从 尤蒂 中列出了所有引物序列 表S4 .
细胞培养
Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 和 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞系是利用E3.5囊胚在杂交中产生的 CAGGCre-ER公司 转基因小鼠系 [41] ES细胞按所述进行培养 [36] 将ES细胞从饲养者MEF中分离出来,用1µg/mL 4-羟基三苯氧胺(4-OHT)处理3天,然后恢复1天。 在EB分化实验中,10 6 在琼脂糖包被的培养皿上,将ES细胞培养在10 mL不含LIF的ES培养基中。 用25µL滴ES细胞以20000细胞/mL的浓度建立悬滴EB。在RA分化实验中,ES细胞在三苯氧胺回收后被镀上,第二天在1µM维甲酸中培养不含LIF的ES细胞。 E13.5 MEF按说明生成 [31] 将MEF传代1次,用0.5µM 4-OHT处理2天,然后再传代培养3天。
RT-PCR、western blotting和ChIP 用Trizol分离RNA,用Multiscribe逆转录酶合成cDNA。 采用qRT-PCR(Bio-Rad SsoFast EvaGreen,CFX96实时系统)分析基因表达。 所有RT-PCR均归一化为 Gapdh公司 与对照样品相关的表达式和图形。 所有引物序列列于 表S4 如所述进行核裂解物、组蛋白提取物和蛋白质印迹 [31] 使用抗RBBP5(Bethyl Labs A300-109A,1∶5000)、抗ASH2L(Bethyl Labs A300-107A,1∶3000)、抗H3K27me3(Millipore 07-449,1∶2000)、抗H3(Abcam ab1791,1∶10000)、抗GAPDH(Sigma G9545,1∶10000)、抗UTX [29] 或抗UTX(Bethyl Labs A302-374A,1∶4000)抗体。 按照所述执行ChIP [74] 并绘制每个免疫沉淀的ChIP总输入DNA的百分比。 5×10 6 电池由Branson Sonifier以15%的占空比(0.7 s开启0.3 s关闭)进行声波处理。 在一些实验中,在冷水浴中用生物破坏者超声发生器在高设置下对染色质进行30 s的超声处理,休息60 s。使用兔IgG(Sigma,I5006)、抗H3K27me3(Abcam ab6002,2.5µl)、抗-H3K4me3(Abcam ab8580,2µl。 所有ChIP引物均列于 表S4 .免疫荧光实验按所述进行 [31] 抗H3K27me3(细胞信号9733S,1∶500)或ISL1(DSHB 39.4D5-S,1:200)
支持信息
图S1 靶向突变 Jmjd3号机组 .(A) Jmjd3号机组 目的是在第13内含子和第20内含子中引入LoxP站点。 用FLP重组酶去除Neo盒后,FRT位点仍然存在。 JMJD3蛋白的示意图如上所示,表示将用Cre重组酶去除的区域。 从外显子13-21剪接将引入移码和终止密码子。 (B) 验证 Jmjd3号机组 佛罗里达州 等位基因。 WT的Southern印迹和靶向 Jmjd3号机组 +/neofl公司 具有3′探针和XmnI消化物的ES细胞由于一个新的限制性位点而显示出预期的条带转移。 通过转染Flp重组酶从靶向ES细胞中移除新盒,以创建 Jmjd3号机组 +/佛罗里达州 .(C) Jmjd3号机组 佛罗里达州 /佛罗里达州 将小鼠与生殖系Cre重组酶杂交以产生 Jmjd3号机组 Δ/Δ 设计了PCR基因分型方案来区分WT、, Jmjd3号机组 佛罗里达州 、和 Jmjd3号机组 Δ 结果小鼠的等位基因。 (D) Jmjd3号机组 E18.5全胚RNA的RT-PCR证实了缺失。 Jmjd3号机组 Δ/Δ 胚胎缺乏外显子14-17产物,外显子13-22之间的扩增产生一个较小的带,对应于缺少外显子14–20的预期产物。 因此,突变转录物是稳定的,预计会产生缺少JmjC组蛋白去甲基化酶结构域的JMJD3。 (E) 纯合子 Jmjd3号机组 突变胚胎出生了,但无法呼吸,因为它们的蓝色。 (F) Jmjd3号机组 Δ/Δ 胚胎在E10.5时表现正常。
(畅通节能法)
图S2 UTX和JMJD3的母体缺失不会增强胚胎突变表型。 (A) Utx公司 fl/Δ ; Jmjd3号机组 fl/Δ ; 瓦萨 Cre公司 雌性小鼠(卵母细胞缺失 Utx公司 和 Jmjd3号机组 )与 Utx公司 飞行/飞行 ; Jmjd3号机组 fl/Δ ; 瓦萨 Cre公司 雄性小鼠(精子携带缺失 Utx公司 和 Jmjd3号机组 )在E10处解剖了杂交后代的胚胎。 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ (A′)和 Utx公司 Δ/Δ ; Jmjd3号机组 Δ/Δ (A〃)来自UTX和JMJD3母体贡献的杂交胚胎( 图1D、E )。 (B) 的基因分型 Utx公司 和 Jmjd3号机组 胚胎在 图S2A 以证明 Utx公司 和 Jmjd3号机组 floxed(fl)等位基因缺失(Δ)。
(畅通节能法)
图S3 中期妊娠分析 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 雄性胚胎。 (A、B)KDM6成员的定量RT-PCR(A, Utx公司 = 浅灰色, Jmjd3号机组 = 深灰色, 尤蒂 = 黑色)和指示 霍克斯 基因(B, 霍克斯4 = 浅灰色, 霍克斯6 = 深灰色, Hoxa13州 = 黑色)E10.5公螺纹的所有指定组合 Utx公司 和 Jmjd3号机组 相对于 Utx公司 +/年 ; Jmjd3号机组 +/Δ 对照组(每个基因型N≥4个样本)。 (C) 组蛋白提取自 Utx公司 +/年 ; Jmjd3号机组 +/Δ 或 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ H3K27me3相对于总H3负荷控制的胚胎和荧光蛋白印迹图。 (D) C部分的western blot定量,H3k27me3值归一化为总H3,以计算H3k27me3%。 (E) E10.5的H3K27me3免疫荧光 Utx公司 +/年 ; Jmjd3号机组 +/Δ 或 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 心肌。 (F) E10.5的H3K27me3免疫荧光 Utx公司 +/年 ; Jmjd3号机组 +/Δ 或 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 脊髓近端ISL1阳性运动神经元。 (G) 组蛋白提取自 Utx公司 +/年 ; Jmjd3号机组 +/Δ 或 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ H3K27me3相对于总H4负荷控制的MEF线和荧光蛋白印迹图。 (H) H3K27me3%蛋白质印迹定量,来自 Utx公司 +/年 ; Jmjd3号机组 +/Δ (灰色)或 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ (黑色)MEF相对于总H4。 蛋白质水平显著增加(*p值=0.05)。
(畅通节能法)
图S4 他莫昔芬的疗效 Cre公司 急诊室 导入 Utx公司 和 Jmjd3号机组 悬浮ES细胞系。 (A) A的PCR基因分型 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞株未经治疗(−TX)或接受他莫昔芬治疗2天(+TX) Utx公司 , Jmjd3号机组 ,性别和Cre的存在。 对照PCR反应包括 Utx公司 或 Jmjd3号机组 floxed等位基因( 佛罗里达州 ), Utx公司 或 Jmjd3号机组 缺失等位基因( Δ )、男性DNA(男性)、女性DNA(女性)、Cre阴性DNA(阴性)、Cre-阳性DNA(阳性)、水(H)。 (B) 一种蛋白质印迹 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞系未经治疗(−TX)或接受他莫昔芬治疗2天(+TX) Utx公司 GT1/年 UTX(αUTX)或加载控制(αGAPDH)的ES线。 这个 Utx公司 GT1/年 线应捕获所有 Utx公司 产品。 因此,在140KD的所有泳道中存在的带是非特异性带,而不是替代产物,因为它在 Utx公司 GT1/年 样品。 (C) 第B部分中描述的3条线路的RT-PCR Utx公司 被floxed等位基因(Exon 3)和JmjC结构域删除的区域。 请注意,包含JmjC域的所有转录本在 Utx公司 GT1/年 RNA。 (D) 使用第二个独立UTX抗体进行Western blot。
(畅通节能法)
图S5 悬垂EB分析和本构删除 Utx公司 和 Jmjd3号机组 (A)作为ES细胞大规模培养中EB形成的一种替代方法,悬滴EB是从定义的滴体积中的定义细胞数生成的。 (B) 荧光western blot分析H3K27me3随EB分化的丢失。 H3K27me3相对于总H4被印迹。 (C) 印迹定量 图S5B H3K27me3%是在构成性长期缺失后相对于总H4(D)分化绘制的 Utx公司 和 Jmjd3号机组 . Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 用TX处理ES细胞3天,然后在低密度下进行电镀,以便挑选单个细胞集落。 的克隆 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 细胞增殖3周并传代数代,然后分化为相对于亲本的典型第4天EB结构 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 行。 (E) 中描述的ES细胞(diff−)和第8天EB(diff+)的表达分析 图S5D 对于 Utx公司 , Jmjd3号机组 , Gata6公司 (内胚层),以及 法兰1 (中胚层)。 (F) Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞也用TX处理以产生单细胞克隆(如 图S5D )和 Utx公司 Δ/Δ ; Jmjd3号机组 Δ/Δ ES细胞(Diff−)用RA分化2天(Diff+),RT-PCR比较 Utx公司 , Jmjd3号机组 , 霍克萨1 、和 霍克斯b1 相对于父母 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 行。
(畅通节能法)
图S6 UCSC基因组浏览器视图 霍克斯布 , 霍克斯 、和 霍克斯 集群。 (A–C)UCSC基因组浏览器视图 霍克斯 (A) , 霍克斯 (B) 、和 霍克斯 (C) ,集群。 图中所示为输入(黑色)、WT ES H3K27me3 ChIP(深绿色)、KO ES H3G27me3 ChIP(深红色)、WT-RA H3K17me3 ChIP(浅绿色)、KI RA H3K24me3 ChIP(浅红色)、WI RA H3Ch4me3 ChIP。
(畅通节能法)
图S7 中MLL和PCR2复合物的分析 Utx公司 和 Jmjd3号机组 突变细胞。 (A) MLL复合物成员ASH2L和RBBP5的Western blot分析水平 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞−TX或+TX。(B)WT ES细胞、2天RA分化的ES细胞或2天分化的EB中PRC2组分EZH2和RBBP5的Western blot水平。 (C) EZH2 ChIP-qPCR Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞(深绿色,Diff−)或RA治疗2天后(浅绿色或红色,Diff+)未经治疗(绿色)或用他莫昔芬(红色)预处理。 IgG控件ChIP显示为白色条。 EZH2阴性基因座的定量PCR( Npm1号机组 , 阴性 )用于与 罕见 , 霍克萨1 , 霍克斯州2 , 霍克斯b1 , 霍克斯b2 、和 霍克斯德9 .
(畅通节能法)
图S8 分析 Utx公司 和 Jmjd3号机组 突变MEF。 (A) 的RT-PCR 霍克萨3 , 霍克斯4 , Hoxa13州 ,或 Hoxd13型 在ES细胞、视黄酸处理的ES细胞或MEFs中。 (B) EZH2相对于RBBP5负荷控制的Western blot Utx公司 +/年 ; Jmjd3号机组 +/Δ 或 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ MEF公司。 (C) EZH2或H3K4me3的western blot定量 Utx公司 +/年 ; Jmjd3号机组 +/Δ (灰色)或 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ (黑色)MEF。 蛋白质水平显著增加(*p值=0.04)。
(畅通节能法)
表S1 ES到RA分化中H3K27me3缺失的启动子。 在TSS+/-1 KB范围内,WT RA相对于WT ES(表1)和KO RA相对于KO ES(图2)中H3K27me3归一化序列显著缺失(FDR<0.05)的EdgeR统计比较。 一些基因有多个可供选择的启动子,因此列表中重复的基因以红色突出显示。还表示启动子是否具有相应的RA H3K4me3 MACS峰值(列为1)。
(XLSX)
表S2 KO-RA分化中H3K4me3减少的启动子。 在TSS+/-1 KB范围内,KO RA相对于WT RA中H3K4me3归一化序列读数的显著丢失(FDR<0.05)的EdgeR统计比较。 一些基因有多个备选启动子,因此列表中重复的基因以红色突出显示。也表示启动子是否有相应的WT或KO ES H3K27me3 MACS峰(列为1)。
(XLSX)
表S3 通过WT RA读取H3K27me3序列中富集的KO RA H3K17me3 MACS峰。 在KO RA MACS峰值中H3K27me3归一化序列读数相对于穿过KO RA峰值中心的WT RA显著增加(FDR<0.05)的EdgeR统计比较+/-0.5 KB。 MACS峰以最近的相邻基因列出。 一些基因与多个MACS峰相关,因此列表中重复的基因以红色突出显示。还表示该基因的启动子是否相应减少KO RA H3K4me3(列为1)。
(XLSX)
致谢 我们要感谢马格努森实验室对这份手稿的审查,感谢克里斯蒂安·赫林对UTX抗体的慷慨贡献。
资金筹措表 这项工作得到了NIH R01GM101974(TM)和NRSA博士后研究金GM087905(KBS)的支持。 资助者在研究设计、数据收集和分析、决定出版或编写手稿方面没有任何作用。
工具书类
1 Azuara V、Perry P、Sauer S、Spivakov M、Jorgensen HF等(2006)多能干细胞系的染色质特征。 Nat细胞生物学 8: 532–538. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
2 Bernstein BE、Mikkelsen TS、Xie X、Kamal M、Huebert DJ等(2006)二价染色质结构标志着胚胎干细胞中的关键发育基因。 单元格 125: 315–326. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
三。 Ku M、Koche RP、Rheinbay E、Mendenhall EM、Endoh M等(2008)PRC1和PRC2占用的全基因组分析确定了两类二价结构域。 公共科学图书馆-基因 4:e1000242。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
4 Mikkelsen TS、Ku M、Jaffe DB、Issac B、Lieberman E等(2007)多能干细胞和谱系提交细胞染色质状态的基因组全图。 自然 448: 553–560. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
5 Rugg-Gunn PJ、Cox BJ、Ralston A和Rossant J(2010),干细胞系和早期小鼠胚胎组织谱系中的组蛋白修饰。 美国国家科学院程序 107: 10783–10790. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
6 Sachs M、Onodera C、Blaschke K、Ebata KT、Song JS等(2013)小鼠胚胎生殖系体内的双价染色质标记发育调控基因。 单元格代表 3:1777–84 数字对象标识: 2016年10月10日/j.celrep.2013.04.032 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
7 Hammoud SS,Nix DA,Zhang H,Purwar J,Carrell DT,et al.(2009)人类精子中的独特染色质包裹胚胎发育基因。 自然 460: 473–478. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
8 Lindeman LC,Andersen IS,Reiner AH,Li N,Aanes H,et al.(2011)合子基因组激活前通过修饰组蛋白制备发育基因表达。 开发人员单元格 21: 993–1004. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
9 Dahl JA、Reiner AH、Klungland A、Wakayama T、Collas P(2010)发育调控启动子上的组蛋白H3赖氨酸27甲基化不对称区分了小鼠植入前胚胎中的前两个谱系。 公共科学图书馆一号 5:e9150。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
10 Alder O、Lavial F、Helness A、Brookes E、Pinho S等(2010)Ring1B和Suv39h1描绘了早期小鼠谱系承诺期间二价基因的不同染色质状态。 开发 137: 2483–2492. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
11 Cui K,Zang C,Roh TY,Schones DE,Childs RW,et al.(2009)多能人造血干细胞中的染色质特征表明二价基因在分化过程中的命运。 细胞干细胞 4: 80–93. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
12 van Arensbergen J、Garcia Hurtado J、Moran I、Maestro MA、Xu X等人(2010)胰腺器官发生过程中多梳靶点的抑制使产生胰岛素的β细胞能够采用神经基因活性程序。 基因组研究 20: 722–732. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
13 Roh TY,Cuddapah S,Cui K,Zhao K(2006)人类T细胞组蛋白修饰的基因组景观。 美国国家科学院程序 103: 15782–15787. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
14 Zhao XD,Han X,Chew JL,Liu J,Chiu KP,et al.(2007)组蛋白H3 Lys4和27个三甲基化的全基因组定位揭示了人类胚胎干细胞中不同的基因组分室。 细胞干细胞 1: 286–298. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
15 Pan G,Tian S,Nie J,Yang C,Ruotti V,et al.(2007)人类胚胎干细胞组蛋白H3赖氨酸4和赖氨酸27甲基化的全基因组分析。 细胞干细胞 1: 299–312. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
16 Wang AH、Zare H、Mousavi K、Wang C、Moravec CE等(2013)组蛋白伴侣Spt6协调组蛋白H3K27去甲基化和肌生成。 欧洲工商管理硕士J 32: 1075–1086. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
17 Kartikasari AE,Zhou JX,Kanji MS,Chan DN,Sinha A,et al.(2013)组蛋白脱甲基酶Jmjd3依次与转录因子Tbx3和Eomes结合,以驱动内胚层分化。 欧洲工商管理硕士J 32: 1393–1408. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
18 Ramadoss S,Chen X,Wang CY(2012)组蛋白去甲基化酶KDM6B促进上皮-间质转化。 生物化学杂志 287: 44508–44517. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
19 Jiang W,Wang J,Zhang Y(2012)组蛋白H3K27me3脱甲基酶KDM6A和KDM6B通过调节WNT信号通路调节人类ESC的最终内皮分化。 单元格Res 23: 122–130. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
20 Wang JK,Tsai MC,Poulin G,Adler AS,Chen S,et al.(2010)组蛋白去甲基化酶UTX实现RB依赖性细胞命运控制。 基因开发 24: 327–332. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
21 Seenundun S,Rampalli S,Liu QC,Aziz A,Pali C,et al.(2010)UTX在肌肉发生过程中调节肌肉特异性基因H3K27me3的去甲基化。 欧洲工商管理硕士J 29: 1401–1411. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
22 Burgold T、Spreafico F、De Santa F、Totaro MG、Prosperini E等(2008)组蛋白H3赖氨酸27特异性脱甲基酶Jmjd3是神经承诺所必需的。 公共科学图书馆一号 3:e3034。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
23 Satoh T、Takeuchi O、Vandenbon A、Yasuda K、Tanaka Y等(2010)Jmjd3-Irf4轴调节M2巨噬细胞极化和宿主对蠕虫感染的反应。 自然免疫 11: 936–944. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
24 Sen GL、Webster DE、Barragan DI、Chang HY、Khavari PA(2008)组蛋白脱甲基酶JMJD3对自我更新哺乳动物组织分化的控制。 基因开发 22: 1865–1870. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
25 Barradas M,Anderton E,Acosta JC,Li S,Banito A等人(2009)组蛋白去甲基酶JMJD3通过致癌RAS对INK4a/ARF的表观遗传学控制做出贡献 23:1177-1182。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
26 Agger K、Cloos PA、Rudkjaer L、Williams K、Andersen G等(2009)H3K27me3脱甲基酶JMJD3有助于激活INK4A-ARF基因座,以应对癌基因和应激诱导的衰老。 基因开发 23: 1171–1176. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
27 Lan F,Bayliss PE,Rinn JL,Whetstine JR,Wang JK,et al.(2007)组蛋白H3赖氨酸27脱甲基酶调节动物的后部发育。 自然 449: 689–694. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
28 De Santa F、Totaro MG、Prosperini E、Notarbarolo S、Testa G等(2007)组蛋白H3赖氨酸-27脱甲基酶Jmjd3将炎症与抑制多梳介导的基因沉默联系起来。 单元格 130: 1083–1094. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
29 Agger K、Cloos PA、Christensen J、Pasini D、Rose S等(2007)UTX和JMJD3是参与HOX基因调控和发育的组蛋白H3K27脱甲基酶。 自然 449: 731–734. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
30 Lee MG、Villa R、Trojer P、Norman J、Yan KP等(2007)H3K27脱甲基调节多梳招募和H2A泛素化。 科学类 318: 447–450. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
31 Shpargel KB、Sengoku T、Yokoyama S、Magnuson T(2012)UTX和UTY证明了组蛋白去甲基化酶在小鼠胚胎发育中的非依赖性功能。 公共科学图书馆-基因 8:e1002964。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
32 Wang C,Lee JE,Cho YW,Xiao Y,Jin Q,et al.(2012)UTX独立于H3K27脱甲基酶活性调节胚胎干细胞的中胚层分化。 美国国家科学院程序 109: 15324–15329. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
33 Hong S,Cho YW,Yu LR,Yu H,Veenstra TD,et al.(2007)鉴定JmjC结构域UTX和JMJD3为组蛋白H3赖氨酸27脱甲基酶。 美国国家科学院程序 104: 18439–18444. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
34 Walport LJ、Hopkinson RJ、Vollmar M、Madden SK、Gileadi C等(2014)人类UTY(KDM6C)是一种雄性特异性N-甲基赖氨酸-Demethylase。 生物化学杂志 289: 18302–18313. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
35 Burgold T、Voituron N、Caganova M、Tripathi PP、Menuet C等(2012)H3K27脱甲基酶JMJD3是维持胚胎呼吸神经网络、新生儿呼吸和存活所必需的。 单元格代表 2: 1244–1258. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
36 Chamberlain SJ,Yee D,Magnuson T(2008)多梳抑制复合物2对于维持胚胎干细胞多能性是不可或缺的。 干细胞 26: 1496–1505. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
37 Faust C,Schumacher A,Holdener B,Magnuson T(1995)。种子突变破坏小鼠前中胚层的产生。 开发 121: 273–285. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
38 Pasini D、Bracken AP、Jensen MR、Lazzerini Denchi E、Helin K(2004)Suz12对小鼠发育和EZH2组蛋白甲基转移酶活性至关重要。 欧洲工商管理硕士J 23: 4061–4071. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
39 O'Carroll D、Erhardt S、Pagani M、Barton SC、Surani MA等(2001)多梳组基因Ezh2是小鼠早期发育所必需的。 分子细胞生物学 21: 4330–4336. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
40 Copur O,Muller J(2013)组蛋白H3-K27脱甲基酶Utx以时间限制的方式调节果蝇中HOX基因的表达。 开发 140: 3478–3485. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
41 Hayashi S,McMahon AP(2002)通过三苯氧胺诱导的Cre形式在不同组织中进行有效重组:一种用于小鼠中暂时调节基因激活/失活的工具。 求文献一篇 244: 305–318. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
42 Walker E,Chang WY,Hunkapiller J,Cagney G,Garcha K,et al.(2010)Polycomb-like 2与PRC2相关,并在小鼠胚胎干细胞自我更新和分化过程中调节转录网络。 细胞干细胞 6: 153–166. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
43 Zhang H,Bradley A(1996)BMP2缺乏的小鼠无法存活,并且在羊膜/绒毛膜和心脏发育方面存在缺陷。 开发 第122页:2977–2986页。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
44 Meyers EN,Lewandowski M,Martin GR(1998)通过Cre和Flp介导的重组产生的Fgf8突变等位基因系列。 自然基因 18: 136–141. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
45 Molkentin JD,Lin Q,Duncan SA,Olson EN(1997)转录因子GATA4对心脏管形成和腹侧形态发生的要求。 基因开发 11: 1061–1072. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
46 Morrisey EE,Tang Z,Sigrist K,Lu MM,Jiang F,et al.(1998)GATA6调节HNF4,是小鼠胚胎内脏内胚层分化所必需的。 基因开发 12: 3579–3590. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
47 Arnold SJ、Hofmann UK、Bikoff EK、Robertson EJ(2008),中胚层蛋白在小鼠轴形成、上皮-间充质转变和内胚层规范中的关键作用。 开发 135: 501–511. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
48 Russ AP、Wattler S、Colledge WH、Aparicio SA、Carlton MB等(2000)小鼠滋养层发育和中胚层形成需要Eomesodermin。 自然 404: 95–99. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
49 Herrmann BG(1991)Brachyury基因在全山TWis/TWis突变胚胎中的表达模式。 开发 第113页:913–917页。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
50 Winner G,Blessing M,Labosky PA,Hogan BL(1995)骨形态发生蛋白-4是小鼠中胚层形成和图案形成所必需的。 基因开发 9: 2105–2116. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
51 Liu P、Wakamiya M、Shea MJ、Albrecht U、Behringer RR等(1999)脊椎动物轴形成中Wnt3的要求。 自然基因 22: 361–365. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
52 Carver EA,Jiang R,Lan Y,Oram KF,Gridley T(2001)小鼠蜗牛基因编码上皮-间质转化的关键调节因子。 分子细胞生物学 21: 8184–8188. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
53 Xie W,Schultz MD,Lister R,Hou Z,Rajagopal N,et al.(2013)人类胚胎干细胞多系分化的表观基因组分析。 单元格 153: 1134–1148. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
54 Gifford CA、Ziller MJ、Gu H、Trannell C、Donaghey J等(2013)《人类胚胎干细胞规范期间的转录和表观遗传动力学》。 单元格 153: 1149–1163. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
55 Mansour AA,Gafni O,Weinberger L,Zviran A,Ayyash M,et al.(2012)H3K27脱甲基酶Utx调节体细胞和生殖细胞表观遗传重编程。 自然 488: 409–413. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
56 Welstead GG、Creyghton MP、Bilodeau S、Cheng AW、Markoulaki S等(2012年)X-linked H3K27me3去甲基酶Utx是以性别特异的方式进行胚胎发育所必需的。 美国国家科学院程序 109: 13004–13009. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
57 Morales Torres C,Laugesen A,Helin K(2013)Utx是胚胎干细胞分化过程中正确诱导外胚层和中胚层所必需的。 公共科学图书馆一号 8:e60020。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
58 Shahhoseini M、Taghizadeh Z、Hatami M、Baharvand H(2013)人类胚胎干细胞神经分化过程中聚集HOX基因的维甲酸依赖性组蛋白3去甲基化。 生物化学细胞生物学 91: 116–122. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
59 Lee S、Lee JW、Lee SK(2012)UTX,组蛋白H3-赖氨酸27脱甲基酶,作为激活心脏发育程序的关键开关。 开发人员单元格 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
60 Huang C,Xiang Y,Wang Y,Li X,Xu L,et al.(2010)双特异性组蛋白脱甲基酶KIAA1718(KDM7A)通过FGF4调节神经分化。 单元格Res 20: 154–165. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
61 Loenarz C,Ge W,Coleman ML,Rose NR,Cooper CD,et al.(2010)PHF8,一个与唇腭裂和精神发育迟滞相关的基因,编码Nepsilon-二甲基赖氨酸脱甲基酶。 人类分子遗传学 19: 217–222. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
62 Yu L,Wang Y,Huang S,Wang J,Deng Z,et al.(2010)新型组蛋白脱甲基酶PHF8的结构见解。 单元格Res 20:166–173。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
63 Sengoku T,Yokoyama S(2011)通过UTX/KDM6A进行组蛋白H3-Lys-27去甲基化的结构基础。 基因开发 25: 2266–2277. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
64 Chen Z,Zang J,Kappler J,Hong X,Crawford F,et al.(2007)JMJD2A识别甲基化组蛋白尾部的结构基础。 美国国家科学院程序 104: 10818–10823. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
65 Deal RB,Henikoff JG,Henikoff S(2010)通过组蛋白代谢标记确定的核小体周转的基因组动力学。 科学类 328: 1161–1164. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
66 Hansen KH,Bracken AP,Pasini D,Dietrich N,Gehani SS,et al.(2008)H3K27me3表观遗传标记的传递模型。自然细胞生物学 10: 1291–1300. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
67 Petruk S、Sedkov Y、Johnston DM、Hodgson JW、Black KL等(2012)通过复制,TrxG和PcG蛋白而非甲基化组蛋白仍然与DNA相关。 单元格 150: 922–933. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
68 Francis NJ、Follmer NE、Simon MD、Aghia G、Butler JD(2009)。体外DNA复制期间,多梳蛋白质仍与染色质和DNA结合。 单元格 第137页:110–122页。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
69 Inoue A,Zhang Y(2011)小鼠植入前胚胎中5-羟甲基胞嘧啶的复制依赖性丢失。 科学类 334: 194. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
70 Ohno R、Nakayama M、Naruse C、Okashita N、Takano O等(2013)。复制依赖性被动机制调节小鼠原始生殖细胞中的DNA去甲基化。 开发 140: 2892–903 数字对象标识: 10.1242/dev.093229 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
71 Miller SA、Mohn SE、Weinmann AS(2010)Jmjd3和UTX在染色质重塑中发挥脱甲基酶依赖性作用,以调节T盒家族成员依赖性基因表达。 分子电池 40: 594–605. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
72 Vandamme J、Lettier G、Sidoli S、Di Schiavi E、Norregaard Jensen O等(2012)秀丽线虫H3K27脱甲基酶UTX-1对正常发育至关重要,与其酶活性无关。 公共科学图书馆-基因 8:e1002647。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
73 Gallardo T、Shirley L、John GB、Castrillon DH(2007)生殖细胞特异性小鼠转基因Cre系的产生,Vasa-Cre。 起源 45: 413–417. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
74 Rahl PB、Lin CY、Seila AC、Flynn RA、McCuine S等(2010)c-Myc调节转录暂停释放。 单元格 141: 432–445. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
75 Calabrese JM、Sun W、Song L、Mugford JW、Williams L等(2012)调控元件的定点沉默作为X失活机制。 单元格 151: 951–963. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
关联数据 本节收集本文中包含的任何数据引用、数据可用性声明或补充材料。
补充资料
图S1 靶向突变 Jmjd3号机组 .(A) Jmjd3号机组 目的是在第13内含子和第20内含子中引入LoxP站点。 用FLP重组酶去除Neo盒后,FRT位点仍然存在。 JMJD3蛋白的示意图如上所示,表示将用Cre重组酶去除的区域。 从外显子13-21剪接将引入移码和终止密码子。 (B) 验证 Jmjd3号机组 佛罗里达州 等位基因。 WT的Southern印迹和靶向 Jmjd3号机组 +/neofl公司 具有3′探针和XmnI消化物的ES细胞由于一个新的限制性位点而显示出预期的条带转移。 通过转染Flp重组酶从靶向ES细胞中移除新盒,以创建 Jmjd3号机组 +/佛罗里达州 .(C) Jmjd3号机组 佛罗里达州 /佛罗里达州 将小鼠与生殖系Cre重组酶杂交以产生 Jmjd3号机组 Δ/Δ 设计了PCR基因分型方案来区分WT、, Jmjd3号机组 佛罗里达州 、和 Jmjd3号机组 Δ 结果小鼠的等位基因。 (D) Jmjd3号机组 E18.5全胚RNA的RT-PCR证实了缺失。 Jmjd3号机组 Δ/Δ 胚胎缺乏外显子14-17产物,外显子13-22之间的扩增产生一个较小的带,对应于缺少外显子14–20的预期产物。 因此,突变转录物是稳定的,预计会产生缺少JmjC组蛋白去甲基化酶结构域的JMJD3。 (E) 纯合子 Jmjd3号机组 突变胚胎出生了,但无法呼吸,因为它们的蓝色。 (F) Jmjd3号机组 Δ/Δ 胚胎在E10.5时表现正常。
(畅通节能法)
图S2 UTX和JMJD3的母体缺失不会增强胚胎突变表型。 (A) Utx公司 fl/Δ ; Jmjd3号机组 fl/Δ ; 瓦萨 Cre公司 雌性小鼠(卵母细胞缺失 Utx公司 和 Jmjd3号机组 )与 Utx公司 飞行/飞行 ; Jmjd3号机组 fl/Δ ; 瓦萨 Cre公司 雄性小鼠(精子携带缺失 Utx公司 和 Jmjd3号机组 )在E10处解剖了杂交后代的胚胎。 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ (A′)和 Utx公司 Δ/Δ ; Jmjd3号机组 Δ/Δ (A〃)来自UTX和JMJD3母体贡献的杂交胚胎( 图1D、E )。 (B) 的基因分型 Utx公司 和 Jmjd3号机组 胚胎在 图S2A 以证明 Utx公司 和 Jmjd3号机组 floxed(fl)等位基因缺失(Δ)。
(畅通节能法)
图S3 中期妊娠分析 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 雄性胚胎。 (A、B)KDM6成员的定量RT-PCR(A, Utx公司 = 浅灰色, Jmjd3号机组 = 深灰色, 尤蒂 = 黑色)和指示 霍克斯 基因(B, 霍克斯4 = 浅灰色, 霍克斯6 = 深灰色, Hoxa13州 = 黑色)E10.5公螺纹的所有指定组合 Utx公司 和 Jmjd3号机组 相对于 Utx公司 +/年 ; Jmjd3号机组 +/Δ 对照组(每个基因型N≥4个样本)。 (C) 组蛋白提取自 Utx公司 +/年 ; Jmjd3号机组 +/Δ 或 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ H3K27me3相对于总H3负荷控制的胚胎和荧光蛋白印迹图。 (D) C部分的western blot定量,H3k27me3值归一化为总H3,以计算H3k27me3%。 (E) E10.5的H3K27me3免疫荧光 Utx公司 +/年 ; Jmjd3号机组 +/Δ 或 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 心肌。 (F) E10.5的H3K27me3免疫荧光 Utx公司 +/年 ; Jmjd3号机组 +/Δ 或 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 脊髓近端ISL1阳性运动神经元。 (G) 组蛋白提取自 Utx公司 +/年 ; Jmjd3号机组 +/Δ 或 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ H3K27me3相对于总H4负荷控制的MEF线和荧光蛋白印迹图。 (H) H3K27me3%蛋白质印迹定量,来自 Utx公司 +/年 ; Jmjd3号机组 +/Δ (灰色)或 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ (黑色)MEF相对于总H4。 蛋白质水平显著增加(*p值=0.05)。
(畅通节能法)
图S4 他莫昔芬的疗效 Cre公司 急诊室 导入 Utx公司 和 Jmjd3号机组 悬浮ES细胞系。 (A) A的PCR基因分型 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞株未经治疗(−TX)或接受他莫昔芬治疗2天(+TX) Utx公司 , Jmjd3号机组 ,性别和Cre的存在。 对照PCR反应包括 Utx公司 或 Jmjd3号机组 floxed等位基因( 佛罗里达州 ), Utx公司 或 Jmjd3号机组 缺失等位基因( Δ )、男性DNA(男性)、女性DNA(女性)、Cre阴性DNA(阴性)、Cre-阳性DNA(阳性)、水(H)。 (B) 一种蛋白质印迹 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞系未经治疗(−TX)或接受他莫昔芬治疗2天(+TX) Utx公司 GT1/年 UTX(αUTX)或加载控制(αGAPDH)的ES线。 这个 Utx公司 GT1/年 线应捕获所有 Utx公司 产品。 因此,在140KD的所有泳道中存在的带是非特异性带,而不是替代产物,因为它在 Utx公司 GT1/年 样品。 (C) 第B部分中描述的3条线路的RT-PCR Utx公司 被floxed等位基因(Exon 3)和JmjC结构域删除的区域。 请注意,包含JmjC域的所有转录本在 Utx公司 GT1/年 RNA。 (D) 使用第二个独立UTX抗体进行Western blot。
(畅通节能法)
图S5 悬垂EB分析和本构删除 Utx公司 和 Jmjd3号机组 (A)作为ES细胞大规模培养中EB形成的一种替代方法,悬滴EB是从定义的滴体积中的定义细胞数生成的。 (B) 荧光western blot分析H3K27me3随EB分化的丢失。 H3K27me3相对于总H4被印迹。 (C) 印迹定量 图S5B H3K27me3%是在构成性长期缺失后相对于总H4(D)分化绘制的 Utx公司 和 Jmjd3号机组 . Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 用TX处理ES细胞3天,然后在低密度下进行电镀,以便挑选单个细胞集落。 的克隆 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ 细胞增殖3周并传代数代,然后分化为相对于亲本的典型第4天EB结构 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 行。 (E) 中描述的ES细胞(diff−)和第8天EB(diff+)的表达分析 图S5D 对于 Utx公司 , Jmjd3号机组 , Gata6公司 (内胚层),以及 法兰1 (中胚层)。 (F) Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞也用TX处理以产生单细胞克隆(如 图S5D )和 Utx公司 Δ/Δ ; Jmjd3号机组 Δ/Δ ES细胞(Diff−)用RA分化2天(Diff+),RT-PCR比较 Utx公司 , Jmjd3号机组 , 霍克萨1 、和 霍克斯b1 相对于父母 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 行。
(畅通节能法)
图S6 UCSC基因组浏览器视图 霍克斯布 , 霍克斯 、和 霍克斯 集群。 (A–C)UCSC基因组浏览器视图 霍克斯 (A) , 霍克斯 (B) 、和 霍克斯 (C) ,集群。 图中所示为输入(黑色)、WT ES H3K27me3 ChIP(深绿色)、KO ES H3G27me3 ChIP(深红色)、WT-RA H3K17me3 ChIP(浅绿色)、KI RA H3K24me3 ChIP(浅红色)、WI RA H3Ch4me3 ChIP。
(畅通节能法)
图S7 中MLL和PCR2复合物的分析 Utx公司 和 Jmjd3号机组 突变细胞。 (A) MLL复合物成员ASH2L和RBBP5的Western blot分析水平 Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞−TX或+TX。(B)WT ES细胞、2天RA分化的ES细胞或2天分化的EB中PRC2组分EZH2和RBBP5的Western blot水平。 (C) EZH2 ChIP-qPCR Utx公司 飞行/飞行 ; Jmjd3号机组 飞行/飞行 ; Cre公司 急诊室 ES细胞(深绿色,Diff−)或RA治疗2天后(浅绿色或红色,Diff+)未经治疗(绿色)或用他莫昔芬(红色)预处理。 IgG控件ChIP显示为白色条。 EZH2阴性基因座的定量PCR( Npm1号机组 , 阴性 )用于与 罕见 , 霍克萨1 , 霍克斯州2 , 霍克斯b1 , 霍克斯b2 、和 霍克斯德9 .
(畅通节能法)
图S8 分析 Utx公司 和 Jmjd3号机组 突变MEF。 (A) 的RT-PCR 霍克萨3 , 霍克斯4 , Hoxa13州 ,或 Hoxd13型 在ES细胞、视黄酸处理的ES细胞或MEFs中。 (B) EZH2相对于RBBP5负荷控制的Western blot Utx公司 +/年 ; Jmjd3号机组 +/Δ 或 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ MEF公司。 (C) EZH2或H3K4me3的western blot定量 Utx公司 +/年 ; Jmjd3号机组 +/Δ (灰色)或 Utx公司 Δ/年 ; Jmjd3号机组 Δ/Δ (黑色)MEF。 蛋白质水平显著增加(*p值=0.04)。
(畅通节能法)
表S1 ES到RA分化中H3K27me3缺失的启动子。 在TSS+/-1 KB范围内,WT RA相对于WT ES(表1)和KO RA相对于KO ES(图2)中H3K27me3归一化序列显著缺失(FDR<0.05)的EdgeR统计比较。 一些基因有多个可供选择的启动子,因此列表中重复的基因以红色突出显示。还表示启动子是否具有相应的RA H3K4me3 MACS峰值(列为1)。
(XLSX)
表S2 KO-RA分化中H3K4me3减少的启动子。 在TSS+/-1 KB范围内,KO RA相对于WT RA中H3K4me3归一化序列读数的显著丢失(FDR<0.05)的EdgeR统计比较。 一些基因有多个备选启动子,因此列表中重复的基因以红色突出显示。也表示启动子是否有相应的WT或KO ES H3K27me3 MACS峰(列为1)。
(XLSX)
表S3 通过WT RA读取H3K27me3序列中富集的KO RA H3K17me3 MACS峰。 在KO RA MACS峰值中H3K27me3归一化序列读数相对于穿过KO RA峰值中心的WT RA显著增加(FDR<0.05)的EdgeR统计比较+/-0.5 KB。 MACS峰以最近的相邻基因列出。 一些基因与多个MACS峰相关,因此列表中重复的基因以红色突出显示。还表示该基因的启动子是否相应减少KO RA H3K4me3(列为1)。
(XLSX)
PLoS Genetics的文章由以下人员提供 多环芳烃