摘要 谷氨酰胺酶(GLS)催化的脱酰胺反应将氨基酸谷氨酰胺转化为谷氨酸。 该酶有两种亚型,GLS2亚型由抑癌基因p53调节。 这里,我们表明p53家族成员TAp73也驱动GLS2的表达。 具体而言,我们证明TAp73在维甲酸诱导的神经母细胞瘤细胞终末神经元分化过程中调节GLS2,GLS2的过度表达或抑制调节神经元分化和细胞内ATP水平。 此外,通过去除生长介质中的谷氨酰胺抑制GLS活性,会损害皮层神经元的体外分化。 最后,GLS2的表达在小鼠小脑发育过程中增加。 尽管p73对于GLS2的体内表达是不可或缺的,但TAp73的缺失会影响皮层神经元中的GABA和谷氨酸水平。 总之,这些发现表明GLS2至少部分作用于p73下游的神经元分化,并强调了p73在调节神经递质合成中的可能作用。
关键词: p73,GLS2,神经元分化,凋亡,p53家族,代谢,神经递质
介绍 谷氨酰胺(Gln)是一种氨基酸,在许多代谢途径中起着关键作用。 1 , 2 哺乳动物谷氨酰胺酶(GLS)是一种负责将谷氨酰胺水解脱酰胺为谷氨酸(Glu)和铵离子的酶。 不同染色体上的两个同源基因编码不同的GLS同工酶:肾型同工酶GLS1和肝型同工工酶GLS2。 三 , 4 尽管早期研究表明GLS1广泛表达, 2 GLS2主要表达于肝脏, 4 最近的观察表明,这种表达模式更为复杂。 事实上,GLS2也在大脑中被检测到, 5 胰腺, 6 癌细胞, 7 和免疫系统的细胞。 8 这两种亚型都已在人类和小鼠大脑中鉴定出来。 在亚细胞水平上,GLS2定位于线粒体内膜,而在神经元中,它被观察到位于细胞核中。 5 特定谷氨酰胺酶mRNA物种的丰度可能会因组织类型和组织的发育或代谢状态而发生显著变化; 因此,每个转录物可能代表不同刺激的特定靶标。 然而,尽管GLS分布已被广泛研究,但GLS1/GLS2表达的调控尚不清楚。 最近,两个独立的小组表明GLS2是抑癌基因p53的直接靶点, 9 , 10 在非应激和应激条件下,p53驱动GLS2的表达。 GLS2水平的增加促进Gln代谢,Gln水解产生的Glu是谷胱甘肽(GSH)生物合成的前体,因此通过调节GSH/GSSG比率促进抗氧化防御。 此外,谷氨酸可进一步转化为α-酮戊二酸,为三羧酸循环提供营养,导致线粒体呼吸和ATP生成增加。 因此,总的来说,GLS2在能量代谢和抗氧化防御中起着关键作用。
p73是一种多效性蛋白,属于p53家族。 11 - 15 它参与多种生物学过程, 16 - 19 区别, 20 - 22 神经干细胞维护, 23 - 26 老化, 27 - 29 和新陈代谢 27 通过基因的调节 30 - 32 和microRNA表达。 p73缺乏的小鼠表现出神经元病变,包括脑积水和海马发育不全,CA1-CA3锥体细胞层和齿状回有缺陷。 33 , 34 此外,由于成熟皮层神经元的丢失,它们的皮层厚度也会减少。 35 最近,有研究表明,TAp73的表达与神经元分化平行增加,其异位表达可诱导神经母细胞瘤细胞株中突起的生长和神经元标记物的表达,表明其具有促分化作用。 20 特别是,TAp73至少部分通过microRNA-34a调节神经元分化。 在这里,我们证明,与p53一样,p73能够驱动GLS2的表达。 我们证明,GLS2表达本身可诱导神经母细胞瘤(NB)细胞系中的神经元分化,并且GLS2的调节可影响维甲酸(RA)诱导的NB分化和体外皮层神经元的自发分化。 这些数据表明,GLS2是调节p73神经元效应的机制之一。
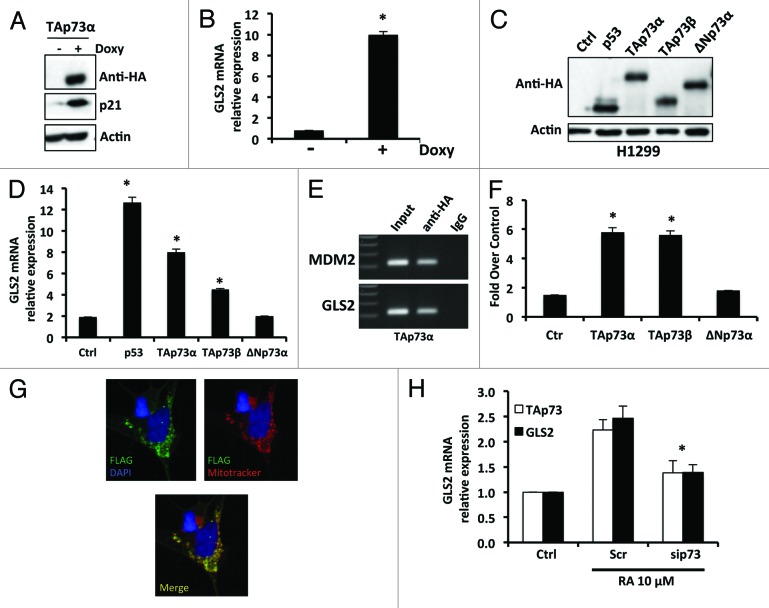
结果 TAp73调节GLS2的表达 由于TAp73和GLS2都在大脑中表达,并且由于p53家族蛋白之间存在广泛的功能相似性,我们询问TAp73是否像p53一样能够调节GLS2的表达。 我们首先采用SAOS2-TAp73α诱导细胞系,用多西环素处理,并在诱导24小时后提取总RNA。 正如预期的那样,TAp73α的表达以及众所周知的TAp73靶点p21的表达均被诱导( 图1A ). 在这种细胞环境中,我们还观察到GLS2 mRNA的显著上调( 图1B ). 为了证实TAp73能够调节GLS2的表达,我们在H1299细胞中瞬时表达了TAp73的不同亚型( 图1C ). 如所示 图1D TAp73α和β异位表达后,GLS2 mRNA显著诱导(6-8倍)。 在过表达ΔNp73α的细胞中未观察到GLS2表达的诱导。 接下来,我们询问GLS2是否由TAp73直接调节。 我们首先分析了人类GLS2启动子,并确定了一个与转录起始位点相关的位于−787的p53共有DNA结合元件。 为了验证TAp73α是否能够结合这个假定的反应元件,我们进行了染色质免疫沉淀分析(ChIP)。 如所示 图1E ,TAp73结合含有p53应答元件的GLS2启动子。 为了证实这种结合在功能上具有重要意义,我们用GLS2-核糖核酸酶报告子结构转染TAp73。 TAp73α或β的表达导致荧光素酶活性增加约6倍( 图1F ). 为了进一步证实TAp73调节GLS2表达的能力,我们使用了一个神经元终末分化的体外模型,其中TAp73已被证明是一个阳性调节器。 20 , 22 首先,我们对GLS2的细胞内定位和GLS亚型的表达的细胞系统进行了表征。 在SH-SH5Y细胞中,GLS2定位于线粒体(皮尔逊相关系数0.69),如 图1G 和 图S1A 在细胞核水平上未检测到GLS2的表达。 此外,我们发现GLS1也在SH-SY5Y细胞中表达( 图S1B ). 然后,我们用维甲酸(RA)处理SH-SY5Y细胞,以诱导终末分化并分离总RNA 图1H ,类风湿关节炎治疗后GLS2 RNA表达增加。 此外,当RNA干扰抑制TAp73表达时,RA诱导的GLS2表达增加被消除( 图1H ).
图1。 TAp73驱动GLS2的表达。 ( A类 )用多西环素(Doxy)处理SAOS-2-TAp73α诱导细胞系24 h,以过度表达人TAp73β蛋白,并通过实时PCR评估GLS2的内源性水平( B类 ). TAp73α的诱导导致( P(P) <0.05)通过实时PCR评估GLS2表达增加。 ( C类 )将所示质粒转染H1299细胞,通过实时PCR评估GLS2的表达,如( D类 ). ( E类 )如ChIP所示,TAp73与GLS2启动子结合。 ( F类 )TAp73通过荧光素酶活性评估激活GLS2启动子。 共转染 雷尼利亚 荧光素酶控制质粒用于正常化转染效率。 ( G公司 )外源性GLS2定位于线粒体。用FLAG-GLS2表达载体转染SH-SY5Y,24h后用MitoTracker染色 ® “材料和方法”中描述的红色CMXRos和针对FLAG表位的抗体。 图中显示了具有代表性的显微照片。 放大40倍。 ( H(H) )TAp73在神经母细胞瘤细胞的神经终末分化过程中调节GLS2的表达。 用10μM维甲酸处理SH-SY5Y细胞以诱导分化。 维甲酸(RA)治疗诱导GLS2的表达。 抑制由维甲酸诱导的TAp73表达可阻止GLS2的上调。 实时PCR数据归一化为看家基因GAPDH,相对于对照(Ctrl)数据表示3个不同实验的平均值±标准差* P(P) < 0.05
总之,这些结果表明TAp73直接调节GLS2的表达,并提示GLS2在调节RA诱导的神经母细胞瘤细胞终末分化中的潜在作用。
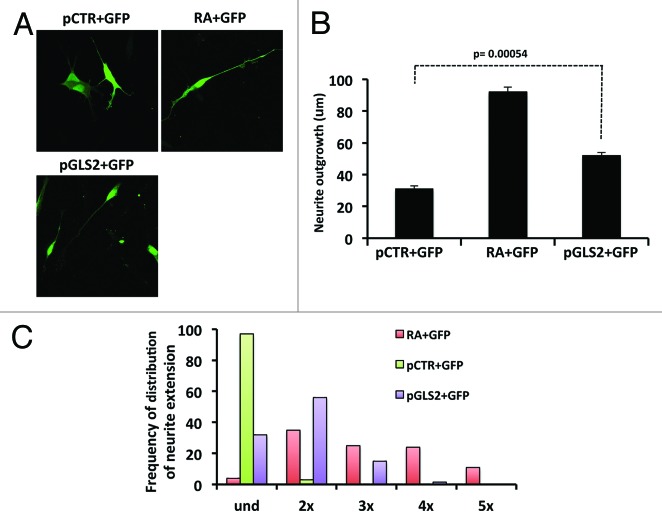
GLS2的表达对神经母细胞瘤细胞系终末神经元分化的影响 由于我们已经证明RA通过TAp73依赖机制诱导GLS2的表达,因此我们询问GLS2本身是否在NB细胞的最终神经元分化中发挥作用。 为了评估这一点,我们在SH-SY5Y细胞中过度表达GLS2和GFP( 图2A )24h后,评估神经突起的生长。 图2B 结果表明,GLS2(pGLS2)的过度表达显著增加了神经突起的生长,但程度与RA不同。 转染GFP(C+GFP)或GFP+空载体(pCTR+GFP。 此外,如所示 图2C 过度表达GLS2的细胞显示出两倍于胞体长度的高频率神经突起,在较小程度上是胞体长度3倍。 GFP+空载体转染细胞仍处于未分化状态(und)。
图2。 GLS2的异位表达增加了神经突起的生长。 ( A类 )SHSY-5Y细胞系中神经突起生长的典型图像。 用所示质粒转染细胞,然后不治疗或用RA治疗。 图中显示了具有代表性的显微照片。 放大40倍( B类 )48小时后,按照“材料和方法”中的描述固定细胞并分析其轴突延伸情况。 ( C类 )过度表达GLS2(紫柱)的SH-SY5Y细胞的轴突比细胞体长2-3倍。 数据表示3个不同实验的平均值±标准差。
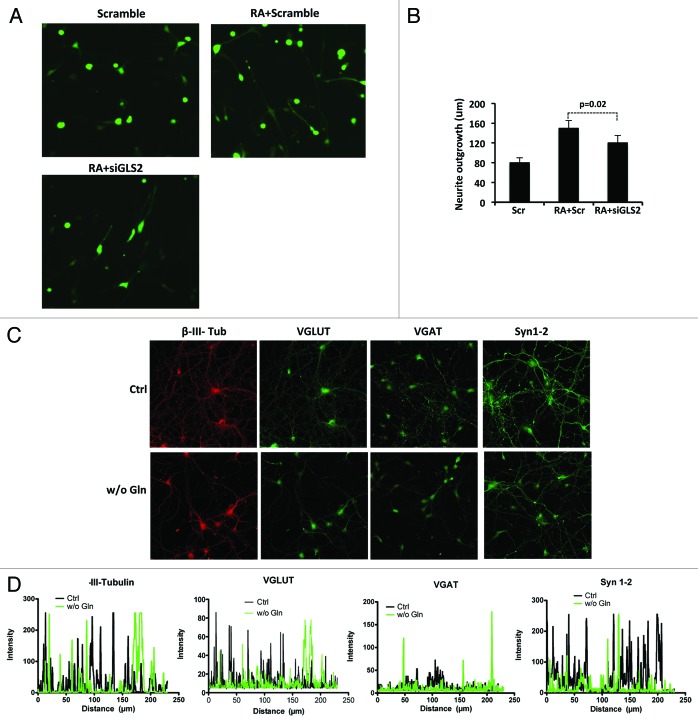
内源性GLS2在神经元分化中的作用 为了评估内源性GLS2是否也有助于神经元分化,我们敲除了RA治疗的SH-SY5Y细胞中GLS2的表达( 图3A ; 图S1C ). 图3B 显示GLS2表达的抑制导致了适度但显著的( P(P) =0.02)24小时RA诱导的轴突延伸减少。这种小影响可能是由于上述SH-SY5Y细胞中GLS1亚型伴随表达的代偿作用。 为了更好地理解GLS亚型在神经元分化中的作用,在皮层神经元体外分化过程中,我们通过撤回Gln来抑制GLS活性。 将初级皮层神经元进行培养,24小时后用不含Gln的培养基替换完整培养基。 6天后,对含有或不含Gln的皮层神经元进行免疫细胞化学处理。 如所示 图3C和D ,Gln的剥夺导致轴突数量的减少,如β-III微管蛋白染色所示。 这种减少是通过对皮层神经元进行特异性突触蛋白VGAT、VGLUT和突触肽1/2染色来证实的。 正常培养基和无Gln培养基中的皮层神经元凋亡无显著差异( 图S2 ). 36
图3。 抑制内源性GLS2水平可减少RA诱导的神经突起生长。 ( A类 )SHSY-5Y细胞系中神经突起生长的典型图像。 细胞转染Scramb+GFP或siGLS2+GFP,未经处理或用维甲酸(RA)处理。 ( B类 )48小时后,按照方法中的描述固定细胞并分析其轴突延伸情况。 数据代表3个不同实验的平均值±标准差。 谷氨酰胺戒断损伤皮层神经元的体外终末分化。 ( C类 )皮层神经元在谷氨酰胺存在或不存在的情况下培养,并在7天后固定和染色所指示的蛋白质。 放大40倍。 ( D类 )使用Zeiss LSM 510软件分析对神经元标记物β-III-Tubulin和所示突触蛋白的荧光强度进行量化。
综上所述,这些观察结果表明GLS2参与调节RA处理的NB细胞和皮层神经元的神经元分化。
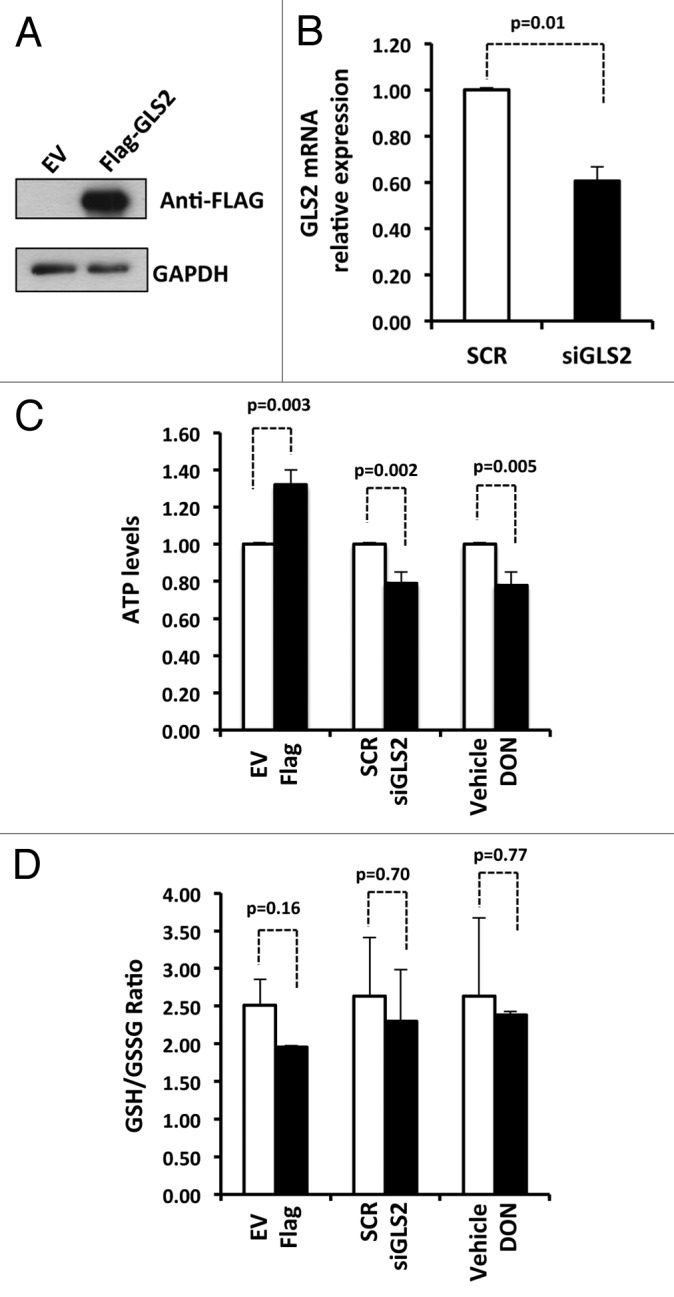
GLS2在NB细胞中的代谢功能 众所周知,GLS2在能量代谢和抗氧化防御中起着关键作用。 事实上,它调节细胞中的ATP水平和GSH/GSSG比率。 9 , 10 , 37 因此,我们询问GLS2是否也能在SH-SY5Y细胞中发挥同样的功能。 首先,我们过度表达了GLS2( 图4A )并测定细胞内ATP水平。 如所示 图4C (左手杆),GLS2的异位表达导致ATP细胞内水平显著增加(约+40%)。 相反,当我们通过siRNA敲低GLS2表达时( 图4B ),我们观察到ATP水平显著降低(约-20%)。 当我们用谷氨酰胺拮抗剂DON抑制GLS2的活性时,也得到了相同的结果( 图4C ). 然而 图4D 表明GLS2的过度表达和敲除均未显著影响GSH/GSSG比率。
图4。 GLS2调节细胞内ATP水平。 ( A类 )用空载体(EV)或FLAG-GLS2转染SHSY-5Y细胞后,显示GLS2表达的典型western blot。 ( B类 )实时PCR显示用短干扰RNA转染SHSY-5Y细胞后GLS2表达受到抑制(siGLS2)。 加扰(SCR)。 实时PCR数据归一化为相对于打乱(SCR)的看家基因GAPDH。 数据代表3个不同实验的平均值±标准差。 ( C类 )按照“材料和方法”中的描述,测量转染或按指示处理的SHSY-5Y中的细胞内ATP水平。 在200μM下使用谷氨酰胺酶DON抑制剂(6-重氮-5-氧-L-亮氨酸)。 ( D类 )GLS2对SHSY-5Y细胞内GSH和GSSG水平无影响。 按照“材料和方法”中的描述测量GSH/GSSG的比率。 数据表示3个不同实验的平均值±标准差。
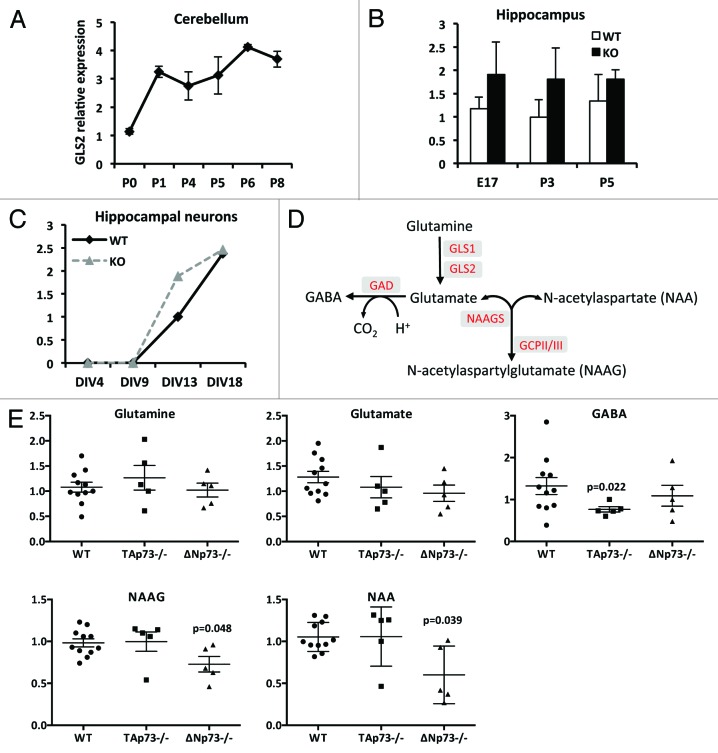
GLS2在神经元发育过程中的表达 为了进一步研究GLS2是否参与体内神经元分化,我们监测了其在小脑发育过程中的表达。 我们收集了不同阶段(从出生后第0天到第8天)的小鼠小脑,提取总RNA,并使用qPCR评估GLS2的表达水平。 图5A 显示GLS2的表达从P0增加到P1,然后至少在P8之前保持不变。
图5。 GLS2的体内表达。 ( A类 )GLS2在小鼠小脑发育过程中表达增加。 从野生型小鼠(每点4只)中分离小脑,并在小脑发育期间通过出生时实时PCR(P0)和出生后(P)天评估GLS2的表达。 ( B类 )野生型和p73海马中GLS2的表达 −/− 指定年龄的小鼠(E,胚胎;P,出生后)。 ( C类 )野生型和p73海马神经元体外终末分化过程中GLS2的表达 −/− 老鼠。 实时数据归一化为看家基因GAPDH相对值。 数据代表3个不同实验的平均值±标准差。 ( D类 )神经递质生物合成示意图。 红色表示参与每个反应的酶。 谷氨酰胺酶; 谷氨酸脱羧酶; N-乙酰谷氨酸合成酶; GCP,谷氨酸羧肽酶。 ( E类 )p73缺乏对神经递质细胞内水平的影响。 来自野生型(WT)TAp73的皮层神经元 −/− 和ΔNp73 −/− 培养7天后收获,并按照“材料和方法”中的描述进行质谱分析。
我们的体外数据促使我们探索TAp73是否也在体内调节GLS2的表达。 为此,我们首先从野生型(WT)和p73中提取海马RNA −/− 并监测GLS2的表达。 如所示 图5B ,在WT和p73之间GLS2 mRNA的表达没有发现差异 −/− 老鼠。 当我们比较海马神经元体外分化过程中GLS2的表达时,得到了相同的结果。 的确,如所示 图5C ,在p73的分化过程中GLS2表达似乎增加 −/− 海马神经元,至少在某些时间点。
尽管我们的研究结果表明,GLS2的体内表达不需要p73,但我们试图研究p73的缺失是否会影响谷氨酸代谢( 图5D ). 来自WT、TAp73的皮层神经元 −/− 和ΔNp73 −/− 小鼠被电镀,7天后收获,并进行质谱分析。 有趣的是,如所示 图5E ,TAp73的皮层神经元 −/− GABA水平似乎有所降低,这可能是由于谷氨酸水平稍低所致。 然而,天冬氨酸(也由谷氨酰胺转运体转运)和N-乙酰天冬氨酰谷氨酸(NAAG)水平在TAp73中没有变化 −/− 神经元。 因此,这些神经元中GABA的减少更可能是谷氨酸脱羧酶(GAD)活性改变的结果。 相反,NAAG及其前体N-乙酰天冬氨酸(NAA)以及抑制性神经递质甘氨酸( 图S3A ),在ΔNp73中减少 −/− 第7类神经元。 p73中这些分子水平降低 −/− 在体外培养过程中,神经元可能导致神经元功能改变或反映神经元分化的延迟。
谷氨酸是谷胱甘肽生物合成中的前体氨基酸之一。 我们观察到来自TAp73的皮层神经元 −/− 小鼠GSH水平和GSH/GSSG比率下降( 图S3B ). 然而,这些差异并没有达到统计显著性。
讨论 p53家族参与发育的许多方面 38 - 41 尤其是p73调节神经元分化。 首先,p73缺失导致神经元缺陷,包括脑积水和海马发育不全,CA1-CA3锥体细胞层和齿状回异常。 33 , 34 其次,TAp73在microRNA miR-34a的转录过程中至少部分地调节皮层神经元的神经元分化。 20 , 42 第三,TAp73参与维甲酸(RA)诱导的NB细胞的终末分化,并且与TAp73的表达增加有关。 此外,TAp73自身的异位表达可诱导终末神经元分化。 22 最近,我们还证明了TAp73通过miR-34a调节RA诱导的NB细胞分化,因为RA-诱导的NB-细胞分化受到TAp73敲低和antagomiR-34a的抑制。 20 在本报告中,我们表明TAp73能够直接调节GLS2的表达。 我们的结果表明,在维甲酸诱导NB细胞向神经元分化的过程中,GLS2受TAp73的控制,并且GLS2本身可以调节神经元的分化。
GLS2最近引起了人们的关注,因为它是p53抑癌基因的靶点。 9 , 10 特别是,GLS2调节癌细胞的能量代谢和抗氧化防御。 事实上,我们的研究结果表明并证实,GLS2至少在调节细胞内ATP水平方面发挥着关键作用。 然而,GLS2也参与了细胞分化。 7 我们的发现加强了GLS2在细胞分化,特别是神经元分化中的可能作用。 因此,GLS2增益和丧失功能实验分别导致神经元分化的增加和减少。
因此,正如TAp73敲除小鼠表型所揭示的那样,TAp73在神经元分化中的作用是复杂的,涉及几个下游途径。 本报告证明,GLS2和miR-34a是参与NB细胞分化的TAp73靶点,尤其是直接操纵GLS2表达本身调节NB分化,Gln剥夺影响体外皮层神经元的分化 , 表明TAp73的神经效应部分是由于其对代谢的影响,因为包括TAp73在内的p53家族成员已被报道具有代谢效应 43 - 45 除了调节Gln代谢之外。 尽管TAp73对GLS2表达的体内调节并不重要,但我们的研究结果表明,TAp73的缺失会影响谷氨酸代谢。 事实上,来自TAp73的皮层神经元 −/− 小鼠的神经递质谷氨酸和GABA水平降低。 因为神经元分化是一个复杂的生物过程,受内在途径调节 46 - 51 和外部信号, 52 , 53 TAp73的其他代谢作用是否也会影响这一生物过程,这将是一个有趣的问题。
材料和方法 老鼠 根据内政部颁发的项目许可证,饲养老鼠并执行列出的程序。 TAp73 −/− 和ΔNp73 −/− 小鼠的产生如前所述。 40 , 42
细胞培养和转染 TAp73α-SAOS-2-Tet-On细胞在RPMI、250μM L-谷氨酰胺(Gibco)、青霉素/链霉素1 U/ml(Gibco-)和10%无Tet-free FCS(Clontech)中生长; HEK 293E细胞在DMEM高糖、10%FBS、青霉素(100U)、链霉素(100μg)(Invitrogen)中培养; SH-SY5Y细胞在DMEM 10%FCS、青霉素/链霉素1 U/ml(Gibco)中保存,H1299细胞在RPMI、250μM L-谷氨酰胺(Gibco)、青霉素-链霉素1 U/ml(Gibco)、10%FCS(Invitrogen)中生长。 为了分化,SH-SY5Y细胞在添加1%FCS和10μM RA的DMEM中培养。
根据制造商的方案(Invitrogen),用Lipofectamine 2000转染细胞。 人类GLS2-表达载体由新泽西州癌症研究所冯兆辉博士善意提供。 如前所述,从E17.5胚胎小鼠制备初级皮层神经元培养物。 42
RNA提取和实时PCR 根据制造商的说明,使用Trizol(Invitrogen)从细胞或组织中分离出总RNA。 使用RevertAid H Minus逆转录酶和寡核苷酸(dT)(Thermo Scientific)逆转录总RNA(3μg)。 qRT-PCR在ABI PRISM 7000序列检测系统(Applied Biosystem)中使用SYBR绿色预混料(AppliedBiosystim)和特异性引物进行。 根据阈值周期(Ct)定义每个基因的表达,并使用2 -ΔΔCt 方法参照家政基因GAPDH的表达进行归一化。 使用以下引物:小鼠GAPDH Fwd 5′-CAATGAATAC GGCTACAGCA AC-3′和小鼠GAPDH-Rev 5′-AGGAGATGC TCAGTGTTGG-3′; 小鼠GLS2 Fwd 5′-AGCGTATCCC TATCACAG TTCA-3′和小鼠GLS2-Rev 5′-GCAGTCCAGA G-3′; 人TAp73 Fwd 5′-CTCTGGAGCT CTCTGGAACC A-3′和人TAp73Rev 5′-CGCCCACAC CTCATTATTC-3′; 人GLS2 Fwd 5′-TGCCTATAGTT GGCGATCT CA-3′和人GLS2Rev 5′-GTCCATATC CATGGCTGAC AA-3′; 人类GAPDH Fwd 5′-AGCCACATCG CTCAGACC-3′和人类GAPDH-Rev 5′-GCCAATACG ACCAAATC-3′; 人GLS1 Fwd 5′-GCTTGCTCC ATTGAAGTGA CT-3′; 和人类GLS1 Rev 5′-TTGGGCAGAA ACCACCATTA G-3′。
染色质免疫沉淀 将TAp73α-SaOS-2诱导细胞在含有1%甲醛的溶液中交联10分钟,并按照制造商的说明使用MAGnify ChIP系统(Invitrogen)进行ChIP分析。 对细胞裂解液进行超声处理,以获得约700 bp的染色质片段。 使用抗HA特异性抗体(16B12,Covance)和非特异性IgG作为对照,免疫沉淀免疫复合物。 收集的DNA片段通过PCR进行检测。 以下寡核苷酸用于扩增GLS2启动子中发现的p53推定应答元件(RE):Fwd 5′-GGCCTCCAA GTCACCAGTT CA-3′Rev 5′-TGTTTTTTGCT TGTTCGCC TTCT-3′。 用一组引物Fwd 5′-GGTTGACTCA GCTTCCTC TTG-3′和Rev 5′-GGAAATGCA TGGTTTAAAT AGCC-3′(119 bp)扩增位于hMDM2上的p53 RE作为阳性对照。
荧光素酶检测 HEK 293E细胞被镀在12孔板(1×10 5 和1.5×10 5 每口井)。 24小时后,将pGL3控制载体(200 ng)与TAp73α、β和ΔNp73α或空载体共转染 雷尼利亚 荧光素酶pRL-CMV载体(10ng),使用Lipofectamine 2000。 转染后24小时使用双荧光素酶报告物测定系统(Promega)测量荧光素酶活性; 使用OPTOCOMP I光度计测量10秒以上的光发射。 转染效率使用标准化 雷尼利亚 荧光素酶活性。
蛋白质印迹 用含有抑制剂鸡尾酒(Roche)的RIPA缓冲液提取蛋白质,并使用Bradford染色法(Biorad)测定蛋白质浓度。 对总蛋白(30μg)进行SDS-PAGE,然后用推荐稀释度的适当抗体进行免疫印迹。 然后将印迹与过氧化物酶连接的二级抗体孵育,然后使用超级信号化学发光试剂盒(Thermo-scientific)增强化学发光检测。 抗体:HA-HRP(1:5000;Sigma)、p21(1:1000,Santa Cruz)、FLAG M2克隆(1:5000,Sigma-Aldrich)和GAPDH(1:10000;Sigma-Aldrich)。
神经母细胞生长试验 使用Lipofcamine 2000转染SHSY-5Y细胞,然后用RA(10μM)处理,24小时或48小时后进行分析。 使用NeuronJ插件用NIH ImageJ半自动追踪投影图像。 分析每个GFP阳性细胞的轴突长度。
ATP和GSH/GSSG测量 使用ELITEN ATP分析系统生物发光检测试剂盒(Promega)测量细胞内ATP水平。 使用GSH/GSSG-Glo测定法(Promega)测量GSH和GSSG水平。 简单地说,用FLAG-GLS2或siGLS2转染细胞,分别在24小时或48小时后,按照制造商的说明进行采集和处理。
免疫荧光 用人FLAG-GLS2转染SH-SY5Y细胞,24小时后用MitoTracker在37°C下培养30分钟 ® 红色CMXRos(Invitrogen)。 然后用温培养基冲洗细胞两次,固定,并进行免疫荧光处理。 SHSY-5Y细胞用抗FLAG(1:1000,Sigma-Aldrich)抗体染色。 用3%多聚甲醛在PBS中固定含或不含谷氨酰胺培养的皮层神经元,然后用0.1%Triton X-100处理5分钟,用10%正常山羊血清在PBS在RT中处理1小时。然后在4°C下过夜,用以下主要抗体对细胞进行染色:神经特异性抗β-Ⅲ-管蛋白(1:2000;Promega), 抗VGAT(1:500;Synaptic系统)、抗VGLUT1(1:500,SynapticSystem)和抗Synaps1-2(1:500:Synaptec系统)。 在3次洗涤(PBS中10分钟)后,用Alexa Fluor共轭二级抗体(1:1000;Jackson ImmunoResearch Laboratories)培养细胞。 3次洗涤(10 min,PBS)后,细胞核用DAPI(1:10000)染色10 min; 此步骤之后,再进行进一步清洗(PBS中10分钟)。 然后用Aquapolymount防褪色溶液(Polysciences)将盖玻片安装到玻片上,并在共焦显微镜下观察(蔡司LSM 510)。 使用Volocity 3D图像分析软件6.3版(Perkin Elmer)进行结肠镜检分析。
皮层神经元的代谢组学分析 采集DIV7皮层神经元,并立即将其储存在−80°C的温度下,并按照前述方法处理样品。 54 , 55 简单地说,样品制备过程是使用自动化MicroLab STAR进行的 ® 汉密尔顿公司的系统。 为了进行质量控制,在提取过程的第一步之前添加回收标准。 样品制备是使用一系列专有的有机和水萃取液进行的,以去除蛋白质部分,同时最大限度地回收小分子。 所得提取物分为两个部分:一个用于LC分析,另一个用于GC分析。 样品被短暂放置在TurboVap上 ® (Zymark)去除有机溶剂。 然后将每个样品冷冻并在真空下干燥。 然后为合适的仪器(LC/MS或GC/MS)制备样品。通过与纯化的标准品或反复出现的未知实体的文库条目进行比较来鉴定化合物。 已知化学实体的鉴定是基于与纯化标准品的代谢组学文库条目的比较。
统计分析 所有结果均表示为平均值±标准差。 P(P) <0.05被认为是显著的。 对于代谢组学分析,我们执行Welch 2样本 t吨 测验。
致谢 我们感谢David J Read的技术支持。 这项工作得到了英国医学研究委员会的支持; 由“Allenza contro il Cancro”(ACC12)、MIUR/PRIN(20078P7T3K_001)/FIRB(RBIP06LCA9_0023,RBIP06LCA9_0C)、AIRC(2011-IG11955)、AIRC5xmille(#9979)、Telethon Grant GGPO9133、Min.Salute(Ricerca nologica 26/07)和IDI-IRCCS(RF06 c.73,RF07 c.57,RF08 c.15,RF07 c.57)授予GM。
词汇表 缩写:
TAp73 转录活性p73
ΔNp73 氨基截断p73
格林 谷氨酰胺
谷氨酸 谷氨酸盐
无线电高度表 维甲酸
注 神经母细胞瘤
P(P) 产后日
炸薯条 染色质免疫沉淀
GFP公司 绿色荧光蛋白
GABA公司 γ-氨基丁酸
VGAT公司 囊泡GABA转运体
VGLUT公司 囊泡膜谷氨酸转运体
大学教师 6-重氮-5-氧代-L-去甲亮氨酸
二甲醚 Dulbecco最小基本介质
FBS公司 胎牛血清
计算机断层扫描 周期
参考
1 Matés JM、Segura JA、Campos-Sandoval JA、Lobo C、Alonso L、Alonso FJ、Márquez J.谷氨酰胺稳态和线粒体动力学。 国际生物化学与细胞生物学杂志。 2009; 41:2051–61. doi:10.1016/j.bicel.2009.03.003。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
2 Kovacevic Z,McGivan JD。 谷氨酰胺和谷氨酸的线粒体代谢及其生理意义。 《生理学评论》1983; 63:547–605. doi:10.1152/physrev.1983.63.2.547。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
三。 Shapiro RA、Farrell L、Srinivasan M、Curthoys NP。编码线粒体谷氨酰胺酶肾脏同工酶的cDNA的分离、表征和体外表达。 生物化学杂志。 1991; 266:18792–6. [ 公共医学 ] [ 谷歌学者 ]
4 Smith EM,Watford M.大鼠肝谷氨酰胺酶cDNA的分子克隆。 与肾脏型谷氨酰胺酶序列相似。 生物化学杂志。 1990; 265:10631–6. [ 公共医学 ] [ 谷歌学者 ]
5. Olalla L、Gutiérrez A、Campos JA、Khan ZU、Alonso FJ、Segura JA、Márquez J、Aledo JC。 哺乳动物脑中L型谷氨酰胺酶的核定位。 生物化学杂志。 2002; 277:38939–44. doi:10.1074/jbc。 C200373200。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
6 Gómez-Fabre PM、Aledo JC、Del Castillo-Olivares A、Alonso FJ、Nüñez De Castro I、Campos JA、Márquez J.人类乳腺癌细胞谷氨酰胺酶的分子克隆、测序和表达研究。 《生物化学杂志》2000; 345:365–75. doi:10.1042/0264-6021:3450365。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
7 Pérez-Gómez C、Campos-Sandoval JA、Alonso FJ、Segura JA、Manzanares E、Ruiz-Sánchez P、González ME、Márquez J、MatéS JM。谷氨酰胺酶K和L同工酶在人类肿瘤细胞中的共表达。 《生物化学杂志》2005; 386:535–42. doi:10.1042/BJ20040996。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
8 Castell L,Vance C,Abbott R,Marquez J,Eggleton P.谷氨酰胺酶在人类中性粒细胞中的颗粒定位以及谷氨酰胺利用对中性粒细胞活性的影响。 生物化学杂志。 2004; 279:13305–10. doi:10.1074/jbc。 M309520200。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
9. 铃木S、田中T、波尤罗夫斯基MV、长野H、马雅玛T、大久保S、洛克辛M、细川H、中山T、铃木Y等。磷酸活化谷氨酰胺酶(GLS2),一种p53诱导的谷氨酰胺代谢和活性氧物种调节器。 美国国家科学院院刊2010; 107:7461–6. doi:10.1073/pnas.1002459107。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
10 胡伟,张C,吴锐,孙毅,莱文A,冯Z。谷氨酰胺酶2,一种调节能量代谢和抗氧化功能的新型p53靶基因。 美国国家科学院院刊2010; 107:7455–60. doi:10.1073/pnas.1001006107。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
11 Dötsch V、Bernassola F、Coutandin D、Candi E、Melino G.p63和p73是p53的祖先。 冷泉Harb Perspect生物。 2010; 2:a004887。 doi:10.1101/cshperspect.a004887。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
12 Rufini A、Agostini M、Grespi F、Tomasini R、Sayan BS、Niklison-Chirou MV、Conforti F、Velletri T、Mastino A、Mak TW等,《癌症》第73页。 基因癌症。 2011; 2:491–502. doi:10.1177/1947601911408890。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
13 Killick R、Niklison-Chirou M、Tomasini R、Bano D、Rufini A、Grespi F、Velletri T、Tucci P、Sayan BS、Conforti F等。p73:神经生物学中的多功能蛋白质。 摩尔神经生物学。 2011; 43:139–46. doi:10.1007/s12035-011-8172-6。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
14 McCubrey JA,Demidenko ZN。 p53基因域循环、生长和衰老的最新发现。 老龄化(纽约州奥尔巴尼市)2012; 4:887–93. doi:10.18632/aging.100529。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
15 Amelio I、Grespi F、Annicchiarico-Petruzzelli M、Melino G.p63人类生殖监护人。 细胞周期。 2012; 11:4545–51. doi:10.4161/cc.22819。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
16 Gong JG、Costanzo A、Yang HQ、Melino G、Kaelin WG,Jr.、Levrero M、Wang JY。 酪氨酸激酶c-Abl调节p73对顺铂诱导的DNA损伤的凋亡反应。 自然。 1999; 399:806–9. doi:10.1038/21690。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
17. Muppani N,Nyman U,Joseph B.TAp73alpha保护小细胞肺癌细胞免受caspase-2诱导的线粒体介导的凋亡细胞死亡。 Oncotarget公司。 2011; 2:1145–54. doi:10.18632/目标391。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
18 Al-Bahlani S、Fraser M、Wong AY、Sayan BS、Bergeron R、Melino G、Tsang BK。P73通过钙/钙蛋白酶依赖机制调节顺铂诱导的卵巢癌细胞凋亡。 致癌物。 2011; 30:4219–30. doi:10.1038/onc.2011.134。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
19 Grespi F、Amelio I、Tucci P、Annicchiarico-Petruzzelli M、Melino G。小鼠p73 C末端亚型的组织特异性表达。 细胞周期。 2012; 11:4474–83. doi:10.4161/cc.22787。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
20 Agostini M、Tucci P、Killick R、Candi E、Sayan BS、Rivetti di Val Cervo P、Nicotera P、McKeon F、Knight RA、Mak TW等。TAp73的神经分化是通过调节突触蛋白靶点的microRNA-34a介导的。 美国国家科学院院刊2011; 108:21093–8. doi:10.1073/pnas.1112061109。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
21 Billon N、Terrinoni A、Jolicoeur C、McCarthy A、Richardson WD、Melino G、Raff M。p53和p73在少突胶质细胞发育过程中的作用。 发展。 2004; 131:1211–20. doi:10.1242/dev.01035。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
22 De Laurenzi V、RaschelláG、Barcaroli D、Annicchiarico-Petruzzelli M、Ranalli M、Catani MV、Tanno B、Costanzo A、Levrero M、Melino G。p73在神经母细胞瘤细胞系中诱导神经元分化。 生物化学杂志。 2000; 275:15226–31. doi:10.1074/jbc.275.20.15226。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
23 Agostini M、Tucci P、Chen H、Knight RA、Bano D、Nicotera P、McKeon F、Melino G.p73调节神经干细胞的维持。 生物化学与生物物理研究委员会。 2010; 403:13–7. doi:10.1016/j.bbrc.2010.1087。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
24 Talos F、Abraham A、Vaseva AV、Holembowski L、Tsirka SE、Scheel A、Bode D、Dobbelstein M、Brück W、Moll UM。p73是胚胎和成年CNS神经发生中神经干细胞维持的重要调节器。 细胞死亡不同。 2010; 17:1816–29. doi:10.1038/cdd.2010.131。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
25 Gonzalez-Cano L、Herreros-Villanueva M、Fernandez-Alonso R、Ayuso-Sacido A、Meyer G、Garcia-Verdugo JM、Silva A、Marques MM、Marin MC。p73缺陷导致独立于p53的小鼠神经祖细胞的自我更新受损和早期神经元分化。 细胞死亡疾病。 2010; 1:e109。 doi:10.1038/cddis.2010.87。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
26 Flores ER.p73对记忆的持久性至关重要。 细胞死亡不同。 2011; 18:381–2. doi:10.1038/cdd.2010.178。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
27 Rufini A、Niklison-Chirou MV、Inoue S、Tomasini R、Harris IS、Marino A、Federici M、Dinsdale D、Knight RA、Melino G等。TAp73缺失通过代谢失调加速衰老。 基因开发2012; 26:2009–14. doi:10.1101/gad.197640.112。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
28. Grespi F、Melino G.P73和年龄相关疾病:是否与帕金森病有关? 老龄化(纽约州奥尔巴尼市)2012; 4:923–31. doi:10.18632/aging.100515。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
29 Guglielmino MR、Santoncito M、Vento M、Ragusa M、Barbagallo D、BorzP、Casciano I、Banelli B、Barbieri O、Astigiano S等。TAp73在高龄女性卵母细胞中下调。 细胞周期。 2011; 10:3253–6. doi:10.4161/cc.10.19.17585。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
30 Melino G、Bernassola F、Ranalli M、Yee K、Zong WX、Corazzari M、Knight RA、Green DR、Thompson C、Vousden KH。p73通过PUMA反式激活和Bax线粒体易位诱导细胞凋亡。 生物化学杂志。 2004; 279:8076–83. doi:10.1074/jbc。 M307469200。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
31 Conforti F、Sayan AE、Sreekumar R和Sayan BS。翻译后修饰对p73活性的调节。 细胞死亡疾病。 2012; 3:e285。 doi:10.1038/cddis.2012.27。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
32 Graupner V、Alexander E、Overkamp T、Rothfuss O、De Laurenzi V、Gillissen BF、Daniel PT、Schulze Osthoff K、Essmann F。p53和p73在启动子水平上对促凋亡多结构域蛋白Bak的差异调节。 细胞死亡不同。 2011; 18:1130–9. doi:10.1038/cdd.2010.179。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
33 Tomasini R、Tsuchihara K、Wilhelm M、Fujitani M、Rufini A、Cheung CC、Khan F、Itie-Youten A、Wakeham A、Tsao MS等。TAp73基因敲除显示基因组不稳定,具有不育和抑癌功能。 基因开发2008; 22:2677–91. doi:10.1101/gad.1695308。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
34 Yang A、Walker N、Bronson R、Kaghad M、Oosterwegel M、Bonnin J、Vagner C、Bonnet H、Dikkes P、Sharpe A等。p73缺陷小鼠有神经、信息素和炎症缺陷,但缺乏自发性肿瘤。 自然。 2000; 404:99–103. doi:10.1038/35003607。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
35 Wilhelm MT、Rufini A、Wetzel MK、Tsuchihara K、Inoue S、Tomasini R、Itie-Youten A、Wakeham A、Arsenian-Henriksson M、Melino G等。同种异型特异性p73敲除小鼠揭示了delta Np73在DNA损伤反应途径中的新作用。 基因开发2010; 24:549–60. doi:10.1101/gad.1873910。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
36. Chen J,Herrup K。谷氨酰胺可作为神经保护剂对抗DNA损伤、β-淀粉样蛋白和H2O2诱导的应激。 公共科学图书馆一号。 2012; 7:e33177。 doi:10.1371/journal.pone.0033177。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
37 Giacobe A、Bongiorno-Borbone L、Bernassola F、Terrinoni A、Markert EK、Levine AJ、Feng Z、Agostini M、Zolla L、Agro AF等。p63调节谷氨酰胺酶2的表达。 细胞周期。 2013; 12:1395–405. doi:10.4161/cc.24478。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
38 Danilova N,Sakamoto KM,Lin S.发育中的p53家族。 机械开发2008; 125:919–31. doi:10.1016/j.mod.2008.09.003。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
39 Moll UM,Slade N.,第63页和第73页:在发育和肿瘤形成中的作用。 2004年Mol Cancer Res; 2:371–86. [ 公共医学 ] [ 谷歌学者 ]
40 Shalom-Feuerstein R、Lena AM、Zhou H、De La Forest Divonne S、Van Bokhoven H、Candi E、Melino G、Abedam D。ΔNp63是表皮形态发生的外胚层守门员。 细胞死亡不同。 2011; 18:887–96. doi:10.1038/cdd.2010.159。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
41 Paris M、Rouleau M、Pucéat M、Abedam D。TAp63对皮肤老化和心脏发育的调节。 细胞死亡不同。 2012; 19:186–93. doi:10.1038/cdd.2011.81。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
42 Agostini M、Tucci P、Steinert JR、Shalom-Feuerstein R、Rouleau M、Abedam D、Forsythe ID、Young KW、Ventura A、Concepcion CP等。microRNA-34a调节神经突起生长、脊柱形态和功能。 美国国家科学院院刊2011; 108:21099–104. doi:10.1073/pnas.1112063108。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
43 Vousden KH、Ryan KM、p53和新陈代谢。 Nat Rev癌症。 2009; 9:691–700. doi:10.1038/nrc2715。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
44 Thotala DK、Hallahan DE、Yazlovitskaya EM。糖原合成酶激酶3β抑制剂通过调节MDM2-p53通路保护海马神经元免受辐射诱导的凋亡。 细胞死亡不同。 2012; 19:387–96. doi:10.1038/cdd.2011.94。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
45. Madan E、Gogna R、Bhatt M、Pati U、Kuppusamy P、Mahdi AA。p53对葡萄糖代谢的调节:肿瘤抑制剂的新作用。 Oncotarget公司。 2011; 2:948–57. doi:10.18632/目标389。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
46 Ninkovic J,Götz M.成年神经发生中的信号传导:从干细胞生态位到神经元网络。 神经生物电流。 2007; 17:338–44. doi:10.1016/j.conb.2007.04.006。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
47 Zimmer B、Kuegler PB、Baudis B、Genewsky A、Tanavde V、Koh W、Tan B、Waldmann T、Kadereit S、Leist M。胚胎干细胞神经元分化过程中的基因表达协调波是发育神经毒性测试新方法的基础。 细胞死亡不同。 2011; 18:383–95. doi:10.1038/cdd.2010.109。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
48 Volvert ML、Rogister F、Moonen G、Malgrange B、Nguyen L.MicroRNAs调节大脑皮层神经发生。 细胞死亡不同。 2012; 19:1573–81. doi:10.1038/cdd.2012.96。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
49 Brett JO、Renault VM、Rafalski VA、Webb AE、Brunet A。microRNA簇miR-106b~25调节成人神经干/祖细胞增殖和神经元分化。 老龄化(纽约州奥尔巴尼)2011; 3:108–24. doi:10.18632/aging.100285。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
50 Nigro A、Menon R、Bergamaschi A、Clovis YM、Baldi A、Ehrmann M、Comi G、De Pietri Tonelli D、Farina C、Martino G等。MiR-30e和MiR-181d通过HtrA1调节控制放射状胶质细胞增殖。 细胞死亡疾病。 2012; 3:e360。 doi:10.1038/cddis.2012.98。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
51 Frank CL、Tsai LH。 核心细胞周期调节器在神经元迁移、神经元成熟和突触可塑性中的替代功能。 神经元。 2009; 62:312–26. doi:10.1016/j.neuron.2009.03.029。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
52 陈恩,那不勒斯JL。 全反式维甲酸通过膜相关的RARalpha刺激翻译并诱导海马神经元形成脊柱。 FASEB J.2008; 22:236–45. doi:10.1096/fj.07-8739com。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
53 Aoto J,Nam CI,Poon MM,Ting P,Chen L.全反式维甲酸在稳态突触可塑性中的突触信号传导。 神经元。 2008; 60:308–20. doi:10.1016/j.neuron.2008.012。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
54 Tucci P、Porta G、Agostini M、Dinsdale D、Iavicoli I、Cain K、Finazi-AgroóA、Melino G、Willis A。作为防晒霜和化妆品的常见成分,TiO2纳米颗粒对人类角质形成细胞的代谢作用。 细胞死亡疾病。 2013; 4:e549。 doi:10.1038/cddis.2013.76。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
55 Tucci P、Porta G、Agostini M、Antonov A、Garabadgiu AV、Melino G、Willis AE。雷帕霉素调节生化代谢物。 细胞周期。 2013; 12:2454–67. doi:10.4161/cc.25450。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
关联数据 本节收集本文中包含的任何数据引用、数据可用性声明或补充材料。