摘要 索拉非尼(Sorafenib)被批准用于治疗肝癌,也显示出很有希望的抗纤维化活性,因此在抗纤维化临床试验之前,改善其剂量要求和疗效窗口是重要的目标。
目标 确定索拉非尼对培养的人星状细胞和实验性肝纤维化大鼠的最小有效剂量和最佳治疗时机。
方法 在人类星状细胞系(LX-2)中评估索拉非尼的作用。 体内 ,大鼠每周前三次接受TAA治疗8周(150 mg/kg IP),并在开始给予TAA 8周、第4周至第8周或第8周至第12周期间每天灌胃1.25、5或7 mg/kg剂量的PBS或索拉非尼。
结果 索拉非尼治疗显著抑制LX-2增殖>75%(7.5或15µM)。 7.5µM索拉非尼治疗12小时后,显著抑制TGFβ1、TIMP-1、I型胶原和MMP2 mRNA的表达,但不抑制β-PDGFR或I型TGFβR的表达。 体内 ,索拉非尼与TAA同时开始治疗时以及与TAA治疗第4-8周期间显著抑制肝纤维化。 相反,当肝硬化已经形成后开始时,索拉非尼对纤维化基因表达或纤维化没有显著影响。
结论 索拉非尼对培养的人HSC具有抗增殖和抗纤维化作用,是治疗TAA诱导的大鼠肝纤维化的有效药物。 该药物在肝纤维化早期的相对低剂量下有效,但在肝硬化已经形成的情况下无效。
介绍 肝纤维化是一种可逆的伤口愈合反应,是急性或慢性肝损伤时细胞外基质(ECM)积聚的结果[ 1 ]. 肝星状细胞(HSC)是位于肝细胞和肝纤维化主要效应细胞窦内皮细胞之间的内皮下间隙的窦周细胞。 肝损伤期间,HSC被激活,并产生纤维化肝脏的大部分基质成分,包括胶原蛋白。 血小板衍生生长因子(PDGF)是一种有效的HSC有丝分裂原,是HSC激活的最具特征的途径之一[ 2 ]. 在HSC早期激活期间诱导β-PDGF受体激活其下游效应器,包括ERK/MAP激酶途径[ 三 , 4 ]. 抗纤维化药物拮抗β-PDGF受体和相关酪氨酸激酶受体是抗纤维化治疗的诱人前景。
索拉非尼是一种广泛使用的多酪氨酸激酶抑制剂,是FDA批准的治疗肝细胞癌和肾细胞癌的药物[ 5 – 7 ]. 其作用机制主要是抑制RAF/MEK/ERK通路,在体内减少肿瘤细胞增殖和血管生成,同时增加肿瘤细胞凋亡[ 8 ]. 先前的研究表明索拉非尼具有抗肝纤维化的活性,可以减轻胆管结扎(BDL)肝纤维化模型中基质积聚和血管重塑[ 9 ]. 然而,这些研究尚未确定索拉非尼在纤维化自然发展过程中的什么时候仍然有效,也未检测到实质细胞损伤和纤维化模型,这是人类疾病中更常见的损伤模式。
开发适合人类使用的抗纤维化治疗仍然是一个难以实现的目标。 在本研究中,我们在动物模型中检查了索拉非尼治疗的剂量要求和疗效窗口,作为考虑在纤维化肝病患者中进行抗纤维化临床试验的前奏。 具体而言,我们已经在培养的人类HSC和硫代乙酰胺(TAA)诱导的大鼠肝纤维化模型中确定了索拉非尼治疗的最小有效剂量和最佳时间,这是一个最接近人类肝纤维化的成熟模型。
材料和方法 文化研究 LX-2细胞和原代人类星状细胞保存在含有10%胎牛血清和1%青霉素链霉素抗生素(Gibco,Invitrogen)的高糖Dulbecco改良鹰培养基中。 在含有0.2%BSA或10%胎牛血清的培养基中,以7.5µM和15µM的浓度用索拉非尼(拜耳Onyx)处理细胞12、24、48或72小时。
AlamarBlue®细胞活力测定 使用alamarBlue®(Invitrogen)评估细胞活力。 在12和24小时内,用7.5和15µM处理每孔含有约5000个LX-2细胞的96孔板。 将AlamarBlue®试剂直接添加到每个孔中,在37°C下培养平板,使细胞将resazurin转化为resurufin,并测量荧光信号。
原发性人类HSC的分离 如前所述,在原发性良性肿瘤或结肠癌单一转移进行肝切除的患者中,从正常人肝脏的楔形切片中分离出原发性HSC[ 10 ]. 通过在塑料上培养7-14天激活HSC,并传代至第3代进行以下实验。 除了原发性造血干细胞外,我们还利用了一种经过充分验证的永生化人造血干细胞系LX-2,其特征与原发性活化的造血干细胞非常相似[ 11 ].
细胞增殖试验 DNA合成使用 三 如前所述掺入H-胸苷[ 11 ]. LX-2细胞以每孔20000个细胞的密度接种在24孔板中。 24小时后,将培养基更换为含有0.2%胎牛血清的Dulbecco改良Eagle培养基12小时,然后用索拉非尼(7.5µM和15µM)处理细胞24或48小时,以及1 Ci/mL 三 收获前添加H-胸腺嘧啶核苷4小时。 然后用冰镇PBS清洗细胞三次,并在4°C的甲醇中固定30分钟。 细胞在0.25%氢氧化钠/0.25%十二烷基硫酸钠中溶解。 用盐酸(1N)中和后,使用闪烁计数器(贝克曼·库尔特)测量放射性。
DNA分离和电泳 为了检测LX-2细胞中的片段或凋亡DNA(小DNA片段),根据制造商的指南,使用凋亡DNA阶梯提取试剂盒(美国山景城BioVision),从用10µg/ml索拉非尼和载体处理12和48小时的LX-2电池中分离出DNA。 样品在2%琼脂糖凝胶中运行,用溴化乙锭染色,并通过紫外线透照进行可视化。
逆转录和实时定量PCR 使用RNeasy Mini试剂盒(加利福尼亚州巴伦西亚Qiagen)提取并纯化LX-2细胞、初级星状细胞或100 mg大鼠全肝组织中的RNA,并使用SprintTM RT Complete-RNA-to-cDNA EcoDry™Premix(双引物)管(加利福尼亚州山景城Clontech)将1µg总mRNA反向转录到互补DNA(cDNA)中, 并在LightCycler®480 RealTime PCR System(Roche)上使用SYBR green qPCR Master Mix(罗氏)进行定量PCR分析。 数据表示为GAPDH正常化后成纤维基因的相对表达。
西部印记 使用RIPA裂解缓冲液(50 mM Tris-HCl pH=8,150 mM NaCl,1%IGEPAL,0.5%脱氧胆酸钠和0.1%SDS)以及补充蛋白酶抑制剂混合物和蛋白磷酸酶抑制剂混合物(罗氏)从细胞中提取总蛋白。 通过均质法提取大鼠肝组织中的蛋白质。 蛋白质浓度用Bio-Rad DC试剂盒(Bio-Rad)测定。 使用的抗体如下:兔抗I型胶原蛋白抗体(1:2000)(Rockland)、鼠抗aSMA抗体(1:500)(Millipore)和兔抗GAPDH抗体(1:200)(Santa Cruz)。
体内 TAA治疗大鼠的研究
雄性Sprague-Dawley大鼠体重280-300克或8-10周龄(Jackson Laboratory),根据NIH指南进行饲养,并经西奈山IACUC委员会批准。 大鼠被饲养在西奈山医学中心的动物护理设施中,在恒温条件下进行12小时的光暗循环。 在研究期间,大鼠可以自由饮用自来水。
体内 研究采用了“预防”(第2组)、“治疗”(第3组)和“逆转”(第4组)治疗方案以及对照组(第1组)( 补充图1 ). 每组包含4个不同的亚组,每个亚组包含7只大鼠。 第1组每周腹腔注射磷酸盐缓冲液(PBS),不注射TAA。 在第2、3和4组中,大鼠通过IP给予150 mg/kg TAA(西格玛化学公司,密苏里州圣路易斯),每周三次,持续8周,以诱导肝硬化。 大鼠每日灌胃索拉非尼,剂量为1.25 mg/kg/天(亚组A)、5 mg/kg/D(亚组B)、7 mg/kg/日(亚组C)和溶媒对照组(12.5%克雷马弗(西格玛)、12.5%乙醇和75%水)(亚组D); 与TAA同时开始8周(第2组),在第4-8周期间(第3组),或在TAA停止后第8-12周开始(第4组)。
在处死时,用一根插入门静脉的16G血管导管测量门静脉压力,以测量水柱的高度。 在含有EDTA的微滤管中采集血液,以5000 rpm的速度造粒10分钟,获取AST、ALT、肌酐和胆红素的血浆样本,并取出肝脏,称重和处理。 脾脏也被取出并称重后丢弃。
肝脏组织学和纤维化定量 将肝脏固定在3.7%福尔马林中,包埋在石蜡中并切片。 肝脏切片用饱和苦味酸中0.1%天狼星红染色(均来自Sigma Chemical Co.)。 每只动物取4张苦味酸红染色载玻片,每张载玻片随机取9张图像,每只动物共取36张图像,使用计算机化BIOQUANT生命科学形态计量学α系统进行胶原蛋白定量。
统计分析 数据表示为至少三次独立测定的平均值±SD。 通过双尾Student’s进行比较 t吨 -测试。 数据被认为具有统计学意义,p<0.05。
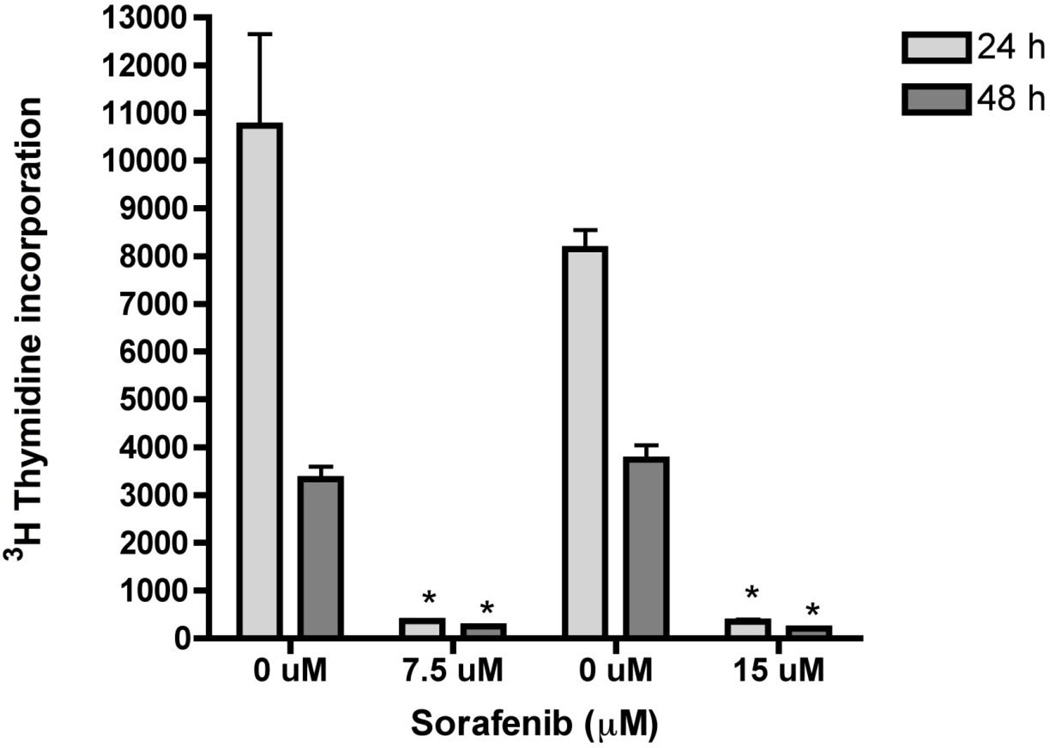
结果 索拉非尼对人星状细胞系LX-2的影响 以前的研究表明索拉非尼抑制HSC中剂量依赖性物质的细胞增殖和活性并诱导凋亡[ 12 ]. 与这些结果一致,浓度为7.5µM和15µM的索拉非尼在检测的剂量和时间点均显著抑制LX-2增殖75%以上( 图1 ). 毒性低至3.5µM(数据未显示)。 为了证实索拉非尼存在时细胞凋亡和氧化应激,检测DNA片段( 图2 )在48小时时,还观察到线粒体活性在48小时显著降低80%( 图3 ).
图1。 索拉非尼抑制HSC增殖。
将LX-2细胞与7.5或15µM索拉非尼培养24和48小时。 通过以下方法评估细胞增殖 三 在纳入评估前4小时添加H-胸腺嘧啶核苷。 索拉非尼在12小时和24小时内均显著抑制DNA合成。 数值为平均值±SD(n=3)* 第页 与对照组相比<0.001。
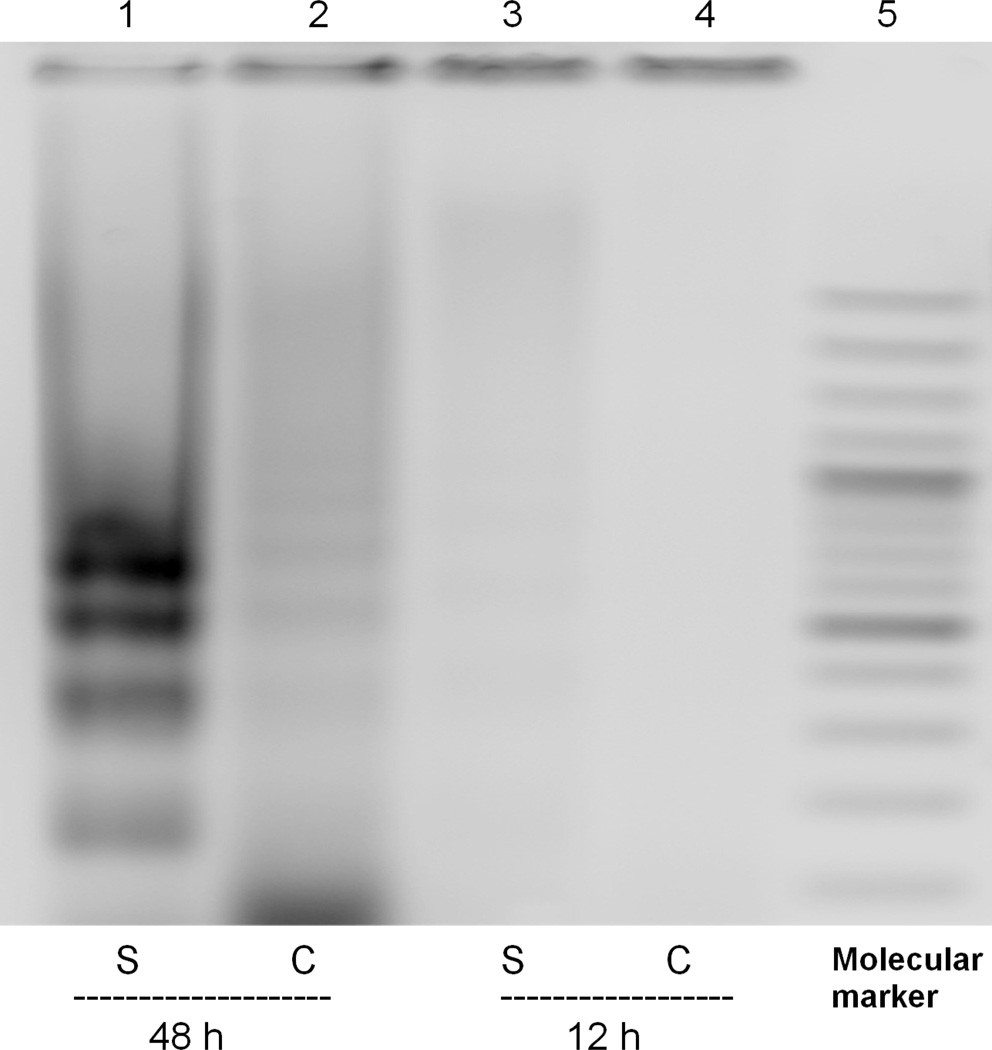
图2。 索拉非尼诱导LX-2细胞凋亡。
用15µM索拉非尼或载药处理的LX-2细胞,并分离DNA。 48小时后,在索拉非尼处理的细胞中观察到约150 kb的DNA片段。
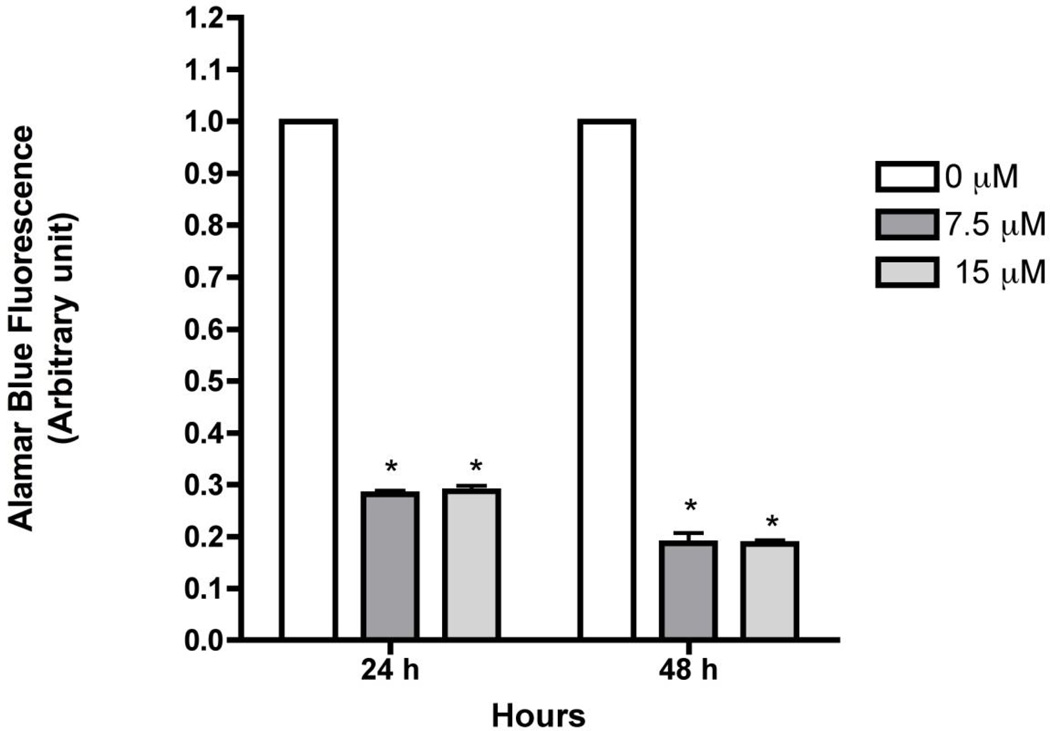
图3。 索拉非尼影响LX-2细胞的细胞活力。
用7.5和15µM处理LX-2细胞12和24小时。 使用alamarBlue®评估细胞活力,并测量荧光。 在这两种浓度下,细胞活力在24小时时降低高达70%,在48小时时降低高达80%。
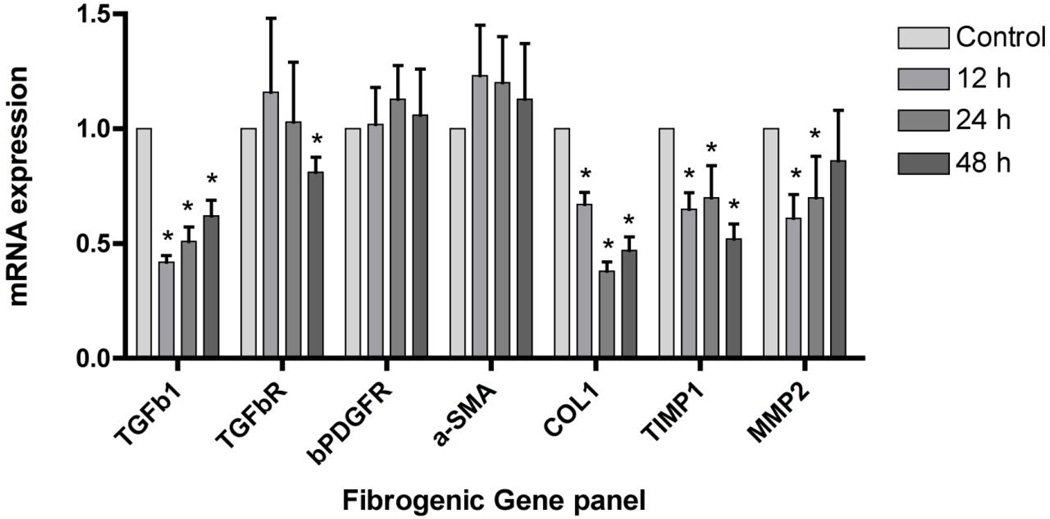
接下来,我们通过实时PCR评估索拉非尼对一组纤维原性mRNA的影响( 图4 ). 在用浓度为7.5µM的索拉非尼处理12、24和48小时的细胞中,编码胶原α1(I)(Collα 1 (1) )、金属蛋白酶组织抑制剂1(TIMP1)和基质金属蛋白酶2(MMP2)。 α-平滑肌肌动蛋白(α-SMA)、血小板衍生生长因子受体-β(β-PDGFR)和转化生长因子β受体1(TGFβR1)的表达没有受到相同程度的影响。 48小时时,TGFβR1的mRNA表达轻微但显著降低。
图4。 索拉非尼下调LX-2细胞中纤维生成基因的表达。
将LX-2细胞与7.5µM索拉非尼培养12、24和48小时。 索拉非尼降低了Collα1、TIMP1、MMP2的成纤维mRNA表达。 α-SMA、β-PDGFR和TGFβR1 mRNA的表达在一定程度上没有受到影响。 48小时时,TGFβR1的mRNA表达轻微但显著降低。 n=3* 第页 <0.001.
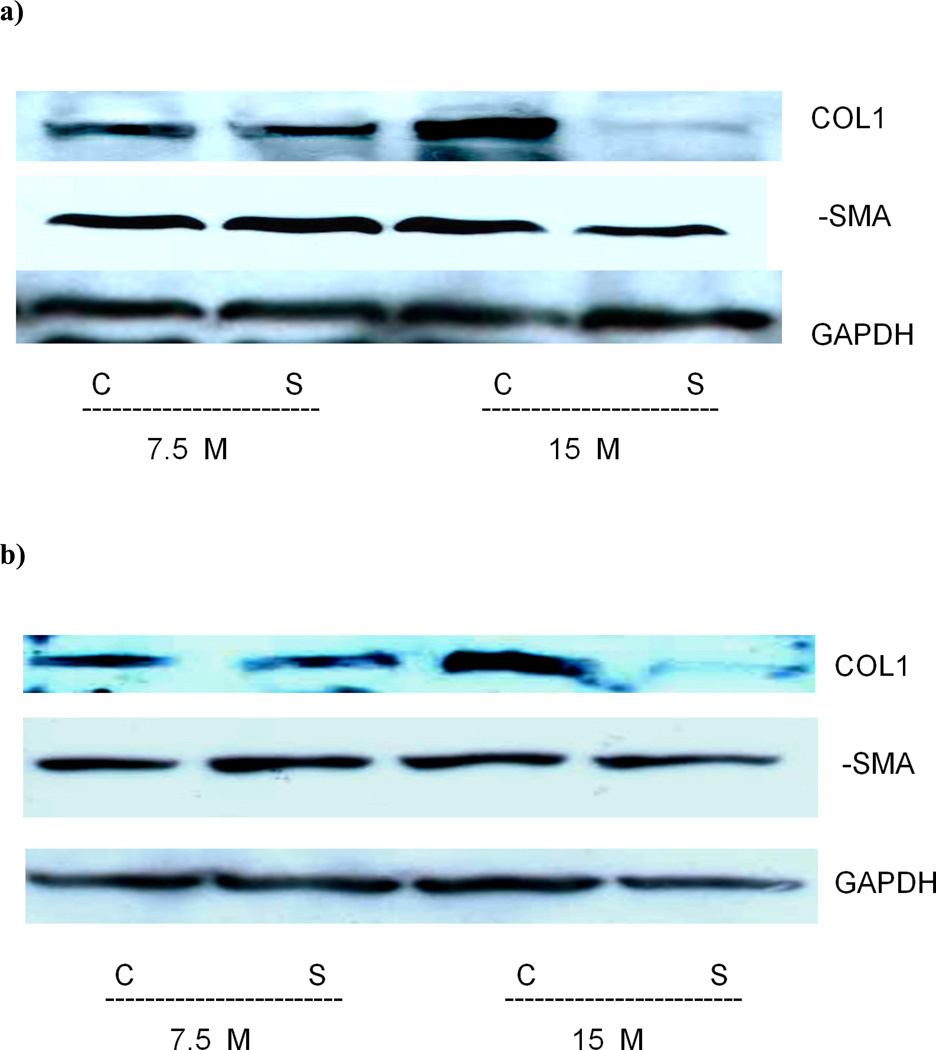
Collα的评估 1 (I) α-SMA蛋白在LX-2细胞中的表达,Western印迹证实索拉非尼抑制Collα 1 (一) 蛋白质表达在15µM而不是7.5µM时,而α-SMA表达在24小时时受到轻微抑制( 图5a ). 这也在原代人星状细胞(HSC)中显示,但α-SMA水平没有受到影响( 图5b ).
图5。 经索拉非尼处理的LX-2和人类原代细胞中胶原1而非α平滑肌肌动蛋白表达减少。
从用7.5和15µM处理24小时的LX-2(5a)或原代人星状细胞(5b)中提取总蛋白。 在15µM的较高浓度下,可以观察到胶原蛋白1的减少。 在原代人星状细胞中检测到α-SMA蛋白略有减少。 GAPDH被用作参考基因。
索拉非尼抗TAA诱导的肝纤维化作用 体内 为了研究索拉非尼对肝纤维化的直接影响,我们进行了 体内 硫代乙酰胺(TAA)致大鼠肝损伤模型的研究[ 13 , 14 ]. 索拉非尼之前未在TAA所致的实质损伤模型中进行过评估,该模型更类似于人类疾病,因为其坏死和炎症程度低于CCl 4 诱导性肝损伤[ 13 ]. 此外,服用TAA 5-6周后,自发可逆性最小(数据未显示)。 使用了四种不同的给药方案,其中所有动物均使用载体或索拉非尼给予TAA 8周,持续4周或8周( 补充图1 ):第1组,每周注射PBS的对照组,用于统计比较; 第2组:同时服用TAA和索拉非尼的“预防性”方案; 第3组:“治疗性”方案,索拉非尼在8周TAA给药开始后仅4周开始服用,随后继续服用4周,以及; 第4组:“可逆性”方案,即在完成8周的TAA后才给予索拉非尼4周。
实时PCR、Western blot、Sirius红染色和Bioquant胶原蛋白定量的综合数据( 图6 , 7 和 8 )证明索拉非尼在“治疗”治疗组(第3组)中最有效,而“预防”方案(第2组)显示出非剂量依赖性疗效,而药物在“可逆性”中无效(第4组)(数据未显示)。
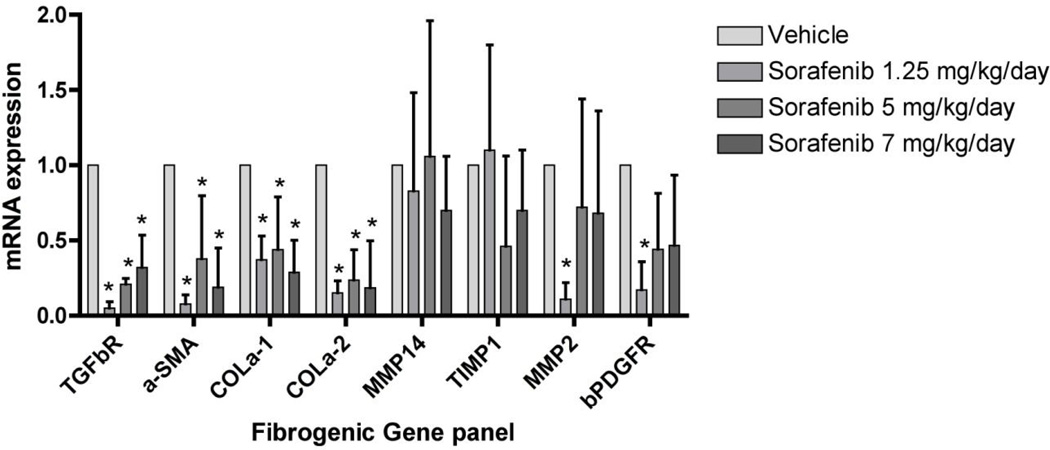
图6。 索拉非尼对TAA诱导的大鼠肝纤维化中成纤维mRNA表达的下调。
实时PCR用于量化与纤维化相关的关键基因的表达。 观察到TGF-β1、a-SMA、I型胶原持续下调,而MMP2、TIMP1和β-PDGFR在低剂量下下调。 MMP14未受到显著影响。 n=3* 第页 <0.001.
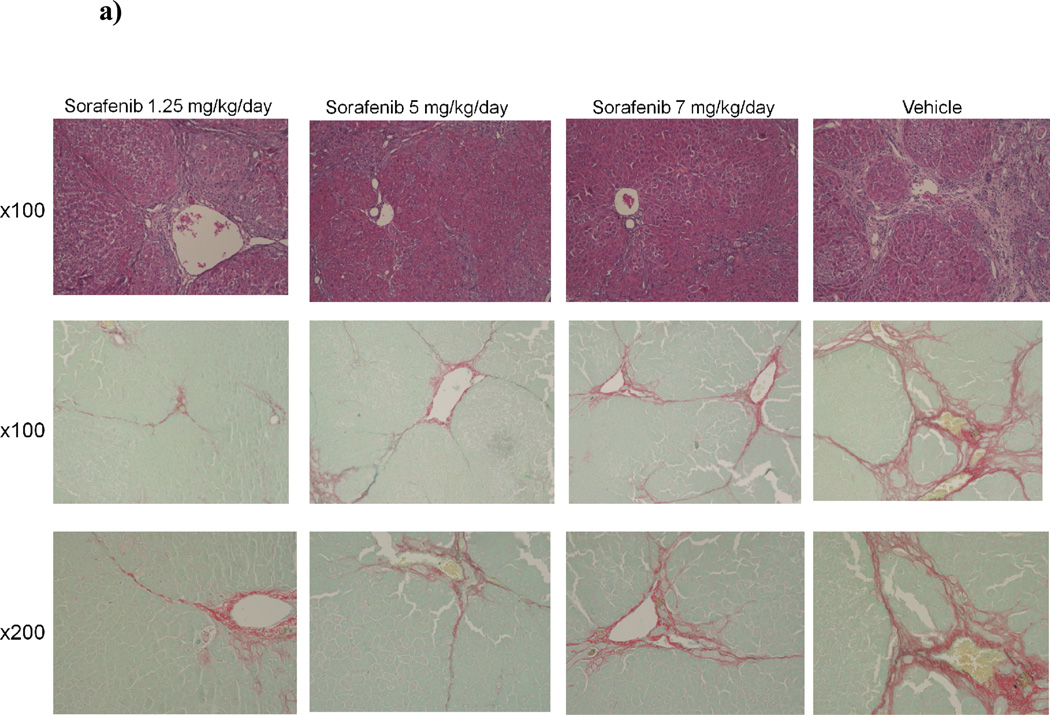
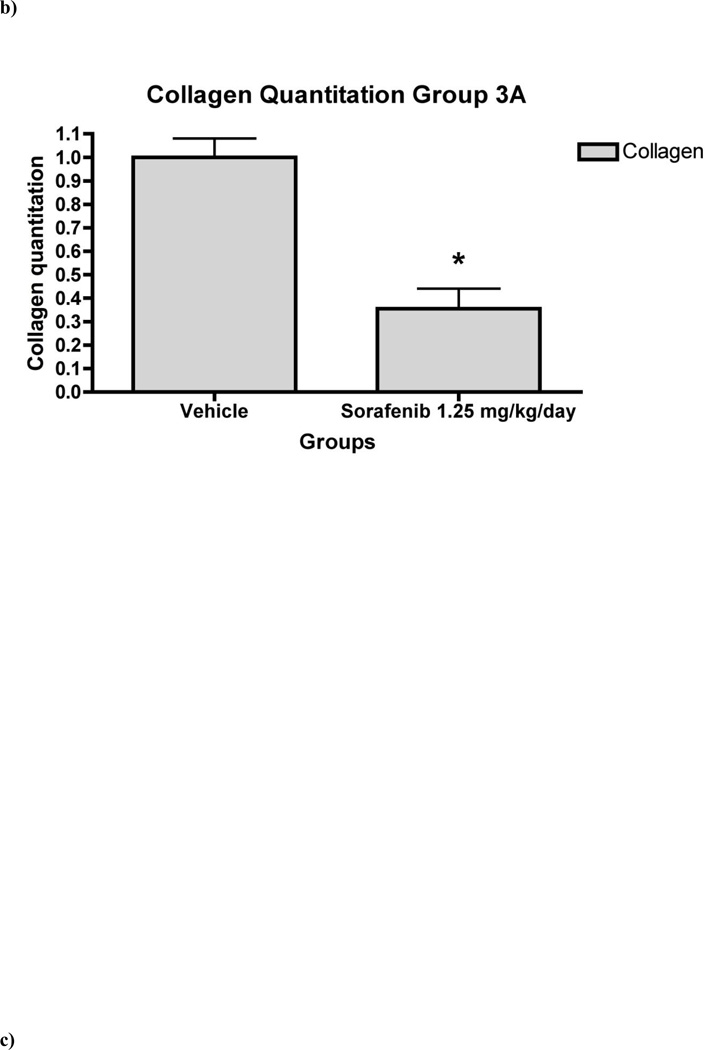
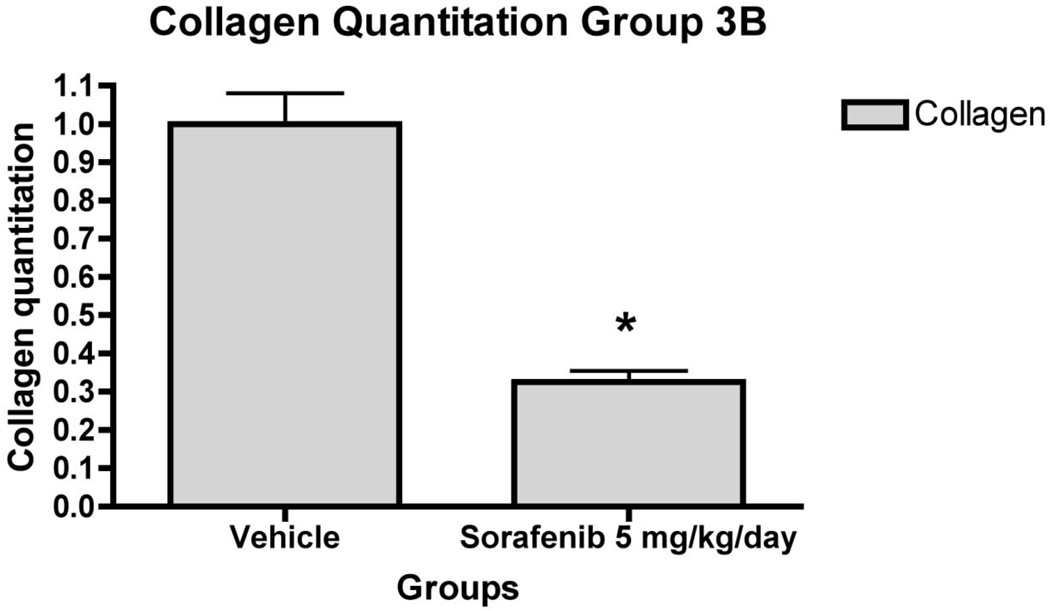
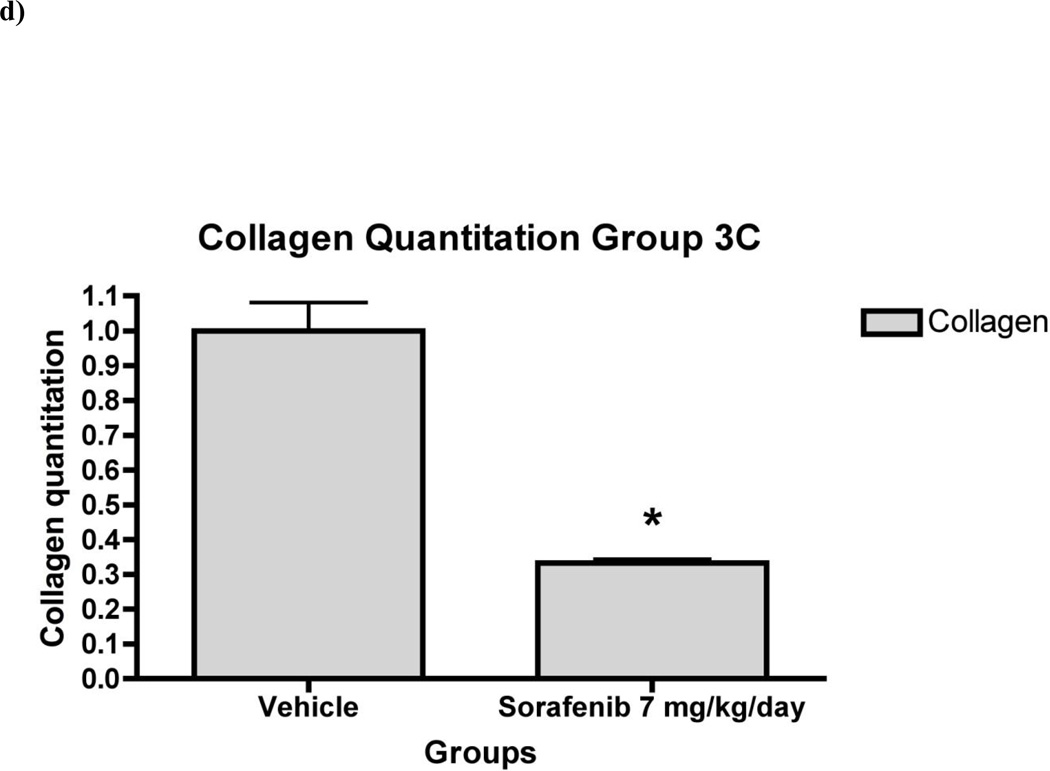
图7。 “治疗”组大鼠肝组织的肝纤维化明显减轻。
7a)第3组动物的代表性肝脏切片中,放大100倍和200倍的H&E和天狼星红的大鼠肝脏组织学。 通过分析每只动物36个天狼星红染肝切片来评估相对纤维化面积(以占肝总面积的百分比表示)。 在100倍放大的条件下采集每个场,并使用计算机化生物量形态测量系统进行分析。 用索拉非尼7b)1.25 mg/kg/天7c)5 mg/kg/天和7d)7 mg/kg/日治疗的动物肝脏纤维化存在统计学显著差异* p<0.001
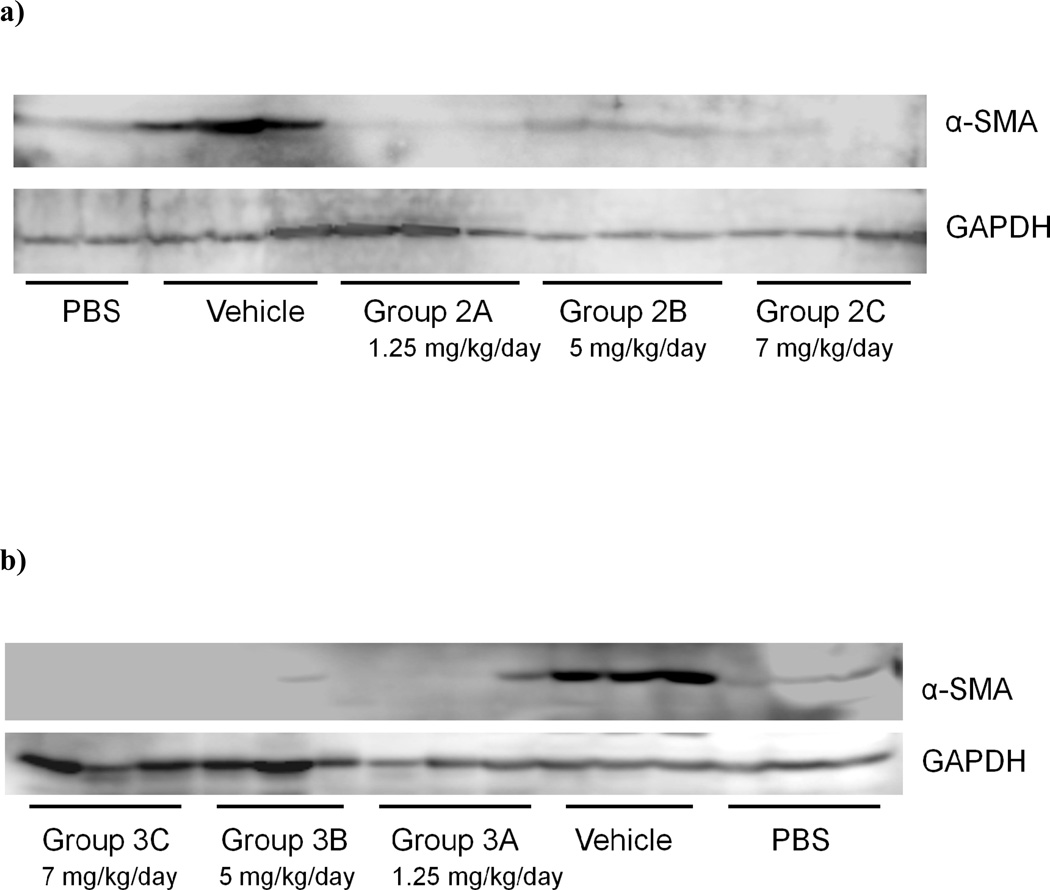
图8。 索拉非尼抑制TAA治疗大鼠肝脏中α-SMA蛋白的表达。
western blot分析索拉非尼治疗大鼠肝脏a-SMA蛋白的表达; a) TAA治疗开始,第2组和b)第4-8周,第3组。 与给药大鼠相比,a-SMA蛋白表达显著降低。
在“治疗”组(第3组)中,纤维生成基因(包括Collα)持续下调 1 (一) 和Collα 2 (I)( 图6 )与形态计量学的胶原蛋白定量结果一致,该结果表明,与车辆注射的肝脏相比,胶原蛋白面积减少了70%( 图7 ). 索拉非尼还下调了MMP2、α-SMA、β-PDGFR和TGFβR1的mRNA( 图6 ). 第4组的mRNA表达或胶原减少没有显著变化(数据未显示)。
除第2组接受索拉非尼5mg/kg/天治疗的动物外,所有亚组的肝脏重量与体重比率均无显著差异,与相应的对照药物亚组相比,该比率有所降低( 表1 ). 各亚组之间的门静脉压力没有显著差异(参见 补充图2、3和4 ).
表1。
体重(g) 肝脏重量(g) 重量/重量(%)
第1组PBS 365-34.5 11.3-1 3.1-0.4
第2组A 321-11.4 17-2.6 5.3-0.9
第2组B 288-44.1 11.2-3.5 3.9-0.8 *
第2组C 229-29.9 9.5-3 4.2-1.1
第2组D 317-16 15-1.4 4.7-0.3
组3A 320-23.8 14.3-1.8 4.5-0.6
组3 B 319-16.2 12.7-3 3.9-0.97
第3组C 311-12.8 11.3-0.8 3.6-0.27
组3 D 342-41 14.7-3 4.3-1.1
组4A 368-19.9 18-1.6 4.9-0.4
第4 B组 371-25.4 14.6-2.5 4.1-0.7
组4C 354-12.9 16.3-1.1 4.6-0.3
第4组D 383-13.5 16.5-1.9 4.3-0.4
索拉非尼抑制TAA治疗大鼠肝脏α-SMA蛋白的表达 如所示 图8a和8b Western blot证实,在TAA治疗开始时(第2组)或第4-8周(第3组),用索拉非尼治疗的动物的α-SMA显著降低。 相反,在TAA给药后8周开始治疗时,索拉非尼对α-SMA蛋白表达没有显著影响,此时肝硬化已经形成(数据未显示)。
讨论 以前的报道表明索拉非尼通过靶向与βPDGF受体和Raf/ERK信号通路相关的酪氨酸激酶抑制肿瘤细胞和HSC的增殖活性[ 4 , 5 , 8 , 15 ]. 在本研究中,我们证明索拉非尼在7.5µM和15µM的浓度下24小时内抑制人类HSC细胞株增殖超过75%,评估方法如下 三 H胸腺嘧啶掺入。 索拉非尼除了抑制HSC增殖外,还诱导LX-2细胞凋亡( 图2 ),这是一项重要发现,因为HSC凋亡促进了肝纤维化的解决[ 16 ].
活化的HSC产生纤维化肝脏的大部分细胞外基质(ECM)蛋白,包括纤维和非纤维胶原[ 17 , 18 ]. TGFβ是一种来源于旁分泌和自分泌的促成纤维细胞因子,是活化HSC产生胶原蛋白1的强烈刺激物[ 19 , 20 ]. 在我们的实验中,索拉非尼抑制TGFβ1和Coll1 体内 以及在培养中,通过蛋白质印迹与蛋白质表达的变化相关( 图5 和 8 ). 在开始服用TAA 4周后开始服用索拉非尼,胶原沉积减少了60%以上(第3组),即使剂量为1.25 mg/kg/天也有效( 图7b )根据实时PCR数据和胶原蛋白定量,以及较高剂量( 图7c和7d ). 胶原蛋白沉积的减少与胶原蛋白α的显著抑制平行 1 (一) 和α 2 (一) 整个肝脏中的mRNA( 图6 ). 此外,原发性mRNA的减少反映了HSC激活的抑制,如肝脏中αSMA和TGFβ1 mRNA表达水平的降低所证明的。 有趣的是,体内对αSMA表达的影响大于分离的星状细胞,这可能表明药物对星状细胞激活的一些影响是通过对邻近细胞,尤其是窦内皮细胞的影响介导的。 与第3组的结果相反,在第4组TAA治疗8周后肝硬化形成后开始治疗4周时,索拉非尼对纤维化基因表达或胶原沉积没有显著影响(数据未显示)。
纤维化反映了基质金属蛋白酶和基质金属蛋白酶介导的细胞外基质生成和降解之间的平衡,基质金属蛋白酶在胶原降解中起关键作用[ 21 ]. 与早期研究一致[ 12 ],我们的结果表明索拉非尼显著降低培养激活的HSC中TIMP1 mRNA的表达,表明该药物通过减少TIMP-1的表达,直接或间接地减少I型胶原合成,可能通过增加净基质蛋白酶活性,从而介导胶原沉积的减少, 一种关键的金属蛋白酶抑制剂。
我们的发现大大改进了临床试验的最佳参数,以评估索拉非尼作为人类慢性肝病的抗纤维化药物。 对HSC激活的主要影响 体内 与药物在持续性肝损伤中的疗效一致,但在肝硬化中不一致。 此外,缺乏对血清AST和ALT的影响表明索拉非尼主要通过其对纤维化的影响而不是通过减轻肝损伤来抗纤维化。 重要的是,该药物在相对较低剂量下的疗效意味着人类抗纤维化剂量可能低于目前用于肝癌治疗的剂量,这将提高耐受性和依从性。 此外,抗纤维化治疗的目标是降低纤维化进展的速度,但不一定完全消除它。 有鉴于此,索拉非尼作为人类抗纤维化药物的评估值得进一步评估。
补充材料 10620_2012_2325_MOESM1_ESM公司
致谢 利息清单
这项工作得到了拜耳奥尼公司(10-0752)与西奈山医学院肝病科签订的研究合同的支持。 斯科特·弗里德曼(Scott Friedman)是拜耳-纽约咨询公司(Bayer-Onyx)的顾问,也是专家咨询委员会(Expert Advisory Board)的成员。 拜耳-Onyx的工作人员对数据的生成或解释或手稿的准备没有任何意见。
参考文献
1. Lee UE,Friedman SL。肝纤维化的机制。 最佳实践和研究。 临床胃肠病学。 2011; 25(2):195–206. doi:10.1016/j.bpg.2011.02.005。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
2 Wong L,等。体内和培养中细胞激活期间大鼠肝脂肪细胞中β-血小板衍生生长因子受体的诱导。 临床研究杂志。 1994; 94(4):1563–1569. doi:10.1172/JCI117497。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
三。 Pinzani M,Marra F.肝星状细胞中的细胞因子受体和信号传导。 肝病研讨会。 2001; 21(3):397–416. doi:10.1055/s-2001-17554。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
4 Borkham Kamphorst E等。PDGF-D在肝纤维化中的促纤维化潜力。 肝病杂志。 2007; 46(6):1064–1074. doi:10.1016/j.jhep.2007.01.029。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
5 Wilhelm SM等。索拉非尼的临床前概述,索拉非尼布是一种针对Raf和VEGF以及PDGF受体酪氨酸激酶信号的多激酶抑制剂。 分子癌症治疗。 2008; 7(10):3129–3140. doi:10.1158/1535-7163.MCT-08-0013。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
6 Llovet JM等。索拉非尼治疗晚期肝癌。 新英格兰医学杂志。 2008; 359(4):378–390. doi:10.1056/NEJMoa0708857。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
7 Escudier B等人。索拉非尼治疗晚期肾细胞癌。 新英格兰医学杂志。 2007; 356(2):125–134. doi:10.1056/NEJMoa060655。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
8 Liu L,et al.Sorafenib在肝癌模型PLC/PRF/5中阻断RAF/MEK/ERK通路,抑制肿瘤血管生成,诱导肿瘤细胞凋亡。 癌症研究。 2006; 66(24):11851–11858. doi:10.1158/0008-5472.CAN-06-1377。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
9 Thabut D等。补充性血管和基质调节途径是索拉非尼治疗肝纤维化的有益机制的基础。 肝病学。 2011; 54(2):573–585. doi:10.1002/hep.24427。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
10 Friedman SL等。从正常人肝脏中分离的肝脂肪细胞和Kupffer细胞:原代培养中的形态和功能特征。 肝病学。 1992; 15(2):234–243. doi:10.1002/hep.184010211。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
11 Xu L,等。人肝星状细胞系,LX-1和LX-2:肝纤维化分析的新工具。 内脏。 2005; 54(1):142–151. doi:10.1136/gut.2004.042127。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
12 王毅等。索拉非尼对肝星状细胞和肝纤维化抗纤维化作用的新见解。 肝病杂志。 2010; 53(1):132–144. doi:10.1016/j.jhep.2010.02.027。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
13 Muller A等。硫代乙酰胺诱导大鼠肝硬化样肝损伤——该动物模型的有效性和可靠性。 实验病理学。 1988; 34(4):229–236. doi:10.1016/s0232-1513(88)80155-5。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
14 Li X,Benjamin IS,Alexander B.大鼠硫代乙酰胺诱导的大结节性肝硬化的可复制生成,无死亡。 肝病杂志。 2002; 36(4):488–493. doi:10.1016/s0168-8278(02)00011-9。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
15 Wilhelm SM等。BAY 43-9006具有广谱口服抗肿瘤活性,靶向参与肿瘤进展和血管生成的RAF/MEK/ERK途径和受体酪氨酸激酶。 癌症研究。 2004; 64(19):7099–7109. doi:10.1158/0008-5472.CAN-04-1443。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
16 Iredale JP等。大鼠肝纤维化自发消退的机制。 肝星状细胞凋亡和金属蛋白酶抑制剂在肝脏的表达降低。 临床研究杂志。 1998; 102(3):538–549. doi:10.1172/JCI1018。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
17 Parola M,Marra F,Pinzani M。肌成纤维细胞样细胞和肝纤维化:快速发展情景中的新兴概念。医学的分子方面。 2008; 29(1–2):58–66. doi:10.1016/j.mam.2007.09.002。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
18 Friedman SL.肝纤维化的分子调控,组织损伤的综合细胞反应。 生物化学杂志。 2000; 275(4):2247–2250. doi:10.1074/jbc.275.4.2247。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
19 Zavadil J,Bottinger EP。 TGF-β和上皮-间充质转化。 致癌物。 2005; 24(37):5764–5774. doi:10.1038/sj.onc.1208927。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
20 Garcia-Trevijano ER等。转化生长因子β1通过过氧化氢-C/EBPβ依赖机制诱导大鼠肝星状细胞中α1(I)前胶原mRNA的表达。 肝病学。 1999; 29(3):960–970. doi:10.1002/hep.510290346。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
21 Yoshiji H等。金属蛋白酶组织抑制剂-1减弱转基因小鼠的自发性肝纤维化消退。 肝病学。 2002; 36(第4部分第1节):850-860。 doi:10.1053/jhep.2002.35625。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
关联数据 本节收集本文中包含的任何数据引用、数据可用性声明或补充材料。
补充资料 10620_2012_2325_MOESM1_ESM公司