摘要 介绍 外周血单个核细胞(PBMC)表达Ras鸟嘌呤核苷酸释放蛋白4(RasGRP4)。 我们研究的目的是鉴定人类血液中表达hRasGRP4的细胞,然后确定是否有任何类风湿关节炎(RA)患者的hRasGRP4发生改变。
方法 从正常人的PBMC中纯化单核细胞和T细胞,并评估其RasGRP4 mRNA/蛋白的表达。 通过实时定量PCR评估健康志愿者和RA患者PBMC中RasGRP4转录物的水平。 还测定了RasGRP4 cDNA的核苷酸序列。 评估PBMCs/单核细胞中RasGRP4蛋白的表达。 重组hRasGRP4在哺乳动物细胞中表达。
结果 循环CD14 + 正常人的细胞表达hRasGRP4。 RA患者PBMC中hRasGRP4转录物的水平显著高于健康人。 对这些PBMC的hRasGRP4 cDNA进行序列分析,发现了10个新的剪接变异体。 RA患者的hRasGRP4转录物异常剪接的频率高于正常人。 其中一种异常剪接变异体的存在与RA有关。 PBMC中hRasGRP4蛋白水平趋于较低。 正如预期的那样,缺陷转录物导致P44/42有丝分裂原活化蛋白(MAP)激酶活化方面的改变和/或非功能蛋白。
结论 RA患者PBMC中hRasGRP4转录物缺陷亚型的鉴定增加了以下可能性:发育中单核细胞中hRas GRP4表达失调在RA患者亚群中起致病作用。
介绍 Ras鸟嘌呤核苷酸释放蛋白(RasGRP)4是一种钙调节的鸟氨酸核苷酸交换因子(GEF)和二酰甘油(DAG)/佛波酯受体。 Yang及其同事在寻找肥大细胞(MC)中选择性表达的新转录物时,最初克隆了小鼠、大鼠和人类的cDNA以及编码这种信号蛋白的基因[ 1 - 三 ]. 其他人在搜索编码急性髓细胞白血病患者致癌蛋白的转录物时分离出hRasGRP4 cDNA[ 4 ]. 小鼠和人类RasGRP4 mRNA在未定义的外周血单个核细胞(PBMC)中丰富[ 1 , 三 ]. 尽管所有检测到的正常人和小鼠组织中的成熟MC都表达RasGRP4[ 1 - 三 ],该信号蛋白是否在另一种细胞类型中表达尚待确定。
小鼠、大鼠和人RasGRP4的不同亚型[ 1 , 2 , 5 ]其家族成员RasGRP1已被鉴定为在每种情况下都是由其前体转录物的可变剪接引起的。 例如 滞后 由于未能正确处理前体mRasGRP1转录物,小鼠患上类似于系统性红斑狼疮(SLE)的淋巴增生性疾病[ 6 ]. 为了支持这些小鼠数据,我们确定了一组SLE患者,他们的循环T细胞和PBMC中缺乏hRasGRP1的正常亚型[ 7 ]. 在少数肥大细胞增多症和哮喘患者的PBMC以及从一名MC白血病患者建立的HMC-1细胞系中检测到hRasGRP4转录物的剪接变体[ 1 ]. 这些数据提高了hRasGRP4在某些疾病状态下表达改变的可能性。
RasGRP4调节HMC-1细胞系中许多基因的表达,包括编码前列腺素D的转录物 2 合成酶、转录因子GATA-1和白细胞介素(IL)-13抑制受体IL13Rα2[ 5 , 8 ]. 为了支持这些 在体外 数据,成熟的RasGRP4 + 小鼠和大鼠腹腔中的MC优先将花生四烯酸代谢为前列腺素D 2 [ 9 ]因为他们的前列腺素D水平很高 2 合成酶[ 10 ].
类风湿关节炎(RA)是一种慢性炎症性疾病,其特征是独特的滑膜炎,导致关节进行性破坏。 虽然已知几种遗传易感性和环境因素会增加患RA的风险,但其发病机制尚不完全清楚[ 11 , 12 ]. MC与RA和这种自身免疫性疾病的实验模型有关。 从RA患者关节分离的组织标本中hTryptase-β的数量增加 + MC和这些效应细胞往往位于血管翳和软骨的交界处,以及血管翳侵入皮质骨的区域[ 13 - 15 ]. MC-不足WBB6F 1 -工具包 W公司 /工具包 W-v型 和WCB6F 1 -基特尔 斯里兰卡 /基特尔 Sl-d公司 小鼠对胶原蛋白、葡萄糖-6-磷酸异构酶或甲基化牛血清白蛋白(BSA)自身抗体诱导的关节炎具有抵抗力[ 16 - 19 ]. 活化的MC产生多种促炎因子,包括各种颗粒丝氨酸蛋白酶。 在K/BxN鼠标血清传输中[ 20 ]和甲基化BSA/IL-1[ 19 ]关节炎模型,MC-限制性胰蛋白酶•肝素复合物调节中性粒细胞的积聚和软骨中聚集蛋白聚糖的丢失。
MC、单核细胞和巨噬细胞来源于人类共同的祖细胞[ 21 ],和人胰蛋白酶-β + MC可以由人脐血和PBMC生成[ 22 ]. 循环髓样细胞也分化为组织旁巨噬细胞和树突状细胞。 RA滑膜中富含巨噬细胞。 激活后,这些免疫细胞释放大量炎症细胞因子和生长因子(例如,IL-1β、IL-6、肿瘤坏死因子-α(TNF-α)和转化生长因子-β),参与滑膜炎症和增生[ 23 - 25 ]. 因此,MC和髓细胞在RA的病理生理学中起着关键作用。
在本研究中,我们发现CD14 + 人PBMC中的髓细胞表达hRasGRP4。 由于hRasGRP1的失调发生在SLE患者的亚群中[ 7 ]我们假设hRasGRP4可能在PBMC中异常表达,从而在某些RA患者中产生MC、巨噬细胞和可能的其他细胞类型。 我们现在报告,RA患者PBMC中hRasGRP4转录物的异常剪接很常见。 累积的数据增加了hRasGRP4表达改变在RA患者子集中发生的可能性。
材料和方法 健康个体和RA及其他自身免疫性疾病患者 研究了42名明显健康的日本个体(6名男性和36名女性,49.8±6.7岁,平均±SD)和57名日本RA患者(16名男性和41名女性,61.1±13.5岁,平均值±SD)。 根据美国风湿病学会1987年修订的自身免疫性疾病分类标准,风湿病学家将后一队列中的所有患者诊断为RA[ 26 ]. 我们RA患者的平均病程为126个月(范围为0至504个月)。 28个关节的疾病活动评分(DAS28ESR4)[ 27 ]分析时为3.3±1.3(范围为1.3至6.8)。 其中51名患者(89%)正在接受抗风湿药物治疗。 其中37名(65%)、13名(27%)、7名(12%)和39名(68%)患者分别服用了甲氨蝶呤、磺胺吡啶、布西拉明和泼尼松龙。 三名患者服用生物制剂。 36名患有其他自身免疫性疾病的患者作为自身免疫性对照。 对照组患者患有SLE( n个 =10),多发性肌炎/皮肌炎( n个 =8),系统性硬化( n个 =8),或Sjögren综合征( n个 = 10). 我们的研究得到北海道大学医学研究生院人类伦理委员会的批准,并获得了每个受试者的知情同意。
细胞分离 使用Ficoll-paque PLUS(瑞典乌普萨拉Amersham Biosciences)从健康个体或患者抽取的约10 ml外周血中采集PBMC。 CD14号机组 + 使用微珠和磁性细胞分选分离单元(Miltenyi Biotec,Bergisch Gladbach,德国)从产生的PBMC中纯化细胞。 CD14、CD3和CD19微球通过负选择富集PBMC中的非单核细胞、非T细胞和非B细胞。 这部分被认为含有未分化细胞,包括肥大细胞祖细胞[ 28 ]. 还使用RosetteSep人类T细胞浓缩鸡尾酒(StemCell Technology,加拿大不列颠哥伦比亚省温哥华)从PBMC中纯化T细胞。 对于CD14,获得的细胞的纯度通常大于85% + 髓系细胞和>95%的CD3 + T细胞,分别使用藻红蛋白标记的抗CD14抗体和抗CD3抗体(BD Biosciences)在FACS Calibur流式细胞仪(BD bioscience,San Jose,CA,USA)上进行评估。
RA患者中hRasGRP4转录水平的评估和新hRasGRP4转录物的分离 从整个PBMC中收集总RNA,并使用RNeasy Mini试剂盒(Qiagen,Valencia,CA,USA)分离细胞。 使用QuantiTect逆转录试剂盒(Qiagen)将获得的转录物转化为cDNA。 然后用PCR方法扩增hRasGRP4 cDNA的编码区,该方法使用正向5’-AGCATGAACAGAAAGACAGATAAG-3’和反向5’-TGTCTTAGGAATCGGCTTGGA-3’引物,这些引物对应于GenBank登录号中注明的正常hRasGP4转录物中翻译起始和终止位点的核苷酸序列 [ NM:170604 ]分别是。 经过热变性步骤后,后续PCR步骤的25个循环中的每一个都包括94℃下的15 s变性步骤、59℃下的30 s退火步骤和72℃下的1.5 min延伸步骤。 编码看家蛋白人类甘油醛-3-磷酸脱氢酶(hGAPDH)的转录物在这些转录物分析中起控制作用。
采用实时定量PCR(qPCR)方法监测38名健康人、41名RA患者和36名其他风湿性疾病患者分馏细胞系和PBMC中hRasGRP4转录物的总体水平。 在这些实验中,使用ABI Prism 7000序列检测系统(Applied Biosystems,Foster City,CA,USA)和特异于hRasGRP4(Hs00364781m1)和hGAPDH(Hs00266705m1)的TaqMan MGB探针(Applied Biosystems),将hRasGRP4转录物的水平标准化为hGAPDH转录物的水平。 我们在这些qPCR中选择了一个hRasGRP4特异性引物组,该引物组识别位于外显子7和8之间的连接核苷酸序列。 使用可比较的循环阈值(C T型 )ΔC的方法 T型 是RNA样本中hRasGRP4转录物相对于hGAPDH转录物的水平。 每个样本中hRasGRP4转录物表达的差异被定义为mRNA水平的折叠变化2 -ΔΔCT .
还使用从16名健康人、23名RA患者(18名接受治疗,5名未接受治疗)、, 和20例其他自身免疫性疾病患者(5例SLE,5例Sjögren综合征,5例炎性肌炎和5例系统性硬化症。在每一例中,生成的hRasGRP4 cDNA亚克隆到pcDNA3.1 V5-His-TOPO(Invitrogen,Carlsbad,CA,USA), 使用ABI Prism 3130遗传分析仪(Applied Biosystems)对每个个体的五个任意选择的cDNA进行测序。
巨噬细胞和破骨细胞中hRasGRP4转录水平的评估 巨噬细胞从外周血CD14中分化出来 + 使用先前报道的技术在几种细胞因子存在下的细胞[ 29 ]. 简言之,巨噬细胞是通过培养CD14获得的 + 细胞在M-CSF(50 ng/ml)的存在下。 在37°C的湿度室中培养7天后,收集分化细胞。 破骨细胞在M-CSF(33 ng/ml)和RANK配体(66 ng/ml)的存在下分化(Lonza Walkersville,Inc.,Walkersvelle,MD,USA)。 14天后,收集细胞。 从每个细胞系收集RNA,并使用针对hRasGRP4和hGAPDH的TaqMan MGB探针检测两个细胞系的hRasGRP4表达。 评估破骨细胞组织蛋白酶K(分化破骨细胞的特异标记之一)的表达,以确认其分化(探针ID:Hs00166156m1)(应用生物系统)[ 30 ]. RasGRP1在PBMC和破骨细胞中的表达也进行了检测(探针ID:Hs00996734m1)(应用生物系统)。
使用抗肽方法获得识别hRasGRP4 N末端的抗体 针对新的14聚体合成肽MNRKDSKRKSHQEC产生兔抗hRasGRP4抗体,该肽对应于hRasGP4正常亚型的N末端。 基本局部比对搜索工具(BLAST)的蛋白质搜索显示,在任何其他已知人类蛋白质中没有类似序列。 使用该合成肽,产生并纯化兔抗hRasGRP4多克隆抗体,如前所述,用于产生兔抗hRasGRP1抗体[ 7 ]. 所生成的抗hRasGRP4抗体的特异性通过使用免疫印迹和免疫组织化学中用于免疫的相同肽的吸收试验得到证实,该肽使用上皮细胞系HEK-293(系CRL-1573;美国型培养物收藏)的裂解物进行免疫 用表达载体转染,用C末端V5表位标签编码hRasGRP4(数据未显示)。
利用哺乳动物细胞系和无细胞转录-翻译实验制备重组hRasGRP4蛋白 编码hRasGRP4及其剪接变异体(变异体5和6)的表达结构被转染到通常缺乏hRasGRP4的上皮细胞系HEK-293中。 将编码正常RasGRP4及其剪接变异体的cDNA亚克隆到pcDNA3.1 V5-His-TOPO(Invitrogen)中。 我们制作了带有或不带有C端子V5标记的hRasGRP4构造。 使用Lipofectamine 2000试剂(Invitrogen)进行转染。 通过SDS-PAGE免疫印迹和免疫组织化学方法评估RasGRP4在蛋白水平的存在。 根据制造商的说明,使用PROTEINscript II T7试剂盒(美国德克萨斯州奥斯汀Ambion)进行无细胞转录:翻译分析。 对编码全长正常RasGRP4、剪接变体5和剪接变体6的结构进行系统测试,并通过免疫印迹法进行评估。
免疫组织化学 对PBMC-derived CD14进行免疫组织化学 + 髓系细胞和T细胞,以及表达hRasGRP4的HEK293细胞。 未转染的HEK293细胞作为阴性对照。 在每种情况下,使用Shandon Cytospin 4细胞离心机(Thermo Fisher Scientific Inc.,Waltham,MA,USA)将总共500000个细胞放置在载玻片上。 hRasGRP4基因 + HEK293细胞在Lab-Tek II室滑片系统(美国纽约州罗切斯特Nalge Nunc International)上培养。 将制备好的载玻片固定并用4%多聚甲醛和0.2%皂苷进行渗透(eBioscience,加州圣地亚哥,美国)。 使用3%过氧化氢在无水甲醇中的溶液淬火内源过氧化物; 用3%的BSA溶液在磷酸盐缓冲盐水中进行封闭。 使用我们的兔抗hRasGRP4抗体(1μg/ml)或兔抗β-肌动蛋白抗血清(Sigma-Aldrich,St.Louis,MO,USA)稀释至1:80,然后使用相关的生物素化抗体和过氧化物酶结合链霉亲和素(Nichirei Biosciences,Tokyo,Japan)进行免疫组织化学。 无关的兔IgG作为我们抗hRasGRP4抗体的另一个阴性对照。 使用我们的抗hRasGRP4抗体(1μg/ml)和合成hRasGRP4衍生肽(100 ng/ml)的混合物进行吸收染色。 使用含有3,3'-二氨基联苯胺(DAB)的0.6%过氧化氢(Nichirei Biosciences)溶液观察免疫反应。 用苏木精进行核染色,并用光学显微镜检查染色细胞。
免疫印迹法 使用Lightning-link HRP偶联试剂盒(英国剑桥Innova Biosciences)将抗hRasGRP4抗体与辣根过氧化物酶偶联后,CD14中hRasGRP4蛋白的水平 + 如前所述,使用免疫印迹方法评估外周血细胞[ 7 ]. 使用NIH支持的ImageJ软件测量免疫反应带的密度[ 31 ]. 抗磷酸P44/42丝裂原活化蛋白激酶(MAPK)(Erk1/2)抗体和抗pan-P44/42 MAPK抗体购自Cell Signaling Technologies(马萨诸塞州贝弗利)。
统计分析 采用X平方检验或Fisher精确检验比较患者PBMC中已识别hRasGRP4变异的频率。 为了评估特定hRasGRP4亚型的表达,我们首先将ΔΔ-CT值的正常范围定义为健康志愿者的平均值±2 SD。 然后量化RA患者中hRasGRP4转录物的水平。 使用Fisher精确检验比较对照个体和患者中hRasGRP4转录物的表达。 使用Mann-Whitney的U检验比较剪接变异体的发生率和该基因的表达水平。 在所有统计分析中,使用了JMP 9.0版软件(SAS Institute Inc.,Cary,NC,USA)。
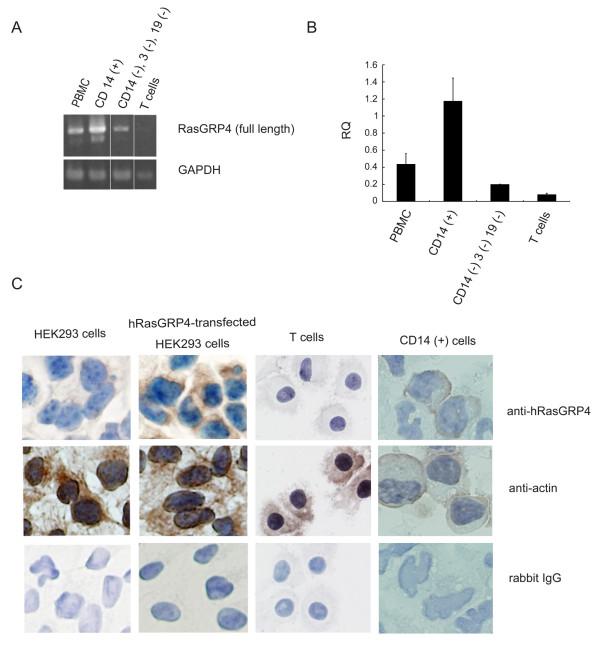
结果 CD14中hRasGRP4 mRNA和蛋白亚型的鉴定 + 髓样细胞 循环的 体内 -分化的、未分化的人PBMC和PBMC衍生的CD3 + T细胞,CD14 + 髓细胞和CD14 - /CD3(CD3) - /CD19编号 - 最初使用半定量逆转录聚合酶链反应方法评估细胞是否存在hRasGRP4 mRNA。 使用与蛋白质编码结构域的起始和终止相对应的引物,发现编码hRasGRP4正常同种型的大约1.5-kb的cDNA在循环CD14中丰富 + 正常人PBMC中的细胞(图 1安培 ),如前所述[ 1 ]. 使用不同引物的实时qPCR方法证实了这些细胞中存在大量hRasGRP4 mRNA(图 1B年 ). CD14的非T、非B、非单核细胞群体 - /CD3(CD3) - /CD19编号 - 这些PBMC中的细胞含有相对较低量的hRasGRP4mRNA,并且在富集的外周血T细胞中hRasGRP4转录物的水平低于检测。 与这些转录物数据一致,CD14 + 细胞纯化自 体内 -经免疫组织化学评估,分化的人PBMC含有hRasGRP4蛋白(图 1摄氏度 ). 正如预期的那样,T细胞中未检测到免疫反应性hRasGRP4蛋白。 hRasGRP4水平不同的转染HEK293细胞作为阳性和阴性对照。
图1。
外周血hRasGRP4表达的评价 . A类 ,评估未分离外周血单个核细胞(PBMC)、PBMC衍生CD14中hRasGRP4 mRNA水平 + 细胞,CD14 - /CD3(CD3) - /CD19编号 - 从健康个体分离的细胞和T细胞。 使用hRasGRP4基因第1外显子/第17外显子引物进行RT-PCR/凝胶分离,以评估每种细胞类型中的转录表达。 在下部面板中使用人类甘油醛-3-磷酸脱氢酶(hGAPDH)特异性引物作为阳性对照。 显示了三个独立实验的代表性结果。 B类 ,使用识别外显子7和外显子8连接部分的引物集的qPCR方法。 增量-C T型 hRasGRP4转录水平相对于CD14中hGAPDH转录水平 + 细胞定义为1。 qPCR分析以一式三份的方式进行三次,误差条表示标准误差。 C类 ,免疫组织化学; PBMC衍生CD14 + 骨髓细胞和T细胞用抗hRasGRP4抗体染色(顶部面板)。 对于阴性和阳性对照,hRasGRP4蛋白水平不同的HEK293细胞也用抗hRasGRP4抗体染色。 对于其他对照组,复制细胞用抗β-肌动蛋白抗体(中间面板)或无关的兔IgG(底部面板)染色。 显示了三到四个程序的代表性结果。
CD14期间hRasGRP4转录水平 + 细胞发育为巨噬细胞和破骨细胞 hRasGRP4转录水平下降,而CD14 + 外周血细胞分化为巨噬细胞(附加文件 1 /图s1A)。 破骨细胞中RasGRP4表达减少(附加文件 1 /图s1B,左侧面板),至少RasGRP1没有对此进行反击(数据未显示)。 光镜下证实了多核破骨细胞的发育。 组织蛋白酶K在这些细胞中的表达升高得到证实(附加文件 1 /图s1B,右面板)。
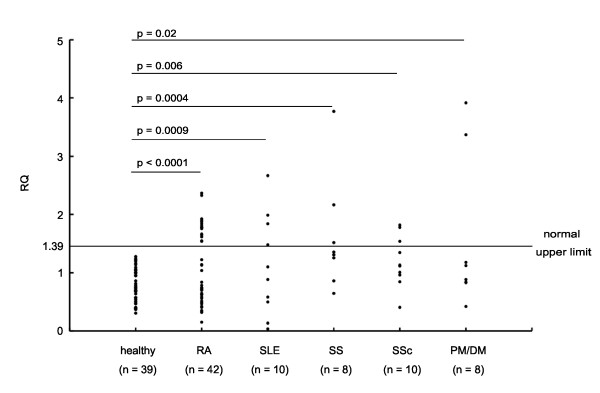
RA和其他自身免疫性疾病患者hRasGRP4转录物的定量评估 我们将PBMC中hRasGRP4转录物的正常水平指定为健康个体PBMC中hRasGRP4转录物的平均±2 SD。 41%的RA患者的hRasGRP4转录物水平高于正常水平( P(P) <0.0001)(图 2 ). 患有其他自身免疫性疾病(SLE)患者的PBMC中hRasGRP4转录水平也较高( P(P) =0.0009),多发性肌炎/皮肌炎( P(P) =0.02),系统性硬化( P(P) =0.006)和Sjögren综合征( P(P) = 0.0004). 因此,PBMC中hRasGRP4 mRNA数量增加似乎是识别自身免疫性疾病患者的有用标记。 尽管有这些数据,但RA患者PBMC中hRasGRP4转录水平与所检查的临床特征(例如年龄、病程、DAS28、血沉(ESR)或血清基质金属蛋白酶3(MMP3))无关(数据未显示)。 同样在健康个体中,RasGRP4表达水平不受年龄的影响(数据未显示)。 此外,hRasGRP4转录水平不受我们RA患者PBMC中单核细胞比率(以淋巴细胞和单核细胞总数表示)的影响(附加文件 2 /图s2)。 因此,使用PBMC而不是纯化的单核细胞来评估hRasGRP4转录水平是可以接受的。
图2。
PBMC中hRasGRP4 mRNA水平的评估 使用qPCR方法量化健康个体和患有类风湿关节炎(RA)和其他风湿性疾病(如SLE、Sjögren综合征(SS)、系统性硬化(SSc)和多发性肌炎/皮肌炎(PM/DM))的患者外周血单个核细胞(PBMC)中hRasGRP4转录物的总体水平。 所示为每个样本中hRasGRP4转录物的人甘油醛-3-磷酸脱氢酶(hGAPDH)校正水平的相对数量(RQ)。 其中一名健康个体被分配来确定1的值。 在所有健康个体和患者中,以一式三份的方式进行分析,平均值绘制在图中。转录水平的正常上限定义为健康对照组的平均转录水平+2SD。 hRasGRP4转录水平高于正常上限的患者数量采用Fisher精确检验进行评估。
鉴定10个新的hRasGRP4转录物,这些转录物经历了前体转录物的缺陷剪接 对16名健康人和23名RA患者(包括5名未接受治疗的患者)的hRasGRP4 cDNA进行序列分析,发现hRasGRP4的12种亚型是由其前体转录物的选择性剪接引起的(图 三 ). 四种先前确定的hRasGRP4亚型被指定为剪接变异体1至4[ 1 ]. 在我们的RA患者中发现的两种选择性剪接亚型对应于变异体1和2。 然而,其他10种亚型(指定为变体5至14)之前没有描述过。 这些新的剪接变体缺乏整个外显子9(剪接变体5,GenBank登录号:( FJ768677型 )); 第9外显子的前207个核苷酸(剪接变异体6,GenBank登录号:( FJ768678型 )); 外显子7(剪接变异体7,GenBank登录号:( 峡湾768679 )); 外显子7、8和9(剪接变异体8,GenBank登录号:( FJ768680型 ]); 外显子7和8(剪接变异体10,GenBank登录号:( FJ768682型 )); 外显子6(剪接变异体11); 以及在外显子12的5’端的12个核酸(剪接变体13)。 剪接变体9中的内含子14尚未被移除(GenBank登录号:( FJ768681型 )); 在剪接变异体12中,来自内含子11的143个核苷酸没有被删除; 内含子11中的143个核苷酸和内含子14中的95个核苷酸没有从剪接变异体14中删除。
图3。
PBMC中编码异常hRasGRP4亚型的新转录物 顶部面板显示了hRasGRP4的外显子结构和相应的功能基序,包括Ras交换基序(REM)、CDC25-like GEF结构域(CDC25框)、钙结合EF-hands和二酰甘油结合C1结构域。 下部面板中的拼接变异体5至14对应于我们RA患者中发现的10个新的hRasGRP4转录物。 如果翻译,则显示每个表达亚型中的氨基酸(AA)数量。 从16名健康人中分离并测序了80个hRasGRP4特异性cDNA。 其中2、13、1、1和1个cDNA分别对应于剪接变异体1、5、6、7和8。 该对照组中其余62个cDNA序列与正常全长hRasGRP4亚型相对应。 分别从18名接受治疗的RA患者和5名未治疗的RA病人中分离并测序了90和25 hRasGRP4特异性cDNA。 显示了这些患者中识别出的缺陷转录本的类型和数量。 对20例其他自身免疫性疾病患者的100个hRasGRP4 cDNA进行测序,结果显示36个缺陷hRasGRP4转录本和64个正常hRasGRP4转录物。 变体1、9、12和14具有提前翻译终止密码子(*)。 内含子1为3.9 kb,这个约17.2 kb的人类基因中的许多其他内含子大于1 kb。 由于用于识别和定量新亚型的PCR方法会遗漏包含内含子1的亚型,因此可能在含有一个或多个大内含子的PBMC中存在额外的剪接变体。
在我们的RA患者组中最常见的异常hRasGRP4转录本是剪接变异体5,它缺少整个外显子9。 该外显子的缺失不会导致处理的转录物中的帧移位异常或过早翻译终止密码子,但会导致92个氨基酸的缺失,这些氨基酸对应于信号蛋白中CDC25样催化结构域的C末端一半[ 1 ]. 第二个最常见的亚型是变体6,它导致69个相同氨基酸的损失。 剪接变异体9、12和14是变化更为严重的亚型,因为它们在每个实例中都会产生一个提前翻译终止密码子。 hRasGRP4剪接变体和剪接变体6在RA患者PBMC中的克隆数更常见(表 1 ). 20个克隆对应于我们RA患者的剪接变异体6,而不是来自少数表达该变异体多克隆的患者。 剪接变异体6的分布是8例RA患者的一个克隆和6例RA患者中的两个克隆。 我们的RA患者中,没有一名患者的序列克隆中的剪接变异体6超过一半。 除了剪接变异体6外,其他自身免疫性疾病患者的PBMC中这些剪接变种的频率与健康人相比没有显著差异。 剪接变异体6在正常人PBMC中几乎未检测到。 在健康受试者中,RasGRP4剪接变异体的频率与年龄无关(数据未显示)。 在RA患者中,剪接变异体6的存在与任何评估的临床特征(即年龄、疾病活动性、血清MMP3水平、疾病持续时间或治疗)无关(表 2 ). 然而,这种特定的变异在我们的男性RA患者中更为常见。 实时qPCR评估的hRasGRP4转录物水平在具有剪接变异体6的个体中显著升高( P(P) =0.02,使用Mann-Whitney的U检验计算)。 由于RasGRP4的异常剪接在RA患者中最为明显,因此我们在接下来的研究中重点关注RA患者中RasGRP3的表达。
表1。 健康人、RA患者和自身免疫对照者hRasGRP4亚型的统计分析
正常的 变量(%) 或 95%置信区间
P(P)- 价值
任何变体
健康受试者 62 18 (22.5)
RA患者(总数) 47 74 (67.3) 5.42 2.86至10.3 0.00000016
RA患者(未治疗) 9 16 (64.0) 6.12 2.32至16.2 0.00029
自身免疫控制 69 31 (31.0) 1.55 0.79至3.04 0.27
非变量6 变体6 或
95%置信区间 .
P(P)- 价值
变体6
健康受试者 79 1 (1.3)
RA患者 95 20 (18.0) 16.6 2.18至126 0.00035
自身免疫控制 92 8 (8.0) 6.87 0.84至56.1 0.038
表2。 hRasGRP4变异体6与非变异体RA患者的临床特征比较
变量6(-) 变量6(+)
P(P) -价值
年龄(岁) 62.6 ± 6.2 61.4 ± 11.2 0.96*
男性/女性 0/10 6/7 0.012 †
DAS28(ESR4) 3.8 ± 1.2 3.4 ± 1.85 0.31*
基质金属蛋白酶-3 307 ± 127 148 ± 109 0.057
疾病持续时间(月) {平均值(范围)} 100(0至492) 143(0至504) 0.58*
接受治疗的患者 4 8
未接受治疗的患者 2 三 0.77 †
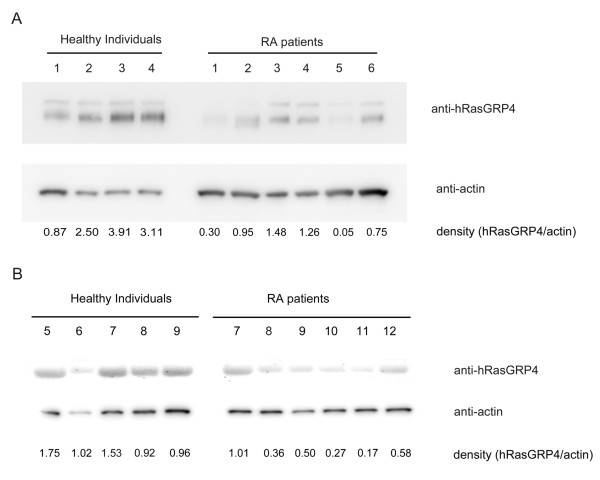
PBMC和CD14中的hRasGRP4蛋白水平 + 健康人和RA患者外周血细胞的分离 我们许多RA患者PBMC中hRasGRP4蛋白的水平低于健康对照个体(图 4A级 ). 我们的免疫印迹分析几乎没有检测到与剪接变异体5或6相对应的异常大小的条带,除了患者1和2有可检测到的较小的条带。 尽管我们的抗体仍有可能不识别选择性剪接的同种型,但具有C末端V5标签的重组hRasGRP4剪接变体6被我们的抗hRasGRP4抗体和抗V5抗体清楚地识别(数据未显示)。 我们的大多数RA患者从同时获得的样本中表达hRasGRP4转录物的异常亚型(表 三 ). CD14中hRasGRP4蛋白的水平 + RA患者的外周血细胞也低于健康人(图 4B类 ).
图4。
免疫印迹法检测hRasGRP4在外周血中的蛋白表达 . A类 RA患者和健康对照者外周血单个核细胞的免疫印迹。 从类风湿性关节炎(RA)患者和健康对照的外周血单核细胞制备裂解物。 对每个裂解物中约3μg的蛋白质进行SDS-PAGE。 使用过氧化物酶偶联的抗hRasGRP4抗体和抗β-肌动蛋白抗体进行免疫印迹。 在A组中评估了4名健康人和6名RA患者的PBMC。 B类 .循环CD14的免疫印迹 + 从五名健康对照组和六名RA患者中分离出的细胞。
表3。 患者和健康对照的临床特征和hRasGRP4 cDNA序列,其外周血样本与图4A中的样本同时获得
年龄 性别 DAS28系统 治疗 克隆1 克隆2 克隆3 克隆4 克隆5
健康1 32 F类 0 没有人 佛罗里达州 佛罗里达州 变体5 佛罗里达州 佛罗里达州
健康2 31 F类 0 没有人 佛罗里达州 佛罗里达州 变体5 变体6 佛罗里达州
健康3 38 F类 0 没有人 佛罗里达州 佛罗里达州 变体7 佛罗里达州 佛罗里达州
健康4 38 F类 0 没有人 佛罗里达州 佛罗里达州 佛罗里达州 佛罗里达州
无线电高度表1 70 M(M) 3.22 MTX 8 mg/周 +国际单项体育联合会 佛罗里达州 佛罗里达州 佛罗里达州 变体6 佛罗里达州
无线电高度表2 66 F类 3.82 MTX 6 mg/周 佛罗里达州 佛罗里达州 佛罗里达州 变体6 变量2
无线电高度表3 61 F类 2.17 MTX 10.5毫克/周 +TAC 3毫克/天 变体5 变体5 变体5 变体5 变体5
无线电高度表4 33 F类 4.87 MTX 8毫克/周 +PSL 5 mg/天 变体5 佛罗里达州 变体5 佛罗里达州 变体5
无线电高度表5 78 M(M) 2.65 MTX 6 mg/周 +SSZ 1000毫克/天 佛罗里达州 变量6 变体5 变体5 变体6
无线电高度表6 53 F类 2.27 MTX 10 mg/周 +PSL 2 mg/天 变体5 变体5 变体5 变体5 变体5
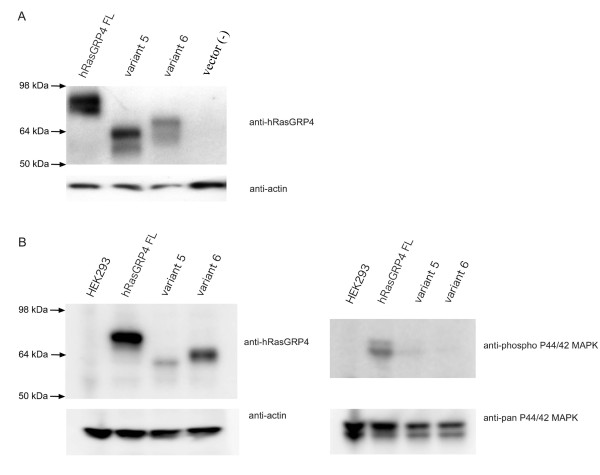
使用无细胞转录-翻译分析和哺乳动物细胞系的重组hRasGRP4蛋白 在无细胞转录翻译分析中,全长hRasGRP4、剪接变体5和剪接变体6在预期大小的蛋白质水平上表达(图 5A级 ). 在哺乳动物细胞转染系统中观察到类似的蛋白质表达(图 5亿 ,左侧面板)。 将全长RasGRP4转染到HEK293细胞后,与未转染细胞相比,P44/42 MAP激酶自然激活(图 5亿 ,右侧面板)。 然而,用剪接变异体6转染几乎没有激活P44/42 MAPK。 因此,正如预期的那样,hRasGRP4剪接变异体6在激活Ras-Erk通路方面存在功能缺陷。
图5。
hRasGRP4及其剪接变异体在转录翻译试验和哺乳动物细胞中的强制表达 . A类 无细胞转录翻译测定。 用兔网织红细胞裂解物对编码全长hRasGRP4及其剪接变异体5和6的载体进行无细胞转录翻译试验。 使用抗hRasGRP4-辣根过氧化物酶(HRP)对结果产物进行免疫印迹。 B类 hRasGRP4及其剪接变异体在哺乳动物细胞中的表达。 编码全长hRasGRP4及其剪接变异体5或6的载体被转染到HEK293细胞中。 使用抗hRasGRP4-HRP、抗磷酸或抗pan P44/42丝裂原活化蛋白激酶(MAPK)(Erk1/2)对细胞裂解物进行免疫印迹。 给出了三个独立实验的代表性结果。
讨论 据我们所知,这是首次报道hRasGRP4在健康人外周血单核细胞中的mRNA和蛋白质水平上大量表达。 这一发现为单核细胞谱系细胞生物学和该谱系细胞在疾病中发挥重要作用的领域开辟了新的视角。 在本研究的后半部分,我们揭示了RA患者PBMC中hRasGRP4的失调。
已经得出结论,信号蛋白RasGRP4在小鼠、大鼠和人类MC发育的最后阶段起着重要作用[ 1 , 5 , 8 ]. 然而,hRasGRP4 mRNA也在小鼠和人PBMC中未定义的细胞群中检测到[ 1 ]. 为了支持后一个数据,hRasGRP4转录物也被发现存在于从急性髓细胞白血病患者分离的转化白细胞中[ 4 ]. 虽然外周血中存在MC祖细胞,但这些细胞数量很少,并且有CD13 + /CD14号机组 - /CD34型 + /CD117号 + 表型[ 28 , 32 ]. 因此,我们推测另一个细胞群体可能与正常小鼠和人类PBMC中存在大量RasGRP4 mRNA和蛋白有关。 我们现在显示CD14 + PBMC中的髓样细胞在mRNA和蛋白质水平表达这种GEF(图 1A、C ). GenBank-UniGene数据库中大约830万人类dbEST中,只有26个dbEST来自hRasGRP4基因。 其中12个来自血液或骨髓,其次是5个来自肾脏。 因此,这种信号蛋白在人类中通常受到高度限制。 超过300000个dbEST已保存在源自成人肺部的数据库中。 虽然肺含有大量巨噬细胞,但数据库中只有一个肺衍生的dbEST来自hRasGRP4基因。 为了支持这些dbEST数据,小鼠和人肺中RasGRP4转录物的水平低于RNA印迹分析的检测水平[ 1 ]. 因为hRasGRP4 mRNA和蛋白在富含巨噬细胞的器官中检测不到,并且因为人类PBMC在接触凝集素时停止表达hRasGRP4 体外 [ 1 ],我们得出结论,当PBMC中的单核细胞分化为组织中的成熟巨噬细胞时,它们停止表达这种信号蛋白。 根据这一结论, 在体外 -经qPCR评估,发育的人类巨噬细胞和破骨细胞hRasGRP4 mRNA水平低得多(附加文件 1 /图S1)。
由于单核细胞系是炎症性关节炎不可或缺的启动子/效应器,我们接下来重点研究RA患者中hRasGRP4的表达,然后从定量和定性两方面评估RA患者PBMC中hRas GRP4表达。 在本研究中,我们注意到hRasGRP4 mRNA水平较高(图 2 )但RA患者PBMC中某些缺陷hRasGRP4亚型的频率更高(图 三 和表 1 ). 在我们的RA患者中,hRasGRP4的表达水平与任何研究的临床和实验室特征无关。 据报道,在一名支气管哮喘患者中存在hRasGRP4的选择性剪接异构体,并被指定为剪接变异体1、2和4[ 1 ]. 尽管我们在队列中也检测到剪接变异体1和2转录物,但这些变异体的频率较低。 相反,我们发现了10个新的剪接变异体,其中包括2个主要变异体在RA患者中优先表达(图 三 ). 最丰富的交替剪接亚型是剪接变异体5。 该变体缺少外显子9,但核苷酸序列保持在框架中。 第二个丰富的剪接变异体6缺少外显子9的5’-部分,也在框架中。 尽管该剪接变异体在患者组中的发病率相对较高,但在健康个体中很少发现。 此外,剪接变异体6与qPCR定量的高水平hRasGRP4 mRNA有关。 由于用于qPCR的探针理论上可以识别大多数异常hRasGRP4亚型,如剪接变异体5、6、9和11-14,因此产生大量缺陷剪接变种的细胞很可能试图通过产生更多hRasGRP4 mRNA来弥补这个问题, 在从C3H/HeJ小鼠株发育而来的MCs中发现了一种天然存在的mRasGRP4剪接变异体,该变异体对佛波酯无反应[ 2 ]. 在从该小鼠株发育而来的骨髓源性MCs中,编码该缺陷mRasGRP4亚型的转录物水平明显高于从A/J小鼠发育而来、优先表达mRasGRP4正常亚型的相应MCs。 累积的数据表明,当某些细胞谱系无法产生正常/功能性信号蛋白时,这些细胞会增加其缺陷转录物的生成,以弥补缺陷亚型。 事实上,RA患者的外周血细胞不能表达大量正常的hRasGRP4蛋白(图 4A级 ). 尽管剪接变异体5缺少整个外显子9,而剪接变种6在外显子九中使用了另一个剪接供体位点,但即使RA患者的基因组DNA在所有测序克隆中都有第九外显子异常,我们也没有在该外显子的外显子、剪接供者位点和剪接受体位点中发现任何点突变(数据未显示)。 尽管RA患者中hRasGRP4转录物缺陷的原因尚不清楚,但hRasGRP4转录缺陷的存在似乎不是治疗诱导的现象,因为非治疗RA患者也有高频率的hRasGRP4 cDNA缺陷(表 1 ). 其他次要变异体,如剪接变异体7、8和11,其缺少外显子1至3,剪接变种13,其缺乏外显子12的5'-部分,没有任何提前翻译终止密码子。 我们研究中发现的其他四种hRasGRP4剪接变体包含一个提前翻译终止密码子。 尽管这些转录物是非传感介导mRNA衰变的候选物,但如果翻译,这些剪接变体将编码缺失DAG/佛波酯结合序列的非功能性hRasGRP4亚型。 hRasGRP4在单核细胞中的剪接是如何控制的,尚待进一步研究确定。 由其多态性引起的CD44选择性剪接的功能方面与类风湿关节炎有关[ 33 - 35 ]. 虽然我们无法阐明与RasGRP4选择性剪接相关的遗传易感性,但我们认为全长RasGRP3蛋白水平至少部分受表观遗传因素(如选择性剪接)的调控。
由于hRasGRP4的外显子9编码hRasGRP4中保守的催化CDC25盒的大部分,如果在CD14中翻译,剪接变异体5和6很可能存在功能缺陷 + 细胞 体内 事实上,至少在我们的哺乳动物细胞表达系统中,与正常hRasGRP4相比,剪接变体6在激活P44/42 MAPK方面存在功能缺陷(图 5亿 ). 尽管RA患者单核细胞中剪接变异体6在蛋白水平上的表达尚不清楚,但RasGRP4和/或功能异常的RasGRP3亚型的低表达可能会影响单核细胞发育为巨噬细胞或破骨细胞,从而导致RA患者这些细胞的功能改变。
结论 我们澄清了hRasGRP4在CD14中表达 + PBMC中的单核细胞。 由于hRasGRP4在单核细胞中的表达可能受到发育控制,外周血单核细胞hRasGRP4表达的失调可能会影响进一步分化的细胞(如巨噬细胞和破骨细胞)的细胞功能,在RA患者的一部分中起病理作用。
缩写 BLAST:基本局部对齐搜索工具; BSA:牛血清白蛋白; DAB:3,3'-二氨基联苯胺四氯化氢; DAS28:28个关节的疾病活动评分; DAG:二酰甘油; 血沉:红细胞沉降率; GEF:鸟嘌呤核苷酸交换因子; HRP:辣根过氧化物酶; hGAPDH:人甘油醛-3-磷酸脱氢酶; IL:白细胞介素; MAPK:丝裂原活化蛋白激酶; MCs:肥大细胞; PM/DM:多发性肌炎/皮肌炎; PBMCs:外周血单个核细胞; PBMCs:外周血单个核细胞; RasGRP:Ras鸟嘌呤核苷酸释放蛋白; RA:类风湿性关节炎; REM:Ras交换图案; RQ:相对数量; SLE:系统性红斑狼疮; SS:舍格伦综合征; SSc:系统性硬化; TNF-α:肿瘤坏死因子-α
作者的贡献 TH设计并执行了实验,并进行了统计分析。 SY设计了这项研究,进行了实验并起草了手稿。 香港设计并执行实验,帮助收集和获取数据,并起草手稿。 HT帮助收集和获取数据,并起草手稿。 TA和TK参与了研究的解释和设计,并起草了手稿。 所有作者都参与了最后的手稿。 所有作者都已阅读并批准手稿出版。
补充材料
附加文件1 图S1。 CD14+外周血单核细胞和 在体外 培养的巨噬细胞或成骨细胞 . A类 使用实时qPCR评估CD14+外周血单核细胞和体外培养的巨噬细胞中的hRasGRP4转录物。 第一次实验时,CD14+细胞中抗GAPDH的hRasGRP4转录物水平定义为1。 B类 通过实时qPCR(左面板)测量体外培养破骨细胞中的.hRasGRP4转录物。 测定组织蛋白酶K(CTSK)的表达,以确认破骨细胞的发育(右图)。 在这些小组中,一次实验中PBMC中针对GAPDH转录物的目标基因转录物数量被定义为1。 所有实验均以一式三份的方式进行,误差条表示标准误差。 OC,破骨细胞; 外周血单个核细胞; RQ,相对量化。
附加文件2 图S2。 hRasGRP4转录水平和外周血单核细胞比率 . A类 RA患者PBMC中hRasGRP4转录水平与单核细胞占单核细胞加淋巴细胞总数的比率之间的关系。 用Spearman的rho分析测定PBMC中hRasGRP4的相对定量与单核细胞/(单核细胞+淋巴细胞)比值之间的线性关系。 B类 RA患者PBMC中hRasGRP4转录水平与外周WBC中单核细胞百分比之间的关系。 使用Spearman rho分析测量了PBMC中hRasGRP4的相对定量与WBC中单核细胞百分比之间的线性关系。 外周血单个核细胞; RQ,相对量化。
参与者信息 Toko Hashimoto,电子邮件: thashimo@bidmc.harvard.edu。
安田信介,电子邮件: syasuda@med.hokudia.ac.jp。
Hideyuki Koide,电子邮件: hkoid@huhp.hokudai.ac.jp。
Hiroshi Kataoka,电子邮件: Hiroshi.Kataoka@umassmededu。
Tetsuya Horita,电子邮件: thorita@med.hokudai.ac.jp。
Tatsuya Attsumi,电子邮件: at3tat@med.hokudai.ac.jp。
小池高雄,电子邮件: tkoike@med.hokudai.ac.jp。
致谢 我们感谢Richard L.Stevens博士(马萨诸塞州波士顿Brigham and Women's Hospital和哈佛医学院)的有益讨论。 我们还感谢久保田女士(北海道大学医学研究生院)的技术援助。
这项工作得到了日本卫生、劳动和福利部的支持; 日本教育、文化、体育、科学和技术部; 日本科学促进会。
工具书类
Yang Y,Li L,Wong GW,Krilis SA,Madhusudhan MS,Sali A,Stevens RL.RasGRP4,一种新的肥大细胞限制性Ras鸟嘌呤核苷酸释放蛋白,具有钙和二酰甘油结合基序。 在哮喘、肥大细胞增多症和肥大细胞白血病患者中鉴定此信号蛋白的缺陷变体,并证明RasGRP4在肥大细胞发育和功能中的重要性。 生物化学杂志。 2002; 277:25756–25774. doi:10.1074/jbc。 M202575200。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Li L,Yang Y,Stevens RL.大鼠Ras鸟嘌呤核苷酸释放蛋白4的克隆及其在大鼠肥大细胞及其骨髓祖细胞中的表达评估。 分子免疫学。 2002; 38:1283–1288. doi:10.1016/S0161-5890(02)00076-7。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Li L,Yang Y,Wong GW,Stevens RL。气道低反应性C3H/HeJ小鼠的肥大细胞表达一种独特的信号蛋白Ras鸟嘌呤核苷酸释放蛋白4的同种型,该蛋白对二酰甘油和佛波酯没有反应。 免疫学杂志。 2003; 171:390–397. doi:10.4049/jimmunol.171.1.390。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Reuther GW、Lambert QT、Rebhun JF、Caligiuri MA、Quilliam LA、Der CJ。 RasGRP4是一种从急性髓细胞白血病中分离出来的新型Ras激活剂。 生物化学杂志。 2002; 277:30508–30514. doi:10.1074/jbc。 M111330200。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Li L,Yang Y,Stevens RL。RasGRP4调节人和大鼠肥大细胞系中前列腺素D2的表达。 生物化学杂志。 2003; 278:4725–4729. doi:10.1074/jbc。 C200635200。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Layer K、Lin G、Nencioni A、Hu W、Schmucker A、Antov AN、Li X、Takamatsu S、Chevassut T、Dower NA、Stang SL、Beier D、Buhlmann J、Bronson RT、Elkon KB、Stone JC、Van Parijs L、Lim B.Rasgrp1自发突变导致的自身免疫。 免疫。 2003; 19:243–255. doi:10.1016/S1074-7613(03)00209-7。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Yasuda S、Stevens RL、Terada T、Takeda M、Hashimoto T、Fukae J、Horita T、Kataoka H、Atsumi T、Koike T。系统性红斑狼疮患者亚群中Ras鸟苷核苷释放蛋白1的缺陷表达。 免疫学杂志。 2007; 179:4890–4900. doi:10.4049/jimmunol.179.7.4890。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Katsoulotos GP、Qi M、Qi JC、Tanaka K、Hughes WE、Molloy TJ、Adachi R、Stevens RL、Krilis SA。人类肥大细胞系内ras鸟嘌呤核苷酸释放蛋白4的二酰甘油依赖性易位导致显著的表型变化,包括白细胞介素13受体α2的表达。 生物化学杂志。 2008; 283:1610–1621. doi:10.1074/jbc。 M707042200。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Lewis RA、Soter NA、Diamond PT、Austen KF、Oates JA、Roberts LJ。 用抗IgE激活大鼠和人肥大细胞后产生前列腺素D2。 免疫学杂志。 1982; 129:1627–1631. [ 公共医学 ] [ 谷歌学者 ]
Kanaoka Y,Ago H,Inagaki E,Nanayama T,Miyano M,Kikuno R,Fujii Y,Eguchi N,Toh H,Urade Y,Hayaushi O。造血前列腺素D合成酶的克隆和晶体结构。 单元格。 1997; 90:1085–1095. doi:10.1016/S0092-8674(00)80374-8。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Kochi Y,Suzuki A,Yamada R,Yamamoto K。类风湿关节炎的种族遗传异质性——发病机制的影响。 Nat Rev风湿病。 2010; 6:290–295. doi:10.1038/nrreum.2010.23。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Tobon GJ、Youinou P、Saraux A。环境、地质流行病学和自身免疫性疾病:类风湿性关节炎。 J自动免疫。 2010; 35:10–14. doi:10.1016/j.jaut.2009.12.009。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Crisp AJ、Chapman CM、Kirkham SE、Schiller AL、Krane SM。类风湿关节炎关节肥大细胞增多症。 大黄性关节炎。 1984; 27:845–851. doi:10.1002/art.1780270802。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Bromley M,Woolley DE。类风湿病变的组织病理学。 软骨侵蚀部位的细胞类型鉴定。 大黄性关节炎。 1984; 27:857–863. doi:10.1002/第1780270804条。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Tetlow LC,Woolley DE。类风湿病变处的肥大细胞、细胞因子和金属蛋白酶:双重免疫定位研究。 大黄疾病年鉴。 1995; 54:896–903. doi:10.1136/ard.54.11.896。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
范登·布鲁克MF、范登伯格WB、范德普特LB。肥大细胞在小鼠抗原诱导性关节炎中的作用。 风湿病学杂志。 1988; 15:544–551. [ 公共医学 ] [ 谷歌学者 ]
Lee DM、Friend DS、Gurish MF、Benoist C、Mathis D、Brenner MB。 肥大细胞:自身抗体和炎症性关节炎之间的细胞联系。 科学。 2002; 297:1689–1692. doi:10.1126/science.1073176。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Corr M,Crain B.FcgammaR信号在关节炎K/B×N血清转移模型中的作用。 免疫学杂志。 2002; 169:6604–6609. doi:10.4049/jimmunol.169.11.6604。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
McNeil HP、Shin K、Campbell IK、Wicks IP、Adachi R、Lee DM、Stevens RL。小鼠肥大细胞限制性四聚体形成类胰蛋白酶小鼠肥大细胞蛋白酶6和小鼠肥大胞蛋白酶7是炎症性关节炎的关键介质。 大黄性关节炎。 2008; 58:2338–2346. doi:10.1002/art.23639。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Shin K、Nigrovic PA、Crish J、Boilard E、McNeil HP、Larabee KS、Adachi R、Gurish MF、Gobezie R、Stevens RL、Lee DM。肥大细胞通过类胰蛋白酶/肝素复合物导致自身免疫性炎性关节炎。 免疫学杂志。 2009; 182:647–656. doi:10.4049/jimmunol.182.1.647。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Valent P、Ashman LK、Hinterberger W、Eckersberger F、Majdic O、Lechner K、Bettelheim P.肥大细胞分型:不同造血细胞类型的证明以及与单核吞噬细胞免疫表型关系的证据。 鲜血。 1989; 73:1778–1785. [ 公共医学 ] [ 谷歌学者 ]
Saito H、Ebisawa M、Tachimoto H、Shichijo M、Fukagawa K、Matsumoto K、Iikura Y、Awaji T、Tsujimoto G、Yanagida M、Uzumaki H、Takahashi G、Tusji K、Nakahata T。由脐血单个核细胞中的钢因子、IL-6和前列腺素E2诱导的人类肥大细胞的选择性生长。 免疫学杂志。 1996; 157:343–350. [ 公共医学 ] [ 谷歌学者 ]
Szekanecz Z,Koch AE。类风湿性关节炎中的巨噬细胞及其产物。 当前操作风湿病。 2007; 19:289–295. doi:10.1097/BOR.0b013e32805e87ae。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Lutzky V,Hannawi S,Thomas R.类风湿关节炎滑膜细胞。 树突状细胞。 关节炎研究与治疗。 2007; 9:219. doi:10.1186/ar2200。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
类风湿关节炎滑膜的Schett G.细胞。 破骨细胞。 关节炎研究与治疗。 2007; 9:203. doi:10.1186/ar2110。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Arnett FC、Edworthy SM、Bloch DA、McShane DJ、Fries JF、Cooper NS、Healey LA、Kaplan SR、Liang MH、Luthra HS、Medsger TA Jr、Mitchell DM、Neustadt DH、Pinals JG、Schaller JG、Sharp JT、Wilder RL、Hunder GG。美国风湿病协会1987年修订了类风湿关节炎分类标准。 大黄性关节炎。 1988; 31:315–324. doi:10.1002/art.1780310302。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Prevoo ML、van’t Hof MA、Kuper HH、van Leeuwen MA、van de Putte LB和van Riel PL。包括二十八个关节计数的改良疾病活动评分。 类风湿关节炎患者前瞻性纵向研究的发展和验证。 大黄性关节炎。 1995; 38:44–48. doi:10.1002/art.1780380107。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Kirshenbaum AS、Goff JP、Semere T、Foster B、Scott LM、Metcalfe DD。证明人类肥大细胞起源于CD34(+)、c-kit(+)的祖细胞群,并表达氨肽酶N(CD13)血液。 1999; 94:2333–2342. [ 公共医学 ] [ 谷歌学者 ]
Akagawa堪萨斯州。 集落刺激因子诱导的人单核细胞来源巨噬细胞的功能异质性。 国际血液学杂志。 2002; 76:27–34. doi:10.1007/BF02982715。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Littlewood-Evans A、Kokubo T、Ishibashi O、Inaoka T、Wlodarski B、Gallagher JA、Bilbe G。通过原位杂交和免疫组织化学在人破骨细胞中定位组织蛋白酶K。 骨头。 1997; 20:81–86. doi:10.1016/S8756-3282(96)00351-1。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Java中的图像处理和分析。 http://rsbweb.nih.gov/ij/
Wang XS,Yip KH,Sam SW,Lau HY。软毛制剂是培养成熟人类肥大细胞的一种方便的祖细胞来源。 免疫学方法杂志。 2006; 309:69–74. doi:10.1016/j.jim.2005.11.012。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Wibulswas A、Croft D、Pitsillides AA、Bacarese-Hamilton I、McIntyre P、Genot E、Kramer IM。 表位CD44v3和CD44v6对类风湿关节炎来源的成纤维细胞样滑膜细胞侵袭行为的影响。 大黄性关节炎。 2002; 46:2059–2064. doi:10.1002/art.10421。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Golan I、Nedvetzki S、Eshkar-Sebban L、Levartovsky D、Elkayam O、Caspi D、Aamar S、Amital H、Rubinow A、Naor D。类风湿关节炎患者CD44变异体中额外三核苷酸的表达可产生疾病特异性单克隆抗体。 J自动免疫。 2007; 28:99–113. doi:10.1016/j.jaut.2007.02.007。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Naor D,Nedvetzki S.CD44在类风湿关节炎中的作用。 关节炎研究与治疗。 2003; 5:105–115. doi:10.1186/ar746。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
关联数据 本节收集本文中包含的任何数据引用、数据可用性声明或补充材料。
补充资料
附加文件1 图S1。 CD14+外周血单核细胞和 在体外 培养的巨噬细胞或成骨细胞 . A类 使用实时qPCR评估CD14+外周血单核细胞和体外培养的巨噬细胞中的hRasGRP4转录物。 第一次实验时,CD14+细胞中抗GAPDH的hRasGRP4转录物水平定义为1。 B类 通过实时qPCR(左面板)测量体外培养破骨细胞中的.hRasGRP4转录物。 测定组织蛋白酶K(CTSK)的表达,以确认破骨细胞的发育(右图)。 在这些小组中,一次实验中PBMC中针对GAPDH转录物的目标基因转录物数量被定义为1。 所有实验均以一式三份的方式进行,误差条表示标准误差。 OC,破骨细胞; 外周血单个核细胞; RQ,相对量化。
附加文件2 图S2。 hRasGRP4转录水平和外周血单核细胞比率 . A类 RA患者PBMC中hRasGRP4转录水平与单核细胞占单核细胞加淋巴细胞总数的比率之间的关系。 用Spearman的rho分析测定PBMC中hRasGRP4的相对定量与单核细胞/(单核细胞+淋巴细胞)比值之间的线性关系。 B类 RA患者PBMC中hRasGRP4转录水平与外周血白细胞中单核细胞百分比之间的关系。 用Spearman的rho分析测定PBMC中hRasGRP4的相对定量与WBC中单核细胞百分比之间的线性关系。 外周血单个核细胞; RQ,相对量化。