BCL-2家族蛋白“仅BH3结构域”亚群的成员将近端死亡信号与核心凋亡途径连接(1–5). 激活CD95(Fas)或TNFR1死亡受体后,BID被裂解并激活为p15 tBID(6–8)在使用纯化线粒体的模型系统中,它作为死亡配体,诱导BAK齐聚(9)和BAX(10). tBID不会导致纯化的细胞色素c释放贝克-线粒体缺陷,表明tBID和BAK的相互作用至少在体外是一个关键事件(9).
在这里,我们通过使用逆转录病毒载体在小鼠胚胎成纤维细胞(MEF)中表达tBID来评估BAK是否是tBID诱导完整细胞凋亡所必需的。在贝克-tBID表达载体感染24小时后出现缺陷型和野生型MEF(图1A),但不使用空矢量(pMIG)(11)只表达绿色荧光蛋白(GFP)。另一个“多结构域”促凋亡BCL-2成员BAX缺陷的MEFs也被杀死。相反,Bax、Bak通过多种标记物(包括Annexin-V染色)评估,双缺陷MEF对tBID诱导的细胞死亡具有完全抵抗力(图1C)和细胞形态(图1A). 感染细胞可通过GFP的表达进行鉴定(图1B)并通过控制pMIG病毒在所有遗传背景下的感染率显示出类似的感染率(图1D). 对tBID感染的MEF中GFP表达的分析显示,野生型凋亡细胞中存在少量GFP,Bax公司−/−、和贝克−/−MEF公司(图1D). 相反,将tBID矢量引入Bax、Bak双敲除(DKO)MEF显示形态正常的细胞表达高水平的GFP(图1、B和D). 猿猴病毒40(SV40)转化的野生型和DKO基因型MEF细胞系也分别对tBID敏感和耐药(12). 蛋白免疫分析证实p15 BID在DKO MEF中表达,在凋亡的野生型MEF中少量表达(图1E). 在野生型和DKO MEF中,p15 BID定位于线粒体,作为一种完整的膜蛋白(12)表明尽管tBID表达并靶向线粒体,但它并没有杀死DKO MEF。仅BAX的再表达不足以杀死DKO MEF,但确实恢复了tBID的杀伤作用,证实tBID需要一个多域促凋亡成员来诱导凋亡(图1C).
图1。
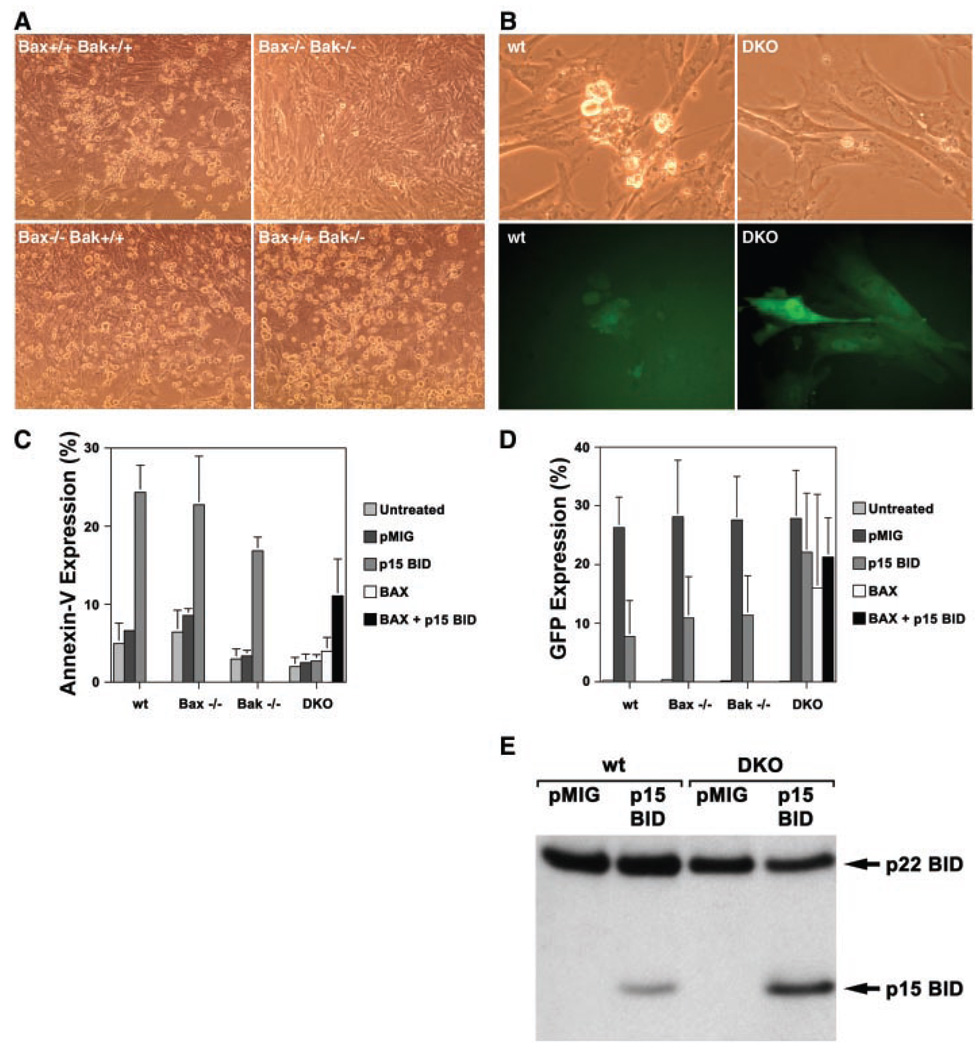
的电阻Bax、Bak双缺陷小鼠胚胎成纤维细胞(MEFs)对tBID诱导的凋亡。(A类)野生型亮场显微镜(×20倍放大),Bax公司−/− 贝克−/−,Bax公司−/− 贝克+/+、和Bax公司+/+ 贝克−/−在感染tBID表达载体24小时后,初生胚胎日13.5个MEF。将小鼠p15 BID和BAX克隆到逆转录病毒表达载体MSCV-IRES-GFP(pMIG)中(11). 如前所述,通过转染293GPG包装细胞系产生逆转录病毒(33). 转染后3天和5天收集含有逆转录病毒的上清液,并在聚布伦(8µg/ml)存在下用于感染MEFs。(B类)感染tBID载体24小时后,野生型(wt)和DKO MEF同一场(×40倍放大)的亮场和GFP荧光。(C类)感染pMIG(空载体控制)、tBID和/或BAX载体后24小时内MEF中细胞凋亡的定量。细胞死亡通过Annexin-V染色的流式细胞术检测(Bio-vision)进行定量。所示值为三个独立实验的平均值±1 SD。(D类)感染pMIG、tBID和/或BAX载体24小时后GFP阳性细胞的定量。流式细胞术检测GFP阳性细胞。所示值为三个独立实验的平均值±1 SD。(E类)SV40-转化的全细胞裂解物Bid抗体免疫印迹(34)感染pMIG或tBID载体后17小时的野生型和DKO MEF。
解释这些观察结果的一个机制是,如果tBID诱导BAX和BAK的激活,导致线粒体功能障碍,包括细胞色素c的释放。我们测试了BAX和BAK的激活状态以及细胞色素c在表达tBID的初级MEF中的细胞内分布。用化学交联剂双马来酰亚胺基己烷(BMH)处理来自对照组和表达p15 BID的初级MEF的线粒体,以检查BAK齐聚状态。正如我们在肝细胞中观察到的那样(9)在表达p15 BID的细胞中,对照细胞中迁移速度较快的非活性BAK构象消失,交联BAK多聚体的数量相应增加,这与二聚体和三聚体的形成一致(图2A). 该过程似乎与BAX无关,因为p15 BID导致BAK在Bax公司−/−MEF公司(图2A). 野生型MEF中p15 BID的表达导致细胞溶质BAX作为完整的线粒体膜蛋白移位和插入(12)与BAX在Fas活化肝细胞中的作用一样(图3B). 在GFP阳性、表达tBID的DKO MEF中,细胞色素c保持点状线粒体模式,但在表达tBID-的野生型MEF中细胞色素c重新分布为弥散的细胞溶质模式(图2B). 因此,促凋亡BAX、BAK或两者的激活是tBID诱导细胞色素c在体内释放所必需的。我们测试了钡/钡通过向MEF细胞质中微量注射细胞色素c,缺失细胞在线粒体下游有完整的凋亡途径。微量注射细胞色素c后,DKO和野生型MEF显示出相似的细胞死亡(图2C)表明细胞色素c下游的凋亡途径释放(13)不依赖于BAX或BAK的功能。
图2。
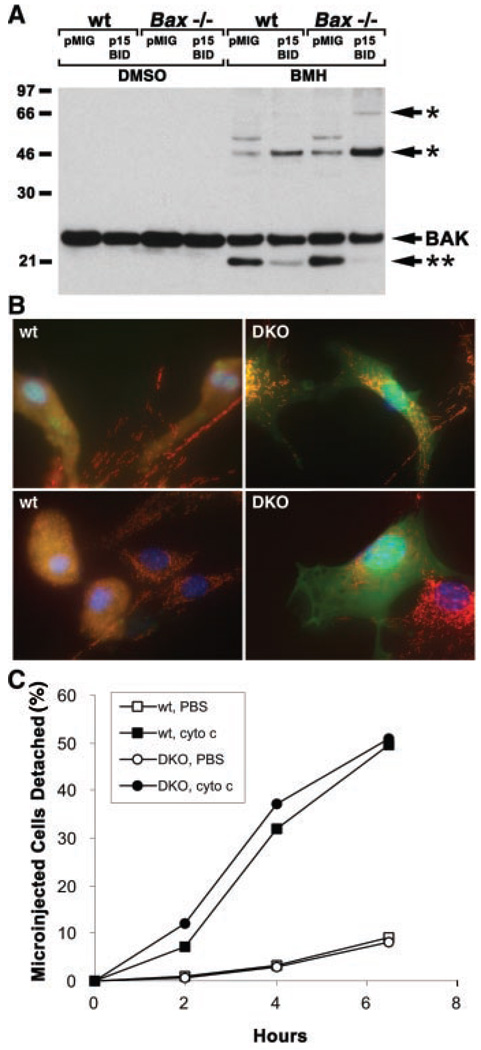
tBID下游和细胞色素c释放上游的BAX和BAK的功能。(A类)tBID诱导的BAK齐聚反应与BAX无关。如前所述,从pMIG或tBID载体感染的MEF中制备富含线粒体的部分(14)并用含有控制缓冲液的二甲基亚砜(DMSO)或10 mM BMH交联剂(Pierce)处理。通过BAK(Upstate Biotechnology,上游生物技术)免疫印迹抗体检测交叉BAK物种。*表示BAK复合物与二聚体或三聚体一致;**表示不活动的BAK一致性。(B类)DKO MEF中的细胞色素c释放。三色荧光显微镜(35)在感染tBID和GFP表达载体后24小时,检测野生型和DKO MEF。红色表示细胞色素c免疫染色。蓝色是DNA的赫斯特染色。绿色是受感染细胞中GFP的表达。GFP和细胞色素c染色重叠用黄色表示。结果代表了三个独立的实验。(C类)微量注射细胞色素c后DKO MEF的凋亡。将初级MEF镀在1%明胶涂层的网格盖玻片上。将溶解在磷酸盐缓冲盐水(PBS)或PBS对照中的纯化细胞色素c(1.6 mg/ml)与0.5%异硫氰酸荧光素-共轭葡聚糖以1:1的比例混合,并在150 hPa的压力和0.5 s的注射时间下用Eppendorf 5246 Transjector微量注射到细胞中。凋亡细胞从盖玻片上脱落,并被计数为凋亡的测量值,从而可以从三个独立的实验中绘制出微注射脱落细胞平均百分比的时间进程。
图3。
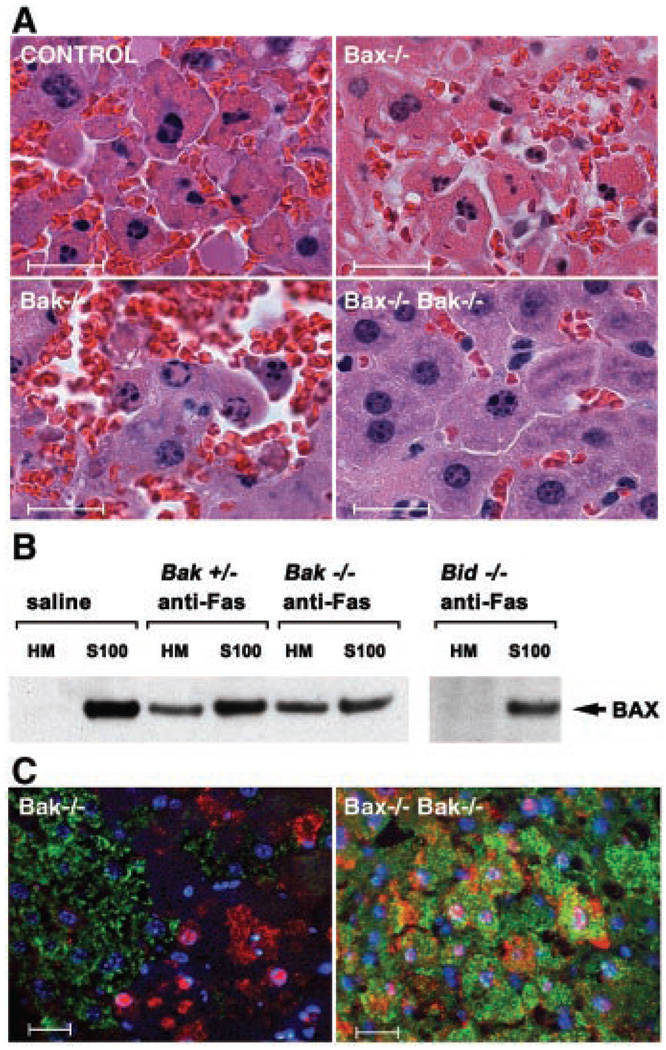
BID下游BAX和BAK在Fas诱导的肝细胞凋亡中的作用。(A类)苏木精和伊红染色的肝脏切片贝克−/−,Bax公司−/−和用Fas抗体(抗Fas)治疗的DKO小鼠。Bar表示20µm。(B类)肝细胞中Fas诱导的BAX从胞浆向线粒体的移位位于BID下游,但与BAK无关。如前所述制备的肝细胞线粒体(HM)和细胞溶质(S100)部分的BAX免疫印迹(8)来自野生型,投标−/−,贝克+/−、和贝克−/−用生理盐水或抗Fas药物治疗的小鼠。(C类)抗Fas治疗后肝脏的三色免疫组织化学贝克−/−和DKO小鼠。细胞色素c染色为绿色,活化的Caspase-3/7(CM1抗体)为红色,细胞核用Hoechst染色为蓝色。Bar表示20µm。如前所述,对经抗Fas治疗的动物的肝脏进行组织学和免疫组织化学染色(14).
为了检测细胞原位死亡是否需要BAK或BAX分子,我们评估了注射Fas激动性抗体的小鼠肝脏的凋亡。贝克-缺乏Fas的小鼠易受Fas诱导的肝细胞凋亡和出血性坏死的影响(图3A和表1)死亡时间与野生型或杂合子同卵对照相似。这与对Fas的抗性形成对比投标-缺陷小鼠(14). 体内通过Fas激活的肝细胞亚细胞分馏显示,BAX在体内从胞浆转运到线粒体贝克-有缺陷,但不是投标-缺陷小鼠(图3B).Bax公司-缺陷小鼠也死于Fas诱导的肝细胞凋亡(图3A和表1). 因此,BID似乎在肝细胞和MEF中的BAX和BAK的上游发挥作用。
表1。
缺乏药物的小鼠的敏感性Bax、Bak或两者都与抗Fas注射有关。小鼠每克体重静脉注射0.5微克Fas(Jo2,Pharmingen)单克隆抗体,并在垂死或观察24小时后处死。死亡小鼠的平均生存时间为小时±1 SD。
| 基因型 |
死亡/
注入 |
平均存活率
(小时) |
|
贝克−/−
|
9/13 |
5.2 ± 1.7 |
|
贝克+/−或+/+
|
9/14 |
6.0 ± 2.7 |
|
Bax公司−/−
|
7/10 |
3.8 ± 1.2 |
|
Bax公司+/−或+/+
|
13/13 |
2.6 ± 1.9 |
|
Bax公司−/−,贝克−/−
|
0/3 |
(9小时后死亡) |
接下来,我们测试了BAX和BAK的消除是否会对Fas诱导的肝细胞凋亡产生抵抗。绝大多数Bax、BakDKO小鼠在出生前后死亡,只有一小部分存活到成年(15). 我们给三只可用的DKO小鼠注射Fas抗体,所有这些小鼠均存活9小时,然后将其处死并检查其肝脏(表1). DKO小鼠肝细胞最多出现中度凋亡,部分动物无凋亡(图3A). 受影响的DKO肝细胞的免疫组织化学特征仅限于Caspase-3活化的局部区域,而不释放细胞色素c(图3C),与中看到的类似投标−/−肝细胞(14). 这些关于有限数量的DKO小鼠的数据与单一缺陷小鼠的数据进行了对比,表明BID依赖性凋亡也在肝细胞中使用BAX或BAK。这表明,当原位激活时,“外源性”(死亡受体)途径也可能依赖于选定细胞类型中的“多结构域”促凋亡蛋白(14,16).
接下来,我们研究了在其他刺激导致线粒体释放细胞色素c后,BAX、BAK或两者是否都是死亡所必需的(17–21). 野生型,Bax公司−/−、和贝克−/−MEF易感,而DKO MEF对staurosporine(激酶抑制剂)、etoposide(拓扑异构酶II抑制剂)和紫外线辐射(UVC)具有耐药性,即使在非常高的剂量下(图4,A到D). 时间进程研究和剂量反应评估表明,DKO MEF对这些刺激有明显的抵抗力,通过核小体DNA片段评估表明长期存活(图4A),染料排除(图4D)或Annexin-V染色(图4E). 此外,DKO MEF,但不是单一缺陷的MEF,被证明对来自内质网(ER)的应激信号具有抵抗力(22–24)由thapsigargin诱导(抑制Ca2+腺苷三磷酸酶泵)、衣霉素(抑制N-连接糖基化)(图4B)或brefeldin A(抑制ER-Golgi转运)(12). 进一步的评估表明,DKO细胞中的线粒体后事件被阻止,包括在所有这些刺激后效应胱天蛋白酶活性的激活(图4C). DKO MEF对血清(生长因子)缺乏引起的细胞死亡也有抵抗力(图4F). 相反,投标−/−细胞对所有这些信号都敏感(图4,A和B),表明他们不依赖BID,并且BID不是BAX或BAK的唯一激活器。DKO MEF易受肿瘤坏死因子α(TNF-α)和放线菌素D的外源信号的影响,在这种细胞类型中,放线菌肽D诱导线粒体非依赖性caspase级联反应(图4,A和C).
图4。
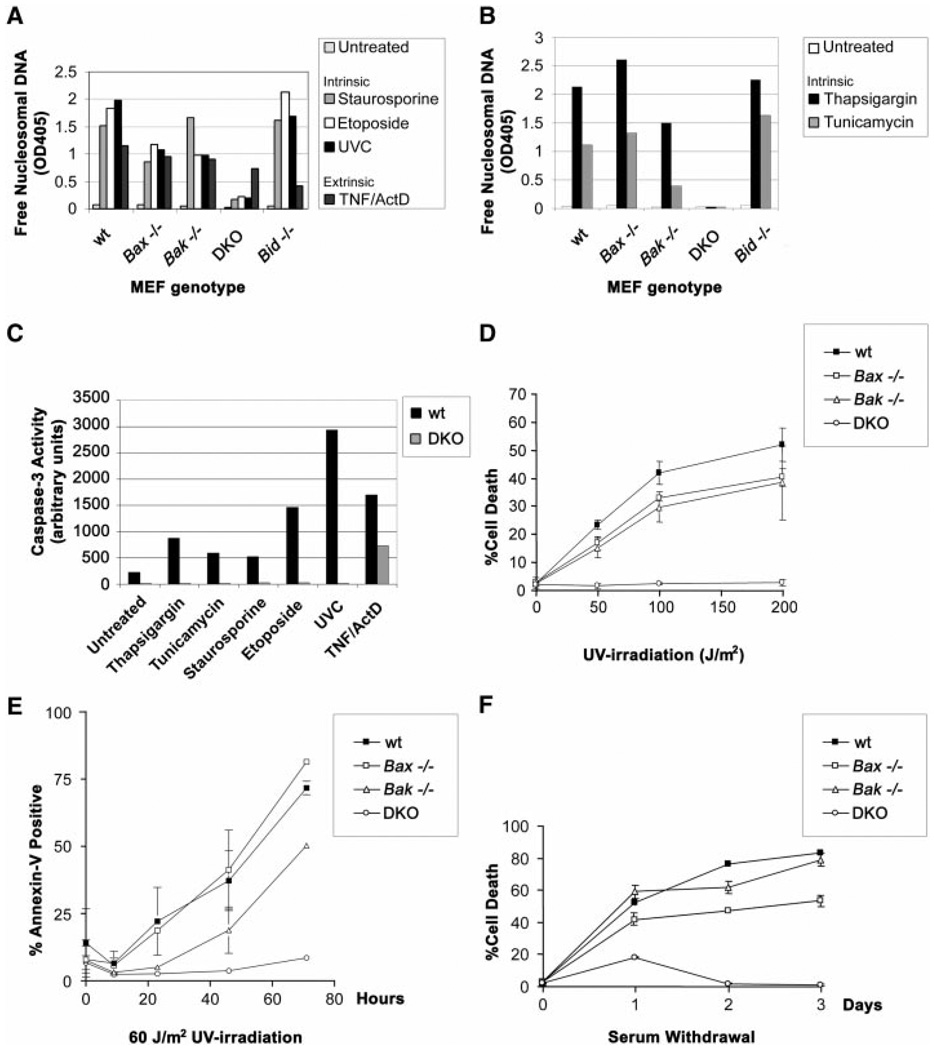
的电阻Bax、Bak多重内在死亡信号的双重缺陷MEF。(A类)线粒体依赖性内在信号对MEF凋亡死亡的敏感性。野生型,Bax公司−/−,贝克−/−、DKO和投标−/−用1µM staurosporine、100µM etoposide、UVC(60 J/M)处理原发性MEF2)或TNF-α(1 ng/ml)+放线菌素D(2µg/ml),显示48小时的时间点。绘制了凋亡DNA片段(Roche)酶联免疫吸附试验重复样品的平均值,作为三个独立实验的代表。(B类)内质网刺激对MEF凋亡死亡的敏感性。如(A)所示,用2µM的thapsigargin或tunicamycin(1µg/ml)处理基因型MEF,绘制凋亡DNA片段48小时时重复样品的平均值。刺激后4天通过Annexin-V染色评估DKO MEF也显示长期存活(12). (C类)使用DEVD-AFC荧光底物(Clontech)定量效应器caspase活性(例如caspase-3)。用以下死亡信号处理野生型和DKO MEF,并在指定的时间点收获:2µM thapsigargin(36小时)、tunicamycin(1µg/ml;36小时),1µM staurosporine(16小时),100µM etoposide(24小时),UVC(60 J/M2; 24小时)和TNF-α(1 ng/ml)+放线菌素D(2µg/ml;16小时)。结果代表了三个独立的实验。(D类)MEFs对UVC辐射的剂量反应。通过台盼蓝排除法定量细胞死亡,并绘制24小时时间点。(E类)紫外线照射后MEF凋亡的时间进程(60 J/m2). 通过流式细胞术检测Annexin-V染色定量细胞死亡。在staurosporine和etoposide以及UVC治疗后4天,也观察到DKO MEF的长期存活(12). (F类)MEF细胞凋亡对血清退出的反应时间进程。通过台盼蓝排除法对细胞死亡进行定量。
抗凋亡或促凋亡BCL-2成员是否发挥主导作用还存在很大的不确定性。我们的研究表明,在体内,完整的细胞需要一个多域促凋亡成员来响应不同的死亡信号。tBID必须激活BAX或BAK,以启动肝细胞和MEF中的线粒体功能障碍和细胞死亡。可以想象,在其他组织中,这种功能可能由其他促凋亡多域家族成员发挥,如BOK(25). BAX或BAK的活化和齐聚被认为可以形成同聚孔(9,26),形成依赖电压的阴离子通道-包含孔隙(27),或线粒体膜透化(28)启动细胞色素c的释放。细胞色素c的释放激活Apaf-1–Caspase-9凋亡小体和下游效应Caspase(13)细胞色素c大量丢失后,进行性caspase非依赖性线粒体功能障碍可导致细胞死亡(29). 线粒体下游的细胞色素c或Caspase-9和Apaf-1基因敲除表明,staurosporine、etoposide和辐射的损伤取决于线粒体释放细胞色素c所介导的信号(17–21). 这个Bax、Bak-紧靠线粒体上游的缺陷细胞似乎能更好地抵御这些药物。即使内质网应激诱导的凋亡也需要BAX或BAK,这可能反映了BAX或BAK在内质网部位的作用不明确(30,31)或ER通路对线粒体的最终依赖(32). BAX和BAK的其他上游激活剂明显存在,如投标-缺乏BAX和BAK的细胞往往容易受到无法杀死它们的刺激。我们的功能丧失研究表明,在包括质膜、细胞核和内质网在内的多个部位启动看似无关的信号后,凋亡前BAX和BAK分子的缺失会造成严重的阻滞,保护线粒体并抑制凋亡。
参考文献和注释
-
1绿色DR.细胞。2000;102:1. doi:10.1016/s0092-8674(00)00003-9。[内政部] [公共医学] [谷歌学者]
-
2Kroemer G,Reed JC。《自然医学》2000;5:513. doi:10.1038/74994。[内政部] [公共医学] [谷歌学者]
-
三。Adams JM,Cory S.科学。1998;281:1322. doi:10.126/science.2815381.1322。[内政部] [公共医学] [谷歌学者]
-
4Gross A,McDonnell JM,Korsmeyer SJ,《基因开发》,1999年;13:1899. doi:10.1101/gad.13.1899。[内政部] [公共医学] [谷歌学者]
-
5黄DC,Strasser A.Cell。2000;103:839. doi:10.1016/s0092-8674(00)00187-2。[内政部] [公共医学] [谷歌学者]
-
6李浩,朱浩,徐希杰,袁J.Cell。1998;94:491. doi:10.1016/s0092-8674(00)81590-1。[内政部] [公共医学] [谷歌学者]
-
7罗X、布迪哈乔I、邹H、屠夫C、王X。牢房。1998;94:481. doi:10.1016/s0092-8674(00)81589-5。[内政部] [公共医学] [谷歌学者]
-
8Gross A等人,《生物学杂志》。化学。1999;274:1156. doi:10.1074/jbc.274.2.1156。[内政部] [公共医学] [谷歌学者]
-
9魏MC等,《基因发育》2000;14:2060.[PMC免费文章] [公共医学] [谷歌学者]
-
10Eskes R、Desagher S、Antonsson B、Martinou JC。分子细胞。《生物》2000;20:929. doi:10.1128/mcb.20.3.929-935.2000。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
11Van Parijs L等人,《免疫》。1999;11:281. doi:10.1016/s1074-7613(00)80103-x。[内政部] [公共医学] [谷歌学者]
-
12Wei MC,Zong W-X.未发布数据。[谷歌学者]
-
13李鹏等。细胞。1997;91:479. doi:10.1016/s092-8674(00)80434-1。[内政部] [公共医学] [谷歌学者]
-
14Yin XM等人《自然》。1999;400:886. doi:10.1038/23730。[内政部] [公共医学] [谷歌学者]
-
15Lindsten T等人,《分子细胞》。2000;6:1380.[谷歌学者]
-
16Scaffidi C等人,EMBO J.1998;17:1675. doi:10.1093/emboj/17.6.1675。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
17Hakem R等人,《细胞》。1998;94分39秒。doi:10.1016/s0092-8674(00)81477-4。[内政部] [公共医学] [谷歌学者]
-
18Kuida K等人,《细胞》。1998;94:325. doi:10.1016/s0092-8674(00)81476-2。[内政部] [公共医学] [谷歌学者]
-
19Yoshida H等人,《细胞》。1998;94:739. doi:10.1016/s0092-8674(00)81733-x。[内政部] [公共医学] [谷歌学者]
-
20Cecconi F、Alvarez-Bolado G、Meyer BI、Roth KA、Gruss P.Cell。1998;94:727. doi:10.1016/s0092-8674(00)81732-8。[内政部] [公共医学] [谷歌学者]
-
21李凯等。细胞。2000;101:389. doi:10.1016/s0092-8674(00)80849-1。[内政部] [公共医学] [谷歌学者]
-
22考夫曼RJ.Genes Dev.1999;13:1211. doi:10.1101/gad.13.10.1211。[内政部] [公共医学] [谷歌学者]
-
23Nakagawa T等人,《自然》。2000;403:98. doi:10.1038/47513。[内政部] [公共医学] [谷歌学者]
-
24He H、Lam M、McCormick TS、Distelhorst CW。《细胞生物学杂志》。1997;138:1219. doi:10.1083/jcb.138.6.1219。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
25许SY、凯皮亚A、麦基E、洛梅利M、许AJ。程序。国家。阿卡德。科学。美国1997年;94:12401. doi:10.1073/pnas.94.23.12401。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
26Saito M、Korsmeyer SJ、Schlesinger PH.《自然细胞生物学》。2000;2:553. doi:10.1038/35019596。[内政部] [公共医学] [谷歌学者]
-
27清水S、成田M、筑本Y。自然。1999;399:483. doi:10.1038/20959。[内政部] [公共医学] [谷歌学者]
-
28Kluck RM等人,《细胞生物学杂志》。1999;147:809. doi:10.1083/jcb.147.4.809。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
29Mootha VK等人,EMBO J.2001;20:661. doi:10.1093/emboj/204.661。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
30朱伟等,EMBO J.1996;下午15:4130。[PMC免费文章] [公共医学] [谷歌学者]
-
31Ng FW等,《细胞生物学杂志》。1997;139:327. doi:10.1083/jcb.139.2.327。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
32Hacki J等人。癌基因。2000;19:2286. doi:10.1038/sj.onc.1203592。[内政部] [公共医学] [谷歌学者]
-
33Ory DS、Neugeboren BA、Mulligan RC。程序。国家。阿卡德。科学。美国1996年;93:11400. doi:10.1073/pnas.93.21.11400。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
34原代鼠胚胎成纤维细胞由Bax公司+/−;贝克+/−或Bax公司+/−;贝克−/−怀孕后13.5天定时交配。通过转染含有SV40基因组DNA的质粒使原代MEF永生化。将初级MEF置于六孔板中,并根据制造商的说明,使用Fugene(Roche)转染1µg总DNA。通过连续稀释产生稳定的永生克隆。
-
35细胞固定在3%多聚甲醛中,并在1%牛血清白蛋白和0.1%Triton X-100中渗透。将细胞与细胞色素c的一级抗体(克隆6H2.B4,Pharmingen)和小鼠的Cy3-共轭山羊二级抗体(Jackson Immunoresearch Laboratories)和Hoechst 33258(Molecular Probes)依次孵育,然后将其安装在盖玻片下N个-没食子酸丙酯。使用安装在尼康Eclipse E600上的SPOT摄像机(诊断)和PlanFluor物镜或奥林巴斯IX50显微镜采集图像。
-
36我们感谢E.Smith的图形和手稿准备工作,感谢B.Avery和S.Wade的畜牧业工作,感谢C.Gramm的技术援助,感谢C.Beard的逆转录病毒援助,感谢P.Tegtmeyer的SV40表达载体,感谢W.Sellers使用微注射器。M.C.W.部分由NIH培训拨款5T32AT09361支持。W.-X.Z.由癌症研究所的博士后资助。这项工作得到了NIH拨款R01CA50239和R37CA48023的部分支持。






