RKIP公司(R(右)自动对焦k个酶我非抑制剂对蛋白质)是一组进化上保守的蛋白质,称为PEBP(P(P)磷脂酰e(电子)乙醇胺-b编结对蛋白质)。最近,我们和其他人已经确定RKIP是一种转移抑制蛋白,并对其进行了表征。在分子水平上,RKIP通过抑制增殖和存活的Raf-MEK-ERK和NF-κB信号通路发挥作用(白·查特吉等。, 2004;杨帕克等。, 2005). 与它对Raf和NF-κB信号的抑制作用一致,我们和其他人已经证明RKIP在许多肿瘤中的表达水平下调,包括高转移前列腺癌、乳腺癌和结肠癌、肝细胞癌、黑色素瘤和胰岛素瘤(哈根·阿尔穆拉等。, 2006;白·查特吉等。, 2004;傅,史密斯等。2003年;Al-Mulla Hegan等。, 2005;李、田等。, 2006;巴塔伊尔·舒埃勒等。, 2004;巴塔伊尔·舒埃勒等。, 2006;张,付等。, 2004). 在小鼠模型中,RKIP表达的恢复抑制前列腺癌转移,这一发现突显了RKIP在转移中的重要性(北川付等。, 2005;傅,史密斯等。2003年). 最近的研究表明,RKIP也是人类前列腺癌发病机制的良好预后标志(北川付等。, 2005)结直肠癌总生存率和无病生存率的预后指标(阿尔·穆拉,哈根等。, 2006). 总之,这些研究表明,RKIP是一种新型的肿瘤转移抑制因子,是导致细胞凋亡的信号转导途径的效应器。尽管有大量实验证据表明肿瘤中RKIP表达降低的有害后果,但肿瘤中RJIP下调的机制尚不完全清楚。
为了建立一个研究RKIP转录调控的系统,我们检测了不同转移能力的癌细胞株中RKIP的表达水平。根据临床肿瘤研究,我们观察到在转移潜能增加的乳腺癌和前列腺癌细胞系中,RKIP蛋白的表达水平逐渐降低。RKIP在侵袭性和转移性乳腺(MB231、MB435和578T)和前列腺(DU145和PC3)细胞系中的表达较低,在非侵袭性细胞系如MCF7、BT20和LNCaP中的表达较高(图1a). 值得注意的是,RKIP蛋白水平与细胞间黏附蛋白E-cadherin(E-cad)的水平密切相关。E-caderin是一种被广泛证实的肿瘤转移抑制蛋白,受蜗牛和密切相关的Slug转录因子调控(奥利米达·佩纳多等。, 2007). 通过qRT-PCR对不同癌细胞系中RKIP转录物水平的定量表明,它们与蛋白质水平相关(图1b)这表明RKIP表达通过mRNA稳定性或转录起始的变化在RNA水平下调。
图1。RKIP在高转移癌细胞中的表达受到抑制。
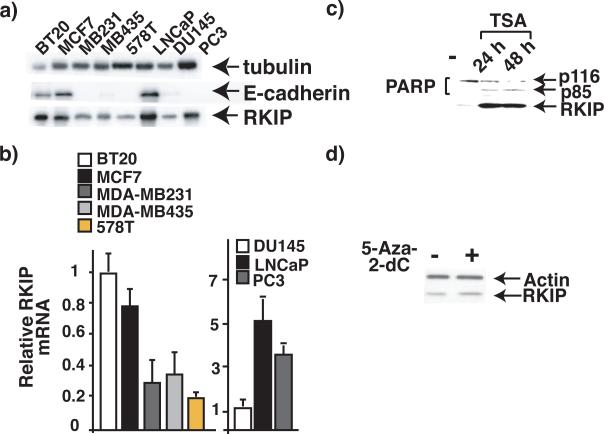
a)前列腺癌或乳腺癌细胞提取物与特异性抗体的免疫印迹分析。b)通过qRT-PCR测量前列腺癌细胞内RKIP mRNA的内源性水平,并将其归一化为GAPDH(左)或mATP6的水平。每个条形代表平均值±PCR反应的SEM(标准误差平均值)一式三份。c-d)前列腺癌细胞DU145经c)TSA或d)5-Aza-2-dC处理24或48小时后的提取物免疫印迹分析,如图所示。所示数据代表三个独立实验。
DNA甲基化是基因沉默的一种重要的表观遗传机制,通常被癌细胞用来灭活抑癌基因(Baylin&Herman,2000年;赫尔曼和巴林出版社,2000年). 甲基化通常发生在含有CpG二核苷酸的DNA小片段或位于近端启动子区的CpG岛上。甲基化CpG岛是组蛋白脱乙酰酶募集的对接位点,导致稳定的转录抑制。甲基化启动子被抑制的状态可以被甲基化抑制剂5-Aza2dC或组蛋白去乙酰化酶抑制剂曲古抑菌素a(TSA)逆转。为了确定转移性前列腺细胞系中甲基化是否抑制RKIP,我们检测了TSA对RKIP表达的影响。针对RKIP的免疫印迹显示,TSA处理导致DU145细胞中RKIP表达的显著增加。与其作为一种重要的凋亡调节器的作用一致,TSA处理细胞中RKIP表达的增加也伴随着广泛的凋亡,如常见的凋亡标记物PARP的裂解所测(图1c). 为了直接表明甲基化抑制了RKIP的表达,用3 M 5-Aza-2dC处理DU145细胞72 h。用RKIP特异性抗体免疫印迹监测RKIP表达。然而,与TSA不同,5-Aza-2dC对RKIP表达没有影响(图1d). 如报告所示(Soengas,Capodieci公司等。, 2001),用同样浓度的5-Aza-2dC处理黑色素瘤细胞,可强烈诱导促凋亡Apaf1(未显示)。使用去甲基化试剂5-Aza-2dC的这些结果清楚地表明,启动子高甲基化不是DU145中RKIP下调的原因。我们发现,TSA可以诱导RKIP的表达,这意味着RKIP的表达可能在癌细胞中被积极抑制。
基因表达研究已确定E-cad的转录抑制是癌症转移的关键事件。在这个过程中涉及的转录因子中,蜗牛被证明是电子cad转录(尼托,2002;蒂里,2002). 鉴于RKIP在转移癌细胞系中的表达下调,以及RKIP和E-cad在几个癌细胞系的共同表达(图1a),我们假设蜗牛可能与RKIP作用于同一途径。与这一假设一致,我们在前列腺癌细胞系中观察到蜗牛蛋白的表达与RKIP的表达呈负相关(图2a). 为了直接检测蜗牛在RKIP表达中的因果作用,我们将一种通过逆转录病毒感染构建的蜗牛表达构建物引入到RKIP水平相对较高的非转移癌细胞系LNCaP中。为了避免高度不稳定的蜗牛对RKIP表达的可能影响,一种突变的稳定变异体(蜗牛-6SA),其共有GSK-3β位点中的六个可磷酸化Ser全部突变为Ala(周、邓等。, 2004)与野生型蜗牛一起使用。正如预期的那样,在稳定感染的LNCaP细胞中检测到大量蜗牛-6SA(图2b)尽管野生型蜗牛几乎无法被发现。
图2。蜗牛是RKIP表达的直接阻遏物。
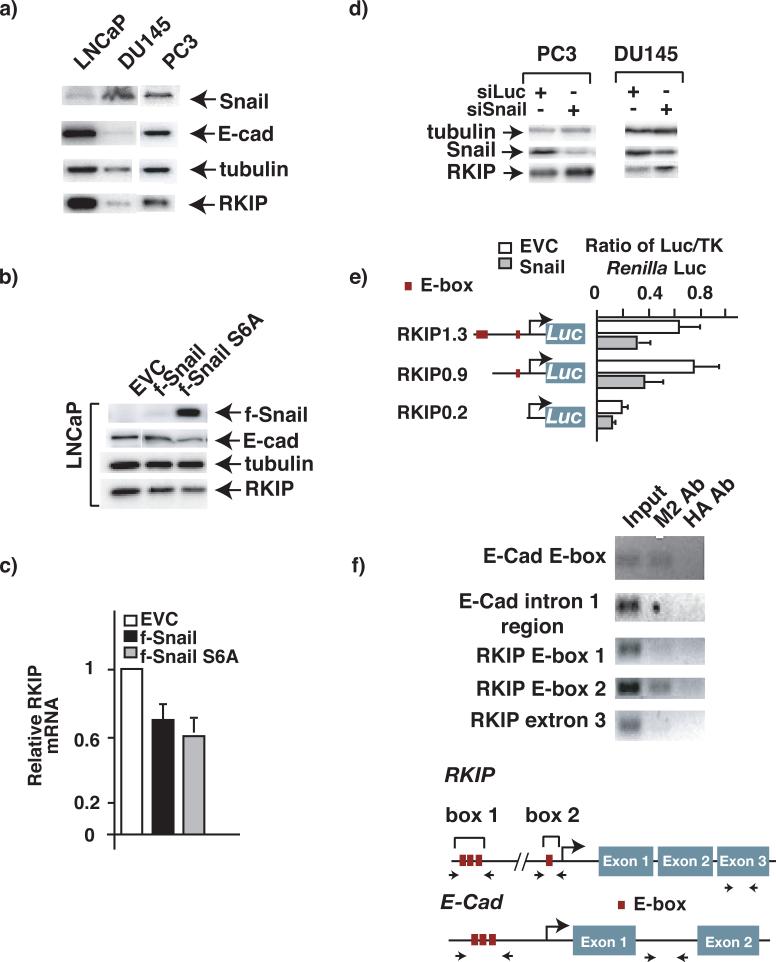
a)通过Western blot分析比较前列腺癌细胞系中RKIP和蜗牛的表达。使用多克隆抗RKIP或蜗牛抗体对Triton x-100提取的细胞裂解物(30μg)进行免疫印迹。用抗肌动蛋白血清重新切割同一膜,作为负荷对照。b-c)蜗牛异位表达抑制RKIP表达。b) 用特定抗体对稳定感染指示逆转录病毒或EVC(空载体对照)的癌细胞提取物进行免疫印迹分析。c) 稳定感染所示逆转录病毒的LNCaP细胞中RKIP mRNA水平的比较。用qRT-PCR测定感染细胞内RKIP mRNA的内源性水平,并将其归一化为GAPDH水平。每个条形代表平均值±PCR反应的SEM一式三份。d) 蜗牛在前列腺癌细胞中的下调增强了RKIP的表达。细胞被表达shRNA的逆转录病毒稳定感染荧光素酶或蜗牛通过免疫印迹分析测定感染细胞内RKIP、微管蛋白和蜗牛蛋白的内源性水平。e) 蜗牛抑制癌细胞中的RKIP启动子报告子。用指定的效应质粒和报告质粒转染MCF7细胞。转染48h后收集细胞进行荧光素酶检测。包含RKIP启动子区域的RKIP-LUC报告子的示意图显示在左侧。显示了假定电气箱的位置。TK代表胸苷激酶。f) 蜗牛与RKIP公司发起人。在稳定表达Flag-taged蜗牛蛋白的LNCaP细胞上使用抗Flag或抗HA抗体进行ChIP分析。用抗体免疫沉淀下来的DNA用引物对PCR扩增,如下图箭头所示。
根据先前发表的结果,蜗牛S6A的异位表达下调了LNCaP细胞中E-cad的表达。此外,我们观察到相同细胞中RKIP在蛋白质和RNA水平上的表达显著下降,而感染空病毒控制(EVC)则没有影响(图2b-c). RKIP表达的抑制与蜗牛表达水平相关,因为蜗牛变体S6A相对于野生型蜗牛具有更强的作用(图2b-c). 相反,当特异性siRNA抑制蜗牛的表达时,转移性PC3和DU145前列腺癌细胞中RKIP的表达水平增加(图2d)这意味着蜗牛是RKIP的生理相关阻遏物。
检查RKIP公司启动子显示至少有四个潜在的蜗牛结合共识位点(E-box:CANNTG)聚集在近端的两个位置RKIP公司发起人。为了确定蜗牛是否以E-box依赖的方式调节RKIP表达,我们检测了过度表达蜗牛对RKIP公司启动子驱动的荧光素酶报告子在MCF7乳腺癌细胞中的表达,其天然蜗牛表达水平低,相对容易转染。三个不同的RKIP公司使用包含所有四个、一个或无E-box结合位点的启动子荧光素酶报告子。与蜗牛的异位表达下调RKIP的观察结果一致,蜗牛的强迫表达被抑制RKIP公司包含一个或全部四个电子盒的荧光素酶记者顺式-元素,而RKIP公司缺乏所有电子盒子元素的记者对蜗牛的镇压反应不佳(图2e).
确定蜗牛是否与RKIP公司该启动子直接用稳定表达鞭毛标记的蜗牛S6A的LNCaP细胞制备的纯化交联染色质进行染色质免疫沉淀(ChIP)实验。为了支持蜗牛在RKIP表达中的调节作用,发现可检测到的蜗牛数量与RKIP公司启动子位于E-box 2,但不位于E-box 1或外显子3RKIP公司基因座(图2f). 正如预期的那样,我们的阳性对照显示蜗牛与它已知的直接靶基因——蜗牛体内的E-box结合钙黏蛋白基因启动子-但不到内含子区域。这些结果证实了瞬时报告试验,该试验表明近端E-Box足以抑制蜗牛介导的RKIP公司发起人。
我们推断,如果蜗牛是前列腺癌中RKIP表达的生理相关抑制剂,那么我们应该观察它们在癌症样本中的表达模式之间的负相关。因此,我们查询了来自人类前列腺癌(包括Oncomine)的公开可用DNA微阵列表达数据集(网址:www.oncomine.org)和NCBI的基因表达总览(GEO)(http://www.ncbi.nlm.nih.gov/enterz/query.fcgi?db=gds)RKIP和蜗牛。我们最初专注于研究进展性前列腺癌和转移的数据集。确定了10个数据集,包括正常和/或良性前列腺增生(BPH)、局限性前列腺癌(PCA)和前列腺癌转移(MPC)的分析。其中一个(巴雷特·达纳塞卡兰等。, 2001)数据集#1显示,从正常前列腺癌到局限性前列腺癌到转移性前列腺癌,蜗牛的表达在统计学上显著增加。正如预期的那样,E-cad的表达在局部癌症样本和转移样本之间也显著降低,E-cad是蜗牛的已证实直接靶点。重要的是,同一数据集显示,随着前列腺癌的进展,RKIP表达显著下降(图3a). 样本参照他们自己的前列腺癌患者的正常邻近前列腺(NAP)组织池。
图3。前列腺癌标本中RKIP的表达与蜗牛呈负相关。
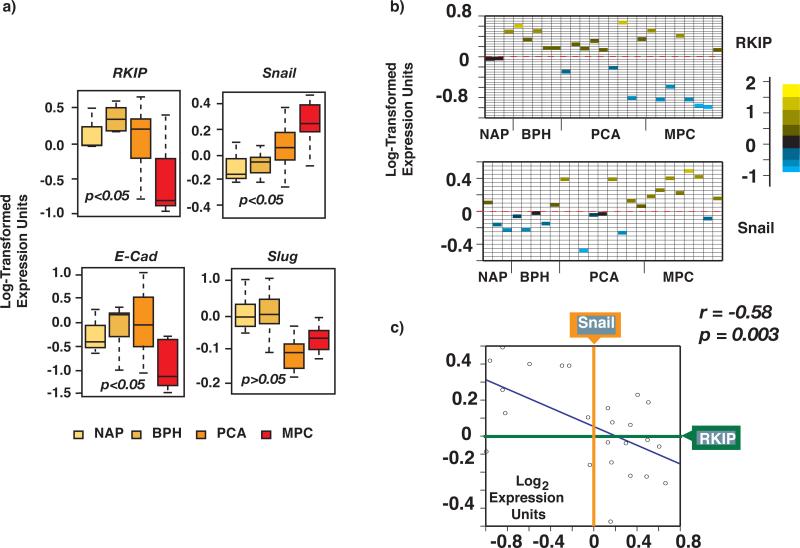
a)前列腺癌微阵列数据集中RKIP和蜗牛水平的方框图。方框表示分布的标准偏差,穿过方框的线表示该分布的平均值。方框上方和下方的水平线表示分布的极值。使用统计程序R.NAP N=3、BPH N=5、PCA N=10和MET N=7,对参考前列腺癌样本与患者正常邻前列腺(NAP)样本池的比率进行对数转换和绘图。b)绘制每个样本的RKIP或蜗牛的对数转换表达单位。样本分为NAP、BPH、PCA和MPC,如a)所示。c) a)中显示的蜗牛与所有样本RKIP的散点图
为了研究RKIP和蜗牛表达之间的相关性,我们在数据集#1中比较了它们在每个前列腺癌样本中的表达(图3b). 我们还通过绘制蜗牛对RKIP的对数转换表达单位直接量化了它们的表达关系,并使用皮尔逊相关系数测量了它们的表现相似性第页。如所示图3c我们在所有样本中观察到RKIP和蜗牛之间存在显著的负相关第页=-0.58和对值=0.003。正如预期的那样,E-cad的表达也与所有样本中的蜗牛呈显著负相关(第页= -0.57;对值=0.003)(图3c). 密歇根大学Arul Chinnaiyan博士提供的另一个数据集(数据集#2)也获得了类似的结果(未显示)。
由于蜗牛超家族的另一个成员Slug与蜗牛具有许多生理功能,并与促进癌症侵袭有关,因此确定其表达是否也与RKIP水平呈负相关是很有意义的。出乎意料的是,我们不仅没有观察到Slugs的表达水平从正常样本到BPH、PCA和MPC样本有任何增加,而且事实上,这两个数据集的表达水平都有所下降(图3a). 尽管PCA和MPC样本之间的Slug略有增加,但差异在统计学上并不显著。
最近有报道称RKIP在转移性前列腺癌中下调(Fu,北川等。, 2005;傅,史密斯等。2003年). 然而,尚不清楚RKIP在癌症中是如何下调的,也不知道它是如何转录调控的。我们通过qRT-PCR显示,在高转移前列腺癌细胞系PC3和DU145中,稳态RKIP mRNA降低。甲基化抑制剂5-Aza2dC和组蛋白去乙酰化酶抑制剂曲古抑菌素A(TSA)的研究表明,前列腺癌转移中RKIP表达的转录启动受到积极抑制。
蜗牛锌指转录因子超家族对于胚胎发生过程中上皮-间充质转化(EMT)的诱导至关重要。EMT程序中的异常已被证明会驱动癌细胞的侵袭和转移(蒂里,2002). EMT的过程涉及显著的表型变化,包括上皮标志物的丢失、间充质标志物的获得和细胞形状的变化。蜗牛导致EMT的下游效应器目标之一是电子cadE-cad的表达在维持上皮细胞的细胞间粘附中起关键作用。蜗牛直接将电子cad强抑制转录的启动子(桑乔·巴特勒等。, 2000;佩雷兹·莫雷诺·卡诺等。, 2000). 在包括前列腺癌在内的各种癌症中,观察到E-cad和蜗牛的表达呈负相关。(莫雷诺-布诺·布兰科等。, 2002;Jiao,Miyazaki宫崎骏等。, 2002;多明格斯·波斯尔等。, 2001;神田横山等。, 2001). 在这项研究中,我们提出了令人信服的证据,表明RKIP是蜗牛在晚期前列腺癌中的另一个转录靶点。在转移性前列腺癌样本中,我们观察到RKIP表达水平与转录抑制因子蜗牛之间存在统计学意义上的负相关。我们观察到RKIP在低转移细胞系LNCaP中高表达,但在DU145和PC3细胞系中表达降低。RKIP在这些细胞系中的表达与E-cad表达相似,并且与蜗牛表达呈负相关。我们发现过度表达或敲倒蜗牛可以调节RKIP表达,蜗牛可以抑制RKIP启动子活性在体外.
转录因子蜗牛具有一个保守的羧基末端区域,包含四到六个C2H2型锌指重复序列(Knight&Shimeld,2001年)和一个氨基蜗牛/Gfi(SNAG)结构域。当手指作为序列特异性DNA结合基序发挥作用时,SNAG域是增强哺乳动物细胞中阻遏物活性的效应域(陈格里姆斯等。, 1996;斯科特·中山等。, 1998). 研究表明,蜗牛通过与E-box结合来抑制转录起始顺式-元素和招募染色质重塑mSin3A和组蛋白去乙酰化酶包含阻遏物复合物。通过ChIP分析,我们发现Snail与RKIP启动子中假定的E-box 2存在物理联系。我们还发现E-box 2的存在与蜗牛对RKIP启动子的抑制有关。然而,目前我们不知道E-box 2是否是蜗牛介导的观察到的抑制所必需的。我们也不知道锌指或SNAG结构域是否对RKIP表达的抑制至关重要。
除了电子cad,蜗牛还有许多其他下游效应器目标。研究表明,蜗牛可以下调紧密连接组分克劳丁和闭塞素以及上皮标记物黏蛋白-1的表达。它还增加了间充质标记物波形蛋白和纤维连接蛋白的表达,金属蛋白酶-2和-9等参与癌症侵袭的蛋白质,以及转录因子ZEB-1和LEF-1的表达(德克雷恩、范罗伊等。,2005年;尼托,2002). 蜗牛如何负调控基因表达的分子机制已经部分阐明,涉及蜗牛与靶基因启动子的直接结合。相比之下,对于蜗牛如何激活基因表达,我们知之甚少。蜗牛似乎是通过涉及另一种介质的间接机制激活的。例如,已有研究表明,蜗牛诱导MMP-9的表达依赖于Raf-MEK-Erk和PI3K信号通路(奥尔米达·若尔达等。, 2005). 在蜗牛表达细胞中也观察到NF-κB与MMP-9启动子的结合增加。鉴于RKIP对Raf和NF-κB信号通路的抑制作用,蜗牛对MMP-9或其他靶基因的激活可能是由RKIP的抑制引起的。除了调控编码对细胞-细胞和细胞-基质相互作用重要蛋白的基因外,蜗牛在促进细胞凋亡抵抗和调节细胞周期进展方面也发挥着重要作用(McClinic卡吉塔等。, 2004;莫拉莱斯织女星等。, 2004). 蜗牛靶基因的相关基因库尚未完全阐明。由于RKIP在细胞生存和增殖中具有负面作用,它可能是蜗牛转录轴的一个新的下游效应器,对癌症的进展和转移至关重要。
致谢
我们感谢Stephen J Weiss和Mien-Chie Hung的质粒构建。我们还感谢Chinnaiyan的实验室在研究RKIP和蜗牛在前列腺癌中的表达相关性方面提供的帮助。这项工作得到了国家卫生研究院对KCY(R01 GM64767)的拨款支持,AD和WK得到了英国癌症研究院的支持,UTHSC的转化研究激励奖也得到了KCY的支持。
工具书类
-
Al-Mulla F、Hagan S、Behbehani AI、Bitar MS、George SS、Going JJ、Garcia JJ、Scott L、Fyfe N、Murray GI、Kolch W.Raf激酶抑制剂蛋白在结直肠癌患者生存分析中的表达。临床肿瘤学杂志。2006;24:5672–9. doi:10.1200/JCO.2006.07.5499。[内政部] [公共医学] [谷歌学者]
-
Batlle E、Sancho E、Franci C、Dominguez D、Monfar M、Baulida J、Garcia De Herreros A。转录因子snail是上皮性肿瘤细胞中E-cadherin基因表达的阻遏物。自然细胞生物学。2000;2:84–9. doi:10.1038/35000034。[内政部] [公共医学] [谷歌学者]
-
Baylin SB、Herman JG。肿瘤发生中的DNA超甲基化:表观遗传学与遗传学的结合。趋势基因。2000;16:168–74。doi:10.1016/s0168-9525(99)01971-x。[内政部] [公共医学] [谷歌学者]
-
Blanco MJ、Moreno-Bueno G、Sarrio D、Locascio A、Cano A、Palacios J、Nieto MA。乳腺癌中蜗牛表达与组织学分级和淋巴结状态的相关性。致癌物。2002;21:3241–6. doi:10.1038/sj.onc.1205416。[内政部] [公共医学] [谷歌学者]
-
Cano A、Perez-Moreno MA、Rodrigo I、Locascio A、Blanco MJ、del Barrio MG、Portillo F、Nieto MA。转录因子snail通过抑制E-cadherin的表达来控制上皮-间质转换。自然细胞生物学。2000;2:76–83. doi:10.1038/35000025。[内政部] [公共医学] [谷歌学者]
-
Chatterjee D、Bai Y、Wang Z、Beach S、Mott S、Roy R、Braastad C、Sun Y、Mukhopadhyay A、Aggarwal BB、Darnowski J、Pantazis P、Wyche J、Fu Z、Kitagwa Y、Keller ET、Sedivy JM、Yeung KC。RKIP使前列腺癌和乳腺癌细胞对药物诱导的凋亡敏感。生物化学杂志。2004;279:17515–23. doi:10.1074/jbc。M313816200。[内政部] [公共医学] [谷歌学者]
-
De Craene B,van Roy F,Berx G.《蜗牛转录因子家族的信号级联展开》。细胞信号。2005;17:535–47. doi:10.1016/j.cellsig.2004.10.011。[内政部] [公共医学] [谷歌学者]
-
Dhanasekaran SM、Barrette TR、Ghosh D、Shah R、Varambally S、Kurachi K、Pienta KJ、Rubin MA、Chinnaiyan AM。前列腺癌预后生物标志物的描述。自然。2001;412:822–6。doi:10.1038/35090585。[内政部] [公共医学] [谷歌学者]
-
Fu Z、Kitagawa Y、Shen R、Shah R、Mehra R、Rhodes D、Keller PJ、Mizokami A、Dunn R、Chinnaiyan AM、Yao Z、Keller-ET。转移抑制基因Raf激酶抑制剂蛋白(RKIP)是前列腺癌的一种新的预后标记物。前列腺。2005年doi:10.1002/pros.20319。[内政部] [公共医学] [谷歌学者]
-
Fu Z,Smith PC,Zhang L,Rubin MA,Dunn RL,Yao Z,Keller ET。raf激酶抑制剂蛋白表达对前列腺癌转移的抑制作用。2003年国家癌症研究所杂志;95:878–89. doi:10.1093/jnci/95.12.878。[内政部] [公共医学] [谷歌学者]
-
Grimes HL,Chan TO,Zweidler-McKay PA,Tong B,Tsichlis PN。Gfi-1原癌蛋白包含一个新的转录抑制域SNAG,并抑制白细胞介素-2戒断诱导的G1期阻滞。分子细胞生物学。1996;16:6263–72. doi:10.1128/mcb.16.11.6263。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
Hegan S,Al-Mulla F,Mallon E,Oien KA,Ferrier R,Gusterson B,Garcia JJC,Kolch W.乳腺癌转移中Raf-1激酶抑制剂蛋白(RKIP)表达的减少。临床癌症研究。2005年doi:10.1158/1078-0432.CCR-05-0283。[内政部] [公共医学] [谷歌学者]
-
Herman JG,Baylin SB。人类癌症中的启动子区超甲基化和基因沉默。当前顶级微生物免疫学。2000;249:35–54. doi:10.1007/978-3-642-59696-43。[内政部] [公共医学] [谷歌学者]
-
Jiao W,Miyazaki K,Kitajima Y.体外和体内肝细胞癌细胞系中E-cadherin和蜗牛表达的反向相关性。英国癌症杂志。2002;86:98–101. doi:10.1038/sj.bjc.6600017。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
Jorda M、Olmeda D、Vinyals A、Valero E、Cubillo E、Llorens A、Cano A、Fabra A.MDCK上皮细胞系中MMP-9对蜗牛转录因子表达的上调。细胞科学杂志。2005;118:3371–85. doi:10.1242/jcs.02465。[内政部] [公共医学] [谷歌学者]
-
Kajita M,McClinic KN,Wade PA。转录因子蜗牛和蛞蝓的异常表达改变了对基因毒性应激的反应。分子细胞生物学。2004;24:7559-66。doi:10.1128/MCB.24.17.7559-7566.2004。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
Knight RD,Shimeld SM。双孢菌中保守C2H2锌指基因家族的鉴定。基因组生物学。2001;2 doi:10.1186/gb-2001-2-5-research0016。研究0016。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
Lee HC,Tian B,Sedvy JM,Wands JR,Kim M。raf激酶抑制剂蛋白的缺失促进人肝癌细胞的增殖和迁移。胃肠病学。2006;131:1208–17. doi:10.1053/j.gastro.2006.07.012。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
Nakayama H、Scott IC、Cross JC。滋养层巨细胞向内复制的过渡受mSNA锌指转录因子调节。开发生物。1998;199:150–63. doi:10.1006/dbio.1998.8914。[内政部] [公共医学] [谷歌学者]
-
Nieto MA。锌指转录因子的蜗牛超家族。Nat Rev Mol细胞生物学。2002;3:155–66. doi:10.1038/nrm757。[内政部] [公共医学] [谷歌学者]
-
Park S、Yeung ML、Beach S、Shields JM、Yeung KC。RKIP下调黑色素瘤癌细胞中的B-Raf激酶活性。致癌物。2005;24:3535–3540. doi:10.1038/sj.onc.1208435。[内政部] [公共医学] [谷歌学者]
-
Peinado H、Olmeda D、Cano A.蜗牛、Zeb和bHLH因子在肿瘤进展中的作用:与上皮表型的联合?Nat Rev癌症。2007;7:415–28. doi:10.1038/nrc2131。[内政部] [公共医学] [谷歌学者]
-
Poser I、Dominguez D、de Herreros AG、Varnai A、Buettner R、Bosserhoff AK。黑色素瘤细胞中E-cadherin表达的缺失涉及转录抑制因子Snail的上调。生物化学杂志。2001;276:24661–6. doi:10.1074/jbc。M011224200。[内政部] [公共医学] [谷歌学者]
-
Schuerer MM、Bataille F、Hagan S、Kolch W、Bosserhoff AK。黑色素瘤细胞系中Raf激酶抑制剂蛋白表达的减少与Ras-细胞外信号调节激酶信号的增加有关。癌症研究2004;64:5186–92. doi:10.1158/0008-5472.CAN-03-3861。[内政部] [公共医学] [谷歌学者]
-
Schuerer MM、Bataille F、Weiss TS、Hellerbrand C、Bosserhoff AK。肝细胞癌中Raf激酶抑制剂蛋白下调。2006年Oncol众议员;16:451–6.[公共医学] [谷歌学者]
-
Soengas MS、Capodieci P、Polsky D、Mora J、Esteller M、Opitz-Araya X、McCombie R、Herman JG、Gerald WL、Lazebnik YA、Cordon-Cardo C、Lowe SW。恶性黑色素瘤中凋亡效应物Apaf-1的失活。自然。2001;409:207–11. doi:10.1038/35051606。[内政部] [公共医学] [谷歌学者]
-
Thiery JP。肿瘤进展中的上皮-间充质转化。Nat Rev癌症。2002;2:442–54. doi:10.1038/nrc822。[内政部] [公共医学] [谷歌学者]
-
Vega S、Morales AV、Ocana OH、Valdes F、Fabregat I、Nieto MA。蜗牛阻断细胞周期并赋予细胞死亡抵抗力。基因开发2004;18:1131–43. doi:10.10101/gad.294104。[内政部] [PMC免费文章] [公共医学] [谷歌学者]
-
Yokoyama K、Kamata N、Hayashi E、Hoteiya T、Ueda N、Fujimoto R、Nagayama M。体外口腔鳞癌细胞中E-cadherin和蜗牛表达的反向相关性。口腔癌。2001;37:65–71. doi:10.1016/s1368-8375(00)00059-2。[内政部] [公共医学] [谷歌学者]
-
Zhang L,Fu Z,Binkley C,Giordano T,Burant CF,Logsdon CD,Simeone DM。Raf激酶抑制蛋白抑制β细胞增殖。外科手术。2004;136:708–15. doi:10.1016/j.surg.2003.12013。[内政部] [公共医学] [谷歌学者]
-
周碧萍,邓杰,夏伟,徐杰,李英明,Gunduz M,Hung MC。GSK-3介导的磷酸化对蜗牛上皮-间质转化的双重调控。自然细胞生物学。2004;6:931–40. doi:10.1038/ncb1173。[内政部] [公共医学] [谷歌学者]





