背景 zeste同源物2增强子(Ezh2)是多梳组(PcG)蛋白家族的一员,通过重塑染色质抑制基因表达[ 1 ]. 作为组蛋白甲基转移酶,Ezh2催化组蛋白H3赖氨酸27(H3-K27)三甲基化[ 2 ]这是基因沉默的标志[ 三 ]. Ezh2是多梳抑制复合物2(PRC2)的重要组成部分,是维持基因沉默所必需的。 Ezh2与其他PcG蛋白的结合对其甲基转移酶功能至关重要,因为PRC2的药物破坏抑制H3-K27的甲基化[ 4 ]. Ezh2需要被YY1和E2F等DNA结合蛋白招募,以与染色质结合并发挥其功能[ 5 , 6 ]. 此外,Ezh2及其相关PcG蛋白调节各种生物过程,包括X染色体失活[ 7 ]、干细胞自我更新和衰竭[ 8 , 9 ]、骨骼肌分化[ 10 ],肌动蛋白聚合[ 11 ]和生物钟功能[ 12 ].
越来越多的证据表明Ezh2在癌症中起着重要作用。 许多研究表明Ezh2过表达是前列腺癌(PCa)中的一种常见现象,与PCa患者的不良临床结局有关[ 6 , 13 - 15 ]. 因此,Ezh2被认为是一个真正的致癌基因[ 13 ]其升高可作为前列腺肿瘤侵袭性和转移性的标志物。 几项研究也表明了Ezh2作为PCa治疗靶点的前景。 小干扰RNA(siRNA)敲低Ezh2降低前列腺细胞增殖[ 13 ]抑制骨组织中PC-3细胞的转移瘤生长[ 16 ]. 另一方面,Ezh2促进PCa细胞的增殖和侵袭[ 17 ]前列腺细胞中外源性表达的Ezh2促进增殖[ 18 ]. 这些研究表明Ezh2在侵袭性PCa中的作用,并提示Ezh2可能是PCa治疗的靶点[ 18 ]. 总之,Ezh2在PCa中起致癌作用,阐明调节Ezh2功能的机制可能为治疗这种癌症提供基本的治疗思路。
先前的研究表明,Ezh2可以在转录或翻译水平上进行调节。 抑癌基因p53[ 19 ]和转录因子E2F[ 6 ]可以与Ezh2基因的启动子结合,分别抑制或反式抑制其表达。 此外,Ezh2通过Akt进行翻译后修饰,从而降低其甲基转移酶活性[ 20 ]. 最近,越来越多的证据表明,microRNAs(miRNAs)可以在转录后水平调节基因表达。 因此,我们想研究Ezh2是否也受miRNAs调控。
微RNA是一组含有17-24核苷酸的小RNA,通过干扰mRNA翻译来调节基因表达[ 21 ]. 大量证据表明,miRNAs可能通过作为致癌基因或肿瘤抑制因子来调节肿瘤的发生[ 22 ]. 有趣的是,不同的癌症在miRNA表达谱研究中表现出特征性的miRNA特征[ 23 ]. 然而,在理解miRNA-介导的癌症发展和进展的确切机制方面仍然存在差距。 由于Ezh2在前列腺癌进展中的重要性及其作为前列腺癌治疗靶点的潜力,鉴定调节Ezh2表达的miRNA可能有助于开发前列腺癌治疗的新治疗方法。 最近的一项研究表明,miR-101的基因组缺失导致Ezh2在人类癌症样本中过表达,这表明miR-101调节的Ezh2功能在前列腺癌发展中的生理意义[ 24 ]. 在当前研究中,我们证明miR-101负调控PCa细胞中Ezh2的表达,miR-101的表达受雄激素刺激和HIF-1α/HIF-1β诱导的影响。
材料和方法 抗体和试剂 抗Ezh2(4905)、HIF-1β/ARNT(3718S)、三甲基-甾酮H3-Lys 27(H3K27m3,9756)和拉明A/C(2032)的抗体购自Cell Signaling Technology(Danvers,MA)。 HIF-1α抗体由Constantinos Koumenis博士(宾夕法尼亚大学医学院)善意提供。 组蛋白H3(C-16,sc-8654)和雄激素受体抗体(N-20,sc-816)购自圣克鲁斯生物技术公司(加州圣克鲁斯)。
微RNA、siRNA、DNA质粒和转染 Dharmacon,Inc.(伊利诺伊州芝加哥)合成了所有microRNA模拟物(miR-101、miR-26a和一个干扰对照),序列如下:miR-101,UACAGUACUGUGAACUGAA; miR-26a:UUCAAGUAAUCCAGGAUGCU; 和加扰控制(miR-cont):UCACAACCUAGAAAGAGUAGA。 用于对照的siRNAs(GGG-CCA TGG-CAC-GTA-CGG-CAA-G)和Ezh2(GGT-GAT CAC-AGG-ATA-GGT-ATT)通过携带抗嘌呤霉素cDNA的慢病毒载体pLU传递[ 25 ].
为了生成报告构建物,我们从人类基因组DNA(P/N:5-0109,Affymetrix,Inc.)中扩增了一个493-碱基对(bp)DNA片段,该片段由Ezh2编码区的最后50 bps和Ezh2 mRNA的3’-UTR的443 bps组成。 Ezh2的这个3'-UTR区域包含miR-101和miR-26a的预测靶位点,然后在Gaussia荧光素酶(GLuc)下游亚克隆,GLuc由磷酸甘油激酶(PGK)启动子驱动。 我们还构建了带有这些miRNAs突变靶点的质粒。 miRNA的种子序列识别其靶位点3'端的7-8核苷酸对miRNA介导的翻译抑制至关重要。 因此,在Ezh2 3'-UTR中miR-101和miR-26a的预测靶位点中,我们分别用扰码序列替换这两个miRNAs种子序列识别的核苷酸。 因此,我们生成了三个对照报告质粒,其中两个miR-101靶位点分别或组合发生突变( 45 AGTACTGT公司 66 至A CCG公司 C G公司 G公司 C 、和/或 101 GTACTGTA公司 121 到 C T型 G公司 C A类 G公司 自动变速箱 ,突变核苷酸以粗体显示),以及一个带有突变miR-26a靶位点的对照报告质粒( 236 塔克塔加 257 到 CTGCA公司 G公司 计算机断层扫描 ). 为了在PC-3细胞中表达Ezh2,Ezh2 cDNA(由Sartorelli博士慷慨提供[ 10 ])分别亚克隆到慢病毒载体pSL4中,pSL4共同表达嘌呤霉素N-乙酰转移酶,使感染细胞对嘌呤菌素产生耐药性。
细胞培养、瞬时转染和慢病毒的产生 PWR-1E、LNCaP、DU145和PC-3细胞系取自美国型培养物收集中心(弗吉尼亚州马纳萨斯)。 LNCaP、DU145和PC-3细胞在添加1%青霉素/链霉素和10%胎牛血清的RPMI 1640中保存。 在雄激素饥饿实验中,LNCaP细胞也在含有1%炭化型FBS(Invitrogen)的无酚红RPMI培养基中培养,并用0、0.01、0.1和10 nM R1881(一种合成的非芳香化雄激素)处理。 PC-3细胞也用溶于RPMI培养基中的100μM甲磺酸去铁胺(DFO,Sigma)处理0和6小时。 PWR-1E细胞保存在角质形成细胞-SFM(Invitrogen)中。 根据制造商提供的方案,使用Lipofectamine 2000(Invitrogen)瞬时转染PC-3细胞。 根据制造商的方案,SiPort NeoFX脂质体胺(Ambion)用于LNCaP的瞬时转染。 慢病毒的生产遵循先前报道的方案[ 26 ]. 简而言之,使用磷酸钙-DNA沉淀转染方案,用空pSL4载体pSL4-Ezh2、pLU-cont(对照)siRNA或pLU-Ezh2 siRNA以及三种包装质粒(pMDLg/pRRE、pRSV-RSE和pVSV-G)转染293T细胞。 转染48小时后收集含有病毒颗粒的培养基。 通过在25000rpm、4°C下超速离心90分钟来浓缩培养基中的慢病毒,并在-80°C下储存。 为了感染细胞,将浓缩的慢病毒加入含有8μg/ml聚布伦的培养基中。 病毒添加后6 h,用正常培养基替换培养基。
荧光素酶报告试验 将培养在12孔板上的每个PC-3细胞孔转染50 ng报告质粒或突变报告质粒miR-101或miR-26a模拟物(每个孔中的最终浓度为100 nM)、100 ng表达由β-肌动蛋白启动子驱动的分泌型碱性磷酸酶(SEAP)的质粒和其他表达质粒(如需要)。 在转染48小时后收集转染孔中的等分培养基,以测量荧光素酶活性。 将50μl培养基(必要时稀释)与100μl底物溶液混合,底物溶液中含有0.5μg/ml的柯来特嗪(CTZ)、200 mM NaCl、50 mM Tris·HCl和0.01%的Triton X-100,pH值为8.7。 在480 nm波长下测量光发射,并用SEAP表达进行归一化[ 27 ].
组蛋白提取 细胞在Triton提取缓冲液(磷酸盐缓冲液,含有0.5%Triton X-100,2 mM苯甲基磺酰氟,0.02%NaN)中重新悬浮 三 ),在冰上轻轻摇晃溶解10分钟,并在4°C下以2000 rpm离心10分钟。 用Triton提取缓冲液清洗细胞颗粒,并如上所述进行离心。 为了提取组蛋白,将细胞颗粒重新悬浮在0.2 N HCl中,并在4°C下轻轻摇晃培养过夜。 在4°C下以2000 rpm离心10分钟后,将含有组蛋白提取物的上清液转移到新试管中,并通过Western blot进行分析。
克隆形成试验 用对照miRNA(miR-cont)或miR-101模拟物(使用Lipofectamine 2000(Invitrogen))转染PC-3细胞。 转染后48小时,在6厘米的细胞培养皿中以不同密度(125、250、500、1000和2000)培养细胞。 7-10天后,用10%福尔马林固定细胞,并用0.1%结晶紫染色。 每个培养皿中计数50个或更多细胞的菌落。
雄激素缺乏和比卡鲁胺治疗 将LNCaP细胞接种在完整培养基中培养48 h。用含1%炭化裂解FBS(Invitrogen)的无酚红色RPMI培养基代替培养基。 在用0、0.01、0.1、1.0和10 nM R1881处理之前,允许细胞再适应这种雄激素缺乏状态24小时。 为了抑制雄激素受体,在添加R1881之前,用5μM比卡鲁胺(B9061,Sigma)预处理雄激素剥夺条件下的LNCaP细胞。
WST-1细胞增殖试验 对LNCaP、DU-145和PC-3细胞进行不同的检测。 将LNCaP细胞以6000个细胞/孔的密度接种在96周的平板上,并使用siPort NeoFX脂质体胺(Ambion)转染对照miRNA(miR-cont)或miR-101模拟物。 在每个时间点,使用WST-1(Roche)按照制造商的方案测量三倍的细胞增殖。 使用脂质体2000(Invitrogen)在6孔板中用miR-cont或miR-101模拟物转染DU-145和PC-3细胞。 转染48小时后,将细胞以2000个细胞/ml的密度分三次接种在96周的平板中。 如上所述,测定每个时间点的细胞增殖。
实时RT-PCR分析 使用TRIzol试剂(Invitrogen)提取细胞总RNA。 细胞中成熟形式的miR-101或miR-26a的水平通过TaqMan MicroRNA Assays(Applied Biosystems)测定,并将数据标准化为U6表达(Applied Biosystems)。 为了测定细胞中Ezh2 mRNA的水平,将2μg RNA与0.5μg/μl寡核苷酸引物(Promega)在70°C下孵育5分钟。然后添加以下逆转录酶混合物,并在42°C下培养1小时:5μl 5×MMLV缓冲液、5μl 10 mM dNTP、0.6μl RNasin、1μl MMLV逆转录酶, 13.4μl无核水。 然后使用Taqman基因表达分析进行定量PCR分析,以检测Ezh2的表达,并将数据归一化为GAPDH表达(应用生物系统)。 所有分析均使用ABI7000序列检测系统进行。 ΔΔC T型 方法[ 28 ]用于计算相对表达式。
Matrigel侵犯分析 将100μl Matrigel(BD Biosciences,在血清自由冷细胞培养基中稀释至1 mg/ml)添加到24孔跨孔板的上室中,并在37°C下培养4小时,直到Matrigel固化。 待测细胞在无FBS培养基中饥饿18-24 h,然后用胰蛋白酶消化法收获,用含1%FBS的培养基洗涤3次,然后在相同的培养基中以1×10的密度重新悬浮 6 细胞/ml。用加热的无血清培养基轻轻清洗聚合的Matrigel。 在Matrigel顶部添加100μl细胞悬浮液,同时在每个底室中添加650μl含有10%FBS的完整培养基。 将组装好的培养箱在37°C的细胞培养箱中培养48小时。仔细抽吸顶部和底部培养箱中的培养基,然后用PBS冲洗。通过计算结晶紫染色的细胞数量来量化细胞侵袭。
迁移分析 通过miR-cont或miR-101模拟物转染LNCaP细胞。 72小时后,细胞在RPMI中以1×10的密度用1%的FBS重新悬浮 5 细胞/ml。向上室添加500μl细胞悬浮液(Becton Dickinson,35-3097,8μm孔径),同时向下室添加750μl含有5%FBS的RPMI。 将培养箱在37°C的细胞培养箱中培养24小时。通过计算结晶紫染色的细胞数量来量化细胞迁移。
伤口愈合分析 将miR-cont或miR-101模拟物转染的LNCaP细胞接种在6孔板中,培养72h,获得80%的单层融合。 用塑料吸管尖端刮伤细胞,形成伤口,用新鲜培养基代替培养基。 立即(第0天)和连续5天每天拍摄图像。 实验结束时,通过伤口大小定性评估细胞迁移。
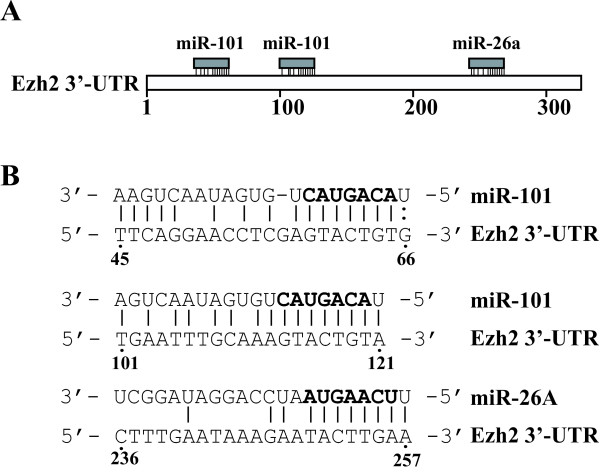
结果 Ezh2 mRNA的3'-UTR含有miR-101和miR-26a的保守靶位点 为了鉴定可能调控Ezh2表达的miRNAs,我们使用桑格研究所(Sanger Institute)提供的算法分析了人类Ezh2的3'-UTR序列(参见[ 29 ]和 http://microrna.sanger.ac.uk/ )预测潜在的miRNA靶位点。 我们确定了一些可能调节Ezh2表达的miRNA候选基因。 我们选择miR-101和miR-26a进行进一步研究,因为这两个miRNAs表现出较高的结合分数,并且它们在Ezh2的3'-UTR上的靶位点在人类、猴子、小鼠、鸡和鸭嘴兽等多种物种中都是保守的。 此外,当我们使用其他miRNA目标预测算法时[ 30 - 32 ]为了分析Ezh2序列,这两个miRNAs也出现在了候选序列中。 重要的是,最近的两项研究表明miR-26a靶向Ezh2[ 33 , 34 ]其他研究表明这两种miRNA在癌症中下调[ 35 , 36 ]. 如果我们任意将Ezh2 mRNA终止密码子后面的核苷酸指定为“1”,其下游侧指定为“+”,则miR-101的两个预测靶位点出现在45-66和101-121,而一个miR-26a靶位点出现于236-257(图。 1安培 ). miR-101和miR-26a在人类Ezh2 3'-UTR上与其假定靶序列的比对如图所示。 1磅 .
图1。
miR-101和miR-26a在Ezh2 3'-UTR中的预测靶点示意图 . 答:。 Ezh2的3'-UTR中有两个预测的miR-101靶点和一个预测的miR-26a靶点。 Ezh2终止密码子后面的第一个核苷酸被任意指定为“1”。 B。 miR-101和miR-26a与Ezh2的3'-UTR中相应潜在靶位点的序列比对。 两个miRNAs的种子序列用粗体标记,并指示miRNAs和Ezh2 3'-UTR之间的匹配或互补核苷酸。 Ezh2 3'-UTR上每个预测目标的位置标记在路线下方。
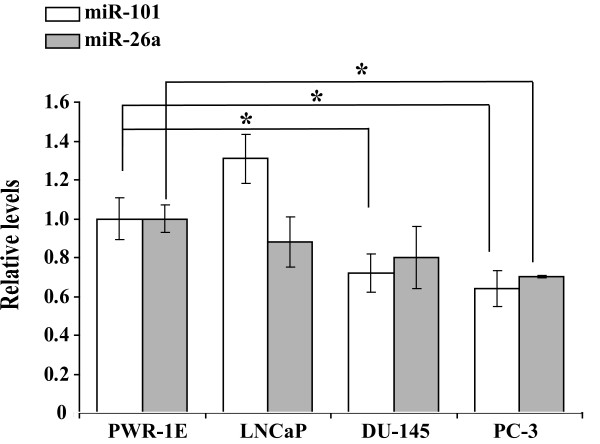
miR-101和miR-26a在前列腺癌细胞系中的表达 先前对miRNA谱的研究表明,前列腺癌中miR-101和miR-26a的水平降低[ 35 , 36 ]. 为了确定这两种miRNA的表达与前列腺癌细胞系恶性程度之间的相关性,我们使用实时RT-PCR研究了成熟形式miR-101和miR-26a在四种不同前列腺细胞系中的表达:PWR-1E、LNCaP、DU-145和PC-3。 PWR-1E是一种非肿瘤性前列腺上皮细胞系[ 37 ]如前一项研究所述,其他三种细胞系具有致瘤性,并表现出更强的侵袭性,顺序为LNCaP、DU-145和PC-3[ 38 ]. 如图所示。 2 与PWR-1E细胞相比,DU-145和PC-3细胞的miR-101表达显著降低(分别降低34%和41%,p<0.05),而LNCaP细胞的miR-101表达略有增加(图。 2 ). 尽管miR-26a的表达与这四种细胞系的侵袭性之间的负相关仅为微小,但PC-3和PWR-1E之间的表达差异仍然显著(减少30%,p=0.05)。
图2。
前列腺癌细胞系中miR-101和miR-26a的表达分析 RT-PCR使用从PWR-1E、LNCaP、DU-145和PC-3细胞中分别提取的RNA,以及miR-101或miR-26a特异的干环引物。 使用FAM标记的miR-101或miR-26a探针(Applied BioSystems)通过Taqman实时PCR对生成的cDNA进行进一步分析。 每个样品分析三次。 数据表示为两个实验的平均值,并使用ΔΔC归一化为内源性U6 RNA的表达 T型 方法[ 28 ]如材料和方法所述。 学生T检验用于确定统计显著性,星号表示p值不高于0.05。
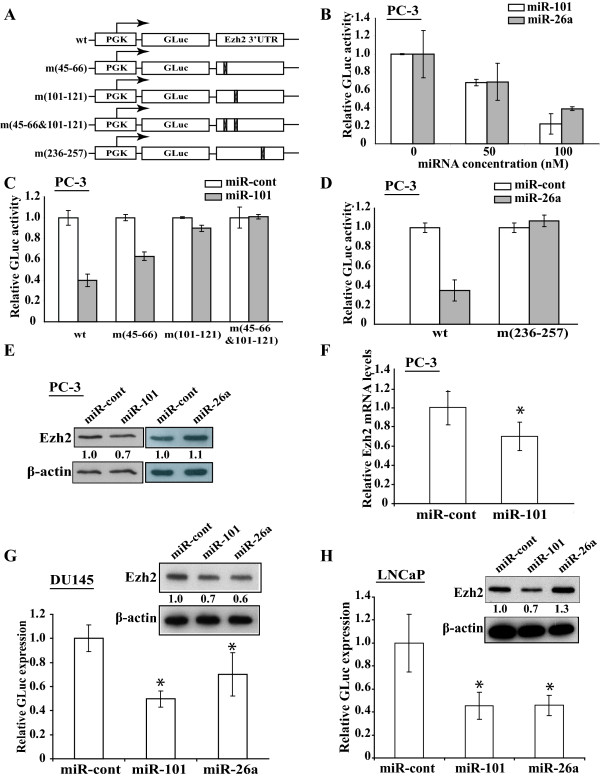
外源性表达的miR-101和miR-26a对Ezh2表达的影响 为了确定miR-101和miR-26a是否靶向Ezh2的3'-UTR,我们研究了这两种miRNAs对含有GLuc和Ezh2 3'-UTR的报告子的影响。 完整的(wt)报告子及其在miR-101或miR-26a结合位点带有替换核苷酸的突变版本如图所示。 3A级 当增加miR-101和miR-26a的数量(0,50,100 nM)转染到PC-3细胞时,具有完整Ezh2 3'-UTR的报告构建物显示GLuc表达降低(图。 第3页 ). 在我们同时突变两个miR-101靶点后,生成的报告基因结构m(45-66和101-121)完全失去了对转染miR-101的反应(图。 3C公司 ). 然而,当我们分别突变两个靶点时,我们观察到两个报告结构m(45-66)和m(101-121)的GLuc表达可以被miR-101部分抑制(图。 3C公司 ). 有趣的是,Ezh2 3'-UTR的核苷酸(nt)101-121的突变导致了比nt45-66更深刻的影响,表明miR-101与这两个位点的相互作用不同。 类似地,带有突变miR-26a靶位点m(236-257)的报告结构也失去了对报告结构的抑制(图。 三维 ). 因此,报告者分析研究表明,报告者构建物的Ezh2 3'-UTR中存在这些miRNA靶位点是miR-101和miR-26a抑制的必要条件。
图3。
报告人试验中Ezh2 3'-UTR的miR-101和miR-26a分析及内源性Ezh2表达 . 答:。 在野生型(wt)报告子中,在PGK启动子驱动的GLuc下游亚克隆了一个493 bp的片段,该片段包含Ezh2编码区的最后50 bps和Ezh2 3'-UTR的前443 bps,包含预测的miR-101和miR-26a靶位点。 四个报告结构包含miR-101靶位点Ezh2 3'-UTR的突变:m(45-66)、m(101-121)和m(45-6和101-121; miR-26a靶点:m(236-257)。 B。 增加的miR-101和miR-26a(0、50和100 nM,必要时用miR cont补偿至100 nM)与在 “A” 将SEAP表达质粒导入PC-3细胞(三倍体)。 GLuc活性由SEAP活性测定并归一化(详见材料和方法)。 C、。 将100 nM的miR-cont或miR-101与50 ng所示报告构建物和SEAP表达质粒共同转染。 如上所述测量并归一化GLuc活性。 D。 实验的执行方式为 “C” 使用标记的miR-26a和报告质粒。 E.公司。 用miR-cont、miR-101或miR-26a(120nM)转染PC-3细胞。 通过蛋白质印迹法测定Ezh2和β-肌动蛋白的表达。 用β-肌动蛋白归一化的相对Ezh2水平被指出。 F、。 实时RT-PCR分析微RNA转染细胞中Ezh2 mRNA水平(归一化为GAPDH)。 星号:p≤0.05。 G公司 和 H(H) GLuc活性测定(三倍)和Western blot C、 D类 和 E类 DU-145中( G公司 )和LNCaP( H(H) )单元格。
为了确定miR-101和miR-26a对内源性Ezh2表达的调节,我们分别转染了PC-3细胞中miR-101与miR-26a的合成模拟物,并通过Western blot研究了Ezh2的表达。 如图所示。 第三方 ,外源性表达的miR-101降低内源性Ezh2蛋白的表达,表明miR-101对Ezh2 mRNA翻译起负调控作用。 有趣的是,miR-26a对Ezh2没有任何可检测到的抑制作用(图。 第三方 ),尽管它有效地抑制了包含Ezh2 3'-UTR的报告结构的表达(图。 第3页 ). 除了蛋白质变化外,我们还检测到,与miR-cont转染的细胞相比,miR-101转染的PC-3细胞中Ezh2 mRNA显著减少(30%±15,p<0.05,图。 3英尺 ).
我们还将这些研究扩展到其他前列腺细胞系。 在DU145和LNCaP细胞中的报告者分析显示,miR-101和miR-26a,而不是miR-cont,显著抑制了带有Ezh2 3'-UTR的报告者结构的表达。 在DU145细胞中,miR-101和miR-26a都降低了Ezh2的表达(图。 第三代移动通信 ). 然而,在LNCaP细胞中,miR-101而非miR-26a下调了Ezh2的表达(图。 3小时 ).
先前的研究表明,基因3'-UTR的突变或多态性可能会消除其对miRNAs调节的反应性[ 39 , 40 ]. 因此,我们询问内源性Ezh2对异位miR-26a表达的惰性是否是由于PC-3细胞中Ezh2 3'-UTR处miR-26a靶位点的改变所致。 我们扩增了含有miR-26a靶位点的PC-3细胞基因组DNA中的区域,并通过DNA测序分析了PCR片段。 然而,与NCBI中的人类基因组DNA序列相比,我们没有发现预测的miR-26靶点有任何变化(数据未显示)。
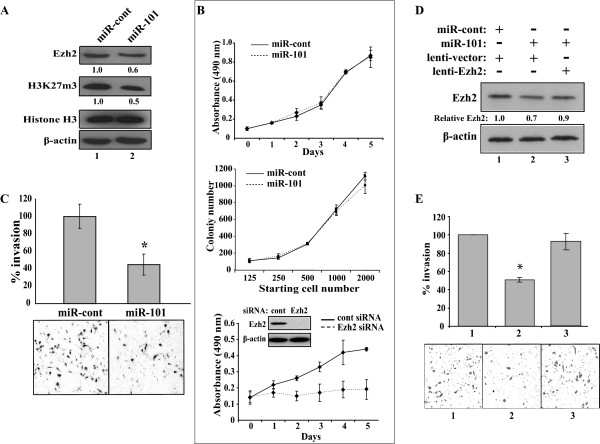
异位miR-101对前列腺癌细胞增殖、存活和侵袭性的影响 由于我们的数据表明miR-101抑制了Ezh2的表达,我们询问miR-101介导的Ezh2减少是否会影响组蛋白甲基化和PC-3细胞的生长、生存能力和侵袭性。 Ezh2通过介导组蛋白H3-K27三甲基化调节其靶基因的表达[ 41 ]. 因此,我们在miR-101转染的PC-3细胞中检测了这种修饰。 如图所示。 4A级 ,miR-101的异位表达导致Ezh2和组蛋白H3-K27甲基化的同时降低,而总组蛋白H3保持不变。 使用这些细胞来确定miR-101对细胞生长的影响,我们没有检测到细胞增殖的显著变化(图。 4B类 ,顶部面板)。 同时,克隆形成试验表明,miR-101没有改变PC-3细胞的集落形成,这表明细胞存活率没有改变(图。 4B类 ,中间面板)。 我们询问miR-101在PC-3细胞中适度减少Ezh2是否不足以引起细胞生长的任何变化。 因此,我们用携带Ezh2-siRNA的慢病毒感染PC-3细胞,该慢病毒可以将内源性Ezh2-siRNA敲低90%以上。 在细胞增殖研究中,与表达对照siRNA的细胞相比,这些Ezh2-siRNA转导的PC-3细胞在细胞增殖方面表现出明显缺陷(图。 4B类 ,底部面板)。
图4。
外源性表达miR-101对PC-3细胞生长、存活和侵袭性的影响 . 答:。 异位miR-101对组蛋白H3-K27甲基化的影响。 用miR-cont或miR-101(120 nM)转染PC-3细胞。 使用所示抗体通过Western blots分析转染细胞的等分样品。 相对蛋白质表达在每张图片的底部。 B。 Ezh2下调对PC-3细胞增殖和集落形成的影响。 在顶部和中间面板中,转染PC-3细胞的等分样品 “A” 通过WST-1增殖试验(顶部)和克隆形成试验(中部)进行研究。 在底部面板中,通过WST-1试验检测携带对照和Ezh2 siRNA的慢病毒感染的PC-3细胞,并通过Western blot检测Ezh2敲除。 C、。 异位miR-101对PC-3细胞侵袭性的影响 A类 星号表示p<0.05,并显示代表性图像。 D类 和 E类 恢复Ezh2表达对miR-101转染PC-3细胞的影响。 在 D类 如图所示,PC-3细胞感染了由pSL4载体或pSL4-Ezh2产生的慢病毒。 在感染后48小时,细胞被转染120 nM的miR-cont或标记的miR-101。 再过48小时,用所示抗体通过Western blots分析细胞。 在 E类 ,感染/转染PC-3细胞的等分样品,具有相应的样品编号(1、2和3) D类 通过侵袭实验进行研究。 侵袭百分比用“*”表示,表示p<0.05和代表性图像。
我们使用Matrigel侵袭试验进一步研究了这些细胞的侵袭能力。 如图所示。 4摄氏度 与表达miR-cont的细胞相比,表达异位miR-101的PC-3细胞的穿透能力显著降低(46%±12,p<0.05),表明异位miR-01抑制PCa细胞的侵袭性。 由于Ezh2抑制和PCa减弱进展之间的相关性已被充分记录[ 13 , 17 ],我们询问miR-101降低Ezh2是否是miR-101转染细胞侵袭性降低的主要原因。 我们用表达Ezh2的慢病毒感染miR-101转染的PC-3细胞,这可以将Ezh2表达恢复到与内源性Ezh2相当的水平(90%)(图。 4D(四维) ). 在侵袭试验中,Ezh2表达恢复的PC-3细胞与miR-cont转染的细胞表现出相似的穿透能力(92%±2.6,p<0.05,与图的第3列和第1列相比)。 第4页 )表明miR-101主要通过下调Ezh2表达来减弱PC-3细胞的侵袭性。
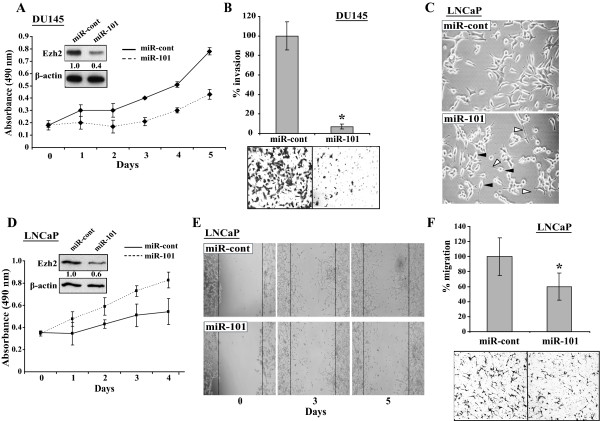
我们询问是否可以将体外表达miR-101的PC-3细胞现象扩展到其他前列腺细胞系。 因此,我们研究了异位miR-101对DU-145和LNCaP细胞的影响。 在DU-145细胞中,我们观察到miR-101抑制细胞增殖和侵袭(图。 5A级 和 5亿 ). 这一结果与Chinnaiyan小组最近的一项研究一致[ 24 ]. PC-3和DU-145都是侵袭性和雄激素受体(AR)阴性的前列腺癌细胞系。 我们进一步研究了miR-101对侵袭性相对较低且AR阳性的LNCaP细胞的影响。 我们首先观察到,与表达miR-cont的LNCaP细胞的典型纺锤形形态相比,表达异位miR-101的LNCa细胞随着细胞质部分的延伸和胞体的圆形而表现出形态学变化(图。 5摄氏度 ). 这可能不是由神经内分泌分化引起的,因为神经内分泌细胞的一些标记物没有显示出显著变化(数据未显示)。 值得注意的是,在miR-101转染的PC-3和DU-145细胞中未观察到这些形态学变化(数据未显示)。 出乎意料的是,与miR-cont转染细胞相比,表达异位miR-101的LNCaP细胞的细胞增殖增加,这与miR-101对DU-145细胞的作用相反(图。 第五天 ). 这种现象在多个独立的实验中是可以重现的。 由于LNCaP细胞的这些形态变化可能会改变其细胞骨架结构并影响细胞迁移,因此我们使用伤口愈合和Boyden Chamber细胞迁移分析来评估这些细胞的迁移。 在这两项研究中,miR-101转染的LNCaP细胞比miR-cont转染的细胞迁移率降低(图。 第五版 和 5楼 ).
图5。
miR-101对DU-145和LNCaP细胞的影响 . A和B。 异位miR-101对DU-145细胞增殖和侵袭性的影响。 用120 nM的miR-cont或miR-101模拟物转染DU-145细胞,并在转染后72 h收集细胞。 每种处理的细胞等分试样分三份进行研究( A类 )WST-1细胞增殖试验和( B )基质侵入试验。 这些转染细胞的Western blot分析显示为“ A类 “和入侵检测的代表性图像也显示在” B ”(右侧面板)。 C 、和 D类 异位miR-101对LNCaP细胞形态和增殖的影响。 在 C ,在显微镜下(20×)对转染后72 h的LNCaP细胞进行成像。 黑色箭头表示细胞体的圆形,而白色箭头表示细胞胞质部分的延伸。 在 D类 将LNCaP细胞以6000个细胞/孔的密度分三份接种在96 well平板中,并转染120 nM的miR-cont或miR-101模拟物。 用WST-1试剂检测细胞增殖。 E类 用miRNA模拟物(120nM)转染的LNCaP细胞的伤口愈合测定。 在指定的时间点拍摄图像。 F类 .转染miRNA模拟物(120 nM)的LNCaP细胞的Boyden室迁移试验。 结晶紫染色后,用下图所示图像量化细胞数量。
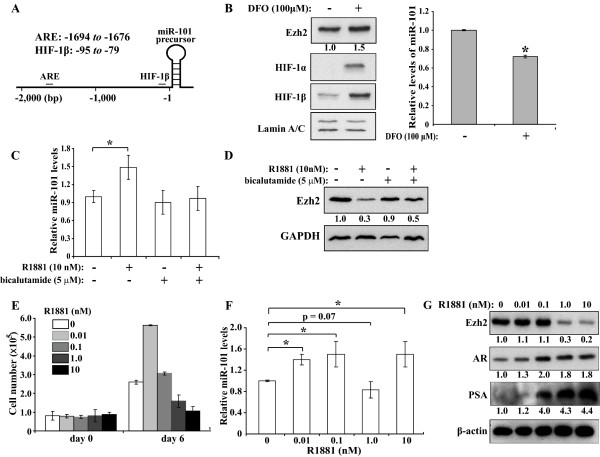
HIF-1α/HIF-1β和雄激素受体对miR-101表达的影响 与蛋白质编码的mRNAs一样,miRNAs也从基因组DNA中的基因转录而来。 因此,每个miRNA的表达都是由启动子驱动并由转录因子调节的[ 42 ]. 为了研究调节miR-101表达的机制,我们使用预测DNA上转录因子结合元件的算法分析了其编码序列在人类基因组中的上游区域[ 43 ]. 我们鉴定了许多有潜力调节miR-101表达的蛋白质,并重点研究了具有高结合概率评分和先前报道的在癌症中的作用的调节蛋白质。 其中两种蛋白质是低氧诱导因子-1β(HIF-1β)和AR,其结合元件分别位于miR-101前体的上游-95至79和-1694至-1676(图。 6A级 ).
图6。
HIF-1β和AR对miR-101表达的影响 . 答:。 miR-101编码区上游HIF-1β和AR结合元件示意图。 B。 DFO处理的PC-3细胞的蛋白质和miR-101表达。 用100μM DFO或mock处理的PC-3细胞的核蛋白通过Western blot(左面板)和Real-Time RT-PCR(右面板,两个单独实验的平均值,三倍样品)进行分析。 C 和 D类 用R1881和比卡鲁胺处理LNCaP细胞,并用( C )miR-101的实时RT-PCR(三个单独实验的平均值)和( D类 )Ezh2的Western blot。 E、 F类 和 G.公司。 R1881对LNCaP细胞生长、miR-101水平和基因表达的影响。 在 E类 ,细胞接种于1×10 5 细胞/孔在6孔板上,在苯酚无红RPMI培养基中,含1%炭化裂解FBS,然后处理0、0.01、0.1、1.0和10 nM的R1881。 在第0天和第6天,对三倍的细胞进行计数。 数据是三个或更多单独实验的平均值。 在 F类 通过实时RT-PCR测定第6天提取RNA中的miR-101水平,每个样品分析三次。 数据是四个独立实验的平均值。 学生t检验用于确定统计显著性(*表示p<0.05)。 在 G公司 ,使用左侧标记的抗体通过Western blot分析治疗第6天的全细胞裂解物。
HIF-1β与HIF-1α相互作用形成异二聚体,调节PCa血管生成和进展中低氧反应基因的转录[ 44 ]. HIF-1α的表达可被多种信号通路刺激。 因此,为了确定HIF-1β对miR-101的影响,我们用100μM甲磺酸去铁胺(DFO)处理PC-3细胞,DFO是一种诱导HIF-1α表达的铁螯合剂[ 45 ]. 如图的左侧面板所示。 6亿 在DFO处理后6 h,PC-3细胞与模拟处理细胞相比,Ezh2表达增加,HIF-1α和HIF-1β同时增加。 重要的是,与对照组相比,DFO处理的PC-3细胞中的miR-101水平显著降低至72%(p<0.05)(右图。 6亿 )表明HIF-1α/HIF-1β异二聚体下调miR-101。
为了测试AR如何调节miR-101的表达,我们用10 nM的R1881处理雄激素依赖性LNCaP细胞,观察到miR-101显著增加(50%±20,图。 6摄氏度 ). 为了确定这种现象是否与AR的功能有关,我们用5μM的比卡鲁胺(AR的拮抗剂)预处理LNCaP细胞。由于抑制了功能性AR,我们消除了R1881引起的miR-101诱导(图。 6摄氏度 ). 一致地,随着R1881对miR-101的诱导,我们观察到Ezh2同时减少,而比卡鲁胺治疗可以部分恢复(图。 第6天 ).
AR在正常前列腺的发育和前列腺癌的生长中起着重要作用[ 46 ]. R1881可诱导LNCaP细胞分化并影响其增殖[ 47 , 48 ]. 特别是不同浓度的R1881对LNCaP细胞的生长有不同的影响[ 47 ]. 因此,我们研究了在含有1%炭样血清和0、0.01、0.1、1或10nM R1881的培养基中培养的LNCaP细胞的miR-101和Ezh2表达。 在第0天和第6天对经过这些处理的细胞进行计数以评估其生长情况,同时通过实时PCR和Western blot分别测定miR-101水平和蛋白表达。 如图所示。 第六版 ,LNCaP细胞对R1881的反应表现出双相生长速率。 虽然0.01 nM的R1881刺激了LNCaP细胞的生长,但R1881的进一步增加对细胞增殖产生了不利影响。 该观察结果与之前关于R1881对LNCaP细胞作用的研究一致[ 47 ]. 同时,0.01、0.1和10nM的R1881处理显著增加了LNCaP细胞中miR-101的表达(分别增加了40%±14、50%±29和50%±26。p<0.05,n=4,图。 第6页 ). 然而,由于未知原因,1 nM的R1881并未显著改变miR-101水平(p=0.07,n=4),这在4项单独研究中是可重复的。 R1881的作用通过标记的PSA诱导来验证,以响应R1881浓度的增加,这与以前的研究一致[ 47 , 48 ]. 同时AR水平也升高(图。 6克 ). 此外,除R1881的1.0nM外,Ezh2的整体表达与AR增加和miR-101诱导呈负相关(图。 第6页 和 6克 ).
讨论 前列腺肿瘤的发生伴随着放松调控的基因表达。 已经证实,异常的DNA甲基化和组蛋白修饰有助于这些过程。 近年来,肿瘤细胞中miRNA谱的变化及其在肿瘤发生中的作用越来越受到重视。 由于miRNAs的主要生物学功能是介导基因表达,我们研究了前列腺肿瘤发生中的关键基因是如何被不同的miRNAs调节的,以及miRNA-介导的基因表达是否在前列腺癌发展中重要。 多项研究表明,Ezh2可能是前列腺癌的预后标志物和治疗靶点[ 15 , 18 , 49 ]. 因此,我们的初步研究探讨了前列腺肿瘤发生过程中Ezh2的表达是否受到miRNAs的调节。
在本报告中,我们证明了Ezh2的3'-UTR包含miR-101和miR-26a的靶位点,这些位点在不同物种之间是保守的。 然而,尽管miR-101的异位表达降低了所有三种受试细胞系中的内源性Ezh2,但miR-26a仅抑制DU-145细胞中的Ezh2而不抑制PC-3和LNCaP细胞中的E zh2。 这一观察背后的机制尚不清楚,对miRNAs动态调控的深入理解可能为这一现象提供了解释。 目前,有几种算法可用于预测给定mRNA序列中潜在的miRNA靶位点。 大多数算法都采用了一种评分系统,该系统使用动态编程比对来识别高度互补的位点,并在microRNA的5'端奖励互补性。然而,这些算法无法预测潜在的靶位点是否被二级结构或RNA结合蛋白所阻断,从而使其无法访问[ 50 ]. 最近的一份报告也表明,microRNA靶位点内的单核苷酸多态性影响miRNA-介导的基因抑制,从而影响肿瘤易感性[ 40 ]. 因此,mRNA中存在miRNA靶位点并不能保证该基因受该miRNA调控。另一方面,少数证据表明,某些miRNA调控的基因可能不包含大多数算法预测的典型靶位点[ 51 - 53 ]. 由于我们的DNA测序分析没有检测到PC-3细胞Ezh2 3'-UTR中潜在的miR-26a靶位点的任何突变,我们预测miR-26a对内源性Ezh2表达缺乏抑制可能是由于PC-3和LNCaP细胞中RNA结合蛋白的干扰。 当含有443-bp Ezh2 3'-UTR的493-bp DNA片段亚克隆到报告构建物中时,由于报告质粒的稳健表达,这些干扰miRNA结合的潜在RNA结合蛋白可能已经饱和。 这可能解释了报告结构对所有三种细胞系中异位miR-26a的反应性。 由于细胞蛋白和微环境的组成具有细胞类型特异性,内源性Ezh2表达对miR-26a的反应也可能发生改变。 因此,miR-26a可以下调DU145细胞中的Ezh2,但在PC-3和LNCaP细胞中没有下调(图。 第三代移动通信 ). 此外,miR-26a也被报道负调控成肌细胞和淋巴瘤细胞中Ezh2的表达[ 33 , 34 ].
微小RNA与将靶基因的表达微调到生理相关水平有关[ 54 , 55 ]. 因此,与先前关于miRNA调节其他基因表达的报道一致,异位表达的miR-101并没有显著抑制内源性Ezh2的表达,尽管它对荧光素酶报告基因构建体表现出更明显的抑制作用。 当然,miR-101不能是Ezh2表达的唯一调节器,它很可能在不同的生理条件下与其他miRNAs或转录因子协同调节Ezh2的表达。 然而,可以合理地预测,下调的miR-101有助于PCa细胞中Ezh2表达的增加,与正常前列腺细胞中的水平相比。
我们观察到异位miR-101抑制了Ezh2的表达,并显著降低了所有三种受试细胞系的侵袭性。 重要的是,我们的miR-101对Ezh2负调控的结果与Chinnaiyan组最近的一份报告一致,该报告显示miR-101的基因组缺失导致PCa中Ezh2上调[ 24 ]. 至少在PC-3细胞中,这种现象是由于Ezh2的表达同时减少,因为Ezh2在外周表达恢复了侵袭性(图。 第4页 ). 我们同样观察到miR-101对DU145细胞侵袭性和LNCaP细胞迁移能力的抑制作用(图。 5亿 和 5楼 ). 然而,miR-101对PC-3、DU-145和LNCaP细胞的增殖有不同的影响(图。 4B类 , 5A级 和 第五天 ). 虽然异位miR-101导致DU-145细胞的生长缺陷,但对PC-3细胞的生长没有影响,但它令人惊讶地促进了LNCaP细胞的增殖,同时出现了PC-3和DU-145中未观察到的形态学变化。 这些结果表明异位miR-101在不同前列腺细胞系中具有不同的作用。 这些表型差异背后的机制需要进一步研究。 值得注意的是,PC-3细胞比DU-145和LNCaP细胞更具攻击性,PC-3和DU145均为雄激素非依赖性和AR阴性。 LNCaP细胞是雄激素依赖性细胞,在这三种细胞系中恶性程度最低。 因此,miR-101导入对细胞增殖的影响可能依赖于细胞的攻击性和AR状态。
异位miR-101的LNCaP细胞出现形态学改变。 在延时视频显微镜研究中,我们观察到这些细胞形成细胞质延伸,使人想起丝状伪足,这在表达miR-cont的细胞中没有显示(数据未显示)。 当我们进一步研究这种形态变化是否影响细胞迁移时,我们检测到与miR-cont细胞相比,miR-101转染LNCaP细胞的迁移率降低(图。 5E-F型 ). 目前尚不清楚Ezh2是否对这些变更进行了监管。 我们预测其他参与细胞迁移的miR-101调节基因可能在LNCaP细胞的这种形态变化中起作用。
我们没有检测到PWR-1E、LNCaP、DU-145和PC-3细胞系之间Ezh2 mRNA水平的任何显著差异,这与之前的研究一致[ 13 ]. 这些结果表明,至少在这些细胞系中,Ezh2在PCa中的过度表达可能在转录后水平上受到调节,但在转录时没有。
HIF-1β和AR对miR-101的影响表明,miRNA的表达对生理和环境变化有反应。 DFO诱导的HIF-1α和HIF-1β表达导致miR-101表达降低,表明miR-101是低氧调节信号通路中的一个成分。 我们还观察到经10 nM R1881处理的LNCaP细胞中miR-101的上调,该R1881被AR拮抗剂比卡鲁胺减弱。 值得注意的是,仅比卡鲁胺并未显著降低miR-101水平(图。 6摄氏度 )这表明,在没有雄激素刺激的情况下,AR对miR-101的表达没有任何可检测的影响。 然而,在我们的进一步研究中,尽管R1881在0.01和0.1 nM下表现出与在10 nM下相似的效果,但在多次实验中,R1881的1 nM对miR-101的表达没有任何刺激作用(图。 第6页 ). 同时,在0.01 nM的R1881中,随着miR-101表达的增加,细胞增殖出乎意料地增强(图。 第六版 和 第6页 ). 解释这些意外变化的机制尚不清楚。 我们预测雄激素刺激信号通路的差异激活可能与之有关。 特别是在1 nM的R1881中,需要鉴定的某些蛋白质或途径可能已经改变,这导致AR对miR-101的调节被绕过,从而导致观察结果与其他R1881水平的观察结果不一致。 此前的多项研究也证实雄激素对前列腺细胞增殖的差异作用[ 47 , 48 ].
我们还注意到,在R1881的特定浓度(0.1和1.0 nM)下,miR-101和Ezh2的表达水平(图。 第6页 和 6克 )没有显示出我们在图中观察到的相关性。 6摄氏度 我们预测,在这些条件下,其他R1881/雄激素受体调节途径可能在介导Ezh2表达中发挥作用。
总的来说,HIF-1α/HIF-1β和雄激素受体的调节表明miR-101在肿瘤进展和正常前列腺发育中的作用。 需要进一步研究,以阐明前列腺癌缺氧和前列腺细胞分化过程中miR-101表达改变的机制。
结论 目前对前列腺癌的治疗经常导致癌症复发,且具有更具侵袭性和难治性的特点。 因此,确定新的治疗靶点并开发更有效的治疗方法至关重要。 Ezh2调节组蛋白甲基化并导致PCa的表观遗传学异常。 重要的是,Ezh2的过度表达与该癌的病理程度和肿瘤进展相关,表明其作为治疗靶点的潜力。 MiR-101负调控Ezh2的表达,同时减弱前列腺癌细胞的侵袭能力,这可以通过体外表达的Ezh2来挽救。 这意味着miR-101对Ezh2的抑制是一种可作为PCa治疗新策略的前瞻性方法。 此外,miR-101的水平随着雄激素治疗和HIF-1α/HIF-1β诱导而波动,表明其在不同的生理条件下受到不同的调节。 总之,我们的研究表明miR-101在前列腺肿瘤发生中起调节作用,恢复miR-101水平可能是治疗前列腺癌的有效方法。
作者的贡献 PC和GS启动了该项目并设计了研究。 PC执行了实验。 MW和WH协助Matrigel侵入试验和其他一些实验。 ZD、SDC、JX和ML参与了本研究的设计。 所有作者都在讨论、阅读和校对最终手稿中提供了帮助。
参与者信息 Paul Cao,电子邮件: pcao@wfubmc.edu。
邓志勇,电子邮件: zdeng@wfubmc.edu。
Wan Meimei,电子邮箱: mwan@wfubmc.edu。
黄伟伟,电子邮件: whuang@wfubmc.edu。
Scott D Cramer,电子邮件: scramer@wfubmc.edu。
Xu Jianfeng,电子邮件: jxu@wfubmc.edu。
Ming Lei,电子邮件: leiming70@hotmail.com。
隋光超,电子邮件: gsui@wfubmc.edu。
致谢 我们感谢马克·米勒博士、史蒂文·克里德尔博士和道格·莱尔斯博士对手稿的批判性阅读和讨论。 井上和树博士、达伦·西尔斯博士、乔治·库利克博士和礼来·郑博士慷慨地提供了一些建议和试剂。 我们得到了Nilamadhab Mishra博士实时PCR分析和Amy Tolin女士入侵检测的帮助。 我们感谢WFUHS综合癌症中心的细胞和病毒载体核心实验室提供细胞培养材料。 这项工作得到了NCI对PC的培训拨款5T32CA079448-09、美国癌症学会的研究学者拨款(RSG-09-082-01-MGO)和威克森林大学医学院对GS的启动基金的支持。
工具书类
Schuettengruber B、Chourrout D、Vervoort M、Leblanc B、Cavalli G。多梳和三疣蛋白对基因组的调控。 单元格。 2007; 128:735–745。 doi:10.1016/j.cell.2007.02.009。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Cao R,Wang L,Wang H,Xia L,Erdjument-Bromage H,Tempst P,Jones RS,Zhang Y.组蛋白H3赖氨酸27甲基化在多梳组沉默中的作用。 科学。 2002; 298:1039–1043. doi:10.1126/science.1076997。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Smith ER、Lee MG、Winter B、Droz NM、Eissenberg JC、Shiekhattar R、Shilatifard A.果蝇UTX是一种组蛋白H3 Lys27脱甲基酶,与RNA聚合酶II的伸长形式共定位。 分子细胞生物学。 2008; 28:1041–1046. doi:10.1128/MCB.01504-07。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Tan J,Yang X,Zhuang L,Jiang X,Chen W,Lee PL,Karuturi RK,Tan PB,Liu ET,Yu Q.多聚抑制复合物2介导的基因抑制的药理学破坏选择性诱导癌细胞凋亡。 基因开发2007; 21:1050–1063. doi:10.1101/gad.1524107。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Wilkinson FH、Park K、Atchison ML。YY1 REPO结构域在体内对DNA的多梳招募。 美国国家科学院院刊2006; 103:19296–19301. doi:10.1073/pnas.0603564103。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Bracken AP、Pasini D、Capra M、Prosperini E、Colli E、Helin K。EZH2是pRB-E2F通路的下游,对肿瘤的增殖和扩增至关重要。 EMBO J.2003; 22:5323–5335. doi:10.1093/emboj/cdg542。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Plath K,Fang J,Mlynarczyk-Evans SK,Cao R,Worringer KA,Wang H,de la Cruz CC,Otte AP,Panning B,Zhang Y.组蛋白H3赖氨酸27甲基化在X失活中的作用。 科学。 2003; 300:131–135. doi:10.1126/science.1084274。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Gil J,Bernard D,Peters G.多梳组蛋白在干细胞自我更新和癌症中的作用。 DNA细胞生物学。 2005; 24:117–125. doi:10.1089/dna.2005.24.117。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Kamminga LM、Bystrykh LV、de Boer A、Houwer S、Douma J、Weersing E、Dontje B、de Haan G。Polycomb组基因Ezh2可防止造血干细胞衰竭。 鲜血。 2006; 107:2170–2179. doi:10.1182/血液-2005-09-3585。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Caretti G、Di Padova M、Micales B、Lyons GE、Sartoreli V。Polycomb Ezh2甲基转移酶调节肌肉基因表达和骨骼肌分化。 基因开发2004; 18:2627–2638. doi:10.1101/gad.1241904。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Su IH、Dobenecker MW、Dickinson E、Oser M、Basavaraj A、Marqueron R、Viale A、Reinberg D、Wulfing C、Tarakhovsky A。多梳群蛋白ezh2控制肌动蛋白聚合和细胞信号传导。 单元格。 2005; 121:425–436. doi:10.1016/j.cell.2005.02.029。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Etchegaray JP、Yang X、DeBruyne JP、Peters AH、Weaver DR、Jenuwein T、Reppert SM。哺乳动物生物钟功能需要多梳组蛋白EZH2。 生物化学杂志。 2006; 281:21209–21215. doi:10.1074/jbc。 M603722200。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Varambally S、Dhanasekaran SM、Zhou M、Barrette TR、Kumar Sinha C、Sanda MG、Ghosh D、Pienta KJ、Sewalt RG、Otte AP。 多梳组蛋白EZH2参与前列腺癌的进展。 自然。 2002; 419:624–629. doi:10.1038/nature01075。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Rhodes DR、Sanda MG、Otte AP、Chinnaiyan AM、Rubin MA。确定前列腺特异性抗原定义前列腺癌复发风险的多重生物标记物方法。 2003年国家癌症研究所杂志; 第95:661–668页。 doi:10.1093/jnci/95.9.661。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Yu J,Yu J、Rhodes DR、Tomlins SA、Cao X、Chen G、Mehra R、Wang X、Ghosh D、Shah RB。 转移性前列腺癌的多梳抑制特征可预测癌症预后。 癌症研究2007; 67:10657–10663. doi:10.1158/0008-5472.CAN-07-2498。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Takeshita F、Minakuchi Y、Nagahara S、Honma K、Sasaki H、Hirai K、Teratani T、Namatame N、Yamamoto Y、Hanai K。通过体内使用非胶原蛋白,将小干扰RNA高效传递至骨转移瘤。 美国国家科学院院刊2005; 102:12177–12182. doi:10.1073/pnas.0501753102。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Bryant RJ、Cross NA、Eaton CL、Hamdy FC、Cunliffe VT。EZH2促进前列腺癌细胞的增殖和侵袭性。 前列腺。 2007; 67:547–556. doi:10.1002/pros.20550。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Sellers WR,Loda M.EZH2多梳转录阻遏物——转移性前列腺癌的标记物或移动者? 癌细胞。 2002; 2:349–350. doi:10.1016/S1535-6108(02)00187-3。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Tang X,Milyavsky M,Shats I,Erez N,Goldfinger N,Rotter V。激活的p53抑制组蛋白甲基转移酶EZH2基因。 致癌物。 2004; 23:5759–5769. doi:10.1038/sj.onc.1207706。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Cha TL,Zhou BP,Xia W,Wu Y,Yang CC,Chen CT,Ping B,Otte AP,Hung MC。Akt介导的EZH2磷酸化抑制组蛋白H3中赖氨酸27的甲基化。 科学。 2005; 310:306–310. doi:10.1126/science.1118947。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Lai EC。微RNA是对调节转录后负调控的3'UTR序列基序的补充。 自然遗传学。 2002; 30:363–364. doi:10.1038/ng865。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Fabbri M、Croce CM、Calin GA、MicroRNAs。 癌症杂志2008; 14:1–6. doi:10.1097/PPO.0b013e318164145e。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Barbarotto E,Schmittgen TD,Calin GA。微RNA与癌症:简介,简介,简介。 国际癌症杂志。 2008; 122:969–977页。 doi:10.1002/ijc.23343。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Varambally S、Cao Q、Mani RS、Shankar S、Wang X、Ateeq B、Laxman B、Cao X、Jing X、Ramnarayanan K。microRNA-101的基因组缺失导致组蛋白甲基转移酶EZH2在癌症中过度表达。 科学。 2008; 322:1695–1699. doi:10.1126/science.1165395。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Deng Z,Wan M,Sui G.PIASy-介导的阴阳1的sumoylation依赖于它们的相互作用,而不是无名指。 分子细胞生物学。 2007; 27:3780–3792. doi:10.1128/MCB.01761-06。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Rubinson DA、Dillon CP、Kwiatkowski AV、Sievers C、Yang L、Kopinja J、Rooney DL、Ihrig MM、McManus MT、Gertler FB。 一种基于慢病毒的系统,通过RNA干扰使初级哺乳动物细胞、干细胞和转基因小鼠中的基因沉默。 自然遗传学。 2003; 33:401–406. doi:10.1038/ng1117。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
邓Z,万M,曹P,饶A,克拉默SD,隋G.阴阳1调节雄激素受体的转录活性。 致癌物。 2009; 28:3746–3757. doi:10.1038/onc.2009.231。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Livak KJ,Schmittgen TD.使用实时定量PCR和2(-Delta Delta C(T))方法分析相关基因表达数据。 方法。 2001; 25:402–408. doi:10.1006/meth.2001.1262。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Griffiths-Jones S、Saini HK、van Dongen S、Enright AJ。 miRBase:微RNA基因组学工具。 核酸研究2008; 36:D154–158。 doi:10.1093/nar/gkm952。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
John B、Enright AJ、Aravin A、Tuschl T、Sander C、Marks DS。人类微RNA靶点。 《公共科学图书馆·生物》。 2004; 2:e363。 doi:10.1371/journal.pbio.0020363。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Lewis BP、Burge CB、Bartel DP。 保守的种子配对,通常两侧有腺苷,表明数千人类基因是microRNA的靶标。 单元格。 2005; 120:15–20. doi:10.1016/j.cell.2004.12.035。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Krek A、Grun D、Poy MN、Wolf R、Rosenberg L、Epstein EJ、MacMenamin P、da Piedade I、Gunsalus KC、Stoffel M、Rajewsky N.组合微RNA靶预测。 自然遗传学。 2005; 37:495–500. doi:10.1038/ng1536。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Wong CF,Tellam RL.MicroRNA-26a在肌发生过程中靶向Zeste同源物2的组蛋白甲基转移酶增强子。 生物化学杂志。 2008; 283:9836–9843. doi:10.1074/jbc。 M709614200。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Sander S、Bullinger L、Klapproth K、Fiedler K、Kestler HA、Barth TF、Moller P、Stilgenbauer S、Pollack JR、Wirth T。MYC通过抑制其负调控因子miR-26a刺激EZH2表达。 鲜血。 2008; 112:4202–4212. doi:10.1182/bloud-2008-03-147645。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Lu J,Getz G,Miska EA,Alvarez-Saavedra E,Lamb J,Peck D,Sweet-Condero A,Ebert BL,Mak RH,Ferrando AA。微RNA表达谱对人类癌症进行分类。 自然。 2005; 第435:834–838页。 doi:10.1038/nature03702。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Volinia S、Calin GA、Liu CG、Ambs S、Cimmino A、Petrocca F、Visone R、Iorio M、Roldo C、Ferracin M。人类实体肿瘤的microRNA表达特征定义了癌症基因靶点。 美国国家科学院院刊2006; 103:2257–2261. doi:10.1073/pnas.0510565103。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Webber MM、Bello D、Kleinman HK、Wartinger DD、Williams DE、Rhim JS。 前列腺特异性抗原和雄激素受体对永生化成人前列腺上皮细胞系的诱导和鉴定。 致癌。 1996; 17:1641–1646. doi:10.1093/carcin/17.8.1641。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Engl T、Relja B、Blumenberg C、Muller I、Ringel EM、Beecken WD、Jonas D、Blaheta RA。 前列腺肿瘤CXC-趋化因子谱与细胞粘附内皮和细胞外基质相关。生命科学。 2006; 78:1784–1793. doi:10.1016/j.lfs.2005.08.019。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Mishra PJ、Humeniuk R、Mishra PJ、Longo-Sorbello GS、Banerjee D、Bertino JR。二氢叶酸还原酶基因中miR-24 microRNA结合位点多态性导致甲氨蝶呤耐药。 美国国家科学院院刊2007; 104:13513–13518. doi:10.1073/pnas.070627104。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Nicoloso MS、Sun H、Spizzo R、Kim H、Wickramasinghe P、Shimizu M、Wojcik SE、Ferdin J、Kunej T、Xiao L.microRNA靶位点内的单核苷酸多态性影响肿瘤易感性。 《癌症研究》,第2789-2798页。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ]
Cao R,Zhang Y.组蛋白H3中E(Z)/EZH2介导的赖氨酸27甲基化的功能。 2004年通用操作基因开发; 14:155–164. doi:10.1016/j.gde.2004.02.001。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Rodriguez A、Griffiths-Jones S、Ashurst JL、Bradley A.哺乳动物微RNA宿主基因和转录单位的鉴定。 基因组研究2004; 14:1902–1910. doi:10.1101/gr.2722704。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Heinemeyer T、Wingender E、Reuter I、Hermjakob H、Kel AE、Kel OV、Ignatieva EV、Ananko EA、Podkolodnaya OA、Kolpakov FA。转录调控数据库:TRANSFAC、TRRD和COMPEL。 1998年《核酸研究》; 26:362–367. doi:10.1093/nar/261.362。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Kimbro KS,Simons JW。 人类乳腺癌和前列腺癌中的低氧诱导因子-1。 内分泌相关癌。 2006; 13:739–749. doi:10.1677/erc.1.00728。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Martinez-Romero R、Martinez-Lara E、Aguilar-Quesada R、Peralta A、Oliver FJ、Siles E.PARP-1通过调节一氧化氮和氧化应激调节去铁胺诱导的HIF-1α积累。 细胞生物化学杂志。 2008; 104:2248–2260. doi:10.1002/jcb.21781。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Heinlein CA,Chang C.前列腺癌雄激素受体。 Endocr Rev.2004; 25:276–308. doi:10.1210/er.2002-0032。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Ripple MO,Henry WF,Rago RP,Wilding G.雄激素治疗人类前列腺癌细胞引起的促氧化剂-抗氧化剂转换。 美国国家癌症研究所杂志,1997; 89:40–48. doi:10.1093/jnci/89.1.40。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
邵C、王毅、岳HH、张玉田、石池、刘菲、鲍天勇、杨志勇、袁JL、邵国喜。 雄激素对前列腺癌细胞的双相作用及其与雄激素受体辅激活物多巴脱羧酶的相关性。 安德洛尔J。 2007; 28:804–812。 doi:10.2164/jandrol.106.002154。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Tonini T、D'Andrilli G、Fucito A、Gaspa L、Bagella L。Ezh2多梳蛋白在肿瘤发生过程中干扰生长抑制关键元素途径的重要性。 细胞生理学杂志。 2008; 214:295–300. doi:10.1002/jcp.21241。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Kedde M、Strasser MJ、Boldajipour B、Vrielink JA、Slanchev K、le Sage C、Nagel R、Voorhoeve PM、van Duijse J、Orom UA。RNA结合蛋白Dnd1抑制微RNA对靶mRNA的访问。细胞。 2007; 131:1273–1286. doi:10.1016/j.cell.2007.11.034。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Kruger J,Rehmsmeier M.RNA杂交:微RNA靶点预测简单、快速、灵活。 2006年《核酸研究》; 34:W451–454。 doi:10.1093/nar/gkl243。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
To KK,Zhan Z,Litman T,Bates SE。通过推测的小RNA调节转录稳定性和蛋白质翻译,调节S1结肠癌细胞株中其mRNA 3'非翻译区ABCG2的表达。 分子细胞生物学。 2008; 28:5147–5161. doi:10.1128/MCB.00331-08。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Sandberg R、Neilson JR、Sarma A、Sharp PA、Burge CB。 增殖细胞表达的mRNA具有缩短的3'非翻译区和较少的microRNA靶位点。 科学。 2008; 320:1643–1647. doi:10.1126/science.1155390。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
霍伯特·O·miRNAs演奏一首曲子。 单元格。 2007; 131:22–24. doi:10.1016/j.cell.2007.09.031。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Karres JS、Hilgers V、Carrera I、Treisman J、Cohen SM。保守的microRNA miR-8调节阿托品水平以防止果蝇的神经退化。 单元格。 2007; 131:136–145. doi:10.1016/j.cell.2007.09.020。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]