摘要 背景 蛋白激酶C(PKC)亚型是乳腺癌治疗的潜在靶点。 本研究旨在评估哪些PKC亚型可能是不同乳腺癌亚型的最佳靶点。
结果 在两组原发性乳腺癌患者中,PKCα水平与雌激素和孕激素受体阴性、肿瘤分级和增殖活性相关,而PKCδ和PKCε与临床病理参数无关。 独立于其他因素,PKCα阳性肿瘤患者的生存率低于PKCα阴性肿瘤患者。 细胞系研究表明,PKCα水平在MDA-MB-231中较高,而在增殖较慢的T47D细胞中不存在。 此外,PKCα沉默降低了MDA-MB-231细胞的增殖。 PKCα抑制或下调也会减少细胞迁移 在体外 .
结论 PKCα是乳腺癌预后不良的标志物,与乳腺癌进展相关的细胞功能相关并对其重要。
背景 乳腺癌是一种异质性疾病,包括几个具有不同形态、遗传变化和治疗反应的亚组[ 1 , 2 ]. 因此,重要的是要对每个亚组的相关治疗目标有更多的了解,以优化针对个别患者的定制治疗方案。 许多细胞内信号蛋白被认为是阻断乳腺癌细胞恶性肿瘤的潜在靶点。 蛋白激酶C(PKC)亚型就是这种潜在治疗靶点的例子。
PKC是一个丝氨酸/苏氨酸激酶家族,参与增殖、分化、凋亡和迁移等多种过程。 PKC亚型根据调控域的结构分为三个亚组:经典亚型(PKCα、βI、βII和γ)、新型亚型(PKCδ、ε和θ)和非典型亚型(CKCζ和/λ)。 经典和新型PKC包含一个二酰甘油(DAG)结合C1结构域,因此通过激活导致DAG生成的途径进行调节。 非典型PKC对DAG不敏感,并以不同的方式进行调节[ 三 ].
一些研究表明,DAG敏感的经典和新型PKC亚型促进乳腺癌细胞的恶性特征。 PKCα与雌激素受体(ER)阴性偶联[ 4 ]和培养细胞的雌激素依赖性生长[ 5 , 6 ]与PKCα阳性肿瘤患者相比,PKCα阴性肿瘤患者对内分泌治疗的反应更好[ 7 , 8 ]. 此外,PKCα表达增加导致更具攻击性的表型[ 4 ]与MCF-7细胞对细胞抑制药物的耐药性有关[ 9 , 10 ]. PKCα也被评估为乳腺癌的治疗靶点[ 11 ]. 然而,与正常乳腺组织相比,乳腺癌中PKCα水平降低[ 12 , 13 ]. 因此,有证据表明PKCα在乳腺癌中具有促进和抑制作用。
PKCδ在乳腺癌中的作用尚不明确。 与PKCδ阴性肿瘤患者相比,PKCδ阳性肿瘤患者的内分泌反应更好[ 8 ]PKCδ已被证明对紫外线诱导培养的乳腺癌细胞凋亡至关重要[ 14 ]. 然而,一些研究指出PKCδ在乳腺癌中的促肿瘤作用。 PKCδ可诱导培养乳腺癌细胞对三苯氧胺和辐射的耐药性[ 15 , 16 ]并且已经证明可以促进两种转移[ 17 - 19 ]和扩散[ 20 ]小鼠乳腺癌和上皮细胞。 我们最近发现PKCδ的缺失足以促使乳腺癌细胞凋亡[ 21 ].
PKCε在乳腺癌中经常被认为具有致癌作用。 PKCε的表达水平与乳腺癌患者的肿瘤分级、HER2表达、ER阴性和生存率差有关。 此外,在MDA-MB-231乳腺癌细胞中,PKCε的下调降低了小鼠的肿瘤生长和转移能力[ 22 ]. 也有证据表明PKCε保护细胞免受凋亡损伤[ 23 - 25 ].
综上所述 在体外 和 体内 数据强调PKCα、PKCδ和PKCε是乳腺癌治疗靶点的未来候选物,也是疾病预后的标志物。 然而,到目前为止,对于不同亚型作为乳腺癌诊断和预后标记物的潜力,人们的认识还很有限。 本研究通过分析这些PKC亚型在原发性乳腺癌组织中的表达水平,阐明了这一问题,我们的结果表明PKCα是乳腺癌侵袭性的潜在标志物。
方法 细胞培养 所有细胞系均取自ATCC。 将MCF-7、MDA-MB-231和MDA-MB-468乳腺癌细胞保存在添加了10%胎牛血清(FBS;Invitrogen)、1mM丙酮酸钠(PAA laboratories Gmbh)、100 IU/ml青霉素和100μg/ml链霉素(均为Gibco)的RPMI 1640培养基(Sigma)中。 T47D细胞在补充有10%FBS、10 mM HEPES(PAA laboratories Gmbh)、100 IU/ml青霉素和100μg/ml链霉素的DMEM中生长。 MCF-7和T47D细胞培养基中额外添加了0.01 mg/ml胰岛素(诺和诺德A/S)。
转染 对于siRNA转染,细胞接种在35-50%的汇合处,并在不含抗生素的完整培养基中生长24小时。 使用4μl/ml Lipofectamine 2000(Invitrogen)和40 nM siRNA(Invit罗gen,表 1 )根据供应商协议,在Optimem(Gibco)中。
表1。
小干扰RNA 寡核苷酸
控制 GACAGUGUGACGUCGAUUGCAUG(加古古古古加古古堡)
PKCα#1 CCGAGUGAAACUCACGGACUUCAAU公司
PKCα#2 CCAUCGAUUGUUCUUUUCUUCAUAA公司
PKCδ CCAAGUGUGUAUGUCUGUUCAGUA公司
PKCε CACAAGUUCGGGUAUCCACAACUACA公司
根据供应商的协议,用含有2μl/mL Lipofectamine 2000和2μg/mL DNA的Optimem替换正常培养基,进行质粒转染5小时。 编码与增强型绿色荧光蛋白(EGFP)融合的PKC结构的质粒已在前面描述过[ 26 ].
肿瘤材料 第一组最初由114名在乌梅大学医院被诊断为乳腺癌的患者的肿瘤组成,并按照地区指南进行治疗。 表中描述了队列 2 。由于组织芯片中缺乏肿瘤材料,根据所研究的参数,可以分析42-60个肿瘤。 Ki-67分为<20%和>20%阳性细胞两组。
表2。
队列 我 二
患者人数 114 512
诊断年龄,中位数(范围) 60(30-80) 65 (27-96)
肿瘤大小(mm),中位数(范围) 22 (8-100) 16 (1-100)
节点状态
积极的 53 168
否定 48 298
缺少 13 58
ER状态
积极的 82 417
否定 31 72
缺少 1 35
第二组包括1988年至1992年间在马尔默大学医院病理科确诊的512例连续乳腺癌病例。 表中描述了队列 2 。由于组织芯片中缺乏肿瘤材料,根据所研究的参数,可以分析223-263个肿瘤。 Ki-67分为三组,0-10%、11-25%和26-100%阳性细胞。
这些队列代表了所有组织学亚型的混合,其比例与常见发病率相对应。 组织微阵列的构建和队列的临床病理特性已在其他地方详细描述[ 27 - 32 ]. 获得了Lund和UmeáEthical董事会的道德许可。 由于缺乏材料而无法评估PKC表达的肿瘤数量在表中显示为未评估。
细胞颗粒阵列 细胞在磷酸盐缓冲盐水(PBS)中洗涤,并在PBS中的4%多聚甲醛中固定25分钟,最后5分钟内存在Mayer苏木精(5μl/ml)。 将细胞制成颗粒,去除多聚甲醛,然后在70%乙醇中培养过夜,然后使用浓度增加的乙醇进行脱水,最后使用二甲苯。 脱水后,将细胞颗粒包埋在石蜡中并排列成细胞线阵列。
免疫组织化学 将石蜡块切片(4μm)干燥、脱蜡、再水化并在1×高pH(DAKO)目标回收溶液中进行微波处理。 所有切片均在DAKO Techmate™机器中染色,并使用DAB进行可视化。 使用的抗体为PKCα(1:2000)、PKCδ(1:1000)、PKCε(1:400;所有圣克鲁斯生物技术公司,产品编号sc-208、sc-937和sc-214)和Ki-67(1:200;DAKO)。 用相同的染色溶液同时对一组患者的所有组织微阵列切片进行染色,确保每个肿瘤的条件相同。 PKC染色根据细胞质染色强度进行评分,0表示缺乏染色,1表示低染色,2表示中等染色,3表示强染色。 两名研究人员对所有队列进行了独立检查,并对不一致的结果进行了重新评估。 对于乳腺癌细胞系的Ki-67分析,Ki-67染色强度被评分为阴性-低染色或中等-强染色。
样品制备和Western blot 细胞在冰镇PBS中清洗两次,并用RIPA缓冲液(10 mM Tris-HCl pH 7.2,160 mM NaCl,1%Triton-X100,1%脱氧胆酸钠,0.1%十二烷基硫酸钠,1 mM EDTA,1 mM-EGTA)在冰上溶解30分钟,并添加40μl/ml完整蛋白酶抑制剂(罗氏应用科学)。 在14000× 克 在4°C下保持10分钟。
用SDS-PAGE分离蛋白质并转移到聚偏二氟乙烯膜(Millipore)。 用含有0.05%吐温和5%非脂肪乳的PBS封闭膜,并用PKCδ(1:500)、PKCε(1:500,PKCα(1:3000)和肌动蛋白(1:2000;MP Biomedicals,克隆C4)抗体进行检测。 用辣根过氧化物酶标记的二级抗体(Amersham Biosciences),以SuperSignal系统(Pierce Chemical)为底物,观察蛋白质。 化学发光用CCD摄像机(富士胶片)检测。
细胞生长分析(WST-1分析) 细胞以每孔2000个细胞的密度接种在96周的培养板中,并培养24小时。 为了进行细胞系比较,在播种后24小时和48小时测量活细胞数。 对于PKC的抑制或激活实验,2μM Gö6976(钙生物化学)或同等体积的二甲基亚砜,或16 nM 12- 哦 -播种24小时后,在完全培养基(CM)或无血清培养基(SFM)中添加十四烷基佛波-13-醋酸盐(TPA;Sigma),并在估计活细胞数之前培养细胞72小时。 活细胞数量通过WST-1细胞活性测定进行评估(罗氏应用科学公司)。 在Antos 2020(Antos Labtech Instruments)的ELISA平板读取器中测量吸光度。
免疫荧光和共焦显微镜 PKCα的免疫荧光按所述进行[ 33 ]使用Alexa Fluor 488-共轭二级抗体。 细胞使用蔡司LSM 710共焦系统进行检查,使用Alexa Fluor 488的标准设置。
细胞周期分析 MDA-MB-231细胞以每35 mm细胞培养皿10万个细胞的密度接种,并用siRNA转染。转染后,细胞在SFM或CM中培养24小时。 将细胞胰蛋白酶化,并在-20°C的70%乙醇中固定20分钟,在PBS中洗涤,并用含有3.5μM Tris-HCl(pH 7.6)、10 mM NaCl、50μg/ml碘化丙啶(PI)、20μg/ml RNase和0.1%igepal CA-630的溶液在冰上培养20分钟,以标记DNA。 在FL-2通道上为PI信号采集了10000个事件。 使用CellQuest软件(Becton Dickinson)进行样品采集和分析。
伤口愈合分析 以每35 mm细胞培养皿150000个细胞的密度接种MDA-MB-231或MCF-7细胞,并用siRNA转染。转染后,用200μl移液管尖端在细胞培养皿的汇合区域划痕。 在指定的时间点拍摄每个划痕的选定区域的照片。 对于PKC抑制剂的实验,MDA-MB-231细胞以350000细胞/35 mm细胞培养皿的密度接种,并培养24小时,然后划痕并添加PKC抑制剂。 在刮擦后0小时和16小时拍摄每个刮擦的选定区域的照片。 使用ImageJ软件测量剩余的伤口面积。
统计 对于TMA分析,使用皮尔逊双尾显著性检验计算变量之间的相关性。 使用χ 2 -测试。 根据PKC的表达,采用Kaplan-Meier分析和对数秩检验来说明无复发生存期(RFS)和乳腺癌特异性生存期(BCSS)之间的差异。 在单变量和多变量分析中,采用Cox回归比例风险模型估计PKCα表达对乳腺癌特异性生存率的影响,并根据诺丁汉组织学分级(NHG)、年龄、淋巴结状态和队列II的肿瘤大小进行调整。 对于 在体外 实验中,通过方差分析(ANOVA)和Duncan的多范围检验评估差异的显著性。 如果 第页 -值<0.05。 所有统计计算均使用SPSS V.11.0进行。
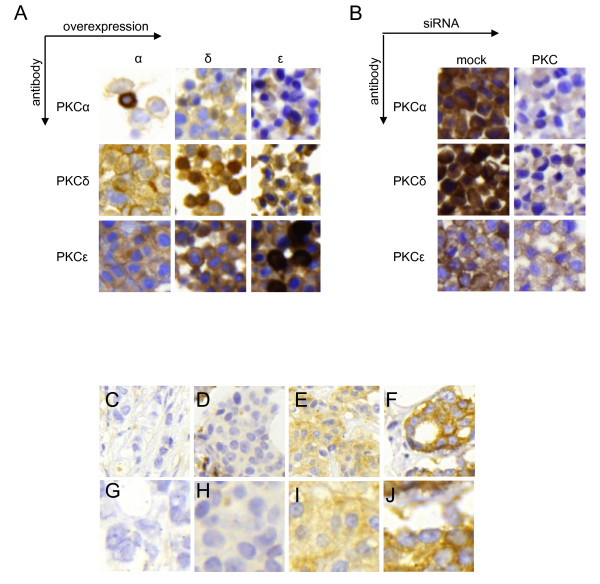
结果 PKC在乳腺癌肿瘤中的表达 对两组原发性乳腺癌患者(详见实验程序)进行PKC亚型表达分析。 对几批抗体进行测试,以确定与其他亚型无交叉反应的抗体。 交叉反应是PKC亚型分析中的一个臭名昭著的问题。 对于PKCα、PKCδ和PKCε,我们可以获得与其他亚型没有交叉反应的抗体(图 第1页 和 1B年 ). 如图所示 第1页 在同源亚型过度表达的一些细胞中,只有强烈的免疫反应。 在图中 1B年 可以看出,siRNA的下调消除或显著减少了抗体对同源亚型的染色。
图1。
原发性乳腺癌的免疫组织化学染色及抗体特异性的验证 用编码PKCα(α)、PKCδ(δ)或PKCε。 将转染细胞的颗粒排列在细胞系阵列中,并使用针对指示PKC亚型的抗体进行免疫组织化学。 (C-J)队列II乳腺癌标本中PKCα的免疫组化染色示例,在20倍放大(C-F)和40倍放大(G-J)下显示阴性(C和G)、低(D和H)、中度(E和I)和强(F和J)染色。
当存在于肿瘤中时,所研究的所有PKC亚型通常都是细胞质的,并在所有肿瘤细胞中表达。 因此,分析中只考虑了细胞质染色强度。 图 1C-J型 显示了不同PKCα染色强度的肿瘤示例,从阴性到强染色。
最初对较小队列(队列I)的TMA进行评估(表 三 和 4 ). PKCα染色强度与ER缺乏(p<0.001)、孕酮受体缺乏(PR;p=0.002)以及肿瘤分级(p=0.001)和增殖率(Ki-67;p<0.000)显著相关。 PKCα水平与其他临床病理参数如局部或远端转移没有显著相关性(表 三 ). PKCδ和PKCε与所分析的任何临床病理参数均无显著相关性(表 三 ).
表3。 队列I和队列II中PKCα、PKCδ和PKCε强度与临床病理变量之间的相关性。
队列 我 二
变量 PKCα PKCδ PKCε PKCα PKCε
NHG公司
ρ 0.401 -0.049 -0.029 0.247 -0.011
第页 0.001 0.719 0.833 <0.001 0.863
n个 60 57 55 249 263
雌激素受体
ρ -0.482 0.210 -0.016 -0.334 0.068
第页 <0.001 0.120 0.907 <0.001 0.273
n个 59 56 54 244 261
孕酮受体
ρ -0.402 -0.081 -0.216 -0.280 0.062
第页 0.002 0.554 0.120 <0.001 0.342
n个 58 55 53 223 240
Ki-67阳性
ρ 0.535 0.229 0.280 0.295 -0.056
第页 <0.001 0.144 0.069 <0.001 0.363
n个 46 42 43 244 261
节点状态
ρ -0.027 0.095 -0.002 0.029 0.028
第页 0.842 0.495 0.987 0.666 0.667
n个 56 54 52 224 233
远处转移
ρ 0.159 0.162 -0.064 0.090 0.037
第页 0.226 0.227 0.642 0.159 0.556
n个 60 57 55 247 261
表4。 队列I和队列II中PKCα、PKCδ和PKCε强度与组织学类型之间的关系。
第一组 管道 小叶的 髓质 粘液的
PKCα强度 0 25 三 0 2
p*=0.295 1 20 0 1 0
2 4 0 0 0
三 4 0 1 0
不适用。 42 三 0 2
PKCδ强度 0 12 0 0 1
p*=0.850 1 33 1 2 1
2 7 0 0 0
三 0 0 0 0
不适用。 43 5 0 2
PKCε强度 0 0 0 0 0
p*=0.800 1 12 0 1 0
2 29 1 1 2
三 9 0 0 0
不适用。 45 5 0 2
队列II 管道 小叶的 髓质 粘液的 管状的 混合的
PKCα强度 0 124 17 1 10 14 13
第页* <0.001 1 34 4 5 2 三 三
2 10 0 4 0 0 1
三 三 0 2 0 0 0
不适用。 168 52 三 5 17 17
PKCε强度 0 2 1 0 0 0 0
p*=0.328 1 38 9 7 4 5 5
2 90 19 4 7 9 7
三 41 5 1 1 1 7
不适用。 168 39 三 5 19 15
较大的队列(队列II;表 三 和 4 )然后分析PKCα的表达水平,因为该亚型与第一队列中的几个临床病理参数和PKCε相关,因为我们的数据与已发表的研究有点矛盾[ 22 ]. 队列II的结果证实了队列I的发现,其中PKCα水平高的肿瘤增殖率较高(p<0.001),ER(p<0.00 1)和PR-阴性(p<00.001),组织学分级较高(p<0.001)。 此外,一个χ 2 分析表明,在队列II的不同组织学亚组中,PKCα水平高低的肿瘤分布不均匀(表 4 ). 这种偏斜分布与骨髓型肿瘤有关。 符合以下标准的肿瘤被定义为髓质肿瘤:1)淋巴细胞质反应,2)显微镜下的界限,3)合胞体生长模式,4)分化差的核分级和高有丝分裂率。 对于这一组,十二分之二的被调查肿瘤(17%)具有高PKCα表达水平,而所有被评估乳腺癌的相应数量为五分之二百五十(2%)。 只有8%的髓质肿瘤PKCα阴性,而所有肿瘤的PKCα阳性率为72%。 因此,在PKCα水平较高的肿瘤中,髓样癌的比例过高。 PKCε的结果与队列I相似,与任何相关的临床病理参数无关。
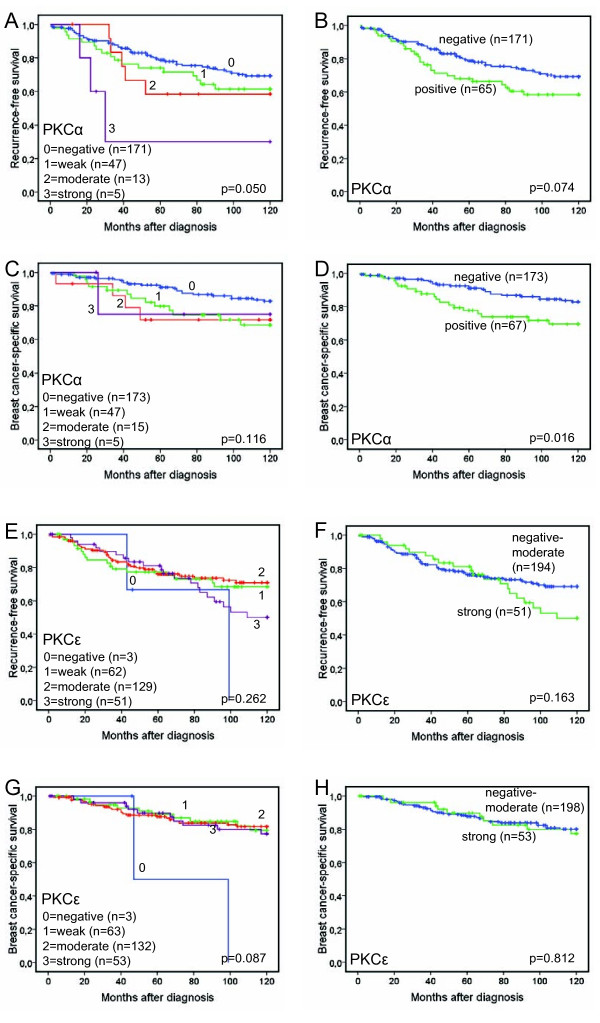
PKCα表达与预后不良相关 接下来,我们分析了PKCα和PKCε的表达与患者10年生存率之间的关系(图 2 ). 如图所示 2安培 ,较低的PKCα水平与显著延长的10年RFS相关(p=0.050)。 10年BCSS也出现了类似的趋势,但没有达到统计显著性(图 2摄氏度 ; p=0.116)。 由于大多数肿瘤的PKCα为阴性,而其他组(染色强度1-3)较小,因此将一个二分法变量定义为无染色和任何染色,用于无复发和乳腺癌特异性生存的相同分析。 当二分法时,PKCα阳性与较差的10年RFS的非显著趋势相关,图 2B型 ; p=0.074)。 然而,与PKCα阳性肿瘤患者相比,PKCα阴性肿瘤患者的10年BCSS显著改善(图 二维 ; p=0.016)。 我们还进行了Cox回归比例风险分析,证明了根据PKCα表达在单变量和多变量分析中对相对风险(RR)的估计,并根据诊断年龄、肿瘤大小、NHG、淋巴结状态和ER表达进行了调整(表 5 ). 这表明,PKCα阳性与10年期不良BCSS之间的相关性与已确定的预后参数无关(多变量RR=2.123,95%CI 1.092至4.126,p=0.026)。
图2。
根据PKCα和PKCε表达的无复发生存率和乳腺癌特异性生存率 根据PKCα(A-D)和PKCε(E-H)的表达,Kaplan-Meier估计了10年无复发生存期(A-B和E-F)和乳腺癌特异性生存期(C-D和G-H)。
表5。 根据PKCα在所有患者中的表达以及排除骨髓癌患者时,对队列II乳腺癌特异性生存期进行Cox单变量和多变量分析。
所有患者 髓样癌除外
RR(95%置信区间) p值 RR(95%置信区间) p值
单变量 单变量
PKCα阴性 1 1
PKCα阳性 2.105(1.148至3.862) 0.016 1.995(1.069至3.721) 0.030
多变量 多变量
PKCα阴性 1 1
PKCα阳性 2.123(1.092至4.126) 0.026 1.978(0.984至3.975) 0.055
由于所分析的大多数髓样癌均为PKCα阳性,因此这些肿瘤患者通常预后良好[ 34 ]在排除髓样癌患者后,我们还检测了10年的BCSS,发现PKCα仍然是一个独立的预后因素(表 5 ).
无论是在所有组(染色强度0-3)中,还是在将其分为染色强度0-2和3时(图 2E-H型 ). 由于阴性肿瘤所占比例较小,因此选择了较高的临界值对PKCε进行二分。
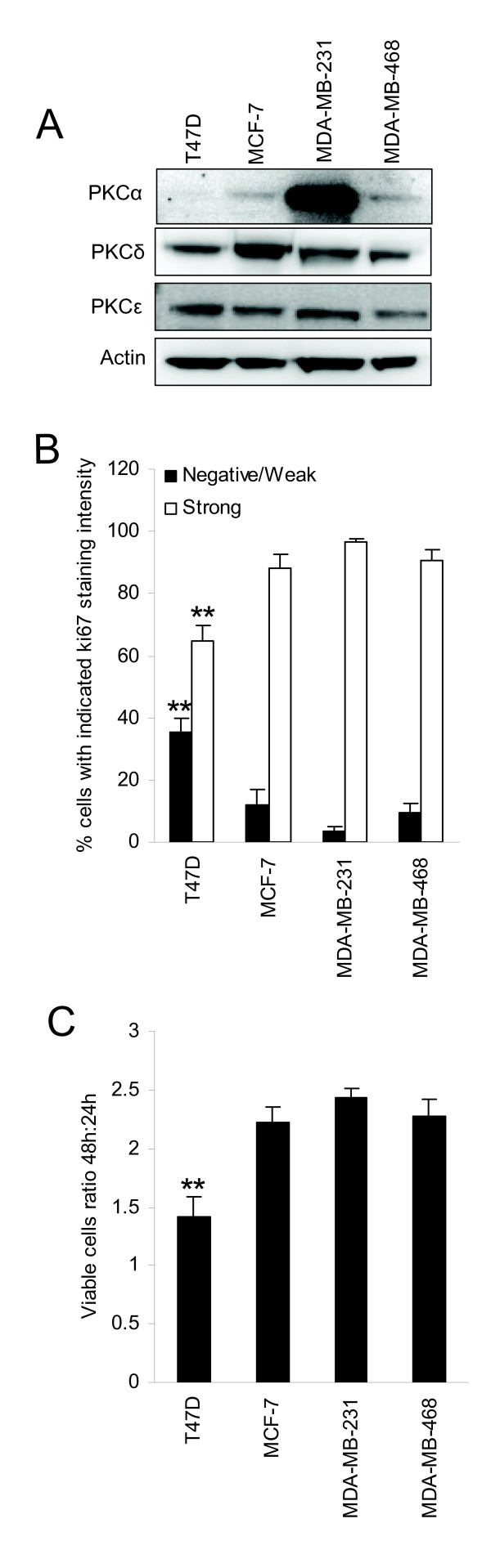
PKC在乳腺癌细胞系中的表达 为了评估不同的乳腺癌细胞株是否代表肿瘤中PKC亚型的表达模式,我们测量了四种乳腺癌细胞系中PKC的水平(图 3A级 ). 与MCF-7和MDA-MB-468细胞相比,MDA-MB-231细胞中PKCα水平较高。 在T47D细胞中未检测到PKCα。 MCF-7细胞中PKCδ水平较高,而PKCε的表达水平没有显著差异。
图3。
乳腺癌细胞系PKC的表达与增殖 Western blot显示T47D、MCF-7、MDA-MB-231和MDA-MB-468乳腺癌细胞(A)中PKCα、PKCδ和PKCε的表达水平。 增殖细胞的细胞颗粒用抗Ki-67免疫组织化学染色。 每个细胞系至少有200个细胞被评为阴性-弱染色或强染色强度(B)。 培养24小时和48小时后,用WST-1法测定活细胞数。 48小时与24小时的比值被用作细胞增殖的指标(C)。 在所有实验中,细胞都是在完全培养基中生长的。 蛋白质印迹是三个独立实验的代表。 B和C中的数据为平均值±SEM,n=3。 星号表示具有统计意义的差异(* 第页 <0.05和** 第页 <0.01)与其他细胞系(B和C)相比。
为了研究PKCα与肿瘤中观察到的高增殖率之间的关系,我们检测了细胞系的增殖率(图 3B公司 和 3厘米 ). T47D没有检测到PKCα,是增殖能力最低的细胞系,支持肿瘤数据。 另一方面,对于PKCα水平明显最高的MDA-MB-231,97%的细胞具有中等或强的Ki-67染色强度(图 3B公司 ). 对于PKCα水平较低但可检测到的细胞系MCF-7和MDA-MB-468,相应的数量分别为88%和91%。 这与MDA-MB-231细胞没有显著差异,考虑到这些细胞系中阳性细胞的比例接近100%,这是意料之外的。 Ki-67数据得到了细胞系生长率的支持,该生长率由培养48小时后的活细胞数与24小时后获得的细胞数之比估算得出(图 3厘米 ).
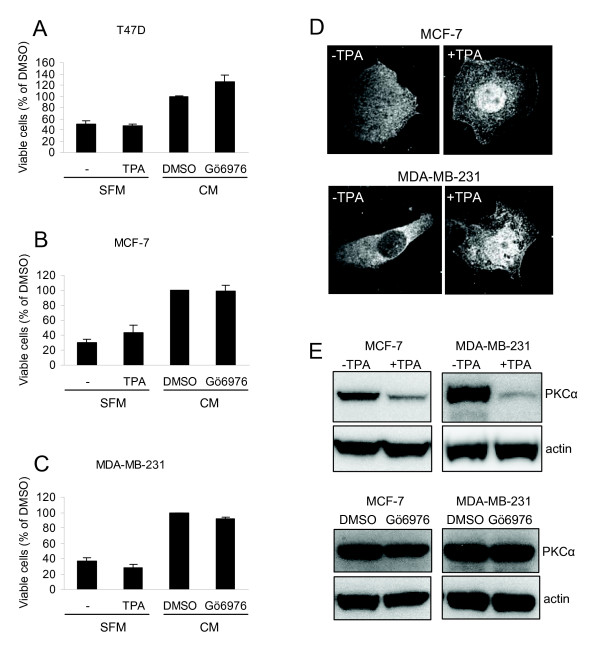
PKCα在无血清条件下对乳腺癌细胞增殖至关重要 为了进一步研究PKCα对乳腺癌细胞增殖是否重要,研究了PKC激活剂和抑制剂的作用(图 4A-C型 ). 在无血清条件下,TPA激活PKC不足以促进细胞生长,正如活细胞数量所示,活细胞数量代表增殖和细胞死亡的总和效应。 TPA确实影响PKCα,如PKCα迁移到MCF-7和MDA-MB-231细胞的质膜和细胞核中的富集所示(图 4D(四维) ). 这表明经TPA治疗后PKCα被激活,但PKCα的总水平也降低(图 第4页 )这使得TPA对细胞中PKCα净效应的估计变得复杂。
图4。
PKC激活或抑制后的细胞生长分析 在WST-1分析之前,将T47D(A)、MCF-7(B)和MDA-MB-231(C)乳腺癌细胞在无血清培养基(SFM)或2μM Gö6976、GF109203X或同等体积的二甲基亚砜(DMSO)中无或存在16 nM TPA的培养基中培养72小时。 数据(平均值±SEM,n=3)表示在控制条件下获得的活细胞百分比。 用免疫荧光和共聚焦显微镜(D)检测PKCα在对照或TPA处理的MCF-7和MDA-MB-231细胞中的定位。 通过Western blot(E)分析TPA或Gö6976治疗后PKCα的水平。
经典PKC抑制剂Gö6976并没有显著减少细胞数量,这表明PKCα的活性对正常条件下乳腺癌细胞的生长并不重要。
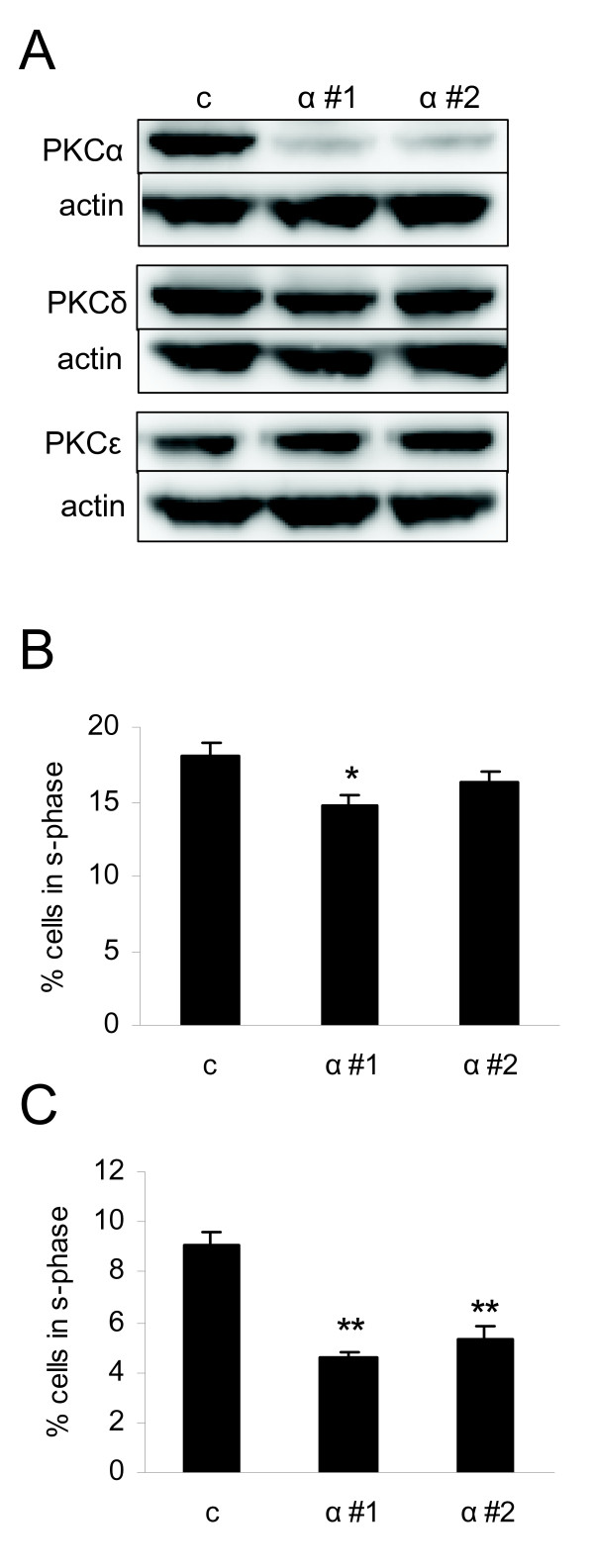
PKCα的促增殖作用与其催化活性无关[ 35 ]. 这一事实,加上TPA和Gö6976除了调节PKCα活性外,还可能具有非特异性的作用,导致我们使用siRNA寡核苷酸,然后分析细胞周期分布,更具体地分析PKCα的作用。 在MDA-MB-231细胞中,PKCα水平被下调,两种siRNAs都以PKCα为靶点,这并不影响其他PKC亚型的表达水平(图 5A级 ). 当细胞在含血清的完全培养基中生长时,只有一种PKCα寡核苷酸(α#1)显著影响细胞周期分布(CM;图 第5页 ). 与对照组相比,寡核苷酸略微减少了S期细胞的数量。 然而,在无血清培养基(SFM)下,与对照细胞相比,使用任一siRNA下调PKCα导致S期细胞数量显著减少(图 5摄氏度 ). 结果表明,PKCα对细胞增殖起着重要作用,尤其是在亚优化条件下。 在最佳生长条件下,PKCα可能是多余的增殖因子。
图5。
PKCα下调的MDA-MB-231细胞的细胞周期分布 用靶向PKCα(α#1和α#2)或对照寡核苷酸的两种不同siRNA转染MDA-MB-231细胞。 转染后,用完全培养基(CM)或无血清培养基(SFM)培养细胞24小时。 贴壁细胞随后进行Western blot(A)或碘化丙啶染色和流式细胞术(B和C)。 蛋白质印迹是三个独立实验的代表。 B和C中的数据(平均值±SEM,n=3)显示了s期细胞的百分比。
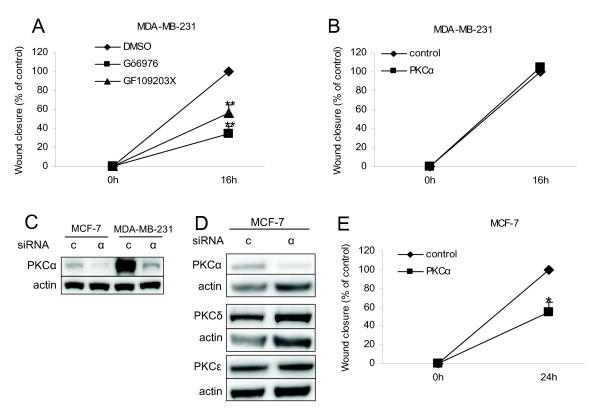
PKCα活性对乳腺癌细胞迁移是必需的 在乳腺癌中,PKCα与细胞迁移能力的增强有关,因为PKCα的过度表达已被证明可以促进乳腺癌细胞的迁移和转移[ 4 , 36 , 37 ]. 基于此,我们旨在研究内源性PKCα对乳腺癌细胞运动的重要性。 在没有或存在PKC抑制剂的情况下,对MDA-MB-231细胞进行伤口愈合分析(图 6A级 ). 抑制经典PKC(Gö6976)或经典和新型PKC(GF109203X)分别将DMSO处理细胞的伤口闭合抑制到34%和56%,表明PKC活性对MDA-MB-231细胞迁移能力很重要。 由于PKC抑制剂是异型非特异性的,我们在伤口愈合试验之前用siRNA下调MDA-MB-231细胞中的PKCα,以更具体地研究PKCα在迁移中的作用。 然而,PKCα的下调并不影响MDA-MB-231细胞的迁移(图 6亿 ). 与本研究中研究的其他细胞系相比,MDA-MB-231细胞具有较高的PKCα基础水平(图 3A级 ). 用靶向PKCα的siRNA转染这些细胞可能无法充分降低PKCα水平。 与MCF-7细胞的比较(图 6摄氏度 )事实证明,在对MDA-MB-231细胞进行siRNA处理后,这些细胞中的PKCα水平与MCF-7细胞中的水平大致相同。 因此,为了获得更显著的PKCα耗竭,我们下调了MCF-7细胞中的PKCα,然后进行了伤口愈合测定(图 第六版 ). MCF-7细胞中PKCα的沉默并不影响研究的其他PKC亚型(图 第6天 ). 在这些细胞中,PKCα的下调显著减少了55%的对照细胞向伤口的迁移(图 第六版 ). 结果表明PKCα活性对乳腺癌细胞的迁移至关重要 在体外 .
图6。
MDA-MB-231和MCF-7细胞的迁移 MDA-MB-231细胞在PKC抑制剂存在或不存在的情况下(A)或在用靶向PKCα(α)的siRNA或对照寡核苷酸转染后(c)(B)进行伤口愈合测定。 在进行创伤愈合试验(E)之前,MCF-7细胞(C和D)中的PKCα下调。 数据(平均值±SEM,n=4)表明,与对照条件下的闭合相比,伤口闭合。 星号表示具有统计意义的差异(* 第页 <0.05和** 第页 <0.01)。
讨论 一些研究表明,DAG-敏感的PKC亚型有助于乳腺癌的进展和乳腺癌细胞的恶性特征。 特别是PKCα、PKCδ和PKCε亚型已被强调为治疗乳腺癌或该疾病特定亚群的潜在靶点。 这导致我们设计了这项研究,其中检测了这些PKC亚型在原发性乳腺癌肿瘤中的表达,以评估其作为肿瘤侵袭性标记物的实用性。
为了证实这一分析,我们使用了两个不同的原发性乳腺癌肿瘤队列,队列的结果相似。 我们发现PKCα水平与包括ER阴性在内的几种肿瘤侵袭性标记物之间存在显著相关性。 最近的一项研究也观察到PKCα水平与ER阴性之间的相关性[ 8 ]使用70例接受过系统内分泌治疗的患者肿瘤。 他们还表明,高PKCα水平预示着内分泌治疗的疗效较差,这也得到了早期一项针对较少患者的研究的支持[ 7 ]. 我们的数据,如两个单独的队列所示,牢固地建立了PKCα和ER阴性之间的关系。 此外,我们发现PKCα与PR阴性之间存在明显的相关性,与肿瘤分级和高增殖率呈正相关,进一步支持了PKCα表达与肿瘤侵袭性相关参数的观点。 最后,对于PKCα阳性的原发性肿瘤患者,PKCα的表达预示着更糟糕的疾病结局,其10年乳腺癌特异性生存期明显较差。 多变量分析结果进一步表明PKCα是乳腺癌的独立预后因素。
然而,其他研究表明,与正常乳腺组织相比,乳腺癌中PKCα的水平实际上降低了[ 12 , 13 ]. 这可能并不一定与我们的发现相矛盾,因为我们材料中的绝大多数癌症样本基本上都是PKCα阴性,这与PKCα下调是乳腺癌进展过程中常见事件的观点一致。 因此,公布的数据和我们的结果表明,大多数乳腺癌是PKCα阴性的,但也有较小的亚组PKCα水平较高,表现出更具侵袭性的临床病理特征。 如果PKCα被用作乳腺癌治疗的靶点,这些数据强调了在进行此类干预之前评估PKCα水平的必要性。
在最大队列(II)中,PKCα水平与组织学亚型也有显著相关性。 在PKCα水平高的组中,骨髓组织学癌的代表性过高。 此外,队列I中唯一的骨髓癌是PKCα阳性。
根据证明PKCα水平与侵袭性特征相关的肿瘤数据,在乳腺癌细胞系中也发现PKCα与恶性特征相关。 PKCα水平升高与三苯氧胺相关并可诱导其产生[ 38 , 39 ]和多药[ 9 , 10 ]ER阳性细胞株的耐药性。 此外,PKCα在MCF-7细胞中的过度表达导致增殖增加,这与我们的肿瘤数据一致[ 4 ]但也使他们更容易受到凋亡损伤[ 40 , 41 ]. 我们发现,与其他细胞系相比,未检测到PKCα表达的细胞系T47D的Ki-67阳性细胞百分比更低,生长速度较慢,与肿瘤数据类似。 然而,PKCα表达最高的细胞系MDA-MB-231与可检测但表达低得多的细胞系相比,Ki-67阳性率稍高。 这可能与Ki-67阳性细胞比例较高(97%)且不能进一步升高有关。
血清中PKCα的抑制作用和血清饥饿时PKC的激活都不会影响细胞系的生长,从而支持PKCα对乳腺癌细胞生长的重要作用。 最近的一篇论文表明,PKCα蛋白(而非活性)对胶质瘤细胞增殖至关重要[ 35 ]. 我们发现,用siRNA下调PKCα对在完全培养基中生长的MDA-MB-231细胞的细胞周期分布产生适度影响。 然而,在无血清条件下,PKCα沉默明显减少了增殖细胞的数量,这表明,与胶质瘤细胞一样,PKCβ蛋白(但可能不是其催化活性)支持次优条件下的增殖。
研究 在体外 已经证明,增加MCF-7细胞中PKCα的表达会使其对PKC激活的反应更加迁移[ 42 ]. 我们对细胞株的实验表明,PKC活性支持MDA-MB-231细胞的迁移。 然而,在该细胞系中,用siRNA下调PKCα并不影响细胞迁移。 MDA-MB-231细胞具有较高的PKCα基础表达水平,PKCα的不完全下调可能解释了其对细胞迁移缺乏影响。 MCF-7细胞中PKCα的下调更有效地抑制了伤口愈合,支持了这一假设。 因此,我们的数据表明,PKCα活性对乳腺癌细胞的迁移很重要,这与先前使用PKCα过表达的研究结果一致。 迁移倾向可能促进肿瘤的转移。 然而,我们的肿瘤数据并不支持PKCα在播散中的作用。 PKCα的表达与淋巴结或远处转移无关。 因此,PKCα对迁移的影响可能主要很重要 在体外 .
对于PKCδ,关于原发性肿瘤中表达水平的信息较少。 一项研究表明,低水平的PKCδ,尤其是结合高PKCα,可以预测内分泌治疗的耐药性[ 8 ]. 在本研究中,我们未观察到PKCδ表达与相关临床病理参数之间的任何显著关联。 因此,改变PKCδ表达似乎不是乳腺癌进展的先决条件。
PKCε被认为是侵袭性乳腺癌的标志物,因为据报道,其在激素受体阴性的高肿瘤级别乳腺癌中的表达升高 HER2型 放大[ 22 ]. 然而,PKCε表达与肿瘤分级之间的关系在本研究中未得到证实,这表明在代表所有乳腺癌组织学亚型的队列中可能并不明显。 在更明确的乳腺癌亚组中,PKCε水平可能是侵袭性的标志。
结论 总之,我们的研究结果表明,PKCα的表达与乳腺癌ER和PR阴性以及高组织学分级和增殖率相关。 PKCα在乳腺癌细胞增殖中也有重要作用 在体外 .PKCα的表达与乳腺癌样本的转移无关,但PKCα活性支持乳腺癌细胞的迁移 在体外 重要的是,PKCα的表达独立于已确定的预后参数,预测10年乳腺癌特异性生存率较差。 因此,我们认为PKCα可能是乳腺癌预测和治疗分层的有用标记物。
作者的贡献 GKL评估了临床样本,进行了统计分析,参与了实验设计并完成了大部分实验工作,并汇编了手稿草稿。
LC做了一些实验工作。
IOZ参与了抗体和临床样本的评估。
德国劳埃德船级社监督了队列I的分析,并参与了解释性讨论。
KJ监督了队列II的分析和患者数据的统计分析,并帮助起草了手稿。
CL构思了这项研究,参与了实验工作的设计,并帮助起草了手稿。
所有作者阅读并批准了最终手稿。
参与者信息 Gry Kalstad Lönne,电子邮件: Gry.Kalstad_Lonne@med.美国。
Louise Cornmark,电子邮件: Lousie.Cornmark@med.美国。
Iris Omanovic Zahirovic,电子邮件: iris_zahirovic@yahoo.se。
戈兰·兰德伯格,电子邮件: Goran.Landberg@med.美国。
Karin Jirström,电子邮件: Karin.Jirstrom@med.美国。
Christer Larsson,电子邮件: Christer.Larsson@med.luse。
致谢 我们感谢Elise Nilsson提供的出色技术援助。 这项工作得到了瑞典癌症协会、瑞典研究委员会、瑞典儿童癌症基金会、马尔默大学医院研究基金会以及科克、克拉福德、奥利、埃洛夫·爱立信和冈纳·尼尔森基金会的资助。
工具书类
Vargo-Gogola T,Rosen JM。乳腺癌建模:一种尺寸并不适合所有人。 Nat Rev癌症。 2007; 7:659–672。 doi:10.1038/nrc2193。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Sorlie T、Perou CM、Tibshirani R、Aas T、Geisler S、Johnsen H、Hastie T、Eisen MB、Rijn M van de、Jeffrey SS。 乳腺癌的基因表达模式区分具有临床意义的肿瘤亚类。 美国国家科学院院刊,2001年; 98:10869–10874. doi:10.1073/pnas.191367098。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
牛顿AC.蛋白激酶C:磷酸化、辅因子和大分子相互作用的结构和空间调节。 《化学》2001年版; 101:2353–2364. doi:10.1021/cr0002801。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Ways DK、Kukoly CA、deVente J、Hooker JL、Bryant WO、Posekany KJ、Fletcher DJ、Cook PP、Parker PJ。 转染蛋白激酶C-α的MCF-7乳腺癌细胞表现出其他蛋白激酶C亚型的表达改变,并显示出更具侵袭性的肿瘤表型。 临床投资杂志。 1995; 95:1906–1915. doi:10.1172/JCI117872。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Chisamore MJ,Ahmed Y,Bentrem DJ,Jordan VC,Tonetti DA。雌二醇对注射过表达蛋白激酶Cα的T47D乳腺癌细胞系的裸鼠的新型抗肿瘤作用。 临床癌症研究2001; 7:3156–3165. [ 公共医学 ] [ 谷歌学者 ]
Tonetti DA,Chisamore MJ,Grdina W,Schurz H,Jordan VC。蛋白激酶CαcDNA在激素依赖性乳腺癌细胞系中的稳定转染。 英国癌症杂志。 2000; 83:782–791. doi:10.1054/bjoc.2000.1326。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Tonetti DA、Morrow M、Kidwai N、Gupta A、Badve S。蛋白激酶Cα表达升高可能预示他莫昔芬治疗失败。 英国癌症杂志。 2003; 88:1400–1402. doi:10.1038/sj.bjc.6600923。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Assender JW、Gee JM、Lewis I、Ellis IO、Robertson JF、Nicholson RI。蛋白激酶C亚型表达作为乳腺癌内分泌治疗疾病预后的预测因子。 临床病理学杂志。 2007; 60:1216–1221. doi:10.1136/jcp.2006.041616。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Gill PK,Gescher A,Gant TW。蛋白激酶C同工酶α和θ对人乳腺癌细胞MDR1启动子活性的调节。 欧洲生物化学杂志。 2001; 268:4151–4157. doi:10.1046/j.1432-1327.2001.02326.x。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Blobe GC、Sachs CW、Khan WA、Fabbro D、Stabel S、Wetsel WC、Obeid LM、Fine RL、Hannun YA。 选择性调节多药耐药MCF-7细胞中蛋白激酶C(PKC)同工酶的表达。 PKCα表达增强的功能意义。 生物化学杂志。 1993; 268:658–664。 [ 公共医学 ] [ 谷歌学者 ]
Roychowdhury D,Lahn M.针对蛋白激酶C-α的反义治疗(Affinitak,LY900003/ISIS 3521):在乳腺癌中的潜在作用。 塞明·昂科尔。 2003; 30:30–33。 doi:10.1053/son.2003.37273。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Ainsworth PD、Winstanley JH、Pearson JM、Bishop HM、Garrod DR。蛋白激酶Cα在正常乳腺、导管原位癌和浸润性导管癌中的表达。 《欧洲癌症杂志》。 2004; 40:2269–2273. doi:10.1016/j.ejca.2004.06.027。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Kerfoot C,Huang W,Rotenberg SA。晚期人类乳腺癌的免疫组织化学分析显示蛋白激酶Cα下调。 组织化学与细胞化学杂志。 2004; 52:419–422. doi:10.1177/002215540405200314。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Zeidan YH、Wu BX、Jenkins RW、Obeid LM、Hannun YA。 蛋白激酶Cδ介导的酸性鞘磷脂酶磷酸化在紫外线诱导线粒体损伤中的新作用。 Faseb J.2008; 22:183–193. 网址:10.1096/fj.07-8967com。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
McCracken MA、Miraglia LJ、McKay RA、Strobl JS。 蛋白激酶Cδ是人类乳腺癌细胞系中的生存因子。 摩尔癌症治疗。 2003; 2:273–281. [ 公共医学 ] [ 谷歌学者 ]
Nabha SM、Glaros S、Hong M、Lykkesfeldt AE、Schiff R、Osborne K、Reddy KB。 PKC-δ的上调有助于乳腺肿瘤细胞抗雌激素抵抗。 致癌物。 2005; 24:3166–3176. doi:10.1038/sj.onc.1208502。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Alonso-Escolano D、Medina C、Cieslik K、Radomski A、Jurasz P、Santos-Martinez MJ、Jiffar T、Ruvolo P、Radomski MW。蛋白激酶Cδ介导血小板诱导的乳腺癌细胞侵袭。 药理学实验与治疗杂志。 2006; 318:373–380. doi:10.1124/jpet.106.103358。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Kiley SC、Clark KJ、Duddy SK、Welch DR、Jaken S.乳腺肿瘤细胞中蛋白激酶Cδ增加:与转化和转移进展的关系。 致癌物。 1999; 18:6748–6757. doi:10.1038/sj.onc.1203101。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Kiley SC、Clark KJ、Goodnough M、Welch DR、Jaken S.蛋白激酶Cδ参与乳腺癌细胞转移。 1999年癌症研究; 59:3230–3238. [ 公共医学 ] [ 谷歌学者 ]
Grossoni VC、Falbo KB、Kazanietz MG、de Kier Joffe ED、Urtreger AJ。 蛋白激酶Cδ增强小鼠乳腺细胞的增殖和存活。 霉菌致癌。 2007; 46:381–390. doi:10.1002/mc.20287。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Lönne GK,Masoumi KC,Lennartsson J,Larsson C。蛋白激酶Cδ通过抑制ERK1/2通路支持MDA-MB-231乳腺癌细胞的存活。 生物化学杂志。 2009; 284:33456–33465。 doi:10.1074/jbc。 M109.036186。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Pan Q、Bao LW、Kleer CG、Sabel MS、Griffith KA、Teknos TN、Merajver SD。蛋白激酶Cε是侵袭性乳腺癌的预测生物标志物,也是RNA干扰抗癌治疗的有效靶点。 2005年癌症研究; 65:8366–8371. doi:10.1158/008-5472.CAN-05-0553。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Lu D,Sivaprasad U,Huang J,Shankar E,Morrow S,Basu A.蛋白激酶C-ε通过抑制Bax易位保护MCF-7细胞免受TNF介导的细胞死亡。 细胞凋亡。 2007 [ 内政部 ] [ 公共医学 ]
Sivaprasad U,Shankar E,Basu A.Bid下调与PKCε介导的TRAIL抵抗相关。 细胞死亡不同。 2007; 14:851–860. doi:10.1038/sj.cdd.4402077。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Lu D,Huang J,Basu A.PKB的解除对乳腺癌细胞中PKC抗凋亡信号的影响。 国际癌症杂志。 2004; 25:671–676. [ 公共医学 ] [ 谷歌学者 ]
Zeidman R、Lofgren B、Pahlman S、Larsson C.PKCε通过其调节域并独立于其催化域,诱导神经母细胞瘤细胞中的神经突样过程。 细胞生物学杂志。 1999; 145:713–726. doi:10.1083/jcb.145.4.713。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Nielsen NH、Arnerlov C、Emdin SO、Landberg G.Cyclin E过度表达,乳腺癌的一个负面预后因素,与雌激素受体状态密切相关。 英国癌症杂志。 1996; 74:874–880. doi:10.1038/bjc.1996.451。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Nielsen NH、Emdin SO、Cajander J、Landberg G.乳腺癌中细胞周期蛋白E和D1的放松调节与视网膜母细胞瘤蛋白的失活有关。 致癌物。 1997; 14:295–304. doi:10.1038/sj.onc.1200833。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Roos G、Nilsson P、Cajander S、Nielsen NH、Arnerlov C、Landberg G。乳腺癌中端粒酶活性与p53状态和临床病理参数的关系。 国际癌症杂志。 1998; 79:343–348. doi:10.1002/(SICI)1097-0215(19980821)79:4<; 343::AID-IJC6>; 3.0.CO版本; 2伏。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Svensson S、Jirstrom K、Ryden L、Roos G、Emdin S、Ostrowski MC、Landberg G。ERK磷酸化与乳腺癌中VEGFR2表达和Ets-2磷酸化相关,与三苯氧胺治疗耐药和预后良好的小肿瘤相关。 致癌物。 2005; 24:4370–4379. doi:10.1038/sj.onc.1208626。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Borgquist S、Holm C、Stendahl M、Anagostaki L、Landberg G、Jirstrom K。雌激素受体α和β与临床病理参数有不同的相关性,它们的共同表达可能预示乳腺癌内分泌治疗的更好反应。 临床病理学杂志。 2008; 61:197–203. doi:10.1136/jcp.2006.040378。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Helczynska K、Larsson A-M、Holmquist Mengelbier L、Bridges E、Fredlund E、Borgquist S、Landberg G、Pahlman S、Jirstrom K。低氧诱导因子-2α与侵袭性乳腺癌的远处复发和不良预后相关。 癌症研究2008; 68:9212–9220. doi:10.1158/0008-5472.CAN-08-1135。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Raghunath A,Ling M,Larsson C。催化域限制了蛋白激酶Cα的移位,以响应Ca2+和二酰甘油的增加。 生物化学杂志2003; 370:901–912. doi:10.1042/BJ20021420。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Malyuchik党卫军,Kiyamova RG。 髓样乳腺癌。 Exp Oncol公司。 2008; 30:96–101。 [ 公共医学 ] [ 谷歌学者 ]
Cameron AJ、Procyk KJ、Leitges M、Parker PJ。 PKCα蛋白而非激酶活性对神经胶质瘤细胞的增殖和存活至关重要。 国际癌症杂志。 2008; 123:769–779. doi:10.1002/ijc.23560。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Ng T、Shima D、Squire A、Bastiaens PI、Gschmeissner S、Humphries MJ、Parker PJ。 PKCα通过结合和控制整合素流量调节β1整合素依赖的细胞运动。 Embo J.1999; 18:3909–3923. doi:10.1093/emboj/18.14.3909。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Abeyweera TP,Chen X,Rotenberg SA。蛋白激酶Cα对α6-微管蛋白的磷酸化激活人类乳腺细胞的运动。 生物化学杂志。 2009 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ]
Frankel LB、Lykkesfeldt AE、Hansen JB、Stenvang J.蛋白激酶Cα是抗雌激素抵抗的标志物,参与三苯氧胺耐药人类乳腺癌细胞的生长。 乳腺癌研究治疗。 2007; 104:165–179. doi:10.1007/s10549-006-9399-1。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Lin X,Yu Y,Zhao H,Zhang Y,Manela J,Tonetti DA。在T47D人乳腺癌肿瘤模型中,需要过度表达PKCα才能实现雌二醇抑制和他莫昔芬耐药。 致癌。 2006; 27:1538–1546. doi:10.1093/carcin/bgl002。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Yde CW、Gyrd-Hansen M、Lykkesfeldt AE、Issinger OG、Stenvang J.获得性抗雌激素抵抗的乳腺癌细胞对顺铂诱导的细胞死亡敏感。 摩尔癌症治疗。 2007; 6:1869–1876. doi:10.1158/1535-7163.MCT-07-0072。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
de Vente JE、Kukoly CA、Bryant WO、Posekany KJ、Chen J、Fletcher DJ、Parker PJ、Pettit GJ、Lozano G、Cook PP。磷酸酯类通过蛋白激酶C亚型表达的改变诱导MCF-7乳腺癌细胞死亡。 p53诱导gadd-45依赖性诱导在引发死亡中的作用。 临床投资杂志。 1995; 96:1874–1886. doi:10.1172/JCI118233。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Parsons M、Keppler MD、Kline A、Messent A、Humphries MJ、Gilchrist R、Hart IR、Quittau-Prevestel C、Hughes WE、Parker PJ、Ng T.蛋白质激酶C-整合素相互作用的定点扰动阻断癌细胞趋化性。 分子细胞生物学。 2002; 22:5897–5911. doi:10.1128/MCB.22.16.5897-5911.2002。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]