摘要 鞘磷脂神经酰胺、鞘氨醇和1-磷酸鞘氨醇(S1P)调节 细胞信号、增殖、凋亡和自噬。 鞘氨醇激酶-1和-2 (SK1和SK2)磷酸化鞘氨醇形成S1P,改变平衡活性 这些脂质对细胞增殖的影响。 我们之前曾报道过 药物抑制SK活性可延缓体内肿瘤生长。 现在 研究表明,SK2-选择性抑制剂 3-(4-氯苯基)-金刚烷-1-羧酸(吡啶-4-基甲基)酰胺(ABC294640) 诱导由微管相关蛋白引起的非凋亡细胞死亡 轻链3断裂,溶酶体形态改变,形成 A-498肾癌细胞中的自噬体和酸性小泡增多。 ABC294640在PC-3前列腺和MDA-MB-231乳腺中引起类似的自噬反应 腺癌细胞。 A-498细胞同时暴露于ABC294640和 3-甲基腺嘌呤,一种自噬抑制剂,将毒性机制转换为 细胞凋亡,但SK2抑制剂的效力降低,表明自噬 是该化合物杀死肿瘤细胞的主要机制。 诱导 蛋白酶体抑制剂的未折叠蛋白反应 N个- (苄氧羰基)亮氨酸亮氨酸 Z轴 -Leu-Leu-Leu-al(MG-132)或热休克蛋白90抑制剂 格尔德霉素在体外协同增强ABC294640的细胞毒性。 在 每日给药携带A-498异种移植物的严重联合免疫缺陷小鼠 ABC294640延缓了肿瘤生长并提高了自噬标记物,但没有 增加末端脱氧核苷酸转移酶介导的dUTP缺口末端 肿瘤中的标记阳性细胞。 这些数据表明ABC294640促进了 肿瘤细胞自噬,最终导致非凋亡细胞死亡和延迟 体内肿瘤生长。 因此,ABC294640可以有效地补充 诱导肿瘤细胞凋亡的抗癌药物。
目前大多数抗癌药物通过诱导细胞凋亡来杀死分裂活跃的细胞 ( 富尔达,2009 ). 除此之外 “经典”癌症化疗,阻断分子 肿瘤细胞增殖途径及诱导替代细胞的治疗 死亡途径对药物开发很重要( 里奇 和Zong,2006年 ). 凋亡细胞死亡涉及一系列导致 细胞形态的特征性变化,包括细胞膜不对称性的丧失, 核分裂、染色质浓缩、染色体DNA分裂和 半胱氨酸天冬氨酸蛋白酶的激活( 里奇和宗,2006年 ). 不幸的是,癌细胞往往对激活凋亡因子的药物产生耐药性 通路( 富尔达,2009 ). 因此,替代电池 死亡途径正在研究中,以用于癌症化疗( 里奇和宗,2006年 ).
自噬是一个可逆的分解代谢适应过程,负责降解 饥饿和/或生长因子缺乏时的长寿蛋白质和细胞存活 ( 昆都和汤普森,2008 ). 在自噬过程中, 部分细胞质被溶酶体消化,从而提供代谢物 用于细胞内稳态。 尽管自噬是一个在细胞中起主要作用的过程 它还能够诱导细胞死亡,其特征是广泛消化 细胞内细胞器( Bursch等人,2000年 ). 重要的是,一些小分子(包括一些抗癌药物)激活 肿瘤细胞体内和体外的自噬(综述于 Lefranc等人,2007年 )表明这种生物的重要性 化学疗法发展的过程。 两个强有力的鞘脂第二信使, 神经酰胺和鞘氨醇-1磷酸盐(S1P)也参与许多细胞 与细胞稳态相关的过程,包括细胞凋亡和自噬( 库维利埃,2007年 ; 拉维厄 等人,2008年 ; Wymann和Schneiter,2008年 ). 鞘氨醇催化促凋亡鞘氨醇转化为前存活S1P 激酶-1(SK1)和SK2,这些酶被认为是药物的重要靶点 发展( Delgado等人,2006年 ; 库维利埃,2007年 ). SK1的过度表达 在一些实体肿瘤中得到证实( French等人。, 2003 ; Taha等人,2004年 ),在可能的地方 促进细胞存活和耐药性并调节自噬( Lavieu等人,2006年 ). 与SK1的作用相比 了解SK2的作用,其活动似乎特定于细胞类型和 电池条件(在中审查 Taha等人,2006年 ).
最近,我们从一个化学库中鉴定出SKs的非脂质小分子抑制剂 ( French等人,2003年 , 2006 ). 乳腺癌同种异体移植中使用这些药物 肿瘤模型对小鼠无毒性延迟肿瘤生长( French等人,2003年 , 2006 ). 我们的长期 目的是识别SK1和SK2的特定小分子抑制剂并开发 SK酶的药理学操作以获得治疗益处。 为此,我们 合成ABC294640( 图1 A) ,第一次口服 可用,SK2-选择性抑制剂。 ABC294640在 与鞘氨醇 K(K) 我 10μM用于重组 人类SK2( French等人,2010年 )并且具有治疗作用 糖尿病视网膜病变模型的疗效( Maines等人。, 2006 )和炎症性肠病( 缅因州等 al.,2008年 ). 重要的是,我们最近证明ABC294640 良好的药理学特性,在小鼠血浆和 无明显毒性的肿瘤( French等人,2010年 ).
图1。
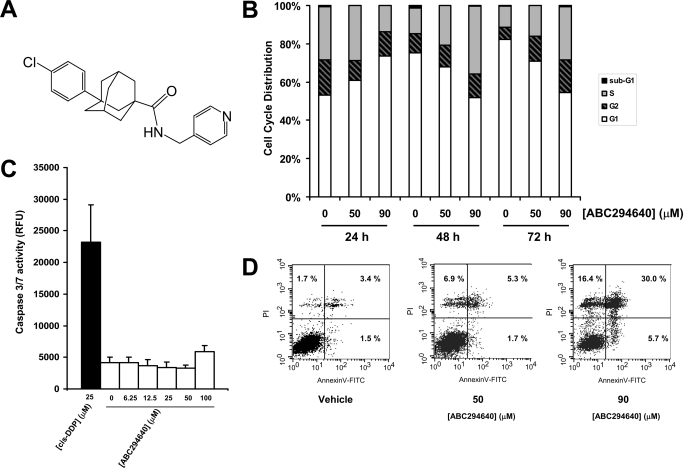
ABC294640诱导A-498细胞的非凋亡性细胞死亡。 A、 化学式 将细胞暴露于指示浓度的ABC294640和 24、48或72小时固定。取细胞核,用PI染色,DNA 通过流式细胞术分析含量,如下所述 材料和 方法 C,细胞暴露于指示浓度的 ABC294640持续72 h,用荧光法测定半胱氨酸天冬氨酸蛋白酶3/7活性 描述如下 材料和方法 .顺铂 ( 顺式- DDP)用作对照(黑条)。 数据表示平均值 三个实验的±标准误差。 D、 细胞暴露于 指示浓度的ABC294640持续72小时,并用PI和 流式细胞术分析前的Annexin-V-FITC,如下所述 材料和方法 。对于每个面板,左下角 表示Annexin V-和PI-阴性细胞; 右下角表示 膜联蛋白V阳性细胞(凋亡细胞); 右上角表示死亡 膜通透性为PI(PI阳性细胞)的细胞被膜联蛋白V染色; 左上角表示游离核。 占总数的百分比 单元格显示在每个象限中。
本研究的主要目的是确定生物过程 负责ABC294640诱导的癌细胞死亡。 为了实现这个目标,我们使用了A-498 肾脏、PC-3前列腺和MDA-MB-231乳腺肿瘤细胞表明ABC294640诱导 非凋亡细胞死亡之前有自噬标记,包括酸化 细胞质小泡,LC3切割增加,以及自噬体的积累。 在 此外,对携带A-498异种移植物的小鼠给予ABC294640可延迟 肿瘤生长和来自治疗小鼠的肿瘤免疫染色显示出特征 体内自噬反应。
材料和方法 试剂和细胞培养。 抗体购买如下:mTOR和磷酸化-mTOR(Ser2448)、Akt、, 磷酸化Akt和p53抗体来自Cell Signaling Technology Inc.(Danvers, MA); ERK和磷酸化ERK抗体来自圣克鲁斯生物技术公司(Santa Cruz Biotechnology Inc.) 加利福尼亚州克鲁兹); LC3抗体来自Novus Biologicals Inc.(利特尔顿,CO); 泛RAS 抗体来自致癌科学(马萨诸塞州剑桥); pan-Bcl-2来自 Sigma-Aldrich(密苏里州圣路易斯)。 与兔二级抗体结合的CY3.5为 从Calbiochem(加利福尼亚州圣地亚哥)购买,并且购买了所有其他抗体 来自Abcam Inc.(马萨诸塞州剑桥)。 MitoTracker绿色、LysoTracker红色、Annexin V、, Superscript III系统从Invitrogen(加利福尼亚州卡尔斯巴德)购买。 ABC294640由Apogee生物技术公司(宾夕法尼亚州Hummelstown)提供。 C6-陶瓷和二甲基鞘氨醇(DMS)购自Avanti Polar Lipids (阿拉巴马州,阿拉巴马州)。 MG-132购自Calbiochem,而格尔德霉素是一种 Jennifer Isaacs博士(南卡罗来纳医科大学, 南卡罗来纳州查尔斯顿)。 所有其他化学品均购自Sigma-Aldrich。 shRNA SK2和ATG7慢病毒颗粒来自圣克鲁斯生物技术公司 Inc.从QIAGEN(加利福尼亚州巴伦西亚)和PerfeCTa SYBR购买了RNeasy工具包 iQ套件的Green Supermix是从Quanta Biosciences(Gaithersburg, MD)。 TUNEL染色试剂盒和四甲基罗丹明购自罗氏公司 诊断(德国曼海姆),Vectastain ABC试剂盒购自Vector 实验室(加利福尼亚州伯林盖姆)。 MDA-MB-231乳腺癌,PC-3 前列腺癌和A-498肾癌细胞购自 美国型培养物收藏馆(弗吉尼亚州马纳萨斯),保存于RPMI 1640 介质、Dulbecco改良的Eagle介质和Eagle的最小基本介质, 分别补充有来自Invitrogen的10%胎牛血清(Carlsbad, 加利福尼亚州)。 American Type Culture Collection对细胞系进行质量控制 通过测试所有人类细胞系的短串联重复序列基因座。 联合免疫缺陷鼠 从国家癌症研究所(马里兰州贝塞斯达)购买。
体外细胞治疗和Western Blot分析。 为了测量体外细胞对ABC294640和其他试剂的敏感性,标准 硫罗丹明B(SRB)测定( Skehan等人。, 1990 )如前所述执行( French等人,2003年 ).
对于SDS-PAGE和免疫印迹,细胞在大约 10 6 细胞/10 cm板,并用如下所示的化合物处理 结果 细胞在缓冲液[50 mM Tris-HCl(pH 8)中溶解,1% 脱氧胆酸钠、1%诺奈德P-40、5 mM EDTA、5 mM-EGTA和150 mM NaCl],以及 在22000℃离心除去不溶性部分 克 持续20分钟,用SDS-PAGE在10%凝胶上分离可溶性部分 蛋白质电泳转移到聚偏二氟乙烯上 膜。 用10%牛血清白蛋白封闭膜,并用 各种初级抗体。 所有免疫印迹均通过增强 化学发光并通过ImageJ程序(美国国立卫生研究院 健康,马里兰州贝塞斯达)。
细胞周期、凋亡和线粒体膜完整性分析。 对于细胞周期分析,细胞暴露于不同浓度的ABC294640 24、48或72小时,用PBS洗涤两次,并在0.5 ml PI染色中培养 溶液(50μg/ml碘化丙啶,40μg/ml核糖核酸酶A PBS)在37°C下保持30分钟。 细胞周期分布在 南卡罗来纳医科大学流式细胞术设备 Dickinson FACSCalibur分析流式细胞仪(BD Biosciences,San Jose,CA)。 caspase-Glo 3/7测定法测定caspase 3和7的活性 (威斯康星州麦迪逊市普罗米加)。 简言之, A-498细胞在96个白色平板中生长,密度为10000个细胞/ 好。 用ABC294640孵育100μl半胱氨酸蛋白酶试剂后 添加,然后在室温下培养板30分钟 孵育后,使用SpectraMax M5板测定发光水平 读者(Invitrogen)。 将暴露于顺铂的细胞作为阳性对照 细胞凋亡。 对于Annexin-V染色,暴露于ABC294640后,细胞 胰蛋白酶化,在含10%胎牛血清的培养基中重新悬浮,洗涤两次 在PBS中,并再次悬浮在Annexin结合缓冲液中(10 mM HEPES,140 mM NaCl,和 2.5 mM氯化钙 2 pH值为7.4)。 至100μl细胞悬液,5 添加μl Annexin-V溶液,并将混合物保存在室内 培养15分钟后,400μl Annexin缓冲液 加入细胞后立即进行流式细胞仪分析。 为了分析 线粒体膜功能,细胞暴露于ABC294640或顺铂(阳性 对照组)在生长培养基中用100 nM四甲基罗丹明染色30 min, 用PBS洗涤后,立即用流式细胞仪对细胞进行分析。 收集粘附细胞和漂浮细胞用于凋亡和流动 细胞分析。
显微镜。 使用LSM 510激光扫描共焦显微镜获得共焦图像 (纽约州桑伍德卡尔蔡司公司),其中两种探测器的增益相等 实验组和对照组,除非另有说明。 字段是随机的 选择,并且每个细胞记录至少五个具有多个细胞的不同图像 实验条件。 对于电子显微镜,细胞在25mm的烧瓶中生长 并暴露于50μM ABC294640中24 h。细胞用2%固定 用2%四氧化锇后固定的己二醛缓冲戊二醛,以及 在乙醇中脱水。 脱水后,以1:1的比例渗透细胞 100%EtOH和Embed 812的溶液,然后用纯Embed 822包埋。 使用卷锯,切割出几个具有代表性的区域并重新埋入 正确的方向,然后切割70-nm薄型截面。 双重染色 用乙酸铀酰和柠檬酸铅进行,薄片 用JEOL(日本东京)JEM 1010透射电子显微镜检查。
细胞器官染色。 MitoTracker绿色用于线粒体可视化,LysoTracker红色用于线粒体可视化 如前所述可视化溶酶体( 拉瓦尔等人。, 2006 ). 将细胞放置过夜并暴露于不同浓度 ABC294640在37°C、10%血清中24、48或72小时 Eagle最小基本培养基(A-498),Dulbecco改良Eagle培养基 (PC-3)或RPMI 1604介质(MDA-MB-231)。 LysoTracker red和MitoTracker 添加绿色以达到50 nM的最终浓度。 1小时后 孵育后,用新鲜培养基替换培养基,共焦成像 已执行。 在一些实验中,酸性囊泡也被吖啶染色 橙色(5μg/ml),添加到含有 替换吖啶后,将10%的血清和细胞培养15分钟 将含有橙色的培养基与正常培养基混合,培养细胞 共焦成像观察前2小时。 免疫荧光染色 对生长在八个室载玻片中的细胞进行LC3-II。 24、48岁之后 将细胞暴露于ABC294640或72小时,取出培养基,固定细胞 在3.7%多聚甲醛中,用0.1%Triton X-100渗透,用2%封闭 牛血清白蛋白在含吐温-20的Tris缓冲盐水中,并用12 μg/ml LC3抗体在封闭溶液中放置30分钟 LC3抗体在封闭溶液中孵育60分钟,培养细胞 与CY3.5偶联的抗兔第二抗体,浓度为0.4 μg/ml。在室温下30分钟后,用 装有吐温-20的Tris缓冲盐水,通过共聚焦观察 显微镜检查。
异种移植研究。 动物研究已按照《护理指南》和 美国国立卫生研究院对实验动物的使用。 联合免疫缺陷鼠 (6-8周龄)注射3×10 6 每只小鼠A-498个细胞,3至4周后,荷瘤小鼠为100至150个 mg用载体或50 mg/kg ABC294640治疗5天/周,持续4周 (每组8只小鼠)。 每周测量两次肿瘤体积 使用以下公式计算:体积=1/2×长度 ×宽度 2 治疗结束时,四只来自 每个队列被处死,石蜡包埋肿瘤切片被染色 苏木精/伊红。 额外的切片在 使用标准程序分级醇,然后根据 按照制造商的说明。 TUNEL阳性细胞百分比为 通过从至少三个细胞中随机计数至少100个细胞来确定 选定字段。 额外的切片用10%的正常山羊血清封闭 湿润室30分钟,然后培养beclin 1或LC3抗体 在4°C下过夜,然后在室内进行60分钟的二次抗体 温度。
shRNA敲除和反转录-聚合酶链 克隆的反应分析。 对于Atg7或SK2的shRNA敲除,A-498细胞以约25%的浓度被接种 在24小时后与适当的病毒颗粒汇合并孵育 存在5μg/ml聚brene。 24小时后,细胞以1:5的比例分裂 通过添加4μg/ml的嘌呤霉素进行筛选。分离后 在耐嘌呤霉素的菌落中,约75%汇合处的细胞 采集用于分析,但仍在选择中。 分离总RNA 转换为cDNA,并评估SK2基因相对于18S的表达 通过使用Bio-Rad(Hercules,CA)MyiQ iCycler仪器的实时PCR。 福沃德 引物为5′-GGAGAAGTGTGAAGATGC-3′(SK2)和 5′-TTGGAGGCAAGTCTGGTG-3′(18S)和反向引物 为5′-GCACAGTGAGTGAGC-3′(SK2)和 5′-CCGCTCCAAGATCCAACTA-3′(18S)。 SK2的相对水平 按照前面所述进行计算( 爱德华兹等人 2000年 ).
统计分析。 采用双向方差分析来评估差异的显著性 在实验组之间。 双方均未成对 t吨 测试和韦尔奇 已更正 t吨 进行测试以访问统计数据 重要性。 差异被认为对 P(P) < 0.05. ABC294640和MG-132之间相互作用的性质或 使用Chou-Talalay方法计算格尔德那霉素,以测定 组合指数( 周和塔拉莱,1984年 ) 使用CalcuSyn软件(密苏里州弗格森市Biosoft)。 基于这种方法, 组合指数值<0.9被视为协同效应,值 >1.1为拮抗值,0.9至1.1被视为 添加剂。
结果 描述ABC294640对细胞凋亡、对照细胞核和 处理后的细胞用PI染色并用流式细胞仪分析( 图1 B) ●●●●。 结果表明,只有一小部分 ABC294640处理的细胞(<1%)含有亚G 1 DNA数量, 即使在有毒药物浓度(>50μM)和长期治疗时 次(72小时)。 DNA片段的缺失表明ABC294640没有 诱导A-498细胞凋亡。 这些结果被缺乏半胱天冬酶所证实 即使在暴露72小时后,ABC294640处理的细胞中仍有3/7的活化( 图1 C) ●●●●。 Annexin-V定量 凋亡/坏死是基于磷脂酰丝氨酸的不对称分布, 在诱导细胞凋亡时,从质膜的细胞质表面翻转到 可与附件五结合的外传单。添加PI 区分坏死或晚期凋亡细胞与早期凋亡细胞。 作为 在中演示 图1 D、 Annexin-V染色 ABC294640处理的细胞毒性浓度(50或90μM)和长 暴露时间(72小时)显示染色细胞数量增加 Annexin-V+PI或PI单独作用(分别为30和16.4%),但只有少数细胞凋亡 细胞被Annexin-V染色,但不被PI染色(90μM时<6%)。 这个 与细胞对PI具有渗透性相一致(因为血浆受损 膜),之前没有激活凋亡机制。 来自所有 三种凋亡检测表明,大多数A-498细胞暴露于ABC294640 死亡时没有显示凋亡的特殊特征。
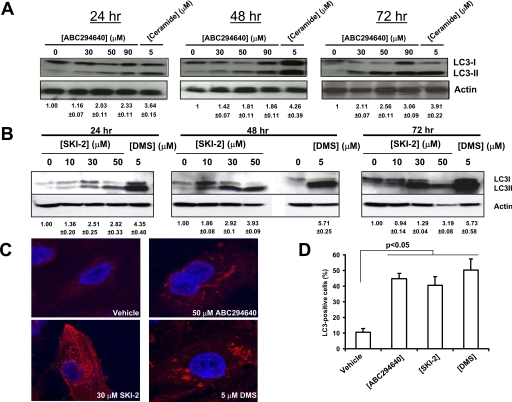
ABC294640处理的A-498细胞缺乏凋亡指标促使我们 调查其他可能导致细胞死亡的过程。 最近的报告显示了角色 自噬和溶酶体在某些癌症诱导的肿瘤细胞死亡中的作用 化学疗法( Lefranc等人,2007年 ; Klonsky等人,2008年 ),所以各种自噬标记 进行了检查。 管蛋白相关蛋白LC3是一种被裂解的细胞溶质蛋白 在诱导自噬后,产生细胞溶质LC3-I(18kDa)和 自噬体相关LC3-II(16kDa)。 我们发现ABC294640引起剂量-和 A-498细胞中LC3的时间依赖性分裂,在 72小时时程( 图2 A) ●●●●。 已知的 自噬诱导鞘脂神经酰胺也促进了快速而显著的分裂 LC3的。 双SK1和SK2抑制剂4-[[4-(4-氯苯基)-2-噻唑基]氨基]苯酚 (SKI-2)和DMS也在24、48或72小时诱导LC3解理( 图2 B) ●●●●。 暴露于任何 三种SK抑制剂显示细胞质中存在点状小点, 表明LC3-II向自噬体募集( 图。 2 C) ●●●●。 暴露于ABC294640、SKI-2或 DMS显示LC3阳性细胞在统计学上显著增加( 图2 D) 。 虽然DMS已知会改变 其他激酶的活性( Igarashi等人。, 1989 ; Megidish等人,1995年 ) 证明LC3裂解和自噬体的形成是由三种 结构不同的SK抑制剂支持自噬是一种常见的假说 对SK药理学抑制的反应,而不是对 ABC294640。
图2。
SK抑制剂对A-498细胞LC3裂解和自噬体形成的影响 细胞。 A、 用指定浓度的ABC294640或5处理细胞 μM神经酰胺用于指定的时间。 LC3-II的产生是 按下述方法进行Western blotting检测 材料和 方法 。通过剥离和重新处理,确认了荷载相等 抗肌动蛋白抗体。 B、 细胞暴露于指示浓度的 SKI-2或5μM DMS,LC3裂解由Western评估 如下文所述,在24、48或72小时对细胞裂解物进行印迹 材料 和方法 C,A-498细胞暴露于载体ABC294640, SKI-2或DMS 48小时,然后如所述对LC3进行固定和免疫染色 在下面 材料和方法 .D,LC3-阳性的量化 细胞。 细胞暴露于50μM ABC294640,30μM SKI-2, 或5μM DMS 48小时。数据表示三个样品的平均值±S.E 实验。 Western blots下面的数字表示相对 LC3-II/肌动蛋白比值与载体处理细胞±S.E.的比较。
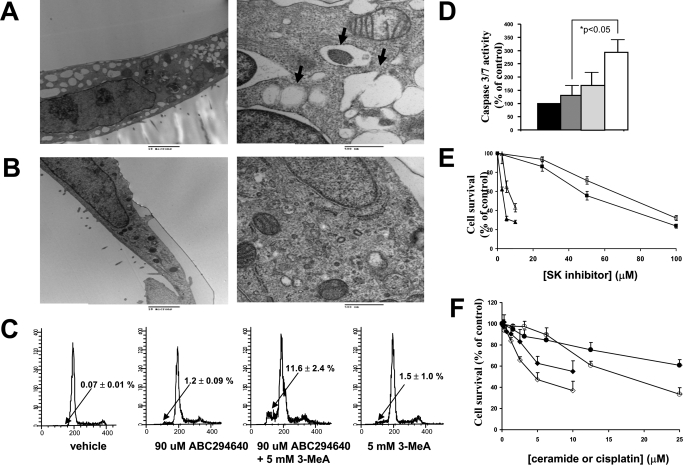
进行电子显微镜检查以进一步证实A-498中的自噬诱导 细胞。 将细胞暴露在50μM ABC294640中24小时,导致 产生许多大的空空泡和含有残余物的自噬空泡 消化物质或完整的细胞器( 图3 A) ●●●●。 与之前的数据一致,没有染色质凝聚或核碎裂 观察到凋亡死亡迹象。 相反,只有少数小的自噬 在载体处理的细胞中观察到液泡( 图。 三 B) ●●●●。
图3。
ABC294640诱导A-498细胞自噬空泡化或凋亡。 A类 和B,用50μM ABC294640(A)或载体(B)处理细胞 24小时后,按照以下说明生成电子显微照片 材料 和方法 低倍下的典型显微照片(左, bar=10μm)或高倍率(右侧,bar=0.5μm) 显示了细胞的超微结构。 箭头表示自噬 液泡。 用ABC294640或3-MeA单独或在 组合72小时,然后处理以分析其DNA含量(C)或 caspase 3/7活性(D)如下所述 材料和 方法 黑色条表示处理过的细胞中caspase 3/7的活性 对于载体,深灰色条表示细胞中caspase 3/7的活性 用90μM ABC294640处理后,浅灰色条代表半胱氨酸天冬氨酸蛋白酶 用5 mM 3-MeA处理的细胞中有3/7的活性,白色条表示 72小时后,用二者处理的细胞中caspase 3/7活性E,A-498细胞 单独使用ABC294640(正方形)或DMS(三角形)处理(填充符号) 或与5 mM 3-MeA(开放符号)联合48小时,细胞存活率为 通过SRB染色进行评估。 F、 A-498野生型单元格(填充符号)或SK2 shRNA-转染的A-498细胞(开放性标志)用顺铂治疗(循环) 或神经酰胺(方格)48小时,并根据标准评估其生存率 SRB分析。
自噬通常是各种有毒侮辱的防御机制( Jin和White,2008年 ). 确定自噬是否 是a-498细胞的一种防御机制,我们试图通过创建一个 Atg7基因的稳定shRNA敲除( Yu等人。, 2004 ). 然而,这导致了致命性,因此没有稳定的克隆可以 证实了自噬在这些肿瘤生存中的重要性 细胞。 因此,我们用III类抑制剂通过药物阻断自噬 磷脂酰肌醇3-激酶(PI3Ks),3-甲基腺嘌呤(3-MeA),如前所述 ( Herman-Antosiewicz等人,2006年 ; Cui等人,2007年 ). A-498细胞暴露于 ABC294640单独或在5 mM 3-MeA存在下,以及DNA含量、半胱天冬酶3/7 测定活性和细胞存活率。 与上述结果一致, ABC294640和3-MeA均未诱导DNA片段化( 图3 C) ●●●●。 然而,ABC294640加3-MeA治疗 这种结合导致了DNA碎片细胞的大量积累。 在 此外,经该组合处理的细胞表达了大量caspase 3/7活性 表明细胞凋亡,而这两种化合物都没有单独引起这种效应( 图3 D) 。 向培养物中添加3-MeA减少 ABC294640和DMS的细胞毒性( 图3 E) , 这表明自噬至少是细胞死亡的部分原因。 添加 针对ABC294640,A-498细胞的3-MeA阻断了LC3-II的生成 (补充图1A),证明3-MeA在抑制自噬方面有效 在这些细胞中。 将ABC294640与 自噬抑制剂氯喹( 阿马拉瓦迪等人。, 2007 )导致两种化合物产生拮抗细胞毒性(数据 未显示)。
为了进一步研究SK2在诱导自噬中的潜在作用,我们创建了 使用慢病毒传递的shRNA从A-498细胞中获得稳定的SK2敲除克隆。 在 与Atg7的研究相比,建立了几个克隆。 然而, 定量检测这些克隆中SK2 mRNA的表达水平 实时PCR表明SK2敲除是可变的和不完整的(补充 图1B),因此没有SK2 mRNA水平低于大约30%对照的克隆 获得细胞。 这与我们使用针对 SK2显示抑制SK2可阻止A-498细胞增殖(未发表 数据)。 部分SK2敲除克隆的水平没有显著增加 LC3-II(补充图1C),表明SK2的部分敲除不会 诱导自噬。 然而,SK2酶的部分敲除使A-498细胞敏化为 以顺铂和神经酰胺为代表的凋亡和自噬诱导剂, 分别( 图3 F) ,表明 ABC294640与其他化疗药物联合使用可能有效。
因为碱性亲脂性化合物可以作为溶酶体促生长剂,因此 对可能的自噬调节剂、溶酶体形态进行评估,以进一步了解 ABC294640诱导自噬的机制。 与对照细胞相比, ABC294640处理24小时后,LysoTracker Red的积累增加 染色和溶酶体增大(“肿胀”) (补充图2)。 量化后 ABC294640处理的细胞为204,而车用处理的细胞则为160 ( 第页 <0.05(两个值),表明溶酶体较高 ABC294640处理的细胞中染料的积累。 酸化加剧 吖啶橙染色证实细胞质细胞器。 吖啶橙进入 细胞的酸性隔室,并被质子化和隔离。 在低pH值下,染料 当被蓝光照射时,会发出红光。 ABC294640处理细胞的染色 吖啶橙显示酸性囊泡的数量和大小增加 细胞器(补充图2)。 相比之下,我们将细胞暴露于神经酰胺或 他莫昔芬,两种已知可诱导癌细胞自噬的分子( Scarlatti等人,2004年 ; Pattingre等人,2008年)。 作为 通过LysoTracker或吖啶橙染色显示,A-498细胞暴露于 他莫昔芬或C6陶瓷表现出类似的溶酶体肿胀,证实两者 三苯氧胺和神经酰胺是溶酶体促生长剂(补充图2、D和E)。 线粒体的MitoTracker绿色染色显示ABC294640处理细胞 积累了正常量的MitoTracker染料,表明这些细胞的线粒体 药物治疗期间细胞保持极化( 普特(Poot et) 1996年 ). 四甲基罗丹明染色证实了这一点 细胞渗透性荧光染料,容易被活性线粒体和 通过流式细胞仪检测,因为ABC294640不影响染料积累(数据不 如图所示)。
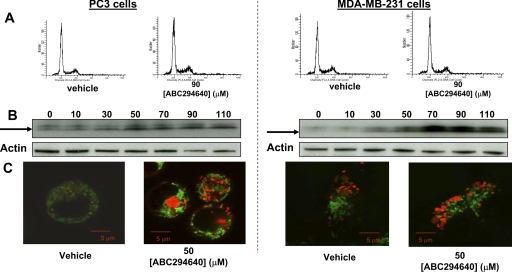
评估ABC294640对自噬(另外两种癌症)影响的一般性 采用前列腺癌(PC-3)和乳腺癌(MDA-MB-231)细胞系。 这些细胞暴露于ABC294640也会导致与之无关的细胞死亡 DNA断裂,即使在高浓度(90μM)和长时间 暴露时间(72小时)( 图4 ). 然而,在这两者中 MDA-MB-231和PC-3细胞ABC294640在24小时时引起LC3的剂量依赖性分裂 胞浆中酸性小室增加。 因此,诱导自噬 ABC294640不仅限于特定的细胞系,而且似乎是一种常见的 肿瘤细胞之间的反应。
图4。
PC-3和MDA-MB-231细胞自噬激活。 A、 PC3细胞(左)或 MDA-MB-231细胞(右)用载体或90μM ABC294640处理 持续72小时。然后将细胞固定在乙醇中,并用PI染色 流式细胞术如下所述 材料和方法 .B、PC3 (左)或MDA-MB-231(右)细胞暴露于指示浓度的 ABC294640(μM)24小时,然后溶解和免疫印迹。 箭头 表示LC3-II。 C、 PC3(左)或MDA-MB-231(右)细胞暴露于50 μM ABC294640 24小时,用MitoTracker绿色和 LysoTracker红色染料,共焦成像如下文所述 材料和方法 .
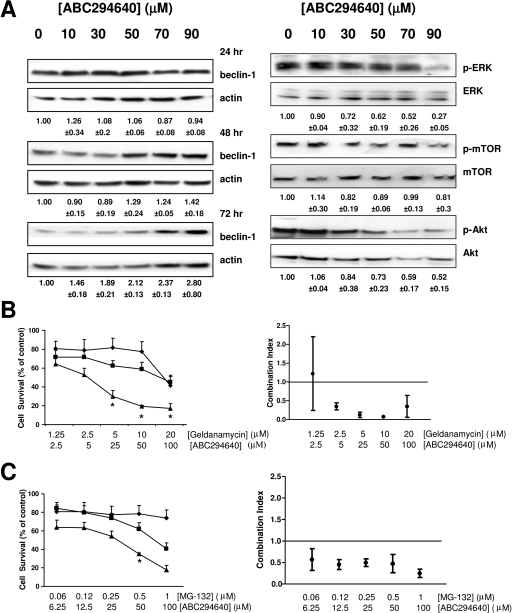
我们还测量了A-498细胞中几种信号和存活蛋白的水平 通过免疫印迹暴露于ABC294640。 beclin 1的表达水平 肿瘤抑制因子和自噬途径中的关键蛋白之一 在48和72小时时随着ABC294640浓度的增加而增加( 图5 A) ●●●●。 MEK/ERK通路在抗肿瘤中的作用 ABC294640的活性通过磷酸化Akt和 用该化合物处理的A-498细胞中的磷酸化ERK。 有趣的是,尽管 Akt和ERK通路可以激活mTOR信号,从而阻断自噬( Meijer和Codogno,2006年 ),ABC294640没有 显著降低磷酸化-mTOR水平。 因此,A-498细胞中的自噬诱导 ABC294640治疗不会引起磷酸化状态的改变 mTOR,但与beclin 1上调有关。
图5。
ABC294640对信号通路的影响及ABC294640的联合作用 用格尔德霉素或MG-132。 A、 细胞暴露于指示浓度 ABC294640进行48 h,用SDS-PAGE进行分级,并探测指示的 蛋白质的Western blotting,如下所述 材料和 方法 也显示了Beclin 1在24和72小时的表达。 数字 下面的蛋白质印迹表明磷酸化蛋白/总蛋白 与载体处理细胞的蛋白质比率±标准 与处理过的车辆相比,相对beclin-1/actin比率的误差 单元格±标准误差。 B和C,A-498细胞暴露于 仅显示ABC294640(灰色条)、格尔德霉素(B,白色 条)、MG-132(C,白色条)或ABC294640和格尔德霉素的组合或 MG-132(黑条),72小时后通过SRB试验评估存活率。 CalcuSyn为各个组合计算的组合指数(CI) 如右图所示。 CI值介于0和1之间表示协同作用,CI 大于1的值表示对抗。 强大的协同作用由接近的值表示 到0.*, 第页 < 0.05.
抗癌化疗通常是由不同药物的联合用药 具体时间表。 基于自噬细胞死亡的发现 ABC294640,并且知道一些错误折叠的蛋白质被自噬降解( 丁和尹,2008 ),我们假设药物 诱导未展开的蛋白质反应,例如蛋白酶体抑制剂(例如MG-132)或 热休克蛋白90抑制剂(如格尔德霉素)可能影响 ABC294640。因此,A-498细胞暴露于ABC29464+格尔德霉素或MG-132 不同药物-药物比例的组合。 细胞存活部分 药物治疗72小时后测定人群( 图。 5 、B和C)。 对组合指数(CalcuSyn)的分析证实 ABC294640和格尔德霉素的组合具有协同细胞毒性,即 组合指数<1.0( 图5 B) ●●●●。 同样,ABC294640和MG-132的组合也具有协同毒性( 图5 C) ●●●●。
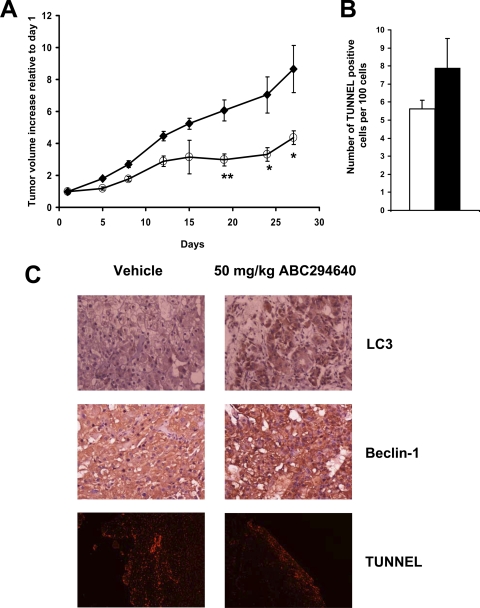
为了进一步研究ABC294640的体内抗肿瘤特性,我们使用了SCID载体 A-498细胞的异种移植。 如所示 图6 A、, 每天服用50 mg/kg ABC294640导致 治疗4周后肿瘤生长。 28天后,切除肿瘤组织, 固定切片,并对玻片进行免疫染色,以评估beclin 1和 LC3和TUNEL染色以确定凋亡细胞的数量( 图6 B) ●●●●。 如所示 图6 C、 beclin 1和LC3的染色强度在 暴露于ABC294640的小鼠的肿瘤与使用汽车治疗的小鼠相比 老鼠。 相反,在 ABC494640和车用治疗肿瘤( 图6 ,B 和C,底部),表明细胞凋亡的增加不是 本模型中肿瘤在体内生长的延迟。 这些数据与 体外观察到自噬诱导和非凋亡细胞死亡。
图6。
ABC294640对小鼠肿瘤生长的影响及其组织学特征 ABC294640治疗肿瘤。 A、 雌性SCID小鼠( n个 =每组8个) 将悬浮在PBS中的A-498细胞皮下注射 肿瘤形成后,每天用0 ( ♦) 或50 mg/kg ABC294640(○)。数值代表平均值 ±S.E.肿瘤体积标准化至每只小鼠治疗第1天。*, 第页 < 0.05; **, 第页 < 0.01. 治疗开始后第27天处死小鼠 用福尔马林固定,肿瘤切片进行TUNEL染色 LC3和beclin 1的免疫染色如下所述 材料和 方法 .B,TUNEL阳性细胞的定量。 黑色条 代表车辆治疗的肿瘤,白色条代表ABC294640治疗的肿瘤 肿瘤。 数据代表三个实验的平均值±S.E。 C、, ABC294640治疗肿瘤的组织学特征。
讨论 S1P在细胞生长和肿瘤发展中的广泛参与促使我们 开发几种具有体内外活性的小分子SK抑制剂 ( French等人,2003年 , 2006 ; 缅因州等,2006年 , 2008 ; 史密斯等人 al.,2008年 ). 开发了一种当前的SK2铅抑制剂ABC294640,以改善 口服生物利用度和酶的特异性阻碍了其他药物的开发 类脂质SK抑制剂( French等人。, 2010 ). 我们之前已经证明ABC294640在 活体( 缅因州等,2006年 , 2008 ; Smith等人,2008年 )和 在本研究中,它也具有抗肿瘤活性( 图。 6 ). ABC294640的药代动力学研究表明,该化合物达到 口服剂量为50μM后,血浆峰值浓度约为20μM mg/kg,清除半衰期约为4.5小时( French等人,2010年 ),这意味着更多 更高剂量和/或更频繁地使用可以获得显著的抗肿瘤效果 管理。 ABC294640目前处于经认证的良好实验室规范毒理学领域 并有望在2010年进入临床试验。 这里展示的工作是 首次详细研究ABC294640在人类肿瘤细胞中的抗肿瘤特性 在体外和体内。 出乎意料的是,我们发现肿瘤细胞暴露在这种药物下 诱导自噬,这可能导致非凋亡细胞死亡。
自噬杀死癌细胞的确切机制尚未确定。 然而,很可能是细胞自噬降解的长期激活 组分,例如负责细胞代谢的关键蛋白质和细胞器 (可能)凋亡,最终将细胞推到恢复点以外 非流行性死亡( 图7 ). 这与 提出了蛋白酶体抑制抗癌药物如Velcade的作用机制。 在暴露于ABC294640的A-498细胞中,我们观察到促存活MAPK的下调 尽管 细胞保存在完全培养基中。 然而,只有一小部分细胞 能够激活凋亡途径,除非通过添加 3-甲基丙烯酸甲酯。 因此,自噬似乎是细胞死亡的主要机制 ABC294640治疗肿瘤细胞。
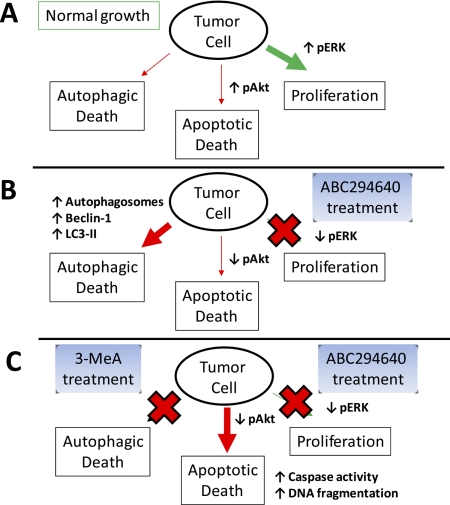
图7。
ABC294640对肿瘤细胞死亡的反应模型。 A、 正常生长下 条件下,MAPK和Akt通路激活,导致高细胞 增殖和低凋亡。 有一个基本水平的自噬来提供 代谢产物支持细胞的快速增殖和能量需求。 B、, 暴露于ABC294640后,MAPK和Akt通路下调,从而 抑制增殖,减弱对凋亡的限制。 同时,ABC294640诱导神经酰胺的产生(通过抑制SK) 加速自噬(表现为自噬体生成增加) 不可持续点,导致自噬死亡。 C、 在3-MeA在场的情况下, 自噬被阻断,导致肿瘤细胞凋亡 DNA断裂和半胱氨酸天冬氨酸蛋白酶激活。
控制肿瘤细胞命运的因素包括受体、酶(如SK1/2)和 转录因子,所有这些都被连接成复杂且通常是冗余的 信令网络。 临床肿瘤学的当前方法是使用 多种药物来避免这种冗余。 这其中的一个主要缺点 方法是需要同时使用多个dug,这可能导致累积 毒性( Hu和Xuan,2008年 ). 一种有效的方法 克服这个障碍是激活可导致肿瘤细胞的替代过程 死亡。 在肿瘤细胞死亡的研究中,细胞凋亡受到了最大的关注,但 很明显,可以通过其他机制去除癌细胞。 一个 尚待研究的途径是自噬,这是一种进化上保守的过程,允许细胞自噬 在营养缺乏的压力下生存。 在自噬过程中 细胞质和细胞器被双膜泡状结构吞噬,称为 自噬体。 这些小泡随后与溶酶体融合,其内容物被降解 通过溶酶体水解酶。 越来越多的证据表明自噬 在一些抗癌药物治疗后被激活,但它对细胞的贡献 死亡和/或抗癌药物耐药性尚不清楚( Lefranc等人,2007年 ; Wang等人。, 2008 ). 最近,一种小分子选择性地靶向von Hippel-Lindau 肿瘤抑制基因缺失的肾细胞癌被证明可以杀死肿瘤细胞 仅通过激活自噬,证明这种机制可以导致 导致肿瘤细胞死亡( Turcotte等人,2008年 ). 凋亡和自噬之间存在相互作用,因为自噬经常被阻断 促进细胞凋亡( Thorburn,2008年 ).
自噬的启动和自噬体的伸长涉及 几种蛋白质,包括支架蛋白beclin 1和 与自噬体相关的LC3-II。 一些信号蛋白对此进行调节 过程。 例如,mTOR信令网络接收来自生长因子的输入 通过I类PI3K信号通路的受体。 PI3K/Akt/mTOR和MEK/ERK 当激活时,这些通路抑制自噬。 在A-498细胞中,用 ABC294640,我们观察到磷酸化Akt和磷酸化ERK1/2水平降低,但没有 mTOR磷酸化状态的改变,表明自噬是由 ABC294640不需要降低磷酸化-mTOR水平。 与中的报告相比 其他系统( Cheng等人,2007年 ),我们没有发现 自噬(和凋亡)抑制剂Bcl-2水平的变化(数据未显示), 结合并抑制beclin 1。 另一方面,beclin 1的上调 暴露于ABC294640的A-498细胞在72小时时观察到蛋白质水平 人结肠癌HT-29细胞beclin 1表达上调 接触C6陶瓷后的自噬( 斯卡拉蒂等人 al.,2004年 ). 我们假设beclin 1的上调对于 ABC294640诱导的长时间自噬。 翻译成动物模型, 每天服用ABC294640导致皮下生长延迟 肾癌细胞的异种移植。 beclin 1和LC3上调,缺乏 肿瘤的免疫染色也发现了细胞凋亡(通过TUNEL分析测定) 组织。 这些结果可能表明自噬的诱导而不是 体内细胞凋亡的增加在延缓肿瘤生长中起着重要作用。
选择A-498肾癌细胞作为生化和 细胞研究,因为肾脏中SK2酶的表达相对较高( Taha等人,2006年 ). 此外,肾癌 临床上特别难以治疗。 因此,了解 SK抑制剂可以激活这些细胞中的哪些死亡机制 它们作为潜在的肾癌药物的进一步发展。 本研究还代表 肾癌细胞自噬的首次报道。 重要的是,机械 这一发现扩展到了其他癌症细胞系,因为MDA-MB-231和PC-3的暴露 ABC294640的细胞不会激活凋亡,而是导致细胞分裂 LC3蛋白和细胞内隔间酸化,表明其普遍存在 促进肿瘤细胞自噬的能力。 此外,我们观察到LC3裂解和 暴露于其他结构分化SK的A-498细胞中自噬体的形成 抑制剂(DMS和SKI-2),表明其他SK抑制剂也诱导自噬, 尽管对于这两种化合物,SK1和SK2的作用无法区分。
作为其临床前开发的一个组成部分,我们还测试了 ABC294640与其他抗癌药物在细胞培养中。 我们发现两种化合物 激活未折叠蛋白反应MG-132和格尔德霉素,协同提高 ABC294640在细胞培养中的细胞毒性。 这些发现对于 为未来临床前和临床研究设计抗癌药物组合, 特别是,建议可能使用ABC294640治疗多发性硬化症 骨髓瘤。 其他研究表明,与信号抑制剂联合使用具有疗效 和抗代谢物(未发表的工作),为广泛抗肿瘤提供了有力的证据 ABC294640的活性。 其促进自噬能力的当前证明 肿瘤细胞强调需要在研究中考虑这种经常被忽视的反应 抗癌药物。
致谢 我们感谢Victoria Findlay博士和David Turner博士在细胞免疫染色方面的帮助 批判性阅读手稿; 细胞与分子的文卡特·拉姆谢什博士 成像核心帮助进行共焦成像实验; Rick Peppler寻求流动帮助 细胞术实验; Margaret Romano准备组织切片; 彭高(音译) 帮助进行逆转录–PCR; 和其他史密斯实验室成员 评论和建议。
这项工作得到了国家健康研究所(Grant R01-CA122226])的支持(至 C.D.S.)。 Hollings癌症中心的成像核心由National支持 卫生研究院【CA138313-01拨款】(致安德鲁·卡夫特博士)。
缩写:
库存1 鞘氨醇激酶-1
库存2 鞘氨醇激酶-2
3-甲基丙烯酸甲酯 3-甲基腺嘌呤
ABC294640型 3-(4-氯苯基)-金刚烷-1-羧酸 (吡啶-4-基甲基)酰胺
DMS系统 二甲基鞘氨醇; LC3; 微管蛋白相关蛋白轻链3
圆周率 碘化丙锭
shRNA 短发夹RNA
滑雪-2 4-[[4-(4-氯苯基)-2-噻唑基]氨基]苯酚
第1阶段 1-磷酸鞘氨醇
SRB公司 硫罗丹明B
隧道 末端脱氧核苷酸转移酶介导的dUTP缺口末端标记
MG-132型
N个- (苄氧羰基)亮氨酸亮氨酸 Z轴 -亮氨酸-亮氨酸-丙氨酸
SCID公司 严重联合免疫缺陷
mTOR公司 雷帕霉素的哺乳动物靶点
甲乙酮 丝裂原活化蛋白激酶
ERK公司 细胞外信号调节激酶
第PAGE页 聚丙烯酰胺凝胶电泳
美国公共广播电视公司 磷酸盐缓冲盐水
聚合酶链反应 聚合酶链反应
MAPK公司 丝裂原活化蛋白激酶
PI3K系列 磷脂酰肌醇3-激酶
CI公司 组合指数。
工具书类
Amaravadi RK、Yu D、Lum JJ、Bui T、Christophorou MA、Evan GI、Thomas-Tikhonenko A、Thompson CB。 (2007)自噬抑制增强 Myc诱导的治疗性细胞凋亡模型 淋巴瘤。 临床杂志 投资117:326–336 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Bursch W,Ellinger A,Gerner C,Frohwein U,Schulte-Hermann R.(2000)程序性细胞死亡(PCD)。 凋亡、自噬性PCD或其他? Ann NY学院 科学926:1-12 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Cheng TJ、Wang YJ、Kao WW、Chen RJ、Ho YS。 (2007)砷防护 硫辛酸诱导U118人脑胶质瘤细胞自噬死亡 酸性。 食品化学 毒理学45:1027–1038 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Chou TC,Talalay P.(1984)定量分析 剂量-效应关系:多种药物或 酶抑制剂。 高级酶 雷古尔22:27–55 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Cui Q,Tashiro S,Onodera S,Minami M,Ikejima T.(2007)自噬先于细胞凋亡 冬凌草甲素治疗人乳腺癌MCF-7细胞。 生物 药牛30:859–864 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Cuvillier O.(2007)鞘氨醇激酶-1:一种潜在的 癌症的治疗靶点。 抗癌药物 药物18:105–110 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Delgado A,Casas J,Llebaria A,Abad JL,Fabrias G.(2006)鞘脂抑制剂 代谢酶。 Biochim生物物理学 《学报》1758:1957–1977 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
丁文轩,尹XM。 (2008)分类、识别和 通过大分子自噬激活错误折叠的蛋白质降解途径 和 蛋白酶体。 自噬4:141–150 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Edwards PA、Tabor D、Kast HR、Venkateswaran A.(2000)基因表达的调节 SREBP和SCAP。 Biochim生物物理学 学报1529:103–113 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
French KJ、Schrecengost RS、Lee BD、庄Y、史密斯SN、Eberly JL、Yun JK、史密斯CD。(2003)发现和评估 人鞘氨醇激酶抑制剂。 癌症 决议63:5962–5969 [ 公共医学 ] [ 谷歌学者 ]
French KJ,Upson JJ,Keller SN,庄Y,Yun JK,Smith CD.(2006)鞘氨醇的抗肿瘤活性 激酶抑制剂。 药理学实验杂志 治疗318:596–603 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
French KJ、Zhuang Y、Maines LW、Gao P、Wang W、Beljanski V、Upson JJ、Green CL、Keller SN、Smith CD。(2010)药理学和抗肿瘤 鞘氨醇选择性抑制剂ABC294640的活性 激酶-2。 药理学实验杂志 治疗方法: 10.124/jpet.109.163444 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Fulda S.(2009)肿瘤抵抗 细胞凋亡。 国际J 癌症124:511–515 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Herman-Antosiewicz A,Johnson DE,Singh SV.(2006)萝卜硫烷导致自噬 抑制细胞色素释放 C类 与前列腺细胞凋亡 癌细胞。 癌症 决议66:5828–5835 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
胡旭,宣瑜(2008)绕过癌症耐药性 通过激活多种死亡途径:规避研究的建议 细胞凋亡诱导的肿瘤耐药性。 癌症 信件259:127–137 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Igarashi Y、Hakomori S、Toyokuni T、Dean B、Fujita S、Sugimoto M、Ogawa T、el Ghendy K、Racker E(1989)化学定义的影响 鞘氨醇及其 N个 -蛋白激酶C上的甲基衍生物和 Src激酶 活动。 生物化学28:6796–6800 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Jin S,White E.(2008)自噬抑制肿瘤 通过代谢管理 强调。 自噬4:563–566 [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Klonsky DJ、Abeliovich H、Agostinis P、Agrawal DK、Aliev G、Askew DS、Baba M、Baehrecke EH、Bahr BA、Ballabio A等(2008)使用指南 高等动物自噬检测方法的解释 真核生物。 自噬4:151–175 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
昆都M,汤普森CB。 (2008)自噬:基本原理和 与疾病的相关性。 年度版次 病态3:427–455 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Lavieu G、Scarlatti F、Sala G、Carpentier S、Levade T、Ghidoni R、Botti J、Codogno P(2006)《自噬的调节 鞘氨醇激酶1及其在营养期间细胞存活中的作用 饥饿。 生物杂志 化学281:8518–8527 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Lavieu G、Scarlatti F、Sala G、Carpentier S、Levade T、Ghidoni R、Botti J、Codogno P.(2008)《西班牙鞘磷脂》 宏观自噬。 方法摩尔 生物学445:159–173 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Lefranc F,Facchini V,Kiss R.(2007)自噬前药物:一种新方法 对抗抗凋亡癌症,特别强调 胶质母细胞瘤。 肿瘤学家12:1395–1403 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Maines LW、Fitzpatrick LR、French KJ、庄Y、夏Z、Keller SN、Upson JJ、Smith CD。(2008)《溃疡性结肠炎的抑制》 小鼠口服鞘氨醇抑制剂 激酶。 挖掘Dis 科学53:997–1012 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Maines LW、French KJ、Wolpert EB、Antonetti DA、Smith CD。(2006) 视网膜内皮细胞鞘氨醇激酶与血管生成的关系 眼部疾病。 投资眼科视力 科学47:5022–5031 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Megidish T,White T,Takio K,Titani K,Igarashi Y,Hakomori S.(1995)信号调节蛋白 14-3-3是鞘氨醇或 N个 , N个 -二甲基鞘氨醇依赖激酶 3T3(A31)电池。 生物化学生物物理研究 社区216:739–747 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Meijer AJ,Codogno P.(2006)信号和自噬调节 健康、衰老和疾病。 分子方面 医学27:411–425 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Pattinger S、Bauvy C、Carpentier S、Levade T、Levine B、Codogno P(2009)JNK1-依赖型Bcl-2的作用 神经酰胺诱导的大自噬中的磷酸化。 生物杂志 化学284:2719–2728 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Poot M,Zhang YZ,Kramer JA,Wells KS,Jones LJ,Hanzel DK,Lugade AG,Singer VL,Haugland RP(1996)线粒体分析 新型固定荧光的形态和功能 污渍。 J组织化学 细胞化学44:1363–1372 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Raval J、Lyman S、Nitta T、Mohuczy D、Lemasters JJ、Kim JS、Behrns KE。(2006)基础活性氧物种 肝硬化患者细胞凋亡易感性的测定 肝细胞。 自由基生物 医学41:1645–1654 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Ricci理学硕士,Zong WX。 (2006)化疗方法 靶向细胞死亡 路径。 肿瘤学家11:342–357 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Scarlatti F、Bauvy C、Ventruti A、Sala G、Cluzeaud F、Vandewalle A、Ghidoni R、Codogno P(2004)神经酰胺介导的大自噬 包括蛋白激酶B的抑制和beclin的上调 1.生物学杂志 化学279:18384–18391 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Skehan P、Storeng R、Scudiero D、Monks A、McMahon J、Vistica D、Warren JT、Bokesch H、Kenney S、Boyd MR(1990)《新比色细胞毒性》 抗癌药物筛选试验。 《国家癌症杂志》 仪器82:1107–1112 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Smith CD、French KJ、Zhuang Y.(2008)发明家; 远地点生物技术 公司、受让人。 鞘氨醇激酶抑制剂 美国专利7338961 2008年3月4日
Taha TA、Hannun YA、Obeid LM。 (2006)鞘氨醇激酶:生化 以及细胞调节和在疾病中的作用。 生物化学分子杂志 生物39:113–131 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Taha TA、Osta W、Kozhaya L、Bielawski J、Johnson KR、Gilladers WE、Dbaibo GS、Hannun YA、Obeid LM。 (2004)鞘氨醇下调 激酶-1通过DNA损伤:依赖蛋白酶和p53。 J型 生物 化学279:20546–20554 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Thorburn A.(2008)细胞凋亡和自噬: 两种可能不同的监管联系 过程。 细胞凋亡13:1–9 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Turcotte S、Chan DA、Sutphin PD、Hay MP、Denny WA、Giaccia AJ。 (2008)靶向缺乏VHL的分子 诱导自噬的肾细胞癌。 癌症 细胞14:90–102 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Wang M、Tan W、Zhou J、Leow J、Go M、Lee HS、Casey PJ。 (2008)一种小分子抑制剂 异丙基半胱氨酸羧甲基转移酶诱导PC3自噬细胞死亡 前列腺癌细胞。 生物杂志 化学283:18678–18684 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Wymann MP,Schneiter R.(2008)脂质信号转导 疾病。 Nat Rev Mol电池 生物学9:162–176 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Yu L、Alva A、Su H、Dutt P、Freundt E、Welsh S、Baehrecke EH、Lenardo MJ。 (2004)ATG7-beclin 1法规 自噬细胞死亡程序 半胱氨酸天冬氨酸蛋白酶-8。 科学304:1500–1502 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
关联数据 本节收集本文中包含的任何数据引用、数据可用性声明或补充材料。
《药理学和实验治疗学杂志》的文章由提供 美国药理学和实验治疗学会