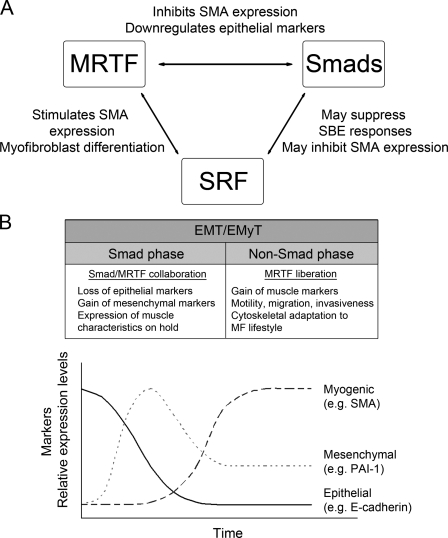
Smad3抑制平滑肌肌动蛋白启动子的激活,并在上皮细胞中作为肌源性编程的计时器。
摘要 上皮-肌成纤维细胞(MF)转变(EMyT)是器官纤维化的关键过程,导致上皮中α-平滑肌肌动蛋白(SMA)表达。 这种肌源性程序激活的机制尚不清楚。 我们之前已经证明,细胞间接触损伤和转化生长因子β(TGF-β)对SMA表达是不可或缺的(二次打击模型),接触破坏会导致心肌相关转录因子(MRTF)的核移位。 由于SMA启动子同时含有MRTF反应性CC(A/T)富GG元件(CArG)盒和TGF-β反应性Smad-binding元件,我们假设肌源性程序是通过MRTF和Smad3之间的协同作用而启动的。 在本研究中,我们表明损伤与TGF-β之间的协同作用只需要CArG元素。 令人惊讶的是,Smad3抑制了由MRTF驱动的SMA启动子的激活,而Smad3沉默造成的损伤足以诱导SMA表达。 此外,Smad3在两次撞击条件下降解,从而释放肌生成程序。 因此,Smad3是上皮细胞MF承诺的关键计时器/延迟层,EMyT可被分解为Smad3促发(间充质)和Smad3抑制(肌源)期。
介绍 上皮-间充质转化(EMT)是一种主要的表型改变,其特征是上皮特征丧失,包括顶基极性和细胞间接触,间充质特性增加,如头尾极性、收缩性增加和细胞外基质蛋白积累( Lee等人,2006年 ; Xu等人,2009年 ). EMT在胚胎发育和伤口愈合中起着关键的生理作用( Nakaya和Sheng,2008年 )并被确定为包括致癌在内的各种病理过程的中心机制( Klymkowsky和Savagner,2009年 )和组织纤维化( Kallui和Neilson,2003年 ). 重要的是,EMT可以沿着成肌程序进一步进展,导致肌成纤维细胞(MFs)的生成,其特征是α-平滑肌肌动蛋白(SMA)的表达。 在本研究中,我们将使用上皮-MF转化(EMyT)这一术语来表示EMT的肌源性形式。 MFs的组织积累和SMA的表达水平与纤维化的严重程度密切相关( Yang和Liu,2001年 ). 此外,对基因标记小鼠的研究表明,在各种肺和肾纤维化模型中,MFs的大部分来源于上皮细胞,这表明EMyT在疾病过程中起着重要作用( Iwano等人,2002年 ; Kim等人,2006年 ). 尽管EMyT在纤维化病理学中具有关键意义,但上皮细胞中启动和调节肌生成程序(SMA表达)的分子机制尚不完全清楚。
越来越多的证据表明,EMT是多个同时输入的结果( Masszi等人,2004年 ; Kim等人,2009年a , b条 ). 我们之前旨在鉴定关键触发因子的实验表明,细胞间接触的损伤(例如,它们被低钙介质[LCM]解偶联或损伤)和TGF-β1(TGF-β)都是诱导肾上皮细胞中SMA表达所必需的( Masszi等人,2004年 ). 因此,这些数据定义了EMyT的双命中模型,该模型特别适用于剖析MF分化背后的关键细胞事件。 然后,我们探讨了接触性损伤影响SMA表达的机制,并确定了心肌相关转录因子(MRTF),一种最近描述的肌源性转录辅激活因子( Wang等人,2002年 ),作为该过程的关键调解人( Fan等人,2007年 ; Sebe等人,2008年 ). SMA启动子的近端包含两个富含CC(A/T)的GG元件(CArG)盒,它们是细胞生长和肌源性分化的主要调节因子血清反应因子(SRF)靶向的顺式元件( Hautmann等人,1999年 ; Miano等人,2007年 ). 心肌蛋白家族的最新发现(心肌蛋白、MRTF-A和-B; Wang等人,2001年 ; Miralles等人,2003年 )解释了SRF如何发挥这些单独的作用(促进生长和肌生成)的古老谜团:心肌蛋白的结合赋予肌肉特异性并增强SRF的活性。 此外,MRTF是细胞骨架基因的主要诱导剂,其本身受细胞骨架的调节。 根据目前的模型,在静止的细胞中,MRTF在胞浆中与G-actin结合,但在肌动蛋白聚合后,它与G-action分离并转移到细胞核( Posern和Treisman,2006年 ). 我们和其他人观察到,上皮单层中细胞接触的解体(例如通过LCM)以Rho/Rho激酶和Rac依赖性的方式激发MRTF的强大核移位( Fan等人,2007年 ; Busche等人,2008年 ; Sebe等人,2008年 ). 重要的是,MRTF对于EMyT期间SMA的表达是必要的( Fan等人,2007年 ; Elberg等人,2008年 ). 然而,仅损伤诱导的MRTF易位不足以表达SMA,因为该过程还需要TGF-β。
TGF-β协同接触性损伤诱导肌源性重编程的机制是什么? 我们认为,通过受体Smads(R-Smads)的信号传递,即激活的TGF-β受体激酶的直接靶点,可能解释了这种协同作用。这个想法来源于以下事实:( Xu等人,2009年 ),(b)SMA启动子含有Smad-binding元件(SBE),该元件特异性结合Smad3( 胡等,2003 ),和(c)Smad3已被证明直接绑定到MRTF( Morita等人,2007a ). 认识到这种情况,我们假设MRTF易位和Smad3信号传导代表了两次打击方案中的接触性损伤和TGF-β依赖性臂。 我们认为MRTF和Smad3独立地靶向SMA启动子中的同源顺式元件,但它们的作用可能不仅仅是相加作用。 或者,Smad3可能直接与MRTF结合,复合物通过CArG或SBE协同驱动启动子。 我们还询问TGF-β信号转导是否改变MRTF的核质交通。
令人惊讶的是,我们发现CArG盒对于SMA启动子激活中接触性损伤和TGF-β之间的协同作用是必要的和充分的,Smad3是MRTF驱动的SMA表达的强烈抑制剂,并且Smad3在EMyT期间降解。 这些结果提示了肌源性重编程的一种新的调控机制,并定义了EMyT中Smad3促发期和Smad3抑制期。
结果 MRTF在EMyT过程中的细胞骨架重编程中起着关键作用 我们以前的研究已经证实,小管细胞EMyT需要细胞间接触的中断(通过LCM)和TGF-β的暴露。 为了确定MRTF在这种双命中模型中SMA表达中的重要性,我们用对照或MRTF特异性siRNA转染细胞,并用LCM和TGF-β同时处理细胞48小时。我们使用了两种特异性siRNA构建物,这两种构建物都能近完全敲除MRTF( 图1 A 和 图S1 ). 如预期( Masszi等人,2004年 )在存在非相关(NR)siRNA的情况下,联合治疗诱导了SMA的稳健表达。 MRTF siRNAs消除了这种反应。 为了评估观察到的抑制作用是否仅限于SMA表达或其他含有CArG盒的基因也可能受到影响,我们检查了CArGome的一些重要代表的命运( Sun等人,2006年 ). 与SMA类似,EMyT期间丝蛋白、SRF、肌球蛋白重链以及少量的CapZ和α1-整合素上调,并且这些反应受到MRTF抑制的强烈抑制( 图1 A 和图S1)。 在休息和刺激条件下,MRTF的下调强烈降低了cofilin的表达。 这些发现表明,MRTF是肌动蛋白骨架相关基因的主调节器,因此是EMyT期间细胞骨架重编程的主调控器。
图1。
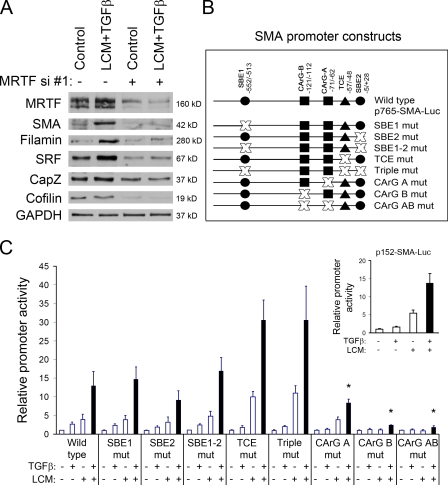
MRTF是EMyT中CArG依赖基因的关键转录因子。 (A) 将转染NR(−)或MRTF siRNA(+)24 h的融合LLC-PK1细胞血清去除3 h,用正常培养基(对照)或LCM与10 ng/ml TGF-β(LCM+TGF-。 (B) 应用SMA启动子荧光素酶构建物。 (C) CArG盒是关键的,而真正的TGF-β反应元件对于个体刺激及其对SMA启动子的协同作用的影响是不可或缺的。 用所示的SMA构建物和肾小球荧光素酶pRL-TK质粒转染近融合单层细胞24小时,然后未经处理或暴露于LCM、TGF-β或这些组合(黑柱)下24小时。(插图)激活仅包含CArGs和TCE的152-bp SMA启动子。 对照组的萤火虫/肾小球比率取1。 误差线表示平均值±SEM。
两个输入的刺激效应在CArG盒上收敛 接下来,我们试图确定负责LCM效应、TGF-β及其协同作用的关键启动子元件。SMA启动子的近端包含几个调控元件,包括两个CArG盒、两个SBE和一个TGF-?控制元件(TCE; 图1B ). 正如我们和其他人进行的早期研究所表明的那样,LCM激活Rho途径( Fan等人,2007年 ; Busche等人,2008年 ),我们假设LCM可能主要通过CArG盒发挥作用,而TGF-β的作用可能主要由SBE和/或TCE介导。为了表征这些元素的重要性,我们生成了一组荧光素酶报告子结构,其中含有SMA启动子的各种突变( 图1B ). 用野生型(WT)或突变型SMA启动子质粒以及内部对照质粒pRL-TK转染细胞,并用TGF-β和/或LCM处理24 h( 图1 C ). 与我们之前的结果一致( Masszi等人,2004年 ; Fan等人,2007年 )TGF-β和接触性损伤均诱导启动子活性适度增加(分别为2.6倍和4倍),而联合治疗协同作用(13倍)。 首先,我们研究了真正的TGF-β反应区域,即两个SBE和TCE位点的作用。 有趣的是,这些元素单独或联合失活突变既不会抑制单独治疗的效果,也不会影响它们的协同作用。此外,当细胞受到LCM或联合治疗的攻击时,TCE中含有突变的启动子结构表现出明显高于WT的激活。 相反,CArG位点的失活大大降低了所有处理的效果。 CArG-A盒的突变具有强烈但不完全的抑制作用,而CArG-B和双突变体对LCM、TGF-β或其组合完全无反应( 图1 C ). 短的152-bp启动子片段包含两个完整的CArG盒,但缺少SBE1和E盒,对这两种刺激仍然敏感( 图1 C ,插图)。 总之,这些发现表明,CArG盒不仅对接触性损伤(Rho/Rho激酶介导; Fan等人,2007年 ; Sebe等人,2008年 )启动子的激活以及TGF-β触发的反应和这些刺激之间的协同作用。 相反,所有真正的TGF-β元素(SBE和TCE)都是可有可无的。
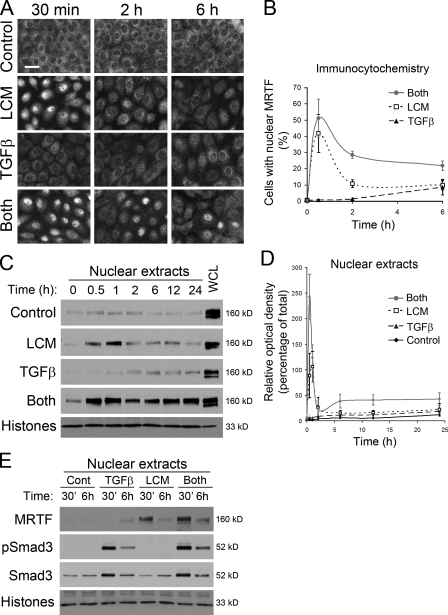
TGF-β延长损伤诱导的MRTF核蓄积 鉴于两次点击的影响在CArG盒上收敛,我们希望确定这些刺激如何影响MRTF的核质转运。 我们问他们的协同作用是否可以用他们对MRTF定位的协同作用来解释。 为了解决这个问题,我们使用了免疫荧光显微镜( 图2,A和B )核提取物的免疫印迹( 图2、C和D ). 这两种方法得到了相似的结果:在未经处理的完整融合单层细胞中,MRTF是细胞溶质。 单用LCM可诱导MRTF快速(30分钟)和强劲的核移位( 图2 ). 然而,这种反应是短暂的,因为在2小时时,核MRTF的细胞数量显著减少( 图2,A和B )以及核MRTF总含量( 图2、C和D ). 此后,MRTF保持在这个略高于基底层的水平。 仅TGF-β在最初2 h内未诱导任何MRTF易位,即使在6 h后,也仅在小部分细胞(~10%)中引起中度易位。 这与我们之前的数据一致,即TGF-β本身无法诱导融合单层中SMA的表达( Fan等人,2007年 ). 重要的是,TGF-β诱导MRTF易位的无能并非由一般无反应性引起:TGF-( 图2 E ). 此外,当TGF-β与LCM一起添加时,具有强核MRTF易位的细胞数量和总核MRTF含量均高于LCM刺激后的峰值,重要的是,在研究期间(24小时),其显著高于LCM诱导的水平。 值得注意的是,当与LCM联合使用时,TGF-β显著促进了核MRTF的积累,即使在单独使用时也没有效果。 这些结果表明,尽管TGF-β对完整上皮中诱导MRTF易位的刺激非常微弱,但它增加并延长了接触性损伤引起的MRTF核蓄积。 这种效应可能有助于组合刺激和随后的EMyT之间的协同作用。
图2。
TGF-β增强并延长损伤诱导的MRTF核蓄积。 (A) 将汇合单层暴露在指示的刺激物下不同时间,进行MRTF染色,并通过免疫荧光显微镜观察。 棒材,30µm。 (B) 图像被量化为MRTF核聚集清晰的细胞百分比。 (C) 从如图所示处理的细胞中制备细胞核提取物。 通过Western blotting从含有等量(5µg)蛋白质的提取物中观察核MRTF。 组蛋白验证了等负荷(显示为LCM条件)。 WCL,全细胞裂解物。 (D) C的密度定量。值是相对于在同一膜上负载的5µg WCL(100%)中的MRTF信号密度表示的( n个 ≥ 3). (E) TGF-β诱导融合LLC-PK1细胞中Smad3的早期和稳健的核移位和磷酸化。 从如图所示处理的细胞中制备核提取物,并用总抗体和磷酸-Smad3抗体进行探测。 误差线表示平均值±SEM。
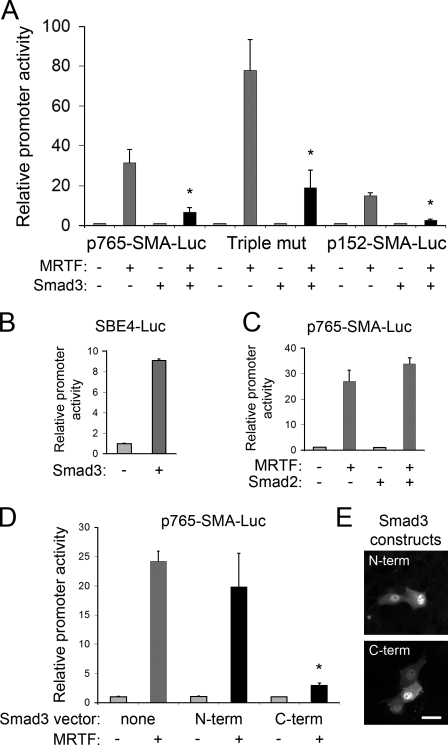
Smad3是MRTF的SMA诱导效应的强抑制剂:一个令人惊讶的发现 Smad3是TGF-β信号传导的中心介质之一,已被证明可直接与MRTF结合( Morita等人,2007a ). 鉴于(a)LCM和TGF-β分别诱导MRTF和Smad3的核易位,(b)这些因素可以相互作用,(c)SMA诱导效应是通过CArG介导的,我们假设Smad3-MRTF复合物可能对CArG顺式元件产生增强效应。 事实上,Smads通过非SBE位点的类似增强作用以前在其他启动子中也有描述( 邱等,2003 ). 为了测试Smad3是否确实能够促进MRTF的转录效应,将细胞与765-bp(WT)SMA-Luc/renilla报告系统以及编码标记MRTF、Myc-tagged Smad3或两者的结构体共同转染( 图3 A ). 正如预期的那样,MRTF强烈诱导了SMA启动子。 Smad3本身并不影响SMA启动子的活性(增加了1.4倍( 图3 B ). 令我们惊讶的是,当与MRTF共表达时,Smad3能有效抑制MRTF诱导的SMA启动子激活( 图3 A ). 这种效应对Smad3是特异性的,因为Smad2的过度表达不会抑制SMA启动子( 图3 C ). 为了确定Smad3是否可以通过影响两个SBE或TCE盒中的任何一个来抑制MRTF(即以CArG无关的方式),我们使用了我们的三-SMA启动子突变,在该突变中这些元件被灭活。 Smad3也有效地抑制了MRTF诱导的该突变体的反应。 此外,在152-bp启动子上观察到同样的抑制作用,这表明抑制不需要额外的上游元件(例如e盒)( 图3 A ). 这些发现表明Smad3干扰通过CArG介导的MRTF的刺激作用。
图3。
Smad3强烈抑制MRTF诱导的SMA启动子刺激,这种作用需要CArG盒和Smad3 C末端。 (A) 用WT或突变SMA-Luc和pRL-TK构建物以及空载体、MRTF和/或Smad3转染细胞48小时。(B)Smad3表达能有效刺激SBE4-Luc报告者。 用空载体或Smad3和SBE4-Luc/pRL-TK系统共同转染细胞。 (C) 用SMA-Luc和空载体、MRTF和/或Smad2共同转染细胞48小时。(D)用空载体(无)、N末端(N末端;1–210 aa)或C末端(C末端;211–425 aa)Smad3结构、SMA-Luc/pRL-TK系统和MRTF或空载体共同转染。 (E) 通过对Myc标记进行免疫染色,可以观察到N端和C端Smad3结构的类似定位。 棒材,20µm。 误差线表示平均值±SEM。
Morita等人(2007a) 已经报道了MRTF与Smad3的C-末端结合,但不与N-末端的一半结合。 为了评估Smad3的抑制作用是否依赖于同一区域,我们测试了N端和C端Smad3结构体的作用( 图3 D ). N端半未能抑制MRTF的作用,而C端半则重述了全长蛋白的作用。 这种差异效应并不是这些Smad3蛋白独特的核定位的结果,因为对它们的Myc表位进行免疫染色显示,它们的表达相似,并且都定位在细胞核占优势的细胞质和细胞核中( 图3E ).
接下来,我们验证了Smad3过度表达不会抑制MRTF的核移位/保留,事实上促进了MRTF核移位/保持( 图S2 ). 因此,Smad3可能有助于TGF-β刺激后MRTF的核滞留时间延长( 图2,A–D )但它强烈抑制MRTF的启动子诱导作用。
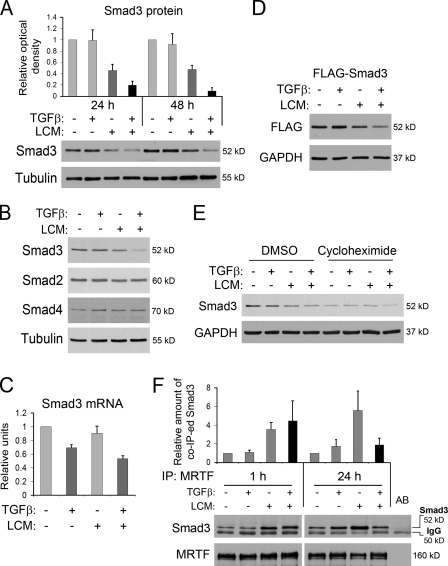
肌源性(两次命中)条件下Smad3表达减少 我们的实验表明,Smad3是TGF-β信号转导的中枢介质,可能是SMA启动子的负调控因子。 然而,我们也已经证明TGF-β对于SMA的表达是必要的。 为了解决这个明显的差异,我们通过测量两种撞击条件下Smad3蛋白表达水平,研究了在EMyT期间Smad3的命运( 图4 A ). 有趣的是,LCM本身诱导Smad3减少50%。 仅TGF-β在24小时后有边际效应,48小时后略有下降。当LCM和TGF-α联合使用时,Smad3表达显著下降,48小时之后下降90%。由于Smad2和Smad4的水平保持不变,这种效应对Smad3具有选择性( 图4 B ).
图4。
肌源性(两次命中)条件导致Smad3的显著丢失,并减轻MRTF–Smad3相互作用。 (A) 根据两次命中方案处理细胞指定的时间,并通过蛋白质印迹评估Smad3的表达。 (B) Smad3降解具有选择性。 施加各种刺激24小时。(C–E)Smad3在mRNA和转录后水平上受到调节。 (C) 处理24小时后,用qPCR测定Smad3 mRNA含量,并将其归一化为GAPDH含量和对照样品。 (D) 如图所示,将Flag-Smad3载体转染的细胞处理24小时。 通过探测标签测量Flag-Smad3水平。 (E) 用5µg/ml环己酰亚胺预孵育细胞,并按指示处理12 h。通过加载等量的蛋白质来补偿因抑制从头合成而导致的总蛋白质损失。 (F) MRTF–二次命中模型中的Smad3关联。 按照指示处理细胞1或24小时,然后用抗MRTF抗体进行免疫沉淀。 探讨了MRTF和共沉淀Smad3的沉淀。 (顶部)归一化为对照的共沉积Smad3的密度定量。 注意,长期联合治疗消除了LCM触发的Smad3和MRTF相关性增加。 误差线表示平均值±SEM。
为了探讨Smad3蛋白减少的机制,我们首先测量了两次命中方案对Smad3 mRNA的影响。TGF-β显著降低Smad3的mRNA,而LCM仅具有边际效应。 联合治疗24小时后减少50%( 图4C ). 由于Smad3蛋白质的总损失超过了这个水平,我们还使用两种方法研究了增强蛋白质降解的潜在贡献。 我们表达由人工(巨细胞病毒)启动子驱动的Flag-Smad3,或用蛋白合成抑制剂环己酰亚胺处理细胞,然后测试各种刺激是否可以(进一步)降低Smad3水平。 LCM和联合治疗(但不是TGF-β)诱导Flag-Smad3蛋白的强烈降低( 图4 D ). 此外,即使在环己酰亚胺存在的情况下,联合处理也促进了内源性Smad3的丢失( 图4 E ). 这些结果表明,肌源性刺激通过转录和转录后机制诱导Smad3蛋白的显著丢失,并且这一过程先于SMA的表达。
二次命中模型中Smad3与MRTF的相互作用 我们的研究结果表明,TGF-β增强的Smad3降解可能是通过MRTF去抑制MF转变的重要贡献者。 为了解决这个想法,我们首先检查了MRTF和Smad3之间的关联是否在两次命中模型的上下文中发生了变化( 图4 F ). 在静息状态下,内源性MRTF的免疫沉淀物含有一些内源性Smad3。 短期(1小时)用LCM或其组合刺激,但不单独刺激TGF-β,增加了两种蛋白质之间的联系。 重要的是,在仅用LCM处理的细胞中,24小时后相关性仍然很高或进一步增加。相反,在LCM和TGF-β存在的情况下,共沉淀Smad3的量下降到未刺激细胞中的水平。 对这一发现最合理的解释是,由于Smad3降解,可用于结合的Smad3较少。 总的来说,长期联合刺激导致细胞核中MRTF水平增加,而MRTF–Smad3相关性没有增加。
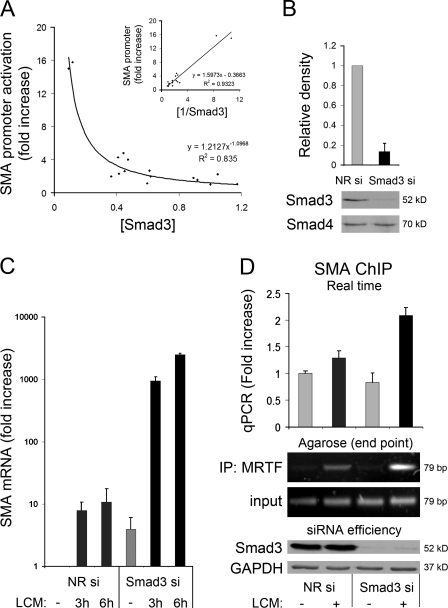
消除Smad3可增强SMA启动子的活性 到目前为止,我们发现Smad3过表达抑制了MRTF的作用,并且Smad3在二次打击模型中降解。 在接下来的实验中,我们试图检验Smad3水平的降低是否确实在EMyT期间的基因重编程中起作用。 我们首先确定在二次命中模型中观察到的Smad3降解水平是否与随后的SMA启动子激活相关。 为此,我们根据双击方案(LCM、TGF-β或两者)处理细胞,并在刺激后的不同时间(2、6、12、24和48小时)制备裂解物。 通过蛋白质印迹测定每个样品中Smad3的表达,如 图4 A 在平行实验中,用765-bp SMA-Luc报告基因转染细胞,并进行Western blots处理,然后测量SMA启动子的活性。 获得这两个数据集后,我们绘制了SMA启动子的激活与相应Smad3表达水平的关系图( 图5 A ). 生成的函数最好用双曲线拟合(另请参见线性化形式; 第页 2 =0.93),表示Smad3水平与相应启动子反应之间的相互关系。
图5。
Smad3表达减少有力地促进SMA启动子活性、SMA mRNA表达以及MRTF和内源性SMA启动子之间的相互作用。 (A) 在LCM或联合治疗后的不同时间(0-48小时),通过Western blotting测定Smad3的相对水平,并与相同治疗后平行测量的相应SMA启动子活性进行对比。 每个点代表三次测定的平均值。 幂函数拟合导致双曲线。 (插图)利用启动子活性的倒数将关系线性化。 (B) Smad3沉默的效率。 (C) Smad3沉默强烈增强LCM诱导的mRNA表达。 用NR或Smad3 siRNA处理细胞,不处理或暴露于LCM中3或6小时,然后处理以提取RNA。 通过qPCR测定SMA mRNA,并将其归一化为GAPDH。 数据表示为与对照相比的折叠变化(对数刻度)。 (D) Smad3沉默增强MRTF与SMA启动子的结合。 将细胞转染为B中的细胞,暴露于正常培养基或LCM中1 h,并使用抗MRTF抗体进行ChIP分析。 (上图)抗体相关SMA启动子信号通过qPCR定量(显示为折叠周期阈值变化)。 (中间)输入的30个PCR循环后琼脂糖凝胶上显示的扩增子和MRTF抗体沉淀。 (底部)证实Smad3下调的蛋白质印迹。 误差线表示平均值±SEM。
接下来,我们测试了Smad3的减少是否确实是导致内源性SMA启动子激活增加的原因。 用Smad3 siRNA处理细胞(导致Smad3表达减少90%; 图5 B )用LCM攻击3或6 h。随后,用定量PCR(qPCR)测定SMA mRNA含量; 图5 C ). 我们使用LCM作为刺激物,因为它仅部分减少Smad3,而它提供了足够的MRTF易位。 在对照细胞中,LCM在6小时后诱导SMA mRNA增加10倍。在没有刺激的情况下下调Smad3也会导致类似的增加。 有趣的是,在Smad3缺失后,LCM引起SMA mRNA的急剧上升(比基线水平高2500倍),与单独消除Smad3的效果相比,刺激达到250倍。
为了测试Smad3的减少是否确实影响了MRTF和内源性SMA启动子之间的相互作用,我们使用了染色质免疫沉淀(ChIP)分析( 图5D ). 用对照或Smad3 siRNA转染细胞,并暴露于正常培养基或LCM。 对MRTF进行免疫沉淀,并用针对SMA启动子近端CArG盒的PCR探针分析沉淀( Elberg等人,2008年 ). 来自对照细胞的MRTF免疫沉淀物捕获了一些SMA CArG-A元素,LCM处理后其水平增加。 仅通过Smad3消除,共沉淀CArG-A信号没有检测到增加; 然而,LCM对Smad3缺失细胞的作用更强( 图5D ). 总的来说,这些发现表明刺激诱导或siRNA诱导的Smad3表达减少促进了MRTF和内源性SMA启动子的CArG-A盒之间的联系,刺激启动子并增加SMA mRNA。
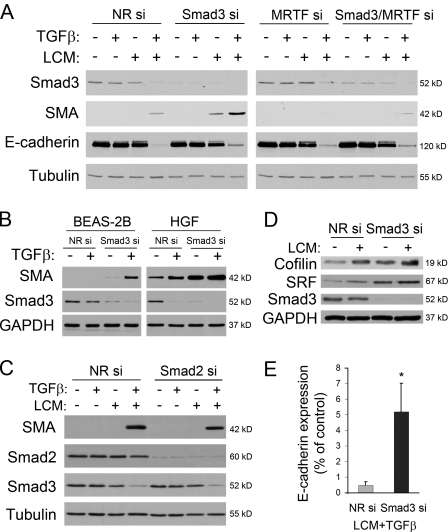
抑制Smad3可增强SMA和其他CArGome蛋白的表达 为了研究Smad3的减少是否真的转化为SMA蛋白水平的升高,我们比较了在对照或Smad3-siRNA存在的情况下,根据两次命中方案处理的细胞中SMA的表达( 图6 A ). 尽管在对照细胞中,暴露于这些刺激48小时后,SMA才被检测到( Masszi等人,2004年 ),在Smad3敲除组中,出现了稳定的SMA表达( 图6 A ). 此外,在Smad3下调细胞中,LCM本身足以刺激SMA蛋白表达。 由于LCM单独不会导致对照细胞中SMA的表达,这一惊人的观察结果表明,Smad3的缺失使TGF-β不需要SMA的表达,并使接触损伤作为一次撞击,足以产生MF。 当使用另一种Smad3特异性siRNA时,获得了相同的结果(未公布的数据)。 为了检测Smad3缺失细胞中SMA的表达是否仍然依赖于MRTF,将细胞与MRTF和Smad3 siRNA共转染。 当LCM或LCM+TGF-β被用作刺激物时,MRTF的缺失也阻止了Smad3敲除细胞中SMA的表达( 图6 A ). 这证实了Smad3的缺失并没有将肌源性程序转移到另一条途径; 相反,它提高了MRTF依赖机制的效率。 重要的是,在BEAS-2B肺上皮细胞和人牙龈成纤维细胞中,还观察到Smad3的缺失使SMA表达增强( 图6 B )这意味着这是一种普遍现象。 Smad2沉默没有这种效果( 图6 C ). Smad3的缺失也促进了cofilin和SRF的表达,表明Smad3也可以抑制其他CArGome蛋白的表达( 图6 D ). 最后,E-钙粘蛋白下调在Smad3缺失细胞中不太稳定( 图6、A和E ),这一发现与 Morita等人(2007a) 在MDCK细胞中。 总之,这些结果表明消除Smad3强烈刺激EMyT,或者相反,Smad3充当MF生成的中断或延迟器。
图6。
一击场景。Smad3沉默导致损伤足以诱导MRTF依赖性SMA表达,并增强其他CArG依赖性基因的表达。 (A) 根据双命中方案,将汇合单层暴露于NR、Smad3、MRTF或Smad3+MRTF siRNAs 24 h,然后进行48 h处理。 制备细胞裂解物,并通过Western blotting检测所示蛋白。 (B) 用NR或Smad3 siRNA转染人肺上皮细胞(BEAS-2B)和牙龈原代成纤维细胞(HGF),24 h后用TGF-β处理48 h。检测全细胞裂解物中的指示蛋白。 (C) Smad2沉默不促进SMA表达。 用针对Smad2的siRNA转染细胞,并如在A中处理2天。探测全细胞裂解物。 (D) 按照指示转染细胞,使其未经处理或暴露于LCM中,并使用抗cofilin和SRF抗体进行Western blotting处理。 (E) Smad3 siRNA细胞中E-cadherin缺失不太完整。 通过密度测定法分析E-cadherin印迹,并将其归一化为对照值。 误差线表示平均值±SEM。
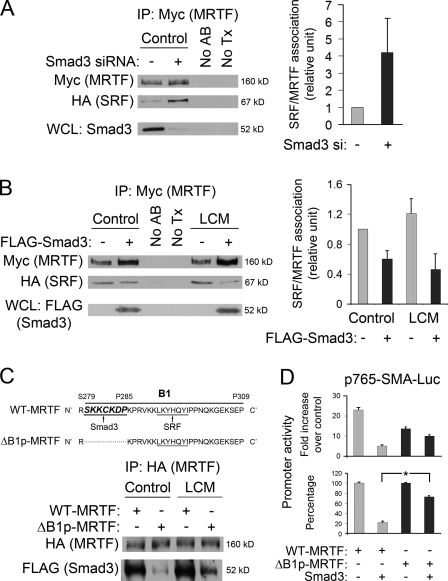
Smad3干扰SRF–MRTF交互 为了深入了解Smad3抑制MRTF功能的分子机制,我们询问它是否干扰MRTF与SRF的相互作用。 为了验证这一点,我们用Myc-MRTF和HA-SRF转染细胞,并在沉默后观察它们的相关性( 图7 A )或Smad3过度表达( 图7 B ). 前者明显促进了SRF与MRTF的相关性,而后者则显著降低了SRF和MRTF之间的相关性。 为了测试MRTF和Smad3之间的关联是否确实对Smad3诱导的抑制至关重要,我们删除了MRTF-B B1盒(ΔB1p; 图7 C ). 之所以选择B1框的此部分,是因为 Morita等人(2007a) 已说明B1盒对Smad3结合至关重要; 然而,它对SRF–MRTF关联也很重要,因此ΔB1在转录上不活跃( Zaromytidou等人,2006年 ). 为了克服这个问题,我们只删除了B1的近端部分,它不包含LKYHQII序列,这是SRF结合的关键核心( Zaromytidou等人,2006年 ). 事实上,ΔB1p保留了大量SMA启动子诱导活性( 图7 D )而它与Smad3的结合显著降低( 图7 C ). 重要的是,与WT相比,ΔB1p对Smad3的抑制作用不太敏感(抑制率为27%对78%; 图7 D ). 这些发现表明Smad3与MRTF的结合是Smad3介导的SMA启动子抑制的关键机制(见讨论)。
图7。
Smad3干扰MRTF–SRF的相互作用。 (A) 用Myc-MRTF和HA-SRF以及NR或Smad3 siRNA转染细胞。通过共免疫沉淀分析MRTF与SRF的相关性。 在全细胞裂解物(WCL)中检测到Smad3沉默。 免疫沉淀对照为无抗体反应(No AB)或Myc转染(No Tx)。 (右)显示了三个实验的密度分析。 (B) Myc-MRTF和HA-SRF与空载体或Smad3共转染。 用抗Myc抗体免疫沉淀MRTF,如A中的对照细胞或LCM处理的细胞(1 h)。 (C) B1区的7-aa序列对Smad3结合至关重要。 SRF绑定核心部分下划线。 预测的Smad3结合位点(S279-P285)以斜体显示。 (顶部)删除后一个区域以生成ΔB1p突变体。 与WT相比,协同免疫沉淀显示Smad3与ΔB1p的相关性降低。(D)ΔB1p突变显示对Smad3抑制的敏感性降低。 将SMA-Luc、ΔB1p或WT-MRTF与空载体或Smad3一起转染细胞。 48小时后进行荧光素酶检测。 将结果归一化为对照组(顶部;相对于对照组的倍数增加)或表示为给定MRTF构造最大效果的百分比(底部)。*, P<0.05。 误差条表示平均值±SEM。
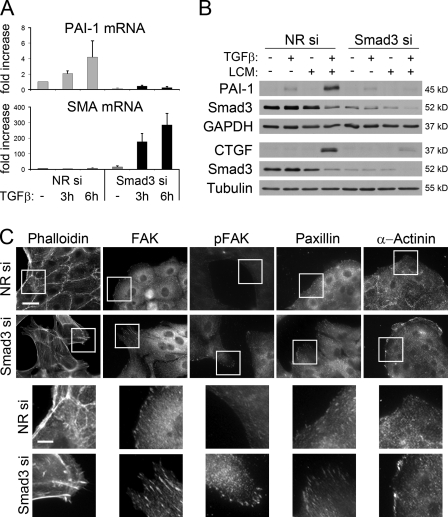
Smad3在间充质和肌肉特性诱导中的相反作用 虽然我们的研究结果表明Smad3在EMyT过程中具有强大的抑制作用,但Smad3也被认为是一种促进EMT的强纤维化转录因子。 为了解释这种明显的差异,我们认为Smad3可能在该过程的第一(间充质)和第二(肌源性)阶段发挥不同的作用。 为了解决这一问题,我们跟踪了Smad3敲除对PAI-1(纤溶酶原激活物抑制剂-1)转录的影响,PAI-1是一种TGF-β反应性促纤维化基因,SMA是MFs的标志。 Smad3沉默在这些基因中诱导对TGF-β的相反反应( 图8 A ). PAI-1 mRNA的基础水平及其TGF-β诱导的升高均受到强烈抑制。 因此,Smad3 siRNA降低TGF-β或联合治疗诱导的PAI-1蛋白表达( 图8 B ). 同样,Smad3的缺失阻止了LCM/TGF-β诱导的结缔组织生长因子(CTGF)的上调,CTGF是EMT的另一种介质( 图8 B ). 相反,Smad3沉默导致非刺激细胞中SMA mRNA显著增加,TGF-β进一步增加( 图8 A ). TGF-β未能在对照细胞中诱导SMA mRNA,而在缺乏Smad3的情况下,它具有实质性作用。 这些数据表明,Smad3对间充质转化关键蛋白的表达至关重要,而它抑制肌源性重编程。
图8。
Smad3沉默对间充质标志物PAI-1的表达和MF特征(SMA和细胞骨架重塑)有相反的影响。 (A) 用qPCR检测对照细胞和Smad3缺失细胞中PAI-1和SMA mRNA( 图5 C )并用载体或TGF-β治疗3或6小时。注意,尽管Smad3缺失强烈刺激TGF-α诱导的SMA mRNA表达,但与LCM相比,该效应仍小得多(~0.125)( 图5 C )事实上,TGF-β单独(与LCM相反)即使在Smad3缺失细胞中也不会诱导SMA表达。 (B) 在含有Smad3和缺失Smad3的细胞中,PAI-1和CTGF蛋白在两次撞击条件下的表达。 用NR或Smad3 siRNA转染细胞24小时,如图所示再处理48小时,然后进行Western blotting。 (C) Smad3缺失诱导细胞骨架重组。 用NR(顶部)或Smad3 siRNA(底部)转染细胞48 h,用罗丹明-指骨肽或FAK、磷酸化FAK(pFAK)、paxillin或actinin染色观察F-actin和局灶性粘连。 Smad3的丢失导致位于岛边缘的细胞中形成中心应力纤维和厚而细长的焦点粘连。 (底部)方框区域的放大倍数较高。 棒材:(顶部)30µm; (底部)10µm。 误差线表示平均值±SEM。
由于许多细胞骨架基因受CArG盒调控,我们研究Smad3下调是否可能诱导F-actin重组为MF样表型。 Smad3沉默后,许多上皮细胞获得了拉长的形状,失去了外周肌动蛋白环,并形成了强大的中央应力纤维( 图8 C ). 此外,这些细胞倾向于从集群边缘迁移,并没有形成具有圆形边界的典型岛屿。 岛周围的对照上皮细胞含有少量和小的局灶性粘连,与细胞边缘平行。 相反,Smad3缺失细胞有许多较大且更成熟的局灶性粘连(通过总粘连和磷酸-FAK、paxillin和α-肌动蛋白染色检测到),垂直于不规则细胞边缘。 总之,Smad3的丢失促进肌动蛋白细胞骨架的MF样重塑,但这些细胞缺乏间充质转化的重要特征,例如PAI-1和CTGF的上调。
讨论 MRTF已成为EMyT期间肌动蛋白骨架重塑和肌源性重编程不可或缺的介质( Fan等人,2007年 ; Morita等人,2007a , b条 ; Elberg等人,2008年 ). 事实上,我们目前的研究表明,除了SMA外,MRTF对于增加或持续表达一系列细胞骨架蛋白是必要的,这些蛋白的基因在其启动子中包含CArG盒( 图1 ). 因此,MRTF信令是一个主要由Rho和Rac控制的过程,如何信令成为一个中心问题( Hill等人,1995年 ; Miralles等人,2003年 ; Fan等人,2007年 ; Busche等人,2008年 ; Sebe等人,2008年 )与(其他)TGF-β诱导途径协作,这些途径对EMyT也是不可或缺的。 我们的实验对这一机制提供了两个重要且令人惊讶的见解:(1)对SMA启动子的详细突变分析表明,不仅接触损伤诱导的MRTF易位,而且TGF-β诱导的通路都以MRTF依赖的CArG盒为靶点( 图1 ). 因此,所有影响都集中在这些要素上,这些要素对于这些投入之间的协同作用是必要的和充分的。 事实上,SBE的失活没有显著影响,而Krüppel-like因子结合位点TCE的破坏促进了启动子的激活,表明这些转录调控因子可能具有抑制作用( Liu等人,2005年 ). (2) TGF-β促进MRTF信号传导和SMA表达的关键机制之一是减少Smad3的表达,即其自身信号传导的主要介质。 重要的是,我们的结果表明Smad3是MRTF的SMA诱导效应的强抑制剂( 图3 和 5–8 )因为(a)内源性Smad3表达与SMA启动子的激活之间存在反向关系,(b)Smad3的过度表达抵消了SMA启动程序——MRTF的刺激作用,以及(c)Smad2的下调导致接触损伤(作为一次打击)足以诱导SMA表达,增加SMA mRNA, 并促进MRTF与内源性SMA启动子的结合。 此外,TGF-β延长MRTF的核蓄积( 图2 ). 这可能是由额外的肌动蛋白聚合以及Smad3依赖的MRTF保留增加引起的(图S2)。 一旦Smad3水平的降低将MRTF从其抑制状态释放出来,这可能使细胞倾向于增强MRTF介导的反式激活。 由于我们的观察结果有些出乎意料,因此将它们整合到当前关于EMT和EMyT机制的知识中非常重要。
关于CArG的核心作用,我们的发现与最近的一项研究一致( Elberg等人,2008年 )研究发现,这两种CArG对TGF-β诱导的人肾小管细胞SMA启动子激活都是必需的。 然而,与其他管状(LLC-PK1)相比,该系统具有一个不寻常的特征[ Fan等人,2007年 ]和MDCK[ Morita等人,2007a ])这些细胞是MRTF的组成核,即使在未刺激的细胞中也是如此。 尽管如此,TGF-β仍然是诱导SMA启动子激活和蛋白表达所必需的,这意味着即使在核MRTF存在的情况下,额外的(尚未确定的)TGF-α依赖机制仍然是必要的。 我们认为TGF-β诱导的Smad3减少以及随后MRTF的去抑制可能是MRTF激活的输入。 我们的研究结果还解释了两次撞击情景的分子基础:第一次撞击是MRTF核转位所必需的(例如通过Rho和Rac激活),而第二次撞击是激活MRTF所必需的,例如通过消除抑制因子。 此外,第二次打击可能会延长MRTF的核驻留时间。 这种观点也可以解释应用的实验系统之间的个体差异:如果MRTF是构成核的( Elberg等人,2008年 ),一次命中(TGF-β)可能就足够了。 或者,在某些细胞中,TGF-β可能触发足够强烈的Rho和/或Rac激活( Bhowmick等人,2001年 )以及随之而来的MRTF易位,因此,它可能会带来这两种需求。 然而,完全完整的上皮细胞或其他融合细胞对TGF-β的成肌作用相对不敏感( Masur等人,1996年 ; Petridou等人,2000年 ; Masszi等人,2004年 ; Fan等人,2007年 ). 这一观察结果与实际病理状况密切相关,并暗示组织损伤可以通过解偶联细胞间接触激活Rho GTPases( Fan等人,2007年 ; Samarin等人,2007年 ; Busche等人,2008年 ; Sebe等人,2008年 )和/或通过整合素刺激( Chen等人,2006年 ; Kim等人,2009年b ),可能极大地增强TGF-β的SMA诱导作用。 这反过来可能导致上皮愈合失调和MF过度分化。
在骨骼肌中,Smad已被证明抑制肌肉发生( 刘等人,2001 ; Zhu等人,2004年 ). 最近,人们提出了一种有趣的机制,即MRTF-a和Smad 1/4之间的复合物可以通过诱导Id3(分化抑制因子-3)蛋白的表达,以非CArG依赖的方式抑制骨骼肌分化( Iwasaki等人,2008年 ). Id3是碱性螺旋-环-螺旋转录因子的拮抗剂,其靶向包括SMA在内的许多肌肉基因启动子中的E盒。 尽管这种机制也可能在上皮细胞中起作用,但Smad3介导的MRTF诱导的SMA启动子激活抑制明显代表了一种独特的调节模式。 从我们的发现中可以明显看出,Smad3对MRTF的抑制作用表现在不包含E盒的短启动子结构中。
我们在MRTF-B的B1区发现了一个7-aa片段,它对MRTF–Smad3结合和Smad3有效抑制MRTF触发的SMA启动子都至关重要。 对我们数据的最简单解释是Smad3和MRTF之间的直接结合抑制了MRTF和CArG盒-SRF复合体之间的相互作用( 图9 A ). 与这种机制一致(a),Smad3和SRF在MRTF上的结合位点相邻,(b)MRTF–SRF关联与Smad3表达呈负相关( 图7 )和(c)Smad3下调增强MRTF与内源性SMA启动子CArG盒的结合( 图5 ). 一种可能的附加机制调用SRF可以直接绑定到Smad3( Lee等人,2007年 )也可能抑制SRF–MRTF关联( 图9 ).
图9。
Smad3是上皮细胞MF承诺的关键延迟者/计时器。 (A) Smad3、MRTF和SRF之间各种双边互动的潜在或测试结果。 (B) 新模型将EMyT的过程分解为Smad3依赖(早期/间叶)和非依赖/抑制(晚期/肌源性)阶段,以及Smad3–MRTF相互作用的拟议作用或其在EMyT各种关键事件中的缺失。
MRTF或心肌蛋白与Smad3的相互作用具有多种功能后果。 MRTF–Smad3复合物通过非常规SBE诱导其负调控因子Slug,参与E-cadherin的下调( Morita等人,2007a ). 这样,MRTF–Smad3复合物有助于上皮特征的丧失,即EMT的第一阶段。 有趣的是,在成纤维细胞中,Smad3被发现以CArG非依赖性的方式增加一些平滑肌相关启动子上的肌钙蛋白或SRF的活性( 邱等,2005 ). 这种效应是否对心肌蛋白而不是MRTF和/或成纤维细胞具有特异性尚待测试。 无论如何,我们的结果表明,Smad3对MRTF介导的、依赖于CArG的SMA转录的抑制作用大大超过了EMyT期间任何潜在的CArG非依赖性刺激作用。 最后,SRF与Smad3结合也可以拮抗SBE介导的TGF-β效应,例如凋亡( Lee等人,2007年 ). 总之,MRTF–Smad3–SRF三角形顶点之间的双边和相互竞争的相互作用可能决定EMyT各个阶段的主要特征和时间( 图9 A ). MRTF与Smad3的相互作用可能有助于抑制上皮标记物,同时,它通过与SRF-MRTF相互作用竞争,使SMA表达和MF转变暂停。 一旦Smad3降解,MRTF–SRF复合物将主导并导致肌源性重编程。
我们表明,转录和转录后机制都有助于两种命中诱导的Smad3水平降低( 图4 ). 与此一致,TGF-β被报道抑制Smad3 mRNA转录( Yanagisawa等人,1998年 )而Smad3在其连接区被各种激酶磷酸化( 郭等人,2008a , b条 )已被提议促进其泛素化和蛋白酶体降解。 未来的工作应确定TGF-β降低Smad3 mRNA和LCM促进Smad3降解的确切机制。
Smad3在纤维发生和EMT(特别是在EMyT中)中的总体作用是复杂和有争议的。 在本研究中,我们将考虑报告的负面和正面影响。 越来越多的证据表明,纤维化的进展与R-Smad表达的下调有关。 肾脏的细胞模型和动物模型( Poncelet等人,2007年 )和肺( Zhao和Geverd,2002年 )纤维化(涉及EMT),Smad3水平显著下降,这一过程与SMA表达相伴随。 在动物模型和纤维原性肾病患者中,Smad2水平降低,Smad泛素化调节因子-2表达增加( Tan等人,2008年 ). 此外,在皮肤和肝脏MF形成过程中观察到Smad3磷酸化降低和核移位( Dooley等人,2001年 ; Reisdorf等人,2001年 ). 尽管这些研究表明纤维化进展和R-Smad下调同时发生,但这些事件之间是否存在因果关系尚不清楚。 Smad3对MRTF的抑制提供了联系这些现象的新机制。 其他令人信服的关于R-Smads缺失与EMT的数据来自TGF-β促肿瘤作用的研究。 在表达Raf–MAPK通路致癌突变的上皮细胞中,TGF-β诱导EMT和Smad3丢失,而Smad3的再表达恢复了上皮表型( Nicolás等人,2003年 ). 此外,消融角质形成细胞中的Smad2可促进EMT和致癌( Hoot等人,2008年 ). 综合考虑,这些研究和我们的研究结果表明,R-Smads在纤维化进展或肿瘤发生过程中可作为EMT或EMyT的负调控因子。
然而,大量文献表明R-Smads是TGF-β诱导的纤维化和EMT的关键介质( Roberts等人,2006年 ). 这一观点的有力支持源于对Smad3基因敲除小鼠的研究( Yang等人,1999年 )在皮肤模型中表现出对基质沉积和EMT敏感性降低( Flanders等人,2003年 ),透镜( Saika等人,2004年 )和肾纤维化( Sato等人,2003年 ). 然而,应该考虑两点。 首先,这种保护作用在很大程度上归因于巨噬细胞募集TGF-β的功能受损( Ashcroft等人,1999年 )尽管不是全部( Lakos等人,2004年 ),Smad3中的纤维化模型 −/− 老鼠。 其次,Smad3蛋白可能无法从这些动物中完全消除。 它们含有一个外显子8缺失,导致Smad3最后89个氨基酸缺失,从而导致功能性空突变。 然而,截短的蛋白质可以在不同的组织中表达(以不同的水平)( Yang等人,1999年 )它还可能与不同的合作伙伴相互作用,这一事实表明,它发挥着主导和消极的作用。 因此,突变体可能失去其促纤维化作用,但可能保持其抗纤维化潜力。 此外,两只Smad3基因敲除小鼠(外显子2或8缺失)的病理学完全不同:第一只死于肠道肿瘤( Zhu等人,1998年 )另一种是自身免疫( Yang等人,1999年 )这意味着截短的蛋白质具有不同的功能。 尽管如此,毫无疑问Smad3可以抑制上皮基因( Morita等人,2007a )对各种间充质基因的表达至关重要( Massague等人,2005年 ). 如何调和这些明显不同的观点? 我们认为解决方案可能在于过程的动态。 根据我们的模型( 图9 B )EMyT可分为Smad3依赖期(早期/间充质)和非依赖期(晚期/肌源性)。 Smad3有助于上皮标记物的丢失,对间充质标记物和某些基质蛋白的表达至关重要。 它还可以通过促进核MRTF积累和合成增强SMA表达的蛋白质(例如ED-A纤维连接蛋白)来制备第二阶段( Isono等人,2002年 ). 这一阶段之后,Smad3逐渐降解,这使得肌源性程序得以动员。 这种转换是运动和收缩表型的先决条件。 这种解释也与Smad3-非依赖EMT的存在相一致( Banh等人,2006年 ). 然而,在缺乏Smad3的情况下,EMT程序转向以肌源性为主的途径。
总之,我们认为Smad3是一种关键的检查点蛋白或计时器,它调节(延迟)MF转换的最终承诺。 显然,未来的研究应该在纤维化疾病的实际病理环境中检验这一观点。 这种情况也可能为旨在减少Smad3功能或表达的抗纤维化治疗的潜在益处和问题提供重要见解。
材料和方法 试剂 兔多克隆抗MRTF(抗BSAC)抗体已在前面描述( Sasazuki等人,2002年 ). 在LLC-PK1细胞的全细胞裂解液中,该抗体在~160 kD时出现双重抗体( Sebe等人,2008年 )其中,核提取物中含量最高的一种更为突出。 针对以下抗原使用商用抗体:Flag(克隆M2)、SMA(克隆1A4)、α-肌动蛋白(克隆BM-75.2)、微管蛋白(Sigma-Aldrich)、cofilin、Smad2、phospho-Smad3、Smad4(细胞信号技术)、c-Myc(克隆9E10)、SRF、CTGF(Santa Cruz Biotechnology,Inc.)、GAPDH(EMD)、组蛋白、α1-整合素、paxillin(Millipore) 、PAI-1、Smad3(Abcam)、FAK、闭塞小带-1、磷酸-FAK(Invitrogen)、E-cadherin和filamin A(克隆5/ABP280;BD)、HA.11(克隆16B12;Covance)和CapZ(AbD-Serotec)。 二级抗体来自Jackson ImmunoResearch Laboratories。 从R&D Systems获得重组人TGF-β。 罗丹明结合的卵磷脂是从Invitrogen中获得的。
细胞培养和治疗 LLC-PK1(氯 4 )细胞,一种猪近端小管上皮细胞系(由田纳西州纳什维尔范德比尔特大学医学院R.C.Harris提供),在37°C的潮湿大气(空气/CO)中,在补充有10%胎牛血清和1%链霉素/青霉素溶液(Invitrogen)的低葡萄糖DME(Invitrogen)中培养 2 比率19:1)与我们之前的研究相同( Masszi等人,2003年 ). 在各种处理之前,将细胞在无血清条件下培养至少3小时。 为了诱导细胞接触分解,用PBS(Invitrogen)彻底清洗细胞,并在名义上无氯化钙的二甲醚(LCM;Invitrogen)中培养细胞。 这种处理导致通过电压计测量的跨上皮电阻立即下降,并在约15分钟内通过相位收缩显微镜观察到细胞接触的破坏。如有指示,用TGF-β处理细胞(生物化学实验为4 ng/ml,启动子萤光素酶测定为10 ng/ml)。 人牙龈成纤维细胞( Pender和McCulloch,1991年 )由C.McCulloch(加拿大安大略省多伦多市多伦多大学)提供,BEAS-2B从美国类型培养物收藏中心购买。
质粒和瞬时转染 p765-SMA-Luc报告基因结构包含pGL3-基本载体(WT)中大鼠SMA启动子近端765-bp部分,该结构在SBE1或SBE2位点(SBE1mut和SBE2mut; 胡等,2003 ),以及带有152-bp长SMA启动子片段的p152-SMA-Luc报告子结构由S.H.Phan(密歇根大学医学院,密歇根州安娜堡)提供。 为了在某些反调节元件中产生额外(或联合)突变,进行了基于PCR的突变。 突变(括号中)和相应的引物对如下:灭活SBE1(C −524 /T、 A类 −525 /C、 和C −528 /A) ,5′-TACAGACTTCATTGACTACACAAAGCTTCCAGACTAC-3′和5′-GTATGTAGTCTGGAAGCTTGTGTAGTCAATGAAGTCT-3′; 突变SBE2(C +15 /T、 A类 +16 /G、 和G +17 /C) ,5′-CACCCACTGCAGCAGTGGAAGCCAGC-3′和5′-CTGGGCTTCTCCACTGCGGTGGT-3′( 胡等,2003 ); 突变TCE(T −53 /C、 克 −52 /T、 和G −50 /C) ,5′-TGGGAAGCGTGCAGGGATCACCA-3′和5′-TTGGTCTGATCCCTGCAGCTCCCA-3′( Hu等人,2007年 ); 灭活CArG-A(C −71 /A、 C类 −70 /A、 G公司 −63 /A、 和G −62 /A) ,5′-CACCCCTGTCTTTGCTAATTGTTTAAGAGCAGTGGGAGG-3′和5′-CCTCCCCTCGCTTCTTAAACAATTAGCAAGACAGGCTG-3′; 并突变CArG-B(C −121 /A、 C −120 /A、 G公司 −113 /A、 和G −112 /A) ,5′-GTTTGTGCTGAGGTAACTATATAATTGGTTAGAGTGAAACG-3′和5′-CGTTCACTCTAACACAATTATATAGTACCTCAGCACAAAAC-3′( 清水等,1995年 ).
这些突变被证明有效地阻断了相应顺式元素的功能:Smad3与突变的SBE1或SBE2的结合( 胡等,2003 )被废除,TCE失去了转录活性( Hu等人,2007年 ). Smad3应答型报告子结构SBE4-Luc由A.B.Roberts(马里兰州贝塞斯达国立卫生研究院)提供。 胸腺嘧啶激酶最小启动子驱动肾小球荧光素酶内部控制质粒pRL-TK购自Promega。 N末端Myc-tagged人类Smad2和N末端Myc或Flag-taged Smad3表达结构(均位于pCMV5B主干中)由L.Attisano(多伦多大学)提供。 从Myc-Smad3构建物生成N-(aa 1–210)和C-末端(aa 211–405)表达构建物。 标记的MRTF-B质粒由E.N.Olson(德克萨斯大学西南医学中心,德克萨斯州达拉斯)提供。 该结构在LLC-PK1细胞中的表达在160和110 kD时产生两条Flag阳性带。 以Flag标记的MRTF-B为模板,生成C-末端Myc-标记的MRTF-B,并将MRTF序列克隆到pcDNA3.1/Myc–His A的Xho1–Apa1位点。整个结构通过测序进行验证。 利用标准PCR方法,在MRTF-B的N末端设计一个双HA标签,从而产生HA–MRTF-B。 通过测序验证了该结构。 使用与特定缺失上游和下游区域互补的引物对,产生了HA标记MRTF-B的B1区域缺失突变。 最终构造包含7-(S279-P285;含)或13-aa缺失(S279-K291;含)。 使用Pfu-Turbo(安捷伦技术公司)进行PCR反应。 结果产物用Dpn1内切酶消化、转化,并通过限制性消化分析或使用缺失两侧的PCR引物筛选菌落。 通过测序验证所选克隆。 编码HA标记人类SRF的pCGN-SRF质粒由R.Prywes产生( Johansen和Prywes,1993年 ). 使用FuGENE 6或Lipofectamine 2000试剂转染细胞。 为了免疫沉淀异源表达的蛋白质,在实验前48小时,用5µg Flag–MRTF-B和1µg Myc-Smad3载体转染生长在10-cm培养皿上的细胞。 在三重转染实验中,用4µg Myc-MRTF、4µgHA-SRF和6µg Flag-Smad3载体转染10 cm培养皿上生长的细胞24小时。
荧光素酶报告分析 荧光素酶报告分析按照我们之前的研究进行( Masszi等人,2003年 , 2004 ). 简言之,将细胞接种到6孔板上,并在约60%的汇合处用0.5µg/孔萤光素酶构建体、0.05µg/孔pRL TK和2µg/孔空载体或表达载体的混合物转染。 16小时后,细胞被血清饥饿3小时,如果没有其他指示,则处理24小时。 最后,根据制造商的说明,对细胞进行裂解,并使用双荧光素酶报告分析系统试剂盒(Promega)和光度计(Lumat 9507;Berthold)测定荧光素酶活性。 对于每种情况,重复进行治疗,并重复至少三次实验。 从每个样本中,对应于特定启动子结构的萤火虫荧光素酶活性被归一化为同一样本的肾小球荧光素酶活性。 结果表示为与未经处理的对照组的平均萤火虫/renilla比率相比的倍数变化。
RNA干扰 从LLC-PK1细胞获得猪MRTF基因的部分序列后,生成MRTF siRNAs。 值得注意的是,通过RT-PCR获得的序列与MRTF-B高度同源,但与MRTF-A不同源,这表明前者是这些细胞中表达的主要且可能是唯一的亚型。 使用siRNA target Finder程序(Applied Biosystems)确定最佳靶序列(5′-AACATGGAGTGCTAGACATT-3′和5′-ACAGCAGTGAAGAGAG-3′)。 针对猪Smad3的siRNAs(靶序列5′-AAGAGTTCACTCCACATTC-3′;基于GenBank序列登录号。 NM_214137.1号 )和Smad2(靶序列5′-AAATACGATAGATCAGTGGGA-3′;GenBank登录号。 西北_001885794.1 )和人类Smad3(靶序列5′-AAGGCAATCACCACCGCAGAAC-3′; NM_005902.3号 )使用Target Finder工具(Applied Biosystems)设计。 NR对照siRNA购自Ambion。 LLC-PK1细胞在无抗生素生长培养基中培养,并使用Lipofectamine RNAiMAX(Invitrogen)转染100 nM siRNA。 对于EMyT诱导,细胞以60%的融合率转染。 过夜培养后,细胞达到完全融合,并在两次撞击模型的适当条件下处理48小时。
蛋白质印迹 处理后,将细胞刮入加入1 mM Na的Triton裂解缓冲液(30 mM Hepes、pH 7.4、100 mM NaCl、1 mM EGTA、20 mM NaF和1%Triton X-100)中 三 VO(旁白) 4 1 mM苯甲基磺酰基氟化物和全迷你蛋白酶抑制剂鸡尾酒(罗氏)。 测定蛋白质浓度,并通过在Laemmli样品缓冲液中煮沸使样品变性(Bio-Rad Laboratories)。 如前所述,对等量的蛋白质(10µg)进行SDS-PAGE和Western blotting( Masszi等人,2004年 ). 使用密度计(GS800;Bio-Rad Laboratories)和Quantity One软件(Bio-Read Laborations)进行密度测定。
蛋白质测定 使用BCA蛋白质测定法(Thermo Fisher Scientific)以牛血清白蛋白为标准测定未变性细胞裂解物的蛋白质浓度。
免疫沉淀 细胞生长在10-cm培养皿上,经过适当处理后,在Triton裂解缓冲液中裂解。 为了去除细胞碎片,在4°C下以12000 rpm的转速旋转样品10分钟,并取全细胞裂解物的小份样品。 用蛋白G琼脂糖珠(Thermo Fisher Scientific)预处理上清液(约1-2 mg蛋白质),并用适当的抗体(1µG/样品)孵育。 为了捕获免疫复合物,将蛋白G琼脂糖珠添加到混合物中1 h。随后,用补充有1 mM Na的Triton裂解缓冲液将珠洗涤三次 三 VO(旁白) 4 将捕获的蛋白质洗脱到Laemmli样品缓冲液(Bio-Read Laboratories)中,并通过Western blotting进行分析。
核提取 根据制造商的建议,使用NE-PER核提取试剂盒(Thermo Fisher Scientific)从生长在6厘米培养皿上的LLC-PK1细胞汇合层中制备核提取物。 收集核提取物,测定其蛋白质浓度,并通过Western blotting分析等蛋白含量(5µg)的样品。 用抗组蛋白抗体检查核蛋白的载量是否相等。
ChIP分析 用于ChIP实验的试剂来自EZ ChIP试剂盒(Millipore),基本上按照制造商的说明进行分析。 使用Lipofectamine RNAiMAX(Invitrogen)用猪Smad3或NR对照siRNA转染LLC-PK1细胞。 通过对从匹配平板制备的细胞裂解物与用于ChIP分析的细胞裂解液进行Western blotting,证实了下调的效率。 下调后,对细胞进行适当处理,通过超声交联、裂解和剪切(450 Sonifer;Branson)。 用5µg兔多克隆MRTF抗体对DNA片段进行免疫沉淀,并从回收的复合物中提取纯化的DNA。 对于阴性对照,使用正常兔IgG作为免疫沉淀抗体进行平行实验。 通过基于SYBR绿色的实时PCR(IQ5循环仪;Bio-Rad实验室)分析每个样本的输入和纯化DNA,使用引物扩增猪SMA启动子的含有CArG的区域。 引物序列如下:5′-AGTTTGTGCTGAGGTCCCTATG-3′和5′-TTCCCCAAACAGAAAGA-3′。 半定量PCR也通过在3%琼脂糖凝胶上运行产品来检测79-bp扩增子。
免疫荧光显微镜 在玻璃盖玻片上生长的细胞用4%多聚甲醛固定30分钟,然后用PBS强烈清洗,并用100 mM甘氨酸在PBS中孵育10分钟。细胞在含有1%Triton X-100和0.5%牛血清白蛋白的PBS中渗透20分钟,在PBS的3%BSA中封闭1小时, 并与一级抗体再孵育1小时。彻底清洗后,用相应的荧光标记的二级抗体与Cy3染料孵育细胞(Jackson ImmunoResearch Laboratories)。 为了同时观察共转染的Myc和Flag-tagged蛋白,首先用抗Flag(M2;Sigma-Aldrich)和Cy3标记的抗鼠抗体孵育样品,并用与FITC(Santa Cruz Biotechnology,Inc.)直接偶联的抗Myc抗体(9E10)染色。 为了观察F-肌动蛋白,将固定细胞与罗丹明标记的卵磷脂(Invitrogen)孵育。 为了进行核标记,用DAPI(Invitrogen)对细胞进行染色,并使用荧光固定介质(Dako)将盖玻片固定在玻片上。 使用显微镜(IX81;Olympus)对样品进行分析,显微镜带有UPlan S-Apo 60×1.42 NA油物镜(Olympus),并与由成像软件(QED InVivo;Media Cybernetics)控制的摄像机(Evolution QEi Monochrome;Media Control)相耦合。 使用ImagePro Plus软件(3DS 5.1;Media Cybernetics)和Photoshop(CS4;Adobe)处理图像。 修改仅限于亮度/对比度的微小调整。 MRTF分布如前所述进行了量化( Fan等人,2007年 ),但使用了更严格的标准来表示MRTF为核。 沿着细胞的一条直线测量染色强度,并测定细胞质和细胞核中的平均强度(通过DAPI染色验证)。 如果核质比>1.5,则MRTF定位为核定位。 该值对应于通过简单目视检查评估的清晰核聚积(在未刺激细胞中,平均比率为0.6;即存在明显的核排斥)。 幻灯片由两名独立观察员进行评估,在三个实验中,对每种情况下至少10个随机选择的区域(>200个细胞)进行量化。
mRNA分析 用猪Smad3或NR siRNA转染LLC-PK1细胞54小时后,去除血清3小时,用TGF-β或LCM处理或不处理3或6小时。在其他实验中,将未转染细胞暴露在二次命中方案的四种条件下24小时。 经过这些处理后,使用RNeasy试剂盒(QIAGEN)提取RNA,并使用iScript逆转录(Bio-Read Laboratories)从1µg总RNA合成cDNA。 基于SYBR绿色的实时PCR用于评估PAI-1、SMA和Smad3的基因表达,使用GAPDH作为内源性对照。 针对已知猪序列设计的引物对如下:SMA,5′-TGTGACAATGGTTCGCTCTGT-3′和5′-TTCGTCACCAGTGTTTTT-3′; Smad3,5′-GCAGACGTCAACAGAGTGCAT-3′和5′-ATTCACGCACCTCGTCCTTCTT-3′; PAI-1,5′-CACTCGCTCTGGTGGTGGTAGA-3′和5′-GTCTCGATGGTGCTTT-3′; GAPDH,5′-GCAAGTGGACATGGTCGCCATCA-3′和5′-AGCTTCCCATTCAGCCTTGACTACT-3′。 半定量PCR产物在2%琼脂糖凝胶上进行分析。
统计分析 数据以至少三个类似实验的斑点或图像或所示实验次数的平均值±SEM表示。 统计显著性由Student’s t吨 酌情使用Prism软件(4.0版;GraphPad software,Inc.)进行方差测试或单向分析(Tukey post-hoc测试)。 P<0.05被认为是显著的,用星号表示。
致谢 这项工作得到了加拿大卫生研究所(CIHR)、加拿大国家科学与工程研究委员会(A.Kapus)和加拿大肾脏基金会(A.Kapus和K.Szászi)的资助。 A.Masszi拥有安大略省博士后奖学金,E.Charbonney拥有皮特斯基金会奖学金,K.Szászi是KRESCENT新研究员奖的获得者(加拿大肾脏基金会、加拿大肾脏学会和CIHR)。
脚注
本文中使用的缩写:
CArG公司 CC(A/T)-富GG元素
炸薯条 染色质免疫沉淀
CTGF公司 结缔组织生长因子
电子病历 上皮-间充质转化
EMyT公司 上皮–MF转变
生命周期管理 低钙培养基
MF公司 肌成纤维细胞
MRTF公司 心肌相关转录因子
尼泊尔卢比 非相关的
定量PCR 定量PCR
R-Smad公司 受体Smad
SBE公司 Smad-binding元素
座椅模块组件 α-平滑肌肌动蛋白
战略参考框架 血清反应因子
三氯乙烯 TGF-β控制元件
重量 野生型
工具书类
Ashcroft G.S.、Yang X.、Glick A.B.、Weinstein M.、Letterio J.L.、Mizel D.E.、Anzano M.、Greenwell Wild T.、Wahl S.M.、Deng C.、Roberts A.B。 1999. 缺乏Smad3的小鼠伤口愈合加快,局部炎症反应受损。 自然细胞生物学。 1:260–266 10.1038/12971 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Banh A.、Deschamps P.A.、Gauldie J.、Overbeek P.A.、Sivak J.G.、West-Mays J.A。 2006 在Smad3缺失的情况下,晶状体特异性TGF-β表达诱导前囊下白内障形成。 投资。 眼科学。 视觉。 科学。 47:3450–3460 10.1167/iovs.05-1208 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Bhowmick N.A.、Ghiassi M.、Bakin A.、Aakre M.、Lundquist C.A.、Engel M.E.、Arteaga C.L.、Moses H.L。 2001 转化生长因子-beta1通过RhoA依赖机制介导上皮向间充质的转分化。 分子生物学。 单元格。 12:27–36 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Busche S.、Descot A.、Julien S.、Genth H.、Posern G。 2008 上皮细胞-细胞接触通过Rac-actin-MAL信号调节SRF介导的转录。 细胞科学杂志。 121:1025–1035 10.1242/jcs.014456 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Chen C.A.、Hwang J.C.、Guh J.Y.、Tsai J.C.、Chen H.C。 2006. TGF-β1和整合素通过增加α-平滑肌肌动蛋白的表达,协同促进大鼠足细胞的分化。 Transl.公司。 物件。 148:134–141 2016年10月10日/j.trsl.2006.03.008 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Dooley S.、Delvoux B.、Streckert M.、Bonzel L.、Stopa M.、ten Dijke P.、Gressner A.M。 2001 通过Smad2/3磷酸化在肝星状细胞中转化生长因子β信号转导,这是一条在体外发展为肌成纤维细胞过程中被阻断的途径。 肝星状细胞转分化过程中的TGF-β信号转导。 FEBS通讯。 502:4–10 10.1016/S0014-5793(01)02656-4 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Elberg G.、Chen L.、Elberg D.、Chan M.D.、Logan C.J.、Turman M.A。 2008 MKL1介导TGF-β1诱导的人肾上皮细胞α-平滑肌肌动蛋白表达。 美国生理学杂志。 肾脏生理学。 294:F1116–F1128 2015年10月15日/邮编:00142.2007 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Fan L.、Sebe A.、Péterfi Z.、Masszi A.、Thirone A.C.、Rotstein O.D.、Nakano H.、McCulloch C.A.、Szászi K.、Mucsi I.、Kapus A。 2007 通过rho-rho激酶-磷酸肌球蛋白途径对上皮-肌成纤维细胞转化的细胞接触依赖性调节。 分子生物学。 单元格。 18:1083–1097 10.1091/桶。 E06-07-0602号 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Flanders K.C.、Major C.D.、Arabshahi A.、Aburime E.E.、Okada M.H.、Fujii M.、Blalock T.D.、Schultz G.S.、Sowers A.、Anzano M.A.等人。 2003 对转化生长因子-beta/Smad3信号传导的干扰会加速先前受照射皮肤的伤口愈合。 美国病理学杂志。 163:2247–2257 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
郭欣、拉米雷斯·A、瓦德尔·D·S、李中、刘欣、王晓峰。 2008年a。 Axin和GSK3-控制Smad3蛋白的稳定性并调节TGF-信号传导。 基因发育。 22:106–120 10.1101/加德满都1590908 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
郭欣、瓦德尔D.S.、王伟、王忠、利伯拉蒂N.T.、永S.、刘欣、王晓峰。 2008年b。 Smad3的配体依赖性泛素化受酪蛋白激酶1γ2(TGF-β信号传导抑制剂)调节。 致癌物。 27:7235–7247 2018年10月10日/2008.337 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Hautmann M.B.、Adam P.J.、Owens G.K。 1999. 平滑肌细胞与非平滑肌细胞中TGF-β诱导平滑肌α-肌动蛋白的相似性和差异。 动脉硬化。 喉咙。 瓦斯克。 生物。 19:2049–2058 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Hill C.S.、Wynne J.、Treisman R。 1995 Rho家族GTPases RhoA、Rac1和CDC42Hs通过SRF调节转录激活。 单元格。 81:1159–1170 10.1016/S0092-8674(05)80020-0 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Hoot K.E.、Lighthall J.、Han G.、Lu S.L.、Li A.、Ju W.、Kulesz-Martin M.、Bottinger E.、Wang X.J。 2008 角质细胞特异性Smad2消融导致皮肤癌形成和进展过程中上皮-间质转化增加。 临床杂志。 投资。 118:2722–2732 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
胡斌、吴忠、潘S.H。 2003 Smad3介导转化生长因子-β诱导的α-平滑肌肌动蛋白表达。 美国J.Respir。 细胞分子生物学。 29:397–404 10.1165/rcmb.2003-0063OC公司 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
胡斌、吴忠、刘涛、乌伦布鲁克M.R.、金浩、潘S.H。 2007 肠富Krüppel-like因子与Smad3相互作用抑制肌成纤维细胞分化。 美国J.Respir。 细胞分子生物学。 36:78–84 10.1165/rcmb.2006-0043OC [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Isono M.、Chen S.、Hong S.W.、Iglesias-de la Cruz M.C.、Ziyadeh F.N。 2002 Smad通路在糖尿病小鼠肾脏中被激活,Smad3介导TGF-β诱导的系膜细胞纤维连接蛋白。 生物化学。 生物物理学。 Res.社区。 296:1356–1365 10.1016/S0006-291X(02)02084-3 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Iwano M.、Plieth D.、Danoff T.M.、Xue C.、Okada H.、Neilson E.G。 2002 有证据表明,在组织纤维化期间,成纤维细胞来源于上皮。 临床杂志。 投资。 110:341–350 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Iwasaki K.、Hayashi K.、Fujioka T.、Sobue K。 2008 Rho/Rho相关激酶信号通过Id3基因的肌钙蛋白相关转录因子A/Smad依赖性转录调节肌源性分化。 生物学杂志。 化学。 283:21230–21241 10.1074/jbc。 M710525200型 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Johansen F.E.、Prywes R。 1993 使用GAL4-SRF构建物鉴定血清反应因子(SRF)中的转录激活和抑制域。 分子细胞。 生物。 13:4640–4647 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Kallui R.、Neilson E.G。 2003 上皮-间充质转化及其对纤维化的影响。 临床杂志。 投资。 112:1776–1784 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Kim K.K.、Kugler M.C.、Wolters P.J.、Robillard L.、Galvez M.G.、Brumwell A.N.、Sheppard D.、Chapman H.A。 2006 肺泡上皮细胞-间充质转化在肺纤维化过程中在体内发生,并受细胞外基质的调节。 国家。 阿卡德。 科学。 美国。 103:13180–13185 10.1073/pnas.0605669103 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Kim K.K.、Wei Y.、Szekeres C.、Kugler M.C.、Wolters P.J.、Hill M.L.、Frank J.A.、Brumwell A.N.、Wheeler S.E.、Kreidberg J.A.、Chapman H.A。 2009年a。 上皮细胞α3beta1整合素连接β-catenin和Smad信号传导,促进肌成纤维细胞形成和肺纤维化。 临床杂志。 投资。 119:213–224 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Kim Y.、Kugler M.C.、Wei Y.、Kim K.K.、Li X.、Brumwell A.N.、Chapman H.A。 2009年b。 整合素α3β1依赖性β-catenin磷酸化将上皮Smad信号与细胞接触联系起来。 《细胞生物学杂志》。 184:309–322 10.1083/jcb.200806067 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Klymkowsky M.W.、Savagner P。 2009 上皮-间充质转化:癌症研究者的概念朋友和敌人。 美国病理学杂志。 174:1588–1593 10.2353/ajpath.2009.080545 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Lakos G.、Takagawa S.、Chen S.J.、Ferreira A.M.、Han G.、Masuda K.、Wang X.J.、DiPietro L.A.、Varga J。 2004 TGF-β/Smad3信号的靶向破坏调节硬皮病小鼠模型中的皮肤纤维化。 美国病理学杂志。 165:203–217 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Lee J.M.、Dedhar S.、Kalluri R.、Thompson E.W。 2006 上皮-间质转化:信号、发育和疾病的新见解。 《细胞生物学杂志》。 172:973–981 10.1083/jcb.200601018 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Lee H.J.、Yun C.H.、Lim S.H.、Kim B.C.、Baik K.G.、Kim J.M.、Kin W.H.、金S.J。 2007 SRF是Smad3介导的TGF-β信号转导的核阻遏物。 致癌物。 26:173–185 10.1038/sj.一次1209774 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Liu D.、Black B.L.、Derynk R。 2001. TGF-β通过Smad3对肌源性转录因子的功能性抑制抑制肌肉分化。 基因发育。 15:2950–2966 10.1101/gad.925901 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Liu Y.、Sinha S.、McDonald O.G.、Shang Y.、Hoofnagle M.H.、Owens G.K。 2005. Kruppel-like factor 4可消除肌钙蛋白诱导的平滑肌基因表达激活。 生物学杂志。 化学。 280:9719–9727 10.1074/jbc。 M412862200 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Massague J.、Seoane J.、Wotton D。 2005 Smad转录因子。 基因发育。 19:2783–2810 10.1101/加德满都1350705 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Masszi A.、Di Ciano C.、Sirokmany G.、Arthur W.T.、Rotstein O.D.、Wang J.、McCulloch C.A.、Rosival L.、Mucsi I.、Kapus A。 2003 Rho在TGF-β1诱导的α-平滑肌肌动蛋白表达中的中心作用。 美国生理学杂志。 肾脏生理学。 284:F911–F924 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Masszi A.、Fan L.、Rosival L.、McCulloch C.A.、Rotstein O.D.、Mucsi I.、Kapus A。 2004. 细胞-细胞接触的完整性是TGF-β1诱导的上皮-肌成纤维细胞转变的关键调节因子:β-catenin的作用。 美国病理学杂志。 165:1955–1967 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Masur S.K.、Dewal H.S.、Dinh T.T.、Erenburg I.、Petridou S。 1996 当低密度镀膜时,肌成纤维细胞与成纤维细胞分化。 程序。 国家。 阿卡德。 科学。 美国。 93:4219–4223 10.1073/pnas.93.9.4219 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Miano J.M.、Long X.、藤原K。 2007 血清反应因子:肌动蛋白细胞骨架和收缩器的主要调节因子。 美国生理学杂志。 细胞生理学。 292:C70–C81 10.1152/ajpcell.00386.2006 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Miralles F.、Posern G.、Zaromytidou A.I.、Treisman R。 2003 肌动蛋白动力学通过调节其辅激活子MAL.细胞来控制SRF的活性。 113:329–342 10.1016/S0092-8674(03)00278-2 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Morita T.、Mayanagi T.、Sobue K。 2007年a。 心肌相关转录因子在上皮-间质转化中的双重作用 段塞 诱导和肌动蛋白重塑。 《细胞生物学杂志》。 179:1027–1042 10.1083/jcb.200708174 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Morita T.、Mayanagi T.、Sobue K。 2007年b。 肌钙蛋白相关转录因子(MRTFs/MAL/MKL)通过转录调节细胞骨架/局部粘附基因重组肌动蛋白细胞骨架。 实验细胞研究。 313:3432–3445 10.1016/j.yexcr.2007.07.008 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Nakaya Y.、Sheng G。 2008 原肠胚形成期间上皮到间充质的转变:胚胎学观点。 发展增长差异。 50:755–766 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Nicolás F.J.、Lehmann K.、Warne P.H.、Hill C.s.、Downward J。 2003 Madin-Darby犬肾细胞的上皮-间充质转化伴随Smad3表达下调,导致对转化生长因子-β诱导的生长停滞产生抵抗。 生物学杂志。 化学。 278:3251–3256 10.1074/jbc。 M209019200号 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Pender N.、McCulloch C.A。 1991 两种人体成纤维细胞亚型对机械拉伸反应的肌动蛋白聚合定量。 细胞科学杂志。 100:187–193 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Petridou S.、Maltseva O.、Spanakis S.、Masur S.K。 2000 成纤维细胞中TGF-β受体的表达和smad2的定位依赖于细胞密度。 投资。 眼科学。 视觉。 科学。 41:89–95 [ 公共医学 ] [ 谷歌学者 ]
Poncelet A.C.、Schnaper H.W.、Tan R.、Liu Y.、Runyan C.E。 2007. Smad3的细胞表型特异性下调涉及减少基因激活和蛋白质降解。 生物学杂志。 化学。 282:15534–15540 10.1074/jbc。 M701991200型 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Posern G.、Treisman R。 2006 Actin’together:血清反应因子、其辅助因子以及与信号转导的联系。 细胞生物学趋势。 16:588–596 2016年10月10日/j.tcb.2006.09.008 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
邱鹏、冯晓华、李磊。 2003 Smad3和SRF相关复合物的相互作用介导TGF-β1信号,以调节肌成纤维细胞分化过程中的SM22转录。 分子细胞杂志。 心脏病。 35:1407–1420 2016年10月10日/j.yjmcc.2003.09.002 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
邱鹏、里奇·R.P.、傅中、曹丁、卡明·J、米亚诺·J.M.、王大中、李海杰、李磊。 2005 心肌素以非依赖于CArG盒的方式增强Smad3介导的转化生长因子-β1信号传导:Smad结合元件是体内SM22alpha转录的重要顺式元件。 循环。 物件。 97:983–991 10.1161/01.RES.0000190604.90049.71 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Reisdorf P.、Lawrence D.A.、Sivan V.、Klising E.、Martin M.T。 2001 转化生长因子-beta1反应的改变涉及皮肤纤维化肌成纤维细胞Smad3信号的下调。 美国病理学杂志。 159:263–272 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Roberts A.B.、Tian F.、Byfield S.D.、Stuelten C.、Oosima A.、Saika S.、Flanders K.C。 2006 Smad3是TGF-β介导的上皮-间质转化、纤维化、肿瘤抑制和转移的关键。 细胞因子生长因子评论。 17:19–27 2016年10月10日/j.cytogfr.2005.09.008 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Saika S.、Kono-Saika S.、Ohnishi Y.、Sato M.、Muragaki Y.、Ooshima A.、Flanders K.C.、Yoo J.、Anzano M.、Liu C.Y.等人。 2004 Smad3信号是晶状体上皮损伤后上皮-间质转化所必需的。 美国病理学杂志。 164:651–663 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Samarin S.N.、Ivanov A.I.、Flatau G.、Parkos C.A.、Nusrat A。 2007 Rho/ROCK-II信号传导介导上皮顶端连接的解体。 分子生物学。 单元格。 18:3429–3439 10.1091/桶。 E07-04-0315号 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Sasazuki T.、Sawada T.、Sakon S.、Kitamura T.、Kishi T.、Okazaki T.、Katano M.、Tanaka M.、Watanabe M.、Yagita H.等人。 2002. 通过功能克隆鉴定一种新的转录激活物BSAC,以抑制肿瘤坏死因子诱导的细胞死亡。 生物学杂志。 化学。 277:28853–28860 10.1074/jbc。 M203190200号 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
佐藤M.、村上Y.、赛卡S.、罗伯茨A.B.、Ooshima A。 2003 靶向性破坏TGF-β1/Smad3信号通路可预防单侧输尿管梗阻引起的肾小管间质纤维化。 临床杂志。 投资。 112:1486–1494 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Sebe A.、Masszi A.、Zulys M.、Yeung T.、Speight P.、Rotstein O.D.、Nakano H.、Mucsi I.、Szászi K.、Kapus A。 2008 Rac、PAK和p38调节心肌相关转录因子的细胞接触依赖性核移位。 FEBS通讯。 582:291–298 2016年10月10日至2007年12月21日 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Shimizu R.T.、Blank R.S.、Jervis R.、Lawrenz-Smith S.C.、Owens G.K。 1995 平滑肌α-肌动蛋白基因启动子在平滑肌细胞与非平滑肌细胞中的调节不同。 生物学杂志。 化学。 270:7631–7643 10.1074/jbc.270.6.2460 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
孙强、陈刚、斯特雷布·J·W、龙·X、杨·Y、小斯托克·C·J、米亚诺·J·M。 2006 定义哺乳动物CArGome。 基因组研究。 16:197–207 10.1101/4108706克 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Tan R.、He W.、Lin X.、Kiss L.P.、Liu Y。 2008 纤维性肾脏中Smad泛素化调节因子-2:调节、靶向特异性和功能意义。 美国生理学杂志。 肾脏生理学。 294:F1076–F1083 10.1152/ajprenal.00323.2007 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Wang D.、Chang P.S.、Wang Z.、Sutherland L.、Richardson J.A.、Small E.、Krieg P.A.、Olson E.N。 2001 心肌蛋白(血清反应因子的转录辅因子)激活心脏基因表达。 单元格。 105:851–862 10.1016/S0092-8674(01)00404-4 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
王德智、李S.、曲棍球运动员D.、萨瑟兰L.、王哲、施拉特G.、理查森J.A.、诺德海姆A.、奥尔森E.N。 2002 心肌蛋白相关转录因子家族增强血清反应因子活性。 程序。 国家。 阿卡德。 科学。 美国。 99:14855–14860 10.1073/pnas.222561499 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Xu J.、Lamouille S.、Derynk R。 2009 TGF-β诱导的上皮细胞向间充质细胞转化。 细胞研究。 19:156–172 2009年10月18日 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Yanagisawa K.、Osada H.、Masuda A.、Kondo M.、Saito T.、Yatabe Y.、Takagi K.,Takahashi T.、Takahahi T。 1998 Smad3诱导人正常肺上皮细胞凋亡和下调Smad3表达以响应TGF-β。 致癌物。 17:1743–1747 10.1038/sj.onc.202052 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
杨杰、刘毅。 2001 肾小管上皮细胞向肌成纤维细胞转变关键事件的解剖及其在肾间质纤维化中的意义。 美国病理学杂志。 159:1465–1475 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
杨欣、莱特里奥·J.J.、莱奇莱德·R.J.、陈·L、海曼·R.、顾·H、罗伯茨·A.B.、邓·C。 1999. SMAD3的靶向破坏导致粘膜免疫受损和T细胞对TGF-β的反应性降低。 EMBO J。 18:1280–1291 10.1093/emboj/18.5.1280 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Zaromytidou A.I.、Miralles F.、Treisman R。 2006 MAL和三元复合因子使用不同的机制接触血清反应因子DNA结合结构域上的共同表面。 分子细胞。 生物。 26:4134–4148 10.1128/MCB.01902-05 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
赵勇,Geverd D.A。 2002 博莱霉素诱导的肺纤维化中Smad3表达的调节:TGF-β信号的负反馈回路。 生物化学。 生物物理学。 Res.社区。 294:319–323 10.1016/S0006-291X(02)00471-0 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Zhu Y.、Richardson J.A.、Parada L.F.、Graff J.M。 1998 Smad3突变小鼠发生转移性结直肠癌。 单元格。 94:703–714 10.1016/S0092-8674(00)81730-4 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Zhu S.、Goldschmidt-Clermont P.J.、Dong C。 2004 转化生长因子-β诱导的肌生成抑制通过Smad途径介导,并受微管动态稳定性的调节。 循环。 物件。 94:617–625 10.1161/01.RES.0000118599.25944.D5 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]