摘要
癌症患者经历了一系列行为改变,包括抑郁、疲劳、睡眠障碍和认知功能障碍。在癌症诊断和治疗的整个过程中,这些行为共病现象都很明显,并且可以持续到生存期。有大量文献描述了癌症患者行为共病的潜在后果,包括生活质量受损、治疗依从性降低以及疾病相关发病率和死亡率增加。癌症的医疗并发症及其治疗,如贫血、甲状腺功能障碍和癌症化疗药物的神经毒性,是这些行为改变的部分原因。然而,神经科学和免疫学/肿瘤学的最新进展揭示了对其他病理生理机制的新见解,这些机制可能会显著促进癌症相关行为变化的发展。人们特别关注免疫过程,特别是先天性免疫炎症反应的激活及其通过神经内分泌途径的调节,而神经内分泌途径又影响中枢神经系统的功能,包括神经递质代谢、神经肽功能、睡眠周期、,区域大脑活动和最终行为。对这些免疫学对大脑的影响的进一步了解为整合癌症患者发生的广泛行为改变提供了一个新的概念框架,并可能揭示治疗干预和未来研究的一系列更为集中的转化靶点。这些进展保证了在识别处于危险中的癌症患者和目前正在遭受痛苦的癌症患者方面取得补充性进展,包括更加强调行为状态是所有癌症患者在整个疾病遭遇过程中评估的“第六个生命体征”。
介绍
接受癌症诊断并管理随后的心理和生理攻击是一项艰巨的挑战。虽然在开发更有效、创伤更小的癌症治疗方法方面取得了巨大进展,但患者仍在与各种行为并发症作斗争,包括抑郁、疲劳、睡眠障碍和认知功能障碍。越来越多的研究已经开始对这些行为共病现象给予越来越多的关注,不仅从其流行程度和后果方面,而且最重要的是从潜在的共同潜在机制和相关的翻译含义方面。这种不断增长的知识将使人们更好地理解治疗策略,并最终指导临床管理。此外,这一知识将成为在癌症患者的日常护理中对行为进行更标准化评估的基础,并将行为实例化为“第六个生命体征”。
在这篇综述中,免疫学/肿瘤学和神经生物学/神经内分泌学的新研究将被描述为与癌症患者面临的主要行为挑战相关。更具体地说,将提供的数据表明,炎症反应增加,部分与神经内分泌系统的调节受损有关,与已知参与行为调节的病理生理通路相互作用,从而可能介导癌症患者行为症状的发展。(图1)值得注意的是,人们对炎症在行为病理学中的作用越来越认识到,炎症是包括心血管疾病、糖尿病和癌症在内的多种疾病中的一种常见机制。1此外,这一新的概念框架可能最终有助于整合癌症患者经历的行为共病谱,并为确定哪些患者在何种治疗条件下风险最大提供组织原则。本文还探讨了本研究的相关翻译含义以及未来的研究方向。
图1。癌症患者行为共病的神经内分泌免疫机制和介导物。
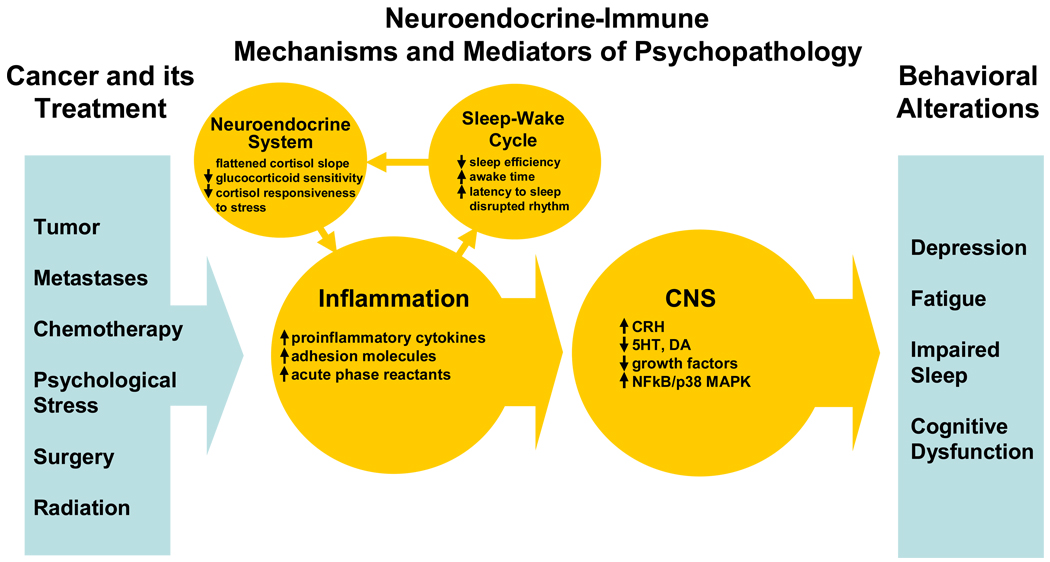
癌症诊断和治疗的各个方面通过组织损伤/破坏和/或心理压力激活炎症。固有免疫反应的细胞因子以及生活方式的改变、癌症的疼痛和其他后果及其治疗会改变睡眠周期,进而导致神经内分泌系统,尤其是下丘脑-垂体-肾上腺轴的破坏。鉴于HPA轴和糖皮质激素在调节炎症反应中的作用,改变HPA轴功能可能会破坏糖皮质激素介导的炎症负调控。无限制的炎症和相关的促炎细胞因子释放增加反过来又与调节行为的中枢神经系统(CNS)通路相互作用,导致病理生理变化,这些变化是抑郁、疲劳、睡眠障碍和认知功能障碍的基础。
炎症和行为
越来越多的数据表明,先天免疫反应(炎症)的激活可能有助于疾病和健康个体的行为改变。对实验动物和人类的研究提供了令人信服的证据,表明先天性免疫细胞因子可诱发一种“疾病行为”综合征,该综合征具有许多与癌症患者常见的行为共患性重叠的特征,包括抑郁、疲劳、睡眠障碍和认知功能障碍。2,三细胞因子的这些行为效应似乎是继发于外周细胞因子信号进入大脑并激活大脑内炎症反应的能力,然后这些炎症反应与已知参与行为障碍的病理生理途径相互作用。4–7事实上,细胞因子诱导的行为改变与相关神经递质(如血清素、去甲肾上腺素和多巴胺)代谢的改变有关,所有这些都在多种行为的调节中发挥着重要作用,是目前可用于治疗抑郁、焦虑和疲劳的精神药理学的主要靶点。8,9例如,先天性免疫细胞因子,包括干扰素(IFN)-α和白细胞介素(IL)-6,已被证明通过诱导吲哚胺2,3双加氧酶(IDO)耗尽氨基酸、色氨酸(5-羟色胺的主要前体)。10–13此外,通过激活p38丝裂原活化蛋白激酶(MAPK)信号通路,发现肿瘤坏死因子(TNF)-α和IL-1可增加血清素和去甲肾上腺素突触再摄取泵的功能和表达。综上所述,这些数据表明,先天性免疫细胞因子可能会对相关神经递质的突触可用性造成“双重打击”,14影响它们的合成和再摄取,从而可能促进行为改变的发展。8
天然免疫细胞因子也被发现增加神经肽促肾上腺皮质激素释放激素(CRH)的mRNA和蛋白。15,16CRH是下丘脑-垂体-肾上腺(HPA)轴的关键调节器,已发现在包括抑郁症在内的许多行为障碍患者的脑脊液中增加。17此外,实验动物服用促肾上腺皮质激素会导致行为改变,包括抑郁和焦虑样行为、睡眠障碍、厌食症和活动减少。17
先天性免疫细胞因子可能通过其对区域脑活动的影响而导致行为改变的另一种机制。这些影响已在癌症和传染病的IFN-α给药背景下进行了研究。例如,在视觉空间注意任务期间,功能磁共振成像显示,注射干扰素-α与前扣带回皮层(dACC)背部区域血流增加有关。18据信,dACC在发现身体和社会威胁、随后吸引注意力和应对资源以将危险降至最低方面发挥着重要作用。19值得注意的是,dACC活性增加已被证明存在情绪和焦虑障碍风险的个体,包括高特质焦虑、神经质和强迫症患者。18研究使用[18F] -氟脱氧葡萄糖(FDG)和正电子发射断层扫描(PET)显示,IFN-α给药也会导致前额叶皮层和基底神经节活动的显著变化,这分别与抑郁和疲劳的发展有关。20,21干扰素-α诱导的与基底神经节相关的神经认知功能改变(即精神运动减慢)也与癌症患者抑郁症状的发展有关。22
除了对支持各种认知过程和行为的大脑区域的功能产生影响外,对实验动物施用先天免疫细胞因子也被证明会破坏海马体的长期增强,从而破坏记忆巩固。23,24此外,活化的巨噬细胞释放IL-6已被证明可以介导头颅x射线照射对海马神经元祖细胞生长和发育的抑制作用。25
最后,正在进行的研究揭示了先天免疫细胞因子与睡眠周期紊乱之间的新关系(图1).26,27睡眠不足导致炎症的细胞和基因组标记28并导致固有免疫细胞因子和系统性炎症标志物(如C反应蛋白(CRP))的循环水平升高。29,30相反,在睡眠开始前,固有免疫细胞因子(如IL-6)的升高与睡眠潜伏期延长有关,31–33IL-6可降低δ波睡眠。34
心理压力和炎症
鉴于心理压力在各种行为障碍的发展中所起的众所周知的作用,35值得注意的是,压力可以激活外周和大脑中的炎症细胞因子及其信号通路[例如核因子-κB(NFkB)]。36–39此外,大鼠的数据表明,压力可以激活大脑中的小胶质细胞,并增加其对免疫刺激的敏感性[即脂多糖(LPS)]。38值得注意的是,大脑中应激诱导的IL-1已被证明显著降低脑源性神经营养因子(BDNF)的表达,BDNF被认为在神经元生长和发育、学习、突触可塑性以及最终的行为障碍中发挥关键作用。40,41
应激对大脑炎症途径的影响被认为是通过激活交感神经系统和释放儿茶酚胺介导的,儿茶酚酚胺与相关细胞上的α和β肾上腺素能受体结合。36,39有趣的是,最近的数据表明,副交感神经系统通过释放乙酰胆碱和随后激活烟碱乙酰胆碱受体的α7亚单位可以抑制炎症信号通路(例如NFkB),42这表明交感和副交感通路对应激期间的炎症反应有相反的影响。
炎症反应的神经内分泌调节
神经内分泌系统,特别是下丘脑-垂体-肾上腺(HPA)轴和糖皮质激素,在炎症反应的负调控中起主要作用。事实上,皮质醇等糖皮质激素是体内最有效的抗炎激素。43这些作用主要由糖皮质激素受体和包括NF-kB在内的相关炎症信号分子之间的蛋白质-蛋白质相互作用介导。44因此,通过改变糖皮质激素的释放(包括昼夜皮质醇节律的改变)或糖皮质激素受体功能的破坏,糖皮质激素信号的破坏可能会导致炎症反应的增加。与细胞因子在这一过程中的潜在作用相关的是,包括p38 MAPK在内的细胞因子信号通路已被证明会破坏糖皮质激素受体信号传导,45,46因此可能有助于降低免疫细胞对糖皮质激素抗炎作用的敏感性。糖皮质激素受体功能的破坏也可能导致HPA轴功能的改变,包括日间皮质醇生成变平,以及服用合成糖皮质激素后无法停止皮质醇的生成(非抑制),地塞米松[表现为异常地塞米森抑制试验(DST)]。值得注意的是,在患有严重抑郁症的健康受试者中,DST反应异常与外周血单核细胞(PBMC)产生IL-1的增加有关。47强烈和/或慢性应激也与HPA轴功能的改变有关,包括皮质醇生成减少、皮质醇昼夜节律变平和糖皮质激素受体功能降低,如对地塞米松的反应改变所示。48综上所述,这些数据表明,细胞因子和应激都可以协同改变HPA轴和糖皮质激素受体功能,导致内源性糖皮质激素抑制炎症反应的能力降低。
炎症及其神经内分泌系统调节的改变在癌症患者行为共病中作用的证据
有许多因素增加了癌症患者炎症途径激活的可能性(图1). 手术、化疗和放疗都与显著的组织损伤和破坏有关,而这些又与先天免疫反应的激活有关。此外,化疗药物和γ射线能够直接诱导NF-kB及其下游促炎基因产物。1此外,接受癌症诊断并与治疗、复发和死亡率方面的长期不确定性作斗争是可以想象的最大压力之一。考虑到压力对炎症反应的影响,癌症患者在接受治疗和接受癌症治疗时所固有的生理和心理挑战的综合作用,使其面临着发展炎症诱导的行为改变的高风险。以下将结合炎症及其神经内分泌系统调节的证据对这些行为变化中最常见的变化进行综述。
抑郁
在困扰癌症患者的所有行为共病中,重度抑郁症是一种研究最多、特征最明显的综合征,其特征是情绪低落和/或无快感,并伴有食欲、睡眠、活动水平和认知功能的改变。癌症患者的重度抑郁发生率很高,中位数患病率(15-29%)大约是普通人群的3-5倍。49,50除了对生活质量产生深远影响外,癌症患者的抑郁症还与医疗利用率增加、治疗依从性差以及在某些情况下癌症复发率和死亡率增加有关。49–52
在两项分别对诊断为重度抑郁症的癌症患者进行的研究中发现,与免疫系统在癌症患者抑郁中的作用有关,IL-6的血浆浓度升高(表1).53,54然而,结果并不一致,尤其是在研究炎症生物标志物和抑郁症状之间的相关性时(通过标准化抑郁评定量表进行测量)。然而值得注意的是,与研究其他疾病患者(包括心血管疾病)以及健康抑郁症患者的丰富文献相比,对抑郁症患者的研究却少得惊人,其中,大量研究揭示了炎症标记物与抑郁症的诊断和抑郁症状严重程度之间的明确关系。6
表1。
| 调查员 |
癌症类型 |
患者样本 |
免疫参数 |
行为共病 |
结果 |
| Greenberg等人,1993年63
|
前列腺 |
15名接受局部放射治疗的男性患者 |
IL-1(血清) |
疲劳 |
IL-1水平随着疲劳而增加。 |
| Morant等人,1993年74
|
混合的 |
31名男性和女性晚期癌症患者和30名健康对照 |
CRP、TNF、IL-1、IL-2R(血清) |
乏力症 |
在乏力症和免疫参数之间未发现有统计学意义的相关性。 |
| Knobel等人,2000年71
|
淋巴瘤 |
33名男性和女性患者接受BMT后4–10年 |
IL-6、TNF-α、sTNFR p55和p75(血清) |
疲劳 |
疲劳和免疫参数之间没有发现统计学上显著的相关性。 |
| Musselman等人,2001年53
|
混合的 |
21名男性和女性胰腺癌、乳腺癌和食管癌患者 |
IL-6(血浆) |
大萧条 |
与非抑郁症患者相比,患有抑郁症的癌症患者的IL-6显著升高。 |
| Geinitz等人,2001年66
|
乳房 |
41例接受保乳手术和放疗的女性患者 |
IL-1β、IL-6、TNF-α(血清) |
疲劳 |
疲劳与免疫参数之间没有相关性。 |
| Bower等人,2002年69
|
乳房 |
40名女性乳腺癌幸存者 |
IL-1β、IL-1ra、sTNFR p75、新喋呤(血清) |
疲劳 |
IL-1ra、TNFR-p75和新喋呤在疲劳患者中显著升高。在大多数患者中未检测到IL-1β。 |
| Bower等人,2003年150
|
乳房 |
39名女性乳腺癌幸存者 |
外周血淋巴细胞表型标记物IL-1ra(血清) |
疲劳 |
疲劳患者的CD3+、CD4+和CD56+数量显著升高,CD3+数量与IL-1ra相关。 |
| Wratten等人,2004年64
|
乳房 |
52名接受局部放射治疗的女性患者 |
IL-6、TNF-α、sICAM-1、TGF-β、PDGF、FGF、CRP(血清) |
疲劳 |
疲劳与基线时的IL-6、sICAM-1和CRP相关,与RT第5周的IL-6相关。控制BMI后,疲劳与免疫参数之间没有相关性。 |
| Dimeo等人,2004年72
|
淋巴瘤、AML、CML ALL、CLL |
71名男性和女性患者3个月内未接受化疗、放射免疫治疗 |
IL-1-α、IL-1ra、IL-6、新喋呤(血清) |
疲劳 |
疲劳与免疫参数之间没有相关性。 |
| Ahlberg等人,2004年67
|
子宫 |
15名接受局部放射治疗的女性患者 |
IL-1、IL-6、TNF-α(血液,未另行规定) |
疲劳 |
RT期间未发现细胞因子变化。疲劳变化与IL-1和TNF变化之间没有相关性。疲劳的变化与IL-6的变化呈负相关。在大多数患者中未检测到IL-1和TNF。 |
| Gelinas等人,2004年151
|
乳房 |
103名女性乳腺癌幸存者 |
IL-1β(血清) |
疲劳 |
疲劳与IL-1β之间没有相关性。IL-1浓度极高(平均值=1152 pg/ml) |
| Pusztai等人,2004年27
|
乳房 |
90名接受化疗的女性患者 |
IL-1β、IL-6、TNF-α、IL-8、IL-10、IL-12(血浆) |
疲劳、抑郁症状 |
在大多数患者中未检测到基线细胞因子水平。在接受紫杉醇化疗的患者中观察到IL-6、IL-8和IL-10的增加。细胞因子的变化与疲劳或抑郁的变化之间没有相关性。 |
| Brown等人,2005年75
|
肺癌 |
38例晚期癌症患者 |
CRP(血液,未另行规定) |
疲劳 |
疲劳与CRP呈正相关。 |
| Costanzo等人,2005年62
|
卵巢 |
61例女性晚期癌症患者术前检查 |
IL-6(血浆和腹水) |
疲劳、抑郁症状 |
疲劳与血浆IL-6呈正相关。抑郁症与IL-6之间没有相关性。 |
| Shafqat等人,2005年68
|
混合的 |
过去6个月内接受治疗的174名男性和女性患者 |
TNF-α(血液,未另行规定) |
疲劳 |
疲劳与TNF之间没有相关性。 |
| Rich等人,2005年79
|
结直肠 |
80名男性和女性转移性疾病患者 |
TNF-α、IL-6、TGF-α(血清) |
WHO表现,疲劳 |
WHO绩效状态>1的患者IL-6和TGF-α增加。TGF-α与疲劳相关。皮质醇节律减弱与TNF-α、IL-6和TGF-α增加相关。 |
| Meyers等人,2005年61
|
白血病 |
54名男性和女性ALS/MDS患者 |
TNF-α、IL-1、IL1ra、IL-6、IL-8(血清) |
神经心理表现,疲劳 |
较高的IL-6与较差的执行功能相关。较高的IL-8与较好的记忆表现相关。IL-6、IL-1ra和TNF-α与疲劳相关。 |
| Mills等人,2005年65
|
乳房 |
29名在蒽环类药物化疗之前和期间患有Ⅰ-ⅢA期疾病的女性 |
IL-6、sICAM、VEGF(血浆) |
疲劳,生活质量 |
sICAM和VEGF与疲劳加剧和生活质量下降有关。 |
| Collado Hidalgo等人200670
|
乳房 |
50名女性乳腺癌幸存者 |
外周血淋巴细胞表型标志物;IL-6、sIL-6R、IL-1ra、TNFR-p75(血浆);LPS刺激IL-6和TNF-α的细胞内表达 |
疲劳 |
疲劳患者血浆IL-1ra、sIL-6R、LPS刺激的IL-6和TNF-α升高,单核细胞表面IL-6R降低,活化T淋巴细胞和髓样树突状细胞减少。 |
| Jehn等人,2006年54
|
转移癌 |
114名男性和女性转移性(4期)疾病患者 |
IL-6(血浆) |
大萧条 |
抑郁症患者血浆IL-6显著升高。 |
| Bower等人。78
|
乳房 |
25名女性乳腺癌幸存者 |
外周血淋巴细胞表型标记物;LPS刺激应激后IL-1-β、IL-6、TNF-α的产生 |
疲劳 |
应激后疲劳患者与非疲劳患者相比,LPS刺激的IL-1-β和IL-6增加。 |
患有严重抑郁症的癌症患者也表现出神经内分泌变化,这可能导致炎症反应的激活,包括两项研究表明,糖皮质激素敏感性降低,表现为DST不抑制53,55(表2)还有一项研究显示,皮质醇昼夜曲线变平。53迄今为止,还没有研究表明抑郁症患者的HPA轴和/或糖皮质激素受体功能与炎症标记物增加有关。
表2。
| 调查员 |
癌症类型 |
患者样本 |
神经内分泌参数 |
行为共病 |
结果 |
| Evans等人,1986年55
|
混合的 |
47名女性患有不同阶段的子宫颈癌、子宫内膜癌和阴道癌 |
直流 |
大萧条 |
21%的患者为DST非抑制剂患者。40%的重度抑郁症患者是DST非抑制剂患者。 |
| Sephton等人,2000年86
|
乳房 |
104名患有转移性疾病的女性 |
唾液皮质醇昼夜节律 |
睡眠 |
皮质醇斜率变平与夜间觉醒增加和存活率降低相关。 |
| Musselman等人,2001年53
|
混合的 |
21名男性和女性胰腺癌、乳腺癌和食管癌患者 |
直流 |
大萧条 |
地塞米松治疗后血浆皮质醇浓度与抑郁相关,但与IL-6无关。 |
| Capuron等人,2003年10
|
黑色素瘤 |
20名男性和女性受试者,阶段III-IV |
促肾上腺皮质激素和皮质醇对干扰素-α的反应 |
大萧条 |
首次注射IFN-α后ACTH和皮质醇反应过度与IFN-α治疗期间抑郁的发生有关。 |
| Bower等人,2005年76
|
乳房 |
29名女性乳腺癌幸存者 |
清醒时以及连续两天1200、1700和2200小时采集的唾液皮质醇样本 |
疲劳 |
疲劳患者皮质醇斜率变平。 |
| Bower等人,2005年;77200778
|
乳房 |
27名女性乳腺癌幸存者 |
在紧张的公开演讲和心算任务中,每隔15分钟采集一次唾液皮质醇样本 |
疲劳 |
与对照组相比,疲劳患者的唾液皮质醇对压力的反应减弱。疲劳患者皮质醇反应迟钝与LPS刺激的IL-6生成增加相关。 |
| Rich等人,2005年79
|
结直肠 |
80名男性和女性转移性疾病患者 |
800和1600小时时获得的血清皮质醇 |
WHO表现,疲劳 |
皮质醇节律平缓与TNF-α、IL-6和TGF-α增加相关。 |
| Jehn等人,2006年54
|
转移癌 |
114名男性和女性转移性(4期)疾病患者 |
昼间皮质醇分泌 |
大萧条 |
与对照组相比,抑郁症患者的皮质醇昼夜分泌变化减少(即皮质醇节律变平)。 |
疲劳
疲劳是癌症治疗最常见、最令人痛苦的副作用之一。56根据样本和评估方法,治疗期间疲劳的患病率估计范围为25-99%。56,57虽然癌症治疗后疲劳通常会下降,但越来越多的证据表明,疲劳可能会在一个重要的患者亚群中持续数月或数年。58,59事实上,最近的一项研究发现,34%的无病乳腺癌存活者在诊断后5-10年内表现出明显的疲劳,60类似于在5年癌症幸存者的异质样本中获得的估计。59
许多研究表明,癌症患者在开始治疗前,炎症标记物与疲劳之间存在关联61,62以及在放射治疗期间63,64和化疗,65尽管有负面调查结果的报道(表1).27,66–68也有证据表明炎症过程在治疗后疲劳中起作用。例如,发现患有持续疲劳的乳腺癌幸存者与非疲劳幸存者相比,几种免疫激活标志物[即IL-1受体拮抗剂(IL-1ra)、可溶性TNF受体p75、新蝶呤]显著升高。69这些发现最近在一个较大的乳腺癌患者队列中得到了复制,疲劳的幸存者再次显示循环IL-1ra和可溶性IL-6受体升高,以及体外LPS刺激后单核细胞产生先天性免疫细胞因子增加。70对完成治疗的血液恶性肿瘤患者进行的两项研究发现,疲劳与炎症标记物之间没有关联。71,72然而,在这两份报告中,在诊断、疾病分期、治疗后的时间长度和疲劳症状持续时间方面存在很大的差异。此外,最近对现有文献的荟萃分析支持了炎症生物标记物与癌症幸存者疲劳之间的关系。73在晚期癌症(活动性疾病)患者中,有混合证据表明疲劳和炎症措施之间存在关联。74,75
有证据表明,疲倦的癌症幸存者细胞因子生成增加可能部分源于HPA轴功能的改变,包括昼间皮质醇分泌的改变和皮质醇对压力反应的降低(表2). 例如,早上血清皮质醇水平较低,69皮质醇昼间斜率变平,76以及皮质醇对急性心理社会应激反应迟钝77发现乳腺癌幸存者持续疲劳。有趣的是,在最近一项对疲劳乳腺癌患者的研究中,应激诱导的炎症反应增加(如对LPS刺激全血的IL-6反应增加)与应激诱导的唾液皮质醇反应减少相关。78炎症细胞因子的增加也与转移性结直肠癌患者皮质醇节律降低有关。79综上所述,这些数据表明,皮质醇分泌在昼夜周期和压力反应中的变化可能在过度炎症反应中起作用,而炎症反应又可能与包括疲劳在内的行为变化有关。
睡眠障碍
超过50%的癌症患者报告有睡眠问题,多导睡眠图数据证实睡眠效率降低,入睡潜伏期延长,夜间醒来时间增加。80,81即使在治疗之前,癌症患者也报告有明显的睡眠障碍,82在癌症幸存者中,睡眠问题远远超出了治疗范围。事实上,近20%的乳腺癌幸存者报告患有6个月以上的慢性失眠症。80,83睡眠障碍代价高昂。例如,失眠是癌症相关疲劳的有力预测因素,58,84,85睡眠活动和昼夜节律的紊乱可以预测转移性疾病患者死亡率的增加。86,87
有趣的是,尽管有数据表明IL-6等先天免疫细胞因子与睡眠之间存在关系,但炎症标记物与癌症患者睡眠之间的关系尚未得到研究。鉴于疲劳和炎症标记物之间的密切关系,似乎睡眠也可能存在类似的关系。显然,这方面需要进行研究。
睡眠障碍可能导致炎症增加的一个重要潜在机制是通过昼夜节律的失同步,包括皮质醇的释放(图1).88下丘脑与位于视交叉上核内的昼夜节律起搏器共同调节20小时昼夜皮质醇分泌。昼夜节律睡眠模式的强迫改变以及睡眠负债的诱导(如慢性睡眠障碍)与皮质醇节律的平缓有关,尤其表现为晚上皮质醇分泌活动增加,这是皮质醇释放的正常静止期。89,90此外,睡眠限制与大鼠ACTH对压力的反应降低有关。91尽管没有充分研究,但至少有一份癌症患者的报告显示,频繁夜间醒来所表现的昼夜节律紊乱与昼夜皮质醇节律平缓有关,而这反过来又与长期生存率降低有关。86,87癌症治疗期间,由于疲劳和白天不活动(导致夜间睡眠受损)的恶性循环和/或癌症治疗后的免疫激活和/或心理压力对睡眠周期的影响,可能会导致昼夜节律的破坏。进一步研究睡眠周期、炎症反应激活和皮质醇昼夜节律,显然有必要进一步阐明这些关系并确定治疗干预要点。
认知功能
癌症治疗期间的认知功能障碍严重影响生活质量和社会/职业功能,是患者管理中的一个主要问题。92癌症患者经常抱怨认知障碍,包括记忆力、注意力、执行功能和心理运动技能的改变。除了直接影响中枢神经系统(CNS)的癌症外,起源于外周组织的癌症也与神经心理变化的发生有关。这些认知变化往往是癌症治疗的次要影响因素,其中最显著的是化疗和放疗。大约25-33%接受全身化疗的患者在认知功能测试中表现出受损。93–96与化疗相关的认知功能障碍似乎具有剂量依赖性;高剂量与更大损伤相关。95,97虽然化疗期间的认知功能障碍通常在治疗后得到解决,但一些研究报告了残余的长期影响。98–100数据表明,化疗还与与认知功能障碍相关的区域脑活动的改变有关。101,102例如[18F] -对接受乳腺癌化疗患者的FDG PET研究表明,与认知障碍相关的背外侧前额叶皮层的代谢活性显著降低。103当直接针对大脑时,毫不奇怪,放射治疗经常伴随着神经并发症,这些并发症可能很严重,并在治疗后持续数年。104然而,有趣的是,在大脑以外的部位受到辐射后,有报道称出现了中度/暂时性认知改变。例如,一项对48名在保乳手术后接受术后放射治疗的女性进行的研究表明认知疲劳开始放射治疗4周和5周后疲劳评估问卷的子量表,与基线值进行比较。66
研究结果表明,炎症因子可能在癌症患者认知功能障碍的病理生理学中发挥作用。23例如,急性髓细胞白血病或骨髓增生异常综合征患者的血浆IL-6与执行功能之间存在显著的负相关(表1).61细胞因子对癌症患者认知影响的最显著例子可能是基于细胞因子的免疫疗法(如IFN-α和IL-2)的神经心理学后遗症。对接受高剂量干扰素-α治疗恶性黑色素瘤的患者进行的一项研究表明,患者经常出现中重度认知症状,尤其是注意力减退(30%的患者)、精神运动迟缓(40%)、记忆障碍(15%)和语言问题(15%)。105接受细胞因子治疗的患者的认知功能障碍在很大程度上取决于治疗参数(剂量、持续时间和给药途径)和给药的细胞因子。106因此,虽然干扰素-α治疗通常与精神运动速度和集中困难的降低有关,但IL-2治疗更经常与工作记忆和执行功能的改变有关。22高剂量细胞因子治疗引起的认知改变通常在治疗后逆转;然而,有报道称存在残余认知功能障碍。107,108
翻译含义
行为风险识别
基于提议的概念框架(图1)在接受与炎症反应激活相关的治疗(如手术、化疗、放射治疗)的患者中,感受到高水平压力(作为癌症诊断或其他生活环境的一个功能)的患者可能最容易发生行为改变。此外,风险增加可能与睡眠-睡眠周期的显著中断有关。行为共病发展的相对风险也可能受到遗传因素的影响。IL-6基因和5-羟色胺转运体基因的功能多态性可能特别相关,因为IL-6与癌症患者的几种行为病理学相关,并且5-羟色宁转运体多态性在应激和行为改变之间的关系中起到了明显的作用。109,110未来的研究明确了癌症及其治疗期间行为改变风险的心理和遗传特征。最后,作为正在进行的炎症在行为共病中的作用和风险识别研究的一部分,应考虑制定癌症患者炎症生物标记物的标准化评估。根据迄今为止的研究,在行为病理学和医学疾病方面,IL-6(通过高灵敏度酶联免疫吸附试验评估)和下游肝源性急性期反应物CRP的变化似乎是最可靠的。6,111–115的确,如所示表1许多癌症患者的研究揭示了IL-6和CRP与抑郁、疲劳和认知功能障碍之间的关系。此外,hsCRP可以在经认证的商业/医院实验室中运行,从而减少研究地点之间的差异。此外,在hsCRP的情况下,已经确定了临界值,该临界值既具有预测有效性,又具有与心血管疾病预后相关的风险分类。113考虑到癌症患者在治疗期间的波动状态,此外,还建议对行为和相关炎症生物标记物进行纵向评估,以增加识别这些变量之间相关关联的可能性,否则这些变量可能会被癌症治疗经历的变迁所混淆。检查癌症幸存者与健康年龄和性别匹配的对照组的炎症生物标志物是减少治疗对炎症和行为变化之间关系影响的另一种策略。
治疗性牺牲
鉴于对癌症患者行为共病潜在综合机制的普遍了解,针对导致广泛症状的途径进行转化研究有多种机会(表3).
表3。
神经内分泌-免疫相互作用与癌症患者行为共病的发展:转化靶点
| 免疫系统 |
| 细胞因子拮抗剂(如TNF-α、IL-1、IL-6) |
| 细胞因子信号通路拮抗剂(例如NFkB抑制剂、p38 MAPK抑制剂) |
| 抗炎药物(例如COX-2抑制剂、PGE2抑制剂) |
| 练习 |
| 神经内分泌系统 |
| CRH拮抗剂 |
| 糖皮质激素受体促进剂(例如磷酸二酯酶IV型抑制剂) |
| 睡眠-睡眠循环 |
| 时间疗法(例如褪黑激素、光疗或睡眠调节) |
| 行为疗法(认知行为疗法、分级运动、改善睡眠卫生) |
| 中枢神经系统 |
| 5HT、NE、DA再摄取抑制剂(例如抗抑郁药) |
| DA激动剂 |
| 神经保护剂(例如生长因子) |
| 强调 |
| 认知行为治疗(例如压力管理、应对技能、分级训练) |
| 放松训练 |
| 支持性心理治疗 |
| 抗焦虑药物(如苯二氮卓类) |
心理治疗/行为干预
考虑到压力诱导的炎症和神经内分泌系统对炎症反应的调节改变的潜在作用,减轻压力和恢复正常昼夜节律的认知行为、支持性或洞察力导向的心理治疗师可能特别相关。相关的认知行为策略包括放松训练、提高应对技能、分级锻炼、建立适当的睡眠习惯和社交节奏(例如标准化的睡觉和起床时间、避免日间小睡、纠正对睡眠的不适应观念)。116–127这种干预可能限制应激对免疫反应的影响,并可能对神经内分泌-免疫相互作用产生直接影响。事实上,认知-行为压力管理和基于思维的压力减轻等心理干预措施已被证明可以缓解乳腺癌患者的心理困扰,同时增加淋巴细胞增殖反应并使每日皮质醇分泌正常化。122–127还有证据表明,有氧运动可以降低癌症幸存者的炎症标记物,128炎症变化可能会介导运动(可能还有其他行为疗法)对癌症相关行为共病的有益影响,这是未来研究的重要途径。129有趣的是,最近的一项认知行为治疗计划侧重于应对、睡眠、体力活动和社会支持,发现54%的癌症幸存者的疲劳程度显著改善,而对照组患者的疲劳程度为4%。116关于改变睡眠周期对癌症患者神经内分泌和免疫功能的影响,Irwin及其同事发现,多种行为疗法(如认知行为疗法、放松疗法、仅行为疗法)在睡眠质量、睡眠开始、,原发性失眠症成年人的睡眠维持130扩展了先前研究的结果。131,132然而,这些方法对癌症患者失眠的疗效知之甚少。83,133事实上,只有一项对照研究检测了行为干预对癌症患者失眠的疗效,134其他研究由于缺乏对照组和/或样本量小而受到限制。135,136此外,没有研究评估这些干预措施对皮质醇节律、炎症介质或行为改变的影响。
生物干预
虽然还需要进一步的研究来描述炎症标记物与癌症患者行为之间的关系;细胞因子拮抗剂、抗炎药和干扰细胞因子信号通路的药物(如NFkB和p38 MAPK)是合理的治疗考虑因素,针对细胞因子对CNS对行为级联中最上游的元素。值得注意的是,鉴于NF-kB和p38通路在癌症发展和进展中的作用,行为科学家有令人兴奋的机会与肿瘤学家合作,检查炎症通路相关拮抗剂的全谱活性。例如,最近的几项试验表明,用依那西普阻断TNF-α对晚期癌症患者是安全的,并且至少有一项研究表明,化疗的耐受性(包括减轻疲劳)得到了改善。137–139
进入中枢神经系统,针对特定症状域的特定单胺类系统的药物制剂(例如用于情绪/焦虑症状的血清素活性药物、用于疲劳和精神运动减慢的多巴胺活性药物)可能是解决神经递质系统中炎症诱导的变化的最佳方法。例如,在对接受治疗的癌症患者进行的至少两项双盲安慰剂对照试验中,发现帕罗西汀(一种血清素再摄取抑制剂)可以减轻抑郁,但对疲劳的影响有限。105,140另一方面,初步证据表明,精神刺激剂哌醋甲酯等多巴胺能药物可以治疗癌症患者的疲劳并改善其神经心理功能141肿瘤相关器质性脑功能障碍患者。142,143
如上所述,CRH由先天性炎症细胞因子刺激,是另一个合理的中枢神经系统靶点,尽管目前还没有CRH拮抗剂,但初步迹象表明这些药物可能对其他健康个体的抑郁症有疗效。144通过促进糖皮质激素受体功能,增强糖皮质激素介导的CRH通路负反馈的药物可能会控制CRH的过度表达。此类药物(包括磷酸二酯酶IV型抑制剂)可能具有额外抑制炎症途径的优势。145支持神经元完整性/可塑性的新疗法(神经保护剂),包括刺激相关生长因子(如BDNF)活性或信号传导的药物,对未来的发展可能特别重要。146,147
关于睡眠和神经内分泌节律,结合时间生物素的疗法(例如褪黑激素受体激动剂、光疗或睡眠调节)可能会使癌症患者的昼夜节律与其环境同步,与这些策略用于治疗时差或轮班工作引起的暂时性心律失常的方式相同。这种治疗可能有助于恢复神经内分泌节律,减少炎症,并可能提高癌症治疗的疗效。148,149
总结
本文描述的研究提供了一个概念框架,旨在整合一系列行为共病,这些行为共病可能具有共同的病理生理特征,有助于识别具有广泛治疗相关性的风险和靶向干预。进一步研究神经内分泌免疫相互作用与多种癌症患者睡眠周期改变和行为共病相关,可能会对癌症及其治疗对行为改变的贡献产生新的见解,并且,行为共存对癌症发展、进展和复发的贡献。最后,鉴于人们对癌症患者行为合并症的病理生理学和治疗越来越了解,标准化的行为评估成为癌症患者常规护理的一部分尤为重要。因此,将行为实例化为第六个生命体征将大大有助于强调进一步研究的必要性以及认识和治疗癌症及其治疗的行为后果的重要性。
致谢
作者要感谢Paige McDonald博士对这份手稿的宝贵投入和支持。该项目部分由国家癌症研究所(NCI)、癌症控制与人口科学、基础与生物行为研究、疾病中心理社会效应的生物机制资助;NCI CA85264、NCI CA112035和CBCRP 11IB-0034、M01-RR00865授予SA-I;NCI CA090407授予JEB;国家心理健康研究所向AHM提供MH069124;美国国立卫生研究院(National Institutes of Health)将AG026364、HL079955、T32-MH19925、CA 0014152授予MRI和Cousins心理神经免疫学中心。
参与者信息
安德鲁·米勒(Andrew H.Miller),佐治亚州亚特兰大埃默里大学医学院
Sonia Ancoli-Israel,加利福尼亚大学圣地亚哥分校
Julienne E.Bower,加州大学洛杉矶分校
法国波尔多波尔多大学露西尔·卡普隆
Michael R.Irwin,加州大学洛杉矶分校



