胰腺导管腺癌(PDAC)是肿瘤学中预后最差的疾病之一,5年生存率<5%,迫切需要新的治疗方案( Bardeesy和DePinho 2002 ). 该病的早期特征是胰腺上皮内瘤样病变(PanIN)在 喀斯特 原癌基因,通过积累其他途径的突变而发展为恶性PDAC,最常见的是肿瘤抑制基因 p16-墨水4A , Trp53基因 、和 Smad4公司 ( Tuveson和Hingorani 2005年 ; Bardeesy等人,2006a ; Hezel等人,2006年 ). 对人类患者中经常发生的突变的了解指导了新一代PDAC小鼠模型的工程,该模型更忠实地再现了人类疾病的病理学( Aguirre等人,2003年 ; Hingorani等人,2003年 )其中,可以评估其他信号通路对PDAC肿瘤发生的贡献。
在初步观察到正常胰腺中检测不到的Sonic Hedgehog配体(Shh)在PDAC样本中高度表达后,Hedgehong通路最近被牵涉到PDAC的形成中( Berman等人,2003年 ; Thayer等人,2003年 ). 典型的刺猬信号需要刺猬家族配体如Shh与Patched(Ptch)12结合 反式 -膜域受体,导致Smoothened(Smo)七 反式 -膜域蛋白。 激活的Smo诱导Gli转录因子家族转录活性成员的核转位,并由此导致Gli转录因子家族转录的升高 格利 靶基因,包括 第1部分 和 Gli1公司 ( 帕斯卡·迪马格里亚诺(Pasca di Magliano)和希布罗克(Hebrok),2003年 ; Jacob和Lum 2007 ). 该信号通路的组成性激活,通过失活 普奇 受体,激活突变 平滑(Smo) ,或提升表达 胶质细胞1 是基底细胞癌、髓母细胞瘤和其他几种癌症的主要促瘤特征( Taipale and Beachy 2001年 ; 鲁宾和德索瓦吉2006 ).
一些证据支持这样的观点,即刺猬信号在胰腺癌的发生中起着重要的功能作用。 首先,强制表达 嘘 在小鼠发育过程中足以诱发类似于PanINs的损伤( Thayer等人,2003年 ; Morton等人,2007年 ). 其次,以前肠发育标记和典型Gli靶基因高表达为特征的Gli驱动转录程序在PanINs中很明显( Thayer等人,2003年 ; Prasad等人,2005年 ). 第三,激活 喀斯特 与激活的合作 Gli2公司 诱导未分化胰腺肿瘤( Pasca di Magliano等人,2006年 ). 最后,据报道,Smo活性抑制剂环胺可诱导细胞凋亡并阻断原发性肿瘤的形成( Thayer等人,2003年 )或转移性传播( Feldmann等人,2007年 )几个PDAC细胞系移植后。 这些结果支持自分泌Shh信号刺激PDAC形成的假说( Rustgi 2006年 ; Jacob和Lum 2007 ). 最近的一项研究确定了下游刺猬信号成分的突变,包括 GLI1型 和 英语3 在所有仔细检查过的人类胰腺癌细胞系中,支持这样的观点,即这种途径对PDAC的形成具有重要的细胞自主性( Jones等人,2008年 ).
虽然在PDAC形成中明确涉及Gli转录和Shh信号传导,但上述研究本身并没有建立自分泌Shh信号或Gli转录在胰腺导管肿瘤发生中的要求。 其中的研究 嘘 和 Gli2公司 事实上,这些贡献被解释为分别是自分泌和细胞自主,并不排除刺猬信号对PDAC形成的潜在关键基质贡献( Thayer等人,2003年 ; Pasca di Magliano等人,2006年 ; Morton等人,2007年 ). 事实上,最近的一项研究表明Smo介导的刺猬信号在基质中起着明确的作用,但在刺猬配体表达的肿瘤细胞移植的异种移植物的上皮细胞室中不起作用( Yauch等人,2008年 ).
为了阐明肿瘤细胞中刺猬信号转导对PDAC发展的重要性,并更好地定位刺猬信息转导的关键节点,以便对该疾病进行潜在的治疗干预 平滑(Smo) 在PDAC致癌模型中,导管上皮需要辅受体 喀斯特 -驱动性恶性肿瘤。 我们确定 平滑(Smo) 在PDAC肿瘤发生过程中,Gli在胰腺上皮中是不必要的,然而在缺乏Smo介导的刺猬信号的情况下,Gli转录靶点的表达仍然保持不变。 然后,我们描述了对Smo-independent Gli转录调控机制以及该转录因子对PDAC细胞生存和转化的需求的初步研究。
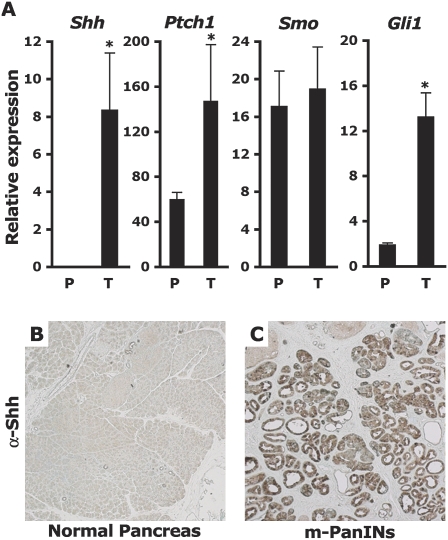
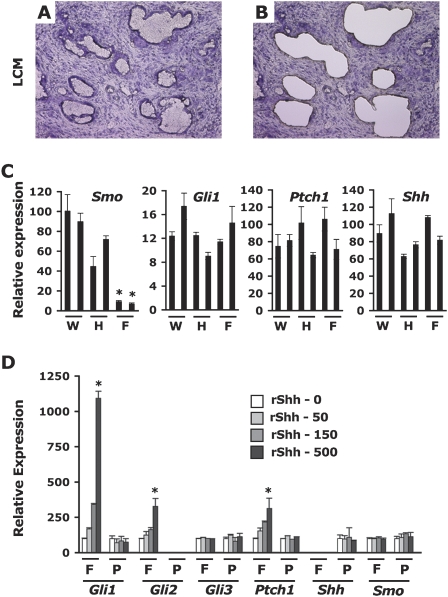
结果 消融Smo在PDAC荷瘤小鼠胰腺中的表达 先前描述了本研究中使用的基因工程PDAC模型的变体( Bardeesy等人,2006a ):模型由激活的 喀斯特 第12天 条件等位基因( LSL-Kras公司 )( Tuveson等人,2004年 ),杂合条件 Trp53基因 功能丧失等位基因( Trp53基因 如果 )( Jonkers等人,2001年 )、和 Cre公司 靶向内源性的重组酶 Ptf1-p48型 轨迹( p48芯 )( Kawaguchi等人,2002年 ). 化合物 p48芯 /+; LSL-Kras公司 G12D系列 /+ ; Trp53基因 如果 /+ 小鼠在出生后4周内出现低度PanIN损伤,9至13周龄发展为侵袭性PDAC,出生后10至29周死于该病,50%的动物在出生后16周内死亡。 PanIN样和PDAC病变来自 p48芯 /+; LSL-Kras公司 第12天 /+ ; Trp53基因 如果 /+ 小鼠表达高水平的 嘘 信使核糖核酸( 图1A ). 正常胰腺组织中未检测到Shh蛋白表达( 图1B )但很容易检测到,仅限于PDAC切片中的导管细胞( 图1C ). 来自该模型的PDAC肿瘤样本也表达了明显水平的 平滑(Smo) mRNA,以及高水平的 第1部分 和 Gli1公司 mRNA( 图1A ).
图1。
刺猬通路成分在PDAC病变中被解除调控。 ( A类 )的表达式 嘘 , 第1部分 , 平滑(Smo) 、和 Gli1公司 约12周龄的总RNA提取物中的mRNA LSL-Kras公司/ +; 第53页 F类/+ 对照胰腺(P)( N个 =3)或 p48芯 /+; LSL-Kras公司 /+; 第53页 如果 /+ 肿瘤(T)( N个 = 3). mRNA水平表示为 mGus公司 控制mRNA。星号表示 P(P) -值<0.01。 ( B类 , C类 )Shh(50×)的免疫化学检测。 ( B类 )正常胰腺未见Shh。 ( C类 )9周龄PDAC小鼠PanIN病变导管细胞内检测到Shh表达。 这些面板代表了两个对照组和两个PDAC小鼠的多个胰腺切片区域。
我们比较了杂合和纯合小鼠PDAC的形成 平滑 条件丧失功能等位基因( 平滑(Smo) 如果 )( Long等人,2001年 ). Smo杂合子小鼠被用作对照,因为之前描述了 平滑(Smo) -空等位基因没有显示单倍体不足表型( Zhang等人,2001年 ). 因此, p48芯 /+; LSL-Kras公司 G12D系列 /+ ; Trp53基因 如果 /+ ; 平滑(Smo) 如果 /+ 小鼠(PDAC Smo F类/+ )与进行了比较 p48芯 /+; LSL克拉斯 G12D系列 /+ ; Trp53基因 如果 /+ ; 平滑(Smo) 如果 / 平滑(Smo) 如果 小鼠(PDAC Smo 上下 )其发展为PanIN样和PDAC病变的倾向及其总体生存率。
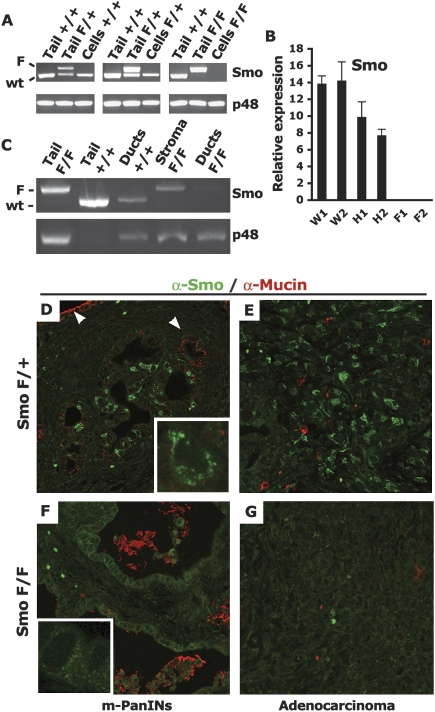
我们首先确定 平滑 通过对这些小鼠PDAC肿瘤细胞株的PCR分析,该等位基因在该模型中得到了正确重组。 三分之三独立衍生的PDAC Smo F类/+ 细胞系携带重组 平滑(Smo) 如果 等位基因和四分之三的独立衍生PDAC Smo 上下 细胞系已经将两者重组 平滑(Smo) 如果 等位基因( 图2A ; 数据未显示)。 我们确认 平滑(Smo) 实时定量RT-PCR检测这些细胞中的mRNA( 图2B ). 此外,为了研究 平滑(Smo) 如果 在胰腺导管等位基因中,我们从PDAC Smo中对肿瘤胰腺的导管结构进行了激光捕获显微切割 F类/+ 和PDAC Smo 上下 小鼠:对两种基因型的导管病变池的分析表明 平滑(Smo) 如果 等位基因在肿瘤导管中广泛重组,但在周围基质中没有重组( 图2C ). 最后,为了验证PDAC Smo中Smo蛋白的损失 上下 胰腺导管,我们对PDAC Smo切片进行荧光免疫染色 F类/+ 和PDAC Smo 上下 9.5岁PDAC荷瘤小鼠的肿瘤。 PDAC Smo中易于检测到颗粒细胞质Smo染色模式 F类/+ 截面( 图2D,E ),类似于所描述的( Incardona等人,2002年 ). Smo中约30%的导管细胞 F类/+ 导管病变表达高水平的Smo蛋白( 图2D ). PDAC Smo中也检测到强Smo染色 如果/+ 肿瘤( 图2E ). 相反,Smo染色在Smo中缺失 上下 导管和肿瘤( 图2F、G ). H&E对连续切片进行染色,以显示 图2,E和G ,表示腺癌区域(补充图1)。 PDAC Smo中的Smo蛋白缺失 上下 小鼠分布广泛,包括在一个PDAC Smo中保留罕见的Smo阳性细胞 上下 小鼠的两个PDAC Smo肿瘤切片完全没有染色 上下 老鼠。 总的来说,这些分析表明,Smo在PDAC Smo导管细胞室中的表达基本消失 上下 老鼠。
图2。
PDAC导管细胞中的平滑细胞被耗尽 上下 老鼠。 ( A类 )重新组合 平滑(Smo) PDAC细胞系中的位点。 PCR扩增 平滑(Smo) 基因座(Smo)或p48-Cre转基因(p48)。 这个 平滑(Smo) 基因分型程序放大非结合条件 平滑(Smo) 如果 等位基因(上带,F)和野生型(wt) 平滑(Smo) 等位基因(低带,野生型)。 当Cre重组 平滑(Smo) 条件位点。 每个PCR反应中使用的输入基因组DNA表示为:(Tail)来自小鼠尾部的基因组DNA,100 ng; (细胞)来自PDAC衍生的肿瘤细胞系的基因组DNA,10ng; (+/+) 平滑(Smo) +/+ ; (F/+) 平滑(Smo) F类/+ ; (前/后) 平滑(Smo) 上下 . ( B类 )耗尽 平滑(Smo) mRNA在重组细胞系中的表达。 总RNA提取物中Smo mRNA的表达 平滑(Smo) +/+ (W) , 平滑(Smo) F类/+ (H) ,或 平滑(Smo) 上下 (F) PDAC细胞系。 mRNA水平以m-Gus对照mRNA的百分比表示。对每个基因型的两个细胞系的总RNA提取物进行三次分析。 ( C类 )体内重组 平滑(Smo) 轨迹。 通过激光捕获显微切割(LCM)从PDAC肿瘤中分离出的导管结构或间质区域的基因组DNA进行与 A类 将每个基因型的两个PDAC肿瘤的导管或间质区合并,并进行PCR扩增。 每个PCR反应中使用的输入基因组DNA表示为:(尾部)来自小鼠尾部的DNA; (导管)LCM捕捉到两个PDAC肿瘤的导管; (基质)LCM捕捉到两个PDAC肿瘤的基质丰富区; (+/+)平滑 +/+ ; (F/+)平滑 F类/+ ; (F/F)平滑 上下 . ( D–G型 )体内Smo蛋白耗竭。 Smo(绿色)和Muc-1(红色)的免疫荧光检测(630×)。 在PDAC Smo内的一组粘蛋白阴性导管中检测到Smo蛋白 F类/+ PanIN样病变( D类 )但不存在于粘蛋白阳性导管(白色箭头)和粘蛋白阴性PDAC Smo中 F类/+ 腺癌病变( E类 ). 在PDAC Smo中无法检测到Smo 上下 PanIN样病变( 如果 )或PDAC Smo 上下 腺癌( G公司 ). 单个PDAC Smo的颗粒细胞质Smo染色 F类/+ 电池(2520×)( D类 , 插入 )个人PDAC Smo中缺失 上下 单元格( 如果 , 插入 ). 这些面板代表了三个PDAC Smo胰腺切片的多个区域 F类/+ 小鼠和三个PDAC Smo 上下 老鼠。
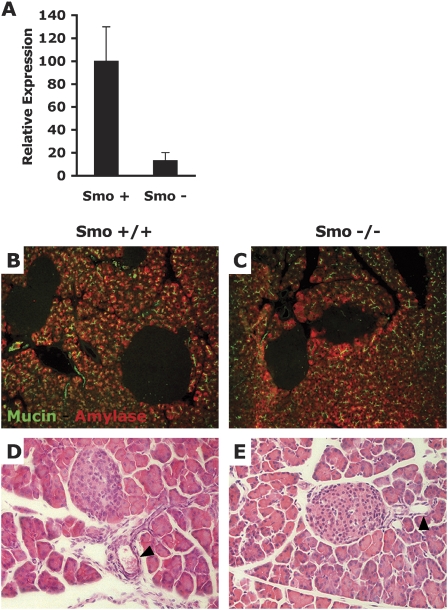
平滑的消耗不会影响胰腺外分泌的发育 在描述 平滑(Smo) 在导管癌变过程中,我们试图验证 平滑(Smo) 这并不影响胰腺的正常发育,因为胰腺中预先存在的发育缺陷原则上会使任何肿瘤表型的解释复杂化。 为此,我们比较了来自 Pdx Cre公司 ; 平滑(Smo) +/+ 和 Pdx-Cre公司 ; 平滑(Smo) F/空 在小鼠中观察到轻微的胰腺内分泌缺陷(J.Lau和M.Hebrok,未证实)。 对12.5日龄胚胎胰腺分离芽cDNA的定量PCR分析表明 平滑(Smo) 突变株的mRNA减少了近90% 平滑(Smo) 胰腺芽提取物( 图3A ). 这一结果表明,绝大多数胰腺祖细胞 Pdx-Cre公司 ; 平滑(Smo) F/空 老鼠基因缺失 平滑(Smo) 功能。 我们对野生型和 平滑(Smo) 用抗Muc1抗体标记导管细胞,用抗α-淀粉酶抗体标记腺泡细胞的突变胰腺。 两组胰腺的两种染色均无差异( 图3B、C ). 此外,我们对野生型和 平滑(Smo) H&E突变胰腺,未发现形态差异( 图3D,E ). 我们得出结论,导管和腺泡谱系的发育在缺乏 平滑 肿瘤表型发生在缺乏 平滑(Smo) 不会受到先前存在的导管或腺泡发育缺陷的影响。
图3。
在没有Smo功能的情况下,胰腺导管和腺泡的发育是正常的。 ( A类 )定量RT-PCR比较 平滑(Smo) 12.5-d分离胰腺芽总RNA提取物中的mRNA Pdx-Cre公司 ; 平滑(Smo) +/+ (平滑 + )胚胎和 Pdx-Cre; 平滑(Smo) F/空 (平滑 − )胚胎。 ( B类 , C类 )胰腺切片的抗Muc1和抗α-淀粉酶染色 Pdx-Cre公司 ; 平滑(Smo) +/+ 老鼠( B类 )和 Pdx-Cre公司 ; 平滑(Smo) 如果 / 空 老鼠( C类 ). ( D类 )胰腺切片的H&E染色 Pdx-Cre公司 ; 平滑(Smo) +/+ 小鼠和 Pdx-Cre; 平滑(Smo) F/空 老鼠。 箭头表示胰腺导管。 这些面板代表了两个胰腺切片的多个区域 Pdx-Cre公司 ; 平滑(Smo) +/+ 和两个 Pdx-Cre公司 ; 平滑(Smo) 如果 / 无效的 老鼠。
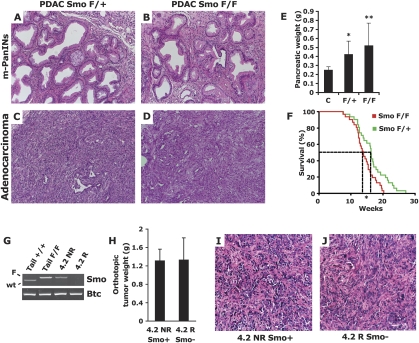
平滑耗尽对PDAC形成的影响 在我们研究中使用的PDAC转基因模型中,胰腺在突变体激活后发生了深刻的表型变化 喀斯特 G12D系列 和杂合子缺失 Trp53基因 遍及发育中的胰腺。 在腺泡导管化生过程之后,9.5周龄时,几乎所有外分泌胰腺都被肿瘤性导管结构取代。 在这个阶段,腺癌病灶与许多含有PanIN样病变的导管病灶混合,由激活的成纤维细胞和免疫细胞组成的厚厚的激活基质相互分隔( 图4A、C ). 当我们比较PDAC Smo的组织病理学时 F类/+ 和PDAC烟雾 上下 胰腺,我们发现Smo的病理学没有明显差异 F类/+ 和Smo 上下 老鼠。 对每个队列中五只小鼠的胰腺进行的分析显示,类似PanIN样病变的病灶被激活的基质包围( 图4A、B )伴随以显著促结缔组织增生成分为特征的散在浸润性腺癌病变( 图4C、D ). 因此,腺泡导管上皮化生和PanIN及腺癌病变的形成并没有受到 平滑(Smo) 在PDAC Smo中 上下 老鼠。 我们还注意到粘液阴性PanIN样病变的导管中完全没有Smo染色( 图2F )PDAC肿瘤区域( 图2E )强调这些晚期肿瘤病变可以在缺乏Smo的情况下发展。
图4。
胰腺上皮中Smo的遗传缺失并不影响PDAC肿瘤的发生。 ( A–D )组织病理学的H&E分析 PDAC Smo公司 F类/+ ( A类 , C类 )和 PDAC Smo公司 上下 ( B类 , D类 )病变显示PanIN样病变的表现无明显差异( A类 , B类 )或PDAC( C类 , D类 ). ( E类 )PDAC Smo的胰腺重量无显著差异 F类/+ 小鼠(F/+; N个 =10)和PDAC Smo 上下 小鼠(F/F; N个 =11)可以检测到[(**) P(P) =0.378)],但在荷瘤小鼠和对照非荷瘤小鼠的胰腺重量之间观察到显著差异[ N个 = 13; (*) P(P) < 0.01]. ( 如果 )PDAC Smo队列的平均生存率 F类/+ 小鼠(绿线; N个 =31)显著大于[17天;(*) P(P) 与PDAC Smo相比,<0.05] 上下 小鼠(红线; N个 =31)。 这些面板代表了八个PDAC Smo胰腺切片的多个区域 F类/+ 老鼠和八只PDAC Smo 上下 老鼠。 ( G公司 )体外重组 平滑(Smo) 源自非融合PDAC 4.2 NR细胞系的PDAC 4.2 R细胞系中的基因座。 PCR扩增 平滑(Smo) 轨迹(Smo)或 Betacellulin公司 控制轨迹( 生物技术委员会 ). 平滑(Smo) 基因分型:未重组 平滑(Smo) 如果 等位基因(上带,F)和野生型 平滑(Smo) 等位基因(低带,野生型)。 当Cre重组 平滑(Smo) 条件基因座。 输入的基因组DNA表明:(尾部)来自小鼠尾部的基因组DNA; 非融合PDAC细胞系(4.2NR)基因组DNA; (4.2R)来自体外重组PDAC细胞系的基因组DNA。 ( H(H) )裸小鼠原位注射4.2 NR胰腺肿瘤的平均重量( N个 =8,平滑 + )或4.2 R电池( N个 =8,平滑 − ). 未检测到显著差异。 ( 我 , J型 )4.2 NR的H&E染色(Smo + )和4.2 R(Smo − )异种移植瘤切片。 这些面板代表了四个4.2 NR和四个4.2 R胰腺肿瘤的多个胰腺切片区域。
考虑到9.5周龄时没有正常胰腺残留,我们使用全胰腺重量作为肿瘤负担的替代测量。 使用这个指标,我们发现PDAC小鼠的胰腺重量大约是Cre阴性对照动物的两倍。 值得注意的是,我们发现Smo与Smo在胰腺肿瘤重量上没有统计学差异 F类/+ 和Smo 上下 动物( 图4E ). 此外,我们对两组31只小鼠进行了年龄测定,以评估PDAC Smo之间可能存在的生存差异 F类/+ 和PDAC Smo 上下 老鼠。 如果PDAC癌细胞产生的Shh以自分泌方式促进肿瘤生长,我们预计PDAC Smo 上下 导管Shh信号传导丧失的小鼠比其PDAC Smo活得更长 F类/+ 室友。 然而,令我们惊讶的是,PDAC Smo 上下 动物平均比PDAC Smo提前17天死亡 F类/+ 对应方( 图4F ). 这种统计上显著的差异可能是由不同小鼠品系之间的轻微遗传变异所解释的,这些小鼠品系是为了产生PDAC Smo 上下 和PDAC Smo F类/+ 复合小鼠。 PDAC Smo缺乏生存优势 上下 然而,老鼠清楚地证明了这一点 平滑(Smo) 在这些小鼠中,缺失并不能减轻PDAC诱导的发病率。
因为有几个 平滑(Smo) -阳性细胞持续存在于三种PDAC Smo中的一种 上下 对老鼠进行了分析,出现了一种可能性 平滑(Smo) PDAC肿瘤内部的功能可能由一些具有干细胞样特性的孤立细胞传递。 在这种情况下,即使是少数剩余的Smo阳性细胞也可能足以执行PDAC肿瘤生长所需的肿瘤细胞固有功能,从而消融 平滑(Smo) 90%以上的癌细胞可能不足以在PDAC肿瘤发生中产生可观察到的缺陷。 为了解决这种可能性,我们进行了第二次实验,其中 平滑(Smo) 功能完全消融。 我们从PDAC Smo中获得的胰腺肿瘤衍生细胞系之一 上下 小鼠在未重组its的情况下进行了转化 平滑(Smo) 条件等位基因( 图4G ,车道3)。 我们继续删除 平滑(Smo) 通过在体外感染表达 Cre公司 重组酶。 通过这个过程,我们获得了基因匹配的PDAC细胞系,这些细胞系的差异仅在于它们的重组状态 平滑(Smo) 条件等位基因( 图4G )我们将其命名为4.2 NR(非合成)和4.2 R(重组)。 我们将每个细胞系中的10000个细胞原位注射到两组八只裸鼠的胰腺中,以评估其体内发生PDAC肿瘤的倾向。 2.5周后,处死两组小鼠,并测量其胰腺肿瘤的重量。 注射4.2NR和4.2R细胞的裸鼠肿瘤重量没有差异( 图4H ). 此外,这些肿瘤的H&E染色切片没有明显的形态学差异( 图4I,J ). 确保 平滑(Smo) 等位基因在4.2NR细胞中没有在体内自发重组,我们对其进行了基因分型 平滑(Smo) 基因座,并在4.2NR中检测到非结合等位基因,但没有检测到4.2R肿瘤基因组DNA(补充图2)以及野生型 平滑(Smo) 全肿瘤DNA中存在等位基因是因为 平滑(Smo) 肿瘤中存在野生型宿主间充质细胞。
因此,靶向消融 平滑(Smo) 在胰腺上皮细胞中,不会影响用于发展PDAC的小鼠的肿瘤等级或肿瘤负担,也不会带来生存优势。 我们得出结论,自分泌Shh信号通过 平滑(Smo) PDAC的发生和发展不需要胰腺导管细胞。
Gli靶基因维持的Smo依赖机制 我们的实验证明 平滑(Smo) 胰腺导管上皮对PDAC的发生和发展是不可或缺的。 有人预计,通过Smo失去Shh信号将导致刺猬靶基因的下调,如 Gli1公司 和 第1部分 这反过来表明,Gli转录程序可能下调,而不会对胰腺癌细胞产生不利影响,这是一个有点出乎意料的结果,因为研究表明Gli转录是这种疾病的显著特征( Thayer等人,2003年 ; Prasad等人,2005年 ). 为了在体内探索这一问题,我们从PDAC Smo获得的冷冻肿瘤切片中对导管结构进行了激光捕获显微解剖 +/+ 、PDAC Smo F类/+ ,或PDAC Smo 上下 老鼠( 图5A、B ). 我们从这些微细切割的导管中提取总RNA,以评估 第1部分 和 Gli1公司 转录本,两个已知的Gli靶基因。 我们还分析了 嘘 成绩单。 我们发现 平滑(Smo) 在显微解剖的肿瘤性Smo中表达显著降低 上下 风管与类似Smo的比较 F类/+ 和Smo +/+ 导管,表达水平 第1部分 和 Gli1公司 不会受到基因消融的显著影响 平滑(Smo) ( 图5C ). 这个意想不到的观察揭示了 胶质细胞1 和 第1部分 在肿瘤导管细胞中通过 平滑(Smo) -独立机制。
图5。
第1部分 和 Gli1公司 在体内Smo缺失的肿瘤导管细胞中保持表达。 ( A类 , B类 )胰管激光显微切割术前( A类 )以及之后( B类 )在H&E染色的冰冻肿瘤切片上捕获(50×)。 ( C类 )的表达式 平滑(Smo) , 第1部分 , 嘘 、和 Gli1公司 从两个PDAC Smo的激光捕获微细切割胰腺管池中提取的总RNA中的mRNA +/+ (W) ,两个PDAC Smo F类/+ (H) ,和两个PDAC Smo 上下 (F) 肿瘤。 mRNA水平以m-Gus对照mRNA的百分比表示( D类 )在原代胰腺成纤维细胞(F)或PDAC细胞系3.3(P)中增加重组Shh浓度(0–50–150–500 ng/mL)刺激后,Hedgehog/Gli信号成分的相对表达(%mGus)。 星号表示 P(P) 值<0.01( C类 )或<0.001( D类 ).
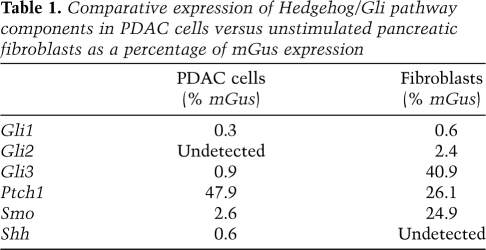
考虑到对 Gli1公司 和 第1部分 转录于 平滑(Smo) 在肿瘤性胰腺导管中,我们询问PDAC癌细胞是否能够传递刺猬信号。 我们通过比较研究了这个问题 平滑(Smo) -阳性肿瘤PDAC细胞 平滑(Smo) -阳性的原代胰腺成纤维细胞在暴露于外源重组Shh(rShh)时诱导Gli靶基因的体外能力。 一旦生长到汇合处,两种类型的细胞在低血清条件下培养16小时,然后用增加的rShh刺激8小时( 图5D ). 作为对rShh的反应,Gli靶基因的转录在原代胰腺成纤维细胞中显著诱导,但在PDAC细胞中没有诱导。 诚然,Hedgehog/Gli机器各组成部分的绝对水平在这两种细胞类型之间存在显著差异( 表1 ),但这两种细胞类型都表达容易检测到的 平滑(Smo) 和 第1部分 这表明它们缺乏反应性并不是由于缺乏Shh受体。 我们得出结论,PDAC细胞和胰腺成纤维细胞都表达 Gli1公司 和 第1部分 抄本。 然而, 平滑(Smo) -阳性PDAC细胞对刺猬配体的直接刺激没有反应,表明其表达 Gli1公司 和 第1部分 与上游Shh/Ptch/Smo信令解耦。
表1。 PDAC细胞与未刺激胰腺成纤维细胞Hedgehog/Gli通路成分mGus表达百分比的比较
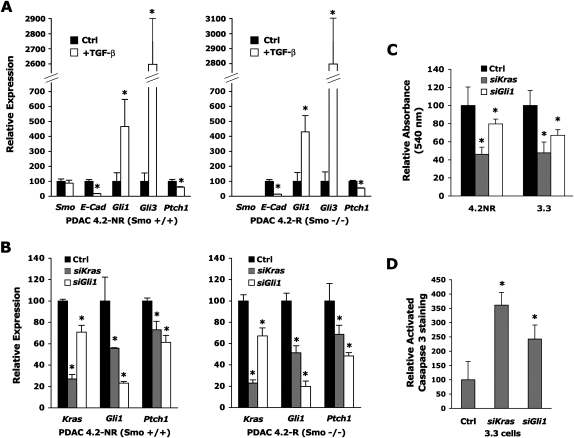
TGF公司- β Kras信号独立于Smo影响Gli靶基因 接下来,我们试图确定可能调节观察到的 Gli1公司 和 第1部分 PDAC细胞中的转录独立于Smo介导的信号。 据报道,TGF-β可诱导 Gli1公司 和 Gli2公司 几种细胞系的mRNA水平( Dennler等人,2007年 ). 鉴于TGF-β1在一个密切相关的小鼠PDAC遗传模型中由PDAC肿瘤细胞在体内高表达( Bardeesy等人,2006b ),以及在本研究中使用的模型(C.Chaudury和D.Hanahan,unpubl.)中,我们评估了TGF-β1信号转导对 胶质细胞1 基因配对中的转录 平滑(Smo) 野生型(4.2 NR)和 平滑(Smo) 上述引入的突变型(4.2R)PDAC细胞系。 我们用或不用重组TGF-β1培养这些细胞,并测量其对 Gli1公司 , Gli2公司 , Gli3公司 , 第1部分 、和 E-钙粘蛋白 后者是已知的由TGF-β途径强烈下调的转录物( 图6A ). 我们发现,无论 平滑(Smo) PDAC细胞的状态,与TGF-β孵育,导致显著上调4.5倍的 Gli1公司 以及>25倍的高程 Gli3公司 ; Gli2公司 在这些细胞中仍然检测不到(数据未显示),但是 第1部分 减少了40%,而 E-钙粘蛋白, 如预期,TGF-β1暴露后下降了90%。 这些显著影响 电子cad , Gli1公司 , Gli3公司 、和 第1部分 在另外两个独立衍生的PDAC细胞系中观察到(数据未显示)。
图6。
TGF-β和激活的Kras信号影响 格利 和 第1部分 以Smo独立的方式表达。 ( A类 )的表达式 平滑(Smo) , 第1部分 , E-Cad、Gli1 、和 Gli3公司 野生型总RNA提取物中的mRNA 平滑(Smo) (4.2 NR)或 平滑(Smo) 用5 ng/mL重组TGF-β1刺激突变型(4.2R)PDAC细胞48小时后。 mRNA水平表示为 米格斯 控制mRNA( B类 )的表达式 喀斯特 , Gli1公司 、和 第1部分 野生型总RNA提取物中的mRNA 平滑(Smo) (4.2 NR)或 平滑(Smo) 用对照siRNA池或靶向siRNA池转染PDAC细胞48小时后突变(4.2R)细胞 喀斯特 或 Gli1公司 .mRNA水平表示为 米格斯 控制mRNA( C类 )转染对照siRNA池或靶向性siRNA池72小时后,用MTT培养的两个PDAC细胞系(4.2 NR和3.3)在540 nm处的吸光度(见材料和方法) 喀斯特 或 Gli1公司 血清饥饿24h后。 ( D类 )用对照siRNA池(Ctrl)或靶向siRNA池转染小鼠PDAC 3.3细胞60 h后,活化Caspase 3免疫荧光染色的相对变化 喀斯特 或 Gli1, 血清饥饿12小时后。 在五个领域中评估染色,每个领域针对每种条件包含至少500个细胞。 Act-Casp-3阳性细胞表达为DAPI细胞核的百分比; Ctrl处理细胞的百分比设置为100%。 星号表示 P(P) -值<0.01( A类 ), <0.05 ( B类 , C类 ),或<0.005( D类 ).
鉴于鼠标PDAC模型旨在表达激活的 喀斯特 癌基因是人类PDAC中检测到的最常见的遗传事件,我们研究了 喀斯特 自身也可能参与监管 Gli1公司 和 第1部分 mRNA水平。 我们转染了基因匹配的 平滑(Smo) 野生型和 平滑(Smo) siRNA构建物靶向突变PDAC细胞 喀斯特 或 Gli1公司 并测量了这种治疗对 喀斯特 , Gli1公司 , Gli2公司 , Gli3公司 、和 第1部分 48小时后,我们发现消耗了80%的 喀斯特 表达式 喀斯特 -靶向siRNAs导致 Gli1公司 和 第1部分 两条PDAC线路中的mRNA( 图6B ). 有趣的是,消耗了80%的 Gli1公司 表达式 Gli1公司 -靶向siRNAs不仅导致 第1部分 ,但也属于 喀斯特 本身( 图6B ),表明相互反馈调节。 Gli2公司 仍然无法检测到,并且 Gli3公司 在PDAC肿瘤细胞中未受影响 喀斯特 损耗(数据未显示)。 因此,我们证明TGF-β1和Kras调节 Gli1公司 和 第1部分 表达独立于 平滑(Smo) -介导信号传导。
PDAC细胞存活和KRAS驱动的转化需要GLI1 接下来,我们问 Gli1公司 PDAC细胞中的表达对PDAC癌细胞的稳态具有重要的功能。 我们首先对用靶向siRNA构建物处理的小鼠PDAC细胞进行细胞生长分析 喀斯特 和 Gli1公司 在两个独立的小鼠PDAC细胞系(4.2 NR和3.3)中,我们发现 喀斯特 和 Gli1公司 siRNA靶向导致转染72小时和血清剥夺24小时后细胞数量显著减少( 图6C ). 我们重复了siRNA靶向,并用标记细胞凋亡的抗裂解caspase-3抗体对3.3细胞培养物进行染色。 我们发现,用 Gli1公司 和 喀斯特 siRNA( 图6D ).
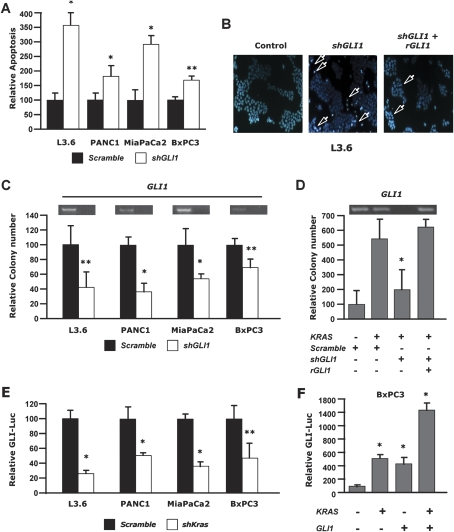
然后我们询问我们在小鼠PDAC细胞中的发现是否也适用于人类PDAC细胞。 我们用shRNA靶向转染了四种人PDAC细胞系 GLI1型 并将其与打乱的shRNA进行比较。三个品系(L3.6、PANC1和MiaPaCa2)在 KRAS公司 而第四种BxPC3是野生型 KRAS公司 ; 所有四行表示的是 KRAS公司 mRNA(数据未显示)。 我们发现,在环己酰胺的刺激下,所有四种人类PDAC细胞系的凋亡都显著增加( 图7A、B ). 然后我们询问,细胞适应性的降低是否也影响了在软琼脂中形成菌落的倾向,软琼脂是一种测量凤尾鱼非依赖性细胞生长并接近肿瘤细胞恶性潜能的转化试验。 在以下情况下,软琼脂中的菌落形成明显受损 GLI1型 这三个国家都在消耗 KRAS公司 突变细胞株,但对 KRAS公司 野生型BXPC3细胞( 图7C )这表明在突变的情况下,细胞转化的GLI1需求更为强烈 KRAS公司 为了研究这种可能性,我们转染了 KRAS公司 具有致癌性的野生型BxPC3细胞 KRAS公司 构建,导致菌落形成显著增加( 图7D ). 值得注意的是,在致癌的背景下 KRAS公司 ,BxPC3菌落形成对 GLI1型 消耗。 该灵敏度被证实为 GLI1型 -具体来说,因为它可以通过共同感染的耐药性来挽救 GLI1型 cDNA构建( rGLI1型 )不是目标 GLI1型 shRNA( 图7D ,右栏)。 野生型诱导的菌落形成 KRAS公司 BxPC3细胞中的过度表达不太明显,对 GLI1型 与突变致癌相比,消耗 KRAS公司 (未显示数据)。
图7。
GLI1型 是生存和维持人类PDAC癌细胞转化表型所必需的。 ( A类 )L3.6、PANC1、MiaPaCa2和BxPC3胰腺癌细胞转染后48 h染色质凝集/边缘化和核碎裂(代表凋亡)的相对变化 第1页 或干扰控制shRNA,然后用25 mM环己酰亚胺进行处理。 对四个高功率场中的300多个细胞进行了计数; 凋亡细胞表示为总细胞的百分比。 ( B类 )转染干扰shRNA的L3.6 PDAC细胞的Hoescht 33342染色, 第1页 ,或 第1页 旁边有一个 第1页 -抵抗的 GLI1型 cDNA构建( rGLI1型 ). 箭头表示表示凋亡的核形态模式(蓝色,Hoechst 33342)。 ( C类 )转染后检测L3.6、PANC1、MiaPaca2和BxPC3胰腺癌细胞的相对集落形成(非肿瘤性凤尾鱼生长) 第1页 或扰乱shRNA(对照)质粒。 ( D类 )BxPC3胰腺癌细胞的相对集落形成(野生型 KRAS公司 )转染致癌基因 KRAS公司 和干扰控制shRNA, shGli1型 ,或 shGli1型 旁边有一个 第1页 -抵抗的 GLI1型 cDNA救援结构( rGli1基因 ). ( E类 )相对变化 萤光素酶 转染Gli-Luciferase报告子的L3.6、PANC1、MiaPaCa2和BxPC3胰腺癌细胞中的活性 shKRAS公司 或加扰控制shRNA( 如果 )相对变化 荧光素酶 BXPC3活性(野生型 KRAS公司 )a转染胰腺癌细胞 GLI-荧光素酶 有或没有记者 KRAS公司 或 GLI1型 表达式构造。 (*)P值<0.01; (**)P值<0.05。
接下来,我们根据小鼠模型的结果测试了以下预测:人类PDAC细胞系中 GLI1型 然而,观察到的耗竭对Shh刺激没有反应,支持了我们的解释,即内源性 GLI1型 在PDAC细胞中,调节与上游Shh信号传导解耦。 我们将L3.6和PANC1细胞暴露于外源性重组Shh,监测GLI-荧光素酶报告子的表达。 Shh对GLI报告者没有影响,但它很容易在成纤维细胞系(CH10T1/2)中诱导(补充图3A)。 相反,在PDAC细胞和成纤维细胞中,转染 GLI1型 GLI荧光素酶报告子的转录显著增加,表明GLI报告子可以对两种细胞类型中升高的GLI转录活性作出反应(补充图3B)。
自 GLI1型 介导致癌的重要功能 KRAS公司 在人类PDAC细胞中,我们研究了 KRAS公司 和GLI转录。 我们发现shRNA-介导的 KRAS公司 通过GLI-荧光素酶报告子的活性检测,人PDAC细胞中GLI转录显著下调( 图7E ). 此外,致癌 KRAS公司 与…合作 GLI1型 当转染到 KRAS公司 野生型BxPC3细胞( 图7F ).
因此,KRAS对于PDAC癌细胞中GLI转录活性的诱导是必需的,并且足以证明SHH-非依赖性GLI转录,以及 GLI1型 明显有助于PDAC癌细胞存活和由 KRAS公司 .
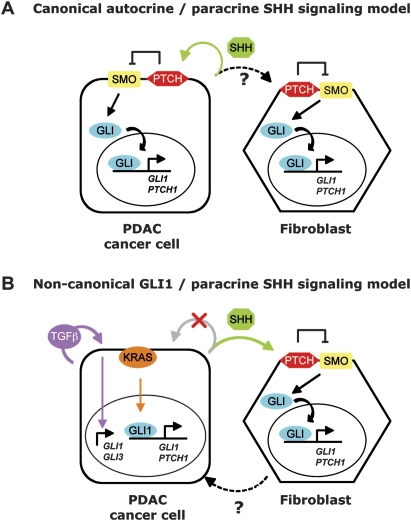
讨论 胰腺癌中Hedgehog信号被解除调控,功能研究表明该途径与胰腺肿瘤发生有关:Shh过度表达足以引发PanIN-like前体病变( Berman等人,2003年 ; Thayer等人,2003年 )并加速小鼠原位异种移植的肿瘤形成( Morton等人,2007年 ),而GLI转录与活化的 喀斯特 诱导侵袭性未分化胰腺肿瘤( Pasca di Magliano等人,2006年 ). 此外,作为Smo抑制剂的环胺对人类PDAC细胞亚群有明显的有害影响( Berman等人,2003年 ; Thayer等人,2003年 ; Feldmann等人,2007年 ). 总的来说,这些研究表明肿瘤导管细胞中的自分泌Shh信号对PDAC癌变很重要,同时与肿瘤间质的潜在但未经测试的相互作用也很重要( 图8A ).
图8。
胰腺导管癌发生中功能显著的刺猬信号和GLI转录的新概念。 ( A类 )PDAC中Hh/Gli信号的传统模型。 早期研究表明,SHH配体的自分泌信号在PDAC细胞中具有重要功能(绿色箭头)。 体内可能向基质发出信号是一个未经验证的假设(黑色虚线箭头),癌细胞和基质细胞(如癌相关成纤维细胞)中的刺猬信号被认为遵循标准刺猬的信号, SHH与PTCH结合并诱导SMO信号传导,从而导致活性GLI转录因子的核移位和GLI靶基因的转录激活,如 GLI1型 和 PTCH1型 . ( B类 )PDAC中Hh/Gli信号传导的精细模型。 我们的研究表明PDAC肿瘤细胞(1)需要 GLI1型 为了转化和存活,(2)不通过SMO共受体(交叉灰色箭头)转导功能显著的SHH配体信号,(3)继续表达 GLI公司 转录靶点独立于 SMO公司 通过部分由KRAS(橙色箭头)和TGFβ(紫色箭头)介导的GLI靶基因的非经典调节。 与PDAC癌细胞中的非经典GLI转录类似,癌细胞产生的SHH以旁分泌方式(绿色箭头)向周围间质发出信号,可能在PDAC发病机制中发挥关键的旁分泌功能( Yauch等人,2008年 ). 作为对SHH的反应,成纤维细胞分泌可能刺激肿瘤细胞生长的信号分子( Yauch等人,2008年 )(黑色虚线箭头)。
然而,最近的一项研究报告称,一种有效且特异的Smo信号抑制剂下调了移植性PDAC肿瘤间质中Gli的转录,但不下调癌细胞中的Gli转录。 此外,基质中刺猬信号的抑制在功能上很重要,因为它足以损害刺猬配体阳性癌细胞皮下异种移植中的肿瘤生长( Yauch等人2008 ). 来自同一组的其他数据也表明胰腺导管上皮细胞在体内不易致癌 平滑(Smo) 信号传导,而致癌表达 平滑(Smo) 间充质细胞诱导间充质肿瘤(Tian和de Sauvage,未证实)。 这些新的观察结果与本文提供的数据一致,支持了刺猬信号在PDAC形成中作用的另一种模型,其中,胰腺导管上皮分泌的刺猬配体不以自分泌方式刺激癌细胞,而是起到旁分泌信号功能, 导致相邻间充质细胞中GLI转录的典型Smo依赖性激活。 此外,我们的研究支持肿瘤胰腺导管细胞不传递刺猬配体信号的观点,因为我们表明,与成纤维细胞不同,PDAC细胞在与Shh孵育后不诱导Gli转录。 我们也证明了独裁 平滑(Smo) -由于基因消融,导管上皮中介导的刺猬信号既不限制PDAC的发生,也不需要其发挥功能 平滑(Smo) 胰腺上皮对PDAC肿瘤的发生没有影响。
然而,当收益或损失 平滑(Smo) 功能不影响胰腺导管细胞,刺猬信号下游效应器转录因子Gli2的类似靶向表达诱导胰腺肿瘤形成并加速Kras诱导的致癌,尽管是非分化的( Pasca di Magliano等人,2006年 ). 此外,GLI介导的转录程序在体内PanIN损伤中明显诱导( Prasad等人,2005年 )认为导管细胞内GLI转录可能对胰腺肿瘤的发生很重要。 值得注意的是,在基因消融后,我们观察到Gli靶基因的表达水平没有显著下降 平滑(Smo) 在肿瘤导管细胞中,显示PDAC细胞中Gli靶基因的表达与上游Hh/Ptch/Smo信号转导解耦。 我们发现两种信号分子,KRAS和TGFβ,显著参与PDAC肿瘤的发生,调节 平滑(Smo) -小鼠PDAC细胞中Gli靶基因的独立表达。 此外,我们发现 GLI1型 是人类PDAC细胞系生存和 KRAS公司 -介导的细胞转化。 对Shh信号的无反应,以及小鼠和人类PDAC细胞中Gli1功能的明显需求,可能有助于解释为什么在其他情况下,基因是刺猬信号的下游效应器或调节器,包括 GLI1型 和 GLI3公司 ,最近被报道在24个人类PDAC衍生的细胞系中100%发生突变,这些细胞系的基因组被全面扫描以寻找突变( Jones等人,2008年 ). 相比之下 PTCH公司 和 SMO公司 我们证明,共受体在胰腺癌细胞中并不重要,但在这些细胞中不容易发生突变,这与PDAC中旁分泌刺猬信号的概念完善一致( 图8B ).
总之,本研究的结果以及来自德索瓦吉组的数据( Yauch等人,2008年 ),揭示了PDAC发病机制中刺猬信号的复杂电路,其中典型旁分泌Shh信号在肿瘤基质的间充质成分中起重要作用,而 SMO公司 -独立、非经典、癌细胞自主, KRAS公司 -肿瘤实质需要受驱动的GLI1转录( 图8B ). 本研究和其他近期研究的共同知识表明,PDAC的创新治疗靶向性有双重策略,即抑制胰腺癌细胞中KRAS自身或Gli转录,同时废除 SMO公司 -肿瘤间质中的依赖性Shh信号。 描述Gli转录抑制剂的最新报告( Lauth等人,2007年 )在这方面,与新一代强效和选择性Smo抑制剂一起,有着值得未来研究的有趣前景( Yauch等人,2008年 ).
材料和方法 小鼠菌株和基因分型 这个 LSL-Kras公司 GD12公司 , Trp53基因 如果 , 平滑(Smo) 如果 、和 p48芯 等位基因已被描述( Jonkers等人,2001年 ; Long等人,2001年 ; Kawaguchi等人,2002年 ; Tuveson等人,2004年 ). 这个 平滑(Smo) 等位基因分型 Smo-for公司 (GTTCCCAGGTTGAAGACAG)在0.5μM下使用 平滑-容重 (ACAGCCACTCAGAAAGC)(野生型等位基因,300碱基对[bp]带)在0.2μM下使用,以及 Smo-rev-mut公司 (CTAAAGCGCATGCTCCAGAC)(flox等位基因,350-bp带)在0.3μM下使用。 PCR条件为6个周期(94°C,1分钟;63°C,30秒;72°C,45秒),然后是32个周期(94C,1 min;60°C,30s;72°C,45秒)和72°C下的5分钟。 PCR条带在3%琼脂糖凝胶上分离。 所有研究均按照加利福尼亚大学动物保护和使用委员会的指导方针进行。
胰腺成纤维细胞PDAC细胞系的分离及组织培养 解剖5 mm PDAC肿瘤碎片,用细剪刀在冷PBS中切碎,并用搅拌棒将其转移到13.5 mL PBS中的血管中。 五毫升 溶组织梭菌 添加胶原酶XI(20 g/mL;Sigma#C7657),并在37°C下高速搅拌容器20 min。 样品通过100μm的过滤器过滤,并保留过滤器中的固体部分; 流通被丢弃。 将固体部分转移到50 mL试管中,在PBS中清洗三次,并在30 mL完整DMEM(10%FBS+抗生素)中重新悬浮。 大块未消化的碎片下沉,上清液被镀在胶原蛋白-I涂层板上。 两周后,菌落生长并克隆到6孔板中(无胶原蛋白)。 PDAC 4.2 NR的体外重组,1×10 9 Ad5CMVCre病毒(GTVC; 网址:http://www.uiowa.edu/ ~基因 )添加到5×10 6 细胞。 48小时后,对细胞进行胰蛋白酶消化,在单细胞溶液中重新悬浮,计数,并在96个平板中连续稀释(水平方向连续稀释1-10次,然后垂直方向连续稀释1-10次); 将含有单个重组细胞集落的微孔扩大并进行基因分型(五个恢复的4.2R克隆中有五个是重组的)。 还进行了一系列稀释以分离4.2 NR的未感染克隆。胰腺成纤维细胞的获得如下:解剖一个野生型胰腺,在冰镇PBS中切成2 mm的碎片,并将其转移到带有无菌搅拌棒的搅拌容器中,搅拌2 mL PBS。25 mL胶原酶V(1 mg/mL;Sigma#C9263) 加入,并将容器在37°C下高速搅拌15分钟。 在完全DMEM中连续三次清洗胶原酶消化。 在10 mL PBS中重新悬浮后,通过100μm滤网过滤样品。 将两种组分(流通组分和固体组分)保存、纺丝并重新悬浮在2 mL 0.25%胰蛋白酶中。 然后在37°C下培养5分钟。 用25 mL完整的DMEM停止消化,将小球旋转并重新悬浮在5 mL完整的DMAM中,然后在六孔板中电镀。 ~2周后(定期更换培养基),细胞在5至6代后衰老。
rShh和rTGFβ1体外刺激PDAC细胞和成纤维细胞 在低血清暴露16小时后,在低血清条件(0.2%FBS)下用0至500 ng/mL重组rShh(rmShh-C25II-N;R&D Systems#464SH)刺激8小时,在10%FBS中用5 ng/mL的重组TGFβ1(R&D System#240-B)刺激48小时。
MTT和siRNA分析 根据制造商的建议,使用Vybrant MTT细胞增殖测定试剂盒(分子探针#V-13154)进行细胞生长测定。 使用Dharmacon siRNA ON-TARGETplus SMART池(Thermo Scientific; 喀斯特 #L-043846-01; Gli1公司 #L-047917-00; 非靶向对照#D-001810-10)和DharmaFECT 2转染试剂(Thermo Scientific#T-2002)。
定量聚合酶链反应 按照制造商的建议,使用RNeasy Mini(Qiagen)制备总RNA。 使用RNeasy Micro(Qiagen)从激光显微切割样品中制备总RNA。 使用DNA-Free RNA Kit(Zymo Research)进行DNA酶处理和RNA清除。 使用iScript(Bio-Rad)进行cDNA合成。 采用以下TaqMan分析(Applied Biosystems)进行PCR:Mm00494645_m1( Gli1公司 ),Mm01293117_m1( 胶质细胞2 ),Mm00492338_m1( Gli3公司 ),Mm00436026_m1( 第1部分 ),Mm00436527_m1( 嘘 ),Mm01162704-m1( 平滑(Smo) )和Mm03053281_s1( 喀斯特 ). 这个 米格斯 该分析由集成DNA技术公司获得。 (F) CTCATCTGGAATTCGCCGA; (R) GGCGAGTAAGATCCCTTC; (探头)fam-CGAACCTCACCGCTGAGTAATCG-bhq1。 在ABI7900HT序列检测系统上进行定量PCR反应。 测定并减去Ct值,得到ΔCt[ΔCt=Ct(试验位点)−Ct(控制位点)]。 相对折叠差计算为2 -ΔCt × 100.
组织学分析、免疫化学和免疫荧光 组织在锌缓冲福尔马林中固定过夜,并嵌入石蜡中。 对7μm厚的切片进行H&E染色或抗原回收程序(Citra;BioGenex)。 在抑制内源性过氧化物酶并阻断载玻片后,在4°C下应用一级抗体过夜。 使用了以下抗体:山羊抗Shh(1:100;研发系统AF445)、兔抗Smo(1:100,Pao Tien Chuang博士赠送的礼物)( Gerber等人,2007年 ),亚美尼亚仓鼠抗Muc1抗体(1:200;新标记HM-1630-P0),兔抗α-淀粉酶(1:500;Sigma A8273),抗活化Caspase3(1:300;细胞信号9661S)。 生物素化或荧光结合抗体用作次级抗体(1:200;Jackson Immunoresearch)。 采用3-3′-DAB四氯化氢(Sigma D4293)作为显色剂。
激光捕获显微切割 将10微米新鲜冰冻PDAC切片涂敷于膜载玻片(徕卡11505151)上,并进行改良H&E染色方案(苏木精溶液;Harris改良,Sigma HHS-16;含Phloine B的Eosin Y溶液,SigmaHT110-3-16;蓝色试剂,0.1%NH 4 俄亥俄州西格玛221228)。 使用Leica AS LMD自动显微镜,在改良h&E染色后3小时内进行激光捕获显微切割。
软琼脂生长试验 使用BTX方波电穿孔器在360 V电压下对所有细胞系电穿孔10毫秒。 L3.6、PANC1、MiaPaca2或BxPC3胰腺癌细胞(1×107)通过干扰控制或shRNA靶向转染 GLI1型 在救援实验中,人类的一种抵抗型 GLI1型 cDNA共转染。 将转染细胞重新悬浮在含有0.33%低熔点琼脂糖的血清培养基中,并将其置于相同培养基中的0.5%琼脂糖缓冲垫上,放置在60 mm的培养皿中。 让细胞生长2周,然后用倒置显微镜计数含有>50个细胞的可见菌落。 三个不同的实验一式三份。 通过PCR对表达进行如下控制:根据制造商的说明(Invitrogen),使用Trizol试剂从胰腺肿瘤细胞系制备RNA。 使用Invitrogen的Superscript试剂盒从RNA中制备cDNA。 使用以下寡核苷酸对从细胞系cDNA中扩增特定GLI1转录物:5′-ACTGAAGACCTCTCCAGC-3′和5′-GCTGACAGTATAGCAGA-3′。 PCR是在以下条件下进行的:在95°C下30次变性30秒,在52°C下退火30秒,以及在72°C下延伸1分钟。 在1%琼脂糖-TAE凝胶上分离并用溴化乙锭染色,以此分析PCR产物的1/1。
细胞凋亡分析 用干扰控制或shRNA靶向转染L3.6、PANC1、MiaPaCa2和BXPC3 GLI1型 转染48小时后,用载体对照(DMSO)或放线菌酮(25μM)处理细胞。 为了进行凋亡测定,采用DNA染色Hoescht 33860,根据细胞核断裂、细胞核边缘化和细胞器紊乱的形态学标准鉴定发生凋亡的细胞。 用蔡司共焦显微镜对阳性细胞进行计数。 GLI1型 转染后48小时用PCR分析表达水平。
荧光素酶检测 所有细胞均按上述方法生长和转染。 荧光素酶报告分析,1×10 6 将细胞以一式三份的形式分布在24孔板中,并使其恢复18小时。随后洗涤细胞,并加入含有1%FBS的新鲜培养基。 按照制造商的建议采集样品并制备用于荧光素酶分析(Promega)。 总蛋白定量用于控制转染效率的样本间差异。
致谢 我们感谢李亚军博士和庄保天博士提供的抗Smo抗体。 我们感谢N.Bardeesy和R.DePinho对手稿的批判性阅读; 哈纳汉和希布罗克科学讨论实验室的成员,特别是P.Olson、J.Morris和M.Pasca di Magliano; 用于TaqMan分析的Helen Diller家族综合癌症中心基因组分析核心设施; 以及E.Drori、M.Vayner、S.Cacacho和A.Wang提供技术援助。 这项工作得到了NIH向M.H.(DK60533-01A1,CA112537-01)、M.E.F.Z(CA125127,Carole和Bob Daly AACR-PANCAN胰腺癌研究职业发展奖,Mayo Clinic Pancreatic SPORE P50 CA102701,衣阿华大学/Mayo诊所淋巴瘤SPORE P50 CA097274)和D.H.(胰腺癌项目赠款; R.DePinho,P.I.)。 O.N.S.是Damon Runyon癌症研究基金会(DRG-1831-04)的默克研究员。
工具书类
Aguirre A.J.、Bardeesy N.、Sinha M.、Lopez L.、Tuveson D.A.、Horner J.、Redston M.S.、DePinho R.A.激活的Kras和Ink4a/Arf缺乏协同产生转移性胰腺导管腺癌。 基因与发育2003; 17:3112–3126. doi:10.1101/gad.1158703。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Bardeesy N.、DePinho R.A.胰腺癌生物学和遗传学。 Nat.Rev.癌症。 2002年; 2:897–909. doi:10.1038/nrc949。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Bardeesy N.、Aguirre A.J.、Chu G.C.、Cheng K.H.、Lopez L.V.、Hezel A.F.、Feng B.、Brennan C.、Weissleder R.、Mahmood U.等。p16(Ink4a)和p19(Arf)–p53途径均限制小鼠胰腺癌的进展。 程序。 国家。 阿卡德。 科学。 2006年a; 103:5947–5952。 doi:10.1073/pnas.0601273103。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Bardeesy N.、Cheng K.H.、Berger J.H.、Chu G.C.、Pahler J.、Olson P.、Hezel A.F.、Horner J.,Lauwers G.Y.、Hanahan D.等人。Smad4对正常胰腺发育是不可或缺的,但在胰腺癌的进展和肿瘤生物学中至关重要。 基因与发育2006b; 20:3130–3146. doi:10.1101/gad.1478706。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Berman D.M.、Karhadkar S.S.、Maitra A.、Montes De Oca R.、Gerstenblith M.R.、Briggs K.、Parker A.R.、Shimada Y.、Eshleman J.R.、Watkins D.N.等。广泛要求刺激消化道肿瘤生长中的刺猬配体。 自然。 2003; 425:846–851. doi:10.1038/nature01972。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Dennler S.、Andre J.、Alexaki I.、Li A.、Magnaldo T.、ten Dijke P.、Wang X.J.、Verrecchia F.、Mauviel A.通过转化生长因子-β:Smad3依赖性激活Gli2和Gli1在体内外的表达来诱导Sonic Hedgehog介质。 癌症研究2007; 67:6981–6986. doi:10.1158/0008-5472.CAN-07-0491。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Feldmann G.、Dhara S.、Fendrich V.、Bedja D.、Beaty R.、Mullendore M.、Karikari C.、Alvarez H.、Iacobuzio Donahue C.、Jimeno A.等人。阻断刺猬信号抑制胰腺癌侵袭和转移:实体癌联合治疗的新范式。 癌症研究2007; 67:2187–2196. doi:10.1158/0008-5472.CAN-06-3281。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Gerber A.N.、Wilson C.W.、Li Y.J.、Chuang P.T.。刺猬通过抑制MyoD介导的转录激活来调节癌基因Gli1和Gli2阻止成肌细胞分化。 致癌物。 2007; 26:1122–1136. doi:10.1038/sj.onc.1209891。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Hezel A.F.、Kimmelman A.C.、Stanger B.Z.、Bardeesy N.、Depinho R.A.胰腺导管腺癌的遗传学和生物学。 基因与发育2006; 20:1218–1249. doi:10.10101/gad.1415606。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Hingorani S.R.、Petricoin E.F.、Maitra A.、Rajapakse V.、King C.、Jacobetz M.A.、Ross S.、Conrads T.P.、Veenstra T.D.、Hitt B.A.等人。小鼠浸润前和浸润性导管胰腺癌及其早期检测。 癌细胞。 2003; 4:437–450. doi:10.1016/s1535-6108(03)00309-x。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Incardona J.P.、Gruenberg J.、Roelink H.Sonic刺猬诱导内体中补丁和光滑的分离。 货币。 生物杂志,2002年; 12:983–995. doi:10.1016/s0960-9822(02)00895-3。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Jacob L.,Lum L.《在发育和疾病中解构刺猬途径》。 科学。 2007; 318:66–68. doi:10.1126/science.1147314。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Jones S.、Zhang X.、Parsons D.W.、Lin J.C.、Leary R.J.、Angenendt P.、Mankoo P.、Carter H.、Kamiyama H.、Jimeno A.等。全球基因组分析揭示的人类胰腺癌的核心信号通路。 科学。 2008; 321:1801–1806. doi:10.1126/science.1164368。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Jonkers J.、Meuwissen R.、van der Gulden H.、Peterse H.、van der Valk M.、Berns A.乳腺癌条件小鼠模型中BRCA2和p53的协同抑癌活性。 自然基因。 2001; 29:418–425. doi:10.1038/ng747。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Kawaguchi Y.、Cooper B.、Gannon M.、Ray M.、MacDonald R.J.、Wright C.V.转录调控因子Ptf1a在将肠道祖细胞转化为胰腺祖细胞中的作用。 自然遗传学。 2002年; 32:128–134. doi:10.1038/ng959。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Lauth M.,Bergstrom A.,Shimokawa T.,Toftgard R.小分子拮抗剂对GLI介导的转录和肿瘤细胞生长的抑制。 程序。 国家。 阿卡德。 科学。 2007; 104:8455–8460. doi:10.1073/pnas.0609699104。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Long F.,Zhang X.M.,Karp S.,Yang Y.,McMahon A.P.软骨内骨骼中刺猬信号的遗传操作揭示了其在软骨细胞增殖调节中的直接作用。 发展。 2001; 128:5099–5108. doi:10.1242/dev.128.24.5099。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Morton J.P.、Mongeau M.E.、Klimstra D.S.、Morris J.P.、Lee Y.C.、Kawaguchi Y.、Wright C.V.、Hebrok M.、Lewis B.C.声波刺猬在胰腺肿瘤发生过程中处于多个阶段。 程序。 国家。 阿卡德。 科学。 2007; 104:5103–5108. doi:10.1073/pnas.0701158104。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Pasca di Magliano M.、Hebrok M.Hedgehog在癌症形成和维持中的信号传递。 Nat.Rev.癌症。 2003; 3:903–911. doi:10.1038/nrc1229。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Pasca di Magliano M.、Sekine S.、Ermilov A.、Ferris J.、Dlugosz A.A.、Hebrok M.Hedgehog/Ras相互作用调节胰腺癌的早期阶段。 基因与发育2006; 20:3161–3173. doi:10.10101/gad.1470806。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Prasad N.B.、Biankin A.V.、Fukushima N.、Maitra A.、Dhara S.、Elkahloun A.G.、Hruban R.H.、Goggins M.、Leach S.D.胰腺上皮内瘤变的基因表达谱反映了Hedgehog信号对胰腺导管上皮细胞的影响。 2005年癌症研究; 65:1619–1626. doi:10.1158/0008-5472.CAN-04-1413。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Rubin L.L.,de Sauvage F.J.针对癌症中的Hedgehog途径。 Nat.Rev.药物发现。 2006; 5:1026–1033. doi:10.1038/nrd2086。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Rustgi A.K.胰腺癌的分子发病机制:阐明复杂的电路。 基因与发育2006; 20:3049–3053. doi:10.1101/gad.1501106。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Taipale J.,Beachy P.A.癌症中的刺猬和Wnt信号通路。 自然。 2001; 411:349–354. doi:10.1038/35077219。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Thayer S.P.、di Magliano M.P.、Heiser P.W.、Nielsen C.M.、Roberts D.J.、Lauwers G.Y.、Qi Y.P.、Gysin S.、Fernandez-del Castillo C.、Yajnik V.等。Hedgehog是胰腺癌肿瘤发生的早期和晚期介体。 自然。 2003; 425:851–856. doi:10.1038/nature02009。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Tuveson D.A.、Hingorani S.R.《人类和小鼠的导管性胰腺癌》。 冷泉港。 交响乐团。 数量。 生物学2005; 70:65–72. doi:10.1101/sqb.2005.70.040。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Tuveson D.A.、Shaw A.T.、Willis N.A.、Silver D.P.、Jackson E.L.、Chang S.、Mercer K.L.、Grochow R.、Hock H.、Crowley D.等人。内源性致癌K-ras(G12D)刺激增殖和广泛的肿瘤和发育缺陷。 癌细胞。 2004; 5:375–387. doi:10.1016/s1535-6108(04)00085-6。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Yauch R.L.、Gould S.E.、Scales S.J.、Tang T.、Tian H.、Ahn C.P.、Marshall D.、Fu L.、Januario T.、Kallop D.等。癌症中刺猬信号的旁分泌需求。 自然。 2008; 455:406–410. doi:10.1038/nature02775。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Zhang X.M.、Ramalho-Santos M.、McMahon A.P.平滑突变体揭示了Shh和Ihh信号的冗余作用,包括小鼠节点对L/R对称性的调节。 单元格。 2001; 106:781–792. [ 公共医学 ] [ 谷歌学者 ]