胰腺导管腺癌(PDA)是西方国家第四大癌症死亡原因( 杰马尔 等 , 2007 ). 它是一种预后不良的疾病,生存率与肿瘤进一步相关,肿瘤局部延伸至胰腺以外,并在区域淋巴结转移( 布图里尼 等 , 2008 ). 这种特殊的转移倾向背后的原因目前尚不清楚。 看来,为了改善临床结果,需要对胰腺癌进展的可能机制有一些了解。
转移过程是一个复杂的机制,其中许多因素可能会影响肿瘤的传播( 墨菲,2001 ). 近年来,趋化因子在肿瘤转移过程中的作用越来越受到人们的关注。 趋化因子及其受体是常规免疫监测、炎症和发育过程中细胞迁移的关键介质( 辛格 等 , 2007 ; 奥海尔 等 , 2008 ). CXCR4是研究得最好的趋化因子受体之一,主要是因为它是HIV进入的共受体,并且能够介导多种癌症的转移( 巴尔克维尔,2004年a ). CXCR4选择性结合CXC趋化因子基质细胞衍生因子1(SDF-1或CXCL12),已发现其在肿瘤发生、增殖、转移和肿瘤血管生成中发挥重要作用( 汉堡和Kipps,2006年 ). CXCR4在23多种实体癌中的表达在上皮性肿瘤细胞表面上调( 巴尔克维尔,2004年b ). 此外,CXCR4阳性肿瘤细胞可以在SDF-1梯度的作用下向远处器官迁移。 随着CXCR4的抑制,某些类型的癌细胞的生长和侵袭可能受到损害( 穆勒 等 , 2001 ; 奥塔亚诺 等 , 2005 ). 据报道,SDF-1/CXCR4在前列腺癌、卵巢癌、结直肠癌、肝细胞癌和胰腺癌中的作用( 哈特 等 , 2005 ; 江 等 , 2006 ; 席曼斯基 等 , 2006 ; 吉田县 等 , 2008 ). 据报道,CXCR4在胰腺癌细胞中表达水平较高,可能影响PDA患者的临床结局( 韦勒 等 , 2006 ; 比拉多 等 , 2006 ). 微阵列结果显示,胰腺癌患者的胰液中CXCR4基因的RNA水平增加( 罗杰斯 等 , 2006 ). 最近的证据表明,多种因素可以增强CXCR4的表达,如低氧诱导因子1、血管内皮生长因子、核因子κB活化和肝细胞生长因子( 单身汉 等 , 2002 ; 施塔勒 等 , 2003 ; 赫尔比希 等 , 2003 ; 马特细 等 , 2005 ). 然而,SDF-1/CXCR4对胰腺癌进展的下游调节作用的相关机制尚不清楚。
Wnt公司/ β -catenin典型Wnt-signaling通路与结肠、直肠、乳腺和肝脏等多个部位的肿瘤发生有关( Peifer和Polakis,2000年 ). 其核心部分,即, β -catenin在这个过程中起着关键作用( Nelson和Nusse,2004年 ). 首先, β -当Wnt缺乏或Wnt抑制剂存在时,连环蛋白在Wnt途径的失活阶段被磷酸化。 Wnt因子异常分泌或APC突变可能导致异常 β -连环蛋白激活进而导致Wnt信号的激活和上皮-间充质转化(EMT)过程( 布拉伯茨 等 , 2001 ; Reya和Clevers,2005年 ). Wnt的一些下游靶基因/ β -已经报道了连环蛋白信号,它通过影响细胞生长、细胞周期、细胞存活和侵袭在致癌过程中发挥关键作用( www.stanford.edu/~rnusse/wntwindow.html ). APC突变或 β -其他胃肠道肿瘤中常见的连环蛋白在PDA中并不总是能检测到( 亚伯拉罕 等 , 2002 ). Wnt信号的异常激活是人类胰腺癌的一个重要特征,这一点可以通过异常的 β -catenin在相当一部分肿瘤中的表达(30–65%)( 洛伊 等 , 2003 ; Al-Aynati公司 等 , 2004 ; 曾 等 , 2006 ).
基于先前对CXCR4的中心作用和经典Wnt通路的研究,我们假设CXCR4通过Wnt在胰腺癌转移中发挥作用/ β -连环蛋白途径( 王和马,2007 ). 本研究的目的是确定CXCR4在胰腺癌中的作用并阐明其潜在机制。
材料和方法 细胞系和培养条件 人胰腺癌细胞系(PC-2、PC-3、Miapaca-2、Bxpc-3和Panc-1)保存在西安交通大学第一附属医院肝胆外科。 细胞在DMEM(Invitrogen,Carlsbad,CA,USA)中培养,DMEM补充10%FBS(Invit罗gen,Callsbad −1 )和链霉素(0.1毫克毫升 −1 ).
免疫组织化学 标本来源于西安交通大学第一附属医院肝胆外科48例胰腺癌和8例正常胰腺标本。 根据制造商的说明,使用SABC试剂盒(Maxim,中国福州)对CXCR4进行免疫组织化学染色。 CXCR4(1:50)的一级抗体从eBioscience(美国加利福尼亚州圣地亚哥)获得,并在4°C下培养过夜。 为了评估蛋白质表达,染色强度分为0(阴性)、1(弱)、2(中等)或3(强)。 根据阳性染色面积占肿瘤总面积的百分比,将染色范围分为0(0%)、1(1-10%)、2(11-50%)、3(51-80%)和4(>81%)。 通过乘以染色强度和染色程度获得最终的免疫组织化学染色评分( 狮子座 等 , 2006 ).
CXCR4 shRNA表达载体构建 人类CXCR4基因序列(Genbank登录号。 NM_003467 )根据制造商的协议,使用Genscript(美国新泽西州皮斯卡塔韦)和Ambion(美国德克萨斯州奥斯汀应用生物系统公司)提供的基于网络的siRNA目标查找器和设计工具分析潜在的siRNA靶点。 合成了以下shRNA插入序列:5′-gatccTGAGAAGACGGACAAttcaagagaTTGTCCGTCAT GCTTCTCAttttttggaaa-3′(目标位置:301)和5′-gatccAGCGAGAGACATTCTCtcaagaGAGATGCCACC TCGCTttttggaaa-3′(目标位置:1093)。 作为阴性对照,还设计了一个插入序列为5′-gatccTTCCGAACGTCACGTTcaagagaACGTGACA的载体 CGTTCGGAGAAttttggaaa-3′,不针对人类基因组中的任何区域。 退火正反义寡核苷酸。 消化后 巴姆 HI和 Hin公司 dIII,将片段插入shRNA表达载体pRNAT-U6.1/Neo(GenScript Corp.,Piscataway,NJ,USA),并通过质粒测序确认。
CXCR4 shRNA表达载体的稳定转染 在24孔板中,5×10 4 转染前1天,细胞每孔电镀一次。 根据制造商的建议,使用脂质体胺2000(Invitrogen,Carlsbad,CA,USA)进行转染。 转染后24小时,细胞溶液以1:10稀释并再生。 在10%DMEM培养基中,400 μ 克毫升 −1 在细胞粘附到平板上后,添加G418(Invitrogen,Carlsbad,CA,USA)进行选择。 在96 well平板中使用有限稀释液进行重复菌落选择。 14天后,G418(200 μ 克毫升 −1 )添加用于未来稳定转染细胞培养。
定量实时聚合酶链反应(QT–PCR)检测mRNA表达 提取总RNA,2×10 5 用Trizol试剂(Invitrogen,Carlsbad,CA,USA)采集细胞。 按照制造商的说明,使用SYBR®ExScript™RT–PCR试剂盒(中国大连塔卡拉生物科技有限公司)进行cDNA合成:将500 ng总RNA与2 μ l of 5×ExScript™RTase缓冲区,0.5 μ l dNTP混合物,0.5 μ l随机六聚体,0.25 μ ExScript™Rtase的l和0.25 μ 总体积为10升的核糖核酸酶抑制剂 μ l.反应在42°C下进行12分钟,然后在95°C下使逆转录酶失活2分钟。cDNA存储在−20°C下。 使用SYBR Green Master Mix在ABI PRISM®7300序列检测系统(美国加利福尼亚州福斯特市应用生物系统公司)上进行QT–PCR。 最终反应体积为25 μ l,含有12.5 μ l 2×SYBR®Premix Ex Taq™,1.0 μ 每层底漆(10 μ M(M) ), 0.5 μ l 50×ROX参考染料,1.0 μ l cDNA。 循环条件如下:在95℃下初始变性10 min,然后在95℃条件下40个循环变性15 s,在60℃条件下60 s。每次测量均进行三次,每次分析均不包括模板对照。 在每个QT–PCR中,进行解离曲线分析。 GAPDH作为内控基因控制。 使用 2 −ΔΔ C类 t吨 方法( Livak和Schmittgen,2001年 ).
细胞增殖试验 细胞以5×10的浓度接种在96个平板中 三 实验前一天。 3-[4,5-二甲基噻唑-2-基]-2,5-二苯基四唑溴化铵(MTT,0.5 mg ml −1 (美国密苏里州圣路易斯Sigma-Aldrich)在播种后1、2、3、4、5天添加到每口井中。 通常,细胞在37°C下培养4小时,然后在150 μ 添加了1 DMSO。 在490 nm波长下测量吸收值。
流式细胞术分析 流式细胞仪分析前,1×10 6 收集细胞,用PBS洗涤两次,并用冰镇70%乙醇在4°C下固定24小时。 固定细胞用碘化丙啶染色(贝克曼·库尔特,美国佛罗里达州迈阿密)。 在37°C下培养30 m后,通过流式细胞仪对样品进行分析。 使用MultiCycle软件对DNA直方图进行细胞周期分析。
软琼脂集落形成试验 在六孔板中,每个孔的底层含有1%琼脂糖,中间层含有0.5%琼脂糖(包括7.5×10) 三 细胞和上层培养基。 每六天更换一次顶层培养基。 14天后,用Giemsa溶液(Gibco-BRL,Gaithersburg,MD,USA)对细胞进行染色,并用Quantityone分析软件(BioRad Inc.,Hercules,CA,USA。
蛋白质提取和蛋白质印迹 从1×10中分离出总蛋白 7 200个单元格 μ l含1%Nonide P-40(NP-40)的冰镇裂解缓冲液,50 mmol l −1 Tris(pH 7.4),150毫摩尔升 −1 氯化钠、0.1%十二烷基硫酸钠(SDS)、0.5%脱氧胆酸盐、200 μ 克毫升 −1 苯甲烷磺酰氟(PMSF),和50 μ 克毫升 −1 抑肽酶。 通过在15000下离心除去不溶性材料 克 在4°C下保持15分钟。 用考马斯G-250分光光度法测定提取蛋白的浓度。 澄清蛋白裂解物(30–80 μ g) 在变性SDS-聚丙烯酰胺凝胶(8-12%)上电泳拆分,并电转移到硝化纤维素膜上。 首先用5%脱脂干乳在Tris缓冲盐水(TBS)中封闭膜2小时,然后用针对特定蛋白质和GAPDH的一级抗体进行检测(作为负荷控制)。 在4°C下与一级抗体共培养过夜后,将膜与次级碱性磷酸酶结合的山羊抗兔抗体(1:2000)、山羊抗鼠抗体(1:3000)(中国上海康城)在室温下杂交2小时。 通过增强化学发光(ECL)检测系统(Amersham Bioscience,Piscataway,NJ,USA)检测免疫阳性带,并将图像转移到X射线胶片上。 如果感兴趣的条带出现在每个标记蛋白对应的预期分子量,则western blot分级为阳性。 所有分析均一式两份。 本研究中使用的抗体:CXCR4(1:200)和MMP-9(1:250)(NeoMarkers,Fremont,CA,USA)、Vimentin(1:200)和GAPDH(1:400)(Santa Cruz Biotechnology,Santa Cru,CA,US)、P339-CXCR4抗体(1:200。
β -连环蛋白/Tcf转录报告分析
简言之,1×10 5 在用构建的TOPflash或FOPflash报告质粒(Millipore,Billerica,MA,USA)瞬时转染之前,将细胞每孔接种在24孔板中。 TOPflash由胸腺嘧啶激酶(TK)启动子上游的Tcf/Lef位点和萤火虫荧光素酶基因的三个拷贝组成。 FOPflash由三个Tcf/Lef位点的突变拷贝组成,并用作检测报告者非特异性激活的对照。 所有转染均使用0.8 μ g TOPflash或FOPflash质粒和2 μ l脂质体2000。 为了使报告分析中的转染效率正常化,将细胞与0.02进行共转染 μ g内部对照报告质粒,包含由TK启动子驱动的肾形Renilla reniformis荧光素酶。 在TOPflash或FOPflash转染后24小时,使用双荧光素酶检测系统试剂盒(美国威斯康星州麦迪逊市Promega公司)进行荧光素酶检测。 相对荧光素酶活性报告为转染效率归一化后的折叠诱导。
Matrigel侵犯分析 利用Millicell入侵室(Millipore,Billerica,MA,USA)进行入侵检测。 第8个 μ m孔嵌件涂有15层 μ g Matrigel(美国马萨诸塞州贝德福德市Bedton Dickinson实验室)。 含或不含100 ng ml的正常培养基 −1 SDF-1型 α (R&D systems Inc.,Minneapolis,MN,USA)被添加到底室以诱导癌细胞系。 电池(5×10 4 )在顶室播种。 将基质胶侵入室在湿润的组织培养箱中培养20小时。 用棉签从Matrigel顶部去除非侵入细胞。 滤池底面侵入细胞用甲醇固定,Giemsa染色。 通过对染色细胞的计数来确定侵袭能力。
统计分析 所有统计分析均使用SPSS13.0软件进行。 结果显示为三次重复试验的平均值±标准差。 通过学生的 t吨 -方差检验或分析(ANOVA)。 P(P) <0.05被认为具有统计学意义。
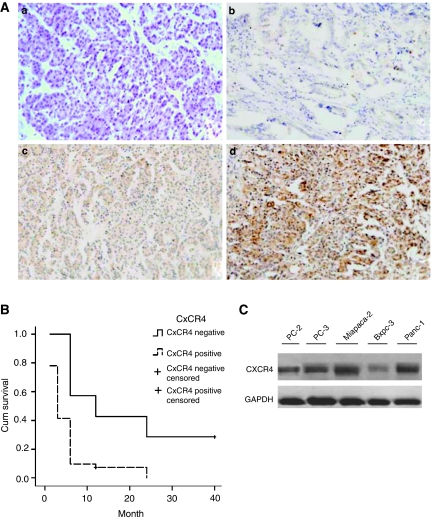
结果 CXCR4表达水平与胰腺癌的关系 免疫组织化学染色结果显示,CXCR4在大多数胰腺癌细胞的细胞质中表达,而在正常胰腺细胞中没有表达。 代表性染色结果如所示 图1A 在非转移细胞和转移细胞之间观察到CXCR4的不同表达,在肿瘤淋巴结转移(TNM)分期之间观察到不同的CXCR4表达( P(P) 分别为0.012和0.005)( 表1 ). CXCR4阳性组和CXCR4阴性组的中位生存时间分别为5.5和13.5个月( P(P) <0.05) ( 图1B ). 此外,CXCR4在胰腺癌细胞系中高表达,尤其是Miapaca-2( 图1C ).
图1。
CXCR4在胰腺癌中的表达。 ( A类 )正常胰腺组织CXCR4的免疫组织化学染色( 一 )和胰腺癌组织( b条 —— d日 )×200:阴性表达( 一 ),弱表达式( b条 ),适度表达( c(c) ),强表达( d日 ); ( B类 )Kaplan-Meier曲线显示,CXCR4阳性和CXCR4阴性组的中位生存时间分别为5.5和13.5个月; ( C类 ). Western blot分析显示CXCR4在5种胰腺癌细胞(PC-2、PC-3、Miapaca-2、Bxpc-3、Panc-1)中表达。 GAPDH被用作负荷控制。
表1。 PDA患者CXCR4表达与临床特征的关系。
临床病理变量
CXCR4中位数得分
P(P) -价值
年龄
> 65 5.6 0.542
< 65 4.4
组织学
嗯 3.1
中等 4.9 0.062
可怜的 5.5
淋巴结转移
积极的 6.1 0.012
否定 3
TNM阶段
我 1.7
二 3.8 0.005
三 5.4
四、 7.9
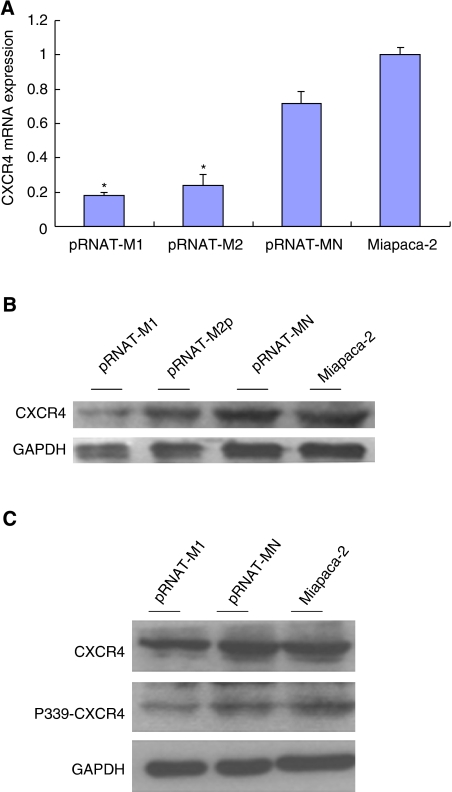
建立稳定的CXCR4击倒 使用shRNA敲除转录物是研究基因功能的有力工具。 研究肿瘤细胞的长期生长模式 在体外 ,我们开发了pRNAT-U6.1/Neo载体,该载体包含能够产生19个核苷酸的双链RNAi寡核苷酸的小发夹构建体。 我们成功获得稳定的shRNA载体转染细胞,称为pRNAT-M1(靶位:301)、pRNAT-M2(靶位;1093)和pRNAT_MN(阴性对照载体)。 QT-PCR分析表明,与pRNAT-MN细胞相比,CXCR4 shRNA-转染细胞系中CXCR4 mRNA的表达被抑制了70%,尤其是在pRNAT-M1细胞中( P(P) <0.05). 与Miapaca-2细胞相比,pRNAT-MN细胞中CXCR4 mRNA表达减少约20%( 图2A ). 此外,与pRNAT-MN细胞相比,pRNAT-M1细胞中CXCR4蛋白水平也显著下调( 图2B ). 值得注意的是,在pRNAT-M1细胞中观察到丝氨酸339处CXCR4磷酸化的降低。 通过带分析,pRNAT-M1细胞中磷酸化CXCR4的比例也降低( 图2C ).
图2。
建立稳定的CXCR4击倒。 ( A类 )不同CXCR4 shRNA表达载体转染后CXCR4表达的QT-PCR分析:pRNAT-M1(靶位301)、pRNAT_M2(靶位1093)、pRNA T-MN(阴性对照)和Miapaca-2, * P(P) 与pRNAT-MN细胞相比<0.05; ( B类 )不同转染胰腺癌细胞的CXCR4抗体免疫印迹。 GAPDH被检测为负荷控制; ( C类 )Western印迹显示CXCR4、丝氨酸339上磷酸化的CXCR4(P339-CXCR4)在转染细胞上的不同表达。 GAPDH被检测为负载控制。
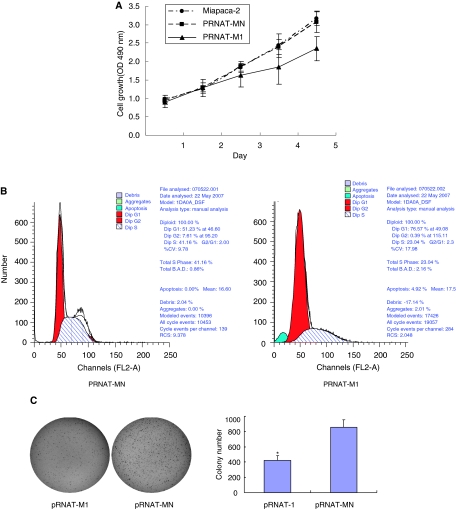
CXCR4的去除抑制细胞增殖,延迟细胞周期并降低克隆形成能力 为了证实CXCR4抑制对细胞生长的影响,培养了稳定的CXCR4 shRNA转染体。 MTT分析显示,pRNAT-M1细胞的生长速度慢于pRNAT-MN细胞。 在接种后的第50天,pRNAT-M1和pRNAT-MN细胞之间出现了不同的生长( P(P) <0.05). 然而,Miapaca-2细胞和pRNAT-MN细胞之间没有差异( P(P) >0.05) ( 图3A ). 根据流式细胞术对细胞周期分布的分析,我们发现从G0期到G1期的进展存在明显的延迟(51.23 与 76.51%),S期下降(41.16 与 23.0%)和G2-M相(1.61 与 0.39%). 此外,在pRNAT-M1细胞中也观察到G1亚凋亡间隔( 图3B ). 探讨CXCR4基因敲除对肿瘤发生的影响 在体外 进行软琼脂集落形成试验。 结果表明,与pRNAT-MN细胞相比,pRNAT-M1细胞的集落形成减少( P(P) <0.05) ( 图3C ).
图3。
CXCR4敲除对细胞表型的影响。 ( A类 )在第1、2、3、4和5天对pRNAT-M1、pRNAT-MN和Miapaca-2进行MTT分析; ( B类 )通过流式细胞术分析pRNAT-M1和pRNAT-MN来证明细胞周期相的分布; ( C类 )采用软琼脂试验评价细胞集落形成能力。 菌落计数如图所示; * P(P) 与pRNAT-MN细胞相比<0.05。
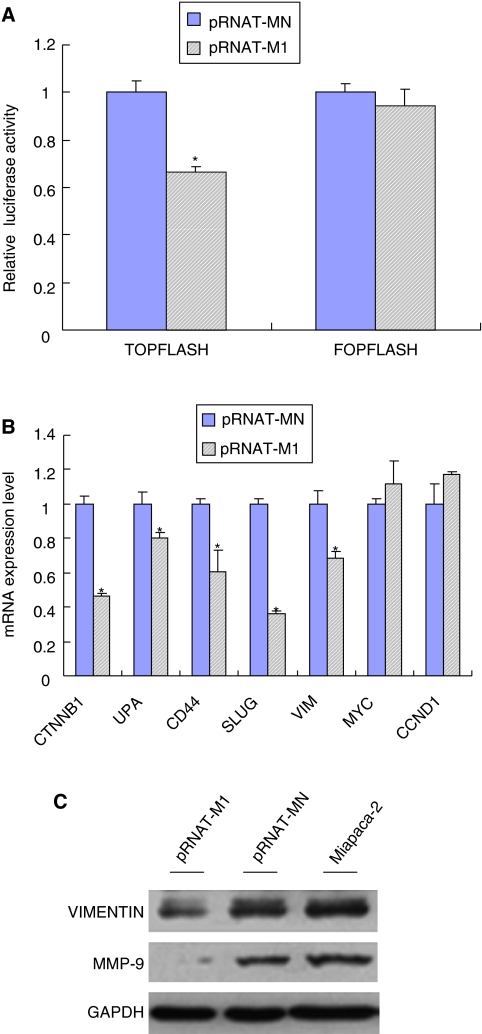
CXCR4敲低抑制Wnt活性、Wnt靶基因和侵袭相关基因 Wnt是胃肠道肿瘤发生的重要途径/ β -catenin通路和与细胞侵袭性相关的基因备受关注。 这个 β -catenin/Tcf转录报告试验被认为是评估Wnt通路活性的重要评估方法。 由于TOPflash有三个TCF结合位点,因此可以应用于表示Wnt途径的激活。 我们的数据表明,与pRNAT-MN细胞相比,CXCR4敲除细胞的TOPflash活性降低( P(P) <0.05)和FOPflash活性不变( 图4A ). 此外,QT-PCR分析表明,pRNAT-M1细胞中的Wnt靶基因如CTNNB1、UPA和CD44受到抑制,但MYC和CCND1的表达没有改变( 图4B ). 同时,抑制CXCR4导致Slug、Vimentin和MMP-9表达降低( P(P) <0.05) ( 图4C ).
图4。
CXCR4基因敲除对Wnt靶基因和侵袭相关基因的影响。 ( A类 ) β -连环蛋白/Tcf转录报告分析。 用对照报告质粒进行标准化,显示出相对荧光素酶活性。 * P(P) 与pRNAT MN细胞相比<0.05; ( B类 )QT–PCR分析以检测CTNNB1( β -catenin)、UPA、SLUG、CD44、MYC(c-MYC)、Vim(Vimentin)、CCND1(cyclin D1)基因表达 −ΔΔ C类 t吨 方法。 * P(P) 与pRNAT-MN细胞相比<0.05; ( C类 )western blot分析检测MMP-9和波形蛋白的表达。 GAPDH被用作负荷控制。
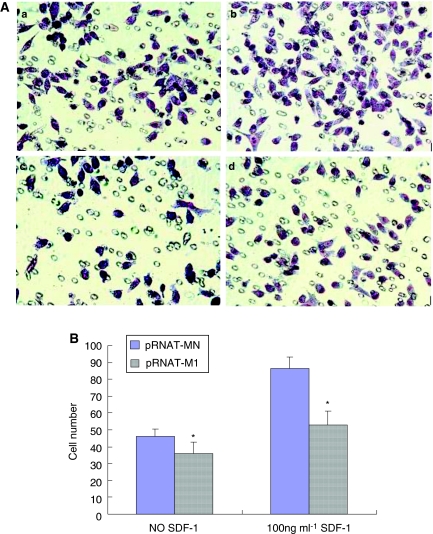
CXCR4基因敲除减少胰腺癌细胞的侵袭 采用Matrigel侵袭试验评估癌细胞的侵袭性。 代表性染色结果显示于 图5A 结果表明,pRNAT-MN细胞比pRNAT-M1细胞更具侵袭性( P(P) <0.05). SDF-1刺激后,pRNAT-MN细胞的侵袭力明显增加( P(P) <0.05),但pRNAT-M1细胞显示出轻微增加( 图5B ).
图5。
CXCR4的废除抑制胰腺癌细胞的侵袭潜能。 × 200; ( A类 )代表性染色图:无SDF-1刺激的pRNAT-MN侵入细胞( 一 ),pRNAT-MN侵入细胞100 ng ml −1 SDF-1刺激( b条 ),pRNAT-M1在无SDF-1刺激的情况下侵入细胞( c(c) ),100 ng ml的pRNAT-M1侵入细胞 −1 SDF-1刺激( d日 ); ( B类 )计数分析图, * P(P) 与pRNAT-MN细胞相比<0.05。
讨论 大多数PDA患者有局部晚期或转移性疾病,因此不适合手术干预( 冬季 等 , 2006 ). 主要原因是胰腺外侵犯和转移到肝、肺或其他组织。 粘附分子、蛋白酶、细胞因子和趋化因子等许多因素都参与了这一过程。 肿瘤微环境中存在一个复杂的趋化因子和趋化因子受体网络。 趋化因子受体CXCR4是典型的靶基因之一( 施拉德尔 等 , 2002 ; 品牌 等 , 2005 ; 索尔 等 , 2005 ; 比拉多 等 , 2006 ). 在本研究中,我们证明CXCR4表达阳性患者的总生存率显著低于CXCR4阴性患者。 CXCR4表达升高与晚期癌症分期和转移相关。 这与以前的报告类似,也表明CXCR4可能是癌症进展的有用标志物( 韦勒 等 , 2006 ; 卡吉亚马 等 , 2008 ).
先前的研究表明,针对CXCR4的siRNA可以抑制乳腺癌的转移 在体外 ( 梁 等 , 2005 ),但CXCR4敲低对胰腺癌的影响尚不清楚。 考虑到CXCR4在癌症进展中的重要作用,我们设计了CXCR4 shRNA载体作为阻断受体/配体相互作用的替代品。 为了避免空载体主干的影响,我们使用pRNAT-MN作为对照细胞,而不是Miapaca-2细胞。 我们的数据表明,质粒能有效抑制CXCR4的表达。 同时,丝氨酸339处CXCR4的磷酸化明显降低,磷酸化CXCR4比例降低。 最近,研究表明,丝氨酸339处CXCR4的磷酸化可能是在细胞上表达CXCR4功能的一种方式( 沃纳 等 , 2005 )因此,我们的数据进一步证实了CXCR4 shRNA转染细胞能够有效抑制胰腺癌中CXCR4的功能。
肿瘤发生是细胞周期紊乱的结果,导致细胞不受控制的增殖和癌症进展。 在本研究中,我们证明,阻断CXCR4不仅可以降低胰腺癌细胞的生长,还可以增加G1以下的凋亡间隔,延长G0-G1周期,减少G2和S期。 同时,它可能会降低锚定植物的独立生长能力。 随着CXCR4基因的敲除,细胞生长、细胞周期和细胞集落形成能力受到抑制,从而有效地阻止了胰腺癌细胞的肿瘤发生。
Wnt信号的解除是某些人类癌症的一个公认特征,例如结直肠癌和黑色素瘤( 伊利亚斯,2005 ). Wnt靶基因的激活将在增殖、侵袭和转移以及血管生成方面促进癌症的发展( 武藤,2006 ; Neth公司 等 , 2007 ). 此外,抑制Wnt信号可以减少胰腺癌细胞的细胞增殖和增加凋亡( 苗族 等 , 2003 ; 帕斯卡·迪马格里亚诺 等 , 2007 ; 纳鲁特 等 , 2007 ). 这里 β -catenin/Tcf实验表明,TOPflash荧光素酶活性明显降低,而FOPflash荧光素酶活性无变化。 此外,Wnt靶基因包括CTNNB1、CD44、UPA和MMP-9的表达显著降低。 因此,我们假设CXCR4敲除细胞中的TCF结合活性可以被有效抑制,这可能会影响Wnt/ β -catenin信号和Wnt靶基因不能被激活。 然而,作为典型的Wnt途径和 β -连环蛋白受多种因素共同调节,仅阻断CXCR4的表达并不能完全抑制Wnt通路。
接下来,我们评估了侵袭相关基因的表达——波形蛋白和Slug的表达。 这两个基因是与EMT过程相关的典型间充质标志物,影响癌转移( 蒂里,2002 ; 盐入 等 , 2006 ). 我们的数据表明,在CXCR4敲除细胞中,波形蛋白和Slug可以下调。 这与对口腔癌的研究一致,该研究表明CXCR4可以影响EMT的形成和癌症的侵袭( 尾上 等 , 2006 ).
在趋化因子和趋化因子受体的相互作用中,SDF-1被证明是CXCR4阳性癌细胞侵袭的刺激因子( 科尔马尔 等 , 2007 ). 确定CXCR4 shRNA对转移的影响是否与胰腺癌有关 在体外 ,我们进行了Matrigel室侵袭试验。 我们的数据显示,在正常条件下,与对照细胞相比,CXCR4转染的癌细胞的侵袭能力受到抑制。 此外,在SDF-1刺激后,在对照细胞和CXCR4敲低细胞之间观察到更多的差异。 然而,我们还发现,由于shRNA对CXCR4有70%的抑制作用,因此不能完全阻断其侵袭能力。
CXCR4是胰腺癌进展的一个有希望的标志物。 CXCR4阳性表达被认为与不良临床结局相关。 此外,CXCR4的废除可通过抑制典型Wnt通路影响胰腺癌细胞表型,包括细胞增殖、集落形成和细胞侵袭。 鉴于CXCR4在胰腺癌进展过程中的重要作用,CXCR4是一个非常有趣的治疗靶点。 了解CXCR4功能的确切机制将有助于了解吸引人的胰腺癌治疗方法。
致谢 我们感谢圣路易斯华盛顿大学医学院的Joshua B Rubin教授慷慨提供磷酸化CXCR4特异性抗体。 我们还感谢王信阳博士、尤元毅博士的技术支持,并感谢徐丽教授、陈伟教授的有益讨论和论文修订。 本研究得到了国家自然科学基金(30700817号)、陕西省科学技术局自然科学基金项目(2006K09-G7号)和西安市科学局自然科学项目(GG06178号)的资助。
工具书类
Abraham SC、Klimstra DS、Wilentz RE、Yeo CJ、Conlon K、Brennan M、Cameron JL、Wu TT、Hruban RH(2002)胰腺实性假乳头状肿瘤与胰腺导管腺癌在基因上不同,几乎总是存在β-catenin突变。 美国病理学杂志 160: 1361–1369 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Al-Aynati MM,Radulovich N,Riddell RH,Tsao MS(2004)胰腺上皮内瘤变中上皮钙粘蛋白和β-catenin的表达变化。 临床癌症研究 10: 1235–1240 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Bachelder RE,Wendt MA,Mercurio AM(2002)血管内皮生长因子通过调节趋化因子受体CXCR4以自分泌方式促进乳腺癌侵袭。 癌症研究 62: 7203–7206 [ 公共医学 ] [ 谷歌学者 ]
Balkwill F(2004a)《癌症与趋化因子网络》,Nat Rev Cancer 4: 40–50 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Balkwill F(2004b)趋化因子受体CXCR4在癌细胞表达中的意义。 赛明癌症生物学 14: 171–179 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Billadeau DD、Chatterjee S、Bramati P、Sreekumar R、Shah V、Hedin K、Urrutia R(2006)《胰腺癌细胞中CXCR4信号的表征》。 国际胃肠病杂志 37: 110–119 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Brabletz T,Jung A,Reu S,Porzner M,Hlubek F,Kunz-Schughart LA,Knuechel R,Kirchner T(2001)结直肠癌中可变β-连环蛋白的表达表明肿瘤环境驱动的肿瘤进展。 《美国科学院院刊》 98: 10356–10361 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Brand S、Dambacher J、Beigel F、Olszak T、Diebold J、Otte JM、Göke B、Eichhorst ST(2005)CXCR4和CXCL12在结直肠癌细胞中反向表达,并调节癌细胞迁移、侵袭和MMP-9活化。 Exp单元Res 310: 117–130 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Burger JA,Kipps TJ(2006)CXCR4:肿瘤细胞与其微环境之间串扰的关键受体。 血液 第107页:1761–1767 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Buturini G、Stocken DD、Wente MN、Jeekel H、Klinkenbijl JH、Bakkevold KE、Takada T、Amano H、Dervinis C、Bassi C、Buchler MW、Neoptolemos JP(2008)胰腺癌患者切缘和治疗对生存的影响:随机对照试验的荟萃分析。 外科学文献 143: 75–83 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Hart CA、Brown M、Bagley S、Sharrard M、Clarke NW(2005)《人类前列腺上皮细胞的侵袭特征:了解转移过程》。 英国癌症杂志 92: 503–512 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Helbig G、Christopherson KW、Bhat-Nakshatri P、Kumar S、Kishimoto H、Miller KD、Broxmeyer HE、Nakshatra H(2003)NF-kappaB通过诱导趋化因子受体CXCR4的表达促进乳腺癌细胞迁移和转移。 生物化学杂志 278: 21631–21638 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Ilyas M(2005)Wnt信号传导和肿瘤发展的机制基础。 病理学杂志 205: 130–144 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Jemal A、Siegel R、Ward E、Murray T、Xu J、Thun MJ(2007)《癌症统计》,2007年。 临床医师肿瘤杂志 57: 43–66 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
姜永平,吴晓霞,石斌,吴文新,尹国荣(2006)人上皮性卵巢癌中趋化因子CXCL12及其受体CXCR4的表达:肿瘤进展的独立预后因素。 妇科肿瘤学 103: 226–233 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Kajiyama H,Shibata K,Terauchi M,Ino K,Nawa A,Kikkawa F(2008)SDF-1alpha/CXCR4轴在上皮性卵巢癌腹膜转移增强中的作用。 国际癌症杂志 122: 91–99 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Kollmar O,Rupertus K,Scheuer C,Junker B,Tilton B,Schilling MK,Menger MD(2007)基质细胞衍生因子-1促进结肠转移的细胞迁移和肿瘤生长。 肿瘤形成 9: 862–870 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Leo C、Horn LC、Rauscher C、Hentschel B、Liebmann A、Hildebrandt G、Hockel M(2006),子宫颈癌中促红细胞生成素和促红细胞形成素受体的表达及其与生存、缺氧和凋亡的关系。 临床癌症研究 12: 6894–6900 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Liang Z,Yoon Y,Votaw J,Goodman MM,Williams L,Shim H(2005)CXCR4沉默阻止乳腺癌转移。 癌症研究 65: 967–971 [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Livak KJ,Schmittgen TD(2001)使用实时定量PCR和2(-Delta Delta C(T))方法分析相关基因表达数据。 方法 25: 402–408 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Lowy AM、Fenoglio-Preiser C、Kim OJ、Kordich J、Gomez A、Knight J、James L、Groden J(2003)β-catenin表达失调与胰腺导管腺癌的肿瘤分化相关。 外科肿瘤学年鉴 10: 284–290 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Matteuci E,Locati M,Desiderio MA(2005)肝细胞生长因子增强CXCR4表达,有利于乳腺癌细胞侵袭。 Exp单元Res 310: 176–185 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Miao J,Kusafuka T,Kuroda S,Yoneda A,Zhou Z,Okada A(2003)与转移相关的胰腺实性和囊性肿瘤中β-catenin的突变及其蛋白积累。 国际分子医学杂志 11: 461–464 [ 公共医学 ] [ 谷歌学者 ]
Muller A、Homey B、Soto H、Ge N、Catron D、Buchanan ME、McClanahan T、Murphy E、Yuan W、Wagner SN、Barrera JL、Mohar A、Verastegui E、Zlotnik A(2001)趋化因子受体参与乳腺癌转移。 自然 410: 50–56 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Murphy PM(2001)《趋化因子与肿瘤转移的分子基础》。 N英格兰J医学 345: 833–835 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Nawroth R,van Zante A,Cervantes S,McManus M,Hebrok M,Rosen SD(2007),细胞外硫酸酯酶,Wnt信号通路的元件,积极调节人类胰腺癌细胞的生长和致瘤性。 公共科学图书馆 2:e392。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Nelson WJ,Nusse R(2004)Wnt、β-连环蛋白和钙粘蛋白途径的融合。 科学类 303: 1483–1487 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Neth P、Ries C、Karow M、Egea V、Ilmer M、Jochum M(2007)干细胞和癌细胞中的Wnt信号转导途径:对细胞侵袭的影响。 干细胞版本 3: 18–29 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
O'Hayre M、Salanga CL、Handel TM、Allen SJ(2008)《趋化因子与癌症:微环境中的迁移、细胞内信号和细胞间通信》。 生物化学杂志 409: 635–649 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Onoue T,Uchida D,Begum NM,Tomizuka Y,Yoshida H,Sato M(2006)口腔鳞状细胞癌细胞中基质细胞衍生因子-1/CXCR4系统诱导的上皮-间质转化。 国际癌症杂志 29: 1133–1138 [ 公共医学 ] [ 谷歌学者 ]
Ottaiano A、di Palma A、Napolitano M、Pisano C、Pignata S、Tatangelo F、Botti G、Acquaviva AM、Castello G、Ascierto PA、Iafaioli RV、Scala S(2005)抗CXCR4抗体对人结肠癌细胞的抑制作用。 癌症免疫疗法 54: 781–791 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Pasca di Magliano M、Biankin AV、Heiser PW、Cano DA、Gutierrez PJ、Deramaudt T、Segara D、Dawson AC、Kench JG、Henshall SM、Sutherland RL、Dlugosz A、Rustgi AK、Hebrok M(2007)胰腺癌典型wnt信号的常见激活。 公共科学图书馆 2:e1155。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Peifer M,Polakis P(2000)肿瘤发生和胚胎发生中的Wnt信号转导——细胞核外的观察。 科学类 287: 1606–1609 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Reya T,Clevers H(2005)干细胞和癌症中的Wnt信号。 自然 434:843–850 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Rogers CD、Fukushima N、Sato N、Shi C、Prasad N、Hustinx SR、Matsubayashi H、Canto M、Eshleman JR、Hruban RH、Goggins M(2006)《通过微阵列和胰液RNA的QPCR分析鉴别胰腺病变》。 癌症生物学治疗 5: 1383–1389 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Saur D、Seidler B、Schneider G、Algül H、Beck R、Senekowitsch-Schmidtke R、Schwaiger M、Schmid RM(2005)CXCR4表达增加胰腺癌小鼠模型的肝和肺转移。 胃肠病学 129: 1237–1250 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Schimanski CC、Bahre R、Gockel I、Müller A、Frerichs K、Hörner V、Teufel A、Simiantonaki N、Biesterfeld S、Wehler T、Schuler M、Achenbach T、Junginger T、Galle PR、Moehler M(2006)肝细胞癌的传播是通过趋化因子受体CXCR4介导的。 英国癌症杂志 95: 210–217 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Schrader AJ、Lechner O、Templin M、Dittmar KE、Machtens S、Mengel M、Probst-Kepper M、Franzke A、Wollensak T、Gatzlaff P、Atzpodien J、Buer J、Lauber J(2002)CXCR4/CXCL12在肾癌中的表达和信号转导。 英国癌症杂志 86: 1250–1256 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Shioiri M、Shida T、Koda K、Oda K、Seike K、Nishimura M、Takano S、Miyazaki M(2006)Slug表达是结直肠癌患者生存不良的独立预后参数。 英国癌症杂志 94: 1816–1822 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Singh S,Sadanandam A,Singh RK(2007)《肿瘤血管生成和转移中的趋化因子》。 癌症转移评论 26: 453–467 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Staller P,Sulitkova J,Lisztwan J,Moch H,Oakeley EJ,Krek W(2003)Chemokine受体CXCR4被von Hippel-Lindau肿瘤抑制因子pVHL下调。 自然 425: 307–311 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Taketo-MM(2006)小鼠模型中的Wnt信号传导和胃肠道肿瘤发生。 癌基因 25: 7522–7530 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Thiery JP(2002)肿瘤进展中的上皮-间充质转变。 Nat Rev癌症 2: 442–454 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Wang Z,Ma Q(2007)Beta-catenin是SDF-1/CXCR4轴在胰腺癌转移中有希望的关键因子。 医学假设期刊 69: 816–820 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Wehler T,Wolfert F,Schimanski CC,Gockel I,Herr W,Biesterfeld S,Seifert JK,Adwan H,Berger MR,Junginger T,Galle PR,Moehler M(2006)胰腺癌趋化因子受体CXCR4的强表达与晚期疾病相关。 及国际医学权威期刊 16: 1159–1164 [ 公共医学 ] [ 谷歌学者 ]
Winter JM、Cameron JL、Campbell KA、Arnold MA、Chang DC、Coleman J、Hodgin MB、Sauter PK、Hruban RH、Riall TS、Schulick RD、Choti MA、Lillemoe KD、Yeo CJ(2006)1423例胰腺癌胰十二指肠切除术:单一机构经验。 胃肠外科杂志 10: 1199–1210 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Woerner BM、Warrington NM、Kung AL、Perry A、Rubin JB(2005),通过磷酸化CXCR4特异性抗体揭示星形细胞瘤中广泛的CXCR4激活。 癌症研究 65: 11392–11399 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Yoshitake N,Fukui H,Yamagishi H,Sekikawa A,Fujii S,Tomita S,Ichikawa K,Imura J,Hiraishi H,Fujimori T(2008)SDF-1α和核CXCR4的表达预测结直肠癌的淋巴结转移。 英国癌症杂志 98: 1682–1689 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Zeng G,Germinaro M,Micsenyi A,Monga NK,Bell A,Sood A,Malhotra V,Sood N,Midda V,Monga DK,Kokkinakis DM,Monga SP(2006)胰腺癌中的异常Wnt/β-catenin信号。 肿瘤形成 8: 279–289 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]