介绍 支持自我更新和分化的多功能神经干/前体细胞(NPC)位于成年哺乳动物中枢神经系统中的特殊隔间或小生境中(Doetsch, 2003 ). 最具特征的壁龛之一是脑室下区(SVZ),即位于侧脑室室管膜衬里下的一层细胞(Martino和Pluchino, 2006 ). SVZ在啮齿动物和人类的神经发生方面具有巨大潜力,它包含三种主要的细胞类型。 显示星形胶质细胞样表型的中枢神经系统干细胞(B型细胞)表达胶质纤维酸性蛋白(GFAP),并产生中间转运扩增祖细胞(C型细胞),其失去GFAP免疫反应性,获得无远端同源盒(Dlx)-2的表达。 反过来,这些C型细胞可以分化为神经母细胞(A型细胞),除双皮质激素外,还表达神经细胞粘附分子(PSA-NCAM)的多唾液酸形式,并迁移到嗅球(OB)。 细胞系分化途径从B型开始,经过C型,到达A型细胞,B型细胞被认为是自我更新的中枢神经系统干细胞(Alvarez-Buylla和Garcia-Verdugo, 2002 )。
SVZ生发龛的不同细胞类型对中枢神经系统损伤后组织修复的相对贡献仍存在争议。 虽然很明显,在急性炎症损伤(如缺血性中风)后,神经发生有促进作用(张 等人。 , 2004 ; 金 等人。 , 2006 )关于内源性脑干细胞室对导致神经退行性变的慢性中枢神经系统炎症的反应,有相互矛盾的证据。 颅脑照射或脂多糖介导的急性炎症(马提诺和普鲁奇诺, 2006 ). 先前对实验性自身免疫性脑脊髓炎(EAE)小鼠的研究报道了PSA-NCAM增殖的短暂增加 + 和NG2 + 胼胝体中的蛋白多糖细胞被推断为SVZ中干细胞和前体细胞增殖增强的证据(Calza 等人。 , 1998 ; 皮卡德·里拉 等人。 , 2002 ; 奈特·乌梅斯马 等人。 , 2007 ). 然而,这些研究都没有直接涉及EAE期间SVZ中特定细胞类型的变化。
在这里,我们使用EAE(一种多发性硬化(Pluchino)小鼠模型)研究了慢性炎症脱髓鞘对SVZ生发龛的影响 等人。 , 2003 ). 该模型对于研究慢性炎症对SVZ的影响非常有用,因为在C57BL/6小鼠品系中,大脑中的自身免疫反应是用髓鞘少突胶质细胞糖蛋白(MOG)(肽35-55)皮下免疫的结果,该糖蛋白靶向嘴侧和室周前脑区。 (Brown和Sawchenko, 2007 ; 政治 等人。 , 2007 )。
材料和方法 EAE诱导 如前所述,在6-8周龄C57Bl/6雌性小鼠中诱导慢性进展性EAE(Pluchino 等人。 , 2003 ; 阿马迪奥 等人。 , 2006 ). 对于靶向EAE,用230 ng TNF-α和250 ng IFN-γ(BD Biosciences,Franklin Lakes,NJ,USA)将MOG 35-55免疫小鼠[免疫后20天(dpi)]和健康对照(HC)立体定位注射到大脑中,溶解在总体积为2μl的无菌盐水中。 更多信息见 补充数据 。
体内 细胞周期长度和生长分数的分析
为了标记快速增殖的SVZ细胞的整个群体,小鼠腹腔注射5′-碘-2′-脱氧尿苷(IddU,第一次注射浓度为100 mg/kg的0.007 N NaOH和0.9%的盐水,而随后注射浓度为70 mg/kg的0.07 N Na氢氧化钠和0.9%盐水) 如前所述,每2小时一次,共14小时(Morshead和van der Kooy, 1992 ). 更多信息见 补充数据 。
体内 慢分化神经干细胞的分析
为了标记缓慢分裂的相对静止的SVZ推测神经干细胞,EAE小鼠每8小时腹腔注射5′-溴-2′-脱氧尿苷(BrdU,70 mg/kg,0.007 N NaOH,0.9%盐水),共连续6天,从13或30 dpi开始,如前所述(Morshead 等人。 , 1998 ). 然后,在祭祀前进行40天的洗脱期。 牺牲时,按照所述取出并固定大脑,制作10μm连续冠状冰冻切片,并用大鼠抗BrdU(克隆ICR1;Abcam,Cambridge,UK)和兔抗GFAP(DAKO)抗体进行染色。 溴化铀 + /GFAP公司 + 在整个SVZ范围内,细胞在bregma+1.2到bregma+0的区域进行评分。 用40×徕卡共聚焦(SP2)物镜对每70μm一个切片进行分析。 计算机辅助三维重建证实了双标记细胞。
逆转录病毒注射 体内 研究 老鼠( n个 =3/组)用2,2,2-三溴乙醇(10 mg/ml;体重的1/27)麻醉,并将头部置于立体定向注射装置中(David Kopf Instruments,Tujunga,CA,USA)。 如前所述(卡尔顿 等人。 , 2003 ; 门(Menn) 等人。 , 2006 )是一种在CMV启动子(rkat 43.2)下表达GFP的复制缺陷型逆转录病毒(Montini 等人。 , 2006 )在右侧脑室内注射,坐标为:A+0; L.+0.8和D.-2.4。 更多信息见 补充数据 。
现场 杂交
现场 按照所述的标准方法进行杂交(Mallamaci 等人。 , 2000 ). 更多信息见 补充数据 。
免疫荧光和免疫组织化学 在处死小鼠时,将其麻醉,并用PBS经心灌注,随后用4%多聚甲醛灌注。 大脑被移除并进行光学和电子显微镜(EM)处理,如所述(Pluchino 等人。 , 2003 ). 如前所述(Muzio 等人。 , 2005 )而内源性过氧化物酶阻断反应是通过在甲醇/H中孵育切片20分钟获得的 2 O(运行) 2 3%溶液。 更多信息见 补充数据 。
相对长度单位 按照前面所述进行传输EM(Doetsch 等人。 , 1997 ). 更多信息见 补充数据 。
原代神经干/前体细胞培养 如前所述(Reynolds和Weiss, 1992 ). 为了分析细胞增殖,将上述分离的原代细胞以8000个细胞/厘米的速度培养 2 在神经圈生长培养基(DMEM/F12,含2 mM 我 -谷氨酰胺、0.6%葡萄糖、0.1 mg/ml载脂蛋白转铁蛋白、0.025 mg/ml胰岛素、9.6µg/ml腐胺、6.3 ng/ml黄体酮、5.2 ng/ml亚硒酸钠、2µg/ml肝素)补充表皮生长因子(EGF)(20 ng/ml)和成纤维细胞生长因子(FGF-II)(10 ng/ml),并在3-5天后收集球体,如所述(Politi 等人。 , 2007 ). 更多信息见 补充数据 。
体外 神经层形成分析(NS-A)
如上所述从HC、完全弗氏佐剂(CFA)和EAE免疫小鼠中分离的原代细胞( n个 =3个),并以8000个细胞/cm的密度在24孔(0.5 ml/孔)无涂层板(科宁,科宁,纽约,美国)中电镀 2 生长介质中,如所述(Politi 等人。 , 2007 ). 更多信息见 补充数据 。
神经集落形成细胞检测(NCFCA) 如上所述从HC、CFA和EAE免疫小鼠中分离的原代细胞( n个 =6个),使用小鼠NeuroCult神经集落形成细胞检测试剂盒(StemCell Technologies,加拿大不列颠哥伦比亚省温哥华)按照制造商的说明进行电镀,密度为6.5×10 5 如前所述,每个35 mm细胞培养皿中的细胞带有2 mm网格(Nunc,Rochester,NY,USA)。 更多信息见 补充数据 。
免疫细胞化学 用PBS冲洗固定细胞,并在含有10%正常山羊血清(NGS)、0.3%Triton X-100和适当的一级抗体或抗血清的PBS中37°C孵育90分钟。 更多信息见 补充数据 。
基因表达分析 将两个96b格式TaqMan®低密度阵列(TLDA)(167个不同基因和3个内务管理)用于基因表达,并在EAE小鼠和HC新鲜衍生的SVZ组织上进行。 在适当的时间点,SVZ组织样本( n个 =每组6只小鼠)使用旋转式均质器在1 ml齐阿唑裂解试剂(美国加利福尼亚州巴伦西亚Qiagen,#79306)中均质。 使用RNeasy Lipid tissue Kit(Qiagen,#74804)从均质组织样品中分离出总RNA,包括酶消化。 最后,将RNA样品重新溶解在30μl无RNase水中,并用A分光光度法测定其浓度 260 (Nanodrop-ND 1000,Nanodrop,德国威明顿,美国)。 更多信息见 补充数据 。
激光捕获显微切割的样品制备 牺牲吧,老鼠( n个 ≥4个/组),通过腹腔注射8%水合氯铵进行深度麻醉,然后用含有10 U/ml肝素的无RNase 0.9%生理盐水快速经心灌注。从颅骨中取出大脑,然后将OCT包埋并浸泡在液氮中快速冷冻。 大脑储存在−80°C。 使用Leica AS LMD仪器(Leica Microsystems,Milan,Italy)进行激光显微切割。 更多信息见 补充数据 。
流式细胞术和核DNA分析 细胞以8000个细胞/厘米的速度进行培养 2 在含有或不含有Th1[500 IU/ml重组小鼠IFN-γ(BD Biosciences)、200 UI/ml重组鼠TNF-α(Pepro Tech Inc.,新泽西州落基山市,美国)、100 UI/ml重构鼠IL-1β(Euroclone,Siziano,意大利)]或Th2[10 ng/ml重组鼠类IL-4(R&D,明尼阿波利斯,明尼苏达州,美国),10 ng/ml重构小鼠IL-5(R&D)的生长培养基中 ,10 ng/ml重组小鼠IL-13(R&D)]细胞因子混合物。 48小时后,收集细胞,机械分离并在PBS中清洗三次。 为了进行细胞核DNA含量分析,然后将细胞重新悬浮在81%PBS 1×、1%ND P-40、10%碘化丙啶(PI)、8%核糖核酸酶(核糖核酸酶A 300 Kuntz单位)溶液中。 如前所述,对核DNA含量进行了分析(Chew 等人。 , 2005 )数据采集利用前向光散射和侧光散射进行门控,以排除细胞碎片和聚集物。 HC和细胞因子条件下NPC的生长分数也由Ki67抗原的表达决定,Ki67抗原在细胞周期的晚期G1、S、G2或M期的增殖细胞中独家表达。 在用冰镇70%乙醇渗透后,用异硫氰酸荧光素(FITC)结合的抗Ki67抗体(BD PharMinen,Franklin Lakes,NJ,USA)培养细胞。 PI荧光使用FACS青色流式细胞仪(丹麦格洛斯特鲁普达科)在线性范围内进行测量,而Ki67染色则使用BD FACSCanto II流式细胞计进行分析。 使用FCS 3软件(Becton Dickinson,Franklin Lakes,NJ,USA)采集并分析所有数据。 至少2×10 4 对事件/样本进行了分析。
统计分析 使用学生的 t吨 -配对或非配对数据的检验,或非参数数据的Mann-Whitney U检验。
结果 成年SVZ常住NPC增殖受损 我们首先研究了慢性CNS炎症对EAE和HC小鼠SVZ中有丝分裂活性祖细胞(C、B和A型细胞)增殖动力学和命运的影响。 我们采用的小鼠模型非常适合研究炎症与SVZ驻留NPC之间的相互作用,因为炎症高峰期前脑前部三分之一的炎症浸润位于SVZ的腹侧和背侧。 在30 dpi时处死6只EAE小鼠,并对前脑炎症损伤进行量化。 共列举了89个病灶(14个,每只小鼠8个)。 总计30/89(33.7%)被归类为实质内病变,26/89(29.2%)为SVZ病变,33/89(37%)为软脑膜病变(每区平均数:实质内=5.0±1.85;SVZ=4.3±0.85;软脑膜=5.5±1.54)( 补充图1 ). 为了使用S期累积标记技术研究细胞周期长度和生长分数,将饱和剂量的IddU(Morshead和van der Kooy, 1992 ; 高桥 等人。 , 1992 ). IddU(独立数据单元) + 在端脑区背侧和腹侧SVZ内计数细胞,范围从短角+1.2到短角+0。
为了研究快速分裂的传递扩增祖细胞(C型细胞),我们使用了短期IddU标记方案(参见 补充数据 ). 我们没有发现细胞周期长度有任何显著差异( T型 c(c) )EAE和HC小鼠的SVZ中( 表1 ). 另一方面,EAE小鼠在20和30dpi时的GF显著低于HC(两者均为 P(P) ≤0.05),尽管在60至90dpi之间观察到回归基线值( 表1 ). 因此,M相限制的磷酸化组蛋白H3(pH3)的绝对数量显著减少 + 在20、30和60dpi的EAE小鼠中观察到SVZ细胞( 图1 A) 与HC(所有 P(P) ≤ 0.05). 同样,pH3数量回归基线值 + 在90 dpi的EAE中观察到细胞(数据未显示)。 最后,如果有任何添加 + /伊巴1 + 和/或CD45 + /Ki67号机组 + EAE小鼠SVZ内发现细胞( 图1 B–E),因此表明局部小胶质细胞或CNS浸润的血源性白细胞的增殖对SVZ背侧定量的总GF没有显著贡献。 神经细胞凋亡不能解释观察到的GF减少,因为caspase-3的数量没有差异 + 在EAE小鼠和HC之间发现SVZ细胞(数据未显示)。
表1。 EAE和HC小鼠SVZ中快速分化(C型)祖细胞的细胞周期分析
老鼠 一 不。
T型 c(c) b条
GF公司 c(c)
第页 2 d日
P(P) -价值
HC(6周龄) 27 12.2 27.2 ± 0.004 0.94 不适用
HC(18周龄) 6 13 24.0 ± 0.4 0.89 NS公司 **
CFA(6周龄) 8 12.2 26.9 ± 0.7 0.93 NS公司 **
EAE 20 dpi 15 12.1 20.0 ± 2.1 0.89 0.002 †
EAE 30 dpi 15 12.9 19.1 ± 1.2 0.86 0.001 †
EAE 60 dpi 12 11.9 27.0±1 0.86 NS公司 †
EAE 90 dpi 8 12.3 24.7 ± 0.79 0.89 NS公司*
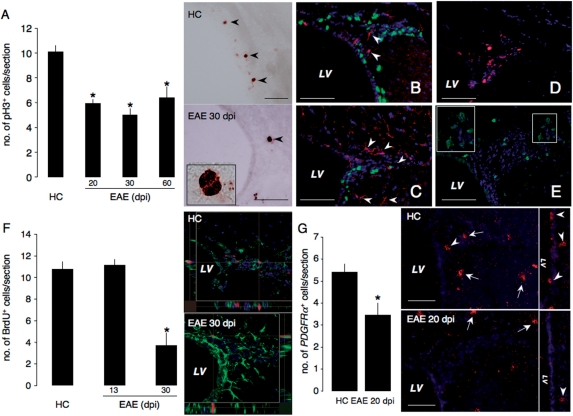
图1。
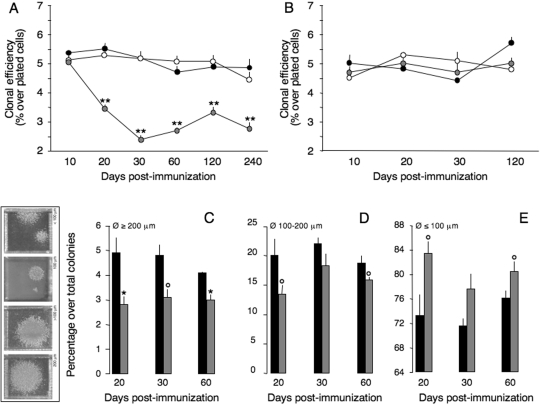
慢性自身免疫性CNS炎症损害SVZ常驻NPC的增殖 体内 . ( A类 )M期限制性磷酸化组蛋白H3(pH3)降低 + 在20、30和60dpi的EAE小鼠SVZ中观察到细胞。 图表中的数据表示为pH3-免疫活性细胞/切片±SEM的平均数,从以下总数中获得 n个 每组≥5只小鼠* P(P) 与HC相比,≤0.05。 pH3的两个代表性图像 + 显示HC和EAE 30 dpi SVZ中的细胞。 标尺50μm。 ( B–E类 )HC小鼠背外侧SVZ冠状切片( B类 和 D类 )和EAE为30 dpi的小鼠( C类 和 E类 )显示快速增殖的IddU + 单元格(绿色 B类 和 C类 ),IddU + /伊巴1 + (绿色和红色 B类 和 C类 )和CD45 + /Ki67号机组 + (绿色和红色 D类 和 E类 EAE和HC中的细胞。 箭头表示Iddu —— /伊巴1 + 两个面板中的单元格。 比例尺:50μm。 ( F类 )在30 dpi的EAE小鼠SVZ中观察到长期BrdU保留细胞减少。 小鼠从13或30 dpi开始接受BrdU治疗6天,并在最后一次注射BrdU 40天后处死。 数据表示为BrdU的平均数 + 细胞/截面±SEM,并从总计 n个 每组≥3只小鼠 n个 ≥2个独立实验* P(P) 与HC相比,≤0.001。 两张具有代表性的共聚焦显微镜照片显示了长期保持的BrdU + (红色)GFAP + 显示HC和EAE 30 dpi SVZ的(绿色)单元格。 ( G公司 )表达mRNA的SVZ细胞减少 PDGFrα 在20 dpi的EAE小鼠SVZ中观察到。 PdgfRα mRNA由位于SVZ内的假定型慢分化细胞以及广泛分布于成人脑实质内的OPC表达(上图中的箭头)。 数据表示为 PDGFrα + 细胞/截面±SEM,并从总计 n个 每组≥3只小鼠。 比例尺:50μm。 细胞核在( B–G类 )已用DAPI复染。 左心室,侧脑室。
这些数据表明,慢性CNS炎症导致GF-b的显著降低,而不是 T型 c(c) -SVZ驻留的转运扩增神经前体细胞(C型细胞),其增殖缺陷往往在炎症消退时尽早恢复。
为了研究缓慢分裂的相对静止的假定CNS干细胞(B型细胞),进行了长期保留分析(BrdU标记)(Morshead 等人。 , 1998 ). 成人SVZ的标签染色假定CNS干细胞(B型细胞)与放射状胶质细胞和实质性星形胶质细胞具有一些关键特征,包括GFAP的免疫反应性(Doetsch 等人。 , 1999 ). 作为这些细胞的明确标识 体内 由于无法获得唯一的分子标记,传统的免疫检测技术很难做到这一点。根据形态学、生物学和分子标准的组合,CNS干细胞被定义为真正的胶质细胞,类似于星形胶质细胞(Pinto和Gotz, 2007 ). 虽然在13dpi时未发现标记阳性SVZ细胞的差异,但保留BrdU的GFAP显著降低 + 与HC相比,EAE小鼠在30 dpi时观察到SVZ细胞( P(P) ≤ 0.001) ( 图1 F) ●●●●。 我们还执行了 就地 血小板衍生生长因子(PDGF)受体α的杂交,这是一种分子标记物,已证明在啮齿动物视神经和脊髓的相对静止的少突胶质前体细胞(OPC)中表达 等人。 , 1983年 , b条 )以及高达80%的成人SVZ B型细胞(Jackson 等人。 , 2006 ; 门(Menn) 等人。 , 2006 ). 与长期保留分析一致,表达mRNA的SVZ细胞显著减少 PDGFrα 与HC相比,在20 dpi的EAE中观察到( P(P) ≤ 0.05) ( 图1 G) 。
因此,在EAE炎症期的高峰期也观察到缓慢分裂的SVZ推测干细胞(B型细胞)减少。
SVZ生态位中细胞之间的时间和空间关系改变 为了更好地描述EAE中功能紊乱的不同SVZ细胞类型的形态学特征,我们对SVZ前角心室侧壁的横截面进行了光和EM分析。 从HC和EAE小鼠获得10、20、30和60dpi的切片,并根据既定的超微结构标准鉴定和评分不同的SVZ细胞类型(Doetsch 等人。 , 1997 )。
在分析的每个时间点,与HC相比,EAE小鼠的每种不同细胞类型的形态学特征没有发生任何变化,例如光滑或粗糙内质网增加,线粒体或脂质体堆积。 然而,在细胞分布和组织上观察到显著差异。 两种半薄截面分析( 图2 A) 此外,EM显示,EAE小鼠在10–30 dpi时,A型祖细胞聚集,与室管膜带下方心室保护性激活的B型细胞邻接的C型和B型细胞减少( 图2 A、 B和E)。
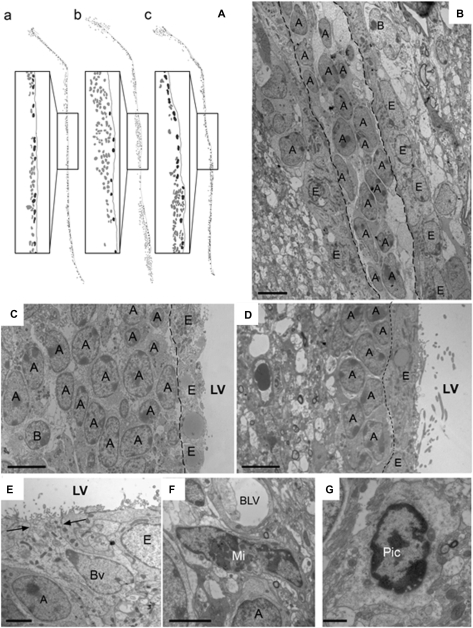
图2。
慢性自身免疫性中枢神经系统炎症损害SVZ生发生态位的细胞组织。 ( A类 )30(b)和60 dpi(c)时HC(a)和EAE小鼠SVZ沿线的细胞组织图。 代表性区域以较高的放大倍数显示。 注意HC中的均质组织,而EAE小鼠在30 dpi时,细胞积累并形成大细胞簇。 这些簇倾向于在60 dpi时恢复。 室管膜细胞为黑色,SVZ细胞为灰色; ( B类 )在30dpi下的EAE SVZ区域的透射EM。 迁移神经母细胞链( A类 )出现在侧脑室(LV),以不连续的线分隔。 室管膜细胞覆盖心室壁( E类 ); ( C类 )30 dpi的EAE小鼠表现出大细胞簇,由多层累积迁移细胞组成( A类 ); ( D类 )HC SVZ显示一组同质的迁移神经母细胞( A类 ). 箭头表示A型细胞之间的典型自由空间,在EAE小鼠中变得不太明显; ( E类 )单个B型细胞或星形胶质细胞的代表性图像( B类 )通过膨胀接触心室(LV)(箭头所示)。 这些星形胶质细胞可能被激活以响应增殖信号,并趋向于在EAE小鼠的SVZ内消失; ( F类 )单个小胶质细胞(Mi)的代表性图像。 其中一些细胞充满致密体,通常位于血管(BLV)附近,在10–30 dpi时,EAE小鼠的SVZ趋于增加; ( G公司 )EAE小鼠SVZ中的Picnotic细胞(Pic)短暂增加。 比例尺英寸 B类 , C类 和 D类 :5μm,当处于 E类 和 F类 :2微米。
在HC中,A型细胞通常被拉长(迁移形态),而在30 dpi的EAE小鼠中,它们表现出更球形。 此外,A型电池(Doetsch 等人。 , 1997 )在EAE小鼠的SVZ中不太明显( 补充图2 )。
偶尔,这会导致非迁移的A型细胞突入心室腔,心室腔似乎与两层E型细胞相邻( 图2 B) ,而一些A型细胞簇似乎通过纹状体沿着血管转移出SVZ(数据未显示)。
尽管EAE小鼠不同SVZ细胞类型的形态学没有改变,但SVZ细胞结构的多灶性紊乱是实质性的。 EAE小鼠在30 dpi时SVZ的某些区域在心室腔界面上显示出多达6至7层A型细胞的局灶性聚集,而HC通常只显示两层A型电池( 图2 C和D)。
量化这些变化(另请参见 补充图2 和补充数据),我们用EM计算了EAE和HC小鼠不同SVZ细胞类型的百分比。与HC(11.2±0.7%, P(P) ≤0.001)。 与HC(0.81±0.1%, P(P) ≤ 0.05). 60 dpi时,EAE小鼠的C型细胞百分比(9.5±0.9%)和有丝分裂(0.95±0.2%)恢复到基线值。 此外,我们发现,与HC(0.35±0.1%)相比,EAE小鼠在20 dpi(0.56±0.3%)时血管周围(激活的)小胶质细胞几乎增加了2倍( 图2 F) ●●●●。 最后,EAE小鼠的picnitis细胞仅在20dpi(1.12±0.5%)时显著增加,而HC(0.3±0.06%, P(P) ≤ 0.05) ( 图2 G) ●●●●。 室管膜细胞、星形胶质细胞和神经元的相对百分比在各组之间没有差异。
EAE小鼠嘴侧迁移流中神经母细胞的迁移缺陷 然后我们假设,由于持续的中枢神经系统炎症,EAE小鼠的A型细胞迁移能力发生改变,SVZ中积聚了非迁移神经母细胞。 为了解决这个问题,我们对EAE和HC小鼠的嘴侧移行流(RMS)进行了半薄切片分析。
我们发现EAE小鼠在30dpi时的RMS严重紊乱( 图3 A) 迁移神经母细胞显著减少( 图3 A、 下部面板中的红细胞)和更多的星形胶质细胞( 图3 A、 下部面板中的绿色单元格)。 60 dpi时EAE小鼠的RMS( 图3 B) 表现出恢复正常形态的趋势( 图3 C) ●●●●。 EM证实了两组小鼠RMS中的细胞身份(数据未显示)。 因此,在20和30 dpi的EAE小鼠中,矢状脑切片的免疫荧光分析显示PSA-NCAM的积累增加 + 更多吻侧SVZ内的成神经细胞,不像HC中检测到的那样密集成排,但分散在RMS内,可能表明存在迁移缺陷( 图3 D、 放大的插图)。 事实上,EAE小鼠RMS周围的星形胶质细胞神经胶质管因GFAP的积累而受到破坏 + 细胞位于RMS内或侧薄壁组织内。
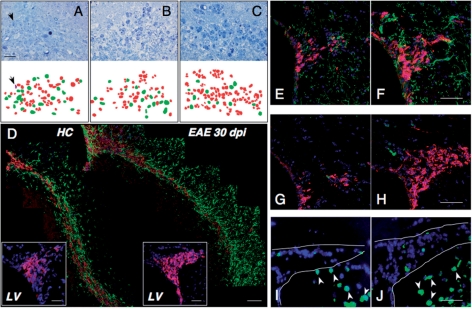
图3。
慢性自身免疫性CNS炎症损害SVZ成神经细胞的迁移。 ( A–C )EAE小鼠30岁时RMS的代表性甲苯胺蓝染色半薄切片( A类 )和60 dpi( B类 )和HC( C类 ). 取下相同的切片,重新切割超薄切片。 在EM上对细胞进行了研究,并将其鉴定为成神经细胞或星形胶质细胞(下部面板中为红色和绿色)。 注意30 dpi时EAE小鼠RMS的紊乱( A类 )迁移神经母细胞和大量星形胶质细胞的数量极低。 60 dpi时EAE小鼠的RMS表现出恢复正常形态的趋势( B类 ),与HC相比( C类 ). 30 dpi处的箭头显示小胶质细胞(紫色)。 比例尺:20μm。 ( D类 )从具有代表性的HC(左侧面板)和EAE为30 dpi的鼠标(右侧面板)对整个RMS进行矢状重建。 PSA-NCAM(红色)检测到迁移神经母细胞,而GFAP(绿色)检测到星形胶质细胞。 注意正常PSA-NCAM + HC小鼠中的迁移细胞链(左侧面板)。 相比之下,PSA-NCAM + 30 dpi时,EAE小鼠RMS中的细胞在向嗅球迁移的过程中出现紊乱(右图)。 EAE小鼠的GFAP数量也增加 + RMS周围薄壁组织内的星形胶质细胞。冠状切面显示迁移链明显紊乱,PSA-NCAM较少 + EAE小鼠背部SVZ水平的成神经细胞(放大插图中的紫色细胞)。 放大插图中的细胞核已用DAPI进行了复染。 比例尺:50μm。 LV=侧脑室。 ( E–J )冠状脑切片显示PSA-NCAM(红色)和NG2(绿色)的双重免疫荧光 E类 和 F类 )或Olig2(绿色 G公司 和 H(H) ). 注意,在30 dpi的EAE小鼠中,NG2和Olig2都没有共同染色( F类 和 H(H) )和HC( E类 和 G公司 ). 在 我 和 J型 ,HC小鼠的NeuN染色(绿色)( 我 )在EAE小鼠中( J型 )分别为30 dpi。 请注意,这两只小鼠的SVZ(周围有一条连续的线)中几乎没有细胞染色,而大多数纹状体神经元染色(箭头)。 在所有面板中,用DAPI对细胞核进行了复染,标尺为100μm。
我们还研究了观察到的非迁移性神经前体细胞的积累是否可能掩盖了向少突胶质细胞和神经发生的转变。 我们没有发现PSA-NCAM的证据 + 共同表达OPCs的两个假定标记之一NG2的细胞( 图3 E和F)和Olig 2( 图3 G和H)。 此外,基于激光捕获显微切割(LCM)的主要(少突胶质)胶质细胞命运决定因素的基因表达分析(例如。 奥利格1 , 奥利格2 , Nkx2.1个 , Nkx2.2个 )在SVZ中,EAE 20 dpi和HC之间没有差异( 补充图3 ). 同样,我们在30 dpi时未发现成熟NeuN的增加 + SVZ内的神经元( 图3 I和J)。 EM分析也证实了后一发现,HC中SVZ神经元的数量(0.34±0.1)与EAE在30dpi时的数量(0.57±0.2; P(P) =NS)。
最后,我们直接分析了新生成的SVZ细胞如何向生理(例如OB)迁移。 为此,我们使用了一种表达绿色荧光蛋白(GFP)的复制缺陷型逆转录病毒。 将载体以20dpi和GFP数量注射到HC和EAE小鼠的右心室 + 注射后19天,在从SVZ前部到OB的区域对细胞进行定量( 图4 A) ●●●●。 与HC相比,EAE小鼠表现出显著的( P(P) ≤0.05)GFP降低 + 细胞沿RMS切向迁移至OB并分化为颗粒神经元和肾小球周围神经元( 图4 B) ●●●●。 相反,在非迁移性GFP亚群中,我们没有观察到EAE 20 dpi和HC之间的任何定量差异 + 在SVZ级别检测到的细胞( 图4 B–F)。
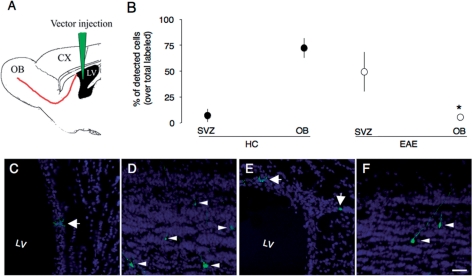
图4。
逆转录病毒细胞追踪显示SVZ子代的迁移行为受损。 ( A类 )将表达绿色荧光蛋白(GFP)的复制缺陷型逆转录病毒立体定向注射到侧脑室,感染S期局限性细胞。 绿线表示针迹,红线表示RMS。注射19天后,GFP + 沿着RMS迁移的细胞在从前SVZ到OB的区域中被编号。 OB,CTX=皮层; LV=侧脑室。 ( B类 )EAE小鼠表现出GFP亚群的显著减少 + 细胞迁移至OB和非迁移GFP增加 + 与HC相比,检测到的细胞非常接近SVZ。 数据表示为从 n个 =每组3只小鼠* P(P) ≤ 0.05. ( C–F类 )GFP公司 + 在SVZ衬里和HC的OB中检测到细胞(绿色)( C类 和 D类 )20 dpi时的EAE( E类 和 F类 ). 中的箭头 C类 和 E类 表示SVZ GFP + 细胞。 箭头指向 D类 和 F类 显示OB GFP + 细胞。 细胞核用DAPI复染。 比例尺:150μm。 左心室,侧脑室。
这些结果提供了明显的迁移障碍的证据,并排除了EAE小鼠新生成的SVZ子代向(少突)胶质生成的转变。
EAE小鼠NPC克隆效率受损 在体外 接下来,我们通过使用 体外 化验。 研究表明,神经球形成细胞主要由C型(和B型)细胞组成 在体外 (莫尔谢德 等人。 , 1994 ). 因此,我们使用了经典 在体外 利用克隆神经球数量进一步表征EAE小鼠SVZ干细胞群体的NS-A 在体外 作为推测干细胞绝对数量的度量 体内 (雷诺兹和韦斯, 1992 ; 莫尔谢德 等人。 , 1994 )。
与HC和CFA免疫小鼠的神经球相比,EAE小鼠的神经小球(初级和次级)在任何时间点都没有显示出大小差异( 补充图4 )因此,表明来自有症状EAE小鼠的SVZ干细胞与来自对照组的细胞在有丝分裂能力上没有差异。 然而,一旦临床EAE开始,SVZ原代神经球的克隆效率在无症状(例如,10dpi)EAE小鼠和HC之间具有可比性,但却变得不同。 事实上,在20、30、60、120和240 dpi时,EAE小鼠产生的初级神经球明显较少(全部 P(P) ≤0.0001),与对照组相比( 图5 A) ●●●●。
图5。
慢性自身免疫性中枢神经系统炎症小鼠的神经球显示自我更新减少。 ( A类 )HC(黑圈)和CFA免疫对照组(白圈)以及EAE小鼠(灰圈)克隆效率的定量分析。 注意,与对照组相比,在20、30、60、120和240 dpi时,EAE小鼠初级神经球的克隆效率显著且持续受损。 ( B类 )EAE小鼠原代神经球的克隆效率在 n个 =10次放大 在体外 它是HC和CFA免疫对照组。 每个实验组共有三到六只小鼠在每个时间点进行分析。 数据表示为平均克隆效率±SEM,总计 n个 ≤3个独立实验** P(P) ≤0.0001。 ( C–E类 )基于神经集落形成细胞(NCFC)分析的( C类 ),中等-( D类 )和小型( E类 )殖民地。 注意,与HC(黑条)相比,EAE小鼠的大中型菌落显著且持续减少,而小菌落增加(灰条)。 数据表示为菌落±SEM的平均百分比占总电镀细胞数的百分比 n个 ≥3个独立实验。 每个实验组共有6只小鼠在每个时间点进行分析* P(P) ≤ 0.05; ° P(P) ≤ 0.005. Ø,菌落直径。
克隆效率的下降在同一时间点的次级神经球中得到证实( 补充图4 )进一步证实了之前 体内 观察到,在小鼠慢性EAE的某些时间点,SVZ干/前体细胞室发生显著损伤。 有趣的是, 在体外 用FGF-II和EGF对EAE小鼠神经球进行扩展培养,共扩增10代,完全逆转了在初级和次级神经球中观察到的克隆效率受损( 图5 B) ●●●●。 为了解决经典NS-A(Bull和Bartlett, 2005 ; Singec公司 等人。 , 2006 ),我们重复了 在体外 使用基于大小的NCFCA量化干细胞样细胞,该NCFCA最近被开发用于区分由 真诚地 根据体外不同的增殖潜能,神经干细胞来源于由祖细胞形成的神经干细胞(路易斯 等人。 , 2008 ). 大型神经集落形成细胞显著减少(假定具有较大的自我更新能力)( 图5 C、, P(P) ≤0.05(20、30和60 dpi)以及中等菌落(假定自我更新能力有限)( 图5 D、, P(P) 与HC相比,EAE小鼠SVZ的细胞在20和60 dpi时均≤0.05。 与此同时,小型群体显著增加(如果有的话,自我更新能力很低)( 图5 E、, P(P) 在20和60dpi下均≤0.05)。 有趣的是,少校 在体外 与HC和CFA免疫对照组相比,EAE小鼠SVZ的SVZ干细胞的生物学特性没有显著改变,即具有有丝分裂原、自我更新和去除丝裂原后的多向分化( 补充图5 )。
进一步证实EAE期间发生的炎症会显著损害慢增殖和快增殖SVZ细胞的动力学 在体外 数据还表明,神经球生长的化学定义的生长因子富集(FGF-II加EGF)微环境可能是 就其本身而言 足以重建观察到的细胞非自主功能障碍。
炎症依赖性细胞周期进程放松调控 为了阐明炎症诱导的SVZ细胞衰竭的一些分子机制,我们在不同的时间点(例如10、20、30和120dpi)对EAE小鼠急性解离的SVZ进行了广泛的基于TaqMan®低密度阵列(TLDA)的基因表达谱分析。 对涉及干细胞、炎症、免疫、自我更新、分化和迁移的167种不同mRNA进行了测量(参见 补充信息 ). 基因表达的差异主要见于20和30dpi的EAE( 第页 2 =0.60和 第页 2 分别=0.59),与10和120 dpi(两者都是 第页 2 = 0.92) ( 补充图6 )。
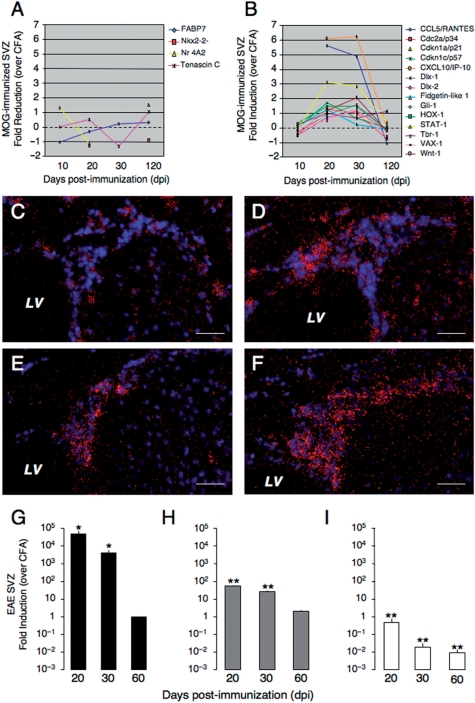
有趣的是,60.5%(101/167)和27.5%(46/167)的筛选基因要么在任何时间点都没有变化,要么在一个以上的时间点都没有表达。 与HC相比,在20和/或30dpi时,EAE小鼠SVZ中只有9%(15/167)的筛选基因上调。 另一方面,在EAE小鼠中,3%(5/167)的基因表达下调,其中我们确定了SVZ生发龛干/前体细胞的至少两个主要标记,如 精氨酸-1 和 腱糖蛋白 (马蒂诺和普鲁奇诺, 2006 )( 图6 A) ●●●●。 根据SVZ的LCM分析( 补充图3 ),我们没有发现(少突胶质细胞)胶质细胞命运基因决定簇的任何上调,例如 Nkx2.2个 ( 图6 A和B)。
图6。
CNS炎症在mRNA水平诱导细胞周期调节器和神经源性转录因子的表达。 ( A类 , B类 )对选定的mRNA进行半定量分析。 中的图形 A类 包括以下列表 n个 =与CFA免疫对照组相比,EAE小鼠SVZ中的5个选定基因在任何时间点均表现出显著下调(倍数减少≥1)。 中的图形 B类 包括以下列表 n个 =与CFA免疫对照组相比,EAE小鼠SVZ中的15个选定基因在任何时间点均表现出显著上调(折叠诱导≥1)。 ( C–F类 ) 现场 杂交 直径x2 ( C类 和 D类 )和 Cdkn1a/p21 ( E类 和 F类 )在两个HC的冠状脑切片上( C类 和 E类 )和EAE 30 dpi( D类 和 F类 ). EAE小鼠显示 直径x2 + 和 Cdkn1a/p21 + 与HC相比,SVZ内的细胞。 在暗场光学显微镜下用20倍物镜捕获放射自显影颗粒(红色),并通过DNA染色(DAPI,蓝色)观察组织。 LV=侧脑室。 比例尺:50μm。 ( G–I型 )IFN-γ和TNF-αmRNA水平显著升高( G公司 和 H(H) 与CFA免疫对照组相比,EAE小鼠在20和30 dpi时的SVZ中。 中的图形 F类 显示出 IL-1β 20和30dpi时EAE小鼠SVZ中的mRNA水平。 数据表示为平均任意单位±SEM,并从以下SVZ中获得 n个 每只小鼠每组每时间点≥6只* P(P) ≤0.05** P(P) ≤ 0.0001.
在上调的基因中,最突出的是炎症调节因子(例如。 CCL5/兰特 , CXCL10/IP-10 和 血红素氧化酶1 ),IFN-γ信号传导下游的转录因子(例如。 状态-1 ),许多细胞周期调节因子(例如。 Cdc2a/p34 , Cdkn1a/p21 和 Cdkn1c/p57 ),和两种神经链特异性转录因子(例如。 直径x1 和 直径x2 )( 图6 B) ●●●●。 作为 体内 证实了后一数据,更多的细胞表达 Cdkn1a/p21 + 和 直径x2 + 与HC相比,30 dpi时EAE小鼠SVZ中观察到mRNA细胞( 图6 C–F)。
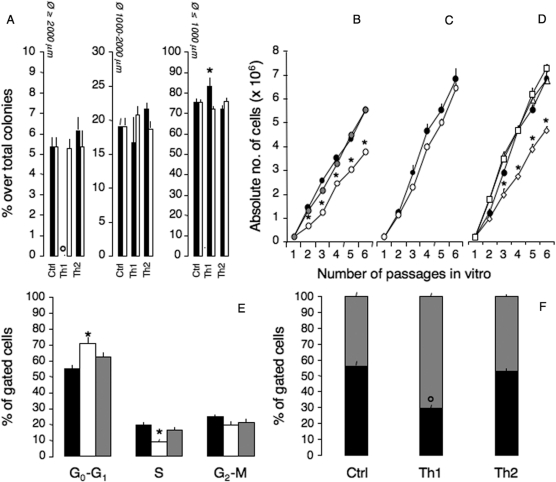
SVZ NPC的静止诱导 在体外 通过炎症细胞因子 我们观察到,EAE小鼠SVZ中的基因表达模式支持了以下观点:增殖和迁移受损 体内 可能是CNS局限性炎症过程导致细胞周期放松调控的结果。 我们发现促炎症(Th1)细胞因子的mRNA水平显著上调,如干扰素(IFN)-γ和肿瘤坏死因子(TNF)-α( 图6 G和H),但不是白细胞介素(IL)-1β( 图6 一) EAE小鼠SVZ中20和30 dpi( P(P) ≤0.005,与CFA免疫小鼠相比)。 鉴于Th1细胞因子在EAE慢性炎症的触发和持续中起着核心作用,因此我们假设Th1细胞素可能有助于EAE小鼠SVZ中观察到的干/前体细胞增殖受损。 HC的原代SVZ细胞在Th1(例如IFN-γ、TNF-α和IL-1β)或Th2(例如IL-4、IL-5和IL-13)细胞因子混合物的持续存在下生长。 当镀有Th1而非Th2时,细胞因子SVZ细胞在形成大型神经集落形成细胞时表现出明显的损伤( P(P) ≤0.0001,与对照SVZ细胞相比)。 与此同时,自我更新能力较低的小型群体也显著增加( P(P) ≤0.05,与对照SVZ细胞相比)。 仅在SVZ细胞试验中加入两种类型的细胞因子48小时后,观察到的结果均未得到( 图7 A) ●●●●。 为了证实NPC的自我更新是否会受到炎症性Th1细胞因子的影响,我们生成了在完全生长培养基(CGM)或富含Th1或Th2细胞因子的CGM中培养的神经球的连续生长曲线。 只有在富含Th1的CGM中培养的神经球表现出生长效率的逐渐显著下降(从两到六次扩增)( 图7 B、 全部 P(P) ≤0.05,与对照神经球相比),而在富含Th2的CGM培养的神经球中没有观察到差异。 有趣的是,当早期Th1细胞因子从CGM中去除并进行细胞扩增时 n个 =再扩增6次,之前接触细胞因子的神经球的生长效率恢复到对照值( 图7 C) ●●●●。 在Th1细胞因子中,IFN-γ-而非TNF-α和IL-1β-似乎在神经球长期增殖能力受损中起着关键作用( P(P) ≤0.05,与对照神经球相比)( 图7 D) ●●●●。 作为进一步的证实,我们发现SVZ NPC暴露于Th1细胞因子而不是Th2细胞因子会导致 G公司 0 / G公司 1 相位( P(P) ≤0.005),并平行减少S期细胞( P(P) ≤0.005)。 在 G公司 2 /组间M相限制细胞( 图7 E) ●●●●。
图7。
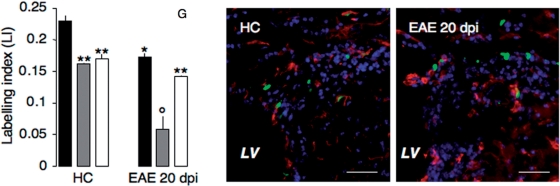
慢性CNS炎症导致神经干细胞静止 在体外 和 体内 . ( A类 )在存在Th1细胞因子(IFN-γ,500 U/ml;TNF-α,200 U/ml,IL-1β100 U/ml)或Th2细胞因子(IL-4、IL-5和IL-13,均为10 ng/ml)的情况下,对主要SVZ NPC进行NCFC分析。 在最后48小时(白色条)或整个试验期间(黑色条),SVZ细胞以克隆密度接种在富含细胞因子的NeuroCult中。 用Th1或Th2细胞因子处理48小时后,所生成的菌落百分比没有差异,而较长时间(3周)的Th1细胞因子处理导致大菌落生成完全失败。 数据表示为菌落/大小占总电镀细胞±SEM的平均百分比,从以下总数中获得 n个 ≥3个独立实验。 ° P(P) ≤ 0.0001; * P(P) ≤ 0.05. ( B–D类 )用富含细胞因子的CGM体外培养NPC的增殖分析。 ( B类 )Th1(白圈)或Th2细胞因子(灰圈)与CGM单独(黑圈)进行比较。 注意,Th1条件细胞的增殖率早在 n个 =扩增2代,而在富含Th2的CGM培养的神经球中没有观察到差异。 ( C类 )Th1细胞因子退出后,NPC在CGM中继续生长 n个 =6次扩增,与对照NPC(黑圈)相比,之前接触Th1细胞因子的NPC(白圈)生长效率没有差异。 ( D类 )成长NPC的增殖分析 在体外 富含单个Th1细胞因子的CGM。 单用干扰素-γ(白钻石)可显著降低生长速度(从四到六次扩增),而用TNF-α或IL1-β处理的细胞在任何时间点的生长效率均无差异。 数据表示为细胞的绝对数量±SEM,总计 n个 ≥3个独立实验* P(P) 与对照组相比,≤0.05。 ( E类 )NPC在富含Th1(白色条)或Th2细胞因子(灰色条)的CGM中培养48小时。 仅用CGM培养的NPC作为对照(黑条)。 注意细胞中显著向G方向移动(33-46%的细胞) 0 /G公司 1 以及在暴露于Th1但不暴露于Th2细胞因子时S期细胞的下降。 数据表示为门控细胞±SEM的平均百分比,总计 n个 ≥5个独立实验** P(P) 与对照组相比,≤0.05。 ( F类 )Ki67的FACS分析。 注意G的显著增加 0 -封闭Ki67 —— Th1细胞因子调节但不在非调节(Ctrl)或Th2细胞因子调节的NPC中的细胞(灰色条)。 黑色条表示Ki67 + 单元格。 数据表示为门控细胞±SEM的平均百分比,总计 n个 ≥10个独立实验。 P(P) 与对照组相比,≤0.0001。 ( G公司 )与基线值相比,在注射细胞因子3天后,HC或EAE 20 dpi小鼠的SVZ背外侧局部注射IFN-γ/TNF-α后,GF显著降低。 细胞因子注射后10天(白条),仅HC的GF仍显著低于正常值。 在处死前,通过连续接触全身IddU 10小时来检测NPC的增殖,并仅通过计算IddU进行评估 + /伊巴1 —— (面板中分别为绿色和红色单元格)SVZ中的单元格。 黑色条表示基线时间点。 数据表示为平均标记指数(L.I.)±SEM,总计 n个 ≥3只小鼠。 在这些面板中,显示了注射IFN-γ/TNF-α的两个代表性HC和EAE小鼠的SVZ图像。 细胞核用DAPI复染。 比例尺:50μm* P(P) ≤0.05** P(P) ≤ 0.005. LV=侧脑室。
然后,我们试图更详细地分析由Ki67抗原的表达所确定的细胞因子条件NPC的增长部分,Ki67抗原是一种分子标记物,在生长后期仅在增殖细胞中表达 1 、S、G 2 或细胞周期的M期。 因此,Ki67的百分比显著增加 —— G公司 0 -当NPC暴露于Th1细胞因子而非Th2细胞因子时,观察到的相限制性静止NPC占培养细胞总数的70.6±1.9%( 图7 F、, P(P) ≤0.0001,与对照和Th2-条件神经球相比)。 Annexin/PI染色评估的细胞凋亡并不能解释任何观察到的现象(数据未显示)。
炎症细胞因子对SVZ细胞周期的影响 体内 进一步研究促炎细胞因子在解除NPC细胞周期调控中的作用 体内 我们分析了HC和EAE小鼠立体定向注射Th1细胞因子混合物(如TNF-α和IFN-γ)后的SVZ,如前所述(Merkler 等人。 , 2006 ). 在细胞因子注射后3天和10天处死小鼠 体内 使用系统性IddU标记增殖细胞进行细胞周期分析。 在注射TNF-α/IFN-γ的HC中发现SVZ快速增殖的转运扩增前体细胞(C型细胞)严重受损( P(P) ≤0.005,与未经治疗的HC小鼠相比)( 图7 G) ●●●●。 类似地,IddU + 与未经治疗的EAE小鼠相比,TNF-α/IFN-γ注射EAE小鼠的前体细胞进一步减少( P(P) ≤ 0.05). 早在首次细胞因子注射后10天,这种表型就部分逆转( 图7 G) 细胞因子等分子的预期半衰期 体内 。
讨论 这里我们发现,在CNS局限性慢性炎症高峰期,EAE小鼠SVZ中快速循环(C型细胞)和缓慢分裂(B型细胞)细胞的增殖均显著减少,同时新生成的非迁移神经母细胞(a型细胞)增加。 此更改与 在体外 和 体内 变化:细胞周期蛋白依赖性激酶抑制剂Cdkn1a/p21的表达(Gartel 等人。 , 1996 )EAE小鼠SVZ增加; EAE小鼠SVZ衍生神经球克隆效率低; 以及Ki67的百分比 —— G公司 0 暴露于促(Th1)而非抗(Th2)炎症细胞因子后,相限制性静止NPC最多增加70%。 这些结果表明,持续的中枢神经系统炎症通过上调细胞周期抑制剂来抑制前体细胞和SVZ生发龛内干细胞进入细胞周期,从而显著改变其细胞动力学。
虽然慢性炎症在降低SVZ细胞的GF中所起的中心作用通过以下事实得到证实,即在EAE小鼠中, 目前尚不清楚为什么SVZ内存在成神经细胞的平行积累。 在这里,我们提供了直接证据,证明SVZ细胞无法在慢性炎症微环境中沿RMS切向迁移至OB。 后一项发现,再加上EM证据显示EAE中SVZ细胞的形态保持但位置改变,提示我们假设持续的CNS局限性炎症也可能影响RMS内形成胶质管的实质性星形胶质细胞,因此, 改变SVZ子代的迁移能力(新生成的PSA-NCAM + 单元格)。 同样,正如之前所建议的那样,一些成神经细胞也很可能将其生理性嘴侧迁移转向胼胝体中更多的尾侧炎症损伤(Picard-Riera 等人。 , 2002 )。
有趣的是,在EAE小鼠的炎症高峰期,SVZ衍生神经球的克隆效率显著降低,但在广泛使用后恢复到正常值 在体外 用生长因子培养。 这一结果与 体内 有证据表明,一旦CNS炎症减轻,SVZ常驻细胞就会表现正常,这表明某些细胞非自主因素可能会暂时改变NPC的自我更新 体内 和 在体外 在这些因素中,促炎细胞因子似乎起着主要作用。 我们发现IFN-γ诱导NPC动力学改变 在体外 和 统计-1 -属于IFN-γ细胞内信号途径(Robinson和O'Garra, 2002 )-在炎症高峰期EAE小鼠SVZ中上调。 此外,IFN-γ还能够限制NPC细胞周期向G 0 阶段 在体外 并损害SVZ细胞的增殖 体内 这些IFN-γ介导的效应是短暂的、可逆的,与诱导凋亡无关,并且得到了先前证据的支持。 先前已经证明,I型和II型干扰素可以通过Janus激酶信号转导子和转录途径激活剂影响不同细胞类型的生长,特别是通过转录因子Stat-1(Bromberg 等人。 , 1996 ). 炎症分子在改变NPC自我更新中所起的中心作用也得到了前炎症细胞因子IL-6(Monje 等人。 , 2003 )。
这里描述的影响与我们研究的特定脑疾病模型有关,不同类型的脑损伤(例如缺血性中风、神经退行性疾病等)可能会导致相反的结果(Calza 等人。 , 1998 ; 皮卡德·里拉 等人。 , 2002 ; 张 等人。 , 2004 ; 金 等人。 , 2006 ; 奈特·乌梅斯马 等人。 , 2007 )例如,最近的研究表明,不同的炎症因子(如IL-4和IFN-γ)或免疫细胞本身可能不同地支持胶质或神经生成(Butovsky 等人。 , 2006 ; Ziv公司 等人。 , 2006 )。
因此,在该模型中,持续的CNS区室化炎症介导SVZ细胞的变化,当炎症减轻时,SVZ细胞会恢复。 复发缓解型多发性硬化症中反复发作的炎症会导致什么结果? 需要评估EAE的其他模型(如SJL/J模型)来回答这个问题。 确定SVZ细胞增殖缺陷在多次炎症发作后是否会继续可逆也很有趣。 还需要进一步研究,以阐明反复的炎症打击是否会导致SVZ发生永久性变化,从而导致内源性神经干/前体细胞室的稳态和修复能力的不可逆转的失败。 我们的研究结果对从生发龛动员鼻咽癌的治疗策略具有指导意义,其有效性取决于炎症的消除以及SVZ细胞的长期可塑性。