肥胖,如果没有纠正 导致心肌肥大,心肌功能和能量代谢受损,导致心脏病发病率和死亡率增加( 11 , 24 , 43 ). 以细胞大小和蛋白质合成增加为特征的心脏肥大与肥胖者心室功能障碍、心力衰竭和恶性心律失常风险明显增加有关( 21 ). 研究表明,在没有任何全身血流动力学改变的情况下,肥胖患者的体重减轻可以缩小心脏尺寸并改善心脏性能( 1 ),表明肥大在持续性肥胖的心脏功能障碍中具有独立作用。 迄今为止,已经确定了过多的细胞信号通路参与了肥厚反应,包括丝氨酸-三烯激酶Akt的强直激活,以响应生长因子、血管紧张素II、机械应激、氧化应激、, 钙调神经磷酸酶和泛素蛋白酶体系统减少末端错误折叠蛋白的降解( 13 , 27 , 32 , 39 ). Akt可能调节与肥厚反应有关的多种信号分子,如哺乳动物雷帕霉素靶点( 38 ),真核起始因子4E-结合蛋白( 48 ),p70S6k( 15 , 39 ),GSK-3β( 15 , 16 ),叉头转录因子( 20 )和GATA4( 25 ). 此外,Akt的活性也受到磷酸酶和张力蛋白同源物(PTEN;Ref。 47 ). 然而,关于Akt在饮食诱导肥胖引起的心脏肥厚反应中的精确调节机制,目前几乎没有可用的信息。
叉头转录因子的Foxo亚家族,包括Foxo1(FKHR)、Foxo3a(FKHRL-1)和Foxo4(AFX),是Akt的下游靶点( 20 ). Akt磷酸化导致Foxo的核排斥(抑制)。 除了Foxo引起的成熟的细胞反应外,包括分化、代谢、增殖、存活和骨骼肌萎缩( 20 , 37 ),该转录因子在心肌细胞萎缩中也有表达,涉及一系列促肾上腺皮质激素的上调( 36 , 37 , 46 ). 在骨骼肌中,促甲状腺激素基因由生长因子Akt介导的Foxo因子转录调控控制( 35 , 37 ). 最近,研究表明Foxo转录因子在生长因子/Akt信号调节下在心肌细胞中表达。 Foxo可能控制一个atrogene转录程序来调节心肌肥大多种调节因子下游的心肌细胞大小( 40 ).
为了更好地理解肥胖相关的心脏肥大背后的机制以及由此产生的肌病变化,富含脂肪的饮食被用于培育饮食诱导的肥胖( 33 ). 我们实验室和其他实验室的最新证据表明,饮食诱导的肥胖与胰岛素抵抗、心肌肥厚和心肌功能障碍有关( 33 , 44 ). 然而,对于饮食诱导的肥胖症,人们发现心肌功能的不同结果。 Wilson等人( 50 )在食用“西方饮食”的大鼠中发现中度心脏功能障碍(45%的热量来自脂肪,与本研究中使用的高脂肪饮食相同)。 证据( 9 , 33 )在“西方饮食”(45%热量来自脂肪)诱导肥胖的大鼠和小鼠模型中,我们组的研究显示心肌和心肌细胞收缩功能障碍与心肌肥厚相关。 相反,Morgan等人( 28 )对已确诊的心力衰竭大鼠进行12周的“西方”高脂饮食(45%脂肪)喂养后,未能确定心脏重塑和收缩功能障碍。 有趣的是,在喂食脂肪成分较高(60%的能量来自脂肪;参考文献。 50 ). 冠状动脉结扎术后类似的高脂肪饮食(60%脂肪)会触发氧化磷酸化和电子传递链复合物活性的增加,而不会对左心室收缩功能或重塑产生不利影响( 34 ). 同样,Stanley及其同事( 4 , 29 )也有报道称,尽管在肥胖发生之前,喂食高脂肪饮食(60%脂肪)12至16周的小鼠和大鼠没有明显的心脏重塑和收缩功能障碍。 为了阐明摄入高脂饮食后心脏肥大和收缩功能障碍的相互作用,本研究旨在检测Akt、Foxo转录因子和萎缩特异性基因转录在高脂饮食诱导的心脏几何和功能改变中的作用。 鉴于泛素相关蛋白清除和钙调神经磷酸酶在心脏重塑和收缩功能调节中的显著作用( 13 , 22 , 31 , 31 )在高脂饮食喂养后,还评估了泛素和钙调神经磷酸酶以及其他肥厚标志物在心肌中的表达。
材料和方法 高脂肪饮食和血清参数。 这里描述的实验程序得到了怀俄明州大学动物使用和护理机构委员会的批准。 简言之,4个月大、体重约20克的雄性FVB小鼠被随机分为低脂组(分别占脂肪和碳水化合物总热量的10%和70%,目录号D12450B)或高脂组(脂肪和碳水化合物分别占总热量的45%和35%(37%饱和脂肪酸、46%单不饱和脂肪酸和19%多不饱和脂肪酸类) ,目录号D12451,通常被称为“西方饮食”( 50 )]6个月的饮食(研究饮食,新泽西州新不伦瑞克)( 33 , 49 ). 低脂肪和高脂肪饮食的胆固醇含量分别为18和196.5 mg/kg。 由于较高的脂肪组成,高脂肪饮食热量丰富(低脂饮食为4.83 kcal/g vs.3.91 kcal/g.)。 为了区分高脂肪饮食对高脂肪饮食诱导的肥胖的影响,第三组小鼠接受限制饮食的高脂肪饮食(约为随意高脂肪饮食摄入的80%),以匹配低脂饮食组的体重增加。 小鼠被单独饲养在一个受气候控制的环境中,12:12小时的光-暗循环,可以自由进食(除非食物受到限制)和饮水。 使用Accu-Chek III血糖分析仪测定血糖水平(禁食12小时后)( 12 ). 收缩压和舒张压用半自动放大尾套装置(IITC,Woodland Hills,CA)检测。 使用小鼠胰岛素ELISA试剂盒测量血胰岛素水平。 使用RIA试剂盒测定血浆瘦素浓度(Linco Research,St.Charles,MO)。
超声心动图评估。 使用配备15-6 MHz线性换能器的二维引导M型超声心动图(Phillips Sonos 5500)对麻醉小鼠(Avertin 2.5%,10μl/g体重ip)的心脏几何结构和功能进行评估(Phillip Medical Systems,Andover,MD)。 使用美国超声心动图学会采用的方法,从M型图像中记录左室前后壁厚度以及舒张和收缩尺寸。 使用(EDD-ESD)/EDD方程,从舒张末期直径(EDD)和收缩末期直径(ESD)计算分数缩短。 估计的超声心动图左室(LV)重量计算为[(LVEDD+间隔壁厚度+后壁厚度) 三 −LVEDD 三 ]×1.055,其中1.055(mg/mm 三 )是心肌密度。 10个心动周期的平均心率( 14 ).
心肌细胞的分离。 氯胺酮/甲苯噻嗪镇静后,取出心脏,用含有以下物质的Krebs-Henseleit碳酸氢盐缓冲液(单位:mM)灌注心脏:118 NaCl,4.7 KCl,1.2 MgSO 4 ,1.2千赫 2 人事军官 4 ,25氯化钠 三 、10 HEPES和11.1葡萄糖。 心脏用胶原酶D消化20分钟。左心室在过滤之前被移除并切碎。 肌细胞产量为~75%,不受高脂肪饮食的影响。 只有边缘清晰的杆状肌细胞被选作机械钙和细胞内钙 2+ 研究( 12 ).
细胞缩短和变长。 使用IonOptix软边系统(IonOptex,Milton,MA)评估心肌细胞的机械特性。 将肌细胞置于安装在Olympus IX-70显微镜平台上的腔室中,并用含有1mM CaCl的Krebs-Henseleit碳酸氢盐缓冲液超泡(~2ml/min,25°C) 2 。除非另有说明,否则以0.5 Hz的频率对肌细胞进行现场刺激。 评估细胞缩短和再延长,包括峰值缩短(PS)−峰值收缩力; 时间到PS(TPS)−收缩持续时间; 时间到90%再增强(TR 90 )−松弛时间; 和最大缩短/缩短速度(±dL/d t吨 )−和最大压力发展和下降( 12 ).
细胞内钙 2+ 瞬态。 用fura 2-AM(0.5μM)加载一组心肌细胞10分钟,并用双激发荧光光电倍增系统(Ionoptix)记录荧光强度。 将肌细胞置于Olympus IX-70倒置显微镜上,并通过Fluor×40油物镜成像。 将细胞暴露在75W灯发出的光下,并通过360或380-nm滤光片,同时以0.5 Hz的频率刺激细胞收缩。 荧光发射在480–520 nm之间检测到,并且根据两个波长(360/380)的FFI比率推断出呋喃2荧光强度(FFI)的定性变化。 计算荧光衰减时间(单指数或双指数衰减)作为细胞内钙的指标 2+ 清算( 12 ).
半胱氨酸天冬氨酸蛋白酶-3分析。 根据公布的方法测定半胱氨酸天冬氨酸蛋白酶-3活性( 23 ). 简单地说,在10000离心之前,将1ml PBS添加到含有左心室组织匀浆的烧瓶中 克 将上清液丢弃,并将匀浆溶解在100μl冰镇细胞裂解缓冲液中(50 mM HEPES pH 7.4、0.1%CHAPS、1 mM DTT、0.1 mM EDTA和0.1%NP-40)。 在96 well板中进行分析,每个孔包含30μl细胞裂解物、70μl分析缓冲液(50 mM HEPES、0.1%CHAPS、100 mM NaCl、10 mM DTT和1 mM EDTA)和20μl caspase-3比色底物Ac-DEVD-pNA(Sigma)。 将96-well板在37°C下孵育1 h,在此期间,允许样品中的半胱氨酸天冬氨酸酶从底物分子中裂解生色团p-NA。 在405nm处检测吸光度,caspase-3活性与显色反应成正比。 蛋白质含量采用Bradford法测定。 caspase-3活性表示为每分钟每毫克蛋白质释放的pNA微粒体。
半胱天冬酶-3/7分析。 Caspase-3和Caspase-7活性是使用Apo-ONE同质Caspase-3/7检测试剂盒(威斯康星州麦迪逊市普罗米加)测定的。 Caspase-3和Caspase-7是半胱氨酸天冬氨酸特异性蛋白酶(Caspase)家族的成员,在哺乳动物细胞的凋亡中起关键作用。 简言之,通过罗丹明110,bis的裂解,在凋亡细胞中检测到caspase-3和caspase-7活性- N个 -哥伦比亚特区- 我 -天门冬氨酰- 我 -谷氨酰- 我 -戊基- 我 -天冬氨酸酰胺(Z-DEVD-R110)底物,在分析前作为荧光底物存在。 为了进行Apo-ONE caspase-3/7分析,我们将caspase-3/4缓冲液和Z-DEVD-R110底物混合并添加到左心室组织匀浆中。 在通过caspase-3和caspase-7活性对DEVD肽进行顺序裂解和去除后,R110离开基团将在499nm的激发波长和521nm的发射波长处产生强烈的荧光。 caspase-3和caspase-7活性与R110荧光成正比,并表示为净荧光( 2 ).
体内显性阴性Foxo3a转染和Western blot分析。 对于体外显性阴性(DN)Foxo3a转染研究,H9C2成肌细胞(ATCC、Manassas、VA)首先在37°C的DMEM培养基(5.5 mM葡萄糖和10%FBS)中与或不与2μl DN-Foxo3a病毒(1:1000)孵育6 h,然后暴露于游离脂肪酸棕榈酸(0.8 mM)24 h。 剂量和治疗持续时间主要基于我们实验室和其他实验室以前的经验( 7 , 9 ). DN Foxo3a(从宾夕法尼亚州Vector Biolabs购买)是Foxo3的截短版本,它没有全长Foxo3a的C末端(D256)的事务激活域。 以前已经证明,截短的Foxo作为Foxo3a诱导的DN转录抑制剂发挥作用( 41 ). 然后从H9C2细胞中提取蛋白质,如前所述,用或不用DN Foxo3a处理( 10 ). 为了刺激胰岛素,在动物死亡和组织采集之前,向小鼠腹腔内注射胰岛素(1.5 U/100 g体重)10分钟。 含有等量蛋白质的样品在小型凝胶装置(Mini-PROTEAN II,Bio-Rad)中的10%SDS-聚丙烯酰胺凝胶上分离,并转移到硝化纤维素膜上。 用TBS-Tween中5%的牛奶封闭膜,并在4°C下与抗-Akt、抗-pAkt、反Foxo3a和抗-pFoxo3a(Thr32)(均来自马萨诸塞州贝弗利的Cell Signaling Technology)孵育过夜; 反GATA4(圣克鲁斯生物技术,加州圣克鲁斯); 抗睫状神经营养因子受体(CNTFR)-α(细胞信号); 抗钙调神经磷酸酶A(马萨诸塞州剑桥市Abcam); 抗泛素(西格玛-阿尔德里奇,密苏里州圣路易斯),稀释比为1:1000; 和抗GAPDH(作为负载控制,1:2000;信令)。 免疫印迹后,扫描胶片,并用Bio-Rad校准密度计检测免疫印迹带的强度( 12 ).
总RNA提取、cDNA合成、反转录和实时PCR。 使用TRIzol试剂(Invitrogen)从左心室提取总RNA,然后进行DNA酶消化以消除基因组DNA污染。 用分光光度计A260读数对RNA进行定量。 上标III使用1μg总RNA在20μl系统中在37°C下合成cDNA 60分钟( http://www.invitrogen.com/content.cfm?pageid=10281 ; Invitrogen)。 底漆是使用Beacon Designer 5.0软件设计的。 小鼠引物如下:atogin-1:正、5′-GCAGAGAGTCGGCAAGTC-3′和反义、5′-CAGGTCGGATCGTAG-3′; 和肌肉特异性无名指(MuRF)-1:感觉,5′-TGGAAACGCTATGGAGAACC-3′; 和反义,5′-ATTCGCAGCCTGGAAGATG-3′。 家政基因GAPDH(小鼠)的引物如下:sense,5′-AATGGTGAAGGTCGGTGAAC-3′; 和反义,5′-CGTTGAGTGGAGTCATACTGAAC-3′。 所有引物均来自Integrated DNA Technologies(IA Coralville)。 使用iCycler-iQ实时PCR检测系统(Bio-Rad)和SYBR绿色qPCR SuperMixes试剂盒(Invitrogen)进行实时PCR。 热循环程序为40次95°C循环15 s,55°C循环45 s,初始循环95°C 10 min。通过监测SYBR绿色荧光随温度升高(0.5°C增量,间隔10 s),在55–95°C范围内进行熔化曲线分析。 PCR-特定产物在熔融曲线>80°C时被确定为一个清晰的单峰。 对每个cDNA样本进行实时PCR。 通过公式2ΔCt(ΔCt=GAPDH Ct−感兴趣基因Ct;参考文献。 19 ).
数据分析。 数据为平均值±标准偏差。统计比较采用方差分析,然后进行纽曼-凯尔斯事后检验。 重要性设置为 P(P) < 0.05.
结果 低脂肪和高脂肪喂养小鼠的一般特征、超声心动图特征和细胞凋亡。 随意喂食高脂肪食物显著增加了体重以及心脏、肝脏和肾脏器官的重量。 限食高脂肪饮食喂养(体重控制)不会影响身体和器官重量。 三组患者的空腹血糖水平、血压(舒张压和收缩压)、心率、壁厚、左心室EDD和标准化左心室质量具有可比性。 高脂肪饮食诱导的肥胖伴随着血清胰岛素和瘦素水平、左心室重量、ESD和缩短分数的显著增加。 虽然体重控制组的血浆胰岛素和瘦素水平中度升高,但限制摄入高脂肪饮食显著减轻了与高脂肪饮食诱导的肥胖相关的高胰岛素血症、高瘦素血症和心肌畸变( 表1 ). 通过caspase-3和caspase-3/7活性测定评估,高脂肪饮食自由进食引发心肌细胞凋亡升高,而高脂肪饮食限制缓解了这一现象( 图1 ).
表1。 喂食低脂肪或高脂肪食物6个月的小鼠的生物特征和超声心动图参数
参数 低脂肪饮食( n个= 19) 高脂肪饮食自由( n个= 20) 称重匹配控制( n个= 13)
体重,g 25.86±0.66 32.58±0.84 * 26.85±0.57 †
心脏重量,mg 121±7 150±7 * 132±6 †
肝脏重量,g 1.37±0.08 1.64±0.08 * 1.40±0.05 †
肾重,g 0.32±0.02 0.43±0.03 * 0.34±0.02 †
空腹血糖,mM 5.17±0.31 5.98±0.31 5.69±0.36
空腹血清胰岛素,ng/ml 0.17±0.02 7.32±0.35 * 0.57±0.09 * †
空腹血清瘦素,ng/ml 3.39±0.38 8.36±1.29 * 4.65±0.41 * †
舒张压,mmHg 74.0±4.1 80.5±4.2 76.6±3.1
收缩压,mmHg 104±6 113±5 111±6
稳定心率,心跳/分钟 413±9 422±15 419±19
壁厚,mm 0.83±0.04 0.89±0.04 0.89±0.05
EDD,毫米 2.70±0.09 2.80±0.15 2.75±0.14
静电放电,毫米 1.39±0.11 1.83±0.14 * 1.48±0.08 †
LV质量,mg 66.9±6.2 87.4±7.5 * 68.4±6.8 †
标准化左心室质量,mg/g 2.38±0.18 2.71±0.20 2.47±0.24
缩短分数,% 49.1±3.0 37.4±1.9 * 49.5±3.9 †
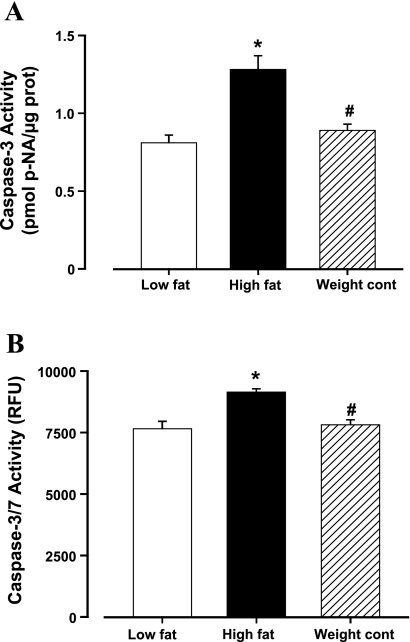
图1。
脂肪饮食对低脂、高脂和高脂饮食限制(体重控制)组小鼠左心室细胞凋亡的影响。 A类 :caspase-3活性。 B :辣椒素-3/7活性。 数据为平均值±SE; n个 =每组5-6只小鼠* P(P) <0.05 vs.低脂组# P(P) 与高脂肪组相比,<0.05。 RFU,相对荧光单位。
心肌细胞收缩和细胞内钙 2+ 属性。 高脂肪饮食诱导的肥胖伴心肌细胞横截面积显著增加,±dL/d降低 t吨 以及延长TPS和TR 90 正常PS( 图2 )有点让人想起我们早期的发现( 33 ). 此外,来自高脂肪喂养的肥胖小鼠的心肌细胞显示出显著升高的基线细胞内Ca 2+ ,降低细胞内钙 2+ 对电刺激的反应增加(ΔFFI),细胞内钙减少 2+ 衰减率(单指数或双指数曲线拟合; 图3 ). 这些心肌细胞机械和细胞内钙 2+ 通过体重控制策略,与高脂肪饮食诱导的肥胖相关的缺陷显著减轻。 尽管如此,高脂肪饮食的食物限制略微但显著延长了TR 90 和双指数细胞内钙 2+ 在不影响任何其他指标的情况下衰减( 图2 F类 和 三 D类 ).
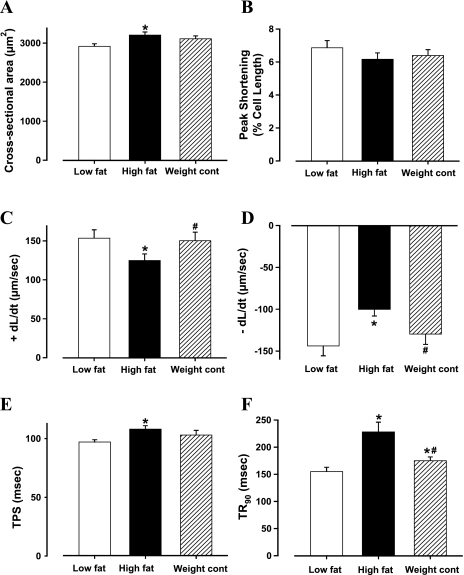
图2。
低脂、高脂和高脂饮食限制(体重控制)组心肌细胞的收缩特性。 A类 :横截面积。 B :峰值缩短(归一化为单元长度); C :最大缩短速度(+dL/d t吨 ). D类 :最大松弛速度(−dL/d t吨 ). E类 :时间-峰值缩短(TPS)。 F类 :时间到90%再增强(TR 90 ). 数据为平均值±SE; n个 =每组6只小鼠的75个细胞* P(P) <0.05 vs.低脂组# P(P) 与高脂肪组相比,<0.05。
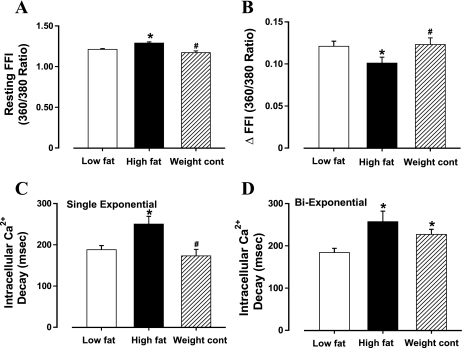
图3。
细胞内钙 2+ 低脂、高脂和高脂饮食限制(体重控制)组心肌细胞的瞬时变化。 A类 :静止呋喃2荧光强度(FFI)。 B :电刺激FFI上升(ΔFFI)。 C :单指数细胞内钙 2+ 衰变。 D类 :双指数细胞内钙 2+ 衰变。 数据为平均值±SE; n个 =每组6只小鼠的60个细胞* P(P) 与低脂组相比<0.05# P(P) 与高脂肪组相比,<0.05。
Akt、pAkt,Foxo3a、pFoxo3a、肥厚因子、MuRF-1和atoggin-1的表达。 免疫印迹数据显示,高脂肪饮食诱导的肥胖显著增强了Akt和Foxo3a的基础磷酸化(显示为绝对磷酸化或标准化磷酸化),而不影响Akt与Foxo3的总蛋白表达。 此外,高脂肪饮食相关肥胖消除了胰岛素刺激的Akt和Foxo3a磷酸化增加(显示为绝对或标准化磷酸化)。 胰岛素暴露不会影响非磷酸化Akt和Foxo3a的水平( 图4 ). 我们的数据进一步表明,高脂肪饮食诱导的肥胖显著降低了包括MuRF-1和atrogin-1在内的多种营养素的转录表达。 这两种营养素的mRNA表达也表现出类似的下降,约为50%。 此外,在高脂饮食喂养6个月后,小鼠心脏中肥大GATA4和CNTFR-α的标记物显著上调。 然而,6个月的高脂肪饮食喂养对心肌钙调神经磷酸酶A和泛素水平没有影响( 图5 ).
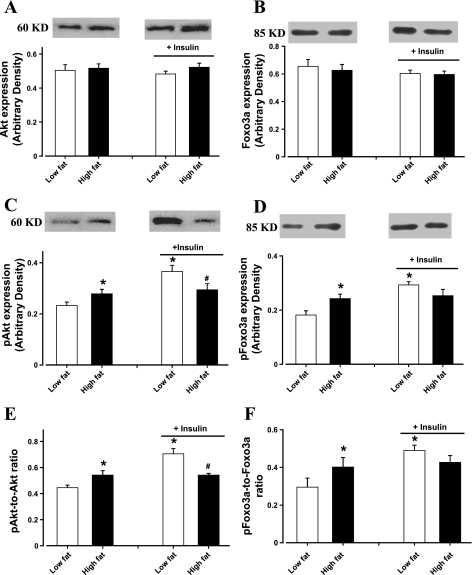
图4。
在缺乏或存在胰岛素刺激(1.5 U/100 g体重,持续10分钟)的情况下,对低脂和高脂喂养小鼠心肌细胞中的Akt和Foxo3a的总量和磷酸化进行Western blot分析。 A类 :总阿克特。 B :总Foxo3a。 C :磷酸化Akt(pAkt)。 D类 :磷酸化Foxo3a(pFoxo3a)。 E类 :pAkt-Akt比率。 F类 :pFoxo3a-Foxo3比值。 插图 :使用特定抗体的Akt、pAkt和pFoxo3a的代表性凝胶。 数据为平均值±SE; n个 =每组5-8人* P(P) <0.05 vs.低脂组# P(P) 与胰岛素刺激低脂组相比,<0.05。
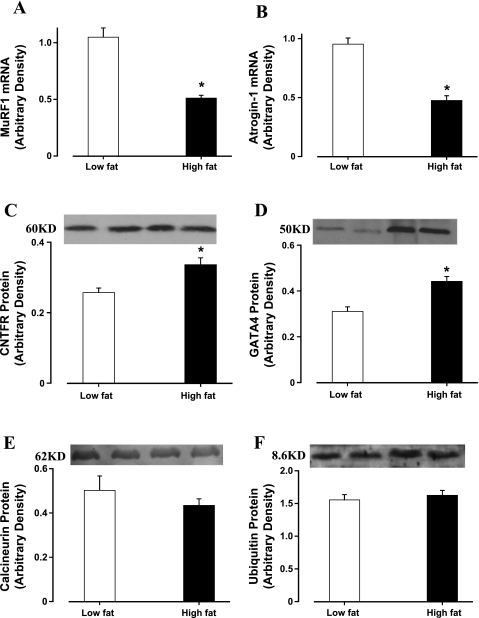
图5。
A类 和 B :RT-PCR测量阿奇金-1( A类 )和肌肉专用无名指(MuRF)( B )在低脂和高脂喂养小鼠的左心室中。 C 和 D类 肥大蛋白睫状神经营养因子受体(CNTFR)-α的Western blot分析( C )和GATA4( D类 )在低脂和高脂喂养小鼠的左心室中。 E类 和 F类 肥大蛋白钙调神经磷酸酶A的Western blot分析( E类 )和泛素( F类 )在低脂和高脂喂养小鼠的左心室中。 数据为平均值±SE; n个 = 4–8. * P(P) 与低脂组相比,<0.05。
DN foxo3a腺病毒对棕榈酸诱导的Akt、PTEN和GATA4反应的影响。 为了研究高脂肪饮食诱导的Akt-Foxo3a变化与心肌肥厚之间的因果关系,在细胞暴露于棕榈酸(0.8 mM)24 h之前,进行体外腺病毒转染研究,将DN Foxo3a病毒转染到H9C2成肌细胞中6 h。 我们的免疫印迹分析显示,棕榈酸显著上调了包括PTEN和GATA4在内的肥大标记物,而Akt和pAkt没有明显变化。 有趣的是,DN Foxo3a腺病毒模拟了棕榈酸诱导的GATA4上调,而没有引起棕榈酸的任何加性效应。 DN Foxo3a本身可诱导pAkt上调和PTEN抑制,棕榈酸可消除其作用( 图6 ). 这些数据表明,DN Foxo3a可能分别触发Akt磷酸化和心脏肥厚标志物表达,使人联想到高脂饮食和棕榈酸。
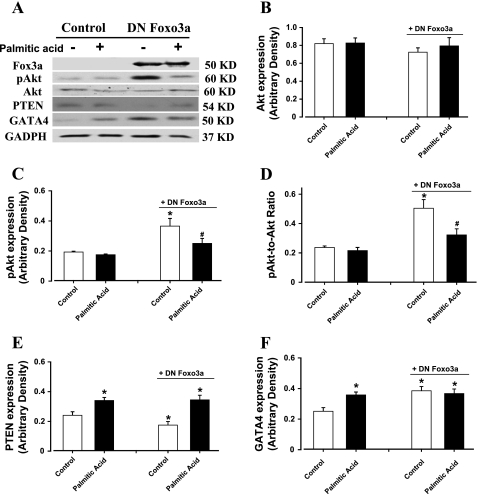
图6。
用0.8 mM棕榈酸处理24 h的H9C2成肌细胞中的Akt、磷酸酶和张力蛋白同源物(PTEN)和GATA4的总蛋白和磷酸化蛋白的Western blot分析。在棕榈酸暴露前,将显性阴性(DN)Foxo3a病毒(1:1000)转染6 h的细胞群。 A类 :使用特定抗体的典型凝胶斑点。 B :总阿克特。 C :磷酸化Akt(pAkt)。 D类 :pAkt-Akt比率。 E类 :私人。 F类 :GATA4。 数据为平均值±SE; n个 =每组6-8人* P(P) 与对照组相比<0.05# P(P) 与DN Foxo3a/对照组相比,<0.05。
讨论 我们研究的主要结果表明,高脂肪饮食相关肥胖会导致心肌肥厚、心肌收缩功能障碍和细胞内钙的受损 2+ 对小鼠的处理,其效果可通过限制高脂肪饮食喂养的食物来调节。 在高脂饮食诱导的肥胖患者中,心肌几何和功能异常与心肌细胞凋亡、Akt和Foxo3a的基础磷酸化升高、Att和FoxoS3a的磷酸化受胰岛素刺激的增加受到抑制以及包括atrogin-1和MuRF-1在内的atrogene表达降低有关, 以及上调肥大标记物GATA4和CNTFR-α。 在我们目前的实验环境中,6个月高脂饮食喂养后,钙调神经磷酸酶和泛素的水平没有受到影响。 这些数据表明,在与高脂肪饮食诱导的肥胖相关的心肌肥厚中,基础Akt-Foxo3a驱动力升高和atrogene转录表达抑制起着主导作用。 我们使用DN Foxo3a病毒进行的体外研究表明,棕榈酸(高脂饮食中的一种主要游离脂肪酸成分)上调了H9C2成肌细胞中的肥大蛋白表达,这让人想起突变的Foxo3a腺病毒。 总之,我们的数据表明,高脂肪饮食相关的肥胖而非高脂肪饮食本身可能对心脏重塑和心脏功能障碍的发展至关重要。
高脂肪饮食摄入会引发血脂异常、胰岛素抵抗、肥胖和2型糖尿病( 三 , 44 ). 我们目前的研究结果表明,尽管体重得到控制,但血浆胰岛素和瘦素水平仍在升高,这一点得到了支持。 虽然生活方式的改变和药物干预已显示出对肥胖患者肥大和功能失调心脏的一些希望( 26 , 43 ),目前还没有发现从根本上调和肥胖患者心脏几何和功能缺陷的唯一靶点。 我们的心肌肥大和心肌及心肌细胞收缩功能受损的数据(缩短分数减少,ESD增大,±dL/d降低 t吨 随意摄入高脂肪饮食后,长时间的收缩和放松)与之前的临床和实验观察结果一致( 4 , 6 , 8 , 29 , 33 , 43 ). 在6个月的随意高脂肪饮食喂养后,存在明显的心脏收缩功能障碍,这有助于认为心脏肥大已促使不同的病理状况从肥胖的代偿期进展到失代偿期。 6个月的高脂肪喂养方案(不考虑饮食限制)几乎没有引起血压和血糖的变化,排除了可能伴随的高血压和全面糖尿病。 受损的细胞内钙 2+ 处理显示为静息细胞内钙升高 2+ 细胞内钙降低 2+ 清除率,降低细胞内钙 2+ 高脂肪饮食肥胖小鼠心肌细胞的升高(ΔFFI)与高脂肪诱导肥胖大鼠模型的数据一致( 33 )并可能导致长时间松弛,减少±dL/d t吨 以及高脂肪饮食小鼠心脏的分数缩短。 事实上,体重控制减轻了高脂肪饮食诱导的心脏重塑和收缩功能障碍,这表明肥胖在高脂肪饮食导致的心脏异常中起着关键作用。 肥胖的存在以及脂肪摄入的持续时间似乎可以解释我们的研究与斯坦利小组的研究之间的差异( 4 , 29 )关于高脂饮食诱导的心脏重塑和收缩反应。 值得一提的是,我们的数据显示,松弛时间延长,细胞内钙 2+ 体重控制的高脂肪饮食组的清除率,表明存在与体重增加无关的高脂肪引起的心肌效应的可能性。
心脏肥大发生在正常生理生长过程中,是对压力或体积压力、心脏蛋白突变或代谢紊乱的适应性反应( 40 ). 这种适应性反应可能会变得不适应,并导致心脏功能障碍( 13 ). 在我们目前的研究中,高脂肪饮食诱导的肥胖促进了Akt和Foxo3a的基础磷酸化,而没有改变Akt与Foxo3a的表达。 胰岛素刺激的Akt和Foxo3a磷酸化减弱,支持胰岛素敏感性降低。 这些数据支持Akt及其下游信号Foxo3a在高脂饮食诱导肥胖患者心脏肥大中的作用。 随意高脂饮食喂养后Akt和Foxo3a的基础磷酸化增加可促进心肌肥大并抑制涉及atrogin-1和MuRF-1的萎缩特异性基因转录,而Foxo3的胰岛素刺激磷酸化减少有利于细胞凋亡。 摄入高脂肪饮食后心肌细胞中caspase活性升高支持了这一点。 Akt信号是心脏生长的重要调节器,其过度表达导致收缩力增强、细胞存活和病理性心脏肥大( 5 , 38 ). 我们观察到基础Foxo3a磷酸化增强和萎缩特异性基因抑制抑制抑制与高脂肪摄入诱导的肥胖下的心肌肥大一致。
我们研究的一个相当有趣的发现表明,DN Foxo3a病毒在高脂肪饮食相关肥胖中模拟增加基础Akt磷酸化和肥大蛋白GATA4。 在高脂饮食诱导的肥胖中,GATA4的上调与萎缩特异性基因转录的下调同步,从而促进心肌肥厚和可能的肥厚性心肌病。 棕榈酸直接促进H9C2成肌细胞中GATA4的表达,这一发现进一步证实了这一观点。 棕榈酸是脂肪组织释放的主要饱和游离脂肪酸,在肥胖患者中棕榈酸水平升高,并导致肥胖相关的心血管并发症( 51 ). 虽然转录辅激活因子PGC-1α(过氧化物酶体增殖物激活受体γ辅激活因子)和Foxo转录因子之间的相互作用可能起作用,但在高脂肪饮食诱导的肥胖中,负责抑制萎缩基因转录的细胞机制尚未完全了解( 36 ). 有必要进行进一步的研究,以检查摄入高脂肪饮食后,无论是否发生肥胖,萎缩基因转录的调节。
我们的体外数据还表明,由于突变型Foxo3a的转染刺激了Akt磷酸化,因此Akt与其下游信号分子Foxo3之间可能存在前馈机制。 萎缩基因atrogin-1通过叉头蛋白的泛素依赖性协同激活抑制Akt依赖性心肌肥大的概念支持了这种前馈假设( 22 ). 尽管如此,我们目前的研究未能检测到泛素表达对高脂饮食诱导肥胖的反应,不支持泛素相关蛋白降解在与高脂饮食导致肥胖相关的心脏肥大和心脏功能障碍中的作用。 泛素蛋白酶体是一种桶状蛋白酶,能够识别和破坏至少有四个泛素残基修饰的蛋白质( 31 ). 同样,我们的数据也表明钙调神经磷酸酶在高脂饮食诱导肥胖的心脏肥大和收缩功能障碍中不太可能发挥作用。
Atrogin-1是一种F-box蛋白,通过参与Akt和泛素连接酶依赖途径抑制心肌肥厚。 因此,肥大启动子钙调神经磷酸酶可能被降解。 有人认为,阿托品素-1本身并不影响Akt活性,而是作为Akt下游叉头转录因子成员的辅激活剂( 22 ). 心脏过度表达阿特拉津-1的小鼠表现出上调的叉头转录因子,同时抑制心肌肥厚,而缺乏阿特拉津1的小鼠表现为相反的生理表型,这表明阿特拉津-1可能通过其对叉头转录因素的影响而破坏心肌肥厚( 22 ). 我们的实验数据支持这一观点,即抑制了atrogin-1 mRNA的表达,提高了Foxo3a的基础磷酸化(活性转录因子的表达减少),尽管这一过程可能独立于泛素蛋白酶体系统和钙调神经磷酸酶。
在我们的研究中,尽管GATA4对棕榈酸和高脂肪饮食喂养的反应具有可比性,但棕榈酸未能概括高脂肪饮食诱导的肥胖对Akt激活的影响。 这种明显的差异可能归因于高脂肪饮食中其他长链脂肪酸的可能贡献以及治疗时间的差异。 我们对棕榈酸引起的PTEN水平升高的观察表明,在缺乏高基础Akt磷酸化的情况下,PTEN可能对棕榈酸致肥大反应有贡献。 众所周知,PTEN信号与心肌肥厚呈正相关,因此是延缓心力衰竭进展的新靶点( 30 ). 此外,已知PTEN对Akt活性有负调节作用,但尚不清楚PTEN是否导致棕榈酸处理后pAkt缺乏反应性( 17 ). CNTF对组织生长和代谢至关重要( 42 ). 通常,CNTFR和心肌肥厚之间存在相互关系( 42 ). 我们发现在心肌肥大的情况下CNTFR-α增强可能代表肥胖相关器官肥大的代偿反应。 最后但并非最不重要的一点是,我们的数据还显示心脏肥大信号分子瘦素升高( 18 )为了应对高脂肪饮食喂养,控制体重可能会减轻这种影响。 这些观察结果表明,显性高瘦素血症在高脂饮食诱导肥胖的心脏肥大和心脏功能障碍中具有潜在作用。
实验限制 在这种规模的研究中,存在许多局限性。 最重要的是,我们研究中使用的饮食中糖分也相对较高; 因此,高脂肪饮食诱导的效果可能是由于脂肪和糖的过剩。 此外,最近的证据( 45 )虽然我们两种饮食中的豆油成分相同,但大豆饮食会加重心脏功能障碍。 其次,我们使用分离的心肌细胞评估心脏收缩和舒张功能,以尽量减少神经体液因素和结缔组织的潜在影响,这两者都可能影响心脏性能的固有改变。 然而,在类似的细胞外环境中记录到心肌细胞的收缩功能,因此不考虑体内脂肪酸循环水平的可能差异。 第三,在我们的体外DN Foxo3a转染研究中,使用了相对较高浓度的棕榈酸,而不是油酸,油酸是猪油的主要成分(负责饮食中的高脂肪成分)。 我们的初步证据没有显示油酸对Akt磷酸化和GATA4表达有任何显著反应(数据未显示)。 油酸和棕榈酸作用之间的这种明显差异表明,脂肪酸的精确组成可能直接影响心肌细胞的表型以及这些细胞对肥大刺激的反应。 虽然由于细胞毒性原因,我们的转染研究不允许更长的暴露时间,但脂肪酸暴露时间可能在肥大信号的发生中起作用。 最后,我们的心肌细胞功能和Akt/Foxo3a磷酸化状态之间的数据基本上是相关的。 使用针对Akt和Foxo3a的生物工程技术(例如使用转基因小鼠)直接评估心肌细胞收缩功能,应能为Akt/Foxo3a磷酸化在心肌细胞功能中的作用提供更直接的证据。
总之,我们的研究提供了几何、心肌收缩和细胞内钙 2+ 高脂饮食诱导肥胖的异常可能与叉头转录因子抑制(Foxo3a磷酸化基础升高)和萎缩特异性基因转录有关。 鉴于DN Foxo3a腺病毒对Akt磷酸化和肥大蛋白上调的影响,使人想起高脂饮食或棕榈酸,我们的数据支持高脂饮食诱导肥胖(可能是胰岛素抵抗和2型糖尿病)的新假设 通过Akt的慢性激活抑制叉头转录因子。 慢性Akt激活能够覆盖Foxo诱导的抗生长程序。 同样,其他肥大激动剂,如血管紧张素II,可能通过磷脂酰肌醇3-激酶/Akt依赖机制触发心肌细胞中Foxo蛋白的失活。 必须仔细研究Akt-forkhead转录因子在肥胖和糖尿病诱导的心肌肥厚和肥厚性心肌病中的作用,以便针对该信号级联实现最佳治疗策略。
赠款 这项工作得到了美国心脏协会太平洋山区协会(#0355521Z)和怀俄明州北落基山脉国立卫生大学区域机构发展奖生物医学研究卓越网络(#5P20RR016474)的部分支持。
致谢 我们感谢Ji Li博士的慷慨支持,以及Qun Li博士和Nair Sreejayan博士对Foxo3a转染研究的协助。
这篇文章的出版费用部分由页面费支付。 因此,物品必须在此标记“ 广告 “根据《美国法典》第18卷第1734节,仅为了表明这一事实。
参考文献
1 Abel ED、Litwin SE、Sweeney G.肥胖患者的心脏重塑。 生理学评论 88: 389–419, 2008. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
2 Alnemri ES、Livingston DJ、Nicholson DW、Salvesen G、Thornberry NA、Wong WW、Yuan J.人类ICE/CED-3蛋白酶命名法。 单元格 87: 171, 1996. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
三。 Axen KV,Dikeakos A,Sclafani A。非肥胖大鼠高膳食脂肪可促进X综合征。 营养学杂志 133: 2244–2249, 2003. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
4 国际象棋DJ、Lei B、Hoit BD、Azimzadeh AM、Stanley WC。 高饱和脂肪饮食对压力过载引起的心肌肥大和功能障碍的影响。 J卡故障 14: 82–88, 2008. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
5 Condorelli G、Drusco A、Stassi G、Bellacosa A、Roncarati R、Iacarino G、Russo MA、Gu Y、Dalton N、Chung C、Latronico MV、Napoli C、Sadoshima J、Croce CM、Ross J Jr.Akt在转基因小鼠体内诱导增强心肌收缩力和细胞大小。 《美国科学院院刊》 99: 12333–12338, 2002. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
6 de Divitis O、Fazio S、Petitto M、Maddalena G、Contaldo F、Mancini M。肥胖和心脏功能。 循环 64: 477–482, 1981. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
7 Dimopoulos N、Watson M、Sakamoto K、Hundal HS。 棕榈酸和棕榈酸对大鼠L6骨骼肌细胞胰岛素作用和葡萄糖利用的差异影响。 生物化学杂志 399: 473–481, 2006. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
8 Dobrian AD、Davies MJ、Schriver SD、Lauterio TJ、Prewitt RL。肥胖诱导高血压大鼠模型中的氧化应激。 高血压 37: 554–560, 2001. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
9 Dong F,Li Q,Sreejayan N,Nunn JM,Ren J.金属硫蛋白预防高脂饮食诱导的心脏收缩功能障碍:过氧化物酶体增殖物激活受体γ辅活化剂1alpha的作用和线粒体生物生成。 糖尿病 56: 2201–2212, 2007. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
10 Dong F,Ren J.Fidarestat通过组蛋白去乙酰化酶Sir2依赖机制改善db/db糖尿病肥胖小鼠的心肌细胞收缩功能。 J高血压 25: 2138–2147, 2007. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
11 Eckel RH,Barouch WW,Ershow AG.国家心脏、肺和血液研究所-国家糖尿病、消化和肾脏疾病研究所肥胖相关心血管疾病病理生理学工作组的报告。 循环 105: 2923–2928, 2002. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
12 Fang CX,Dong F,Ren BH,Epstein PN,Ren J.金属硫蛋白减轻胰岛素抵抗诱导的心脏收缩功能障碍:Akt磷酸化、PTB1B、PPARgamma和c-Jun的作用糖尿病 48: 2412–2421, 2005. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
13 菲德勒B,沃勒特KC。 心肌肥大和衰竭中钙调神经磷酸酶及其相关通路的靶向性。 专家操作目标 9: 963–973, 2005. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
14 Gardin JM、Siri FM、Kitsis RN、Edwards JG、Leinwand LA。小鼠左心室重量和收缩功能的超声心动图评估。 循环研究 76: 907–914, 1995. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
15 Hannigan GE、Coles JG、Dedhar S.整合素连接激酶在心脏收缩力、修复和疾病的心脏中的作用。 循环研究 100: 1408–1414, 2007. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
16 Hardt SE,Sadoshima J.糖原合成酶激酶-3beta:心脏肥大和发育的新调节器。 循环研究 90:1055–10632002年。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
17 Hay N Akt-mTOR探戈及其与癌症的相关性。 癌细胞 8: 179–183, 2005. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
18 Karmazyn M、Purdham DM、Rajapurohitam V、Zeidan A.瘦素作为心脏肥大因子:潜在治疗靶点。 心血管医学趋势 17:206–2112007年。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
19 Kinkel MD,Horton WE Jr.协调Bcl-2缺陷软骨细胞软骨基质基因表达的下调与SOX9表达降低和mRNA稳定性降低相关。 J细胞生物化学 88: 941–953, 2003. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
20 Lam EW、Francis RE、Petkovic M.FOXO转录因子:细胞命运的关键调节器。 生物化学Soc Trans 34: 722–726, 2006. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
21 Levy D、Garrison RJ、Savage DD、Kannel WB、Castelli WP。 Framingham心脏研究中超声心动图测定的左心室重量对预后的影响。 N英格兰J医学 322: 1561–1566, 1990. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
22 Li HH、Willis MS、Lockyer P、Miller N、McDonough H、Glass DJ、Patterson C.Atrogin-1通过叉头蛋白的泛素依赖性协同激活抑制小鼠Akt依赖性心肌肥大。 临床研究杂志 117: 3211–3223, 2007. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
23 Li SY,Gomelsky M,Duan J,Zhang Z,Gomessky L,ZhangX,Epstein PN,Ren J.醛脱氢酶-2(ALDH2)转基因的过度表达可防止人脐静脉内皮细胞中乙醛诱导的细胞损伤:ERK和p38有丝分裂原活化蛋白激酶的作用。 生物化学杂志 279: 11244–11252, 2004. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
24 Li SY,Yang X,Ceylan Isik AF,Du M,Sreejayan N,Ren J。Lep/Lep肥胖患者的心脏收缩功能障碍伴随NADPH氧化酶激活,肌(内质网)Ca的氧化修饰 2+ -ATP酶和肌球蛋白重链同工酶开关。 糖尿病学 49: 1434–1446, 2006. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
25 Liang Q,Molkentin法学博士。 不同的信号通路汇聚在GATA4上以调节心肌肥厚基因的表达。 J Mol Cell心脏病学 34: 611–616, 2002. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
26 Matthaei S、Stumvoll M、Keller M、Haring HU。胰岛素抵抗的病理生理学和药物治疗。 Endocr版本 21: 585–618, 2000. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
27 Meiners S、Dreger H、Fechner M、Bieler S、Rother W、Gunther C、Baumann G、Stangl V和Stangl K。通过抑制泛素蛋白酶系统抑制心肌细胞肥大。 高血压 51: 302–308, 2008. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
28 Morgan EE、Rennison JH、Young ME、McElfresh TA、Kung TA、Tserng KY、Hoit BD、Stanley WC、Chandler MP。过氧化物酶体增殖物激活受体-α慢性激活或高脂喂养对心衰大鼠梗死模型的影响。 美国生理学杂志心脏循环生理学 290:H1899–H19042006年。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
29 Okere IC、Young ME、McElfresh TA、Chess DJ、Sharov VG、Sabbah HN、Hoit BD、Ernsberger P、Chandler MP、Stanley WC。 低碳水化合物/高脂肪饮食可减轻高血压患者的心肌肥厚、重塑和基因表达改变。 高血压 48: 1116–1123, 2006. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
30 Oudit GY、Kassiri Z、Zhou J、Liu QC、Liu PP、Backx PH、Dawood F、Crackower MA、Scholey JW、Penninger JM。PTEN的缺失可减缓病理性肥大和心力衰竭的发展,以应对生物力学应力。 心血管研究 78: 505–514, 2008. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
31 Patterson C,Ike C,Willis PW,Stouffer GA,Willis MS。苦涩的结局:泛素蛋白酶体系统和心脏功能障碍。 循环 115: 1456–1463, 2007. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
32 Pham FH,Cole SM,Clerk A.通过磷脂酰肌醇3′激酶和蛋白激酶B调节心肌细胞蛋白质合成。高级酶调节 41: 73–86, 2001. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
33 Relling DP、Esberg LB、Fang CX、Johnson WT、Murphy EJ、Carlson EC、Saari JT、Ren J.高脂肪饮食诱导的青少年肥胖导致心肌细胞功能障碍和Foxo3a转录因子上调,与脂毒性和凋亡无关。 J高血压 24: 549–561, 2006. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
34 Rennison JH、McElfresh TA、Okere IC、Vazquez EJ、Patel HV、Foster AB、Patol KK、Chen Q、Hoit BD、Tserng KY、Hassan MO、Hoppel CL、Chandler MP。梗死后高脂肪饮食可增强线粒体功能,不会加重左心室功能障碍。 美国生理学杂志心脏循环生理学 292:H1498–H15062007年。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
35 Sacheck JM、Ohtsuka A、McLary SC、Goldberg AL。IGF-I通过抑制蛋白质分解和萎缩相关泛素连接酶、atogin-1和MuRF-1的表达来刺激肌肉生长。 美国生理内分泌代谢杂志 287:E591–e6012004年。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
36 Sandri M,Lin J,Handschin C,Yang W,Arany ZP,Lecker SH,Goldberg AL,Spiegelman BM。PGC-1alpha通过抑制FoxO3作用和萎缩特异性基因转录,保护骨骼肌免受萎缩。 《美国科学院院刊》 103: 16260–16265, 2006. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
37 Sandri M、Sandri C、Gilbert A、Skurk C、Calabria E、Picard A、Walsh K、Schiaffino S、Lecker SH、Goldberg AL。Foxo转录因子诱导萎缩相关的泛素连接酶atogin-1并导致骨骼肌萎缩。 单元格 117:399–412004年。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
38 Shioi T、McMullen JR、Kang PM、Douglas PS、Obata T、Franke TF、Cantley LC、Izumo S.Akt/蛋白激酶B促进转基因小鼠的器官生长。 分子细胞生物学 22: 2799–2809, 2002. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
39 Shiojima I、Yefremashvili M、Luo Z、Kureishi Y、Takahashi A、Tao J、Rosenzweig A、Kahn CR、Abel ED、Walsh K.Akt信号调节出生后心脏生长,以响应胰岛素和营养状况。 生物化学杂志 277: 37670–37677, 2002. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
40 Skurk C、Izumiya Y、Maatz H、Razeghi P、Shiojima I、Sandri M、Sato K、Zeng L、Schiekofer S、Pimentel D、Lecker S、Taegtmeyer H、Goldberg AL、Walsh K。FOXO3a转录因子调节AKT信号下游的心肌细胞大小。 生物化学杂志 280: 20814–20823, 2005. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
41 Skurk C、Maatz H、Kim HS、Yang J、Abid MR、Aird WC、Walsh K。Akt调节的叉头转录因子FOXO3a通过调节caspase-8抑制剂FLIP来控制内皮细胞活性。 生物化学杂志 279: 1513–1525, 2004. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
42 Sleeman MW、Garcia K、Liu R、Murray JD、Malinova L、Moncrieffe M、Yancopoulos GD、Wiegand SJ。睫状神经营养因子可改善糖尿病参数和肝脏脂肪变性,并提高db/db小鼠的基础代谢率。 《美国科学院院刊》 100: 14297–14302, 2003. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
43 将JR肥胖视为心血管危险因素。 美国医学杂志 115 供应商 8A:37S–41S,2003年。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
44 Sparks LM,Xie H,Koza RA,Mynatt R,Hulver MW,Bray GA,Smith SR.高脂饮食协调下调骨骼肌线粒体氧化磷酸化所需的基因。 糖尿病 54: 1926–1933, 2005. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
45 Stauffer BL、Konhilas JP、Luczak ED、Leinwand LA。大豆饮食会加重小鼠的心脏病。 临床研究杂志 116: 209–216, 2006. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
46 Stitt TN、Drujan D、Clarke BA、Panaro F、Timofeyva Y、Kline WO、Gonzalez M、Yancopoulos GD、Glass DJ。IGF-1/PI3K/Akt途径通过抑制FOXO转录因子防止肌肉萎缩诱导的泛素连接酶的表达。 分子电池 14: 395–403, 2004. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
47 Sun H、Kerfant BG、Zhao D、Trivieri MG、Oudit GY、Penninger JM、Backx PH。胰岛素样生长因子-1和PTEN缺失通过增加PI3Kalpha/PKB信号增强心脏L型Ca2+电流。 循环研究 98: 1390–1397, 2006. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
48 Thomas G,Hall MN。TOR信号与细胞生长控制。 Curr Opin细胞生物学 9: 782–787, 1997. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
49 van HM、Compton DS、France CF、Tedesco RP、Fawzi AB、Graziano MP、Sybertz EJ、Strader CD、Davis HR Jr.饮食诱导肥胖小鼠对瘦素产生外周而非中枢抵抗。 临床研究杂志 99:385-3901997年。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
50 Wilson CR、Tran MK、Salazar KL、Young ME、Taegtmeyer H。西方饮食,但不是高脂肪饮食,会导致Wistar大鼠脂肪酸代谢紊乱和心脏收缩功能障碍。 生物化学杂志 406: 457–467, 2007. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
51 Wilson-Fritch L、Nicoloro S、Chouinard M、Lazar MA、Chui PC、Leszyk J、Straubhaar J、捷克议员、Corvera S.肥胖相关脂肪组织线粒体重塑和罗格列酮治疗。 临床研究杂志 114: 1281–1289, 2004. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]