摘要 在非极化上皮细胞中,微管起源于与高尔基复合体分布一致的宽阔核周区域,并向外延伸至细胞外围(核周[PN]组织)。 在上皮细胞极性的发育过程中,微管重组形成平行于侧膜的长皮层丝,顶端膜下由随机取向的短丝和细胞底部的短丝组成的网状结构; 高尔基体位于顶端下膜细胞质的细胞核上方(顶端核[AN]组织)。 微管的AN型组织被认为专一于极化上皮细胞,以促进反高尔基网络(TGN)和质膜之间的囊泡运输。 我们描述了两个具有不同微管分布的MDCK细胞克隆:克隆II/G细胞,在极性发育过程中逐渐将微管和高尔基复合体的PN型分布重组为an型;克隆II/J细胞,维持PN型组织。 然而,这两个细胞克隆表现出相同的顶端和基底外侧蛋白的稳态极性。 在细胞表面极性发育过程中,这两个克隆分别快速建立新合成的gp80和gp135/170以及TGN与顶膜和基底膜之间的E-cadherin的直接靶向通路; 这发生在克隆II/G细胞中AN型微管/高尔基体组织发育之前。 将克隆II/G和II/J细胞暴露于低温和诺克唑破坏了>99%的微管,导致:1)在克隆Ⅱ/G和Ⅱ/J细胞中,新合成的gp135/170和E-cadherin分别向顶膜和基底外侧膜的传递减少25-50%, 但在极性发展的所有阶段,很少或没有错配到相反的膜结构域; 2) 在新建立的克隆II/G和II/J细胞培养物中,新合成的gp80向顶膜的递送减少约40%,向基底外侧膜的递送显著错位; 3)在全极化培养基中,新合成的gp80向两个膜域的可变和非特异性递送。 这些结果定义了几种不同类型的蛋白质,它们对完整微管的依赖性不同,以便在高尔基体和质膜域之间进行有效和特异的靶向。
简介 成纤维细胞和极化上皮细胞膜蛋白的细胞表面分布有明显差异。 一般来说,成纤维细胞中的膜蛋白是随机分布的,除了局限于细胞-细胞外基质界面的特殊细胞粘附复合物。 在极化上皮细胞中,蛋白质局限于离散的膜域,称为顶端和基底外侧。 成纤维细胞和上皮细胞中蛋白质分布的差异分别与特定的细胞功能有关,包括细胞迁移、载体离子和溶质运输。
试图阐明在极化上皮细胞中建立和维持膜蛋白在细胞表面分布的机制,揭示了这些过程的复杂性。 早期对简单上皮细胞的研究表明,顶端和基底外侧膜蛋白在跨高尔基网络(TGN)中被分为不同的运输囊泡,然后被输送到适当的膜域( Rodriguez-Boulan和Nelson,1989年 ; Wandinger-Ness公司 等。 , 1990 ). 因此,有人提出TGN中的蛋白质分选是建立和维持上皮细胞表面极性的基础。 随后,TGN中基底外侧膜蛋白的分选信号被鉴定出来,尽管对顶端蛋白分选信号知之甚少( Matter和Mellman,1994年 ). 然而,最近, 麝香 等。 (1996) 和 吉森 等。 (1996) 发现上皮顶膜和基底外侧膜的标记蛋白在成纤维细胞的TGN中被分为不同的小泡,尽管这些蛋白在传递到质膜后变得随机分布。 这些结果表明TGN中顶端和基底外侧膜蛋白的分选对极化上皮细胞没有特异性, 必须要求其他细胞过程来建立和维持具有极化上皮细胞特征的质膜蛋白的不对称分布:沿着细胞骨架靶向运输小泡,运输小泡在正确的膜域上的特定对接, 以及蛋白质在特定膜域中的滞留或滞留。
细胞骨架一直是研究的重点,以确定囊泡运输至特定膜域和膜蛋白滞留的机制。 在极化上皮细胞中,肌动蛋白细胞骨架分布在贴壁细胞与细胞黏附连接处的侧膜顶端周围,沿侧膜和基底膜呈环状分布; 在形成刷状边界的细胞(例如肠细胞)中,肌动蛋白丝也形成单个微绒毛的核心( 纳尔逊,1991年 ; 梅斯 等。 , 1994 ). 细胞松弛素对肌动蛋白细胞骨架的破坏似乎对囊泡向顶端或基底外侧膜域的转运没有什么影响( 萨拉斯 等。 , 1986 ; 帕奇克 等。 , 1989 ; Ojakian和Schwimmer,1992年 ). 然而,值得注意的是,肌球蛋白存在于纯化的TGN后运输囊泡上,表明肌动蛋白细胞骨架参与囊泡运输( Fath和Burgess,1993年 ). 此外,肌动蛋白为基础的膜细胞骨架需要在基底外侧膜中保留Na/K-ATP酶( 哈默顿 等。 , 1991 ).
完全分化上皮细胞中的微管组织包括一个由细丝组成的顶端网,沿着细胞的顶端-基底轴组织的皮质细丝,以及细胞底部的短细丝( 巴卡廖 等。 , 1989 ; van Zeijl和Matlin,1990年 ; 吉尔伯特 等。 , 1991 ); 我们将这种微管组织称为顶核(AN)型,以将其与非极化上皮细胞和成纤维细胞中的微管组织进行对比,在这些细胞中,微管组织来自一个宽阔的核周区域(PN型)( 巴卡廖 等。 , 1989 ). 先前的研究表明,秋水仙碱或诺可唑破坏微管后,TGN和心尖膜之间的小泡运输受到影响,而向基底外侧质膜的运输则不受影响( 林德勒 等。 1987年 ; Achler公司 等。 , 1989 ; 艾尔斯 等。 , 1989 ; 物质 等。 , 1990 ; van Zeijl和Matlin,1990年 ). 这些结果来自于对全极化上皮细胞中蛋白质运输的分析,在使用微管分裂药物治疗之前,该细胞在检查时具有an-型微管组织( van Zeijl和Matlin,1990年 ; 吉尔伯特 等。 , 1991 ). 有人认为,an型微管组织和高尔基复合体同时重新定位到细胞的顶端区域有助于将蛋白质从TGN有效地传递到顶端膜( van Zeijl和Matlin,1990年 ). 然而,在体外,基底外侧转运小泡与微管结合( 范德斯鲁伊斯 等。 , 1990 )标记蛋白向基底外侧膜的传递似乎需要微管运动蛋白( 拉丰特 等。 , 1994 ).
我们重新评估了微管的作用及其在蛋白质贩运中的具体分布。 我们使用了两个MDCK细胞克隆:克隆II/G细胞在极性发育过程中重组微管和高尔基复合体,从PN型分布到AN型分布,而克隆II/J细胞保持PN型组织。 我们表明,在极性发育过程中,在微管从PN型重组为AN型之前,内源性顶端和基底外侧标记蛋白的传递是高效和特异的。 此外,我们发现微管破裂后,顶端和基底外侧蛋白的传递效率降低。 这些结果表明,尽管微管是有效传递顶端和基底外侧蛋白所必需的,但微管和高尔基复合体的an型分布对于将几种质膜蛋白适当靶向细胞表面并不重要。
材料和方法 细胞和组织培养方法 Madin-Darby犬肾(MDCK)克隆II/G细胞从Gerrit van Meer实验室获得,并按前述方法分离( 高什(Gaush) 等。 , 1966 ; Louvard,1980年 ); 在Nelson实验室独立分离克隆II/J细胞( Nelson和Veshnock,1986年 )来自美国类型培养物收集(马里兰州盖瑟斯堡)获得的MDCK细胞库中的单个细胞克隆。 基于跨上皮电阻[200-300Ω/cm 2 ]克隆II/G和II/J细胞均为II型MDCK细胞,通过免疫荧光和细胞表面生物素化检测,在Na/K-ATP酶、E-cadherin、锚蛋白、fodrin和gp135/170的稳态定位方面无法区分( 沃尔纳 等。 , 1992 ; 梅斯 等。 1995年a , 1995年b ).
如前所述,细胞保存在补充有10%胎牛血清(FBS)、青霉素、链霉素和卡那霉素(DMEM/FBS)的DMEM中( Nelson和Veshnock,1986年 ). 细胞在组织培养皿上以低密度进行常规传代,然后在Transwell 0.45-μm聚碳酸酯过滤器上以汇合密度进行电镀( Costar公司 (马萨诸塞州剑桥市)涂有I型鼠尾胶原蛋白( 哈默顿 等。 , 1991 ; 西默斯 等。 , 1993 ). 在培养基中作为融合单层保存较长时间的细胞每天进行参考。 克隆的低信息复制品繁殖4-6周,然后丢弃。
生成汇合的“接触-活性”细胞单层( Nelson和Veshnock,1987年 ),细胞保持在低密度(2×10 6 细胞/直径150mm的培养皿)并连续传代。 用胰蛋白酶处理后,细胞在1000× 克 持续5分钟,并重悬于含有5μM Ca的DMEM中 2+ 补充10%的FBS,该FBS已经过磷酸盐缓冲盐水(PBS)彻底透析(不含Ca 2+ ). 约2×10 6 将2ml培养基中的细胞加入2.4-cm 2 涂有I型胶原的Transwell过滤器; 将2.5 ml培养基添加到过滤器的外侧(基底侧)隔间。 在37°C下3小时后,此时95%以上的细胞附着在过滤器上,用含有1.8mM Ca的DMEM/FBS代替培养基 2+ 诱导单分子层间的同步细胞接触( 哈默顿 等。 , 1991 ; 西默斯 等。 , 1993 ); 这是对以前协议的修改( Nelson和Veshnock,1987年 )减少细胞暴露于低钙环境的时间 2+ 在介质中。 在切换到正常含钙培养基后,如文中所述,细胞在培养基中保持120小时。
免疫荧光标本的制备和成像 用于检查微管组织的固定和染色方法基本上如前所述( 巴卡廖 等。 , 1989 ). 在诱导细胞与细胞接触后的指定时间,用0.5%戊二醛在100 mM K-哌嗪中固定细胞- N、 N个 ′-双(2-乙磺酸)(PIPES),pH 6.9,4 mM MgCl 2 ,2 mM EGTA,含0.1%Triton X-100。 用1 mg/ml NaBH处理样品,使固定反应停止 4 溶于PBS,pH 8.0。 用PBS多次洗涤后,用α-和β-微管蛋白特异性单克隆抗体培养样品(美国伊利诺伊州阿灵顿高地Amersham)。 用含有0.1%Triton X-100的PBS洗去多余抗体,并用罗丹明结合的驴抗鼠免疫球蛋白G孵育样本( 杰克逊免疫研究 宾夕法尼亚州西格罗夫)。 用含有0.1%Triton X-100的PBS洗去多余的二级抗体,并在室温下用溶解在PBS中的2%多聚甲醛将样品固定30分钟。 样品安装在含有50%甘油和100 mg/ml 1,4-二氮杂二环(2.2.2)辛烷(西格玛,圣路易斯,密苏里州)的PBS中。
用溶解在PBS中的2%多聚甲醛在室温下固定制备的用于检查高尔基复合体的样品10分钟。 用50 mM NH淬火固定反应 4 Cl在室温下在PBS中溶解30分钟。 样品在含有1%十二烷基硫酸钠的PBS中培养1分钟。样品在含有0.1%Triton X-100的PBS内广泛清洗,然后用抗βcop抗体(克隆M3A5)(Sigma)培养。 用含有0.1%Triton X-100的PBS洗去多余抗体,并用体结合驴抗鼠免疫球蛋白G标记样本( 杰克逊免疫研究 ). 用含有0.1%Triton X-100的PBS洗去多余的二级抗体。 样品安装在含有50%甘油、100 mg/ml 1,4-二氮杂二环(2.2.2)辛烷和1μg/ml核酸染色剂TO-PRO-3(分子探针,尤金,OR)的PBS中。
使用 美国伯乐 MRC 1024共焦显微镜( 美国伯乐 (加利福尼亚州里士满)安装在配备He-Ar和Kr-Ar激光器的尼康Diaphot 200倒置显微镜(伊利诺伊州亨特利傅兰雅科学仪器公司)上。 使用100×油浸透镜(数值孔径1.4)采集连续图像,z步长为0.2μm。 立体对图像由MetaMorph图像处理程序(Universal Imaging,West Chester,PA)在Micron Millennia计算机(Micron Electronics,Nampa,ID)上生成。 对处理后的图像进行调整,以优化图像的对比度和亮度。
代谢标记 细胞培养物最初在如上所述补充有10%FBS的DMEM中建立。 细胞在不含蛋氨酸/半胱氨酸(DMEM/FBS,−met,−cys)的DMEM/FPS中预培养60分钟,然后在含有250μCi[ 35 S] 蛋氨酸/半胱氨酸(伊利诺伊州阿灵顿高地阿默沙姆)在37°C下维持1小时。 将细胞在预热的DMEM/FBS中冲洗两次,然后在该培养基中培养5分钟,然后从顶端和基底外侧隔室取出一小份以获取gp80分泌。 然后对过滤器进行区域特异性生物素化,如下所述。
区域特异性生物素化和免疫沉淀 在上述代谢标记期后,MDCK细胞的融合单层 Costar公司 Transwell聚碳酸酯过滤器在冰镇林格盐水(154 mM NaCl,1.8 mM Ca)中清洗两次 2+ ,7.2 mM KCl,10 mM HEPES,pH 7.4)。 NHS-SS-生物素,300μg/ml( 皮尔斯化学公司 ,Rockford,IL),在使用林格氏盐水之前立即制备,添加到过滤器的顶部(400μl)或基底侧(800μl)隔间,并在4°C下培养细胞30分钟,不断摇晃; 林格的生理盐水被添加到对面的隔间。 在4°C条件下,在五次改变Tris生理盐水(120 mM NaCl,10 mM Tris,pH 7.4)的条件下,通过洗涤细胞对生物素化反应进行猝灭,对于微管/对照样品,使用微管稳定缓冲液(0.1 mM PIPES,pH 6.75,1 mM MgSO)进行两次猝灭 4 ,1 mM EDTA,2 M甘油)( van Zeijl和Matlin,1990年 ). 重复的筛选器,其模拟标记为[ 35 S] 蛋氨酸/半胱氨酸和生物素(微管/对照样品)被用来通过测量单分子层的扩散来评估功能性紧密连接的存在[ 三 H] 在与生物素交联试剂孵育期间,菊粉(杜邦新英格兰核电站,马萨诸塞州波士顿)从顶端到基底外侧室。 仅进一步使用了抑制>98%示踪剂扩散的过滤器。
细胞提取和免疫沉淀 在放射免疫沉淀分析(RIPA)缓冲液(150 mM NaCl,10 mM NaPO)中提取细胞 4 pH 7.0,0.1%十二烷基硫酸钠,1%NP-40,1%脱氧胆酸盐)在4°C下保持30分钟( 欣克牌手表 等。 , 1994 ),或微管提取缓冲液(0.1 mM PIPES,pH 6.75,1 mM MgSO 4 ,1 mM EDTA,2 M甘油,0.1%(wt/vol)Triton X-100),37°C下保持20分钟( van Zeijl和Matlin,1990年 ). 从每个代谢标记样品中取出一小份,并用10%三氯乙酸沉淀,以使样品正常化[ 35 S] 蛋氨酸/半胱氨酸掺入。 用5μl免疫前血清和60μl预处理RIPA缓冲液(350μl)中分离的细胞提取物 金黄色葡萄球菌 细胞(Pansorbin;Calbiochem Novabiochen,加利福尼亚州拉荷亚)在4°C下放置60分钟。 同时,一抗15μl钙粘蛋白抗血清( 马尔 等。 , 1993 )或40μl gp135/170单克隆抗体(来自纽约布鲁克林纽约州立大学G.Ojakian博士的礼物)在4°C下添加到蛋白a Sepharose(PAS)珠(新泽西州皮斯卡塔韦Pharmacia Biotech)中60分钟。 对于gp135/170单克隆抗体,在与小鼠单克隆抗体孵育之前,将兔抗鼠二级抗血清(Dako,Carpintia,CA)在4°C下与PAS珠预先结合1 h。 将预先吸收的抗体–PAS复合物添加到预先分离的提取物中,并在4°C下培养120分钟。 如前所述,在严格的条件下清洗免疫沉淀物( 辛克 等。 , 1994 ). 抗体-抗原复合物被解离,生物素化的蛋白质用亲和素琼脂糖重新沉淀( 皮尔斯化学公司 )如前所述,在严格的条件下清洗( 哈默顿 等。 , 1991 ; 西默斯 等。 , 1993 ). 在微管稳定条件下分离的细胞提取物在20000× 克 并分离成可溶和不可溶部分。 然后在室温下将不溶性部分溶解在微管溶解缓冲液(25 mM Tris,pH 7.4,0.4 M NaCl,0.5%SDS)中10 min。
凝胶电泳和免疫印迹 蛋白质样品在100°C的SDS样品缓冲液中培养10分钟,然后在SDS-7.5%聚丙烯酰胺凝胶中分离( 莱姆利,1970年 ). 对于代谢标记样品,凝胶在真空下干燥,并暴露于x射线胶片(XAR-5;Eastman Kodak,Rochester,NY)和磷成像仪屏幕(Molecular Dynamics,Sunnyvale,CA)。 使用激光扫描磷光体成像仪(820型;分子动力学)直接测定凝胶中标记蛋白质的数量。 为了监测gp80在培养基中的外观,在非还原条件下用SDS-PAGE分离顶端或基底外侧培养基的等分样品。 在这些条件下,gp80是MDCK细胞中观察到的主要标记分泌蛋白,并在大约80 kDa时以单一带的形式迁移( 康多·科赫 等。 , 1985 ; 戈特利布 等。 , 1986 ; 城市的 等。 1987年 ).
对于微管蛋白样品,凝胶电泳转移到Immobilon聚偏氟乙烯膜(Millipore,Bedford,MA)。 根据制造商协议(Amersham),使用β-微管蛋白单克隆抗体(Amersham)处理印迹以增强化学发光。 β-微管蛋白单克隆抗体与兔抗鼠辣根过氧化物酶偶联二级抗体(Amersham)结合。
诺卡唑对微管的干扰 在二甲基亚砜中制备诺卡唑库存(10 mg/ml),并在−20°C下储存在一次性小份中。 诺卡唑储备溶液在使用前立即稀释到适当的培养基中,最终浓度为10μg/ml(33μM)。 如图所示的时间线 三 A、 培养物最初在4°C的DMEM/FBS中培养30分钟。然后用DMEM/FFS,−met,−cys替换培养基,并在适当的情况下补充33μM诺卡唑,培养物在4°C.下再培养30分钟。 用DMEM/FBS,−met,−cys参考培养物,在适当的情况下补充33μM诺可唑,并将其移至37°C再保持30分钟。然后按照上述方法对细胞进行脉冲标记,修改为在适当的培养基中加入33μM诺可唑。 需要注意的是,在标记期后进行检测时,在不含诺卡唑的情况下暴露于4°C处理的培养物中的微管组织显示出与极性发展过程中所有时间点保持在37°C下的培养物相同的微管组织(我们未发表的观察结果)。
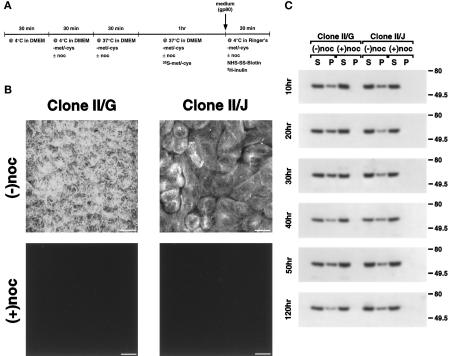
图3。
诺康唑治疗后微管蛋白在MDCK克隆II/G和II/J细胞中的分布。 (A) 用于破坏微管的实验方案时间表。 按照材料和方法中的描述建立融合MDCK克隆II/G和II/J培养物。 (B) 在诺克唑不存在(−noc)或存在(+noc)的情况下培养后,固定120h分化的MDCK克隆II/G和克隆II/J细胞,并用抗α-和β-微管蛋白的单克隆抗体进行免疫荧光处理(见材料和方法),以显示完整微管的分布。 使用0.2μm的z步长从每个样本采集的序列图像生成图像堆栈。 (C) 在诱导细胞-细胞接触后的指定时间,在不存在(−noc)或存在(+noc)诺可唑的情况下孵育的MDCK细胞的两个克隆中测定可溶性(S)和聚合微管蛋白(P)的量。 样品在含有0.1%Triton X-100的微管稳定缓冲液中提取,并在20000× 克 分离可溶性(S)和不溶性部分(P)。 然后将不溶性部分溶解在0.5%Triton X-100中。 用SDS-PAGE分离每个样品的等量上清液和颗粒组分。 然后将凝胶电泳转移到Immobilon聚偏氟乙烯膜上,并用β-微管蛋白单克隆抗体进行检测。 β-微管蛋白抗体用辣根过氧化物酶偶联的第二抗体显示,然后增强化学发光。 给出了每个时间点的两到四个独立实验的代表性样本。 棒材,10μm。
结果 MDCK克隆II/G和II/J细胞建立细胞接触后微管的组织 我们分析了两个独立衍生的MDCK细胞克隆( 高什(Gaush) 等。 , 1966 ; Nelson和Veshnock,1986年 ). 两个克隆形成紧密(TER~250Ωcm 2 )极化单层,其中顶端(gp80,gp135/170)和基底外侧(E-cadherin)蛋白在稳定状态下仅定位于特定的膜域( 沃尔纳 等。 , 1992 ; 梅斯 等。 1995年a , 1995年b ).
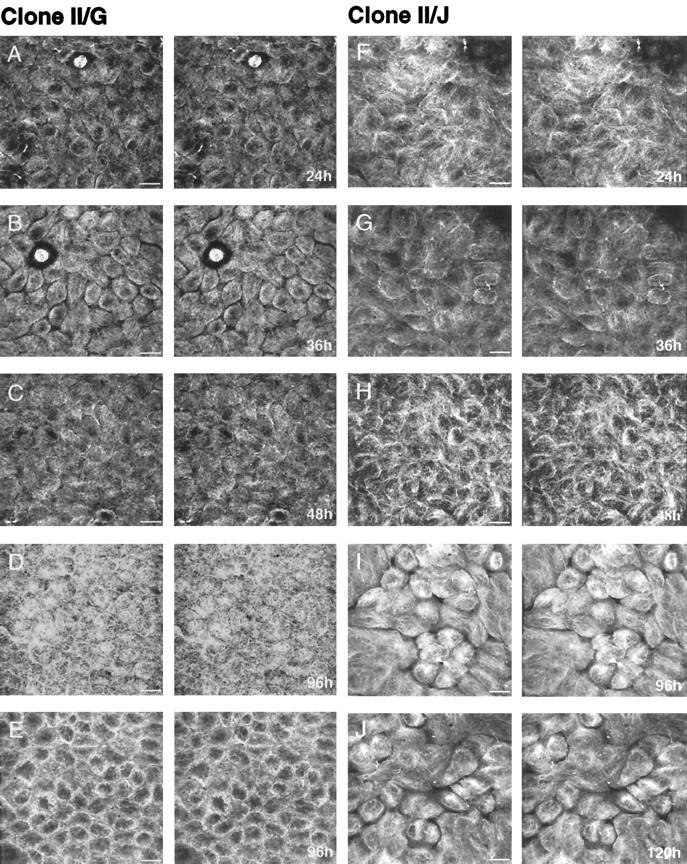
共聚焦免疫荧光显微镜观察微管的分布; 图像被表示为立体对。 在克隆II/G细胞中,诱导细胞-细胞粘附24小时后,微管起源于靠近细胞核的细胞质的一个广阔区域,并向外延伸至质膜(图 1 A) ●●●●。 到48小时,这些细胞中的微管组织发生了显著变化(图 1 C) ●●●●。 微管在顶下膜细胞质中形成一个丝网,长的皮层丝线平行于细胞长度范围内的侧膜,以及沿着基底膜随机组织的短丝网。 在96小时培养的图像中,皮层微管的组织最清晰,其中前8μm的图像堆栈已从立体视图中删除(图 1 E) ●●●●。 在克隆II/G细胞中观察到的微管重组和最终分布与之前报道的类似( 巴卡廖 等。 , 1989 ).
图1。
诱导细胞-细胞接触后不同时间MDCK克隆II/G和II/J细胞微管的共焦图像(立体对)。 融合MDCK克隆II/G(A–E)和II/J(F–J)培养物是通过在含有5μM Ca的DMEM/FBS中的胶原涂层聚碳酸酯过滤器上以融合密度接种“接触幼稚”细胞来建立的 2+ 随后通过升高Ca启动同步电池-电池接触 2+ 培养基浓度达到1.8 mM。在诱导细胞-细胞接触后的指定时间,按照材料和方法中的描述,用抗α-和β-微管蛋白的单克隆抗体固定并处理样品进行免疫荧光。 使用0.2μm的z步长从每个样本收集的序列图像中生成立体成对图像堆栈。 (E) 将图像堆栈的前8μm从96小时克隆II/G细胞样品的立体对中移除,以便可以轻松查看皮层微管的组织。 棒材,10μm。
与克隆II/G细胞中微管的重组形成直接对比的是,克隆II/J细胞的微管分布在细胞极性发育过程中没有改变。 在克隆II/J细胞中,细胞与细胞接触诱导24小时后,微管起源于细胞质宽阔的核周区域,并向外延伸至细胞外围(图 1 F) ; 这种分布与此时克隆II/G细胞中的分布相似(见上文)。 然而,这种微管组织在培养中维持长达120小时的克隆II/J细胞中持续存在(图 1 J) ●●●●。
这些结果表明,在细胞表面极性发育过程中,两个独立衍生的MDCK细胞克隆的微管分布明显不同。 来自两个克隆的非极化细胞的微管阵列是从核周部位(PN型)成核的。 在随后建立细胞表面极性的过程中,克隆II/G细胞中的微管围绕亚顶端位点(AN-型)重组,而克隆II/J细胞中的那些微管维持PN-型微管组织。 然而,这两个克隆的细胞在稳定状态下发育出相同的顶端和基底外侧膜蛋白分布( 沃尔纳 等。 1992年 ; 梅斯 等。 1995年a , 1995年b ). 注意,对两个克隆在每个时间点的细胞形态分析表明,平均1)克隆II/J细胞的高度比克隆II/G细胞的高度低5–15%; 克隆II/J细胞的直径是克隆II/G细胞直径的1.2–1.5倍(我们未发表的观察结果)。
MDCK克隆II/G和II/J细胞粘附后高尔基体分布的变化 先前的研究表明高尔基复合体在细胞中的分布与微管组织直接相关( 巴卡廖 等。 , 1989 ). 因此,我们比较了极性发育过程中克隆II/G和II/J细胞中高尔基体和微管的分布。 高尔基分布由β-COP的分布决定( Allan和Kreis,1986年 ; 杜登 等。 , 1991 ),它本地化为 顺式 -高尔基复合体区域; 结果如表所示 1 细胞-细胞粘附24小时后,克隆II/G和II/J细胞中的高尔基复合体主要位于核周/核周位置(约70%的细胞)。 然而,诱导细胞-细胞接触后约36小时,70%以上II/G细胞中的高尔基复合体重新定位到顶端核位置,伴随着这些细胞中的微管重组。 到48小时,约90%的克隆II/G细胞中的高尔基复合体已重新定位到顶端核位置; 96h后,100%的克隆II/G细胞显示这种高尔基体分布。 相反,II/J细胞中的高尔基复合体在所有检查时间点都主要局限于核周/核周位置(表 1 ). 当高尔基体被C6-NBD陶瓷标记时,也得到了类似的结果(我们未发表的观察结果)。 这些结果证明了微管和高尔基复合体分布的相互关系; 在克隆II/G细胞中,它们最初表现出PN型分布,然后在极性发育过程中重新分布到an型组织,但在克隆II/J细胞中始终保持PN型组织。
表1。 细胞接触开始后不同时间MDCK克隆II/G和II/J细胞中高尔基复合体的定位
单元格类型 高尔基本地化
核周/环状核 无核细胞的
克隆II/G
24小时 60 ± 10 40 ± 10
36小时 26 ± 3 74 ± 3
48小时 6.2 ± 3.7 93.3 ± 4.2
96小时 0 100
120小时 0 100
克隆II/J
24小时 75.3 ± 4.5 24.6 ± 4.5
36小时 54.5 ± 16.1 45.3 ± 20.4
48小时 79.5 ± 11.2 20.5 ± 11.6
96小时 63 ± 14.7 37 ± 14
120小时 65 ± 12.5 35 ± 12.4
MDCK克隆II/G和II/J细胞中新合成蛋白质直接靶向细胞表面途径的建立 MDCK细胞的两个独立衍生克隆产生不同的微管分布,这为直接评估微管组织本身是否指定从TGN到不同质膜域的蛋白质靶向提供了机会。 此外,由于克隆II/G细胞最初具有PN型,然后发展为an型微管/高尔基体组织,我们可以检查向特定质膜结构域的蛋白质运输是否与从PN型到an型微管/高尔基体组织的转变在时间上相关。
我们检测了三种内源性蛋白质直接传递到细胞表面的情况。 通过捕捉第一波新合成的蛋白质到达质膜来确定向顶端或基底外侧膜域的蛋白质输送。 我们监测了主要是顶端分泌蛋白gp80的外观( 康多·科赫 等。 , 1985 ; 戈特利布 等。 , 1986 ; 城市的 等。 1987年 ),顶膜蛋白gp135/170( Ojakian和Schwimmer,1988年 )和基底外侧膜蛋白E-钙粘蛋白( 勒比维奇 等。 , 1990 ).
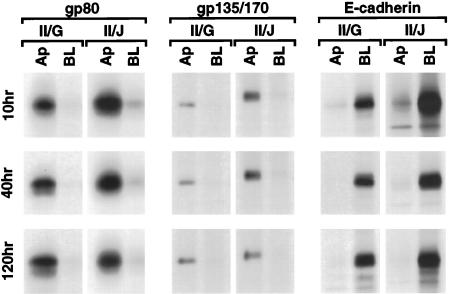
gp80和gp135/170靶向心尖膜 gp80的分泌可以通过从过滤器插入物的顶端和基底外侧室中取出培养基并通过非还原性SDS-PAGE分离蛋白质来检测。 在克隆II/G和II/J细胞中检测到,>80%的新合成gp80是从顶端膜域分泌的(图 2 ). 通过细胞表面区域特异性生物素化检测gp135/170到达质膜; 从细胞中提取生物素化蛋白,用特异性gp135/170抗体亲和分离,然后用亲和素-甘露糖沉淀生物素化gp135/170。 结果表明,在II/G和II/J细胞中,90%以上的新合成gp135/170直接传递到心尖膜(图 2 ).
图2。
在MDCK克隆II/G和II/J细胞中极性发育过程中,新合成的gp80、gp135/170和E-钙粘蛋白靶向质膜。 按照材料和方法中的描述建立融合MDCK克隆II/G和II/J培养物。 每个克隆的重复过滤器在新陈代谢中标记为[ 35 S] 蛋氨酸/半胱氨酸在37°C下保持1小时。 代谢标记期结束后,立即从过滤器的顶部和底部收集培养基,并用SDS-PAGE进行分离,以监测新合成的gp80向顶部(Ap)和基底外侧(BL)表面的传递。 然后用NHS-SS-生物素标记细胞顶部(Ap)或基底外侧(BL)表面。 按照材料和方法中的描述,在RIPA缓冲液中提取细胞。 然后将样品分成两半,用gp135/170单克隆抗体或E-cadherin抗血清沉淀,然后用亲和素琼脂糖沉淀。 在诱导细胞-细胞接触后的指定时间收集的样品中的培养基和免疫沉淀物进行SDS-PAGE和荧光照相。 给出了每个时间点两到四个独立实验的代表性样品的荧光检测结果。
E-Cadherin靶向基底外侧膜 通过细胞表面区域特异性生物素化测定新合成的E-cadherin向细胞表面的传递; 从细胞中提取生物素化蛋白,并用特异性E-钙粘蛋白抗体亲和性分离,然后用亲和糖沉淀生物素化E-钙黏蛋白。 无论何时在克隆II/G和II/J细胞中检测,新合成的E-钙粘蛋白>90%直接靶向基底外侧膜(图 2 ).
综上所述,这些结果表明,在诱导细胞-细胞接触后的10 h内,克隆II/G和II/J细胞中分别建立了gp80和gp135/170以及E-cadherin向心尖和基底外侧质膜的直接传递途径。 此时,微管在两个细胞克隆中都有PN型组织。 克隆II/G细胞中微管重组为an型发生较晚,与这些蛋白靶向性的改变不一致。
完整微管在MDCK克隆II/G和II/J细胞极性发育过程中靶向细胞表面结构域蛋白中的作用 接下来,我们试图检查完整的微管本身是否是蛋白质靶向所必需的,无论是PN型还是AN型组织。 联合使用冷处理和诺康唑,MDCK克隆II/G和II/J细胞中的微管被破坏(图 三 A) ●●●●。 通过在4°C下预孵育细胞,然后添加33μM诺卡唑,启动微管破裂。 诺康唑治疗后,120h分化克隆II/G和II/J细胞的间接免疫荧光显示没有完整的微管(图 三 B) ; 在诱导细胞与细胞接触后,在较短时间内保持培养的细胞中观察到了相同的结果(我们未发表的观察结果)。 为了定量评估微管破坏,我们检测了在微管稳定缓冲液中提取细胞并以20000× 克 在细胞极性发育的不同阶段从对照细胞制备的提取物中,颗粒组分中存在>30%的微管蛋白。 然而,在用33μM诺卡唑处理后,颗粒组分中未检测到微管蛋白,上清液组分中微管蛋白的数量成比例增加,表明该方案已导致>99%的聚合微管蛋白被破坏(图 三 C) ●●●●。
我们研究了在克隆II/G和II/J细胞建立上皮极性的过程中,微管破裂对新合成蛋白靶向顶端和基底外侧膜域的影响。 请注意,尽管微管被破坏,但蛋白质运输仍然可以通过细胞表面区域特异性生物素化进行检测,因为紧密连接仍然不渗透菊糖的细胞旁传代(我们未发表的观察结果)。
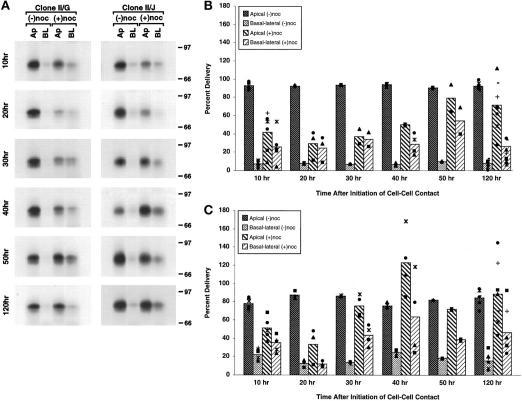
gp80和gp135/170靶向顶膜 细胞-细胞接触诱导后0至40小时,II/G细胞微管破裂,导致gp80的顶端分泌减少~50%(图 4 A) ●●●●。 同时,gp80在基底外侧培养基中的分泌比例增加。 到50小时时,微管破裂对gp80顶端递送的抑制作用不太明显,尽管gp80仍被错误地输送到基底外侧培养基中。 对随后时间点的分析显示,在分泌到根尖和基底外侧培养基中的gp80的量的独立实验之间存在不一致; 典型实验的结果如图所示 4 A、 图中给出了八个独立实验的平均值和个别结果 4 B.注意,在对照克隆II/G细胞的平行培养中,在细胞极性发育期间检查的所有时间点,新合成的gp80中有80%以上是从顶端表面分泌的(图 4 、A和B)。
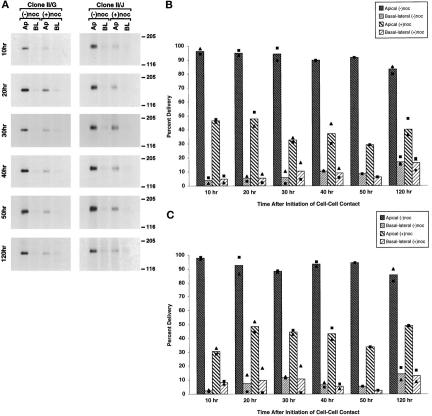
图4。
完整微管在MDCK克隆II/G和II/J细胞极性发育期间将新合成的gp80靶向质膜的作用。 如材料和方法中所述,建立汇合的MDCK克隆II/G和II/J培养物。 如图所示 三 A、 培养物在诺克唑不存在(−noc)或存在(+noc)的条件下培养。 在37°C下的最后一个小时内,培养物的代谢标记为[ 35 S] 蛋氨酸/半胱氨酸。 代谢标记期结束后,从过滤器的顶部和底部室收集培养基。 通过SDS-PAGE分离分泌蛋白,以监测新合成的gp80在诱导细胞-细胞接触(10–120 h)后的指定时间传递到顶端(Ap)和基底外侧(BL)表面。 (A) 给出了每个时间点代表性样品的荧光检测结果。 使用分子动力学荧光成像仪(820型)直接测定凝胶中标记的gp80的量。 MDCK克隆II/G(B)和克隆II/J(C)细胞的蛋白质的扫描密度测定结果显示为在没有诺可唑的情况下新合成的gp80总量的百分比(递送百分比)。 条形图描述了两到九个独立实验的平均值,每个实验都由散点图中的一个符号表示。
在克隆II/J细胞中,诱导细胞与细胞接触10小时后,微管破裂将新合成的gp80分泌抑制到顶端培养基中约30%,同时将gp80分泌增加到基底侧培养基中(图 4 C) ●●●●。 在20小时时,微管破裂后,gp80在顶端培养基中的分泌减少了>50%,但很少或没有gp80分泌到基底外侧培养基中。 诱导细胞-细胞接触30小时后,微管破裂对新合成gp80顶端分泌的抑制作用显著降低,尽管基底侧培养基中分泌了大量gp80。 到50小时时,微管破裂对gp80的顶端分泌没有抑制作用,尽管我们确实观察到分泌到基底外侧培养基中的gp80的量有明显的差异(图 4 C) ●●●●。 与克隆II/G细胞的结果类似,我们后来发现,在独立实验之间,分泌到顶端和基底外侧培养基中的gp80的数量差异很大(图 4 C) ●●●●。 注意,在对照克隆II/J细胞中,>80%的新合成gp80始终分泌到顶端培养基中(图 4 、A和C)。
由于以下原因,我们不认为后期观察到的gp80分泌到心尖和基底外侧介质的变化是由于实验错误造成的:1)多个独立实验记录了这种影响; 2) 新合成的gp80在平行对照细胞中的传递在各个实验之间没有差异; 3) 在每个实验中,用相同的Transwell过滤器制备的其他顶端或基底外侧膜蛋白在实验之间的差异相对较小; 4)由于微管破裂后,紧密连接处仍然不渗透菊糖的细胞旁扩散,因此gp80没有在过滤-插入室之间扩散。 因此,实验之间的差异可能代表了微管破裂后顶端和基底外侧表面gp80分泌的随机性。 尽管gp80在极化MDCK细胞中的靶向作用先前已被证明对微管破坏敏感( 帕奇克 等。 , 1989 )在建立细胞-细胞接触后的不同时间,我们观察到微管破裂后gp80分泌的变化尚未报道。
在每次检测克隆II/G和II/J细胞的微管破裂后,新合成的gp135/170向心尖质膜的传递被抑制了约50%,但与gp80相比,我们没有检测到gp135/1170向基底外侧膜的伴随错配。 注意,90%以上新合成的gp135/170始终直接输送到对照II/G和II/J细胞的顶端质膜(图 5 ).
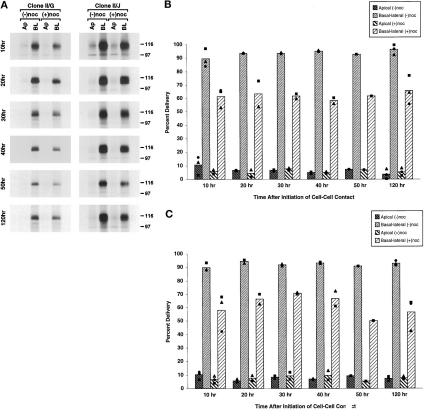
图5。
完整微管在MDCK克隆II/G和II/J细胞极性发育期间将新合成的gp135/170靶向质膜的作用。 按照材料和方法中的描述建立融合MDCK克隆II/G和II/J培养物。 如图所示 三 A、 培养物在诺克唑不存在(−noc)或存在(+noc)的条件下培养。 在37°C的最后一个小时,培养物被代谢标记为[ 35 S] 蛋氨酸/半胱氨酸。 在诱导细胞-细胞接触后的指定时间(10–120 h),用NHS-SS-生物素在顶膜(Ap)或基底膜(BL)上标记双重滤膜。 然后在RIPA缓冲液中提取细胞,如材料和方法所述。 依次用抗gp135/170的单克隆抗体沉淀样品,然后用亲和素琼脂糖沉淀。 然后处理免疫沉淀物进行SDS-PAGE和荧光成像。 (A) 给出了每个时间点代表性样本的荧光成像结果。 使用分子动力学荧光成像仪(820型)直接测定凝胶中标记的gp135/170的量。 MDCK克隆II/G(B)和克隆II/J(C)细胞蛋白质的扫描密度测定结果显示为在没有诺卡唑的情况下传递到质膜的新合成gp135/170总量的百分比(传递百分比)。 条形图描述了一到三个独立实验的平均值,每个实验都由散点图中的一个符号表示。
E-Cadherin靶向基底外侧膜 克隆II/G和II/J细胞中的微管破裂,以及在任何时候的检查,都会导致新合成的E-钙粘蛋白输送到基底外侧质膜的量减少约30%。 我们没有检测到E-cadherin在根尖膜上的任何错配。 注意,在对照克隆II/G和II/J细胞中,90%以上新合成的E-钙粘蛋白始终直接传递到基底外侧质膜(图 6 ).
图6。
在MDCK克隆II/G和II/J细胞极性发育过程中,完整微管在新合成的E-cadherin靶向质膜中的作用。 按照材料和方法中的描述建立融合MDCK克隆II/G和II/J培养物。 如图所示 三 A、 培养物在诺克唑不存在(−noc)或存在(+noc)的条件下培养。 在37°C下的最后一个小时内,培养物的代谢标记为[ 35 S] 蛋氨酸/半胱氨酸。 在诱导细胞-细胞接触后的指定时间(10–120 h),用NHS-SS-生物素在顶膜(Ap)或基底膜(BL)上标记双重滤膜。 然后在RIPA缓冲液中提取细胞,如材料和方法所述。 样品依次用E-cadherin抗血清沉淀,然后用亲和素琼脂糖沉淀。 然后处理免疫沉淀物进行SDS-PAGE和荧光成像。 (A) 给出了每个时间点代表性样品的荧光检测结果。 使用分子动力学荧光成像仪(820型)直接测定凝胶中标记的E-cadherin的数量。 MDCK克隆II/G(B)和克隆II/J(C)细胞的蛋白质的扫描密度测定结果以新合成的E-钙粘蛋白总量的百分比表示,在没有诺可唑的情况下传递到质膜(传递百分比)。 条形图描述了一到三个独立实验的平均值,这些实验由散点图中的一个符号表示。
讨论 我们发现,新合成的gp135/170、gp80和E-cadherin直接传递到克隆II/G和II/J MDCK细胞的正确膜域是在诱导细胞-细胞接触后10小时内建立的(另请参阅, 沃尔纳 等。 , 1992 ; 梅斯 等。 1995年b ). 值得注意的是,此时克隆II/G和II/J细胞都具有PN型微管/高尔基体组织; 直到细胞与细胞粘附后48小时,克隆II/G细胞中才出现AN-型微管组织。 然而,PN型微管组织对于将这些蛋白质传递到细胞表面很重要; MDCK细胞的两个克隆中的微管破裂分别使gp135/170和E-cadherin传递到顶端膜和基底外侧膜的量减少了25-50%。 我们注意到,在没有微管的情况下,这些蛋白质没有错误地转移到错误的膜域。 在新建立的MDCK培养物中,gp80向顶端膜的递送在微管破坏后也减少了约30-50%。 与gp135/170和E-cadherin相反,在没有微管的情况下,检测到gp80向基底外侧膜的一些错配。 在诺卡唑处理的完全分化细胞中,gp80向两个膜域的传递是可变的和非特异性的。 因此,gp80代表一类顶端蛋白,需要完整的微管才能有效和适当地传递到细胞表面。
我们从这些结果中得出两个结论。 首先,完整的微管似乎有助于向顶端和基底外侧质膜传递蛋白质。 这一结果证实了微管在促进蛋白质递送到顶端膜中的作用( 林德勒 等。 1987年 ; Achler公司 等。 , 1989 ; 艾尔斯 等。 , 1989 ; 物质 等。 , 1990 ; van Zeijl和Matlin,1990年 ; 吉尔伯特 等。 , 1991 ). 与之前的几项研究相比( 林德勒 等。 1987年 ; Achler公司 等。 , 1989 ; 艾尔斯 等。 , 1989 ; 物质 等。 , 1990 ; van Zeijl和Matlin,1990年 ),我们的结果表明,微管也需要促进膜蛋白靶向基底外侧膜。 这种差异的原因很难调和。 我们注意到,在我们的实验中,99%以上的微管被破坏。 此外,我们的标记方案旨在捕获到达质膜的蛋白质的初始波,因此,我们不能评论微管破裂对后续追踪时间蛋白质递送动力学的影响(参见 吉尔伯特 等。 , 1991 ).
第二,蛋白质直接传递到细胞表面独立于特定的微管组织。 我们的结果明确表明,AN型微管/高尔基体组织并不代表上皮细胞中的特殊结构框架,用于将囊泡从TGN靶向顶膜或基底外侧膜。 因此,TGN和不同膜域之间的微管极性对于PN型和AN型组织细胞中的囊泡运输并不重要,或者囊泡可以适应不同的微管方向,因为其膜上存在正负端向微管马达。 拉丰特 等。 (1994年) 有证据表明,在极化的MDCK细胞中,正向和负向微管马达都参与血凝素向顶膜的转运,而只有正向马达(驱动蛋白)参与VSV G蛋白向基底外侧膜的转运。 在具有PN型微管组织的细胞中,将含有gp80的小泡输送到顶端(和基底外侧)膜的方向是微管的正极,而在具有AN型组织的细胞内,将含有gp80的小囊输送到顶端需要负端定向马达。 因此,gp80囊泡可能包含正负端导向马达。 然而,目前尚不清楚在PN型细胞中,细胞如何确保含有gp80的小泡主要沿着微管传递,微管向顶端质膜延伸。 在具有an-型微管组织的细胞中,可能是正-端定向马达变得不太活跃,或者负-端定向电动机成为决定囊泡运动方向的主导者; 这种转变可能不会在克隆II/J细胞分化时发生。 与gp80一样,含有gp135/170的囊泡也必须包含正负端导向马达。 然而,我们注意到,在对照条件下或微管破裂后,gp135/170从未错误地定位到基底外侧膜。 E-cadherin从来没有错误地定位到心尖膜,它只需要一个脉冲导向的马达,以便在具有PN或AN型微管组织的细胞中适当地输送到基底外侧膜。
我们以前的研究表明,随着an-型微管/高尔基体组织的发育,α-Na/K-ATPase直接传递到II/G细胞基底外侧膜的比例增加; II/J细胞中的αNa/K-ATP酶向两个膜域的传递保持在~50:50( 梅斯 等。 1995年b ). 然而,在II/G细胞中,α-Na/K-ATP酶而非E-cadherin对基底外侧膜的分选似乎依赖于鞘糖脂(GSL)分选,这将α-Na/K-ATP酶排除在顶端通路之外。 伏马菌素对II/G细胞GSL合成的抑制导致αNa/K-ATP酶与II/J细胞一样平等地递送到顶端和基底外侧膜,而对E-钙粘蛋白的分选没有任何影响( 梅斯 等。 1995年b ). 然而,与E-cadherin一样,微管破裂对αNa/K-ATP酶向心尖膜错配的影响很小或没有影响(即,在诺康唑存在下,传递到心尖膜的αNa/K-ATP酶的量没有改变;Grindstaff和Nelson,未发表的结果;另见 波尔 等。 , 1991 ). 此外,伏马菌素处理II/G细胞不会影响gp80和E-cadherin的分类( 梅斯 等。 1995年b )而微管破裂会显著减少这些蛋白质向相应的膜域的传递。 我们得出结论,谷胱甘肽对TGN中αNa/K-ATP酶分选的影响与微管在TGN和质膜域之间运输囊泡的传递中的作用不同。
快速建立有效且特异的蛋白靶向顶膜和基底外侧膜的方法表明,在诱导细胞接触后,蛋白质转运途径迅速发展。 先前的研究表明,包括gp135/170在内的顶端蛋白在附着于基质的单个MDCK细胞中的细胞表面分布是极化的( 织女星-阿拉斯 等。 1987年 ; Ojakian和Schwimmer,1988年 ). 另一方面,基底膜蛋白随机分布在单个细胞的游离(顶端)表面和基底膜上( Nelson和Veshnock,1986年 ; 织女星-阿拉斯 等。 1987年 ; 萨拉斯 等。 , 1988 ). 这些结果表明,基底外侧蛋白的细胞表面极性需要诱导基于钙粘蛋白的细胞-细胞粘附。 因为在“非极化”成纤维细胞中,顶端和基底外侧膜蛋白会被分选成离散的转运小泡( 麝香 等。 , 1996 ; 吉森 等。 , 1996 )在MDCK细胞中,无论细胞-基质或细胞-细胞粘附状态如何,顶端和基底外侧蛋白的分选都可能是组成性的。
如果所有细胞表面蛋白在TGN中被分类为一类顶端或基底外侧转运小泡,我们预计gp80将表现出gp135/170传递的特征。 与gp135/170类似,gp80在诱导细胞-细胞接触后10小时内直接传递到心尖膜域。 微管破裂最初导致gp80向心尖膜的转运减少30-50%,与gp135/170相似。 然而,与gp135/170相反,大量gp80被错误地定位到基底外侧膜结构域。 我们的结果表明,含有gp80的囊泡需要完整的微管才能将其输送到心尖膜,并且在没有微管的情况下,这些囊泡能够与基底外侧膜对接并融合。 针对MDCK细胞和LLC-PK中的基底蛋白的靶向也有类似的结果报道 1 大鼠肝细胞微管破裂后的肾上皮细胞和血清白蛋白( 波尔 等。 , 1991 ; De Almeida和Stow,1991年 ; 沙特和帕拉德,1991年 ). 这表明gp80代表一类蛋白质,被分类成囊泡群,这些囊泡具有与两个膜域的混杂对接能力。 相比之下,gp135/170和E-cadherin代表另外两类蛋白质,其传递的特异性主要取决于对接和融合机制的膜域特异性组织,而不是基于微管的靶向通路的建立。
总之,我们已经证明,微管和高尔基复合体从“非极化”细胞的PN型组织向an型组织的再分配不需要建立从TGN到顶膜或基底外侧膜域的直接传递途径。 因此,TGN后转运囊泡输送到正确膜域的保真度似乎由特定域的囊泡锁紧机械决定。
致谢 这项工作得到了美国国立卫生研究院对W.J.N.的资助(GM35527)和消化疾病中心对K.K.G.的试点/可行性研究资助。K.K.G.还得到了美国国立癌症研究所对斯坦福大学的癌症生物学资助(CA09302) 是美国国立卫生研究院博士后奖学金的获得者。
参考文献
Achler C,Filmer D,Merte C,Drenckhahn D。微管在顶端膜蛋白极化传递至肠上皮刷状缘中的作用。 细胞生物学杂志。 1989; 109:179–189. doi:10.1083/jcb.109.1.179。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Allan VJ,Kreis TE。 一种与高尔基体膜相关的微管结合蛋白。 细胞生物学杂志。 1986; 103:2229–2239. doi:10.1083/jcb.103.6.2229。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Bacallao R、Antony C、Dotti C、Karsenti E、Stelzer EHK、Simons K。Madin-Darby犬肾细胞在极化上皮形成过程中的亚细胞组织。 细胞生物学杂志。 1989; 109:2817–2832. doi:10.1083/jcb.109.6.2817。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Boll W、Partin JS、Katz AI、Caplan MJ、Jamieson JD。 极化上皮细胞中膜和分泌蛋白基底外侧靶向的不同途径。 美国国家科学院院刊1991; 88:8592–8596. doi:10.1073/pnas.88.19.8592。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
De Almeida JB,斯托JL。 微管的破坏改变了上皮细胞基底膜蛋白聚糖分泌的极性。 美国生理学杂志。 1991; 260:C691–700。 doi:10.1152/ajpcell.1991.261.1.C691。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Duden R、Griffiths G、Frank R、Argos P、Kreis TE。 Beta-COP是一种110 kd的蛋白质,与非甲氰菊酯包被的囊泡和高尔基复合体相关,与β-Adaptin具有同源性。 单元格。 1991; 64:649–665. doi:10.1016/0092-8674(91)90248-w。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Eilers U、Klumperman J、Hauri HP。 诺卡唑是一种微管活性药物,可干扰培养的肠上皮细胞(Caco-2)J细胞生物学中的顶端蛋白传递。 1989; 108:13–22. doi:10.1083/jcb.108.1.13。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Fath KR,Burgess DR.发育中的上皮细胞产生的高尔基衍生小泡结合肌动蛋白丝,并具有肌球蛋白-I作为细胞质定向的外周膜蛋白。 细胞生物学杂志。 1993; 120:117–127. doi:10.1083/jcb.120.1.117。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Gaush CR,Hard WL,Smith TF.已建立犬肾细胞系(MDCK)的特征描述,Proc-Soc-Exp-Biol Med.1966; 122:931–935. doi:10.3181/00379727-122-31293。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Gilbert T、Le Bivic A、Quaroni A、Rodriguez-Boulan E.微管组织及其参与Caco-2肠上皮细胞质膜蛋白的生物遗传途径。 细胞生物学杂志。 1991; 113:275–288. doi:10.1083/jcb.113.275。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Gottlieb TA、Baudry G、Rizzolo L、Colman A、Rindler M、Adesnik M、Sabatini DD。从极化MDCK细胞单层分泌内源性和外源性蛋白质。 美国国家科学院院刊,1986年; 83:2100–2104。 doi:10.1073/pnas.83.7.2100。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Hammerton RW、Krzeminski KA、Mays RW、Ryan TA、Wollner DA、Nelson WJ。 极化上皮细胞中Na+,K+-ATPase的细胞表面分布调控机制。 科学。 1991; 254:847–850. doi:10.1126/science.1658934。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Hinck L、Näthke IS、Papkoff J、Nelson WJ。 钙粘蛋白/连环蛋白复合物形成的动力学:新的蛋白质相互作用和复合物组装途径。 细胞生物学杂志。 1994; 125:1327–1340. doi:10.1083/jcb.125.6.1327。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Kondor-Koch C、Bravo R、Fuller SD、Cutler D、Garoff H。极化上皮细胞MDCK的顶端和基底外侧细胞表面都存在外显途径。 单元格。 1985; 43:297–306. doi:10.1016/0092-8674(85)90035-2。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Laemmli UK。T4噬菌体头部组装过程中结构蛋白的裂解。 自然。 1970; 227:683–685. doi:10.1038/227680a0。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Lafont F,Burkhardt J,Simons K。微管马达参与肾细胞的基底外侧和顶端转运。 自然。 1994; 372:801–803. doi:10.1038/372801a0。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Le Bivic A,Sambuy Y,Mostov K,Rodriguez-Boulan E.MDCK细胞内源性顶膜唾液糖蛋白和uvomorulin的载体靶向。 细胞生物学杂志。 1990; 110:1533–1539. doi:10.1083/jcb.110.5.1533。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Louvard D.培养的肾上皮细胞中,顶膜氨肽酶出现在细胞与细胞接触的部位。 美国国家科学院学报,1980年; 77:4132–4136. doi:10.1073/pnas.77.7.4132。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Marrs JA、Napolitano EW、Murphy-Erdosh C、Mays RW、Reichardt LF、Nelson WJ。 区分膜细胞骨架和钙粘蛋白介导的细胞-细胞粘附在极化上皮中产生不同Na+,K(+)-ATP酶分布中的作用。 细胞生物学杂志。 1993; 123:149–64. doi:10.1083/jcb.123.1.149。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Matter K、Bucher K、Hauri HP。 微管扰动阻碍了直接和间接心尖通路,但不影响肠上皮细胞质膜蛋白的分类(Caco-2)EMBO J.1990; 9点3163分-3170分。 doi:10.1002/j.1460-2075.1990.tb07514.x。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Matter K,Mellman I.细胞极性的机制:上皮细胞的分类和转运。 当前操作细胞生物学。 1994; 6:545–554. doi:10.1016/0955-0674(94)90075-2。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Mays RW、Beck KA、Nelson WJ。 极化上皮细胞中细胞骨架的组织和功能:蛋白质分选机制的一个组成部分。 当前操作细胞生物学。 1994; 6:16–24. doi:10.1016/0955-0674(94)90111-2。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Mays RW、Nelson WJ、Marrs JA。 上皮细胞极性的产生:蛋白质运输、膜细胞骨架和E-cadherin介导的细胞粘附的作用。 冷泉港交响乐团生物。 1995年a; 60:763–773. doi:10.1101/sqb.1995.060.01.082。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Mays RW、Siemers KA、Fritz BA、Lowe AW、van Meer G、Nelson WJ。 在MDCK上皮细胞中产生Na/K-ATP酶极性的机制层次。 细胞生物学杂志。 1995年b; 130:1105–1115. doi:10.1083/jcb.130.5.1105。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Musch A,Xu H,Shields D,Rodriguez-Boulan E.水疱性口炎病毒G蛋白到细胞表面的运输是极化和非极化细胞中的信号介导。 细胞生物学杂志。 1996; 133:543–558. doi:10.1083/jcb.133.3.543。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
尼尔森·WJ。 细胞骨架在极化上皮细胞膜交通中的作用。 精液细胞生物学。 1991; 2:375–385. [ 公共医学 ] [ 谷歌学者 ]
Nelson WJ、Veshnock PJ。 Madin-Darby犬肾上皮细胞极性发育期间膜骨架(fodrin)组织的动力学。 细胞生物学杂志。 1986; 103:1751–1765. doi:10.1083/jcb.103.5.1751。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Nelson WJ、Veshnock PJ。 Madin-Darby犬肾上皮细胞中细胞间接触对饲料蛋白(膜骨架)稳定性的调节。 细胞生物学杂志。 1987; 104:1527–1537. doi:10.1083/jcb.104.6.1527。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Ojakian GK,Schwimmer R.心尖细胞表面糖蛋白的极化分布是通过与madin-darby犬肾细胞的细胞骨架相互作用来维持的。 细胞生物学杂志。 1988; 107:2377–2378. doi:10.1083/jcb.107.6.2377。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Ojakian GK,Schwimmer R.抗微管药物抑制细胞内糖蛋白池极化插入Madin-Darby犬肾(MDCK)细胞的顶膜。 细胞科学杂志。 1992; 103:677–687. doi:10.1242/jcs.103.3.677。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Parczyk K、Haase W、Kondor Koch C。微管参与极化上皮细胞Madin Darby犬肾顶端细胞表面的蛋白质分泌。 生物化学杂志。 1989; 264:16837–16846. [ 公共医学 ] [ 谷歌学者 ]
Rindler MJ、Ivanov IE、Sabatini DD。微管作用药物导致流感血凝素非极化传递到极化Madin-Darby犬肾细胞的细胞表面。 细胞生物学杂志。 1987; 104:231–241. doi:10.1083/jcb.104.2.231。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
罗德里格斯-博兰E,尼尔森WJ。 极化上皮细胞表型的形态发生。 科学。 1989; 245:718–725. doi:10.1126/science.2672330。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Salas PJ、Misek DE、Vega Salas DE、Gundersen D、Cereijido M、Rodriguez-Boulan E.微管和肌动蛋白丝与上皮细胞表面极性的生物发生没有关键关系。 细胞生物学杂志。 1986; 102:1853–1867. doi:10.1083/jcb.102.5.1853。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Salas PJI、Vega Salas D、Hochman J、Rodriguez-Boulan E、Edidin M。在特定质膜结构域中的选择性锚定:在上皮细胞极性中的作用。 细胞生物学杂志。 1988; 107:2363–2376. doi:10.1083/jcb.107.6.2363。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Saucan L,Palade GE。秋水仙碱对体内大鼠肝细胞膜和分泌蛋白转运的差异作用:白蛋白的双极分泌。 肝病学。 1991; 15:714–721. doi:10.1002/hep.1840150427。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
Siemers KA、Wilson R、Mays RW、Ryan TA、Wollner DA、Nelson WJ。 极化上皮细胞中Na+K+-ATP酶的传递。 科学。 1993; 260:554–556. [ 谷歌学者 ]
Urban J,Parczyk K,Leutz A,Kayne M,Kondor-Koch C.极化上皮Madin-Darby犬肾细胞系中80-kD硫酸化糖蛋白复合物的组成性顶端分泌。 细胞生物学杂志。 1987; 105:2735–2743. doi:10.1083/jcb.105.6.2735。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Van der Sluijs P、Bennett MK、Antony C、Simons K、Kreis TE。 体外MDCK细胞胞外囊泡与微管的结合。 细胞科学杂志。 1990; 95:545–553. doi:10.1242/jcs.95.4.545。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
van Zeijl MJAH,Matlin K S.微管扰动以底物依赖的方式抑制极化Madin-Darby犬肾上皮细胞中顶端膜糖蛋白的细胞内转运。 Cell Regul公司。 1990; 1:921–936. doi:10.1091/mbc.11.221。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Vega-Salas DE、Salas PJ、Gundersen D、Rodriguez-Boulan E.上皮(Madin-Darby犬肾)细胞顶端的形成:顶端蛋白的极性独立于紧密连接,而基底侧标记的分离需要细胞间的相互作用。 细胞生物学杂志。 1987; 104:905–916. doi:10.1083/jcb.104.4.905。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Wandinger-Ness A、Bennett MK、Antony C、Simons K。独特的转运小泡介导质膜蛋白向MDCK细胞的顶端和基底外侧结构域的传递。 细胞生物学杂志。 1990; 111:987–1000. doi:10.1083/jcb.11.3.987。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Wollner DA、Krzeminski KA、Nelson WJ。 在上皮细胞极性发育过程中重塑膜蛋白的细胞表面分布。 细胞生物学杂志。 1992; 116:889–899. doi:10.1083/jcb.116.4.889。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
Yoshimori T,Keller P,Roth MG,Simons K。BHK和CHO细胞质膜的不同生物合成转运途径。 细胞生物学杂志。 1996; 133:247–256。 doi:10.1083/jcb.133.2.247。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]