摘要 尽管肿瘤免疫学对大多数癌症临床治疗的影响仍然可以忽略不计,但越来越多的证据表明,常规化疗后,抗癌免疫反应可能有助于癌症的控制。 因此,放射治疗和一些化疗药物,特别是蒽环类药物,可以诱导特异性免疫反应,导致免疫原性癌细胞死亡或免疫刺激性副作用。 这种抗癌免疫反应有助于消除残留的癌细胞(那些无法被化疗杀死的细胞)或将微转移维持在休眠阶段。 基于这些前提,在这篇综述中,我们讨论了这样一个问题:如何通过刺激抗癌免疫反应来改善传统疗法? 此外,我们还讨论了临床试验的基本原理,以评估并最终增加抗肿瘤免疫反应对肿瘤治疗管理的贡献。
不同分子病因的巨大多样性导致了一类威胁生命的疾病——癌症( 1 )-发达国家一半的居民在其一生中受到影响,三分之一的人因此死亡。 肿瘤细胞的细胞生物学变化受表观遗传和遗传重编程的制约,基因组不稳定性是肿瘤发生和肿瘤进展的基本特征。 癌细胞的这种表观遗传修饰通常伴随着“危险信号”的释放,以及异位或突变蛋白的表达。 因此,肿瘤细胞的抗原特性可以被先天免疫系统和同源免疫系统感知。
正如Hanahan和Weinberg最初定义的那样,致瘤过程源于六个标志性标准:即生长信号自足、生长抑制信号抵抗、细胞凋亡抵抗、无限生长潜能、持续血管生成和转移潜能( 1 ). 癌症的第七个潜在标志,避免免疫监视( 2 )使肿瘤细胞逃避抗癌免疫反应或主动抑制它们( 2 , 三 ),已受到严密审查。 最近的几篇综述探讨了免疫监视是否以及在多大程度上控制和影响人类癌症的发展的问题( 4 – 6 ). 越来越多的证据表明,肿瘤在免疫缺陷患者中发生得更频繁,例如在移植受者中( 7 ). 这强烈表明,在小鼠模型中获得的支持免疫监视在肿瘤发生和肿瘤进展中发挥重要作用的大量证据中,至少有一部分可以推断到人类系统。
我们对癌症的分子和细胞病因学的不断扩大的理解尚未伴随着治疗结果的平行改善。 本综述的目的是提出一系列相关问题:抗癌化疗或放疗的成功(或失败)是否取决于免疫系统的贡献? 如果是这样,是否有可能通过刺激抗癌免疫反应来增强传统疗法? 我们如何最好地设计临床试验,以探讨(并最终增加)抗肿瘤免疫反应对肿瘤疾病治疗管理的贡献?
癌症与免疫系统的关系:快速指南 如前所述( 4 ),免疫系统可以阻止肿瘤生长。 因此,在切除T细胞和/或注射抗IFN-γ抗体后,小鼠的隐性癌症变得明显,这表明适应性免疫反应可以在平衡状态下控制癌症( 6 ). 然而,癌细胞通过免疫选择(选择非免疫原性肿瘤细胞变体,也称为免疫编辑)或免疫抑制(主动抑制免疫反应)逃避先天性和适应性免疫反应(免疫监视)。
虽然免疫编辑的概念已经在老鼠身上发展起来,但有证据表明,这种想法也可能适用于人类。 人类中的不稳定微卫星肿瘤(与染色体不稳定的肿瘤相比,可能携带更多的新抗原)明显受CTL浸润,且预后良好( 8 – 10 ). T、NK和NKT细胞浸润肿瘤是多种人类肿瘤(包括黑色素瘤)预后改善的标志( 11 ),冒号( 12 )和卵巢癌( 13 ). 在基底细胞癌患者中发现了自发的肿瘤退化和大量淋巴细胞浸润( 14 )、默克尔细胞癌( 15 )和肺癌( 16 ). 高水平的抗肿瘤抑制蛋白p53抗体对卵巢有积极的预后价值( 17 )和胃癌( 18 ). 在早期乳腺癌患者中,对粘蛋白的自然体液免疫反应对生存率有有利影响。 事实上,粘蛋白MUC1是一种被大多数人类癌症异常过表达的异二聚体跨膜糖蛋白,是一种T细胞识别的肿瘤抗原,为乳腺癌、结肠癌、胰腺癌、卵巢癌和肺癌等不同肿瘤所共有,由于其在正常细胞和肿瘤细胞中的糖基化差异,可能具有肿瘤特异性( 19 ).
一个重要的问题是传统抗癌化疗对肿瘤和免疫系统之间关系的影响。 在肿瘤逃逸阶段进行的治疗不仅影响肿瘤,还调节肿瘤与免疫系统之间的关系。 因此,化疗可以通过简单地减少肿瘤的质量(消除肿瘤)来降低其免疫抑制特性。 作为原则的证明,即使在患有转移性乳腺癌的动物中,单纯的手术切除原发肿瘤(机械去鳞癌)也可以逆转肿瘤诱导的免疫耐受,恢复抗体和细胞介导的免疫反应( 20 ). 通过加强对化疗耐药肿瘤细胞的选择和诱导额外的突变(化疗通常涉及诱变剂),治疗可以诱导新的肿瘤抗原的表达。 化疗可导致免疫原性癌细胞应激或死亡,从而介导某种癌症疫苗接种效应(如下所述)。 此外,化疗可以通过对免疫效应物或调节机制的直接作用,或通过引起淋巴细胞减少症,然后引起可能在抗癌反应中特别活跃的免疫效应物的稳态增殖,间接刺激免疫系统。 这些效应的结合可能会将肿瘤和免疫系统之间的关系从最新阶段(逃逸)“重置”到之前的状态(消除或平衡)。
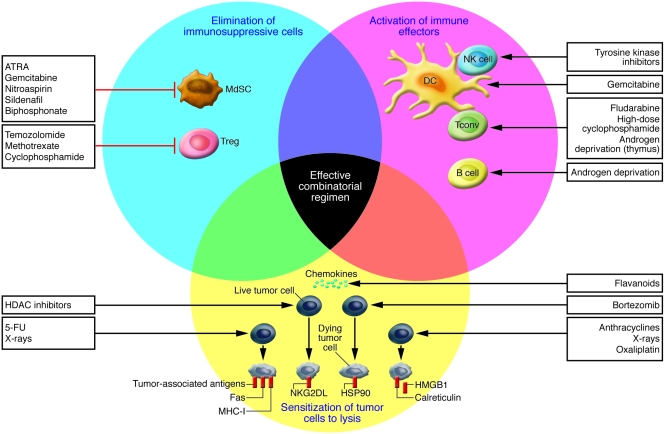
抗癌药物的免疫刺激副作用 尽管细胞毒性抗癌药物以及所谓的靶向药物主要通过对癌细胞的直接作用发挥作用,但其中许多药物对免疫系统具有额外的作用,这可能有助于提高其治疗效果(图 1 ).
图1。 传统抗癌治疗对免疫反应影响的机制。
抗癌疗法可以抑制肿瘤诱导的免疫耐受的抑制机制(蓝色圆圈),增强T和/或B细胞反应(粉色圆圈),或以使肿瘤细胞变得免疫原性和对裂解敏感的方式应激肿瘤细胞(黄色圆圈)。 驱动这些效应的主要药物也显示出来。 低剂量环磷酰胺、吉西他滨等- 反式 -维甲酸(ATRA)作用于免疫抑制细胞,如Tregs或髓样抑制细胞(MdSC),以促进传统效应物(Tconv)对肿瘤的攻击。 硝基阿司匹林也可以实现对MdSCs的药理学抑制( 96 ),西地那非( 97 )和二膦酸盐( 98 ). 雄激素缺乏会增强T细胞和B细胞的反应。 导致淋巴衰竭的策略允许建立记忆效应T细胞,有效地长期保护肿瘤细胞。 酪氨酸激酶抑制剂增强DC/NK细胞的串扰。 蛋白酶体抑制剂硼替佐米诱导骨髓瘤细胞表面分子伴侣蛋白HSP90的表达,从而导致DC摄取、抗原处理和DC成熟。 蒽环类、奥沙利铂和辐射促进肿瘤细胞CRT的肿瘤膜表达和HMGB1的释放,这分别是DC介导的垂死肿瘤吞噬和肿瘤抗原向T细胞交叉呈递所需的事件。 组蛋白去乙酰化酶抑制剂(HDAC)促进NKG2D配体(NKG2DL)的表达,使肿瘤细胞对NK细胞介导的溶解敏感。 暴露于x射线下的肿瘤细胞表达更多的MHC I类分子、肿瘤抗原和Fas,有利于CTL攻击。 类黄酮介导的趋化因子的产生有助于吸引免疫效应物进入肿瘤床。 理想情况下,化疗药物的适当组合可以实现这三种类型的所有有益效果。
短暂性淋巴细胞减少(血淋巴细胞水平异常低)可能会激活体内平衡机制,最终刺激肿瘤特异性效应T细胞。 因此,淋巴细胞减少症的治疗诱导在过继细胞移植(ACT)治疗(包括从内源性肿瘤浸润淋巴细胞体外生成肿瘤反应性淋巴细胞,并在重新注入肿瘤宿主前激活和扩增)的背景下引起了极大的兴趣 接种黑色素瘤疫苗( 21 ). 动物研究表明,淋巴消融增强了过继转移肿瘤特异性CD8的有效性 + T细胞( 22 ). 这些实验数据已经在35名对传统治疗无效的转移性黑色素瘤患者的临床试验中进行了测试。 ACT与肿瘤浸润淋巴细胞(TIL)联合使用后,采用高度消耗淋巴的预处理方案,导致51%的客观应答率与持续性克隆性淋巴细胞增多症和/或抗黑素细胞自身免疫相关( 23 ). 在小鼠中,淋巴衰竭可以与疫苗接种策略相结合,以促进肿瘤抗原特异性中央记忆T细胞的分化( 24 – 27 ). 这些发现的临床相关性已在骨髓瘤随机临床试验中得到验证( 28 ). 接种7价肺炎球菌结合疫苗(PCV;Prevnar)后,首次收集患者体内激发的T细胞。 随后接受大剂量化疗和自体干细胞移植的患者,以及这些体内-激发和体外-扩增T细胞的输注,随后进行强化免疫,在移植后的一个月内,患者的临床相关抗菌免疫得到了强有力的重建( 28 ). IL-15还可以在ACT治疗癌症或HIV后消除T细胞疲劳( 29 ),抗CD40( 30 ),或程序性细胞死亡1(PD-1)阻断( 31 ). 这些发现表明,经过一些额外的改进,化疗或辐射诱导的淋巴衰竭,再加上额外的操作,如ACT和免疫药理学干预,可能会实现抗肿瘤免疫反应。
荷尔蒙疗法,即荷尔蒙操作的使用,是治疗乳腺癌和前列腺癌的临床设备的一部分。 本文综述了雄激素对淋巴细胞发育和活化的影响( 32 ). 实验数据表明,雄激素缺乏增加了胸腺输出的原始T细胞的数量,因此可能有助于拓宽T细胞免疫的储备,导致有效的抗肿瘤免疫反应,并打破肿瘤诱导的耐受性( 33 , 34 ). 此外,雄激素缺乏增加了新生成的IgM的产生 + 来自骨髓的原始B细胞( 35 ). 前列腺癌患者的雄激素消融可能通过增加原始T细胞库来激活对某些前列腺癌抗原的免疫反应(如TCR重排切除环[TREC]分析所示; TREC是从T细胞生殖系DNA中切下的稳定DNA环,以便在T细胞发育早期形成TCR,在胸腺移植物中以高浓度存在),减少和/或稀释Tregs的数量,并有利于T细胞同时浸润到肿瘤床( 36 , 37 ). 一项对73名非转移性前列腺癌患者和50名对照进行的研究表明,新辅助激素和放射治疗(但不是根治性前列腺切除术)可以引起肿瘤特异性自身抗体反应( 38 ). 体液反应出现得早,在大多数情况下持续时间长,提示通过免疫治疗控制B细胞反应。
一些药物(尤其是环磷酰胺,还有氟达拉滨、吉西他滨、奥沙利铂和5-氟尿嘧啶[5-FU])至少可以部分耗尽或暂时灭活肿瘤保护性Tregs( 39 – 41 ). 一些临床试验联合低剂量环磷酰胺和抗肿瘤疫苗治疗转移性黑色素瘤,但没有任何明确结果,可能是由于缺乏统计能力( 42 – 46 ). 在对42名转移性乳腺癌患者进行的一项小型随机研究中,环磷酰胺与一种由与锁孔帽贝血蓝蛋白(KLH)相连的合成唾液酸-Tn表位和佐剂组成的疫苗联合使用。 KLH是从海洋软体动物锁孔帽贝中分离出来的一种天然蛋白质,与弱抗原一起用作载体蛋白,以增强对半抗原、自身抗原和独特型蛋白的免疫反应。 据报道,中位生存期从12个月增加到20个月,具有统计学意义( 47 ). 在肾细胞癌患者中观察到类似的趋势,这些患者接受了用肿瘤裂解物和KLH脉冲处理的异基因成熟树突状细胞免疫,并且也接受了300 mg/m 2 每个月接种前4天和3天静脉注射环磷酰胺( 48 ). 在另一项研究中,10名晚期癌症患者每隔一周接受1次每日剂量的100毫克环磷酰胺治疗,持续4周( 49 ). 这种“节拍性”(即每天口服)环磷酰胺治疗抑制了Treg的抑制功能,恢复了效应T细胞的增殖能力以及NK细胞的细胞毒性( 49 , 50 ).
许多其他抗癌药物也具有免疫刺激作用,这已在临床上得到证实。 例如,据报道,吉西他滨可以提高产生IFN-γ的T细胞和/或CD69的频率 + 胰腺癌患者的活化细胞( 51 ). 在一项I期试验中,吉西他滨在非小细胞肺癌中诱导细胞免疫反应( 52 ). 一项临床试验检测了吉西他滨和细胞因子(GM-CSF和低剂量IL-2)对42名晚期结直肠癌患者的联合作用。 客观应答率和进展时间令人鼓舞,并与应答者肿瘤特异性CTL前体频率增加相关( 53 )促使启动第三阶段试验。 另一个例子是甲磺酸伊马替尼(IM;也称为STI571和Gleevec)的研究,这是酪氨酸激酶BCR-ABL、PDGFR和KIT的抑制剂。 一些胃肠道间质瘤(GISTs)患者对IM有反应,这些患者没有c-KIT突变(因此缺乏IM靶点)( 54 )提示IM具有间接抗肿瘤作用。 事实上,在一小部分GIST患者中,IM导致NK活性增加。 IM诱导NK细胞活化是一个积极的预后参数( 54 )动物实验表明,免疫刺激可能有助于IM对患者的治疗效果( 55 ).
免疫原性癌细胞应激与死亡 转化细胞必须克服肿瘤发生的内在(细胞自主)和外在(免疫介导)障碍。 抗转化的一个重要内在屏障包括致癌应激后DNA损伤反应的激活,导致共济失调毛细血管扩张症突变(ATM)、检查点激酶-1(CHK1)的激活,最后是p53依赖性凋亡( 56 )或衰老( 57 ). 因此,癌前病变和原位癌通常表现为ATM、CHK1和p53的激活,而晚期癌症抑制或失去这种DNA损伤反应。 抑制肿瘤生长的外部屏障包括先天和同源免疫系统中的细胞清除转化细胞。 有趣的是,这些屏障可以用分子术语联系起来( 三 , 58 ). 因此,DNA损伤反应以ATM和CHK1依赖(但p53依赖)的方式诱导肿瘤细胞上NK细胞组2D(NKG2D)配体的表达( 59 ). NKG2D是一种参与肿瘤免疫监测的激活受体,在NK、NKT和γδT细胞上表达,在小鼠和/或活化的人CD8中表达 + T细胞。 因此,NKG2D配体在转化细胞表面的表达有望在肿瘤监测中发挥重要作用(图 1 ).
虽然在DNA损伤的细胞中NKG2D配体的表达并不需要p53( 59 )最近的一项研究强调了p53诱导的肿瘤细胞衰老与先天免疫系统之间的重要合作( 57 ). 在已确诊的肝癌中,p53功能的恢复导致肿瘤退化,但只有在小鼠具有完整的免疫系统时。 因此,p53的重新激活导致肝癌的缓解,这一效应在NK细胞和巨噬细胞消融后消失( 57 ). 这些例子说明了在早期肿瘤发生过程中被激活的分子(例如ATM、CHK1、p53)如何提醒免疫系统介导抗肿瘤反应。 由于使用DNA损伤剂进行化疗通常会激活ATM、CHK1和p53,因此这些药物也会引起ATM、CHK1和p53依赖性免疫效应,这似乎是合理的,但仍有待证明。
化疗药物和辐射可以通过增强MHCⅠ类表达来提高肿瘤细胞的免疫原性( 60 )从而增加了它们对CTL的脆弱性。 同样,一些化疗药物(如基因毒性药物和组蛋白去乙酰化酶抑制剂)增加NKG2D配体的表达( 59 , 61 )从而促进NKG2D表达淋巴细胞(包括NK细胞、NKT细胞和CTL)对肿瘤细胞的裂解。 放疗或化疗造成的DNA损伤的另一个常见影响是死亡受体(尤其是Fas/CD95和TNF-相关凋亡诱导配体[TRAIL]受体)表达的增加( 62 ),能够通过Fas/CD95配体和TRAIL阳性免疫效应器分解肿瘤细胞(图 1 ).
肿瘤细胞的死亡通常是通过凋亡或坏死发生的。 虽然有目的论论据表明,凋亡必须是非免疫原性的,甚至是耐受性的(因为生理性细胞死亡是通过凋亡发生的,但不会导致自身免疫),尽管坏死(通常是病理性的)被认为是促炎性的, 细胞凋亡等于非免疫原性,坏死等于免疫原性的理论方程经不起实验验证。 相反,凋亡在生化方面似乎是不均匀的,这意味着各种途径可以导致细胞死亡并诱导刺激特异性变化。 蒽环类化合物、奥沙利铂和电离辐射具有诱导免疫原性细胞死亡的非凡能力,而绝大多数化疗药物都会诱导非免疫源性细胞死亡( 63 – 66 ). 蒽环类化合物、奥沙利铂和电离辐射也具有诱导伴侣钙网蛋白(CRT)从内质网腔(endo-CRT)到质膜(exto-CRT( 64 , 65 , 67 ). 然后Ecto-CRT促进DC吞噬肿瘤细胞,但不诱导DC成熟。 CRT的中和或敲除消除了肿瘤细胞死亡的免疫原性,而外源性供应重组CRT可以恢复非免疫原性细胞死亡的自身免疫原性( 64 , 65 , 67 )(图 1 ).
另一种伴侣蛋白HSP90最近被报道参与蛋白酶体抑制剂硼替佐米诱导的人类骨髓瘤细胞死亡的免疫原性( 68 ). 在这个体外模型中,暴露于硼替佐米后,HSP90暴露在骨髓瘤细胞的质膜表面,并诱导DC的表型成熟(图 1 ). 另一个作用于DC的因素是高迁移率族蛋白1(HMGB1),这是一种染色质结合蛋白,在蒽环类、草酸铂和电离辐射诱导的细胞死亡后期从细胞中释放出来。 HMGB1随后与DC表面的TLR4相互作用,并影响来自死亡肿瘤细胞的吞噬抗原的细胞内命运。 HMGB1连接TLR4可抑制吞噬体(包含抗原货物)与溶酶体的融合,从而使抗原向抗原提呈室流动( 66 ). HMGB1的中和或敲除消除了死亡肿瘤细胞诱导抗癌免疫反应的能力,强调了其对肿瘤免疫原性的贡献( 66 ). 上述示例说明,依赖于细胞死亡诱导剂,肿瘤细胞可以暴露或释放影响DC(例如CRT)对其摄取、DC成熟(例如HSP90)或DC抗原提呈(例如HMGB1)的因子。
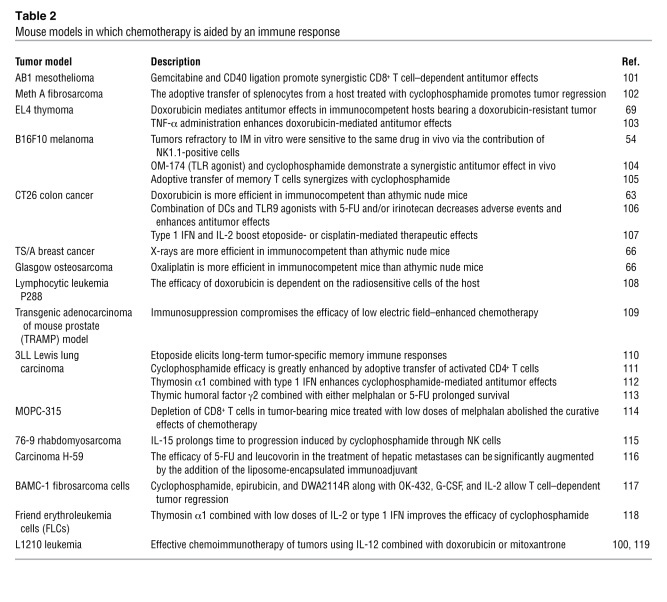
治疗期间免疫反应的分子和/或流行病学证据 开创性工作强调了T细胞对细胞毒药物介导的抗肿瘤作用的贡献(表 1 和 2 ) ( 69 ). 在体外对蒽环类药物阿霉素具有相对耐药性的EL4胸腺瘤细胞克隆在植入具有免疫活性的C57BL/6小鼠中时产生阿霉素敏感性肿瘤。 然而,这种意想不到的治疗效果似乎依赖于脾细胞,这表明免疫可能是蒽环类药物介导的抗肿瘤作用所不可或缺的( 69 ). 虽然实验数据并不总是支持这一论点(表 1 ),其他研究人员在其他几种癌症中也获得了类似的结果(表 2 ),前提是给予免疫原性化学疗法(例如蒽环类或奥沙利铂)。 因此,用奥沙利铂治疗的EL4胸腺瘤、格拉斯哥骨肉瘤和CT26结肠癌,以及用蒽环类药物治疗的CT26结直肠癌和MCA205纤维肉瘤,当宿主具有免疫功能时,表现出比免疫缺陷时更好的治疗反应 数值/数值 老鼠) ( 64 , 66 , 67 , 70 ). 同样,CD4的耗竭 + 或CD8 + 注射特异性单克隆抗体的T细胞损害了阿霉素对CT26肿瘤的治疗效果( 64 ). TS/A是一种来源于BALB/c小鼠自发性乳腺癌的细胞系,与无胸腺宿主相比,它对免疫活性的局部放射治疗也有更好的反应( 66 ). 总之,这些结果表明化疗和放疗的疗效受免疫系统的影响。
表1 .
表2 .
上述结果表明,蒽环类、草酸铂或电离辐射诱导免疫原性肿瘤细胞死亡可刺激免疫反应,有助于抑制肿瘤。 如果这一推测是正确的,人们可以预计,肿瘤衍生蛋白,如CRT和HMGB1(决定肿瘤细胞死亡的免疫原性)及其受体在抗原呈递细胞上的存在,将是完全治疗成功所必需的。 因此,TLR4及其下游效应器MyD88的敲除(但不包括TIR结构域的敲除,该结构域含有介导干扰素-β[TRIF]的适配器,该适配器对TLR的激活作出反应,而TLR的活化介导的信号级联与MyD88介导的不同) 降低CT26结肠癌、TS/A乳腺癌、EL4胸腺瘤或格拉斯哥骨肉瘤小鼠免疫原性化疗的疗效( 66 ).
在欧洲混合血统的个体中,TLR4存在序列多态性(896A→G,Asp299Gly,RefSNP识别号rs4986790),等位基因频率约为6%( 71 , 72 )防止HMGB1以主要的负向方式与TLR4结合( 66 , 70 ). 一项临床研究表明,携带Asp299Gly TLR4等位基因的乳腺癌患者与表现出正常TLR4等位基因的患者在任何经典预后因素上都没有差异。 然而,局部放疗和全身蒽环类化疗后无转移生存率的Kaplan-Meier估计表明,Asp299Gly TLR4等位基因(但不是TLR4突变,RefSNP识别号rs1927911)是早期复发的独立预测因素( 66 , 70 ). 在转移性肾癌中,IL-4启动子的多态性强烈影响预后( 73 ).
许多调查人员使用这个术语 免疫化疗 描述识别肿瘤抗原的单克隆抗体的治疗性滴注。 值得注意的是,免疫化疗对利妥昔单抗(抗CD20)治疗的滤泡性淋巴瘤的疗效在一定程度上取决于Fc受体IIIA基因型决定的抗体依赖性细胞毒性的疗效( 74 , 75 )肿瘤相关巨噬细胞的含量( 76 ).
由于技术原因,很少有研究涉及化疗前后肿瘤特异性效应器或记忆性T细胞或抗体滴度的频率。 在患有急性髓细胞白血病(AML)的婴儿中,化疗后抗白血病前体的出现与维持血液学缓解相关( 77 ). 最近,一项动态免疫监测研究报告了白血病特异性、产生TNF-α的CD4的存在 + IM成功治疗慢性粒细胞白血病患者的T细胞( 78 ). 在大多数患者中,自发和诱导的T细胞反应与血液学和细胞遗传学反应相关。 有趣的是,抗磷脂抗体滴度与维甲酸治疗早幼粒细胞白血病后延长生存期相关( 79 , 80 ). Galanis等人研究了神经元自身抗体在小细胞肺癌患者中的预后价值。 尽管副肿瘤自身抗体的滴度与发病时的小范围疾病相关,但以顺铂为基础的化疗导致患者免疫功能受损,并且不能根据抗体滴度的升高预测进展时间( 81 ).
未来的研究应解决以下问题:在哪些癌症中,免疫原性化学疗法或放射疗法诱导特异性抗肿瘤免疫反应对预后有影响?
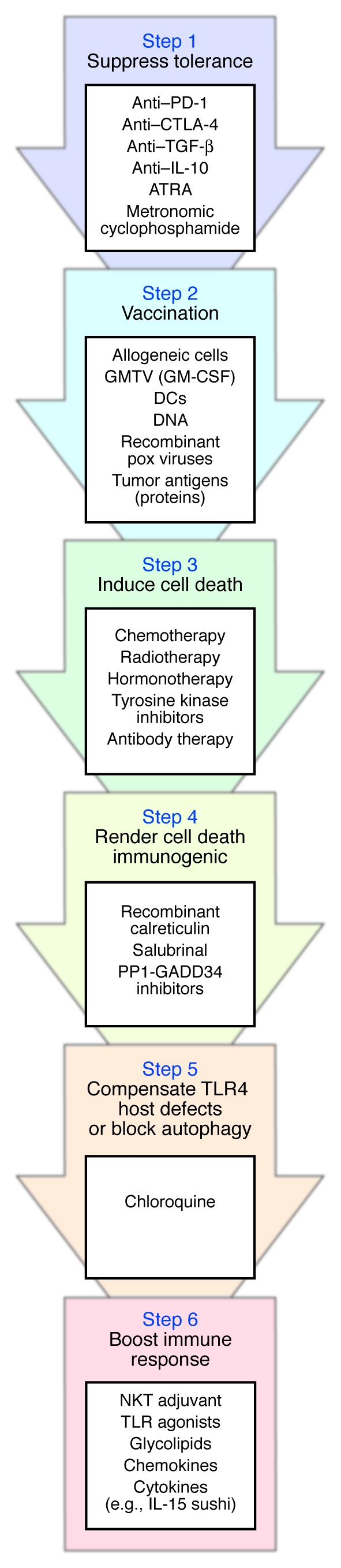
免疫化学疗法 基于上述前提,肿瘤学家和免疫治疗专家可能会讨论优化当前抗癌方法的机会。 这种优化可能源于图中所示的顺序策略 2 关联:(a)耐受性途径的抑制物; (b) 用疫苗启动原始T细胞和b细胞; (c) 细胞毒药物诱导细胞死亡; (d) 使非免疫原性细胞死亡具有免疫原性的药物; (e) 氯喹(用于对抗TLR4的宿主缺陷或阻断自噬和多药耐药性); (f) 以及使用NK、NKT或DC佐剂(例如TLR激动剂、糖脂、细胞因子、趋化因子)维持免疫效应器。
图2。 成功的癌症免疫治疗所需的步骤。
癌症患者的免疫系统受到肿瘤诱导耐受的影响,在用肿瘤疫苗诱导主动免疫反应之前,应先缓解(步骤1)。 一些证据表明,预先接种(步骤2)有利于化疗药物的抗肿瘤作用(步骤3)。 化疗或放疗引发的细胞死亡(步骤3)应通过添加增强肿瘤细胞膜上钙网蛋白表达的化合物使其具有免疫原性(步骤4)。 为了克服假定的TLR4宿主缺陷,该缺陷可能会损害正在形成的免疫反应,建议使用氯喹(步骤5)。 最后,应给予免疫佐剂以维持和增强随后的抗肿瘤免疫反应(步骤6)。 列出了每个步骤中的潜在中介体。 转基因肿瘤疫苗; PP1-GADD34,蛋白磷酸酶1与GADD34复合; IL-15寿司,可溶性IL-15受体α的寿司结构域( 99 ).
由于宿主和肿瘤反应的动力学可能是治疗反应的关键决定因素,未来的研究应侧重于联合治疗并确定化学免疫治疗的最佳时间表。 此外,这种组合虽然可能有效,但也可能充满显著的毒性(即感染性疾病或自身免疫,正如使用淋巴衰竭或抗CTLA4抗体所观察到的那样)。 免疫化疗的I期试验可能有助于确定毒性和达到免疫反应的剂量,但需要进行大规模的随机研究来评估此类治疗组合的最佳方案。
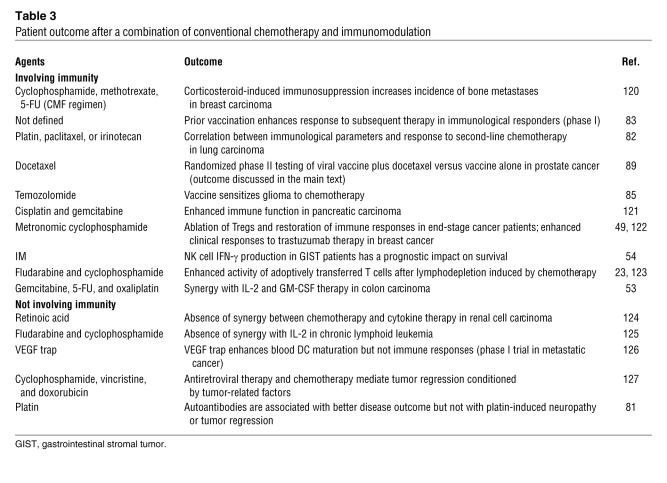
迄今为止,很少有临床研究将常规化疗与抗癌疫苗接种和/或免疫刺激方案相结合(表 三 ). 特别是,对细胞毒疗法和肿瘤疫苗的使用顺序没有系统或随机的评估。 在一项试验中,29名对一线铂类治疗耐药的终末期非小细胞肺癌患者被纳入了一项采用疫苗接种方案的研究,该方案涉及感染了编码p53的腺病毒载体的自体树突状细胞( 82 ). 由于29例患者中有23例肿瘤进展,因此建议将紫杉醇或卡铂作为第二行化疗。 这种二线化疗的有效率为61.5%,接种疫苗后一年存活率高达38%。 已知历史对照组对二线化疗的客观反应率为6%-16%,存活时间超过一年的不到20%。 可以观察到对p53的免疫反应与临床结果之间的直接正相关。 只有30%对疫苗接种没有p53特异性反应的患者对二线化疗有反应,而75%的p53细胞免疫应答者在疫苗接种后对化疗有客观的临床反应( P(P) = 0.08) ( 82 ).
表3 .
在另一项研究中,17名患有各种晚期肿瘤的患者接受了一种封装DNA疫苗,该疫苗编码几乎所有人类肿瘤都表达的致癌物激活物细胞色素P450 1B1。 虽然11名未开发出抗CYP1B1特异性T细胞的患者中有10名对补救治疗无效,但6名对CYP1B1产生免疫的患者中,有5名在一年多的时间内对补救方案表现出明显的反应( 83 ).
回顾性研究基于肽或裂解物负载DC的疫苗接种对常规治疗(开颅术、立体定向放射外科、放射治疗、替莫唑胺单独治疗或与亚硝基脲联合治疗)抗胶质母细胞瘤疗效的影响也得出了类似结论( 84 , 85 ). 比较了12名接受酪氨酸酶相关蛋白2(TRP-2)疫苗治疗的患者、13名接受化疗治疗的患者以及13名接受TRP-2疫苗和化疗联合治疗的胶质母细胞瘤患者的进展率和总生存率。 结果表明,与个体化治疗相比,化疗与先前的治疗性疫苗接种可以协同减缓胶质母细胞瘤的进展,并显著延长患者的生存期。 在某些情况下,作者可以在接种疫苗前后建立胶质母细胞瘤细胞系,与原发性肿瘤细胞相比,免疫选择的肿瘤细胞对替莫唑胺和卡铂的敏感性增加。 这些数据表明,TRP-2的免疫靶向性增加了对细胞死亡诱导物的敏感性( 86 ).
鉴于睾酮在调节B细胞和T细胞免疫反应中发挥作用的证据,将雄激素缺乏与前列腺癌疫苗治疗相结合是有充分理由的,这也得到了一些实验数据的进一步支持( 87 ). 经Aragon-Ching等人审查( 32 ),一期和二期试验表明,雄激素消融可以增强DC、异基因前列腺癌细胞裂解物或分泌肿瘤细胞疫苗的GM-CSF引发的免疫反应( 88 ). Arlen等人( 89 )他们首先进行了一项随机研究,评估了单独疫苗与联合疫苗的使用情况以及每周给予多西他赛和类固醇的情况,并对28例转移性雄激素抵抗前列腺癌患者的免疫反应进行了监测。 首先,他们展示了一种疫苗(混合表达前列腺特异性抗原的重组痘苗病毒[PSA]) 与单独接种疫苗相比,在不影响患者产生肿瘤相关抗原特异性T细胞反应的能力的情况下,可以每周服用多西紫杉醇和地塞米松,或B7.1,然后连续增强鸡痘病毒-PSA。 他们还评估了联合治疗、单独接种疫苗和接种后进展后化疗的临床反应。 虽然联合用药组的无进展生存期与历史对照组相似(中位数为3.2个月vs 3.7个月),但仅使用疫苗治疗疾病进展后接受多西紫杉醇治疗的患者的无进展存活期增加(6.1个月vs.3.7个月中)。 接种疫苗后改用多西紫杉醇的患者继续保持PSA特异性T细胞反应,这与PSA血清水平下降相对应。 Noguchi等人在一份报告中观察到了类似的趋势,其中低剂量的雌激素(氮芥)与HLA-A24限制性肽疫苗联合用于前列腺癌。 在13例患者中,联合治疗与增强CTL反应、肽特异性IgG反应和降低血清PSA水平相关( 90 ).
在一项针对17名结直肠癌患者的研究中,评估了以5-FU为基础的化疗与癌胚抗原衍生肽(CEA衍生肽)作为佐剂相结合的可行性和安全性( 91 ). 17名患者中有8名出现CEA-特异性CTL反应,17名中有6名出现客观反应,这一比率与单纯化疗的历史对照组相似( 91 ). 一项II期试验招募了32名接受模拟CEA抗原的抗独特型抗体治疗的患者,其中14名患者额外接受了基于5-FU的治疗方案。 所有患者均出现CEA特异性体液和细胞免疫反应( 92 ). 以5-FU为基础的治疗方案是局部结肠癌患者淋巴结受累的标准治疗方案,不会影响免疫反应。 这些数据保证了对切除的结肠癌患者进行III期试验。
癌症免疫学中的开放性问题 许多临床肿瘤学家怀疑免疫参数对肿瘤实际管理的总体影响。 如何设计临床研究以提供更充分的证据证明癌症免疫学的重要性?
开展大规模流行病学研究,将癌症的发病率和病程(包括治疗失败)与免疫缺陷的基因型和表型标记物联系起来,这一点很重要。 如上所述,编码TLR4和细胞因子的基因的多态性可能与治疗结果相关,但更大和更系统的研究(如全基因组SNP相关性)在这一领域将很重要。 将细胞内感染因子(包括病毒、李氏杆菌、结核病、支原体等)的易感性与癌症化疗反应不良联系起来也是很有意思的。 此外,应对黑色素瘤疫苗接种研究进行详尽的荟萃分析。 这种荟萃分析应该解决疫苗接种对后期化疗反应的假定积极影响。
肿瘤特异性基因表达或蛋白质组特征对预后的影响应通过研究先前存在的免疫反应标记物来重新解释。 诊断时滤泡性淋巴瘤的分子分析表明,预测生存率的两个基因表达特征包括非恶性肿瘤浸润细胞表达的基因,最有可能是髓细胞和T细胞。 浸润免疫细胞的性质是癌症的主要特征,可以预测生存率( 93 ). 重要的是进行前瞻性试验,在这些试验中,化疗前后进行的一系列肿瘤活检评估局部免疫反应的迹象,作为推测的预后因素。 如果抗癌免疫反应决定了长期治疗的成功,那么抗原提呈的局部征象(即在伪淋巴结构和环境中存在树突状细胞)或T和NK细胞反应(存在效应记忆性T细胞,优先是Th1型,其数量应超过Tregs) 与有利的反应相关。 我们最近的数据表明,新辅助化疗的病理完全反应与治疗诱导的高CD8之间存在相关性,这一工作假设得到了支持 + 56例局部晚期乳腺癌患者的效应T淋巴细胞和低Treg浸润水平( 94 ).
大规模化疗的免疫抑制副作用也应重新评估。 虽然一个周期的淋巴滤过可能会由于体内稳定的T细胞补充而构成治疗优势,但重复的淋巴滤除周期可能会破坏肿瘤特异性免疫效应器的不断增加的数量。 例如,在乳腺癌中,应将弱剂量、重复剂量蒽环类药物(每周,理想情况下不使用糖皮质激素)的治疗与通常的治疗方案进行比较,在通常的治疗方案中,每三周给予一次高剂量的蒽环类药物(通常伴有高剂量的糖皮质激素,以减少化疗相关的不适) 同时监测肿瘤大小(通过PET/CT)和抗肿瘤免疫反应。
同样,考虑到化疗应该引起免疫反应的观点,重新设计不同癌症的治疗管理可能很重要。 因此,小肿瘤(如通过常规放射检查发现的早期乳腺癌)的新辅助化疗(相对于辅助化疗)将提供更多的肿瘤抗原可用于启动T细胞,而高剂量耐受性不应构成问题。 同样,为了疾病分期的目的,保存前哨淋巴结而不是将其系统性切除也很重要。 事实上,前哨淋巴结构成抗原启动的特殊部位,其中活性DC(表达DC-LAMP,一种仅在成熟DC中表达的蛋白)的存在构成阳性预后标记,至少在黑色素瘤中是如此( 95 ).
未来的研究还可能包括临床试验,试图通过服用氯喹来纠正具有Asp299Gly TLR4等位基因的乳腺癌患者化疗反应缺陷。 口服氯喹是一种广泛使用的抗疟药,其毒性可接受。 在缺乏TLR4的小鼠中,氯喹恢复了对奥沙利铂的化疗反应,可能是因为它改善了树突状细胞缺乏的抗原提呈。 在TLR4阴性树突状细胞中,含有肿瘤抗原的吞噬物被溶酶体迅速破坏,而氯喹对溶酶体的抑制可恢复抗原提呈。 类似地,氯喹可以重建体外携带Asp299Gly TLR4等位基因患者的DC对死亡肿瘤细胞抗原的缺陷呈现 ( 66 ).
从生物技术的角度来看,药物筛选方法可用于研究化合物促进CRT易位到反应细胞系(根据其对蒽环类CRT暴露的反应选择)的细胞表面的能力。 这种筛选可以根据诱导免疫原性细胞死亡的能力来选择可用药的化合物(图 1 ).
总之,我们预计临床试验将证实评估和诱导抗癌免疫反应用于预后和治疗目的的潜力,前提是知识产权、许可、, 和责任并不代表工业合作伙伴接受赞助和/或推出联合疗法的重大障碍。 我们共同希望,不断扩大的免疫刺激药典,加上日益成熟的抗癌疫苗接种技术,最终将使我们能够随意触发杀瘤免疫反应。
致谢 作者得到了法律国家癌症控制基金(L.Zitvogel、L.Apetoh和G.Kroemer)、康复医学基金会(L.Apertoh和A.Tesniere)、欧盟(L.Zitvogel获得“ALLOSTEM”和“DC-THERA”资助;“Active p53”、“Apo-Sys”、“ChemoRes”、“Death Train”资助 “右图”和“转死亡”分别写给G.Kroemer)、Cancéropóle Ile-de-France、国家癌症研究所(Institute National du Cancer)和国家康复机构(Agence Nationale de la Recherche)。
脚注
使用的非标准缩写: ACT,过继细胞移植; ATM,共济失调毛细血管扩张症突变; 癌胚抗原; CHK1,检查点激酶-1; CRT,钙网蛋白; 5-氟尿嘧啶; HMGB1,高迁移率族蛋白B1; IM,甲磺酸伊马替尼; 锁孔帽贝血蓝蛋白; NKG2D,NK细胞组2D; 前列腺特异性抗原; TRP-2,酪氨酸酶相关蛋白2。
本文引文: 临床杂志。 投资。 118 :1991–2001 (2008). doi:10.1172/JCI35180。