摘要 丝氨酸/苏氨酸激酶Akt是许多受体信号转导途径的组成部分,可以防止生长因子退出后的细胞死亡。 在这里,我们表明Akt对细胞死亡的抑制并不依赖于新的蛋白质翻译。 相反,Akt抑制细胞死亡需要通过糖酵解来水解葡萄糖。 Akt被发现通过转录后机制调节糖酵解的多个步骤,包括葡萄糖转运蛋白Glut1在细胞表面的定位,以及在缺乏外源性因素的情况下维持己糖激酶功能。 为了测试葡萄糖摄取和磷酸化在生长因子依赖性生存中的作用,用谷氨酸1和己糖激酶1(谷氨酸1/HK1)细胞转染细胞。 Glut1/HK1细胞在细胞表面积累Glut1,并具有与具有组成型活性Akt(mAkt)的细胞相似的高葡萄糖摄取能力。 然而,与mAkt表达细胞不同的是,它们不消耗更多的葡萄糖,不维持延长的磷酸果糖激酶-1蛋白水平和活性,并且在缺乏生长因子的情况下不维持磷酸戊糖穿梭活性。 然而,与对照细胞相比,在退出生长因子后,谷氨酸1和HK1的表达促进了细胞溶质NADH和NADPH水平的增加,阻止了Bax的激活,并促进了生长因子依赖性生存。 这些数据表明Bax构象对葡萄糖代谢敏感,在缺乏生长因子的情况下,维持葡萄糖摄取和磷酸化可以促进细胞存活。 此外,Akt需要葡萄糖和进行糖酵解以防止Bax活化的能力。 因此,通过葡萄糖代谢的转录后调节防止Bax活化可能是Akt在缺乏生长因子的情况下维持长期细胞生存能力的一个必要方面。
严格调节细胞数量以维持组织内环境稳定至关重要。 实现这一点的一种机制是细胞依赖有限的组织特异性细胞外信号( 11 ). 当细胞无法获得足够的外部信号时,就会萎缩并最终发生凋亡( 13 , 49 , 53 ). 萎缩的特征是细胞大小、蛋白质含量、细胞ATP和糖酵解速率降低。 此外,萎缩细胞在有丝分裂刺激下表现出延迟激活和增殖( 49 ). 当促凋亡的Bcl-2家族成员,如Bax,被构象变化激活并定位于线粒体膜时,细胞凋亡开始,导致线粒体外膜完整性的丧失( 21 , 42 ). 一旦外膜破裂,细胞色素 c(c) 凋亡诱导因子和SMAC/DIABLO从膜间隙释放到胞浆中,在胞浆中它们可以促进caspase活化并启动凋亡( 41 ).
线粒体介导的凋亡诱导需要激活促凋亡的Bcl-2家族成员( 38 , 60 , 68 )但导致Bax活化和线粒体完整性丧失的事件尚不确定。 一种可能性是,当细胞被剥夺了促进生存的信号转导途径时,Bax激活和线粒体功能障碍是糖酵解代谢减少的结果。 因子依赖性细胞系的生长因子撤除后葡萄糖摄取减少可能导致线粒体代谢缺乏糖酵解底物,如丙酮酸和NADH。 最终,缺乏电子传递和维持内膜电位的底物可能会损害线粒体适当调节离子交换和体积稳态的能力( 43 )并导致Bax活化和线粒体完整性丧失。 外源性信号维持线粒体稳态的机制以及癌细胞如何克服对外源性信号的依赖以允许肿瘤生长,目前尚不清楚。
许多细胞外信号的信号转导途径中涉及的一个关键分子是原癌基因Akt,一种丝氨酸和苏氨酸激酶。 Akt被发现是v的细胞同源物- 阿克特 ,一个从AKR小鼠自发性胸腺瘤中分离出的病毒癌基因( 6 , 10 , 28 ). 组成活性Akt可以促进细胞在面对各种死亡刺激时的存活,包括退出生长因子( 32 ). 此外,Akt被证明可以调节细胞代谢的各个方面,如胰岛素反应性葡萄糖转运( 23 ). 在连接胰岛素受体后,Akt通过其蛋白同源结构域和磷脂酰肌醇3-激酶(PI3-K)产物的相互作用被招募到质膜上。 在细胞膜上,Akt通过激酶磷酸化被激活,包括PI3-K依赖性激酶PDK1( 2 , 52 ). 通过肉豆蔻酰化(mAkt)靶向质膜可以使Akt具有组成活性,其中Akt被内源性PI3-K依赖性激酶磷酸化。 激活后,Akt可以磷酸化影响葡萄糖摄取和代谢的靶蛋白。 例如,胰岛素激活Akt,促进葡萄糖转运蛋白谷氨酸4移位到细胞表面,使脂肪细胞吸收葡萄糖( 16 , 24 ).
在造血细胞中,即使没有细胞外生存信号,Akt活性也能维持细胞存活。 与抗凋亡Bcl-2蛋白赋予的存活不同,Akt维持细胞存活需要在培养基中存在葡萄糖( 20 , 48 ). 这可能是因为Akt可能通过诱导新的转录和翻译来调节其生存效应,例如Akt介导的促生存转录因子NF-κB的激活所引起的作用( 29 , 33 , 34 , 39 , 50 ). 在这种情况下,Akt对培养基中葡萄糖的需求可能仅仅是为了支持大分子合成,因为葡萄糖是氨基酸、核糖糖和ATP的生产来源。 或者,Akt可以支持缺乏生长因子的细胞的存活,这是维持营养吸收和细胞代谢的直接结果。 造血系统和神经系统的观察结果都支持后一种假设,即细胞代谢在退出生长因子后通常会降低( 12 , 49 , 61 )但是Akt可以阻止这种下降( 15 , 48 )即使在环己酰亚胺(CHX)存在的情况下,Akt也能促进短期存活( 20 ).
为了分析Akt介导的生长因子提取细胞长期存活的机制,我们分析了表达mAkt的细胞和表达糖酵解途径早期成分的细胞的代谢和存活特征。 在这里,我们表明,长期Akt介导的存活并不需要原存活蛋白的转录和翻译,因为mAkt的表达可以促进白细胞介素-3(IL-3)依赖性FL5.12细胞在没有IL-3的情况下的存活,即使新的蛋白翻译受到抑制。 然而,表达mAkt的细胞确实需要可水解的葡萄糖底物来介导IL-3非依赖性存活。 mAkt的表达通过促进谷氨酸1在细胞表面的定位、细胞总己糖激酶活性和磷酸戊糖穿梭活性,导致葡萄糖摄取和磷酸化增加。 为了确定葡萄糖摄取和磷酸化在mAkt介导的存活表型中的作用,分别或同时用谷氨酸1和己糖激酶1(HK1)转染FL5.12细胞。 与mAkt细胞不同,与对照细胞相比,谷氨酸1/HK1细胞的葡萄糖消耗没有升高。 谷氨酸1/HK1细胞不能促进葡萄糖消耗的长期增加,这与磷酸果糖激酶1(PFK1)蛋白水平的降低以及生长因子退出后不能维持磷酸戊糖穿梭活性有关。 然而,与对照细胞相比,谷氨酸1/HK1细胞保持较高的细胞NADH和NADPH[NAD(P)H]水平。 此外,谷氨酸1和HK1的表达足以阻止Bax的激活,并促进一些细胞的长期生长因子依赖性生存,而Akt需要葡萄糖和糖酵解来支持细胞在缺乏生长因子的情况下的生存。 这些数据表明Bax构象变化对葡萄糖代谢的变化很敏感,表明Akt可能通过多种转录后机制促进糖酵解来防止Bax活化和细胞死亡,包括谷氨酸1表面定位、己糖激酶活性刺激、, PFK1表达的转录后调控。
材料和方法 细胞。 将pSFFV中的大鼠谷氨酸1 cDNA(宾夕法尼亚大学费城分校M.Birnbaum慷慨捐赠)和pcDNA3中的HK1(密歇根州立大学兰辛分校J.Wilson慷慨捐赠)单独或联合转染IL-3依赖性造血细胞系FL5.12。 用空pSFFV转染对照细胞。 使用Geneticin(GIBCO-BRL,Grand Island,N.Y.)进行选择并进行免疫荧光标记,然后进行流式细胞术分析,以确定稳定的克隆。 表达mAkt的细胞先前已有描述( 48 )或通过在pEF6载体中用mAkt转染FL5.12细胞生成(Invitrogen,Carlsbad,Calif.)。 对每个转染的三个或更多克隆进行了实验,给出的结果来自每种类型的一个代表性克隆。 在一些实验中,使用了过度表达Bcl-xL的FL5.12细胞(克隆Bcl-xL 4.1)( 49 ). 如前所述,细胞在含有IL-3的RPMI培养基中生长( 7 , 25 , 45 ). 通过添加产生IL-3的WEHI 3B细胞系的条件培养基或添加400 pg重组小鼠IL-3/ml(加州圣地亚哥BD-Pharmingen),向培养基中添加IL-3。 两种IL-3来源的结果一致。 为了抑制PI3-K途径或蛋白质合成,分别在10 mM LY249002(LY)或20μg CHX/ml中培养细胞。 在每次培养开始时添加抑制剂,并在每次实验的第2天补充抑制剂。 在提取葡萄糖的地方,细胞在补充有透析胎牛血清(GIBCO-BRL)的无葡萄糖RPMI培养基(GIBCO-BRL)中生长。 将葡萄糖(西格玛,密苏里州圣路易斯)添加到一些培养物中,使最终浓度达到10 mM。在其他培养物中将2-脱氧葡萄糖(2-DOG;西格玛)添加到最终浓度为10 mM的培养物中。用Z测定细胞浓度 2 粒子计数器(佛罗里达州迈阿密库尔特公司)。 使用制造商描述的诊断试剂盒(Sigma)测量葡萄糖和乳酸浓度。 将一些细胞培养在20μM碘乙酸(IAA;Sigma)中,在含有或不含IL-3的RPMI培养基中,或在存在1 mM甲基丙酮酸(mPyruvate;Sigma-)的情况下。
细胞分离。 如前所述,从生长在有或无IL-3的FL5.12细胞中分离出线粒体( 19 ). 如前所述制备了血浆膜,并进行了一些修改( 31 ). 简言之,15×10 6 在IL-3中生长或从IL-3中取出的细胞在血浆膜涂层缓冲液(PMCB、20 mM 2-吗啉乙醇磺酸、150 mM氯化钠和280 mM山梨醇[pH6.0])中清洗12 h。 将细胞重新悬浮在1 ml PMCB中,并滴加到5 ml含有1%阳离子胶体二氧化硅的PMCB中(Ludox-CL;Sigma)。 然后将细胞在室温下轻轻旋转20分钟。 将细胞在20 ml PMCB中清洗三次,再悬浮在1 ml PMCB内,并滴加到5 ml PMCB(含有0.1%聚丙烯酸,分子量为30K(Sigma))中。 将细胞在室温下轻轻旋转20分钟,在20ml PMCB中洗涤三次,并重悬于1ml裂解缓冲液(2.5mM咪唑σ和5mM EDTA)中。 在冰上放置30分钟后,使用Dounce均质机和密柄杵对细胞进行溶解。 通过在28000× 克 将含有质膜的颗粒在裂解缓冲液中洗涤三次,并在含有2%十二烷基硫酸钠的裂解缓冲液中将二氧化硅煮沸5分钟,使其溶解。 然后测定蛋白质浓度并进行蛋白质印迹。
蛋白质印迹和免疫荧光。 在0.5%NP-40 NET(100 mM NaCl、1 mM EDTA和10 mM Tris[pH8],含蛋白酶抑制剂;BD-Pharmingen)中溶解细胞进行Western blotting,并通过离心进行预处理。 蛋白质浓度通过双茚四酮酸蛋白质分析测定(皮尔斯,罗克福德,伊利诺伊州),并在十二烷基硫酸钠-12%聚丙烯酰胺凝胶电泳凝胶(Invitrogen)上运行10μg蛋白质。 使用兔抗谷氨酸1抗血清(Research Diagnostics Inc.,Flanders,N.J.)检测谷氨酸1,使用山羊抗果糖-6-磷酸激酶(ResearchDiagnostic)检测PFK1,然后使用抗兔辣根过氧化物酶(Santa Cruz Biotechnology,Santa Cru z,Califor.)或抗山羊辣根过氧化物酶酶(Santa-Cruz Biotechnology), 分别使用ECL-Plus(Amersham Biosciences,Piscataway,N.J.)进行检测。 为了进行免疫荧光,将细胞固定在磷酸盐缓冲液(PBS)中的1%多聚甲醛中10分钟。然后将细胞渗透在PBS中的0.03%皂苷(Sigma)中,并在含有10%正常大鼠血清和10μg/ml初级抗体的PBS中0.3%皂苷的染色液中染色30分钟。 使用兔抗谷氨酸1(Research Diagnostics,Inc.)检测谷氨酸1,使用单克隆小鼠免疫球蛋白G1(IgG1)单克隆抗HK1检测HK1(Chemicon,Temecula,Calif.)。 未被一级抗体染色的细胞作为阴性染色对照。 在用PBS中0.03%的皂苷洗涤后,用二级抗体、山羊抗兔异硫氰酸荧光素(FITC;BD-Pharmingen)对细胞进行染色,以检测抗谷氨酰胺染色,用兔抗鼠IgG1-FITC(BD-Pharmin)检测抗HK1染色,在染色液中染色30分钟。 将细胞清洗并重新悬浮在PBS中2%的胎牛血清中进行流式细胞术分析,或将其安装在载玻片上,并使用尼康E800显微镜(光学仪器,宾夕法尼亚州阿德莫尔)、Micromax数码相机(普林斯顿仪器,新泽西州特伦顿)、, 和Metamorph 4.5成像软件(Universal imaging,宾夕法尼亚州唐宁顿)。
北方斑点。 用Trizol(GIBCO-BRL)分离总RNA,并在1%琼脂糖甲醛凝胶上分离10μg。 用小鼠PFK1 cDNA(IMAGE克隆533677;Reseach Genetics,阿拉巴马州亨茨维尔)探测硝化纤维过滤器。 为了证明每条通道中总RNA的等效负载,去除硝化纤维过滤器并与18S RNA特异探针杂交(数据未显示)。
流式细胞术。 使用FACScalibur细胞仪(加州山景城Becton Dickinson)和Cell Quest软件(Becton Dickinson,Calif.)对细胞进行流式细胞术分析。 为了确定细胞活力,用每毫升10μg的活性染料碘化丙啶(PI;分子探针,尤金,俄勒冈州)对细胞进行染色。如前所述,分析白细胞介素-3退出后Bax构象的变化( 40 ),只需稍作修改。 简单地说,用0.25%多聚甲醛在PBS中固定细胞5分钟,并在PBS内洗涤两次。对于初级染色,用10μg纯化的小鼠IgG1单克隆抗体(克隆6A7;BD-Pharmingen)或同种对照单克隆抗体 在含有100μg/ml洋地黄素(Sigma)和10%正常大鼠血清的PBS染色介质中,在室温下保持30分钟。 由于FL5.12细胞表达能够非特异性结合抗体的Fc受体,因此每ml的原代染色中添加5μg阻断性抗FcγIII/II(克隆2.4G2;BD-Pharmingen)。 用100μg/ml的洋地黄素在PBS中清洗细胞,并在4°C下用大鼠抗鼠IgG1-FITC(克隆A85-1;BD-Pharmingen)在洋地黄染色培养基中培养30分钟。 然后在含有100μg洋地黄素/ml的PBS中清洗染色细胞,并在流式细胞术分析之前,通过在含有100 mg洋地黄碱/ml、50μg RNase A(Boehringer Mannheim)/ml和5μg PI/ml的PBS中培养20分钟,对染色细胞进行DNA含量染色。 为了避免完全凋亡细胞中可能出现的潜在染色伪影,分析中排除了亚倍体细胞。
生化分析。 如前所述,通过油分离测定葡萄糖摄取量,并进行少量修改( 61 ). 简单地说,细胞在PBS中清洗一次,然后在葡萄糖摄取缓冲液(8.1 mM Na)中培养15分钟 2 高性能操作 4 ,1.4 mM千赫 2 人事军官 4 、2.6 mM KCl、136 mM NaCl、0.5 mM MgCl 2 和0.9 mM CaCl 2 (最终pH值7.4),37°C,浓度为5×10 6 通过分层25μl 8%蔗糖-20%高氯酸、100μl溴代十二烷和50μl葡萄糖吸收缓冲液(含1μCi[ 三 H] 2狗。 细胞被添加到葡萄糖摄取缓冲液的顶层,用5×10的放射性标记2-DOG 5 以启动葡萄糖摄取测定。 在室温下孵育2分钟后,以最大速度旋转微型离心管1分钟。2分钟孵育中细胞摄取的放射性标记的2-DOG通过溴代十二烷层进入低蔗糖-高氯酸层,而未经孵育[ 三 H] 2-DOG留在上层。 然后将试管冷冻并在溴代十二烷层的中心切割,并测定下层的放射性。
如前所述测定己糖激酶活性( 63 ). 简单地说,进行了光谱光度分析,其中葡萄糖-6-磷酸的形成与NADPH的产生耦合。 电池(5×10 6 )收集并在50 mM磷酸钠-0.1%(vol/vol)Triton X-100缓冲液中溶解。 或者,将纯化线粒体中的10μg蛋白质用于己糖激酶测定。 然后将裂解物和纯化的线粒体添加到含有3 mM葡萄糖、NADP(5 mg/ml)、葡萄糖-6-磷酸脱氢酶(100 U/ml)、220 mM ATP和1%单硫代甘油的反应混合物中。 使用SpectraMax 190分光光度计(加利福尼亚州森尼维尔市分子器件公司)测量340 nm处的NADPH生成,作为吸光度变化。 数据表示为340 nm/second/5×10时吸光度的变化 5 单元格×10 −4 .
如前所述测量PFK1活性( 51 ). 简单地说,将细胞重新悬浮在50μl PFK裂解缓冲液(50 mM HEPES[pH7.0]、100 mM KF和15 mM EGTA[pH7.4])中,在干冰乙醇浴中冷冻并在37°C下解冻。 在30000× 克 在4°C下保持30分钟。 然后将上清液添加到950μl反应缓冲液中(50 mM HEPES[pH7.0],100 mM KCl,5 mM MgCl 2 ,1.5 mM ATP,0.15 mM NADH,5 mM NaHPO 4 ,0.1毫安,1毫安 4 Cl,5 U三糖磷酸异构酶/ml,0.5 U醛缩酶/ml、0.5 Uα-甘油磷酸脱氢酶/ml和5 mM果糖-6-磷酸; 均来自Sigma)。 在室温下每隔15秒在SpectraMax 190分光光度计(分子器件)中读取340 nm处的吸光度,持续30分钟。 数据表示为340 nm/min/5×10时吸光度的变化 5 单元格×10 −2 .
测量细胞溶质NAD(P)H,3×10 7 将FL5.12细胞在有或无IL-3的条件下培养12 h。将细胞制粒并在Krebs缓冲液(115 mM NaCl、2 mM KCl、25 mM NaHCO)中洗涤 三 ,1 mM氯化镁 2 ,2 mM氯化钙 2 和0.25%牛血清白蛋白[BSA](pH 7.4])补充10 mM葡萄糖。 细胞重新悬浮到10个密度 7 细胞/ml,并放置在配有搅拌装置的荧光分光光度计(新泽西州爱迪生市Jovin Yvon公司)的试管中。 NAD(P)H荧光通过在340±5 nm激发和在461±5 nm检测发射来监测一段时间。 将羰基氰化物4-三氟甲氧基苯腙(FCCP;Sigma)和丙酮酸盐添加到细胞中,方法是打开腔室,将药物移液到试管中,并通过上下移液进行多次混合。 在试验箱打开时收集的数据点从记录中删除。 试管中FCCP的最终浓度为5μM,mPyruvate的最终浓度是5 mM。
通过培养2×10测定戊糖磷酸穿梭活性 6 在不含葡萄糖和碳酸氢钠的RPMI培养基(Sigma)中在IL-3中生长或从IL-3中退出12小时的细胞,该培养基补充有透析的胎牛血清(GIBCO-BRL)-20mM HEPES-5mM葡萄糖-0.2μCi d日 -1- 14 C-葡萄糖或 d日 -6- 14 C-葡萄糖。 将细胞放置在封闭的小瓶中,小瓶内有凸起的细胞孔,其中含有100μl 5%氢氧化钾浸泡过的滤纸,并在37°C下培养。 4小时后,取出滤纸并测定其放射性。 通过减去培养样品的放射性水平来计算戊糖磷酸穿梭活性 d日 -6- 14 培养的C-葡萄糖 d日 -1- 14 C-葡萄糖。
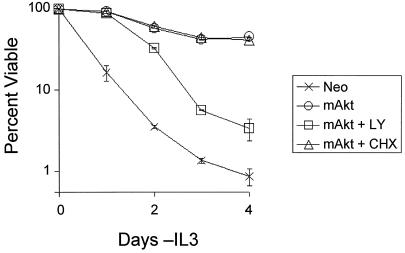
结果 Akt介导的生长因子衍生细胞存活不需要新的蛋白质翻译。 mAkt保护因子依赖细胞免受生长因子提取诱导的凋亡( 48 ). 为了确定这种保护是否由转录和蛋白翻译的生存促进程序的激活介导,从生长因子中提取表达mAkt的细胞和对照细胞,并在存在或不存在蛋白质合成抑制剂CHX或PI3-K抑制剂LY的情况下培养(图。 1 ). 在第2天和第4天补充CHX和LY。 用CHX处理细胞并没有导致mAkt蛋白的损失超过稳定内源性蛋白的下降(数据未显示)。 mAkt蛋白水平的维持可能是由于蛋白质降解减少,这是在抑制蛋白质合成时观察到的( 17 ). CHX治疗对mAkt介导的细胞存活率在6天内没有明显影响(图。 1 和数据未显示)。 无论CHX治疗如何,mAkt的磷酸化均在无IL-3的情况下保持(数据未显示)。 然而,通过在LY中培养细胞来抑制mAkt的激活,导致mAkt去磷酸化(数据未显示),并阻止mAkt介导其生存效应。 虽然在IL-3停药和LY治疗中mAkt磷酸化的调节尚不清楚,但这些数据表明,在缺乏生长因子的情况下,Akt介导的细胞长期存活与Akt维持磷酸化状态的能力相关,而不是诱导新的转录和蛋白翻译。
图1。
Akt不需要蛋白质合成来促进生长因子衍生细胞的存活。 对照组(Neo)和肉豆蔻酰化Akt(mAkt)表达细胞在无抑制剂的培养基或含有PI3-K抑制剂LY或蛋白翻译抑制剂CHX的培养基中从IL-3中提取。 在第2天补充抑制剂。 用LY处理细胞导致mAkt在第2天去磷酸化和失活,而在没有IL-3的情况下,mAkt保持磷酸化(数据未显示)。 通过流式细胞术分析培养细胞在不同时间点的活性,通过PI排除法测定活性。 所示值是三份样品结果的平均值; 误差线表示标准偏差。
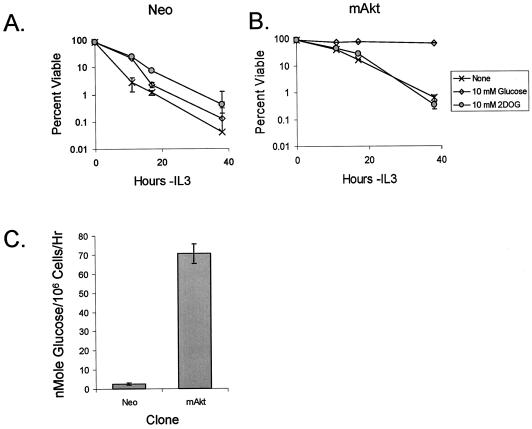
活性成分Akt需要葡萄糖来防止细胞死亡。 与抗凋亡Bcl-2蛋白促进的生长因子依赖性存活不同,mAkt需要在培养基中存在葡萄糖来调节其保护作用( 20 , 48 ). 有人提出,Akt对葡萄糖的这种依赖性促进细胞存活是由于Akt依赖性刺激和维持己糖激酶活性以及葡萄糖-6-磷酸作为信号分子的作用( 20 ). 为了支持这一模型,葡萄糖类似物2-DOG可以被己糖激酶磷酸化,但不能通过糖酵解进一步代谢,足以在照射和取血后维持细胞的短期存活( 20 ). 除了作为潜在的信号分子外,2-DOG还可以通过戊糖磷酸途径代谢生成NADPH( 36 , 37 ). 为了确定2-DOG是否足以使Akt在生长因子退出后促进长期细胞存活,在没有葡萄糖或存在葡萄糖或2-DOG的情况下,对IL-3依赖性FL5.12对照(Neo)和mAkt表达细胞在IL-3退出后的存活率进行测试。 在存在葡萄糖或2-DOG的情况下,对照细胞的死亡速度比不存在葡萄糖的情况下从IL-3中提取的细胞慢(图。 2安培 ). 然而,当从IL-3中取出时,所有对照细胞都迅速发生了凋亡,无论采用何种治疗,38小时存活率都不到1%。 相反,表达mAkt的细胞在含有葡萄糖的培养基中通过IL-3的提取而避免凋亡(图。 2B型 ). 尽管2-DOG使mAkt能够提供与2-DOG在对照细胞中观察到的类似的保护,但在缺乏葡萄糖或用2-DOG替代葡萄糖的情况下,mAkt的表达不再提供长期的死亡保护。 这些数据表明,mAkt细胞需要通过糖酵解来水解葡萄糖,以使mAkt-介导对生长因子提取的保护作用。 葡萄糖水解的直接测量证实,mAkt细胞在提取IL-3时消耗的葡萄糖水平大大高于对照细胞(图。 2摄氏度 ). 葡萄糖水解的需求不仅仅是因为需要生成丙酮酸作为线粒体底物,因为添加mPyruvate不会影响培养物中无葡萄糖或2-DOG的细胞死亡(数据未显示)。
图2。
Akt需要一种可水解的葡萄糖底物,以防止在提取生长因子时死亡。 对照(Neo)(A)和mAkt转染的IL-3依赖性FL5.12(B)细胞在不存在葡萄糖或存在10mM葡萄糖或10mM 2-DOG(一种不能通过糖酵解代谢的葡萄糖类似物)的情况下从IL-3中取出。 在不同的时间点,通过流式细胞术分析细胞,通过碘化丙啶排除法测定细胞活力。 (C) 在没有IL-3的情况下,在10小时后测量Neo和mAkt细胞的糖酵解率。 所示值是三份样品结果的平均值; 误差线表示标准偏差。
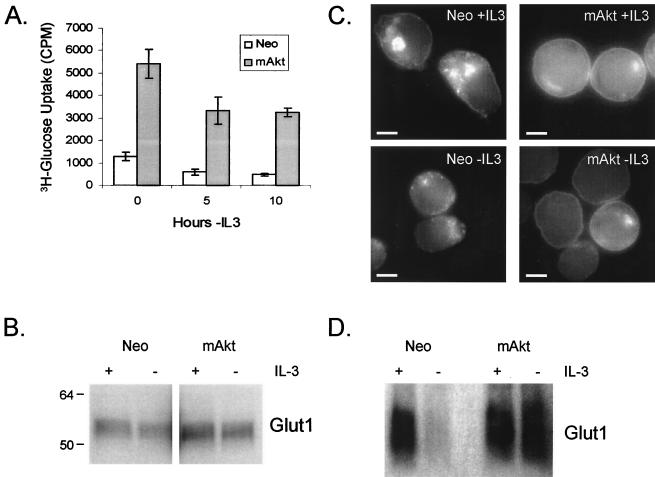
通过mAkt表达增加并维持葡萄糖摄取。 mAkt对葡萄糖水解的需求表明,mAkt可能通过促进葡萄糖代谢来调节其保护作用。 因为已经证明Akt在胰岛素反应性葡萄糖摄取中起着重要作用( 55 )并能调节谷氨酸1 mRNA水平( 5 , 48 ),我们试图确定组成活性Akt是否影响造血细胞的葡萄糖摄取。 将表达mAkt的细胞与对照细胞比较其在存在IL-3或去除IL-3 5或10小时后摄取葡萄糖的能力(图。 3A级 ). 之所以选择这些时间点,是因为在IL-3缺乏12小时之前,对照细胞在IL-3恢复后可以完全恢复,如90%以上的克隆效率所示( 57 ). 对照细胞在被忽视5小时和10小时后,葡萄糖摄取量均降低。 组成性Akt活性增加了FL5.12细胞在所有时间点摄取葡萄糖的能力。 由于谷蛋白1是造血细胞上表达的主要葡萄糖转运蛋白,因此对谷蛋白1的表达进行分析,以确定谷蛋白1表达的变化是否导致mAkt细胞中观察到的葡萄糖摄取增加。 尽管mAkt有能力减弱从IL-3中去除后FL5.12细胞中谷氨酸1 mRNA的丢失( 48 )mAkt表达细胞的葡萄糖摄取能力增加并不是由于谷氨酸总蛋白表达增加。 通过Western blot分析(图。 3B公司 )并通过免疫荧光对Glut1总细胞表达进行流式细胞术分析(图。 4A级 ).
图3。
组成活性Akt促进葡萄糖摄取不是通过调节谷氨酸1蛋白水平,而是通过促进谷氨酸1细胞表面定位。 (A) 对照组(Neo)和mAkt表达的IL-3依赖细胞在有IL-3或无IL-3的情况下培养5或10小时。然后采集细胞,测量其摄取不可水解葡萄糖类似物2-DOG的能力。 所示值是三份样品结果的平均值; 误差线表示标准偏差。 (B) 通过Western blot分析对照细胞和mAkt细胞在IL-3存在或退出IL-3 10 h后葡萄糖转运蛋白谷氨酸1的表达。 每条通道都装载了10μg蛋白质。 (C) 对照(Neo)和mAkt细胞在有IL-3的情况下和无IL-3的10小时后通过免疫荧光染色进行谷氨酸1定位。 每个显微照片都进行了单独的对比,以实现谷氨酸1定位的最佳可视化。 条形代表5μm。 (D) 在有IL-3存在的情况下或在没有IL-3的情况下12小时后,从对照细胞和mAkt表达细胞中分离出质膜,并通过Western blot分析10μg蛋白质的细胞表面谷氨酸1的表达。
图4。
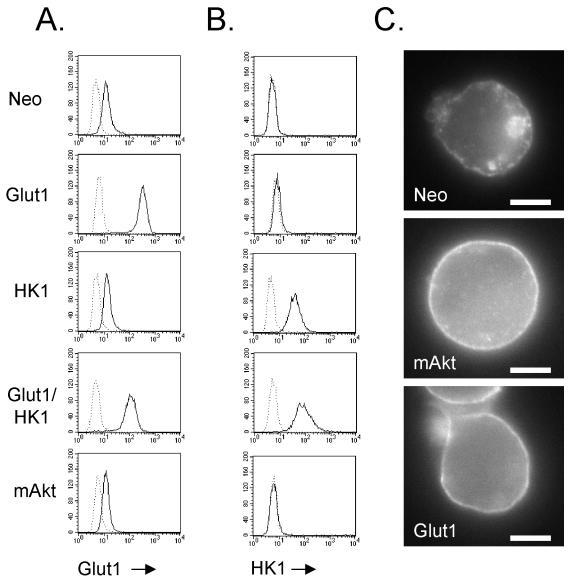
谷氨酸1表达促进谷氨酸1表面定位的积累。 (A和B)对照组和mAkt表达的FL5.12细胞与转染谷氨酸1、HK1或谷氨酸1和HK1的细胞(谷氨酸1/HK1)比较谷氨酸1表达(A)和HK1表达(B)。 (C) 通过谷氨酸蛋白渗透细胞的免疫荧光染色,在对照、mAkt和谷氨酸1细胞中测定谷氨酸1定位。 每个显微照片都进行了单独的对比,以实现谷氨酸1定位的最佳可视化。 谷氨酸过度表达细胞的表面谷氨酸1免疫荧光足够明亮,对比图像后细胞内谷氨酸1变得模糊(数据未显示)。 条形代表5μm。
活性成分Akt促进并维持谷氨酸1表面定位。 葡萄糖转运蛋白可以在许多水平上调节,包括转录、mRNA稳定性和蛋白质定位( 三 - 5 , 27 ). 因为Akt已被证明在脂肪和肌肉细胞中的胰岛素信号传递后,在谷氨酸转位到细胞表面中发挥重要作用( 55 ),我们测试了mAkt是否影响造血细胞中的谷氨酸1定位。 对对照细胞和mAkt表达细胞进行渗透、染色,并通过谷氨酸1免疫荧光分析(图。 3C公司 和 4摄氏度 ). 在生长在IL-3中的对照细胞中,谷蛋白1主要在细胞内发现(图。 3C公司 、左上面板和4C),细胞表面有一个谷氨酸环。 mAkt表达导致谷氨酸1主要定位在细胞表面(图。 3C公司 、右上面板和4C)。 在mAkt表达细胞的胞浆中可检测到含谷氨酰胺的小泡,但程度远低于对照细胞。 当对照细胞被剥夺IL-3 10小时时,Glut1的细胞表面表达显著降低,并且细胞表面Glut1染色环不再可辨别(图。 3C公司 ,左下面板)。 相反,Glut1似乎几乎只局限于细胞质小泡中。 相反,从IL-3中去除10小时后,组成活性Akt保持细胞表面谷氨酸1定位。 为了证实这些结果,从存在IL-3或在不存在IL-3的情况下12小时后生长的对照细胞和表达mAkt的细胞中分离出质膜(图。 三维 ). 免疫荧光表明,当从IL-3中去除时,对照细胞中的血浆膜相关谷氨酸1减少。 然而,即使在没有IL-3的情况下,mAkt细胞上的血浆膜相关谷氨酸1仍然很高。 这些数据表明,Akt活性足以影响谷氨酸1的定位,并表明mAkt细胞葡萄糖摄取能力的增加是谷氨酸1表面定位的结果,而不是谷氨酸1蛋白水平的增加。
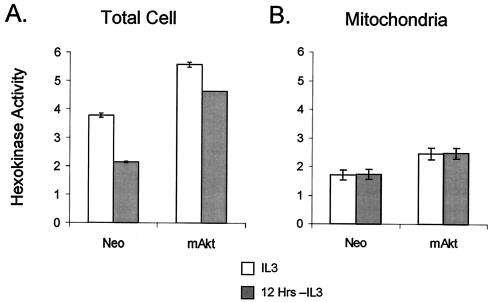
Akt增加己糖激酶活性。 葡萄糖转运蛋白具有促进作用,可沿浓度梯度转运葡萄糖。 细胞不能将葡萄糖保留在细胞质中,直到它被己糖激酶磷酸化。 制备在IL-3中保存或从IL-3中提取12 h的细胞,并测量细胞己糖激酶总活性,以确定IL-3提取对己糖激酶活性的影响,以及Akt的组成性激活是否影响己糖激酶功能(图。 5A级 ). 与葡萄糖摄取一样,IL-3退出后,对照细胞己糖激酶活性降低。 与对照细胞相比,具有组成活性Akt的细胞在IL-3的存在下己糖激酶活性增加。 当IL-3被撤回时,mAkt表达细胞的细胞己糖激酶总活性仅略有下降,保持了两倍于对照细胞的活性。
图5:。
组成活性mAkt细胞增强了其在退出IL-3后保持的己糖激酶活性。 (A) 对照(Neo)和mAkt细胞在IL-3中生长或从IL-3中退出12小时。分析全细胞裂解物的总己糖激酶活性。 (B) 在有IL-3存在的情况下或在没有IL-3的情况下12小时后,从对照细胞和mAkt细胞中分离出线粒体,并分析10μg蛋白质的己糖激酶活性。 所示值是三份样品结果的平均值; 误差线表示标准偏差。
己糖激酶活性可以与细胞溶质或线粒体相关,线粒体相关己糖激酶的活性被认为在细胞凋亡中起重要作用( 20 , 47 ). 因此,来自对照细胞和mAkt表达细胞的线粒体是由在有IL-3存在的情况下生长的细胞或从IL-3中提取的细胞中制备的,持续12小时。而表达mAkt的细胞的线粒体己糖激酶活性高于对照细胞, 无论是对照细胞还是mAkt表达细胞,线粒体己糖激酶活性均不受IL-3撤除的影响(图。 5亿 ). 因此,线粒体己糖激酶活性的丧失并不是生长因子退出后细胞死亡的原因。
谷氨酸1的过度表达促进了谷氨酸1表面定位。 由于mAkt维持了提取细胞对生长因子葡萄糖的摄取和磷酸化,因此我们接下来试图确定这些活性是否足以模拟mAkt对细胞代谢和存活的影响。 哺乳动物中存在己糖激酶的四种主要亚型,1型和2型是线粒体靶向型,而3型和4型是细胞溶质型( 62 ). 因为据报道,Akt可以维持线粒体己糖激酶活性,HK1的过度表达可以在细胞凋亡刺激下支持短期生存能力( 8 , 20 )将谷氨酸1和HK1分别或联合转染FL5.12细胞。 通过流式细胞术分析渗透细胞确定的总谷氨酸1或HK1蛋白水平,选择稳定的谷氨酸1、HK1和谷氨酸/HK1双表达克隆。 所有克隆均表达内源性谷氨酸1。 然而,与未转染谷蛋白1的细胞相比,转染谷胱甘肽1的细胞显著增加了谷蛋白1蛋白的水平,谷蛋白1在只有谷蛋白1细胞和谷蛋白1/HK1双表达克隆中的表达水平同样高(图。 4A级 ). 同样,与未转染HK1的细胞相比,转染HKl的细胞具有高水平的可检测HK1蛋白(图。 4B类 ). 未转染HK1的细胞HK1染色阴性,因为FL5.12细胞不表达内源性HK1,而是表达HK2。 由于谷氨酸1定位于细胞表面的机制尚不清楚,因此对谷氨酸1转染细胞进行分析,以确定谷氨酸1过度表达是否导致细胞表面谷氨酸1蛋白的增加。 对照组、mAkt和谷氨酸1细胞被渗透,通过免疫荧光观察谷氨酸1定位(图。 4摄氏度 ). 研究发现,谷氨酸1过表达细胞的细胞表面谷氨酸1蛋白水平较高。 这种定位模式与谷氨酸1和谷氨酸1/HK1细胞的高糖摄取能力相关(数据未显示)。 Glut1和Glut1/HK1细胞也具有显著的Glut1细胞内池(数据未显示),但细胞表面的高浓度Glut1通过免疫荧光遮挡了这些池的视野。 根据免疫荧光和葡萄糖摄取实验(数据未显示)的测定,退出IL-3后,谷氨酸1-和谷氨酸1/HK1-过度表达细胞中保留了大量的细胞表面谷氨酸1。
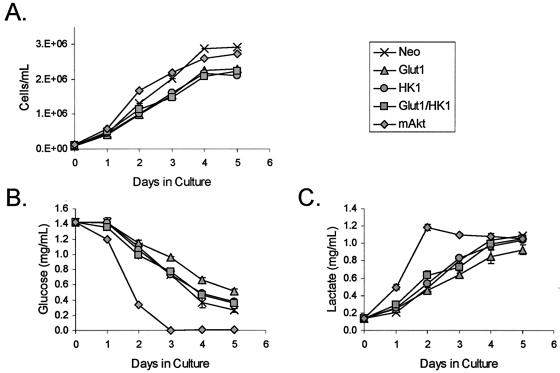
mAkt增加细胞总葡萄糖消耗,而Glut1和HK1的表达则不增加。 由于mAkt细胞与对照细胞相比糖酵解速率增加,我们接下来确定谷氨酸1和HK1的组成性表达是否足以增加葡萄糖消耗。 为了确定谷氨酸/HK1细胞在葡萄糖消耗方面是否与对照细胞不同,对照细胞、表达mAkt的细胞以及表达谷氨酸1和HK1的细胞在IL-3的存在下生长。 建立细胞培养物,连续5天每天测定细胞浓度以及培养上清液中的葡萄糖和乳酸含量。 所有克隆的生长速度相似(图。 6A级 ). 然而,只有mAkt细胞耗尽了其葡萄糖培养物(图。 6亿 ). 这种葡萄糖似乎通过糖酵解代谢,而不是以葡萄糖-6-磷酸或糖原的形式储存,或通过其他途径代谢,因为mAkt的表达导致培养基中乳酸的增加,这与葡萄糖的消耗相当(图。 6摄氏度 ).
图6。
组成活性Akt增加细胞总葡萄糖消耗。 对照组(Neo)、谷氨酸1、HK1、谷氨酸1/HK1和mAkt细胞在IL-3存在下培养,每天观察5天。 (A) 通过测量细胞浓度来测定细胞增殖。 葡萄糖消耗量(B)和乳酸产生量(C)通过测量培养基中的浓度来确定。 所示值是三份培养物结果的平均值; 误差线表示标准偏差。
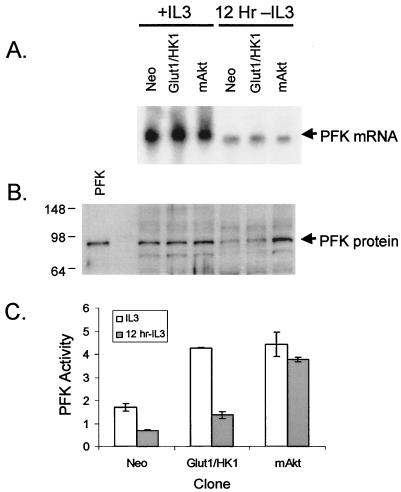
mAkt在IL-3退出后维持PFK1蛋白水平和活性。 糖酵解的关键步骤是PFK1对果糖-6-磷酸的磷酸化。 在此步骤之前,葡萄糖或果糖-6-磷酸可以通过戊糖磷酸途径分流。 ATP在6-磷酸果糖转化为1,6-二磷酸果糖的过程中被PFK1水解。 作为ATP水解的结果,这一步骤代表了葡萄糖对糖酵解的不可逆承诺。 因此,在有IL-3存在或退出IL-3 12小时后,在对照、谷氨酸1/HK1和mAkt细胞中测量PFK1的表达和活性。 退出IL-3后,所有样本中PFK1的mRNA均下降,表明Akt活性并未显著影响PFK1转录(图。 第7章 ). IL-3退出后,对照组和谷氨酸1/HK1细胞中PFK1蛋白水平也显著降低(图。 7亿 ). 然而,在没有IL-3的情况下培养12小时后,mAkt细胞中PFK1蛋白水平仍然很高。 mAkt维持PFK1蛋白水平可能是因为阻止了其降解,因为生长因子-提取细胞启动了一个以Akt可以阻止的显著蛋白水解为特征的细胞萎缩程序( 15 ). 为了证实PFK1蛋白水平与PFK1功能相关,我们测试了在有或无IL-3的条件下培养12小时的细胞裂解液中PFK1的活性(图。 7摄氏度 ). 从IL-3中去除后,对照细胞和谷氨酸1/HK1细胞均未保持PFK1活性。 然而,尽管IL-3缺乏,活性成分Akt仍维持PFK1活性。
图7。
Akt可防止生长因子退出后PFK1蛋白水平和活性的损失。 对照组(Neo)、谷氨酸1/HK1和mAkt细胞在有IL-3的情况下生长,或在无IL-3的条件下生长12小时。 (A) 分离RNA,通过northern杂交检测PFK1的表达。 (B) 用Western blot分析全细胞裂解产物中PFK1蛋白的表达。 纯化的兔肌肉PFK1显示为尺寸标准。 (C) 对细胞裂解物进行PFK1活性测试。 所示值是三份样品结果的平均值; 误差线表示标准偏差。
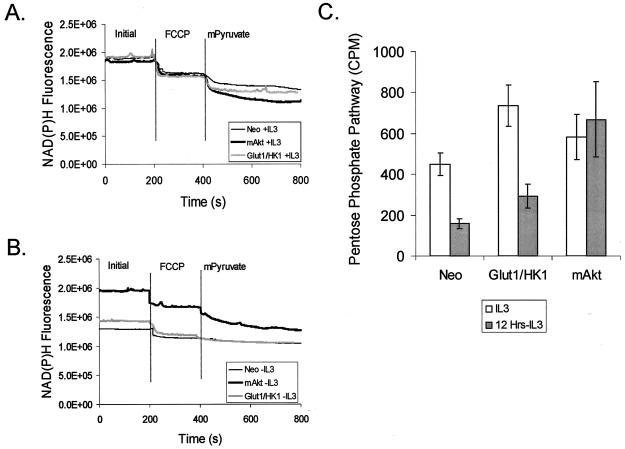
在IL-3退出期间,mAkt维持高细胞溶质NAD(P)H。 为了确定组成型活性Akt在IL-3退出后是否会影响糖酵解酶的活性和己糖激酶下游线粒体底物的产生,在对照、Glut1/HK1和mAkt细胞中测量NAD(P)H水平。 为了测量NAD(P)H,通过荧光分光检测NAD(P)H分析完整的整个细胞(图。 8 ). 测定细胞总NAD(P)H水平,以及线粒体可及和胞质溶胶可及的NAD(P)H水平。 线粒体NAD(P)H通过添加原核细胞FCCP来测量,以引起F电子传输的解耦 1 F类 0 ATP酶,从而改变电化学平衡,有利于NADH氧化为NAD和线粒体NADH的消耗。 因此,添加FCCP后,NAD(P)H荧光与初始细胞总NAD(P)H荧光相比减少,表明线粒体可获得的NADH的相对数量。 为了确定剩余荧光的哪一部分可归因于细胞溶质NAD(P)H,添加了mPyruvate。 丙酮酸盐具有细胞渗透性,可通过乳酸脱氢酶将胞质NADH氧化为NAD。 因此,由于mPyruvate还原为乳酸,NAD(P)H荧光进一步降低,可作为细胞质NADH的指示物。
图8。
去除IL-3后,谷氨酸1/HK1细胞和mAkt细胞部分保持NAD(P)H水平。 对照(Neo)、Glut1/HK1和mAkt细胞在IL-3(A)存在下生长或从IL-3(B)中提取12小时。然后对细胞进行NAD(P)h荧光的荧光光谱分析,以确定每种细胞类型的总的、线粒体可及的和胞质可及的NAD(P)h含量。 建立荧光基线后,用原核细胞FCCP刺激线粒体NADH氧化(垂直线处添加)。 然后,通过观察添加mPyruvate(在垂直线上添加)后NADH荧光随时间的减少来估计每个样品的细胞液NADH含量。 通过细胞溶质酶乳酸脱氢酶的作用,mPyruvate导致细胞溶质NADH的耗竭。 (C) 在有IL-3或无IL-3的情况下12小时后,在对照细胞、谷蛋白1/HK1和mAkt细胞中测定戊糖磷酸穿梭活性。 所示值是三份样品结果的平均值; 误差线表示标准偏差。
在该试验中,在IL-3的存在下,对照、谷氨酸1/HK1和mAkt细胞具有相似的初始和FCCP处理的荧光特征(图。 8安 ). 然而,谷氨酸1/HK1和mAkt细胞增加了胞浆乳酸脱氢酶可用的NAD(P)H,因为添加mPyruvate对其吸光度的影响比对照细胞更大。 在没有IL-3的情况下,对照细胞的NAD(P)H荧光显著降低,其残余荧光受FCCP和mPyruvate的影响小于IL-3的影响(图。 8B类 ). IL-3提取的谷蛋白1/HK1细胞也显著降低了细胞NAD(P)H,但与对照细胞相比,FCCP和mPyruvate-sensitive pool NAD(P)H的水平仍然较高。 然而,具有组成活性Akt的细胞在没有IL-3的情况下仍保持其FCCP和mPyruvate-sensitive荧光,其水平与存在IL-3时的水平相似,这表明mAkt导致细胞继续糖酵解并维持细胞溶质NAD(P)H的产生。 这些数据表明,尽管从IL-3中去除后无法将NAD(P)H的生成维持在mAkt细胞的水平,但谷氨酸1/HK1细胞可以保持比控制细胞更高的葡萄糖衍生代谢底物的生成水平。 与这一发现一致,在IL-3退出后,与对照细胞相比,表达谷氨酰胺的细胞保持糖酵解速率的增加(数据未显示)。
NADH和NADPH显示的荧光曲线通过此处使用的方法无法区分。 为了确定NADPH生成速率作为NADPH对NAD(P)H荧光贡献的指标,测量了磷酸戊糖途径的活性(图。 8摄氏度 ). 对照组、谷氨酸1/HK1和mAkt表达细胞在有或无IL-3的条件下生长12小时,并测量通过戊糖磷酸途径的葡萄糖流量。 停止使用生长因子会导致对照细胞和谷氨酸1/HK1细胞的戊糖磷酸途径活性降低两倍。 然而,即使在没有IL-3的情况下,表达mAkt的细胞也能通过戊糖磷酸途径维持其葡萄糖流量水平。 由于mAkt促进的葡萄糖摄取和磷酸化的维持,这种磷酸戊糖活性的维持是不可能的,因为谷氨酸1/HK1细胞在退出IL-3后也保持了较高的葡萄糖摄取量和磷酸化,但磷酸戊糖的活性降低。 相反,这些数据表明Akt可以直接促进该通路的维持。
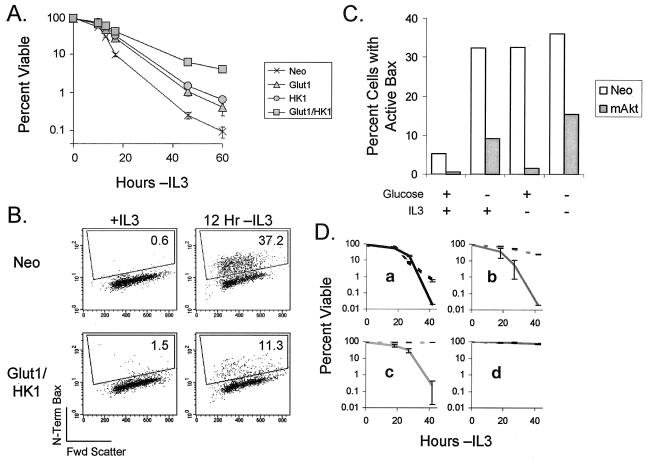
谷氨酸1和HK1通过阻止Bax构象的改变,在IL-3退出后增加细胞存活率。 这些数据表明,Akt促进生长因子依赖性生存的机制之一是通过支持葡萄糖代谢。 为了确定在提取生长因子后维持细胞内可水解葡萄糖的储存是否足以防止细胞死亡,对照组在从IL-3中去除后观察到谷氨酸1、HK1和谷氨酸1/HK1细胞。 在IL-3退出后,对照细胞迅速死亡(图。 9安 ). 然而,表达谷氨酸1和HK1的细胞在没有IL-3的情况下显著提高了生存率。 存活的谷蛋白1/HK1细胞完全可以存活,即使在没有IL-3的情况下5天后也可以通过添加IL-3来恢复,而此时IL-3无法挽救对照细胞(数据未显示)。
图9:。
在缺乏IL-3的情况下,谷氨酸1和HK1的共同表达可提高生存率,并防止Bax构象的改变。 (A) 从IL-3中提取细胞,并通过流式细胞术通过碘化丙啶排除法测量不同时间点的存活率。 所示值是三份样品细胞存活结果的平均值; 误差线表示标准偏差。 (B) 通过流式细胞术测量在IL-3中维持或从IL-3中提取12 h的细胞中Bax的活化。给出了Bax构象变化阳性细胞的百分比。 (C) 对照(Neo)和mAkt表达细胞在葡萄糖或IL-3存在或不存在的情况下培养12 h,如图所示,并测定Bax活化的细胞百分比。 (D) 对照(a)、Glut1/HK1(b)、mAkt(c)和Bcl-xL(D)-过表达的FL5.12细胞在不存在IL-3的情况下用(实线)或不用(虚线)糖酵解抑制剂IAA培养。 培养开始后不同时间点的细胞存活率通过碘化丙啶排除流式细胞术测定。 所示的值是来自一式三份样品的细胞存活结果的平均值; 误差线表示标准偏差。
因为促凋亡的Bcl-2家族成员Bax在启动线粒体细胞死亡途径中起着重要作用( 38 , 60 , 68 ),我们接下来试图确定维持谷氨酸1/HK1细胞内可水解葡萄糖的细胞内储存是否可能通过影响Bax的调节来促进细胞存活。 Bax通常以非活性构象存在于胞浆中。 在凋亡刺激后,一个未知事件导致Bax移位到线粒体,并发生构象变化,揭示了隐藏的N末端表位( 21 , 42 ). 构象改变后,Bax被激活,可以促进线粒体释放细胞色素 c(c) ( 30 ). 因此,使用N-末端Bax特异性抗体,通过流式细胞术分析对照细胞和谷氨酸1/HK1细胞是否存在活化的Bax(图。 8B类 ). 从IL-3中取出12 h的对照细胞中发现大量(37.2%)细胞具有激活的Bax构象。 相反,谷蛋白1/HK1细胞只有少量细胞(11.3%),其中Bax发生了构象变化。 这些数据表明Bax构象变化可能对葡萄糖代谢的变化敏感。
由于谷氨酸1/HK1的表达可以促进生存,并且由于Akt需要葡萄糖来促进生存,因此生存可能需要Akt依赖的葡萄糖代谢增加。 因此,在缺乏IL-3或葡萄糖的细胞中测量了对照细胞和mAkt表达细胞中Bax的活化。 以前,通过使用活化的Bax构象特异性抗体进行免疫沉淀,在细胞群中观察到Bax线粒体重新分布和构象变化( 58 ). 在这里,通过流式细胞仪进行单细胞分析,我们观察到在退出IL-3或葡萄糖后,Bax在对照细胞中被激活(图。 9摄氏度 ). 与之前的工作一致( 56 , 65 ),我们发现,在葡萄糖存在下,表达组成型活性Akt的细胞在退出IL-3后抵抗Bax构象变化。 然而,无论有无IL-3,从培养基中去除葡萄糖都会导致表达mAkt的Bax活性转化细胞增加10倍以上。
为了进一步测试糖酵解在mAkt介导的存活中的作用,用IAA(甘油醛-3-磷酸脱氢酶抑制剂)处理提取的生长因子细胞( 22 , 64 ). 当对照细胞在IL-3退出后发生细胞死亡,IAA几乎没有作用时,IAA治疗阻止了谷氨酸/HK1和mAkt表达细胞的生长因子退出保护细胞(图。 第9天 ). 这并不是由于IAA的一般细胞毒性,因为表达Bcl-xL的FL5.12细胞不受IAA的影响,可能是因为即使糖酵解受到抑制,Bcl-xL也能在缺乏生长因子的情况下保持细胞活力( 48 , 49 ). 这些数据表明,表达谷氨酸1/HK1和mAkt的细胞需要糖酵解来促进细胞存活。 此外,这些数据表明Bax构象变化可能对葡萄糖代谢的变化敏感,并表明促进Glut1/HK1和mAkt细胞的葡萄糖代谢可能通过阻止代谢敏感的Bax构像变化和激活来维持生存。
讨论 丝氨酸/苏氨酸激酶Akt参与许多信号转导途径,这些途径可以防止细胞在退出外源信号后死亡。 mAkt维持生存的机制尚不清楚,但已证明依赖葡萄糖( 20 , 48 ). 在这里,我们表明Akt不需要新的蛋白质翻译,而是利用依赖葡萄糖水解的翻译后机制来促进生长因子-提取细胞的存活。 此外,Akt对葡萄糖代谢的控制发生在多个糖酵解控制点,可能是缺乏生长因子的Akt依赖生存的关键组成部分,因为葡萄糖代谢的维持本身足以减弱Bax构象变化和生长因子提取诱导的细胞死亡。
Akt介导的葡萄糖代谢调节如何阻止Bax活化并促进细胞存活尚不清楚。 一种可能的机制是,Akt驱动的葡萄糖摄取和葡萄糖转运体和己糖激酶的磷酸化分别导致葡萄糖-6-磷酸的积累,从而提供细胞生存信号。 葡萄糖类似物2-DOG足以在短期生存分析中替代葡萄糖的观察结果支持了这种可能性( 20 ). 磷酸2-DOG可能只提供短期生存优势,因为磷酸-2-DOG的积累已被证明会导致己糖激酶蛋白从线粒体外膜分离( 54 )可能导致细胞凋亡( 20 , 47 ). 或者,2-DOG通过戊糖磷酸穿梭物代谢而不是通过糖酵解代谢的能力( 36 , 37 )可能表明NADPH等其他代谢物的产生和调节对短期细胞存活很重要。 即使在缺乏生长因子的情况下,mAkt仍能维持磷酸戊糖穿梭活性,这可能支持NADPH的持续生成和细胞氧化还原调节,以促进细胞短期存活。 然而,2-DOG不能支持mAkt介导的长期存活,这表明磷酸戊糖穿梭物的活性不足以允许长期存活。 相反,Akt驱动的葡萄糖代谢可能通过刺激葡萄糖水解和通过糖酵解生成线粒体代谢底物来促进存活。 为了支持后一种假设,观察到Akt活性可以增加糖酵解速率,促进葡萄糖消耗和乳酸生产( 18 , 20 , 48 ).
Akt通过多种机制调节细胞代谢。 营养物质转运蛋白的细胞内定位是调节代谢的一个重要的主要机制。 Akt还可以调节成肌细胞和脂肪细胞中谷蛋白4的定位,因为胰岛素刺激的谷蛋白4移位被证明依赖于Rho家族GTPase TC10和磷脂酰肌醇3-激酶/Akt途径( 9 , 55 ). 成肌细胞和脂肪细胞也表达谷蛋白1,但在这些情况下,谷蛋白1明显位于细胞表面。 相反,造血细胞不表达谷蛋白4; 相反,谷氨酸1是主要的葡萄糖转运蛋白。 在这里,我们表明,造血细胞中的谷氨酸1定位由细胞因子IL-3和激酶Akt调节。 此外,Akt已被证明以mTOR依赖的方式促进氨基酸转运相关蛋白4F2hc、转铁蛋白受体和低密度脂蛋白受体的表面定位( 15 ). 然而,谷氨酸1在造血细胞中的定位调控机制尚不清楚。 因为成肌细胞和脂肪细胞中谷氨酸1对胰岛素的反应很差( 14 ),谷氨酸1在造血细胞中的定位可能通过与谷氨酸4不同的途径进行调节。 另外,成肌细胞和脂肪细胞中谷氨酸1定位的调节可能不同于造血细胞。 因此,造血细胞中谷氨酸1定位的调节可能与成肌细胞和脂肪细胞中的谷氨酸4类似。
IL-3退出后谷氨酸1/HK1细胞存活率的提高表明,当细胞退出生长因子时,葡萄糖摄取和捕获可以促进细胞存活。 表达谷蛋白1/HK1的细胞在IL-3戒断后存活的能力表明,葡萄糖及其代谢衍生物在生长因子剥夺中受到限制,从而可能通过激活Bax促进细胞凋亡。 然而,Glut1/HK1细胞的存活率不如mAkt表达细胞。 葡萄糖摄取和磷酸化必须伴随其他事件,以使存活率达到与mAkt细胞相似的水平。 正如在缺乏生长因子的情况下,2-DOG无法在mAkt介导的长期存活中替代葡萄糖所表明的那样,磷酸葡萄糖或其类似物的积累本身不足以促进存活。 相反,磷酸葡萄糖必须进一步代谢以支持mAkt依赖性生存。 因此,通过允许IL-3缺失细胞继续获得磷酸葡萄糖,谷氨酸1和HK1的表达可能支持这些代谢途径。 然而,谷氨酸1/HK1细胞不能完全维持PFK1活性,谷氨酸1和HK1表达不能完全维持NAD(P)H水平,相当于在缺乏IL-3的情况下mAkt细胞的水平,以及不能维持磷酸戊糖分流活性, 这可能解释了当缺乏IL-3时,与mAkt细胞相比,谷氨酸1/HK1细胞的长期存活率较低的原因。
从外源信号中提取的细胞的死亡需要促凋亡分子Bax或Bak的作用( 38 , 60 , 68 ). Bax和Bak都需要某种形式的激活来启动线粒体功能障碍和释放线粒体膜间空间的内容物。 Bax必须改变构象并转移到线粒体( 21 , 42 )和Bak必须均聚( 60 ). 这些激活事件的来源都是未知的。 葡萄糖饥饿导致Bax构象改变和移位的能力( 58 )然而,谷蛋白1和HK1表达阻止Bax活化的能力表明Bax对葡萄糖代谢的调节敏感。 因此,在含有生长因子的细胞萎缩期间,葡萄糖代谢丧失和线粒体低极化的影响可能导致Bax和Bak活化,从而导致线粒体内稳态的丧失。 虽然Akt已被证明在细胞从细胞因子中退出时阻止Bax的激活( 56 , 65 ),其机制尚不清楚。 然而,Akt确实需要葡萄糖和细胞能力来进行糖酵解,以防止Bax活化和细胞死亡。 因此,Akt用于防止Bax活化和线粒体完整性丧失的一种可能机制可能是通过其在多个糖酵解点的作用促进葡萄糖捕获和承诺,包括调节葡萄糖转运蛋白、维持己糖激酶功能、, PFK1蛋白水平和活性的稳定。 然而,目前尚不清楚Bax可能对什么代谢产物或代谢途径产生反应,以及这种反应是直接还是间接的,通过仅含BH3的蛋白质的作用( 46 ).
葡萄糖代谢的调节也可能在肿瘤发生中起重要作用。 长期以来,人们一直认为癌细胞的糖酵解代谢增加,称为Warburg效应( 59 ). 最近,葡萄糖转运的调节本身已经牵涉到癌症的发展和进展,因为谷氨酸1表达的增加与肺癌和结直肠癌有关( 26 , 66 , 67 )与乳腺癌预后不良相关( 35 ). 此外,抑制葡萄糖转运和葡萄糖代谢已被证明可以抑制肿瘤生长( 1 , 44 ). 因此,Akt通过糖酵解酶的转录后调节促进葡萄糖摄取和启动糖酵化的能力可能代表了Akt介导的细胞死亡预防、促进细胞生长和促进肿瘤发生的关键方面。
致谢 我们感谢M.J.Birnbaum(宾夕法尼亚州费城宾夕法尼亚大学)和J.E.Wilson(密歇根州兰辛密歇根州立大学)对谷氨酸1和HK1 cDNA的建议和慷慨捐赠。 我们还感谢R.Elstrom、A.Edinger和K.Frauworth提供的技术援助和关键讨论。
这项工作得到了国家癌症研究所的资助。 J.C.R.和D.R.P.得到了欧文顿免疫研究所的支持。 C.J.F.得到了关节炎协会的一个分会资助。 J.C.R.还获得了国家癌症研究所霍华德·特敏K01职业发展奖(K01 CA91905)的支持。
参考文献
1. Aft、R.L.、F.W.Zhang和D.Gius。 2002.2-脱氧-d-葡萄糖作为化疗药物的评估:细胞死亡机制。 英国癌症杂志87 : 805-812. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
2 Alessi,D.R.,S.R.James,C.P.Downes,A.B.Holmes,P.R.Gaffney,C.B.Reese和P.Cohen。 磷酸化并激活蛋白激酶Bα的3-磷酸肌醇依赖性蛋白激酶的特性。 货币。 生物7 : 261-269. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
三。 Atasoy,U.、J.Watson、D.Patel和J.D.Keene。 ELAV蛋白HuA(HuR)可以在细胞核和细胞质之间重新分布,并在血清刺激和T细胞激活期间上调。 细胞科学杂志。 111 : 3145-3156. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
4 Baldwin,S.A.、L.F.Barros和M.Griffiths。 1995年葡萄糖转运蛋白贩运——信号和机制。 Biosci公司。 众议员15 : 419-426. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
5 Barthel,A.、S.T.Okino、J.Liao、K.Nakatani、J.Li、J.P.J.Whitlock和R.A.Roth。 1999.丝氨酸/苏氨酸激酶Akt1对GLUT1基因转录的调节。 生物学杂志。 化学。 274 : 20281-20286. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
6 Bellacosa,A.、J.R.Testa、S.P.Staal和P.N.Tsichlis。 一种逆转录病毒癌基因akt,编码含有SH2样区域的丝氨酸-三氢嘌呤激酶。 科学254 : 274-277. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
7 Boise,L.H.、M.Gonzalez-Garcia、C.E.Postema、L.Ding、T.Lindsten、L.A.Turka、X.Mao、G.Nunez和C.B.Thompson。 1993年。bcl-x,一种bcl-2相关基因,是凋亡细胞死亡的主要调节因子。 单元格74 : 597-608. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
8 Bryson,J.M.、P.E.Coy、K.Gottlob、N.Hay和R.B.Robey。 异位或内源性己糖激酶活性增加可保护肾上皮细胞免受急性氧化诱导的细胞死亡。 生物学杂志。 化学。 277 : 11392-11400. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
9 Chiang,S.H.、C.A.Baumann、M.Kanzaki、D.C.Thurmond、R.T.Watson、C.L.Neudauer、I.G.Macara、J.E.Pessin和A.R.Saltiel。 胰岛素刺激的GLUT4易位需要CAP依赖的TC10激活。 自然410 : 944-948. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
10 Coffer,P.J.和J.R.Woodgett。 与cAMP依赖性和蛋白激酶C家族相关的一种新型蛋白激酶的分子克隆和特性研究。 欧洲生物化学杂志。 201 : 475-481. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
11 我·康隆和M.拉夫。 1999.动物发育中的尺寸控制。 96号单元格 : 235-244. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
12 Deckwerth,T.L.和E.M.J.Johnson。 1993年。与剥夺神经生长因子的交感神经元程序性细胞死亡(凋亡)相关事件的时间分析。 《细胞生物学杂志》。 123 : 1207-1222. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
13. Deshmukh,M.、J.Vasilakos、T.L.Deckwerth、P.A.Lampe、B.D.Shivers和E.M.J.Johnson。 1996年。通过抑制剂或ICE家族蛋白酶保存的NGF缺失交感神经元的遗传和代谢状态。 《细胞生物学杂志》。 135 : 1341-1354. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
14 杜克鲁索、P.H.、L.M.弗莱彻、H.维达尔、M.拉维尔和J.M.塔瓦雷。 脂肪细胞中胰岛素刺激葡萄糖摄取的分子机制。 糖尿病Metab。 28 : 85-92. [ 公共医学 ] [ 谷歌学者 ]
15 爱丁格尔、A.L.和C.B.汤普森。 2002年。Akt通过增加依赖mTOR的营养摄入来维持细胞大小和存活。 分子生物学。 单元格13 : 2276-2288. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
16 Foran、P.G.P.、L.M.Fletcher、P.B.Oatey、N.Mohammed、J.O.Dolly和J.M.Tavare。 1999.蛋白激酶B通过涉及SNAP-23、突触素-2和/或cellubrevin的途径刺激3T3-L1脂肪细胞中GLUT4的移位,但不刺激GLUT1或转铁蛋白受体的移位。 生物学杂志。 化学。 274 : 28087-28095. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
17 富兰克林、J.L.和E.M.约翰逊。 1998年。通过营养因子介导的蛋白质降解与蛋白质合成耦合来控制神经元大小稳态。 《细胞生物学杂志》。 142 : 1313-1324. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
18 Frauworth,K.A.、J.L.Riley、M.H.Harris、R.V.Parry、J.C.Rathmell、D.R.Plas、R.L.Elstrom、C.H.June和C.B.Thompson。 CD28信号通路调节葡萄糖代谢。 豁免权16 : 769-777. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
19 Gottlieb,E.、S.M.Armour和C.B.Thompson。 2002.生长因子缺乏期间线粒体呼吸控制丧失。 程序。 国家。 阿卡德。 科学。 美国99 : 12801-12806. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
20 Gottlob,K.、N.Majewski、S.Kennedy、E.Kandel、R.B.Robey和N.Hay。 Akt/PKB对早期凋亡事件的抑制依赖于糖酵解和线粒体己糖激酶的第一步。 基因发育15 : 1406-1418. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
21 Gross,A.、J.Jockel、M.C.Wei和S.J.Korsmeyer。 BAX的强制二聚化导致其易位、线粒体功能障碍和凋亡。 EMBO期刊17 : 3878-3885. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
22 郭,Z.,J.Lee,M.Lane和M.Mattson。 碘乙酸盐保护海马神经元免受兴奋毒性和氧化损伤:热休克蛋白和Bcl-2的参与。 神经化学杂志。 79 : 361-370. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
23 Hajduch,E.、G.J.Litherland和H.S.Hundal。 蛋白激酶B(PKB/Akt)-葡萄糖转运的关键调节因子? FEBS通讯。 492 : 199-203. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
24 Hill,M.M.、S.F.Clark、D.F.Tucker、M.J.Birnbaum、D.E.James和S.L.Macaulay。 蛋白激酶Bβ/Akt2在脂肪细胞胰岛素刺激GLUT4易位中的作用。 摩尔细胞。 生物19 : 7771-7781. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
25 Hockenbery,D.、G.Nunez、C.Milliman、R.D.Schreiber和S.J.Korsmeyer。 Bcl-2是一种阻止程序性细胞死亡的线粒体内膜蛋白。 性质348 : 334-336. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
26 伊藤、T.、野口勇、N.Udaka、H.Kitamura和S.Satoh。 葡萄糖转运蛋白在胎儿肺和肺肿瘤中的表达。 历史。 组织病理学。 14 : 895-904. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
27 Jain,R.G.、L.G.Andrews、K.M.McGowan、P.H.Pekala和J.D.Keene。 Hel-N1(一种RNA-结合蛋白)的异位表达增加了3T3-L1脂肪细胞中葡萄糖转运蛋白(GLUT1)的表达。 摩尔细胞。 生物17 : 954-962. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
28 Jones,P.F.、T.Jakubowicz、F.J.Pitossi、F.Maurer和B.A.Hemmings。 1991.第二信使亚家族丝氨酸/茶碱蛋白激酶的分子克隆和鉴定。 程序。 国家。 阿卡德。 科学。 美国88 : 4171-4175. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
29 Jones,R.G.、M.Parsons、M.Bonnard、V.S.F.Chan、W.-C.Yeh、J.R.Woodgett和P.S.Ohashi。 蛋白激酶B调节T淋巴细胞存活、核因子κB活化和Bcl-X L(左) 体内水平。 《实验医学杂志》191 : 1721-1733. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
30 Jurgensmeier、J.M.、Q.Deveraux、L.Ellerby、D.Bredensen和J.C.Reed。 1998年Bax直接诱导细胞色素 c(c) 来自分离的线粒体。 国家。 阿卡德。 科学。 美国95 : 4997-5002. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
31 Kamsteg,E.-J.和P.M.T.Deen。 2001.检测卵母细胞质膜中的水通道蛋白-2:一种提高产量和纯度的新分离方法。 生物化学。 生物物理学。 Res.Commun公司。 282 : 683-690. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
32 坎德尔、E.S.和N.海伊。 多功能丝氨酸/苏氨酸激酶Akt/PKB的调节和活性。 实验细胞研究253 : 210-229. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
33. Kane,L.P.、M.N.Mollenauer、Z.Xu、C.W.Turck和A.Weiss。 依赖于Akt的磷酸化特异性调节NF-κB依赖性转录的Cot诱导。 摩尔细胞。 生物22 : 5962-5974. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
34 Kane,L.P.,V.S.Shapiro,D.Stokoe和A.Weiss。 通过Akt/PKB激酶诱导NF-κB。 货币。 生物9 : 601-604. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
35 Kang,S.S.,Y.K.Chun,M.H.Hur,H.K.Lee,Y.J.Kim,S.R.Hong,J.H.Lee,S.G.Lee和Y.K.Park。 人类乳腺癌中葡萄糖转运蛋白1(GLUT1)表达的临床意义。 日本。 癌症研究杂志93 : 1123-1128. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
36 Le Goffe,C.、G.Vallette、L.Charrier、T.Candelon、C.Bou-Hanna、J.-F.Bouhours和C.L.Loboisse。 2002.人类上皮细胞对H的耐药性的代谢控制 2 O(运行) 2 和无压力。 生物化学。 约364 : 349-359. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
37. Le Goffe,C.、G.Vallette、A.Jarry、C.Bou-Hanna和C.L.Laboisse。 1999.体内碳水化合物代谢操纵:破译细胞抵抗一氧化氮攻击的防御机制的新策略。 生物化学。 约344 : 643-648. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
38 Lindsten,T.、A.J.Ross、A.King、W.X.Zong、J.C.Rathmell、H.A.Shiels、E.Ulrich、K.G.Waymire、P.Mahar、K.Frauworth、Y.Chen、M.Wei、V.M.Eng、D.M.Adelman、M.C.Simon、A.Ma、J.A.Golden、G.Evan、S.J.Korsmeyer、G.R.MacGregor和C.B.Thompson。 促凋亡Bcl-2家族成员Bak和Bax的联合功能对多组织的正常发育至关重要。 分子细胞6 : 1389-1399. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
39. Madrid,L.V.、C.Y.Wang、D.C.Guttridge、A.J.Schottelius、A.S.Baldwin,Jr.和M.W.Mayo。 2000。Akt通过刺激NF-κB的RelA/p65亚基的反式激活潜能来抑制细胞凋亡。 摩尔细胞。 生物20 : 1626-1638. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
40 Mandic,A.、K.Viktorsson、M.Molin、G.Akusjarvi、H.Eguchi、S.I.Hayashi、M.Toi、J.Hansson、S.Linder和M.C.Shoshan。 2001。顺铂以ΔMEKK1依赖的方式诱导Bak的促凋亡构象。 摩尔细胞。 生物21 : 3684-3691. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
41 松山,S.和J.C.里德。 线粒体依赖性凋亡和细胞pH调节。 细胞死亡不同。 7 : 1155-1165. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
42 Nechushtan,A.、C.L.Smith、Y.T.Hsu和R.J.Youle。 Bax C末端的构象调节亚细胞定位和细胞死亡。 EMBO期刊18 : 2330-2341. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
43 Nicholls,D.G.和S.J.Ferguson。 1992年,生物能量学2,2。 编辑:英国伦敦学术出版社。
44 Noguchi,Y.、A.Saito、Y.Miyagi、S.Yamanaka、D.Marat、C.Doi、T.Yoshikawa、A.Tsuburaya、T.Ito和S.Satoh。 抑制促进性葡萄糖转运蛋白1 mRNA可以抑制肿瘤生长。 癌症快报。 154 : 175-182. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
45 Nunez,G.、L.London、D.Hockenbey、M.Alexander、J.P.Mckearn和S.J.Korsmeyer。 去调控Bcl-2基因表达可选择性延长生长因子衍生造血细胞系的存活时间。 免疫学杂志。 144 : 3602-3610. [ 公共医学 ] [ 谷歌学者 ]
46 Opferman、J.T.和S.J.Korsmeyer。 2003.免疫系统发育和维持中的细胞凋亡。 自然免疫学。 4 : 410-415. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
47 帕斯托里诺、J.G.、N.Shulga和J.B.Hoek。 2002.己糖激酶II的线粒体结合抑制Bax诱导的细胞色素 c(c) 释放和细胞凋亡。 生物学杂志。 化学。 277 : 7610-7618. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
48 Plas,D.R.、S.Talapatra、A.L.Edinger、J.C.Rathmell和C.B.Thompson。 2001年。Akt和Bcl-xL通过对线粒体生理的不同影响促进生长因子依赖性生存。 生物学杂志。 化学。 276 : 12041-12048. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
49 Rathmell,J.C.、M.G.Vander Heiden、M.H.Harris、K.A.Frauworth和C.B.Thompson。 2000.在缺乏外源信号的情况下,淋巴细胞的营养利用不足以维持细胞大小或生存能力。 分子细胞6 : 683-692. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
50 Romashkova,J.A.和S.S.Makarov。 NF-κB是AKT在抗凋亡PDGF信号传导中的靶点。 性质401 : 86-90. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
51 Sapico,V.和R.L.Anderson。 1970年钾离子对d-果糖1-磷酸激酶的调节。 生物学杂志。 化学。 245 : 3252-3256. [ 公共医学 ] [ 谷歌学者 ]
52 Scheid,M.P.、P.A.Marignani和J.R.Woodgett。 蛋白激酶B.Mol.细胞激活中的多种磷脂酰肌醇3-激酶依赖性步骤。 生物22 : 6247-6260. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
53 Sofroniew,M.V.、J.D.Cooper、C.N.Svendsen、P.Crossman、N.Y.Ip、R.M.Lindsay和F.Zafra。 1993年。在消融产生NGF、BDNF和NT3 mRNAs的靶能力后,成年间隔胆碱能神经元萎缩而非死亡。 《神经科学杂志》。 13 : 5263-5276. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
54 Sui,D.和J.E.Wilson。 1997.哺乳动物己糖激酶同工酶胞内定位的结构决定因素:融合构建物的胞内定位,融合构建物包含己糖激酶同工酶和绿色荧光蛋白的结构元素。 架构(architecture)。 生物化学。 生物物理学。 345 : 111-125. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
55 Summers,S.A.、V.P.Yin、E.L.Whiteman、L.A.Garza、H.Cho、R.L.Tuttle和M.J.Birnbaum。 1999.介导胰岛素刺激葡萄糖转运的信号通路。 纽约学院安。 科学。 892 : 169-186. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
56 Tsuruta,F.、N.Masuyama和Y.Gotoh。 2002.磷脂酰肌醇3-激酶(PI3K)-Akt途径抑制Bax向线粒体的移位。生物杂志。 化学。 277 : 14040-14047. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
57 Vander Heiden,M.G.、N.S.Chandel、E.K.Williamson、P.T.Schumaker和C.B.Thompson。 1997年Bcl-xL调节线粒体的膜电位和体积稳态。细胞91 : 627-637. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
58 Vander Heiden,M.G.、D.R.Plas、J.C.Rathmell、C.J.Fox、M.H.Harris和C.B.Thompson。 2001.生长因子可以通过对葡萄糖代谢的影响影响细胞生长和存活。 摩尔细胞。 生物学21 : 5899-5912. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
59 O.沃伯格。 1956.关于癌细胞的起源。 科学123 : 309-314. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
60 Wei,M.C.、W.X.Zong、E.H.Cheng、T.Lindsten、V.Panoutsakopoulou、A.J.Ross、K.A.Roth、G.R.MacGregor、C.B.Thompson和S.J.Korsmeyer。 促凋亡BAX和BAK:线粒体功能障碍和死亡的必要途径。 科学292 : 727-730. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
61 A.D.Whetton、G.W.Brazill和T.M.Dexter。 1984年。造血细胞生长因子通过其葡萄糖转运作用调节细胞存活。 EMBO期刊3 : 409-413. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
62 J.E.威尔逊。 1995.己糖激酶类。 生理学评论。 生物化学。 药理学。 126 : 65-198. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
63 J.E.威尔逊。 1989年。通过亲和层析步骤在Affi-Gel蓝上快速纯化大鼠脑线粒体己糖激酶。 生物化学准备。 19 : 13-21. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
64 温克勒、B.S.、M.W.绍尔和C.A.斯塔恩斯。 视网膜细胞中巴斯德效应的调节:对理解代偿代谢机制的影响。 实验眼研究76 : 715-723. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
65 Yamaguchi,H.和H.G.Wang。 蛋白激酶PKB/Akt通过抑制Bax构象变化来调节细胞存活和凋亡。 癌基因20 : 7779-7786. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
66 Younes,M.、R.W.Brown、M.Stephenson、M.Gondo和P.T.Cagle。 I期非小细胞肺癌中谷氨酸1和谷氨酸3的过度表达与生存率低相关。 癌症80 : 1046-1051. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
67 Younes,M.、L.V.Lechago和J.Lechago。 人红细胞葡萄糖转运蛋白的过度表达是人类结直肠癌发生的晚期事件,与淋巴结转移的发生率增加有关。 临床。 癌症研究2 : 1151-1154. [ 公共医学 ] [ 谷歌学者 ]
68 Zong,W.X.、T.Lindsten、A.J.Ross、G.R.MacGregor和C.B.Thompson。 2001.在缺乏Bax和Bak的情况下,仅结合生存前Bcl-2家族成员的BH3蛋白无法诱导凋亡。 基因发育15 : 1481-1486. [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]