摘要 G蛋白信号转导(RGS)蛋白的调节器加速 Gα蛋白亚基的GTPase活性 体外 , 负调节G蛋白偶联受体信号。 这个 哺乳动物RGS蛋白的生理作用基本上是未知的。 这个 RGS家族成员 rgs2型 很早就被克隆了 活化后T淋巴细胞反应基因上调。 收件人 调查RGS2的作用 体内 ,我们生成了 rgs2型 -缺陷小鼠。 我们发现 rgs2型 导致小鼠T细胞增殖减少 IL-2产生,转化为抗病毒免疫受损 体内 有趣的是, rgs2型 −/− 老鼠的表现也增加了 焦虑反应和男性在缺乏 认知或运动缺陷。 RGS2也控制突触发育 海马CA1神经元的基础电活动。 因此,RGS2 在T细胞激活、突触发育中起重要作用 海马体和情绪行为。
G蛋白偶联受体 (GPCR)控制基本细胞过程 胚胎发生和神经递质释放促进细胞存活, 增殖和分化。 异三聚体G蛋白是 由α、β和γ亚单位组成,将GPCR刺激传递给 下游信号通路( 1 ). 在配体结合方面,GPCR经历 细胞内环的构象变化促进 Gα上GDP与GTP的交换以及随后Gα的分离 和Gβγ。 GTP结合Gα和自由Gβγ都传播信号 通过与下游效应器的相互作用。 GPCR的停用 信号传导依赖于GαGTP水解的速率。
对GPCR脱敏的研究已经发现 和GTP激活(GAP)因子进化保守家族 Gα被称为“G蛋白信号调节因子”(RGS)。 RGS公司 蛋白质共享RGS结构域(≈120氨基酸),能够 加速Gα依赖的GTP水解及活性物质的转化 GTP-结合Gα到其非活性GDP-结合形式( 2 – 7 ). 第一个RGS 鉴定为酵母蛋白Sst2,在突变株筛选中分离 未能下调GPCR介导的交配反应 信息素( 8 – 9 ). 已鉴定出20多种哺乳动物RGS蛋白 ( 7 , 10 ). 最近的研究表明,RGS9–1控制着 小鼠眼睛的光敏反应( 11 ). Axin,其中包含 RGS结构域,负调控Wnt-signaling途径,以及 阿辛 -突变小鼠胚胎轴发育缺陷 ( 12 ). 然而,Axin对Gα没有可检测的GAP活性( 10 ). 这个 其他哺乳动物RGS蛋白的生理作用尚待研究 已建立。
RGS家族成员 rgs2型 被克隆为早期反应 活化T细胞中基因上调( 13 – 14 ). RGS2也是 刺激后中枢神经系统(CNS)神经元上调 唤起长期神经元可塑性( 15 – 16 ). 体外 ,RGS2 与Gα相互作用 2011年第2季度 并刺激其GTPase 活动( 17 – 18 )和RGS2在细胞中过度表达抑制 Gα 我 - ( 15 )和 Gα 秒 -从属的( 19 )发送信号。 调查 RGS2的作用 体内 ,我们生成了 rgs2型 -缺陷小鼠。 rgs2型 小鼠缺乏 导致T细胞活化受损 体外 和 在里面 活泼地 有趣的是,缺乏RGS2的小鼠也表现出雄性数量减少 攻击性行为和增加的焦虑,而形态学和 电生理分析表明RGS2在海马中的作用 CA1神经元功能。
材料和方法
rgs2型 突变小鼠。
编码RGS结构域的RGS2外显子4和5被替换为 PGK-新 R(右) 在反义方向。 G418-抗性 用PCR和Southern blot筛选E14K胚胎干细胞 用于同源重组。 靶向ES细胞克隆为 注入C57BL/6囊胚和杂合子 rgs-2型 +/− 通过与嵌合体交配获得的小鼠 C57BL/6J小鼠。 PCR引物:野生型等位基因 (5′-CCGAGTTCTGAAGAAAACATTG3′;5′GGGACTCCTGCTCATGTAGCAT3′)和 突变等位基因(5′-GCTAAAAGCGCATGCTCCAGAC-3′; 5′-GGCCCCACATTACACGAAC-3′)。 所有实验均使用 C57BL/6J背景的同窝小鼠(F5代)和小鼠 按照机构指南进行维护。
免疫细胞术。 对胸腺、淋巴结和脾脏的单细胞悬浮液进行染色 与FITC-、藻红蛋白-或生物素缀合的Abs反应 CD3ɛ、TCRαβ、CD4、CD8、CD25、CD44、CD28、CD69、CD11b(Mac-1)、, CD11c、B220、CD43、sIgM、sIg D或Gr-1。 生物素化抗体 使用链霉亲和素RED670进行可视化。 样品分析方法 流式细胞术使用FACScan(Becton Dickinson)。
T细胞和B细胞分析。 对于增殖试验,用 PMA(10 ng/ml,佛波酯-肉豆蔻酸酯醋酸盐)+ 钙 +2 可溶性离子载体(100 ng/ml,离子霉素) 抗CD3(0.1–1μg/ml,克隆145–2C11)、抗CD28(0.02–0.2 μg/ml,克隆37.51)或重组小鼠IL-2(50单位/ml) 一式三份,持续12、24、48、72或120小时,然后进行12小时脉冲 带有[ 三 H] 胸腺嘧啶(1μCi/ml)。 细胞因子 通过ELISA测定产量。 用于B细胞分析,脾B 淋巴细胞被纯化(90-95%的B220 + 单元格) 通过负磁分选和各种刺激激活。 基础 血清Ig水平(IgM、IgG1、IgG2a、IgG-2b、IgG3和IgA)为 通过ELISA测定( 20 ). 用于淋巴细胞脉络膜脑膜炎病毒(LCMV) 感染,小鼠感染了LCMV(700个斑块形成单位, (s.c.)进入后脚垫。 每天测量细胞浸润 如前所述( 21 ).
行为研究。 对4至5个月大的性别匹配的同窝小鼠进行检查 神经运动功能( 22 ):触须、眼睛、, 抬高/支撑/站立、肌肉张力、尾巴悬吊引起的转弯 肢体/手指伸展、耳朵反射、眨眼和瞳孔 对淡淡、甜味/苦味的接受/拒绝的反应,以及 朝向声音的方向。 昼夜活动和野外活动(即。, 笼式交叉、总距离、垂直运动) 装有红外传感器的笼子。 勘探测试由执行 将老鼠放在白色圆盘(直径183-cm)的中央 或者没有对象分布在四个象限中。 老鼠是视频 跟踪(七次试验)。 对粪便颗粒和粪便进行计数。 电动机 通过旋转杆任务分析协调性。 对于平衡任务 老鼠被尾巴抓住,可以抓住悬空的水平线 带有后肢的木棒(3毫米),并记录时间 让老鼠把自己拉到平衡和摔倒的次数。
在空间水迷宫中对小鼠进行了7天的研究 西南象限隐伏台地( 22 ). 第7天,最后一次调查 进行试验(无平台水池中60s)。 从第8天到 16,随着平台向东北方向移动,重新进行了测试 象限(反转,每天2次试验)。 找到平台和 测量总距离。 在T迷宫测试中,在第1天,小鼠 被放置在一个空迷宫中10分钟,只能进入迷宫中央 和右臂。 在迷宫周围放置了几个物体作为线索。 打开 第2天,每个受试者再次被放置在T型迷宫中,并获得 迷宫的左臂。 观察小鼠5分钟 记录在新地区和第一选择的时间。 下台 还进行了回避试验,要求小鼠 请记住,在离开安全平台之前,会导致脚部受伤 冲击(1s,0.12 mA)。 平台上的延迟记录在每个 试验。 使用塑料管的位移测试攻击性 (长30厘米,长3.05厘米)。 A类 rgs公司 2 −/− 和室友控制鼠标 释放到管子的两端,第一只老鼠退出 被认为是“失败者”,也就是说,这只老鼠被认为是 两者中攻击性较小的。 对于光/暗偏好测试, 笼子分为黑暗和光明两部分 每只老鼠每半只测量一次。
电生理学。 电生理学研究按所述进行( 23 ). 将单个海马脑片(400μm)与人工 脑脊液(2毫升/分钟;95%饱和 O(运行) 2 和5%CO 2 30°C)。 在10 kHz下对场电位进行采样,并用 电路板6 软件(Axon Instruments, 加利福尼亚州福斯特市)。 场兴奋性突触后电位(EPSP) 用置于辐射层中的微量移液管(2–4 MΩ)记录 CA1区域。 在沙弗抵押品处进行刺激。 测试 刺激频率为0.1Hz。 破伤风刺激包括 四组100-Hz的刺激以10-s的间隔持续500ms。 EPSP斜率由上升阶段的线性回归计算得出 峰值响应的10–65%。 EPSP斜率的基线值为 从最初5分钟开始,定义为100%。 通过绘制振幅来构建输入/输出关系 突触前截击(输入)vs.EPSP斜率(输出)。
结果和讨论
rgs2型 基因靶向。
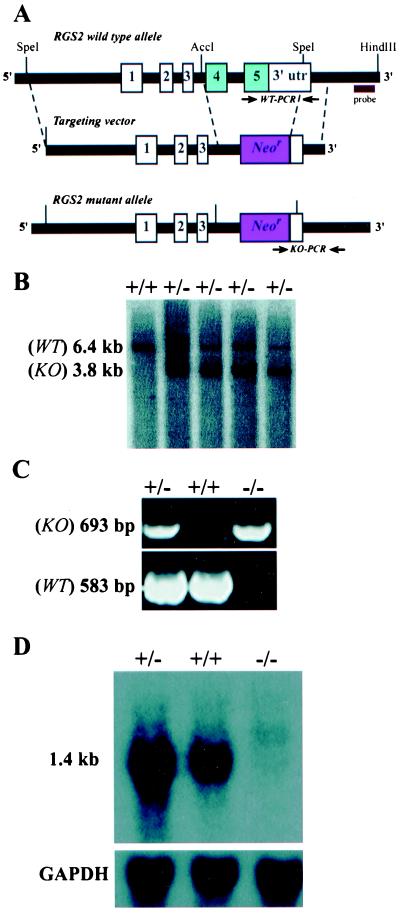
这个 rgs2型 通过替换使ES细胞中的位点失活 外显子4和5对应于RGS结构域(图。 1 A类 ). 培育嵌合小鼠 获得突变株的种系传播 rgs2 等位基因 (图。 1 B类 和 C类 ). 这个 rgs2型 突变 大脑组织的Northern印迹分析表明,该结果无效 (图。 1 D类 ). rgs2型 −/− 老鼠是 出生于预期的孟德尔频率,有生育能力 正常生长。 无解剖或组织学异常 观察。 所有造血谱系的分化,包括 中性粒细胞、巨噬细胞、红细胞和血小板在 rgs2 −/− 老鼠。
图1。
的生成 rgs2型- 缺陷小鼠。 ( A类 ) rgs2型 目标载体。 ( B类 )Southern印迹 (见中的3′侧翼探头 A类 )来自 rgs2型 突变ES细胞克隆。 野生型( 重量 )和突变型 ( 击倒对手 )显示了条带。 ( C类 )的基因分型 rgs2型 老鼠。 WT和KO PCR引物如所示 A类 (箭头)。 野生型的损失 rgs2型 基因组Southern杂交证实了等位基因。 ( D类 ) 脑mRNA的Northern印迹分析 rgs2型 重量 (+/+)、杂合子(+/-)和KO(−/−)小鼠(全长 rgs2型 cDNA探针)。
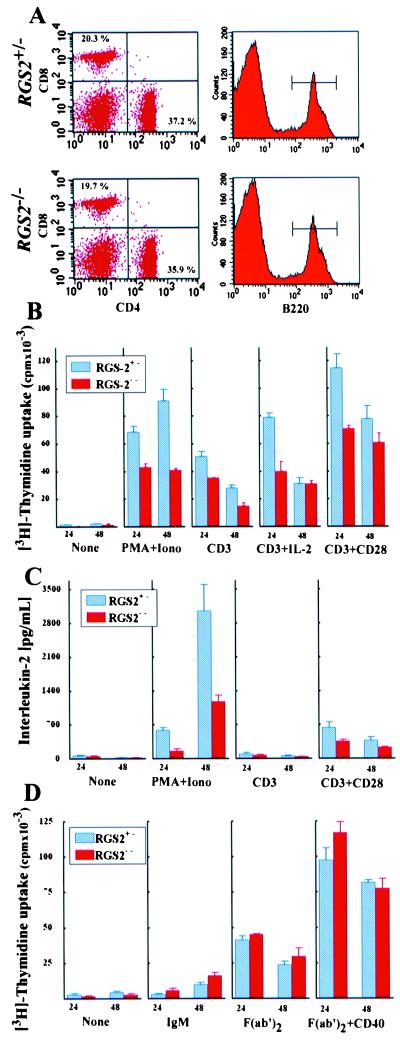
缺陷增殖和IL-2的产生 rgs2型 −/− T细胞。 因为TCR后激活的T细胞中诱导RGS2表达 有丝分裂原如ConA或PMA-plus的参与或刺激 钙 2+ 离子载体(PMA+Iono)(参考。 14 而数据不是 如图所示),我们确定RGS2是否在T细胞激活中起作用。 rgs2型 −/− 小鼠数量正常 CD4亚群 + 和CD8 + T型 淋巴器官中的细胞和B细胞(图。 2 A类 ). 这个 TCRαβ、CD3、CD4、CD8、CD28、CD45、CD5、, 硫酸钾 b条 两个脾脏上的CD44、LFA1、CD25和CD69 和淋巴结外周CD4 + 和 CD8(CD8) + T细胞在 rgs2型 +/− 和 rgs2型 −/− 老鼠(未显示)。 检查 外周T细胞功能,来自淋巴结的T细胞 rgs2型 +/− 和 rgs2型 −/− 室友被刺激 抗CD3抗体、抗CD3加抗CD28抗体或PMA加 钙 2+ -电离层。 扩散 在里面 体外 属于 rgs2型 −/− T细胞是 由于TCR的参与,赤字大幅减少 CD28协同模拟无法克服(图。 2 B类 ). 与RGS2的标识一致 活化T细胞中的早期反应基因( 13 – 14 ),增殖的 刺激24h时缺陷最明显。 诱导和 细胞凋亡动力学在 rgs2型 +/− 和 rgs2型 −/− T细胞(未显示)。 因此,RGS2 作为T细胞TCR激活的直接早期基因下游 细胞。
图2。
增殖和IL-2生成受损 rgs2型 −/− T细胞。 ( A类 )正常 CD4人群 + 和CD8 + T细胞和 B220型 + 淋巴结中的B细胞 rgs2型 −/− 老鼠。 每个象限中的数字 表示每个子集的百分比。 ( B类 )扩散。 淋巴结T细胞(2×10 5 /井)来自 rgs2型 −/− 和 rgs2型 +/− 使用PMA激活小鼠 [10 ng/ml]+钙 +2 -离子载体[100 ng/ml],TCR 用或不用CD28刺激[抗CD3α单克隆抗体(0.1μg/ml)] 共刺激[抗CD28单克隆抗体(0.02μg/ml)]或IL-2[50 单位/ml]。 结果显示为平均值[ 三 H] 胸腺嘧啶 摄取±SD rgs2型 +/− 和 rgs2型 −/− T细胞在统计学上 重要的( t吨 测试, 对 < 0.05). ( C类 )IL-2生成。 淋巴结T细胞被激活 如上所述,并在24和48小时通过ELISA测定IL-2 刺激后。 显示了IL-2产生量±SD的平均值。 ( D类 )B细胞的激活。 纯化脾B细胞 (1 × 10 5 /well)一式三份培养24小时 在单独培养基(无)或含有抗IgM(20)的培养基中培养48小时 μg/ml),抗IgM(Fab′) 2 (15μg/ml)有或无 抗CD40(5μg/ml)。 结果显示为平均值 [ 三 H] 胸腺嘧啶核苷摄取±SD。
除了增殖缺陷外, rgs2型 −/− T细胞显著产生 与对照组相比,T细胞生长因子IL-2水平较低 (图。 2 C类 ). IL-2不足 就其本身而言 不会 解释增殖缺陷,因为补充IL-2没有 恢复增殖正常(图。 2 B类 ). 这个 高亲和力IL-2受体α链(CD25)及其活化标志物 CD69、CD44、ICAM1和CTLA4在正常范围内上调 正常动力学 rgs2型 −/− T细胞 对TCR介入或丝裂原治疗的反应(未显示)。 这个 T细胞增殖功能缺陷(图。 2 B类 ) 和细胞因子的产生(图。 2 C类 )也可以在中观察到 rgs2型 −/− T细胞用 PMA/钙 2+ 电离层,一种绕过的刺激物 近端TCR信号。 与这一发现一致,动力学和 早期TCR介导的信号事件的程度,包括 钙 2+ 动员,整体酪氨酸 磷酸化以及MAPK和SAPK/JNK的激活在 rgs2型 −/− 淋巴结T细胞(未显示), 表明其近端TCR信号通路完整。
关于B细胞, rgs2型 −/− 老鼠 显示正常数字和微分(未显示)。 在 体外 扩散 rgs2型 −/− B类 细胞对抗IgM抗体治疗的反应 F(ab′) 2 抗IgM Ab片段、抗CD40片段, 或LPS与 rgs2型 +/− B类 电池(图。 2 D类 和数据未显示)。 此外,基线 血清Ig水平与 rgs2型 −/− 和 rgs2型 +/− 老鼠。 因此,不需要RGS2 用于B细胞激活。 我们的结果表明,抗原受体触发了 增殖和IL-2需要T细胞中RGS2的表达 生产。
趋化因子是T细胞功能的关键调节因子,通过 静止和活化T细胞表面表达的GPCR( 24 ). 研究还表明,RGS家族成员在 细胞系可以调节趋化因子受体信号( 18 ). 然而,没有 在休息和预激活(6小时)之间观察到差异 在趋化因子治疗前用抗CD3激活) rgs标准 2 +/− 和 rgs标准 2 −/− CD4细胞 + 或CD8 + 增殖或细胞中的T细胞 趋化因子SDF-1α、RANTES或MIP-1α引起的迁移 (未显示)。 这些结果并不排除RGS2对T细胞的调节 对其他趋化因子受体介导的信号的反应性。 此外, rgs标准 2 +/− 和 rgs标准 2 −/− T淋巴细胞显示 对GPCR激动剂溶血磷脂酸的类似反应, 组胺和腺苷(未显示)。 功能如下的GPCR RGS2控制下的T细胞尚待鉴定。
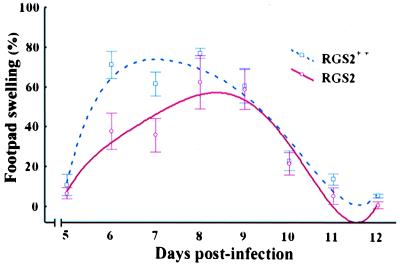
免疫力受损 rgs2型 −/− 老鼠。 确定RGS2是否在T细胞反应中起作用 在里面 活泼地 , rgs2型 +/− 和 rgs2型 −/− 在脚垫中注射老鼠 带LCMV( 21 ). rgs2型 +/− 小鼠产生了 从第6天开始,LCMV诱导的有效脚垫肿胀反应 感染后(图。 三 ). 相比之下 足垫肿胀反应明显减少 rgs2型 −/− 小鼠,表明RGS2 有效的抗病毒反应需要表达 在里面 活泼地 因此 体外 扩散赤字和 IL-2的产生 rgs2型 −/− T细胞 转化为抗病毒反应受损 体内 , 表明RGS2表达在生理上与正常 T细胞功能。 这些结果提供了第一个遗传证据 RGS蛋白在淋巴细胞活化中起作用。
图3。
减少LCMV引起的足垫肿胀 rgs2型 −/− 老鼠。 小鼠在 带有LCMV的脚垫,并测量肿胀度。 脚垫平均肿胀 (与感染前脚垫厚度相比增加的百分比) 每组六只动物。
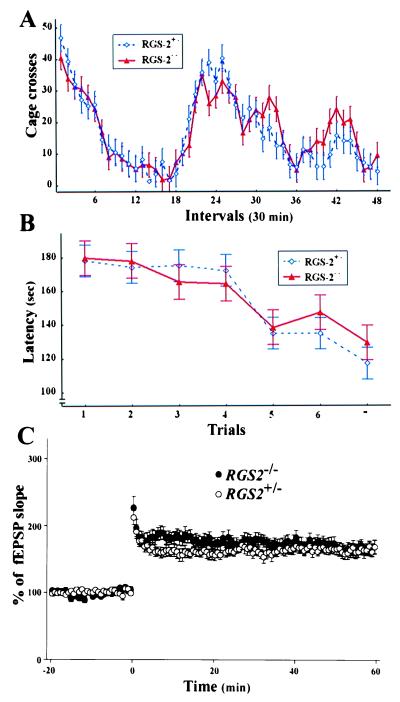
RGS2控制男性攻击和焦虑。 在我们评估突变小鼠的过程中,我们注意到了不寻常的战斗 男性之间 rgs2型 +/− 和 rgs2型 −/− 有时 导致严重受伤。 刺激触发长期可塑性 中枢神经系统诱导海马、皮层、, 尾状壳核、纹状体和杏仁核( 15 – 16 ). 因为这些地区 调节各种行为途径,我们调查RGS2是否 在中枢神经系统功能中起作用。 我们首先确定RGS2是否 小鼠的缺乏导致运动功能的改变。 两者都有 rgs2型 −/− 和 rgs2型 +/− 同窝小鼠表现正常 电机响应(测试列于 材料和方法 ). 突变小鼠的昼夜活动正常(图。 4 A类 ),这是探索性的 在两次独立的野外和勘探试验期间的行为(不是 如图所示)。 rgs2型 −/− 老鼠也表现出 旋转杆的适当性能(图。 4 B类 )和 平衡测试(未显示),确认神经系统的完整性 负责运动协调和平衡的途径。 空间和 条件学习,由隐藏平台、水迷宫、, 和被动回避测试,在 rgs2型 −/− 和 rgs2型 +/− 同窝的人。 长期 个体Schaffer侧支CA1通路的增强 海马切片在 rgs2型 −/− 和 rgs2型 +/− 鼠标(图。 4 C类 ). 这些 数据表明RGS2缺陷对电机没有明显影响 反应、昼夜节律活动、探索行为、运动 协调,或空间学习和记忆。
图4。
正常的昼夜节律活动、运动功能和长期增强 (长期有形资产) rgs2型 −/− 老鼠。 ( A类 ) 在24小时(12小时)内监测昼夜活动 光/暗循环)。 每30分钟累积的平均交叉数 显示间隔±SD。 ( B类 )普通电机 旋转试验中的功能。 保留时间平均值 显示(延迟)±SD。 试验表明 转子转速(每次试验10–40 rpm,增加5 rpm)。 ( C类 )破伤风诱导的CA1神经元LTP。 平均值 从11获得的归一化场EPSP(fEPSP)斜率测量值 海马4片 rgs2型 +/− 和4 rgs2型 −/− 老鼠。
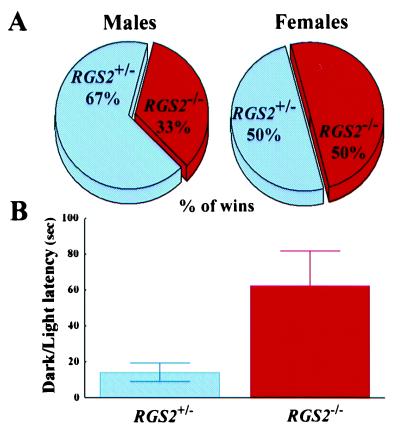
社会支配和领土侵略是很有特色的 雄性小鼠的行为( 25 ). 有趣的是, rgs2型 −/− 雄性小鼠表现出显著的 与他们相比减少了攻击行为 rgs2型 +/− 室友,而 攻击行为 rgs2型 −/− 女性的 小鼠是正常的(图。 5 A类 ). 因为攻击与焦虑有关( 25 ),我们受到 rgs2型 −/− 雄性小鼠到光明/黑暗 偏好测试。 rgs2型 −/− 小鼠表现出 与相比,更喜欢黑暗 rgs2型 +/− 控制室友(图。 5 B类 )表明焦虑加剧。 与此一致 行为表型, rgs2型 −/− 老鼠是 发现粪便颗粒脱落量明显高于 rgs2型 +/− 在 光/暗偏好测试(2.3±0.6 vs.0.8±0.3 颗粒)和勘探试验(3.5±0.6 vs.1.3±0.6 颗粒)。 此外, rgs2 −/− 老鼠 表现出对声音惊吓的反应增强。 这些数据显示 RGS2控制神经回路的攻击性和焦虑。
图5。
RGS2调节男性的攻击性和焦虑。 ( A类 )减少 男性攻击性行为。 攻击性在以下两组中进行测量 男性或女性 rgs2型 −/− 和 rgs2型 +/− 采用替代试验。 以每组位移百分比表示的结果 (“获胜”)。 每组进行了18项试验。 ( B类 )焦虑加剧。 测量焦虑反应 通过暗/光偏好测试。 注意增加的偏好 在黑暗的环境中 rgs2型 −/− 老鼠。 平均暗/光潜伏期±SD的差异为 具有统计学意义( t吨 测试; 对 < 0.05).
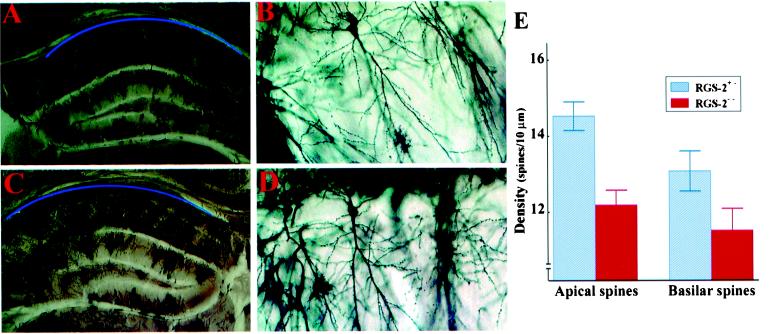
RGS2在突触发育和基底电活动中的作用 海马CA1神经元。 恐惧和焦虑通常涉及杏仁核和某些成分 海马对杏仁核的输入会影响恐惧( 26 ). 海马CA1区神经元向杏仁核投射 海马体的切除会影响恐惧行为( 27 ). 此外,还提出RGS2可以调节活动 G蛋白偶联代谢型谷氨酸受体1 与海马体长期突触可塑性有关( 28 ). 详细检查 rgs2型 −/− 老鼠 结果显示海马体中神经元的数量(图。 6 A–D ),在另一个大脑中 细胞核、脑干、小脑和皮层(未显示) 受RGS2缺陷的影响。 有趣的是,树突 大脑皮层神经元的形态和分支具有可比性 rgs2型 +/− 和 rgs2型 −/− 小鼠,海马CA1神经元 rgs2型 −/− 小鼠表现出显著的 与相比,顶棘和基底棘密度降低 那些 rgs2型 +/− 控制室友(图。 6 E类 ). 脊椎的数量与突触数量相关 和神经元可塑性( 29 ). 重要的是 脊椎数 rgs2型 −/− CA1神经元 与显著减少的电气输入/输出相关 这些单元格中的关系(图。 7 A类 和 B类 ). 这些数据表明,RGS2在 海马CA1突触发育与基础电活动 神经元。
图6。
CA1海马神经元的脊椎密度降低 rgs2型 −/− 老鼠。 ( A–D ) 海马组织学 rgs2型 +/− ( A类 和 B类 )和 rgs2型 −/− ( C类 和 D类 )老鼠。 蓝线划定了CA1神经元区域。 CA1区的正常结构 rgs2型 −/− 老鼠。 高尔基-考克斯染色,×4和 ×200. ( E类 )脊椎数量减少 rgs2型 −/− CA1神经元。 密度 顶棘和基底棘的(棘/10μm±SD)为 由摄像机lucida确定。 顶棘和基底棘的差异 密度具有统计学意义( t吨 测试, 对 < 0.005).
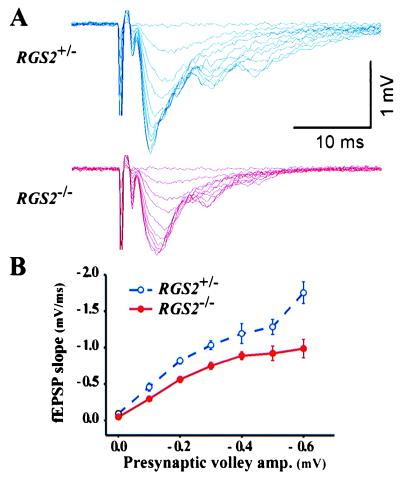
图7。
大脑中CA1神经元的基础电活动受损 rgs2型 −/− 老鼠。 ( A类 和 B类 )CA1途径中输入/输出关系的减少 在里面 rgs2型 −/− 老鼠。 叠加录音 诱发的CA1场兴奋性突触后电位(fEPSP) 电刺激Schaffer侧支输入。 输入:峰值 突触前截击的幅度。 输出:现场EPSP斜率测量 EPSP上升阶段为10–65%。 数据来自七个海马体切片 第页,共四页 rgs2型 +/− 和四个 rgs2 −/− 老鼠。
攻击行为和恐惧反应的改变很重要 高度流行的精神疾病的表现,如 抑郁或成瘾行为。 因为这些疾病 承担着巨大的社会经济负担,这对 确定可能参与启动和/或 这些行为“特征”演变为临床表现 “疾病。”多个G蛋白偶联受体可以调节 这些行为以及调节这些行为的药物 受体已被开发用于缓解焦虑症和 侵略。 我们的研究提供了遗传证据 G蛋白信号转导的分子调节因子RGS2导致受损 海马突触发育,减少男性攻击性 行为,增加恐惧。 因此,RGS-家族成员,如RGS2 可能与人类的遗传倾向有关 神经精神障碍,可能成为 新一代神经药物。 rgs2型 −/− 老鼠也是一种有用的动物 阐明恐惧和男性攻击的分子机制的模型。
G蛋白偶联受体调节 发育、细胞激活和行为。 本研究表明 RGS2是RGS家族的一员,在T细胞中起重要作用 增殖和IL-2生成。 T细胞激活缺陷 观察 体外 转化为抗病毒功能受损 响应 体内 表明RGS2在生理上 与正常T细胞功能和建立 有效的抗病毒免疫反应。 此外,缺乏RGS2的小鼠 表现出明显减少攻击性行为和增加焦虑 在没有任何可测量的认知和运动缺陷的情况下。 此外,形态和电生理分析表明 RGS2的表达是突触产生所必需的 海马CA1神经元的可塑性。 因此,RGS2至关重要 调节T细胞活化、神经元功能和情绪恐惧, 和侵略 体内 .
致谢 我们非常感谢K·巴赫迈尔、Y·Y·孔和我。 科齐拉兹基寻求帮助,桑德斯编辑手稿。 J.M.P.和J.R.由医学研究资助 加拿大委员会。 D.P.S.由美国国立卫生研究院支持 授予AA11605。
缩写
全球采购控制报告 G蛋白偶联受体
间隙 GTP激活
RGS公司 G蛋白信号调节器
中枢神经系统 中心的 神经系统
锿 胚胎干
LCMV公司 淋巴细胞性脉络膜脑膜炎 病毒
EPSP公司 兴奋性的突触后电位
脚注
印刷前在线发布的文章: 程序。 国家。 阿卡德。 科学。 美国 , 10.1073/pnas.220414397。
文章和出版日期见www.pnas.org/cgi/doi/10.1073/pnas.220414397
工具书类
1 Gilman A G.Annu生物化学评论。 1987; 56:615–649. doi:10.1146/annurev.bi.56.070187.003151。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
2 伯曼·D·M、威尔基·T·M、吉尔曼·A·G·赛尔。 1996; 86:445–452. doi:10.1016/s0092-8674(00)80117-8。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
三。 Watson N、Linder M E、Druey K M、Kehrl J H、Blumer K J.Nature(伦敦),1996年; 383:172–175. doi:10.1038/383172a0。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
4 Hunt T W,Fields T A,Casey P J,Peralta E G.Nature(伦敦),1996年; 383:175–177. doi:10.1038/383175a0。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
5 Snow B E、Hall R A、Krumins A M、Brothers G M、Bouchard D、Brother C A、Chung S、Mangion J、Gilman A G等。生物化学杂志。 1998; 273:17749–17755. doi:10.1074/jbc.273.28.17749。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
6 Koelle M R、Horvitz H R、Cell。 1996; 84:115–125. doi:10.1016/s0092-8674(00)80998-8。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
7 Berman D M,Gilman A G.生物化学杂志。 1998; 273:1269–1272. doi:10.1074/jbc.273.3.1269。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
8 Chan R K,Otte C A.《分子细胞生物学》。 1982; 2:11–20. doi:10.1128/mcb.2.1.11。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
9 Dohlman H G、Song J、Ma D、Courchesne W E、Thorner J.《分子细胞生物学》。 1996; 16:5194–5209. doi:10.1128/mcb.16.9.5194。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
10 Siderovski D P,Strockbine B,Behe C I.Crit Rev Biochem分子生物学。 1999; 34:215–251. doi:10.1080/10409239991209273。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
11 Chen C K、Burns M E、He W、Wensel T G、Baylor D A、Simon M I.Nature(伦敦)2000; 403:557–560. doi:10.1038/35000601。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
12 曾力、法戈托·F、张·T、许·W、瓦西塞克·T·J、佩里·W·L、第三、李·J·J、甘比纳·B·M、科斯坦蒂尼·F·赛尔。 1997; 90:181–192. doi:10.1016/s0092-8674(00)80324-4。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
13 Siderovski D P,Heximer S P,Forsdyke D R.DNA细胞生物学。 1994; 13:125–147. doi:10.1089/dna.1994.13.125。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
14 Heximer S P,Cristillo A D,Forsdyke D R.DNA细胞生物学。 1997; 16:589–598. doi:10.1089/dna.1997.16.589。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
15 Ingi T、Krumins A M、Chidiac P、Brothers G M、Chung S、Snow B E、Barnes C A、Lanahan A A、Siderovski D P、Ross E M等,《神经科学杂志》。 1998; 18:7178–7188. doi:10.1523/JNEUROSCI.18-18-07178.1998。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
16 Burchett S A、Volk M L、Bannon M J、Granneman J G.神经化学杂志。 1998; 70:2216–2219. doi:10.1046/j.1471-4159.1998.70052216.x。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
17 Heximer S P、Watson N、Linder M E、Blumer K J、Hepler J R.美国国家科学院院刊1997; 94:14389–14393. doi:10.1073/pnas.94.26.14389。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
18 Beadling C、Druey K、Richter G、Kehrl J、Smith K A.J Immunol。 1999; 162:2677–2682. [ 公共医学 ] [ 谷歌学者 ]
19 曾C-C,张晓云,内分泌。 1998; 139:4470–4475. doi:10.1210/endo.139.11.6282。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
20 Liu Q,Oliveira-Dos-Santos A J,Mariathasan S,Bouchard D,Jones J,Sarao R,Kozieradzki I,Ohashi P,Penninger J M,Dumont D.J Exp Med.1998; 188:1333–1342. doi:10.1084/jem.188.7.1333。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
21 Penninger J M、Fischer K D、Sasaki T、Kozieradzki I、Le J、Tedford K、Bachmaier K、Ohashi P S、Bachmann M F.《欧洲免疫学杂志》。 1999; 29:1709–1718. doi:10.1002/(SICI)1521-4141(199905)29:05<1709::AID-IMMU1709>3.0.CO; 2-O型。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
22 Whishaw I Q,Haun F,Kolb B.In:神经科学中的现代技术。 Windhorst U,Johansson H,编辑。 纽约:施普林格; 1999 [ 谷歌学者 ]
23 Lu Y M、Roder J C、Davidow J、Salter M W。科学。 1998; 279:1363–1367. doi:10.1126/science.279.5355.1363。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
24 Kehrl J H.免疫学。 1998; 8:1–10. doi:10.1016/s1074-7613(00)80453-7。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
25. Parmigiani S,Ferrari P F,Palanza P.Neurosci Biobhav Rev.1998; 23:143–153. doi:10.1016/s0149-7634(98)00016-5。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
26 罗根·M·T,勒杜·J·E·赛尔。 1996; 85:469–475. doi:10.1016/s0092-8674(00)81247-7。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
27 White N M,McDonald R J.Behav Brain Res.1993; 55:269–281. doi:10.1016/0166-4328(93)90122-7。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
28 Kammermeier P J,池田S R.神经元。 1999; 22:819–829. doi:10.1016/s0896-6273(00)80740-0。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
29 Moser M B.细胞分子生命科学。 1999; 55:593–600. doi:10.1007/s000180050317。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]