介绍 在真核细胞中,肌动蛋白丝集中在质膜下称为细胞皮层的一层中。 皮层内的肌动蛋白重排为细胞形状的改变、细胞运动、细胞粘附和细胞间通讯提供了分子基础。 结合膜蛋白和肌动蛋白丝的交联蛋白介导膜相关细胞骨架的形成。 其中一种蛋白质是radixin,它是ERM(ezrin/radixin/moesin)蛋白质的成员,定位于细胞表面结构,如微绒毛、皱褶膜和细胞粘附位点( 佐藤 等 ., 1991 , 1992 ; 弗兰克 等 1993年 ; Amieva和Furthmayr,1995年 ; 塞拉多尔 等 ., 1997 ).
ERM蛋白是近同源物,序列一致性为~75%( 阿平 等 ., 1994 ; 健内 等 ., 1994 ; Bretscher,1999年 ; 马盖特 等 ., 1999 ; Tsukita和Yonemura,1999年 )并具有三个结构域:一个N端FERM(带4.1蛋白和ERM同源性)结构域,包含约300个残基(radidin残基1–297),一个约200个残基的中心螺旋结构域(raditin 310–470)和一个约100个残基组成的C端尾结构域(RAdidin 477–583)。 ERM蛋白的FERM结构域负责与粘附分子的细胞质部分结合,而C末端尾部结构域与F-actin结合( 图鲁宁 等 ., 1994 ). FERM结构域已在位于质膜上的其他几种蛋白质中发现( 奇什蒂 等 ., 1998 )并且目前被认为形成一个蛋白质模块来调节蛋白质-蛋白质和蛋白质-膜的相互作用。
ERM蛋白在细胞皮层和胞浆之间的分配。 在细胞溶质中,ERM蛋白以屏蔽形式存在,其中FERM结构域与C末端尾结构域结合,以相互屏蔽其结合伙伴的结合位点( 安德列奥利 等 ., 1994 ; 马根丹兹 等 ., 1995 ; 加里和布雷彻,1995年 ; 平生 等 ., 1996 ). 该屏蔽分子通过磷脂酰肌醇4,5-二磷酸(PIP2)与FERM结构域的结合而被激活( 尼格利 等 ., 1995 ; 平生 等 ., 1996 ; 中村 等 ., 1999 ; 约内穆拉 等 ., 2002 ). 根蛋白FERM结构域与PIP2的头部基团肌醇-(1,4,5)-三磷酸(IP3)复合的最新晶体结构表明,IP3结合诱导FERM结构区的局部构象变化,从而释放C末端尾结构域( 滨田 等 ., 2000 ). ERM蛋白的未掩蔽状态通过C末端尾部结构域的磷酸化而稳定(综述 Tsukita和Yonemura,1999年 ; 布雷切尔 等 ., 2000 ).
迄今为止,已有三种粘附分子被鉴定为ERM蛋白的可能膜伙伴。 这是一种细胞表面透明质酸受体蛋白CD44( 筑田 等 ., 1994 ; 塞拉多尔 等 ., 1997 ),唾液凝集素家族的细胞表面糖蛋白,CD43( 约内穆拉 等 ., 1993 ; 塞拉多尔 等 ., 1998 )免疫球蛋白超家族膜蛋白ICAM-1( 海斯卡 等 ., 1998 ), -2 ( 海兰德 等 ., 1996 ; 海斯卡 等 ., 1998 )和-3( 塞拉多尔 等 ., 1997 ). 这些ICAM介导白细胞和内皮细胞与β2-整合素的结合。 ICAM-1、-2和-3通过N末端一个或两个免疫球蛋白折叠结构域结合淋巴细胞功能相关抗原-1(LFA-1),ICAM-1通过第三个免疫球蛋白质折叠结构域与补体受体3/Mac-1结合。 因此,ICAM在免疫系统的细胞-细胞通信中发挥着重要作用。
交联蛋白如何识别粘附分子仍然是一个深入研究的领域。 CD44和CD43具有分别由70和124个残基组成的细胞质域。 相反,ICAM的细胞质部分是短的细胞质尾肽。 例如,小鼠ICAM-2尾巴由28个残基组成。 最近,CD43和CD44的可能ERM结合区域已在其相邻的膜区中鉴定出来,这些膜区分别由31个和19个残基组成( 约内穆拉 等 ., 1998 ). 尽管没有发现明显的序列同源性,但所有这些区域都含有重复的碱基残基。 有趣的是,这些带正电荷的区域与钙粘蛋白β-连环蛋白结合的高负电荷区域形成鲜明对比( Huber和Weis,2001年 ). 由于这种基本残基簇是许多粘附分子和受体的膜旁区域的共同特征,ERM蛋白如何区分它们尚不清楚。 在这里,我们报告了与ICAM-2细胞质尾部结合的FERM结构域的第一个晶体结构。 该结构揭示了FERM结构域如何通过与子结构域C的相互作用识别细胞质尾部,该子结构域折叠成磷酸酪氨酸结合(PTB)样结构域,但显示出不同于典型PTB结构域的结合特异性。
结果和讨论 结构确定 如前所述纯化含有残基1–310的小鼠根蛋白FERM结构域( Hamada等人,2001年 ). 合成的小鼠ICAM-2肽由28个全细胞质尾部残基(残基250–277)组成。 获得了与每个不对称单元含有一个分子络合物的ICAM-2肽结合的根蛋白FERM结构域的晶体。 通过使用FERM结构域中的自由基进行分子替换来确定结构( Hamada等人,2000年 )并将分辨率调整为2.4Å 对 22.9%(免费 对 24.0%)。 当前模型包括FERM结构域的2–310个残基和ICAM-2肽的16个残基(残基4–19),以下称为FERM–ICAM-2复合物(图 1 A) ●●●●。 16个残基中的大多数在电子密度图上都有明确的定义(图 1 B) ●●●●。 ICAM-2肽的编号方案如图所示 1 C.没有为三个N-末端残基(残基1-3)和九个C-末端残基建立肽模型,这些残基在当前图谱中定义不清,可能是因为无序。
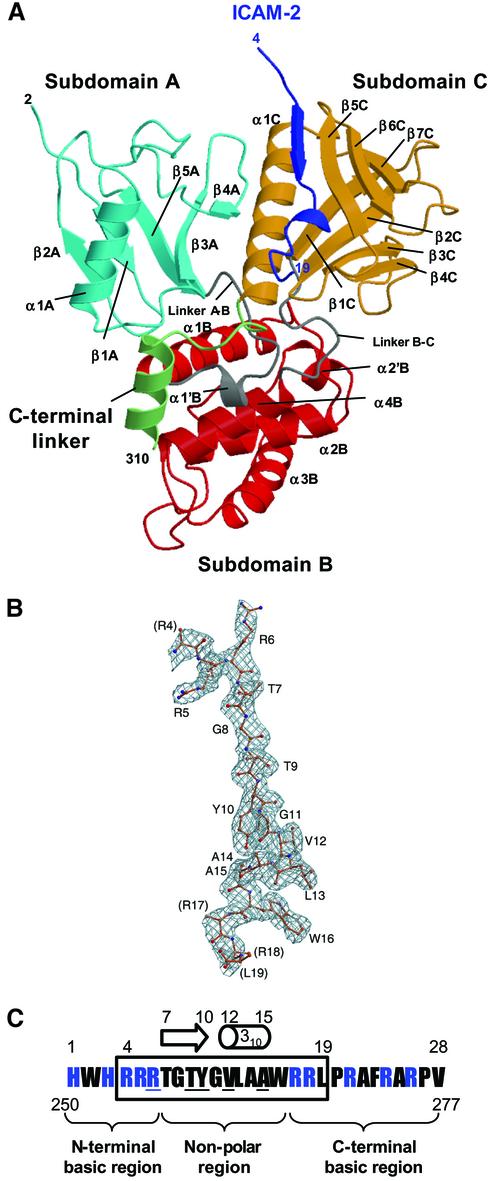
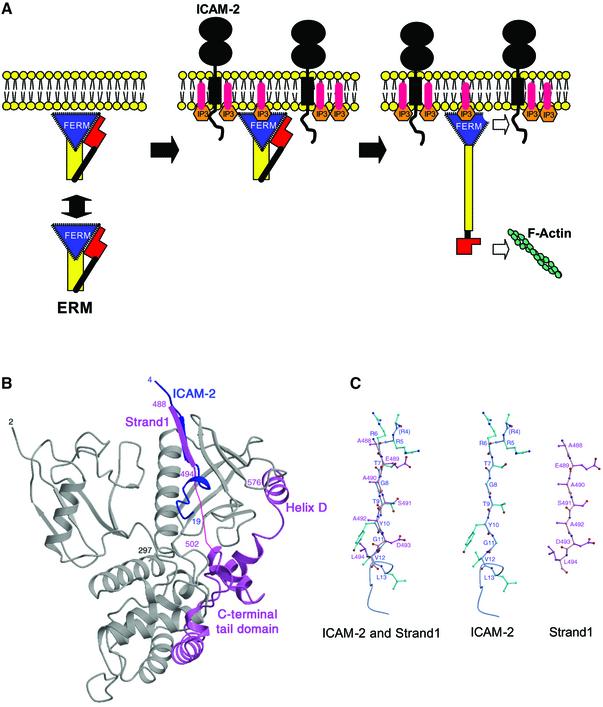
图1。 与ICAM-2尾肽结合的根蛋白FERM结构域的整体结构。 ( A类 )通过带状表示将基数FERM结构域结合到ICAM-2肽的视图。 ICAM-2肽以蓝色显示。 radixin FERM结构域由亚结构域A(浅蓝色)、B(红色)和C(棕色)组成。 连接体A–B(残基83–95)和B–C(残基196–203)为灰色,C末端连接体为绿色。 ( B类 )2中的ICAM-2肽模型 如果 o个 – 如果 c(c) 电子密度图在1σ水平上反相。 氨基酸残基用一个字母代码的标签表示。 括号中的标签表示其侧链未在地图中定义的终端残留物。 ( C类 )基于小鼠ICAM-2细胞质尾部序列合成的28-残基肽用于结构工作。基本残基为蓝色。 该肽有两个基本区域和它们之间的一个非极性区域。 当前地图上定义的16个肽残基被装箱。 与基数FERM域结合的关键残基下划线(见正文)。 短β链(残基7–10)和一条3 10 螺旋线(驻留12–15)用箭头和圆柱表示。
FERM域的总体结构 radidin FERM结构域包含三个亚结构域A(图中N末端82个残基,浅蓝色 1 A) B(残基96-195,红色)和C(残基204-297,棕色)。 亚结构域A具有典型的泛素折叠,亚结构域B具有α-螺旋束结构,被归类为酰基辅酶A结合蛋白样折叠。 子结构域C折叠成一个标准的七种品牌的β-三明治,带有一个长α-螺旋(α1C),被归类为PTB或pleckstrin-homology(PH)结构域。 这些子域结构与FERM域中基数的自由形式和IP3绑定形式基本相同( 滨田 等 ., 2000 ). C中的平均均方根(r.m.s.)偏差 α 通过ICAM-2-和IP3-结合形式中每个子域的成对叠加获得的原子,对于子域A、B和C,分别为0.58Å、0.86和0.89。 亚结构域B在螺旋α2′B和α3B之间有一个短的柔性环(残基160–165),显示出异常的局部偏差(~5Å)。在亚结构域C中,C末端螺旋α1C向结合的ICAM-2肽移动1,这是肽结合诱导的配合。 C末端残留物298–310(图中为绿色 1 A) 目前的结构形成一个稳定的构象,包括一个额外的螺旋(残基300-310)。 脯氨酸残基Pro297和螺旋α1C引导该片段沿着子结构域A和连接子A–B之间的界面运行。
与每个子域中的小偏差相比,ICAM-2结合的FERM结构域与自由形式的总均方根偏差相对较大(1.35Å)。 在这些全局结构比较中,发现主要偏差是由于子域A导致的,子域A相对于子域B和C的相互位置发生了移动,围绕A–B连接子旋转3.5°。 螺旋α1C的运动可能触发A子域的运动,尽管FERM–ICAM-2复合物的结构并不排除A子域运动的晶体阻塞效应。 与moesin FERM–C-tail复合物相比,上述FERM域中的主要结构变化也可见( 皮尔逊 等 ., 2000 ),平均均方根偏差为1.55Å,单位为C α 原子位置。 产生这种大偏差的一个主要差异是子域B和C中的构象差异,它们包含螺旋α2B和环α2B–α2′B以及β-片β5C–β6C–β7C。 如前所述,这些差异是由于与moesin复合体中C末端尾结构域结合时产生的感应配合所致( 滨田 等 ., 2000 ).
肽结构和识别 如图所示 1 C、 ICAM-2肽由三个区域组成:由非极性区域分隔的带正电荷的N端和C端区域。 N端和C端区域都是柔性的,而非极性区域形成一个短的β链(残基7-10),然后是一个短的3 10 螺旋(残基12-15)。 结构肽区域填充了子结构域C分子表面上的一个长而浅的凹槽(图 2 A) ●●●●。 该肽结合槽由螺旋α1C和链β5C的疏水侧链形成(图 2 B) ●●●●。 来自环β4C–β5C的Trp242也参与了沟槽的形成。 ICAM-2肽的11个残基(残基6-16)与子结构域C接触并埋藏1761Å 2 总可及表面积的百分比。 结合肽的β链与来自子结构域C的链β5C形成反平行β–β结合(图 2 C) ●●●●。 ICAM-2与FERM结构域的结合模式与与PTB结构域结合的磷酸酪氨酸肽的结合模式类似,稍后将讨论。 在我们的复杂结构中,八个主链-主链氢键稳定了ICAM-2结合; β链5个,3个 10 ICAM-2肽的螺旋。 这三个氢键有助于稳定空头3 10 螺旋结构,以及两个分子内主链-主链氢键(图 2 C) ●●●●。
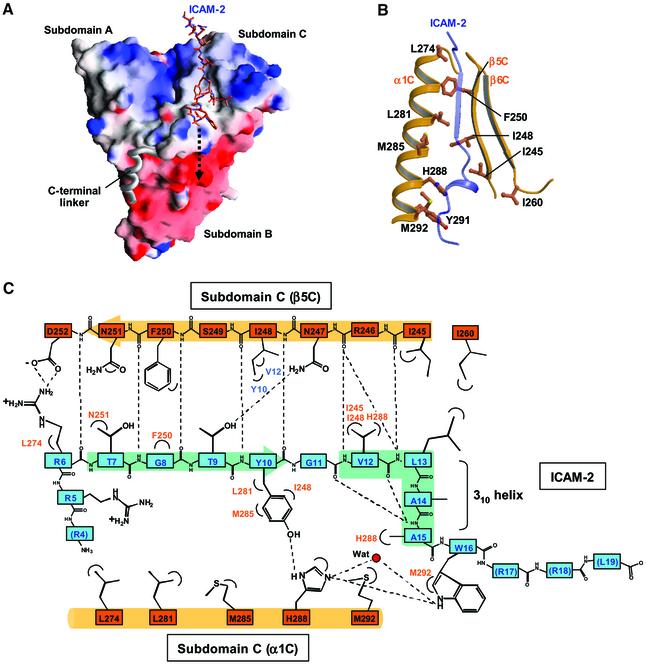
图2。 根蛋白FERM结构域对ICAM-2尾肽的识别。 ( A类 )从图中所示的同一方向观察基FERM域的表面静电势 1 答:。 范德瓦尔斯表面上绘制了正电位(蓝色,+14 kT/e)和负电位(红色,-14 kT/e)。 在复合晶体中发现的ICAM-2肽显示在棒状模型中。 无序的C末端基本区域由虚线箭头表示。 ( B类 )子结构域C上的ICAM-2结合槽主要由螺旋α1C和链β5C的疏水残基形成。 结合的ICAM-2肽显示在透明带模型中。 ( C类 )ICAM-2肽(蓝色)和亚结构域C(棕色)之间相互作用的示意图。 氢键用虚线表示。 ( D类 )FERM–ICAM-2复合物中发现的ICAM-2肽显示为棒状模型(浅蓝色),其相互作用残基来自子结构域C(棕色)。 氢键用虚线表示。 ( E类 )近距离观察ICAM-2肽与来自C亚结构域的His288介导的FERM结构域之间的疏水和氢键相互作用。
ICAM-2肽接触链β5C和螺旋α1C的极性和非极性残基。 接触包含氢键、盐脊和涉及侧链的疏水相互作用,这些共同产生肽结合的特异性(图 2 C和D)。 值得注意的是,ICAM-2肽的一段非极性残基(残基10–16)与短3形成紧密折叠 10 -螺旋线并与槽产生多个接触。 在这些残基中,Tyr10、Val12和Ala15将其侧链深深插入凹槽中,允许与来自螺旋α1C和链β5C的几个非极性残基发生紧密相互作用。 保存良好的His288残基(图 三 A) 来自螺旋的α1C位于与ICAM-2残基多次接触的中心,因此似乎在稳定肽结合方面发挥着关键作用(图 2 E) ●●●●。
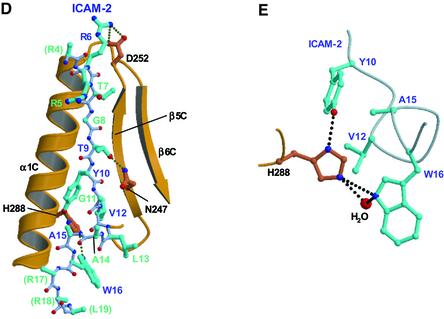
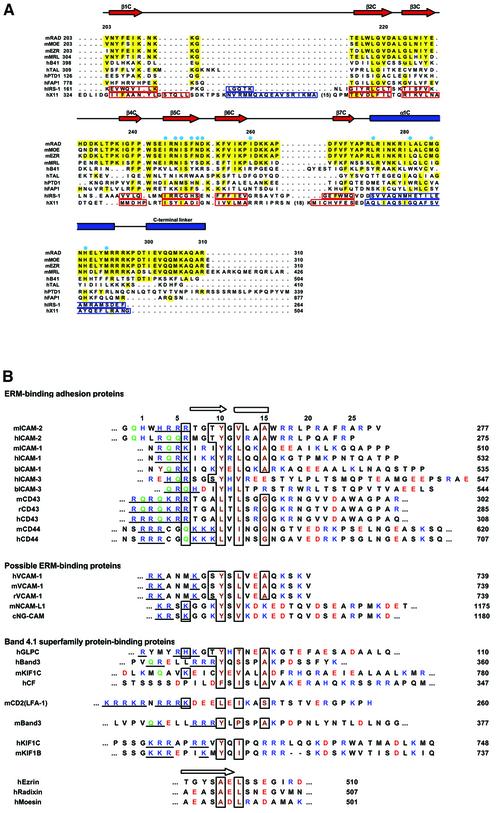
图3。 C亚结构域和FERM-结合肽的序列比对。 ( A类 )FERM结构域C子域与相关PTB结构域的二级结构元素和序列比对。 小鼠根素(mRAD)的FERM亚结构域C及其相关蛋白与位于顶部的根素FERM子结构域C的二级结构元素对齐:α-螺旋(蓝色矩形)和β-链(红色箭头)。 相同的残留物以黄色突出显示。 对齐的FERM亚结构域C为小鼠根蛋白(mRAD)、moesin(mMOE)、ezrin(mEZR)、merlin(mMRL)、人带4.1(hB41)、talin(hTAL)、蛋白酪氨酸磷酸酶D1(hPTPD1)和Fas相关蛋白酪氨酸磷酸酯酶1(hFAP1)。 对齐的PTB域是IRS-1 PTB域(hIRS1)和X11 PTB(hX11)。 这些PTB结构域的二级结构元素用蓝线(α-螺旋线)和红线(β-链)装箱。 小鼠FERM结构域与人类的结构域具有100%的同源性,与其他哺乳动物同源物的结构域的同源性大于99.7%。 蓝色圆圈表示根素C亚结构域残基与ICAM-2肽相互作用。 ( B类 )结合ERM蛋白的粘附分子和相关粘附分子的膜旁细胞质区域的序列比对。 碱性和酸性残留物分别以蓝色和红色显示。 位于N末端区域的基本簇被加下划线。 经常出现在N-末端碱性区域的谷氨酰胺以绿色显示。 用于与根素FERM结构域结合的ICAM-2肽的关键残基用棕色的疏水残基装箱。 来源为小鼠(m)、大鼠(r)、人(h)、牛(b)和线虫(c)。 列右侧的数字表示序列中的C末端残数。 ERM蛋白C末端尾部结构域的N末端区域也在图的底部用箭头表示链1。
使用表面等离子体共振(SPR)测量,我们发现小鼠根蛋白FERM结构域以高亲和力(16.4 nM)结合ICAM-2肽,如表所示 我 基于我们的复杂晶体结构,通过测量确定了几种突变或截短的ICAM-2肽的结合亲和力。 这些测量结果导致与FERM结构域的结合亲和力减弱了2-50倍,并使我们能够识别肽的关键残基,如下所述。
表I.ICAM-2肽与根蛋白FERM结构域的结合亲和力。
ICAM-2结合特异性的一个决定簇是Tyr10,它与His288形成氢键(2.7Å),并与来自子结构域C的Ile248、Leu281和Met285接触。 该Tyr残基在来自不同来源的所有ICAM中保守(图 三 B) ,用丙氨酸残基替换确实会导致结合亲和力显著降低16倍(表中的ICAM-2/Y10 我 ). ICAM-2肽的Val12是保守的,在一些ICAM中被Leu或Ile残基取代,表明其疏水性在与亚结构域C结合中的重要性。 Leu13是变异的,在分子表面与亚结构域C的Ile260接触。 Ala对Val12和Leu13的双重突变将结合亲和力降低11倍(表中的ICAM-2/VL12 我 ).
ICAM-2肽的Trp16也可能与His288形成直接氢键(3.5Å)和水介导氢键,尽管发现Ala对Trp16的单一突变只会将结合亲和力降低两倍(表中的ICAM-2/W16 我 ). 这种出乎意料的小贡献可以用Trp16在分子表面相当裸露来解释。 Trp16在ICAM-2中保守,但在其他ICAMs、CD43和CD44中变异(图 三 B) ●●●●。 关于N端区域的ICAM-2精氨酸三联体,Arg6与来自链β5C C端的Asp252形成盐桥(3.5Å)(图 2 D) ●●●●。 ICAM-2β链的Thr9与FERM链β5C的Asn247形成氢键(3.0Å)。 Arg6或Thr9每次被Ala取代都会导致结合亲和力的微弱降低(表中的ICAM-2/R6和ICAM-2/T9 我 ).
总之,我们提出ERM蛋白的FERM结合基序RxxxTYxVxxA(x代表任何氨基酸残基)。 基序中的关键元素是Y、V和A,它们在与FERM结构域的疏水相互作用中起着核心作用。 在几种来源的FERM结合肽中,Y和V位置仅限于疏水残基,A位置仅限于小残基(图 三 B) ●●●●。 基序中的两个极性残基R和T通过参与与FERM结构域的直接接触而在结合中具有一定意义。 ICAM-2的RxxxTYxVxxA基序之后是C末端基本区域,这对于下一节所述的强结合很重要。
C端特异性 ICAM-2肽的C末端区域与五个Arg残基高度正电荷(图 1 C) ●●●●。 在我们的复杂结构中,这个灵活的C末端区域在结构上没有表现出特定的相互作用,而是向子域B和C之间的高负电荷槽投射(图 2 A) ●●●●。 这个浅槽被假设为与FERM结合粘附分子细胞质尾部的基本残基相互作用的可能场所( 滨田 等 ., 2000 ). 事实上,删除该区域会将与FERM结构域的结合亲和力降低9倍(表中的ICAM-2/s2 我 ). 因此,可以想象该区域与酸性槽发生静电相互作用。 这种相互作用为FERM与ICAM-2的结合对离子强度敏感提供了合理的理由( Yonemura公司 等 ., 1998 ).
FERM与其他粘附分子的结合 最近,CD43在T细胞/APC(抗原呈递细胞)相互作用位点远端的ERM依赖性运动被证明是免疫突触形成的一个重要过程( Allenspach等人,2001年 ; Delon等人,2001年 ; 肖,2001 ). 我们发现FERM结构域将CD43肽与 K(K) d日 104 nM(表 二 ). CD43肽在分别对应于ICAM-2肽的Tyr10和Ala15的位置具有Leu和Gly残基。 这一事实表明,该位置的Tyr和Ala残基不一定是FERM结合的先决条件,并且可以被具有类似性质的残基取代。 此外,Thr9被Ala残基取代。 这些关键残基的替换也见于CD44肽中,这可能是CD43和CD44肽的亲和力弱于ICAM-2肽的原因之一。 ICAM-3肽的亲和力出乎意料地低( K(K) d日 757 nM)。 在ICAM-3肽中,ICAM-2的Ala15被非同源残基取代,并且C末端区域缺少基本残基(图 三 B) ●●●●。 这些可能会降低与FERM域的亲和力。
表二:。 ICAM-2相关肽与基数FERM结构域的结合亲和力。
观察到的ICAMs、CD43和CD44的结合亲和力与之前从 在体外 谷胱甘肽 S公司 -转移酶(GST)下拉结合试验和SPR测量( Hirao等人,1996年 ; Heiska等人,1998年 ; Yonemura等人,1998年 ). 细胞浆尾肽的等电点与其与ERM蛋白的结合亲和力之间存在正相关( Yonemura等人,1998年 ). 我们发现与ICAM-4和ICAM-5没有显著的结合亲和力(数据未显示)。
有趣的是,我们发现来自血管细胞粘附分子1(VCAM-1)的短胞质肽具有与ICAM-2的FERM识别基序有点类似的区域。 该VCAM-1肽缺乏长的C末端碱基区,而我们的SPR测量显示该VCAM1肽对FERM结构域具有显著的亲和力(149 nM)。 在静电相互作用中,接近RxxxTYxVxxA基序的碱基残基可能比C末端的远程碱基残基更重要。 我们还发现,序列相似性有限的神经细胞粘附分子L1(NCAM-L1)表现出相对较高的亲和力(61 nM)。 这两个新发现的粘附分子对radidin FERM结构域的亲和力强于ICAM-3。 值得注意的是,最近的生化研究表明,在粘附白细胞的新型内皮对接结构中,VCAM-1与ERM蛋白的动态相互作用( 巴雷罗 等 ., 2002 )以及轴突NCAM-L1与ERM蛋白的功能结合( 迪克森 等 2002年 ).
我们注意到,本研究中提出的FERM-结合基序类似于联癸糖和神经突蛋白的膜旁区域。 Syndecans是在所有粘附细胞上表达的硫酸乙酰肝素蛋白聚糖,参与细胞-细胞、细胞-基质粘附和硫酸乙酰肝素生长因子的信号传递。 神经毒素是脑特异性的细胞表面蛋白,分别与神经原和神经外毒素、脑特异性粘附分子和神经肽样分子结合。 我们发现,与ICAM-2相比,radidin FERM结构域结合syndecans和neurexin的亲和力相对较低(表 二 ). Syndecans和neurexins在其C末端有PDZ结合序列,分别与含有PDZ的衔接蛋白syntenin和CASK结合。 在细胞中,这些衔接蛋白可以增强合癸糖和神经连接蛋白与ERM蛋白的结合。 细胞内syndecans和neurexin的结合伙伴也可能是ERM蛋白质或其他含FERM的蛋白质的其他成员。 我们需要进一步的实验测试来回答这些问题。
膜靶向和揭开 ICAM-2肽的N-末端区域包含五个碱性残基,His1和3,以及Arg4-6(图 1 C) ●●●●。 在我们的结构中,这个地区是灵活的。 除了Arg6之外,这些基本残基没有观察到与FERM结构域的直接相互作用。 这种缺乏直接相互作用的现象似乎与用丙氨酸替代这些碱性残基一致(表中的ICAM-2/RR 我 )导致结合亲和力下降2倍。 对FERM–ICAM-2和FERM–IP3复合物结构的比较表明,这些Arg残基接近FERM–IP 3复合物中的结合IP3分子,但与叠加结构中的IP3分子没有直接接触。 最近,一些突变被引入ezrin以分析PIP2结合位点( Barret等人,2000年 ). 研究表明,FERM结构域膜结合表面的碱基残基突变会损害PIP2结合,而这些突变不会损害 在体外 与CD44胞质尾部的相互作用。 这一结果可以用我们的晶体结构来解释,其中IP3和ICAM-2的两个结合位点没有如上所述的重叠。
最近的SPR测量表明PIP2与ICAM-1和-2细胞质尾部肽相互作用( 海斯卡 等 ., 1998 ). 在质膜中,负电荷的PIP2分子通过静电相互作用与ICAM-2和其他具有细胞质尾部正电荷膜旁区域的粘附分子共定位,这似乎是合理的。 与黏附分子共定位的PIP2分子可以从胞浆向质膜招募掩盖的ERM蛋白,并解开ERM蛋白以随后与黏附蛋白的胞质尾部结合(图 4 A) ●●●●。
图4。 ERM蛋白的膜靶向和揭开。 ( A类 )ERM蛋白与膜中的PIP2和ICAM-2细胞质尾部结合的模型。 N端FERM、中心螺旋和C端尾域分别用蓝色三角形、黄色矩形和红色块表示。 ERM蛋白在细胞皮层和细胞溶质之间的分配。 与PIP2共定位的质膜中的ICAM-2。 PIP2分子从细胞溶质向质膜招募掩盖的ERM蛋白,并揭开掩盖的ERP蛋白,以便随后与粘附分子(如ICAM-2和肌动蛋白丝)的细胞质尾部结合。 ( B类 )FERM–ICAM-2复合物与莫西蛋白掩蔽形式的比较。 moesin FERM结构域中C-末端尾结构域(粉红色)的重叠–根蛋白FERM结构区上的C-尾复合物(灰色)与ICAM-2肽(蓝色)结合。 ( C类 )ICAM-2的β链(蓝绿色)和moesin C末端尾部结构域的1链(粉红色)的比较。
已发现moesin的C端尾结构域掩盖了亚结构域B和C之间的酸性沟槽( 皮尔逊 等 ., 2000 ),表明掩盖的全长ERM蛋白中的C末端尾部结构域阻止了ICAM-2肽的C末端碱性区与FERM结构域的酸性沟之间的静电相互作用。 此外,C末端尾结构域的N末端区域(链1)被建议结合子结构域C的凹槽,即ICAM-2肽在我们的复合晶体中结合的位置。 如图所示 4 B、 尽管ICAM-2链和C-末端尾部结构域的链1之间的序列同源性不明显(图 三 B) ●●●●。 基于结构的比较表明,用于结合的关键残基ICAM-2的Tyr10被C末端尾结构域的Ala492取代(图 4 C) ●●●●。 除上述直接干扰外,应注意的是,如前所述,ICAM-2束缚和屏蔽形式中FERM域的整体结构在子域B和C处显示出局部结构偏差。 当尾部结构域覆盖在FERM–ICAM-2复合物上时,这些偏差会导致C末端尾部结构域与子域B和C之间的界面处的原子崩溃(图 4 B) ●●●●。
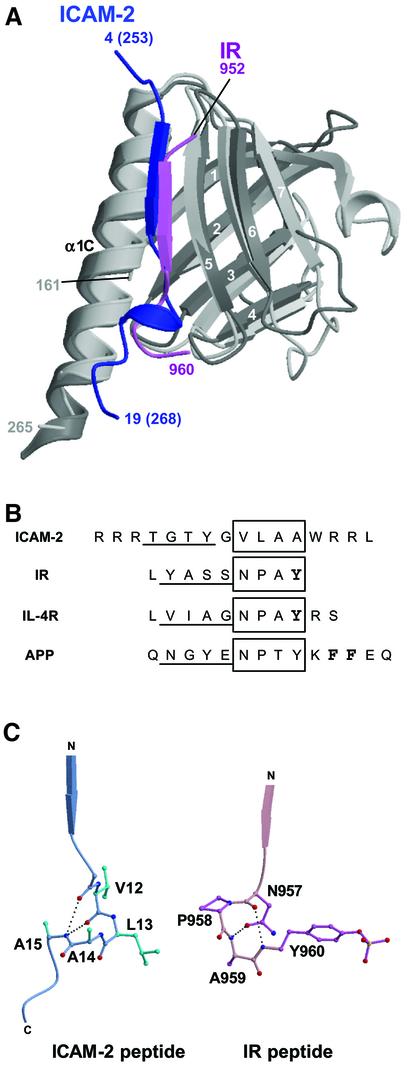
与PTB结构域结合的磷酸酪氨酸肽的比较 之前的结构比较( 滨田 等 ., 2000 )表明子结构域C的折叠类似于PTB结构域,而不是PH结构域。 结合的ICAM-2肽的β链与人胰岛素受体(IR)结合到人胰岛素受体底物1(IRS-1)PTB结构域的磷酸酪氨酸肽(pY肽)的β链重叠( 埃克 等 ., 1996 )(图 5 A) ●●●●。 IR和其他PTB-结合肽具有NPxY基序(图 5 B) 在β链的C末端采用β-圈构象。 然而,ICAM-2肽没有NPxY基序,与该NPxY模序对应的区域形成3 10 螺旋后面是C末端区域,其方向与IR肽的方向不同(图 5 C) ●●●●。
图5。 FERM–ICAM-2复合物与相关PTB–肽复合物的比较。 ( A类 )在与IR肽(粉红色)结合的IRS-1 PTB结构域(浅灰色)上,与ICAM-2尾(蓝色)结合的根蛋白FERM亚结构域C(灰色)的重叠。 ( B类 )基于叠加复合结构的肽序列。 强调了复杂构造中形成的β链。 第三个 10 ICAM-2中的螺旋和PTB结构域结合肽(IR、IL-4R和APP)中的NPxY基序被装箱。 IR和IL-4R肽中的磷酸酪氨酸残基为粗体。 在APP肽中,将肽锚定到X11 PTB结构域的两个Phe残基也以粗体显示。 ( C类 )三者的比较 10 ICAM-2肽中的螺旋结合到radidin FERM结构域,IR肽中NPxY基序的β-转角结合到IRS-1 PTB结构域。 肽内氢键显示为虚线。
与pY肽在μM范围内与PTB结构域结合相比 K(K) d日 ( Dhe-Paganon等人,1999年 ),ICAM-2与FERM结构域的结合更强约100倍。 然而,在多肽具有有序结构的界面处,其埋藏的可及表面积没有显著差异。 例如,在IR肽和IRS-1 PTB结构域之间的复合物中的总埋藏可及表面积为~1560Å 2 ( Eck等人,1996年 ). ICAM-2肽与FERM结构域的相对较强的结合可能归因于C末端碱基残基与亚结构域B和C之间的高负电荷沟槽之间可能存在静电相互作用。 ICAM-2肽结合更强的另一个可能原因可能是主-主-主相互作用的差异。 在FERM–ICAM-2复合物中形成了八个主链-主链氢键,而在IR肽和IRS-1 PTB结构域之间形成了五个。 此外,IR肽中RxxxTYxVxxA基序的关键Y残基缺乏疏水相互作用也可以解释结合亲和力的差异。
有趣的是,神经元特异性X11 PTB结构域已被证明与来自β淀粉样前体蛋白(APP)的非Y肽结合( 张 等 ., 1997 ). 另一类PTB结构域,包含Numb-PTB结构域,结合具有GPpY但不具有NPxpY基序的肽( 锂 等 ., 1998 ). 目前的结构提供了新的证据,证明PTB结构域具有具有不同特异性的多肽结合模式。
与β-catenin的比较 ERM蛋白和其他连接蛋白对粘附分子胞质肽的识别与肌动蛋白细胞骨架的连接是一个有趣的问题。 β-catenin–E-cadherin复合物( Huber和Weis,2001年 ),相互作用表面包含100个E-cadherin肽残基,该肽在β-catenin的α-螺旋犰狳重复序列形成的长凹槽处具有延伸结构。 钙粘蛋白肽与主要由侧链介导的β-catenin具有极性和非极性相互作用,并增加了6100Å的总可及表面积 2 在我们的FERM–ICAM-2和β-catenin–E-cadherin复合物之间,没有发现肽构象和结合模式的相似性。 值得注意的是,β-catenin和E-cadherin肽之间没有主链-主链相互作用。 尽管FERM–ICAM-2复合物的总埋藏可及表面积比β-catenin–E-cadherin复合物小3.5倍,但为什么ICAM-2与FERM结构域的结合亲和力比钙粘蛋白与β-catentin(230 nM)的结合亲和力强14倍仍然是个谜。 与β-catenin结合的肽中缺乏主-主-主相互作用可能与相对较弱的结合亲和力有关。 在β-连环蛋白-E-钙粘蛋白相互作用中,E-钙粘蛋白的磷酸化似乎对β-连环蛋白-E-钙粘蛋白复合物的亲和力和细胞粘附性至关重要( 利克特 等 ., 2000 ).
对其他类FERM域的影响 在其他交联蛋白中发现了FERM样结构域,例如神经纤维瘤病2型肿瘤抑制基因产物,也被称为merlin/schwannomin( 鲁洛 等 ., 1993 ; 特罗法特 等 ., 1993 ),塔利班,结合整合素-β( 卡尔德伍德 等 ., 1999 ; 帕蒂尔 等 ., 1999 )蛋白酪氨酸磷酸酶(PTP),如FAP-1(PTP-BAS),与Fas相关( 佐藤 等 1995年 ),粘着斑激酶(FAK)( 舒尔茨 等 ., 1998 )和膜相关的非常规肌球蛋白,如肌球蛋白VIIa和X( 奇什蒂 等 ., 1998 ). 此外,在结合干扰素受体的Janus激酶(JAK)家族非受体酪氨酸激酶中发现了FERM结构域( 吉罗 等 ., 1999 ). 在这些蛋白质中,merlin FERM结构域与ERM蛋白质的序列同源性相对较高(64%),并且似乎在识别粘附分子方面表现出类似的特异性。 事实上,最近的晶体学研究已经揭示了merlin FERM结构域的结构,与radixin和moesin的结构域非常相似( 康 等 ., 2002 ; 清水 等 ., 2002 ). 与merlin的高序列同源性相比,带4.1(27%)、尾蛋白(24%)和PTP(~25–33%)的同源性较低,FAK和JAK的同源性极低。 因此,目前尚不清楚是否所有这些蛋白都使用PTB样亚结构域C结合其靶受体/粘附分子。 带4.1蛋白结合阴离子交换器/带3和糖蛋白C( Jons和Drenckhahn,1992年 ). 最近,酪氨酸磷酸酶PTPD1被发现与一种新的驱动蛋白样运动蛋白KIF1C结合,PTPD1是一种具有FERM样结构域的酪氨酸磷酸化酶( 多纳 等 ., 1998 ). 我们对这些蛋白质可能结合区域的氨基酸序列的仔细检查表明,它们可能具有FERM结合基序RxxxTYxVxxA的变体,用于与FERM或FERM样结构域结合(图 三 B) ●●●●。
结论 本研究揭示了基数FERM结构域的肽结合模式,该结构域使用PTB-like子域C通过β-β结合识别FERM结合基序RxxxTYxVxxA,并且很可能是子域B和C之间的酸性槽用于静电相互作用。 基序N末端侧翼区域的碱基残基对FERM结合可能不是必需的,但对与酸性脂质成分(如PIP2)的可能相互作用可能很重要。 ICAM-2肽形成一个短的3 10 螺旋而不是由NPxY基序形成的β-转,NPxY是“经典”PTB域识别的特征序列。 已在复合物结构上确定了特定接触点,并使用定量结合分析进行了验证。 这些接触,以及涉及C末端基本区域的静电相互作用(其结构在本研究中未指定),共同实现了高亲和力和特异性。
材料和方法 蛋白质制备和结合研究 小鼠根素的FERM结构域(1–310个残基)被表达为与GST的融合蛋白 大肠杆菌 并通过上述方法进行纯化( Hamada等人,2001年 ). 对于结合研究,在BIAcore生物传感器仪器(BIAcore3000,法玛西亚生物传感器)上进行SPR测量。 粘附分子膜旁区域的生物素化多肽购自Sawady Technology(日本东京)。这些多肽是通过基于Fmoc的策略合成的,带有标准侧链保护基团,并通过反相HPLC纯化。 肽通过N末端生物素部分偶联到链亲和素涂层传感器芯片(传感器芯片SA BIAcore AB)。 将根蛋白FERM域(~0.1–1µM)注入肽链和非链传感器芯片中,以校正背景信号。 所有结合实验均在25°C下进行,缓冲液中的流速为10µl/min(10 mM HEPES pH 7.4,150 mM NaCl,1 mM EDTA,1 mM DTT和0.05%表面活性剂P20)。 使用BIA评估软件(Pharmacia)评估动力学参数。 这个 K(K) d日 通过至少三个独立测量值的平均值获得这些值,并汇总在表中 我 。
结晶和数据收集 为了结晶,将纯化蛋白与等摩尔28残留ICAM-2肽混合,并浓缩至20 mg/ml(0.54 mM)。 复合晶体是从0.27 mM蛋白质/肽溶液中获得的,其化学计量比为1:1,含有50 mM Mes-Na(pH 6.0)、2%聚乙二醇6000(PEG6K)、130 mM NaCl和0.4 mM DTT,温度为4°C。 溶解晶体的小份样品的MALDI-TOF质谱表明,晶体中含有FERM结构域和ICAM-2肽( 滨田 等 ., 2001 ).
在含有7%PEG6K、35%甘油和50 mM Mes-Na缓冲液的溶液中进行低温保护后,从闪速冷冻至100 K的晶体收集所有衍射数据。 晶体属于太空群 P(P) 三 1 21,这是由以下结构分析确定的,带有单元参数, 一 = b条 = 100.44 Å, c(c) = 99.49 Å, γ = 120°. 使用安装在日本Harima SPring-8同步加速器设施的光束线BL41XU上的电荷耦合区域探测器(Mar CCD)收集2.4-数据集。 波长设置为1.00Å,晶体到探测器的距离为160 mm。 数据采集自三个角度范围为180°、步长为1°的晶体,曝光时间为3s。 使用DENZO和SCALEPACK程序处理强度数据( Otwinowski和Minor,1997年 )或DPS-Mosfilm( Rossmann和van Beek,1999年 ). 两个数据集合并为一组数据,用于结构确定(表 三 ).
表III.根素FERM结构域–ICAM-2复合物的结晶分析。
强度数据
分辨率(Å) 2.40
反思
仔细斟酌的 599708
独特的 23153
完整性(%) 一 100.0/100.0
对 sym(对称) b条 (%) 一
7.1/13.7
平均值 我 /σ 一 6.0/5.2版本
精炼
分辨率范围(Å) 15.0–2.40
残留物数量 332
蛋白质 316
肽 16
包括原子 2998
蛋白质 2618
肽 116
水 264
对 晶体 因子/ 对 自由的 系数(%) c(c)
22.9/24.0
平均值 B类 因子(Å 2 ) 49.4
蛋白质 48.9
肽 59.2
R.m.s.偏差 d日 0.008 Å, 1.350°, 1.182°
结构确定和细化 利用基于基FERM结构域自由态结构的搜索模型,通过分子替换计算初始相( Hamada等人,2000年 ). 通过AMoRe程序,使用不同范围的强度数据和积分半径进行多次搜索,获得了明确的旋转和平移解( 纳瓦扎,1994年 ). 使用程序CNS对搜索模型进行刚体细化后( Brünger等人,1998年 ),使用Solomon通过溶剂平坦化和直方图匹配改进了相( 亚伯拉罕和莱斯利,1996年 ). 合成的初始图谱显示了大多数FERM结构域和肽的清晰电子密度。 使用图形程序O将肽的初始模型构建到电子密度图中( Jones等人,1991年 )以及重建FERM域的一部分。 利用CNS模拟退火方法对模型进行了改进( Brünger等人,1998年 ). 经过几个周期的重建和细化,模型被细化为 对 22.9%(免费 对 值24.0%),用于分辨率为2.4Å的强度数据。 目前的模型包括蛋白质的316个残基(来自载体的6个残基)、16个肽残基和264个水分子。 使用PROCHECK程序监测模型的立体化学质量( 拉斯科夫斯基等人,1993年 ).
在肽模型中,Arg4、Arg17、Arg18和Leu19的侧链定义不明确,在当前结构中被丙氨酸取代。 没有为肽的三个N末端和九个C末端残基建立模型,这些残基在当前图谱中定义不明确。 在蛋白质模型中,Pro2和Lys3的侧链定义不明确,在当前结构中被丙氨酸取代。 Asp252处于不允许的主链扭转角区域。
使用Molscript程序绘制了分子主链折叠的带状表示( 克劳利斯,1991年 ),而分子表面表示是使用GRASP程序绘制的( 尼科尔斯 等 ., 1991 ).