摘要 生长因子激活的AGC蛋白激酶RSK、S6K、PKB、MSK和SGK通过激活环和疏水基序(激酶结构域的C端)中的丝氨酸/苏氨酸磷酸化激活。 在其中一些激酶中,疏水基序的磷酸化创建了一个特定的对接位点,该位点招募并激活PDK1,PDK1随后磷酸化激活环。 在这里,我们发现PDK1激酶结构域中有一个口袋,通过识别两个位置相反的精氨酸和赖氨酸残基来识别疏水基序中的磷酸丝氨酸/磷酸苏氨酸。 此外,我们证明RSK2、S6K1、PKBα、MSK1和SGK1包含类似的磷酸结合囊,它们用于与自身磷酸化疏水基序的分子内相互作用。 分子建模和实验数据为一种常见的激活机制提供了证据,其中磷酸化疏水基序和激活环作用于激酶结构的αC-螺旋,诱导催化活性的协同刺激。 序列保守性表明,这一机制是激活40多种人类AGC激酶的关键特征。
关键词: AGC激酶/对接站点/PDK1/PKB/RSK
介绍 生长因子信号转导的重要部分是由AGC激酶家族中一组结构相关的蛋白激酶介导的。 该组包括p90核糖体S6激酶(RSK)、p70核糖体S6激酶(S6K)、蛋白激酶B(PKB)、促分裂原和应激激活蛋白激酶(MSK)、血清和糖皮质激素诱导激酶(SGK)以及蛋白激酶C相关激酶(PRK)。 总之,这些激酶磷酸化大量细胞蛋白,从而调节细胞分裂、存活、代谢、跨膜离子流量、迁移行为和分化。 激酶被部分不同的信号通路激活。 PKB、S6K和SGK是磷脂酰肌醇3-激酶(PI3-K; 明 等 ., 1994 ; 法兰克 等 ., 1995 ; 小林和科恩,1999年 ; 公园 等 ., 1999 )、RSK和MSK分别是ERK和ERK/p38有丝分裂原激活蛋白(MAP)激酶的效应器( 斯特吉尔 等 1988年 ; 迪克 等 ., 1998 ),PRK2受Rho GTPase控制( 弗林 等 ., 2000 ). 对上游通路的不同反应性部分是由于激酶包含位于激酶结构域两侧的不同信号传导模块,例如PKB中的PH结构域、PRK中的Rho结合结构域、S6K中的独特抑制结构域和RSK和MSK中的MAP激酶激活激酶结构域。
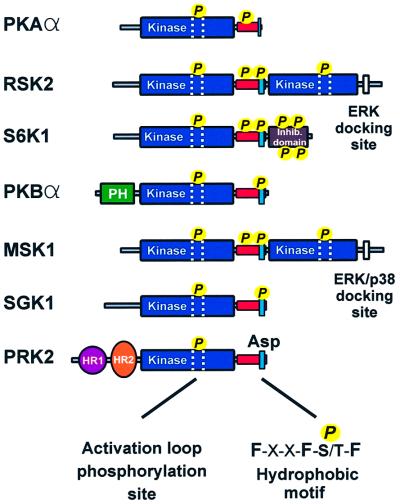
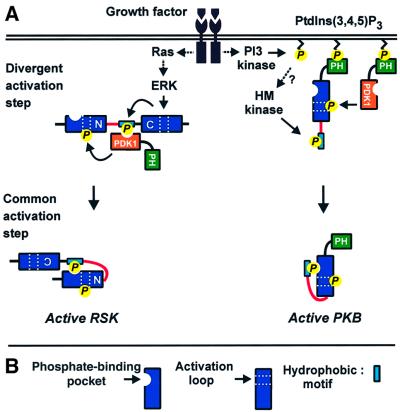
尽管调控方式不同,但这些激酶有两个共同的调控特征,对激活至关重要(图 1 ). 首先,它们都需要激酶结构域内激活环中丝氨酸或苏氨酸残基的磷酸化。 该位点被PKB中的3-磷酸肌醇依赖性激酶-1(PDK1)磷酸化( 阿莱西 等 ., 1997 ; 斯托科 等 ., 1997 ),S6K系列( 阿莱西 等 ., 1998 ; 拉伦 等 ., 1998 )、RSK( 延森 等 ., 1999 ; 理查兹 等 ., 1999 ),新加坡克朗( 小林和科恩,1999年 ; 公园 等 ., 1999 )和PRK( 弗林 等 ., 2000 )而MSK可能会在这个位置自动磷酸化( 威廉姆斯 等 ., 2000 ). 活化环的磷酸化可将催化活性从缺乏增加到通常最大活性的10%。 其次,这组激酶都需要丝氨酸或苏氨酸残基的磷酸化,该残基位于激酶结构域末端保守的尾部区域C中的所谓疏水基序。 该基序的特征是围绕被磷酸化的丝氨酸/苏氨酸残基的三个芳香氨基酸:Phe-X-X-Phe-Ser/Thr-Phe/Tyr。 然而,在也属于这种激酶家族的PRK和非典型PKC中,疏水基序包含一个带负电荷的氨基酸(天冬氨酸或谷氨酸),它类似于磷酸丝氨酸/苏氨酸( 帕雷克 等 ., 2000 ). 在RSK中( Vik和Ryder,1997年 )和MSK( 迪克 等 ., 1998 ),疏水基序由其各自的C末端激酶结构域磷酸化。 对于PKB、S6K和SGK,疏水基序激酶的身份尚未确定。
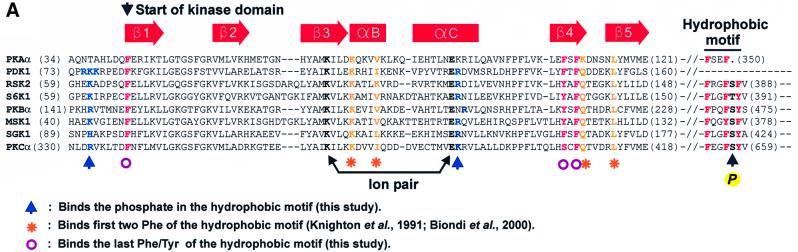
图1。 PKA和主要生长因子激活的AGC激酶的结构比对。 该比对表明,生长因子激活的AGC激酶具有两个调节特征:激活环(点状区域)的磷酸化和位于激酶结构域尾部(红框)C末端的疏水基序(蓝框)的磷酸化合。 请注意,PRK2含有磷酸化天冬氨酸残基,PKA在疏水基序中缺乏磷酸化位点。
最近的研究表明,疏水基序可以作为PDK1在PRK2和PKCζ中的对接位点( 巴伦德兰 等 ., 2000 ),RSK2( 弗罗丁 等 ., 2000 )、S6K1和SGK1( 比昂迪 等 ., 2001 ). 此外,PDK1与RSK2疏水基序的相互作用( 弗罗丁 等 ., 2000 )或PRK2( 比昂迪 等 ., 2000 )将PDK1的催化活性提高了几倍,表明该基序具有招募和激活PDK1两种功能。 通过对PKA晶体结构的分析,确定了PDK1中疏水基序的结合位点( 比昂迪 等 ., 2000 ). PKA也是一种AGC激酶,但它终止于部分疏水基序(Phe-X-X-Phe-COH),没有调节性磷酸化位点。 在PKA晶体结构中,该基序中的两个苯丙氨酸残基与激酶结构域小叶中的疏水囊相互作用( 骑士 等 ., 1991 )苯丙氨酸残基的突变几乎消除了激酶活性( 埃切舍尔 等 ., 1997 ). 基于PKA晶体结构的PDK1模型显示,该口袋在PDK1中保守,并构成PDK1靶激酶疏水基序的结合位点( 比昂迪 等 ., 2000 , 2001 ).
PDK1与疏水基序相互作用的一个重要特征是,基序必须磷酸化(或含有磷酸化的酸性残基)才能发生有效的相互作用( 巴伦德兰 等 ., 2000 ; 弗罗丁 等 ., 2000 ; 比昂迪 等 ., 2001 ). PDK1的疏水囊是否被赋予识别磷酸丝氨酸/磷酸苏氨酸的能力,或者磷酸是否改变疏水基序的构象以使其能够结合疏水囊尚不清楚。 此外,对接机制无法解释为什么PKB和MSK需要疏水基序中的磷酸化,因为PKB似乎没有将该基序用于PDK1对接( 比昂迪 等 ., 2001 )MSK不是PDK1的目标( 威廉姆斯 等 ., 2000 ).
在本研究中,我们在PDK1的疏水囊旁发现了一个磷酸结合位点,该位点识别疏水基序中的磷酸丝氨酸/磷酸苏氨酸。 我们通过显示RSK2、S6K1、PKBα、MSK1和SGK1在其激酶结构域中含有类似的磷酸结合口袋来扩展这些发现。 它们利用磷酸结合囊与自己的磷酸化疏水基序相互作用,导致激酶活性的大量刺激与活化环磷酸化协同作用。 这些发现定义了疏水基序磷酸化位点的一个关键功能,并表明磷酸结合囊是>40个人类AGC激酶的关键调节特征,在这些激酶中磷酸结合囊被保守。 磷酸盐结合囊为旨在激活或抑制这些AGC激酶的药物提供了一个有吸引力的靶点,作为通常靶向ATP结合位点的替代物。
结果 PDK1疏水囊对磷酸/磷酸苏氨酸的识别 先前的研究通过显示激酶结构域小叶中的残基Lys115、Ile119、Gln150和Leu155形成一个疏水囊,可能与PDK1靶激酶疏水基序的前两个苯丙氨酸结合,对PDK1疏水囊进行了部分表征( 比昂迪 等 ., 2000 , 2001 ). 在这里,我们希望确定口袋附近的氨基酸,这些氨基酸可以解释疏水基序中磷酸丝氨酸/苏氨酸的识别。 程序Swiss-Pdb Viewer( Guex和Peitsch,1997年 )用于在PKA晶体结构坐标上建模PDK1序列( 英语 等 ., 1996 )是唯一一个结构已被解决的AGC激酶。 PDK1的模型显示,上述袋状残留物聚集在较大凹槽的一端(数据未显示)。 在沟的深处和靠近该簇的地形上,我们注意到一个精氨酸残基(131)位于保守激酶折叠的所谓αC螺旋中。 此外,我们注意到四个连续的基本残基, 75 精氨酸-赖氨酸-精氨酸 78 ,N端到β链1。 虽然基本簇位于保守激酶折叠之外,因此其位置不太可预测,但β-链1的起始点在地形上接近疏水囊。 我们决定通过更先进的分子模型和生物化学表征来研究这些带正电的氨基酸是否参与磷酸结合。
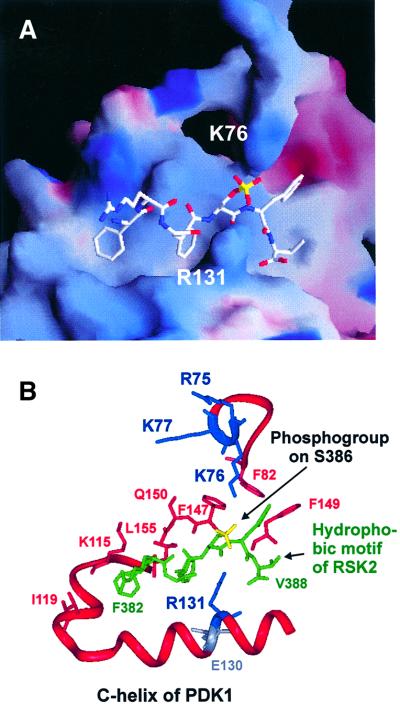
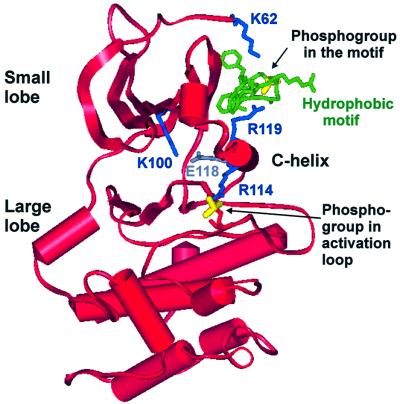
PDK1的残基82–351编码激酶结构域,用于根据封闭、活性构象中PKA结构的坐标和磷酸化活化环对PDK1进行建模( Engh等人,1996年 ). 然后,通过首先将基序的前两个苯丙氨酸固定在PKA晶体结构中相应苯丙氨酸占据的位置,将RSK2在调节位点(Ser386)磷酸化的疏水基序序列模拟到口袋中。 然后,在没有模板的情况下对图案的剩余部分进行建模( 从头算 建模)。 最后,对PDK1的残基75–81(包括基本簇)进行建模 从头算 PDK1激酶结构域。 对接相互作用的结果模型显示,PDK1的Ser386和Arg131的磷酸基并列,二者之间可能形成氢键(图 2 ). 有趣的是,Arg131与谷氨酸残基(PDK1中的130)相邻,谷氨酸残体是所有激酶中极少数保守的残基之一,具有调节作用。 建模还表明Ser386的磷酸基团与PDK1中基本簇的Arg75、Lys76和Lys77结合,但表明一次只能结合其中一个残基。 此外,PDK1的Phe82、Phe147和Phe149的侧链似乎形成了一个疏水位点,该位点容纳疏水基序的最后一个芳香残基。 最后,基序后的缬氨酸可能与PDK1的Leu145形成疏水相互作用。 总之,该模型表明,疏水基序完全占据PDK1激酶结构域小叶的凹槽,基序中的磷酸被两个位置相反的碱基残基占据。
图2。 PDK1与RSK2磷酸化疏水基序之间的对接相互作用模型。 ( A类 )PDK1疏水口袋的静电表面电位模型,蓝色为正电位,红色为负电位。RSK2疏水基序肽(FRGFpSFV)显示为白色,Ser386上的磷酸基显示为黄色。 ( B类 )带文本中讨论的残留物侧链的口袋的带状表示。 PDK1残基为红色、蓝色或灰色,而RSK2疏水基序肽显示为绿色,磷酸基显示为黄色。
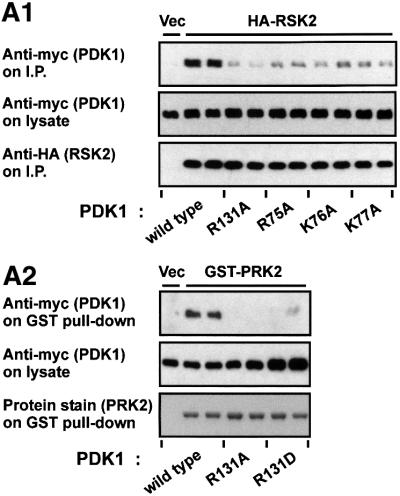
接下来,我们评估了PDK1中预测的磷酸结合残基突变对其结合RSK2能力的影响 体内 采用免疫共沉淀实验。 在裂解之前,细胞暴露于表皮生长因子(EGF)以诱导RSK2疏水基序磷酸化和PDK1向RSK2募集( Frödin等人,2000年 ). RSK2共沉淀野生型PDK1,但PDK1-R131A突变的数量更低(图 三 A1,上面板)或R131D、R131L和R131H突变体(数据未显示)。 此外,PDK1中Arg75、Lys76或Lys77的丙氨酸突变均导致RSK2大大减少PDK1的沉淀。 PRK2,在疏水基序中磷酸丝氨酸/苏氨酸位置含有天冬氨酸,共沉淀野生型PDK1,但不包括PDK1-R131A或PDK1-R31D(图 三 A2,上面板)或R131L和R131H(数据未显示)。 所有PDK1构建体都以相似的水平表达蛋白质(图 三 A、 中间面板)。
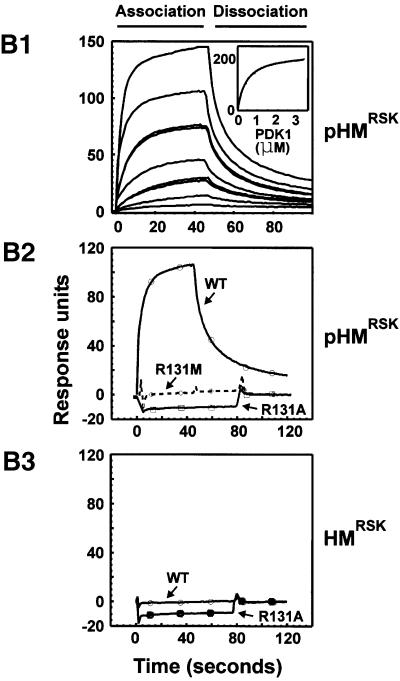
图3。 PDK1中与磷酸化疏水基序相互作用所需的精氨酸/赖氨酸残基的鉴定。 ( A类 )将表达野生型或突变型myc-PDK1的质粒与HA-RSK2、GST-PRK2或空载体(Vec)共同转染COS7细胞。 在48小时和最后3小时的血清饥饿期后,对表达RSK的细胞进行35分钟EGF处理,然后对细胞进行裂解。 分别使用抗HA抗体或谷胱甘肽珠从细胞裂解液中沉淀HA-RSK2和GST-PRK2。 沉淀物经过SDS-PAGE和抗myc抗体免疫印迹检测共沉淀物myc-PDK1(上面板)或抗-HA免疫染色或蛋白质染色,以评估HA-RSK2和GST-PRK2的数量(下面板)。 对沉淀前裂解物进行myc标记免疫印迹(中间板)。 ( B类 )在BiaCore3000系统中,使用表面等离子体共振测量分析了PDK1与RSK2疏水基序的相互作用。 磷酸化基序的生物素化肽(pHM RSK公司 )或非磷酸化(HM RSK公司 )使用Ser386对传感器芯片SA进行涂层(10个响应单元)。 (1) 将不同浓度(0.013–3.33µM)的GST–PDK1注射到pHM涂层芯片上。 在插图中,根据PDK1的不同浓度绘制了稳态结合曲线。 使用Kaleidabrograph软件将数据拟合为双曲线,从而获得动力学常数。 (2和3)将GST–PDK1野生型、–R131A或–R131M以400 nM注入涂有pHM的芯片 RSK公司 和HM RSK公司 分别是。 (A)和(B)中的所有实验进行了三次,结果相似。
表面等离子共振测量表明野生型PDK1与高亲和力结合( K(K) 天 ≅400±20 nM)合成在Ser386磷酸化的RSK2疏水基序合成肽(pHM RSK公司 )而PDK1-R131M或PDK1-R31A对pHM没有检测到的亲和力 RSK公司 (图 三 B1和B2)。 非磷酸化RSK2疏水基序肽(HM RSK公司 )未显示与野生型PDK1或PDK1-R131A结合(图 三 B3)。
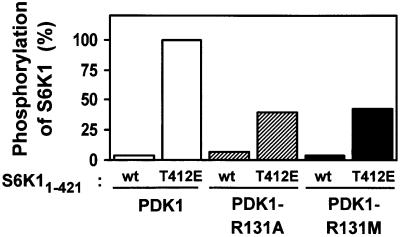
S6K1系列 1–421 当Thr412(即疏水基序的磷酸化位点)突变为谷氨酸时,会成为PDK1的更好底物( 阿莱西 等 ., 1998 ; 丹尼斯 等 ., 1998 )这是由于PDK1通过疏水袋增强了与S6K1的对接( 比昂迪 等 ., 2001 ). S6K1系列 1–421 C末端抑制结构域缺失,阻断PDK1与S6K1的相互作用。 我们使用该测定来评估PDK1中Arg131对PDK1磷酸化S6K1能力的重要性。 如图所示 4 、PDK1、PDK1-R131A和PDK1-R31M均磷酸化S6K1 1–421 糟糕透顶。 PDK1磷酸化S6K1 1–421 T412E高效。 相反,PDK1-R131A和PDK1-R31M磷酸化S6K1的能力降低 1–421 T412E,表明这些突变体在识别E412的负电荷方面受损。 PDK1-R131A或-R131M磷酸化S6K1的能力降低 1–421 T412E不是由于突变导致PDK1催化活性受损所致。 事实上,PDK1疏水囊中的这些和其他突变使PDK1肽底物T308tide的激酶活性增加了2到3倍(数据未显示)。 这表明,如前所述,未占用的口袋可以抑制PDK1活性( 比昂迪 等 ., 2000 ).
图4。 R131对PDK1磷酸化S6K1的能力很重要。 野生型或T412E His-S6K1 1–421 与野生型或突变型GST–PDK1和Mg[γ- 32 P] ATP。 随后,对激酶反应进行SDS-PAGE。 对纳入S6K1蛋白带的放射性进行量化,并以获得的最大值的百分比表示。 结果代表了两个独立的实验。
与丙氨酸、天冬氨酸、亮氨酸、组氨酸或甲硫氨酸(上述数据)相反,碱性氨基酸赖氨酸可以部分取代PDK1中131位的精氨酸。 针对T308肽,PDK1-R131K显示出与PDK1相似的基础活性,但pHM激活的剂量-反应曲线 S6K系列 和HM PRK2系列 浓度分别提高了约10倍和100倍(数据未显示)。
总之,我们的数据强烈表明,PDK1利用C-螺旋中的Arg131和N-末端碱基残基Arg75、Lys76和Lys77来识别其靶激酶疏水基序中的磷酸丝氨酸/磷酸苏氨酸(或模拟酸性残基)。
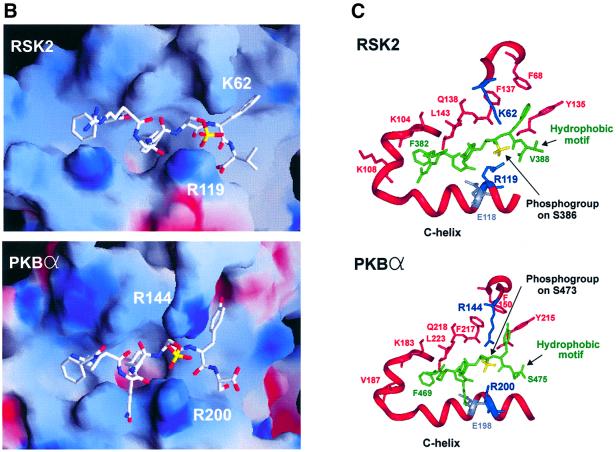
磷酸结合囊在生长因子激活的AGC激酶中保守 PDK1本身属于AGC激酶家族,但不典型,因为它不包含疏水基序。 有趣的是,序列比对表明,在RSK2、S6K1、PKBα、MSK1、SGK1和PKCα中也存在磷酸盐结合囊(图 5 A) ●●●●。 首先,PDK1的C-螺旋中的精氨酸或赖氨酸残基相当于Arg131是保守的。 其次,PDK1的Lys76的基本残基是保守的。 最后,结合疏水基序的三个芳香残基的残基是保守的。 这增加了这些激酶磷酸化疏水基序可能与激酶结构域内的磷酸结合囊相互作用的可能性,这可能通过分子内机制刺激其催化活性。 为了解决这个问题,我们首先在PKA的结构上模拟了包含RSK2(N-末端激酶结构域)或PKBα的激酶结构域的序列,然后将它们各自的磷酸化疏水基序模拟到假定的口袋中。 如图所示 5 B和C,疏水基序分别与RSK2和PKBα的疏水囊完美吻合。 此外,在这两种激酶中,疏水基序的磷酸基与C-螺旋中的保守精氨酸并列,两者之间可能形成氢键。 这两种模型还允许磷酸结合到激酶结构域的带正电残基N末端,即RSK2中的K62和PKBα中的R144。 通过对S6K1、MSK1和SGK1进行建模,获得了非常相似的结果(数据未显示)。
图5。 磷酸结合囊在主要生长因子激活的AGC激酶中保守。 ( A类 )在含有疏水囊的激酶结构域区域以及形成疏水基序的区域中,对选定的AGC激酶进行氨基酸序列比对。 预测与磷酸基相互作用的保守残基、疏水基序的前两个芳香残基和最后一个芳香残基分别用箭头、星号和圆圈表示。 指出了所有激酶中保守的赖氨酸和谷氨酸残基之间的离子对形成。 ( B类 和 C类 )RSK2和PKBα疏水口袋与其各自磷酸化疏水基序FRGFpSFV(RSK2)和FPQFpSYS(PKBα)的分子内相互作用模型。 (B) 口袋的静电表面电位模型,蓝色为正电位,红色为负电位。疏水基序肽显示为白色,磷酸基团显示为黄色。 (C) 带有文本中讨论的残留物侧链的口袋的带状表示。 疏水基序肽显示为绿色,磷酸基显示为黄色。
疏水基序通过磷酸结合囊对AGC激酶进行分子内激活的证据 为了测试疏水基序的分子内功能,设计了一种重组分析,可以评估疏水基序磷酸化、激活环磷酸化及其在催化刺激RSK2、S6K1、MSK1、PKBα和SGK1中的相互作用的贡献。 该分析基于缺失疏水基序和其他C末端结构域的分离激酶结构域,即RSK2和MSK1的C末端激酶结构域和S6K1的抑制结构域。 在本试验中,通过添加在调节位点磷酸化的基序合成肽(pHM),实现疏水基序磷酸化。 活化环磷酸化是通过预先接触PDK1而实现的,然后去除PDK1,RSK2分析除外。 尽管MSK1不是一种生理底物,但它可以被PDK1磷酸化和激活( 弗罗丁 等 ., 2000 ),在这里被利用。
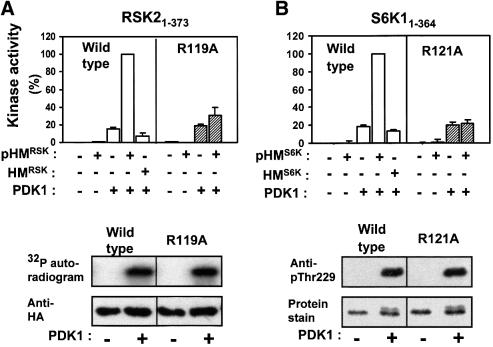
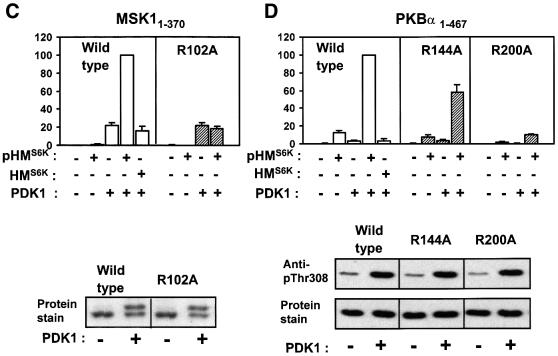
RSK2(RSK2)的激酶结构域 1–373 )单独培养时完全不活动(图 6 A) ●●●●。 添加pHM未实现活化 RSK公司 肽,而与PDK1预孵育激活环的磷酸化导致激酶活性的刺激。 然而,pHM的组合 RSK公司 活化环磷酸化导致RSK2的协同刺激 1–373 催化活性。 在20–30µM pHM下观察到半最大活化 RSK公司 (未显示数据)。 相反,非磷酸化疏水基序肽HM RSK公司 ,没有刺激RSK2的能力 1–373 高达350µM的肽,是这里可能的最高浓度。 为了评估预测的磷酸丝氨酸结合Arg119在C螺旋中的作用,对RSK2进行了类似的实验 1–373 其中Arg119突变为丙氨酸。 RSK2系列 1–373 R119A在激活环磷酸化时表现出正常刺激。 然而,pHM RSK公司 未能刺激RSK2 1–373 R119A催化活性与活化环磷酸化协同作用。 这表明RSK2的激活 1–373 通过pHM需要pHM与Arg119结合,而且R119A突变不会破坏三级结构,因为RSK2 1–373 R119A被PDK1正常激活。
图6。 磷酸化疏水基序对AGC激酶分子内激活的证据。 ( A类 – E类 )上面板:RSK2、S6K1、MSK1、PKBα和SGK1的野生型或点突变激酶结构域,均缺乏疏水基序(SGK1除外 61–431 )PDK1是否预先磷酸化。 此后,去除PDK1(RSK2分析中除外)。 然后,在170µM(A、B和E)或360µM(C和D)的磷酸化(pHM)或非磷酸化(HM)疏水基序肽缺失或存在的情况下测定每个激酶的活性,并以最大活性的百分比表示。 数据是(A)2–4个独立实验的4–10个观察值的平均值±SD,(B–D)三个独立实验或(E)重复样本的平均值,重复样本之间的差异小于5%,重复样本来自两次进行的具有类似结果的实验(A–D,下部面板)。 为了控制等量的蛋白质和PDK1诱导的野生型和突变型激酶磷酸化,对反应的小份进行SDS-PAGE和蛋白质染色/抗-HA印迹或用PDK1位点的磷酸特异性抗体进行印迹。 然而,在(A)中,HA-RSK2的磷酸化 1–373 通过包括[γ- 32 P] 与PDK1预孵育期间的ATP,随后用抗HA抗体沉淀,SDS–PAGE和放射自显影。
在S6K1、MSK1和PKBα(S6K1 1–364 ,MSK1 1–370 和PKBα 1–467 在图中 6 B–D)。 MSK1和PKB的实验是使用来自S6K1的pHM肽进行的,因为pHM MSK公司 肽不可用,pHM 巴基斯坦中央银行 多肽仅诱导PKBα2到3倍的活化 1–467 (未显示数据)。 与其他激酶相比,pHM激活PKBα 1–467 虽然轻微,但在PDK1缺乏共同表达的情况下,很可能是因为PKBα 1–467 被内源性PDK1部分磷酸化(图 6 D、 下部面板)。 S6K1中 1–364 和PKBα 1–467 ,我们还分别对N-末端磷酸结合残基Lys62和Arg144进行了突变。 这导致S6K1的激活减少了50% 1–364 按pHM S6K系列 (标准偏差=12%, n个 =3; 数据未显示)和40%的PKBα活化减少 1–467 按pHM S6K系列 (图 6 D) ●●●●。 欧盟委员会 50 实验表明,与野生型激酶相比,这些突变体对pHM的亲和力低3-4倍(数据未显示)。 对照实验表明,磷酸结合碱基残基的所有突变体均正常表达,PDK1在激活环中磷酸化,类似于野生型酶(图 6 A–D,下部面板)。 MSK1的磷酸化 1–370 由于没有关于激活环位点的磷酸特异性抗体的报道,因此通过延长电泳中的迁移率变化进行了评估。 RSK2的最大比活性 1–373 ,S6K1系列 1–364 ,MSK1 1–370 和PKBα 1–467 通过联合活化环磷酸化和pHM获得的蛋白与EGF或胰岛素激活的全长重组蛋白相似或高出几倍 体内 (未显示数据)。 这可能反映出 体外 实验是在疏水基序和活化环的磷酸化程度高于获得的条件下进行的 体内 。
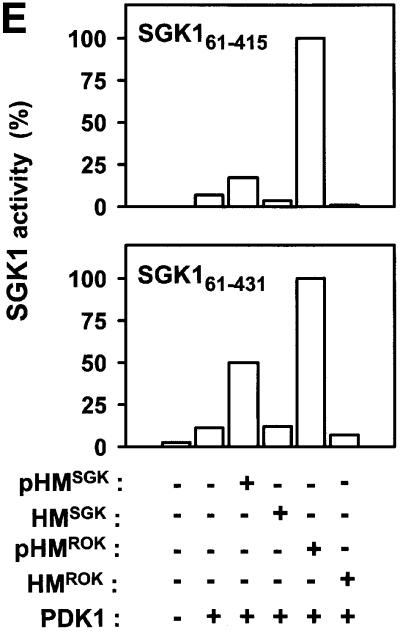
此外,SGK1通过其磷酸化而非非磷酸化的疏水基序被激活(图 6 E) 。 这在SGK1中都观察到 61–415 ,其中疏水基序被删除,并且带有SGK1 61–431 ,保留了它的疏水基序。 两种SGK1结构都缺乏1–60残基,因为全长蛋白的表达水平不足以进行蛋白质纯化( 小林和科恩,1999年 ). 来自Rho激酶-α(也是AGC激酶)的pHM肽可以进一步激活SGK1,但HM不能激活 韩国 相反,来自RSK2、S6K1、PKBα或强直性肌营养不良激酶(DMK)、另一种AGC激酶的pHM,或来自PRK2或PKCζ的HM显示出很少激活SGK1的能力(数据未显示)。 因此,在某些情况下,AGC激酶可以被来自另一AGC激酶的pHM激活。 然而,由于欧盟 50 异源激活值始终大于10µM,这种激活可能不是生理性的。
表面等离子共振分析表明pHM RSK公司 能够绑定RSK2 1–373 ,但不是RSK2 1–373 R119A(图 7 ). 然而,亲和力太低,无法定量估计BiaCore仪器中的离解常数,这与EC一致 50 20–30µM pHM的值 RSK公司 RSK2催化活化 1–373 .HM型 RSK公司 显示不与RSK2结合 1–373 或RSK2 1–373 R119A(数据未显示)。
图7。 RSK2与其磷酸化疏水基序的相互作用。 通过表面等离子共振测量分析了RSK2与其自身疏水基序的相互作用。 生物素化pHM RSK公司 该肽用于覆盖传感器芯片SA(500个响应单位),并测试其与GST–HA-RSK2的结合 1–373 或GST–HA-RSK2 1–373 R119A。 实验进行了多次,结果相似。
总之,这些实验证明磷酸化疏水基序与激活环中的磷酸化事件协同刺激生长因子激活的AGC激酶的催化活性。 此外,数据表明pHM的结合和激活需要C-螺旋中的保守精氨酸,在较小程度上需要激酶结构域的保守碱基残基N末端。
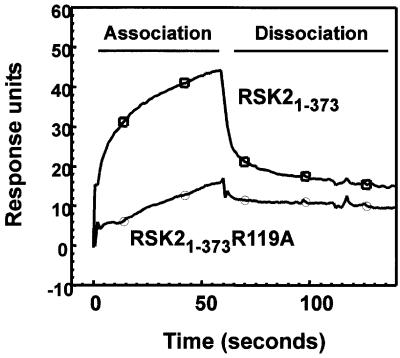
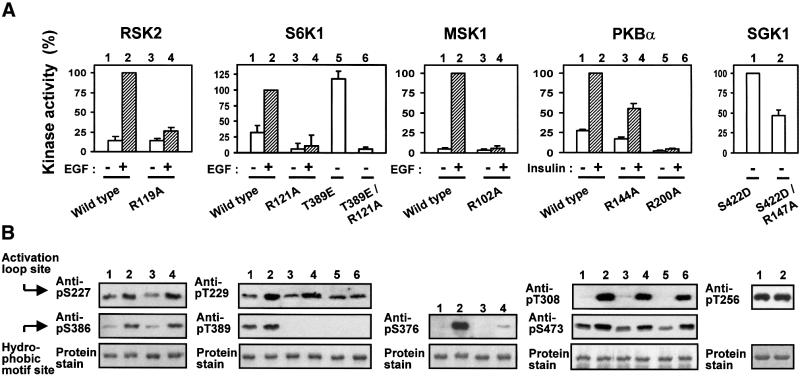
接下来,我们分析了磷酸盐结合残基在 体内 激活(图 8 A) 和磷酸化状态(图 8 B) 对生理刺激作出反应的全长AGC激酶。 在RSK2中,EGF诱导的激活被Arg119突变所消除。 免疫印迹显示,RSK2-R119A的激活环和疏水基序表达和磷酸化正常。 N-末端碱基残基Lys62的突变使激酶活性降低21%(SD=7.0%, n个 =3; 数据未显示)。 在S6K1中,C螺旋中Arg121的突变在很大程度上消除了基础和EGF诱导的活性。 S6K1-R121A表现出激活环的正常表达和磷酸化,但有趣的是,疏水基序的磷酸化大部分缺失。 发生了磷酸化缺失 体内 而不是在免疫沉淀过程中,因为来自EGF处理后用莱姆利缓冲液裂解的细胞的S6K1-R121A在疏水基序中显示出类似的磷酸化缺乏(数据未显示)。 这表明,在S6K1中,当疏水基序磷酸化位点不与疏水囊结合时,会迅速去磷酸化,从而保护其免受磷酸酶作用的影响。 评估Arg121对S6K1活性的作用 体内 因此,我们产生了一个S6K1-T389E突变体,其中疏水基序中的磷酸化位点突变为谷氨酸。 残基Thr389与图中的Thr412是相同的疏水基序残基 4 ,但根据图中使用的长和短S6K1拼接变体,编号不同 4 和 8 分别是。 S6K1-T389E具有较高的基础活性,在所使用的条件下,EGF不会显著增加该活性(数据未显示)。 在S6K1-T389E中引入R121A突变可消除激酶活性,而不会影响激活环的表达水平或磷酸化。 在MSK1中,C-螺旋中Arg102的突变导致激酶活性完全丧失以及疏水基序磷酸化,而表达水平不受影响。 N-末端碱性残基K43的突变对激酶活性没有影响(数据未显示)。 在PKBα中,N端Arg144和C螺旋Arg200的突变分别导致激酶活性的部分和完全丧失。 这两种突变都导致激活环和疏水基序的磷酸化程度有所降低,而不影响表达水平。 最后,由于在所用条件下SGK1不能被胰岛素或EGF持续激活,我们产生了一个在疏水基序磷酸化位点含有天冬氨酸的突变。 SGK1-S422D的基础活性是受刺激的野生型SGK1的3-4倍(数据未显示)。 SGK1-S422D中C螺旋Arg147的突变显著降低了激酶活性,而不影响激活环的表达水平或磷酸化。
图8。 磷酸结合精氨酸在AGC激酶活化和磷酸化中的作用 体内 用表达HA或GST标记的野生型或突变型激酶的质粒转染COS7细胞。 在48小时和最后4小时的血清饥饿期后,将细胞暴露于20 nM EGF中20分钟或1µM胰岛素中8分钟,如图所示,然后进行裂解。 此后,用HA标签抗体或谷胱甘肽珠从细胞裂解液中沉淀激酶。 ( A类 )测定激酶活性,并将其表示为野生型刺激值的百分比。 数据是三个(RSK2、S6K1、MSK1和SGK1)或四个(PKBα)独立实验的平均值±SD,重复进行。 ( B类 )对(A)沉淀的激酶进行SDS-PAGE分析。 用指示的抗磷酸肽抗体对凝胶进行免疫印迹或蛋白质染色。
这些发现表明,磷酸结合的碱性残基对 体内 生长因子激活的AGC激酶的活性。 此外,结果表明,磷酸结合碱基残基可能通过促进催化活化以及保护疏水基序免受胞内磷酸酶的去磷酸化而发挥双重作用。
讨论 疏水基序磷酸化刺激AGC激酶活性的机制尚不清楚。 在本研究中,我们确定了疏水基序的磷酸丝氨酸/磷酸苏氨酸的结合位点,其功能是促进疏水基序与这些激酶中的疏水口袋的相互作用。 此外,我们提出了疏水基序和活化环的磷酸化可以协同刺激催化活性的机制。
虽然我们确定了PDK1中的磷酸结合位点,但这种激酶是一个例外。 PDK1没有疏水基序,它使用磷酸结合囊以磷酸化依赖的方式与某些底物的疏水基序对接。 我们之前已经描述了磷酸化依赖性对接如何使PDK1激活RSK2( 弗罗丁 等 ., 2000 )、S6K1和SGK1( 比昂迪 等 ., 2001 )这里我们描述了这种现象的结构基础。 综上所述,我们的研究结果表明,磷酸结合囊通过介导分子间和分子内激活步骤,在调节生长因子激活的AGC激酶中发挥着中心作用(图 9 ).
图9。 磷酸结合囊在生长因子激活的AGC激酶调节中的作用。 ( A类 )AGC激酶的激活机制可分为发散激活步骤和共同激活步骤。 在这两个步骤中,磷酸结合囊对磷酸丝氨酸/磷酸苏氨酸的识别可能起到关键作用,如这里的RSK和PKB所示。 (1) 在发散步骤中,激酶通过位于激酶结构域两侧的信号传导模块受到路径特异性调节,从而导致疏水基序磷酸化(在RSK中由C末端激酶结构域磷酸化,在PKB中由一个未知激酶磷酸化)。 在RSK(和S6K或SGK)中,疏水基序的磷酸盐随后被PDK1的磷酸盐结合囊识别,导致PDK1募集并随后磷酸化激活环。 因此,调节性磷酸化以强制性顺序发生。 在PKB中,PDK1是通过PH域介导的细胞膜共定位来募集的,因此调节性磷酸化的顺序似乎不是强制性的。 (2) 第二个激活步骤可能是所有含有磷酸化疏水基序的AGC激酶共同的,因此PKC、Rho激酶和Ndr也不在此研究。 在该步骤中,磷酸盐结合位点促进疏水基序与AGC激酶结构域内的疏水口袋的分子内结合。 与活化环磷酸化相一致,这导致激酶结构域的构象变化,从而导致催化活化。 ( B类 )(A)中使用的主要符号的键。
这里进行的结构建模和生化分析表明,磷酸结合位点对磷酸丝氨酸/苏氨酸的识别在所研究的激酶中类似。 当疏水基序停靠在口袋中时,磷酸基团被分别位于激酶结构域N末端和C螺旋中的两个相反位置的精氨酸或赖氨酸残基捕获。 这两个磷酸结合残基似乎并不同样重要,因为N-末端精氨酸/赖氨酸和C-螺旋精氨酸的突变通常分别导致激酶活化的部分和完全丧失。 PDK1的磷酸结合囊可能与其他激酶不同,因为PDK1包含四个N端碱基残基,根据突变分析判断,其中三个可能与疏水基序对接。 口袋附近的正电荷簇可能会吸引靶激酶基序中的磷酸盐,然后基序在口袋中对接。 正如BiaCore和EC所证明的那样,与激酶自身的基序相比,PDK1对其靶激酶磷酸化疏水基序的亲和力要高得多 50 测量值。 据推测,分子内相互作用中的亲和力可能较低,因为pHM的有效浓度较高。 此外,在分子内结合反应中具有低亲和力可能很重要,以便使磷酸化基序暴露于去磷酸化和激酶失活。
最近解决的PDK1晶体结构支持了我们对PDK1的磷酸盐结合囊的表征( 比昂迪 等 ., 2002 ). 在PDK1结构中,来自结晶缓冲液的硫酸根离子(可能模拟磷酸基)结合此处确定的两个碱基残基(Arg131和Lys76)以及Gln150和Thr148。 在我们的模型中,疏水基序的主干位于Thr148和磷酸基团之间,这应排除它们之间的相互作用。 相反,我们的模型允许Gln150与磷酸基团结合。 因此,除此处所述的残基外,Gln150还可能构成新的磷酸盐结合残基。
本研究直接证明磷酸化疏水基序可以通过分子内机制刺激生长因子激活的AGC激酶的催化活性。 这是使用 体外 用分离的RSK2、S6K1、MSK1、PKBα和SGK1激酶结构域进行重组分析,并添加疏水性基序肽。 结果表明,磷酸化的疏水基序不能单独诱导活化,而活化环的磷酸化可以使活性加倍。 然而,磷酸化疏水基序和磷酸化活化环的联合作用导致催化活性的协同刺激。 这些发现与以前关于这些磷酸化位点对PKB活性影响的更间接的研究一致( Alessi等人,1996年 ),S6K系列( Alessi等人,1998年 ; Dennis等人,1998年 )、RSK( Jensen等人,1999年 )和SGK1( 小林和科恩,1999年 ; Park等人,1999年 ).
问题是这两个磷酸化位点如何协同作用以刺激催化。 在这里,我们表明疏水基序中的磷酸盐与C-螺旋中的精氨酸残基相互作用,这可能为这个问题提供了答案。 在精氨酸残基之前,C-螺旋含有蛋白质激酶催化活性所需的保守谷氨酸残基。 现在解决的许多激酶结构表明,激酶的催化活性构象是相似的,而非活性构象则不同(参见 Huse和Kuriyan,2002年 ). 在活性构象中,C-螺旋中的谷氨酸残基(PKA中的Glu 91)与保守的赖氨酸残基形成离子对(PKA里的Lys72),其作用是定位ATP的磷酸盐,以便在激酶反应中进行磷酸转移。 在许多激酶的非活性构象中,C螺旋被移位,从而破坏谷氨酸-赖氨酸离子对。 激活此类激酶的关键步骤涉及C螺旋的重新定位,例如通过调节亚单位,以建立谷氨酸-赖氨酸离子对。 因此,我们建议磷酸化疏水基序与C-螺旋相互作用,以稳定保守的谷氨酸残基,从而与ATP-结合赖氨酸残基形成最佳离子对(图 10 ). 此外,在封闭、活性构象的PKA晶体中,活化环中的磷酸盐与C螺旋中的His87结合。 这种相互作用被认为是稳定封闭和活性构象的,在这种构象中,激酶结构域的小瓣和大瓣相互接近,活性位点的残基被固定在适当的位置进行催化( 约翰逊和刘易斯,2001 ; 约翰逊 等 ., 2001 ). 生长因子激活的AGC激酶也含有组氨酸或精氨酸,其位置相当于PKA C螺旋中的His87(图 5 A) 可能会在激活环中结合磷酸盐。 参考图中的RSK2模型 10 因此,我们建议活化环磷酸和磷酸化疏水基序通过C-螺旋发挥作用,诱导其协同刺激激酶活性:首先,活化环和疏水基序可以合作,将C-螺旋Glu118稳定在与ATP-结合Lys100的离子配对的最佳位置。 此外,基序占据口袋将限制C螺旋的流动性,从而有利于C螺旋Arg114与活化环磷酸结合,从而将激酶稳定在闭合的活性构象中。
图10。 疏水基序和激活环的磷酸盐如何协同激活AGC激酶的模型。 图中模型的功能区表示 5 RSK2的B与其疏水基序相互作用,但从另一个角度来看,它显示了整个RSK2激酶结构域。 该图说明了疏水基序和活化环的磷酸盐如何协同定位C螺旋,以优化Glu118和ATP-结合Lys100的离子配对。 此外,由疏水基序固定的C螺旋可以在大小叶之间起到桥梁的作用,以使激酶稳定在闭合(活性)构象中,如图所示。
我们的手稿提交后, Yang等人(2002) 发表了一个具有非磷酸化疏水基序的PKB结构,该结构与目前的研究结果一致。 在晶体中,疏水基序和C螺旋都不可见,这表明它们具有高度的流动性,因为基序在未磷酸化时不会停靠在口袋中。 体外 ,pHM 巴基斯坦中央银行 和HM PRK2系列 活化的PKB分别是PDK1预先磷酸化的4倍和15倍,而不是PKB-R200D。 最后,热量测量表明HM PRK2系列 PKB中的诱导顺序,通常解释为C螺旋和活性激酶构象的稳定。
我们还获得了磷酸盐结合残基在促进AGC激酶疏水基序磷酸化状态中的作用的证据。 该功能的重要性各不相同,S6K1和MSK1中的重要性较高,PKBα中的重要性较小,RSK2中未观察到该功能。 最有可能的是,基本残基通过保护磷酸丝氨酸/磷酸苏氨酸不被脱磷酸化来促进基序的磷酸化状态,这与结构模型所建议的基本残基之间磷酸的埋藏位置一致。
本研究使用五种不同AGC激酶亚家族成员的激酶进行。 因此,有理由假设此处描述的机制是包含磷酸化疏水基序的AGC激酶中的一般激活机制。 序列比对表明,疏水基序磷酸化位点和C-螺旋中的精氨酸/赖氨酸残基在此处未研究的AGC激酶亚家族中严格共同保守,如PKC、Rho激酶和Ndr相关激酶。 只有在极少数情况下,疏水基序中的负电荷似乎不需要激酶活性。 一个例子是PKCζ疏水基序中的谷氨酸残基,但残基增加了热稳定性,表明确实发生了与口袋的结合,并且具有功能性作用( 巴伦德兰 等 ., 2000 ; 帕雷克 等 ., 2000 ). N-末端碱基残基在约80%具有磷酸化疏水基序的AGC激酶中保守。 在其他激酶家族中,没有两个结合磷酸的碱基残基,这表明碱基残基在激酶折叠中没有结构功能,而只起到结合磷酸的作用。
总之,基于疏水基序和疏水囊之间磷酸化依赖性相互作用的分子内激活机制可能在AGC激酶中普遍存在。 如果是这样的话,该机制将代表迄今为止在蛋白激酶中描述的最普遍的激活机制,仅次于激活环磷酸化。
材料和方法 抗体、cDNA、免疫沉淀/印迹和蛋白质染色在可在 EMBO在线杂志 。
材料 肽序列为:S6肽(RRLSSLRA)、CREB肽(EILSRRPSYRK)、交叉肽(GRPRTSSFAEG)、pHM RSK公司 (KKPPSANAHQLFRGF S公司 mRSK2)的FVAITSDDE,pHM S6K系列 (TLSESANQVFLGF T型 rS6K1)的YVAPSC,pHM 新加坡黄金交易所 (VKEAAEAFLGF S公司 hSGK1)和pHM的YAPPTP 韩国 (VGNQLPFIGF T型 hROKα的YFRENL),带下划线残基磷酸化。
体内AGC激酶分析 将含有沉淀激酶的珠重新悬浮在20µl 1.5×缓冲液A(30 mM Tris–HCl pH 7.5,10 mM MgCl)中 2 ,1 mM二硫苏糖醇)。 通过添加10µl(最终浓度)的ATP(200µM,0.2µCi的[γ- 32 P] ATP)和肽底物:800µM S6肽(RSK,S6K)、166µM交叉肽(PKB,SGK)或200µM CREB肽(MSK)。 在28°C下剧烈摇晃10分钟后(反应与时间呈线性),去除20µl上清液(留下沉淀的激酶)并将其斑点在磷酸纤维素纸上(Whatman p81)。 用150 mM正磷酸清洗后[ 32 P] 磷成像仪(Molecular Dynamics Inc.)对蛋白质底物中的磷酸盐进行定量。
体外AGC激酶测定 在RSK2分析中,200 ng GST–血凝素(HA)-RSK2 1–373 (野生型或R119A)在28°C下,在20µl含有60µM MgATP的缓冲液A中孵育1小时,加入或不加入100 ng His-PDK1 体外 此时,根据时间进程实验测定,PDK1对RSK的磷酸化已达到饱和。 在S6K1、MSK1和PKBα检测中,COS7细胞与表达HA-S6K的质粒共转染 1–364 、HA-MSK1 1–370 ,HA-PKBα 1–467 或其点突变体连同mycPDK1或空载体。 然后使用如上所述的抗HA抗体从裂解细胞中纯化S6K1、MSK1或PKBα,并重新悬浮在20µl缓冲液A中。 在SGK1测定中,GST–SGK1 61–431 或GST–SGK1 61–415 使用或不使用His-PDK1和100µM MgATP培养1小时 体外 然后用镍琼脂糖珠沉淀去除His-PDK1。 GST–SGK1 61–431 (40 ng)或GST–SGK1 61–415 然后将(400 ng)重新悬浮在20µl缓冲液A中。 然后,在没有或存在所示疏水基序肽的情况下,使用上述激酶分析条件测定RSK、S6K、MSK、PKB或SGK活性。 对于RSK,从所有值中减去反应空白(仅PDK1)。 His-S6K1的磷酸化 1–421 由PDK1执行,如所述( Biondi等人,2001年 ).
建模程序 人体PDK1的同源建模和能量最小化 75–351 ,鼠标RSK2 62–351 和人类PKBα 144–417 使用INSIGHT II(97.0)(Biosym/MSI,圣地亚哥)中实现的同源性和发现模块执行序列。 建模实验的模板是PKA(1YDR)( 英语 等 ., 1996 )它与目标具有39-45%的序列一致性和60-64%的相似性。 使用Discover中实现的最陡下降算法执行能量最小化。 计算忽略了溶剂相互作用。 所使用的力场是在INSIGHT II中实现的AMBER。 使用斯克里普斯研究所和分子图形学实验室的AUTODOCK程序(3.0.3版),使用默认参数将疏水基序肽对接到疏水囊中,然后手动进行精制。 疏水基序肽被认为是刚性的,没有扭转角度的灵活性。 程序GRID(版本20)( 古德福德,1985年 )用于计算疏水表面轮廓,用于预测疏水囊的范围。 PROCHECK程序( 拉斯科夫斯基 等 ., 1993 )用于验证能量最小化结构的几何结构。
致谢 致谢 我们感谢Birte Kofoed提供的专家技术援助,Sine Larsen博士、Anne Mölgard博士和Lydia Tabernero博士提供的结构建议,以及George Thomas博士提供的pRK5-GST–S6K1。 这项工作得到了丹麦癌症协会(DP01004)、丹麦诺和诺德基金会和丹麦生长与再生研究中心的资助。
工具书类
Alessi D.R.、Andjelkovic M.、Caudwell B.、Cron P.、Morrice N.、Cohen P.和Hemmings B.A.(1996)胰岛素和IGF-1激活蛋白激酶B的机制。 EMBO J.,第15期,6541–6551页。 [ PMC免费文章 ][ 公共医学 ][ 谷歌学者 ]
Alessi D.R.、James,S.R.、Downes,C.P.、Holmes,A.B.、Gaffney,P.R.、Reese,C.B.和Cohen,P.(1997)磷酸化并激活蛋白激酶Bα的3-磷酸肌醇依赖性蛋白激酶的表征。 货币。 生物学,7261–269。 [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Alessi D.R.、Kozlowski,M.T.、Weng,Q.P.、Morrice,N.和Avruch,J.(1998)3-磷酸肌醇依赖性蛋白激酶1(PDK1)磷酸化并激活p70 S6激酶 体内 和 体外 .货币。 生物学,8,69–81。 [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Balendran A.、Biondi,R.M.、Cheung,P.C.、Casamayor,A.、Deak,M.和Alessi,D.R.(2000)PDK1对蛋白激酶Cζ(PKCζ)和PKC相关激酶2进行磷酸化需要3-磷酸肌醇依赖性蛋白激酶-1(PDK1)对接位点。 生物学杂志。 化学。, 275, 20806–20813. [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Biondi R.M.、Cheung,P.C.、Casamayor,A.、Deak,M.、Currie,R.A.和Alessi,D.R.(2000)PDK1激酶结构域中与PIF和PKA C末端残基相互作用的口袋的鉴定。 EMBO J.,1979-988年。 [ 内政部 ][ PMC免费文章 ][ 公共医学 ][ 谷歌学者 ]
Biondi R.M.、Kieloch,A.、Currie,R.A.、Deak,M.和Alessi,D.R.(2001)PDK1中的PIF-结合囊对S6K和SGK的激活至关重要,但对PKB则不然。 EMBO J.,20,4380–4390。 [ 内政部 ][ PMC免费文章 ][ 公共医学 ][ 谷歌学者 ]
Biondi R.M.、Komander,D.、Thomas,C.C.、Lizcano,J.M.、Deak,M.、Alessi,D.R.和van Aalten,D.M.F.(2002)人类PDK1催化域的高分辨率晶体结构定义了调节性磷酸肽对接位点。 EMBO J.,21,4219–4228。 [ 内政部 ][ PMC免费文章 ][ 公共医学 ][ 谷歌学者 ]
Deak M.、Clifton,A.D.、Lucocq,L.M.和Alessi,D.R.(1998)有丝分裂原和应激激活蛋白激酶-1(MSK1)直接被MAPK和SAPK2/p38激活,可能介导CREB的激活。 EMBO J.,174426–4441。 [ 内政部 ][ PMC免费文章 ][ 公共医学 ][ 谷歌学者 ]
Dennis P.B.、Pullen,N.、Pearson,R.B.、Kozma,S.C.和Thomas,G.(1998),自身抑制域中的磷酸化位点参与p70 6000平方公里 激活环磷酸化。 生物学杂志。 化学。, 273, 14845–14852. [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Engh R.A.、Girod,A.、Kinzel,V.、Huber,R.和Bossemeyer,D.(1996)异喹啉磺酰蛋白激酶抑制剂H7、H8和H89配合物中cAMP依赖性蛋白激酶催化亚基的晶体结构。 选择性的结构影响。 生物学杂志。 化学。, 271, 26157–26164. [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Etcheshere L.C.、van Bemmelen、M.X.P.、Anjard,C.、Traincard,F.、Assemat,K.、Reymond,C.和Veron,M.(1997) 粘液菌 cAMP依赖性蛋白激酶。 N-末端结构域和C-末端残基在催化活性和稳定性中的作用。 《欧洲生物化学杂志》。, 248, 820–826. [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Flynn P.、Mellor,H.、Casamassima,A.和Parker,P.J.(2000)Rho GTPase通过3-磷酸肌醇依赖性蛋白激酶控制蛋白激酶C相关蛋白激酶的激活。 生物学杂志。 化学。, 27511064–11070之间。 [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Franke T.F.、Yang,S.I.、Chan,T.O.、Datta,K.、Kazlauskas,A.、Morrison,D.K.、Kaplan,D.R.和Tsichlis,P.N.(1995)Akt原癌基因编码的蛋白激酶是PDGF激活的磷脂酰肌醇3-激酶的靶点。 手机,81、727–736。 [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Frödin M,Jensen,C.J.,Merienne,K.和Gammeloft,S.(2000)蛋白激酶RSK2中磷酸丝氨酸调节的对接位点,可招募和激活PDK1。 EMBO J.,192924–2934。 [ 内政部 ][ PMC免费文章 ][ 公共医学 ][ 谷歌学者 ]
Goodford P.J.(1985)确定生物重要大分子上能量有利结合位点的计算程序。 医学化学杂志。, 28, 849–857. [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Guex N.和Peitsch,M.C.(1997)《瑞士模式和瑞士数据库查看器:比较蛋白质建模的环境》。 电泳,18,2714–2723。 [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Huse M.和Kuriyan,J.(2002)蛋白质激酶的构象可塑性。 单元格,109,275–282。 [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Jensen C.J.、Buch,M.B.、Krag,T.O.、Hemmings,B.A.、Gammeloft,S.和Frödin,M.(1999)90-kDa核糖体S6激酶被磷酸化,并被3-磷酸肌醇依赖性蛋白激酶-1激活。 生物学杂志。 化学。, 274, 27168–27176. [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Johnson D.A.、Akamine,P.、Radzio-Andzelm,E.、Madhusudan,M.和Taylor,S.S.(2001)cAMP依赖性蛋白激酶的动力学。 化学。 版次:1012243–2270。 [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Johnson Negal和Lewis,R.J.(2001)磷酸化控制的结构基础。 化学。 版次:101、2209–2242。 [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Knighton D.R.、Zheng,J.H.、Teneyck,L.F.、Ashford,V.A.、Xuong,N.H.、Taylor,S.S.和Sowadski,J.M.(1991)环磷酸腺苷依赖性蛋白激酶催化亚基的晶体结构。 科学,253407-414。 [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Kobayashi T.和Cohen,P.(1999)激活磷脂酰肌醇3-激酶的激动剂激活血清和糖皮质激素调节蛋白激酶是由3-磷酸肌醇依赖性蛋白激酶-1(PDK1)和PDK2介导的。 生物化学。 《华尔街日报》,第339、319–328页。 [ PMC免费文章 ][ 公共医学 ][ 谷歌学者 ]
拉斯科夫斯基R.A.、麦克阿瑟M.W.、莫斯D.S.和桑顿J.M.(1993)。 PROCHECK:检查蛋白质结构立体化学质量的程序。 J.应用。 结晶器。, 26, 283–291. [ 谷歌学者 ]
Ming X.F.,Burgering,B.M.,Wennstrom,S.,Claesson Welsh,L.,Heldin,C.H.,Bos,J.L.,Kozma,S.C.和Thomas,G.(1994)通过不依赖于p21ras的途径激活p70/p85 S6激酶。 《自然》,371426-429。 [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Parekh D.B.、Ziegler,W.和Parker,P.J.(2000)多途径控制蛋白激酶C磷酸化。 EMBO J.,第19期,496–503页。 [ 内政部 ][ PMC免费文章 ][ 公共医学 ][ 谷歌学者 ]
Park J.,Leong,M.L.,Buse,P.,Maiyar,A.C.,Firestone,G.L.和Hemmings,B.A.(1999)血清和糖皮质激素诱导激酶(SGK)是PI 3-激酶刺激信号通路的靶点。 EMBO J.,18,3024–3033。 [ 内政部 ][ PMC免费文章 ][ 公共医学 ][ 谷歌学者 ]
Pullen N.、Dennis P.B.、Andjelkovic M.、Dufner A.、Kozma S.C.、Hemmings B.A.和Thomas G.(1998)PDK1对p70s6k的磷酸化和活化。 科学,279707-710。 [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Richards S.A.、Fu,J.、Romanelli,A.、Shimamura,A.和Blenis,J.(1999)核糖体S6激酶1(RSK1)激活需要依赖和独立于MAP激酶ERK.Curr的信号。 生物学,9810-820。 [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Stokoe D.、Stephens,L.R.、Copeland,T.、Gaffney,P.R.、Reese,C.B.、Painter,G.F.、Holmes,A.B.、McCormick,G.和Hawkins,P.T.(1997)磷脂酰肌醇-3,4,5-三磷酸在蛋白激酶B活化中的双重作用。 《科学》,277567-570。 [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Sturgill T.W.、Ray,B.L.、Erikson,E.和Maller,J.L.(1988)胰岛素刺激的MAP-2激酶磷酸化并激活核糖体蛋白S6激酶II。 《自然》,334,715–718。 [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Vik T.A.和Ryder,J.W.(1997)确定丝氨酸380是 爪蟾 第90页rsk。 生物化学。 生物物理学。 Res.Commun.公司。, 235, 398–402. [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Williams M.R.、Arthur,J.S.、Balendran,A.、van der Kaay,J.、Poli,V.、Cohen,P.和Alessi,D.R.(2000)《3-磷酸肌醇依赖性蛋白激酶1在激活胚胎干细胞中定义的AGC激酶中的作用》。 货币。 生物学,10439–448。 [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
Yang J.,Cron,P.,Thompson,V.,Good,V.M.,Hess,D.,Hemmings,B.A.和Barford,D.(2002)疏水基序磷酸化调节蛋白激酶B/AKT的分子机制。 分子细胞,9,1227–1240。 [ 内政部 ][ 公共医学 ][ 谷歌学者 ]
EMBO Journal的文章由以下人员提供 自然出版集团