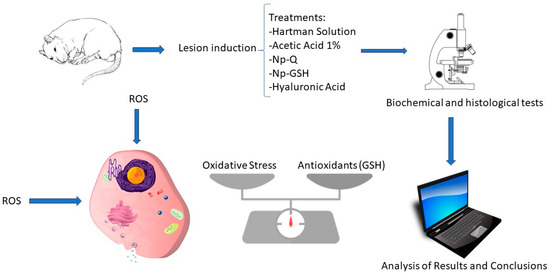
1.简介
骨关节炎是一种退行性、进行性和致残性关节软骨疾病,伴有潜在的骨和软组织改变。其主要特征是关节软骨的进行性侵蚀,相同的炎症过程导致细胞外基质降解和软骨细胞死亡。
软骨的特点是具有最小的修复能力。由于金属蛋白酶、炎症介质和细胞因子的释放,炎症过程有利于关节的恶化,这些物质降解蛋白多糖并减少其合成,导致软骨基质耗竭[1,2]. 另一方面,关节炎引起的缺血和再灌注导致自由基和活性氧的产生,这些自由基和反应氧降解透明质酸和糖胺聚糖链,抑制其合成,增加细胞因子和金属蛋白酶的产生,并诱导软骨细胞凋亡[三]. 目前,没有有效的治疗方法来阻止这种疾病的发展[4]. 关节损伤通常使用非甾体抗炎药(NSAIDs)和糖胺聚糖进行治疗,以防止炎症过程,减轻疼痛,改善关节功能。然而,它们只代表一种对症治疗,其有效性仍有争议[5,6,7,8]. 最近的研究表明,在滑液中使用抗氧化化合物治疗骨关节炎,特别是调节氧化过程,而不是消除自由基或抑制炎症过程[三,7,9,10]. 在本研究中,我们通过解剖雄性Wistar大鼠膝关节交叉韧带,研究了关节内注射壳聚糖纳米粒子和谷胱甘肽对手术诱导的骨关节炎大鼠的影响。这种方法促进了高度可重复的病变,变异性小,进展迅速。它统一了现有的各种变量,是短期研究的理想选择。它可以观察药物的细微作用,否则在加速退化的情况下可能会被忽视[11,12]. 谷胱甘肽(GSH)是主要的细胞抗氧化剂。它的合成只发生在细胞浆中,调节软骨细胞的氧化应激及其对疾病的抵抗力和恢复力。纳米结构系统的存在能够促进抗氧化事件,从而改善与软骨和骨关节炎细胞外基质相关的组织病理学、细胞和生物化学条件,这是该病患者使用的基本可能性。 据认为,导致骨关节炎的细胞事件是氧化-还原失衡、炎症、抗氧化复合物对控制这种状态的低贡献,以及ECM的蛋白聚糖和胶原蛋白的紊乱和功能,其中抗氧化活性的贡献至关重要。
2.材料和方法
2.1、。纳米粒子
采用离子凝胶法制备了谷胱甘肽壳聚糖纳米粒(NP-GSH)[13],从1%乙酸基溶液调节至pH值4.1,并使用1%Pluronic F-68。将溶液分为2种,第一种溶液中,0.3%的壳聚糖和1%的谷胱甘肽被溶解;第二种溶液包括0.1%三聚磷酸钠(STPP)。在混合溶液之前,两种溶液都要通过纸进行独立过滤,以去除不溶性杂质。将两种溶液以1:1的比例混合,将STPP溶液添加到壳聚糖溶液中,并将其搅拌4 h。为了获得与透明质酸(10 mg/mL)相当的壳聚糖浓度,作为本研究的对照处理,在22253 g/4°C/60 min的条件下对已形成的纳米粒子进行超速离心,回收形成的环,并用1%的乙酸溶液清洗4次,将pH值调整到4.1,以消除剩余的未形成纳米粒子的多余材料。 与先前研究中的方法不同,在本研究中,使用的系统是通过膜过滤的。为了对本研究中的纳米粒子进行消毒,在给药前,将其暴露在紫外线下14小时,并在使用前冷藏(4°C)。壳聚糖纳米粒子(NP-Q)是使用相同的方法制备的,仅省略了GSH的添加。
对于纳米粒子的表征,使用Zetasizer和Malvern Panalytical的Nanosight NS300仪器测定了粒径和zeta电位。使用100 kV的钨丝高压进行了透射电子显微镜(TEM)(日本东京日立)。采用2,2′-二硝基-5-5′二硫代二苯甲酸(DTNB)比色法间接定量纳米粒子中的谷胱甘肽,并在425nm波长下测定结果。
2.2. 骨关节炎的诱导
所有研究均按照CICUAE批准的方案(FESC/CICUAE/06/03/2018)进行,该方案用于管理联阿援助团FES-Cuautitlán的实验动物。50只雄性Wistar品系褐家鼠(280–320 g)从FESC多学科研究单位的分离和活体单位获得。将体重280–320 g的雄性大鼠与5只个体放在盒子里。他们在UIM Vivarium随意享用食物和水,尊重环境的光-暗循环。他们被随机分为4组(表1)在术前准备过程中,动物被转移到手术室,在那里给它们注射氯胺酮-甲苯噻嗪(50 mg–10 mg/kg/IM)进行全身麻醉。随后,给予庆大霉素(6 mg/kg/IM)和丁丙诺啡(0.05 mg/kg/SC)。在实施三分法和膝盖刺绣手术方案之前,对每只动物进行称重,并拍摄X光片。对每只大鼠随机选择要使用的膝盖。 任何表现出与诱发损伤、感染或其他病理学无关的疼痛或跛行的动物均被排除在研究之外。按照Hayami和Pickarski(2004)的描述进行前交叉韧带横断术(ACLT)[14]内侧切口,髌骨外侧脱位,关节屈曲,显露并横断颅交叉韧带。与半月板切除术不同,骨关节炎病变是由ACLT引起的,软骨受到有限或部分破坏。 该程序促进了具有良好重复性的实验模型,并有助于短期疾病研究[15]. 在手术干预和相应治疗7天后,将动物带到终点,收集两个膝盖进行进一步研究。 实验组包括10只确诊病变的大鼠。他们在手术后7天接受关节内治疗,每次治疗单剂量,每次治疗使用40µL和胰岛素注射器。使用的治疗方法如下:阴性对照1%乙酸、哈特曼溶液(HS)、10 mg/mL透明质酸(HA)、NP-GSH和NP-Q。
2.2.1. 射线照相研究
在手术、给药和处死前进行计算机放射学研究(计算机放射成像FCR Prima(日本东京富士胶片公司)),对每只大鼠的双膝进行两次注射(内侧和颅尾侧),以评估骨关节炎病变的程度。
2.2.2. 牺牲和样品处理
术后14天,按照与手术相同的方案在麻醉下处死动物,并将其带到终点以恢复双膝。病变对侧为对照侧,ACLT为实验侧。每组五只大鼠被指定用于组织病理学研究,以保持胶囊的完整性。同时,从其余大鼠获取关节软骨,进行GSH生化分析和TBARS定量。根据Bradford方法,部分样品用于测定总蛋白浓度。通过分光光度法定量谷胱甘肽的全部含量[16]. 2.3. 脂质过氧化
脂质过氧化分析是根据Ohkawa等人(1979年)描述的方法进行的,并进行了一些修改[17]. 2.4. 组织病理学和免疫组织化学评价
考虑到关节是由不同组织组成的复杂结构,由特殊组织和关节软骨覆盖在其关节表面的骨基底组成,关节软骨主要由水(60-80%)和由II型胶原纤维形成的细胞外基质(>60%)组成,沉入富含蛋白聚糖(PGs)和糖蛋白(GPs)的基本物质凝胶中,由软骨的唯一常驻细胞合成,软骨细胞浸没在细胞外基质(软骨基质)中,对暴露于研究中的Np的关节进行组织病理学分析,使我们能够以整体和特定的方式了解暴露对某些成分的影响。
作为组织病理学检查的主要染色方法,进行苏木精-伊红染色,以及van Gieson、甲苯胺蓝、藏红O和吖啶橙染色。然后,对2A1型胶原(Col-2)和金属蛋白酶13(MMP-13)进行免疫组化检测。
组织病理切片采用从Mankin系统修改的指南进行评估,该指南分别限定了每个形态学特征[18,19,20]. 免疫组织化学
使用来自Santa Cruz Biotechnology的小鼠单克隆抗体Col2A1(M2139)和MMP-13(C-3),使用生物素化的抗小鼠二级抗体(驴抗小鼠IgG(H+L)生物素,Millipore,Burlington,MA,美国)和抗生物素-生物素复合物(美国加利福尼亚州伯灵盖姆,矢量,ABC Elite PK-6100)。用DAB-过氧化物酶试剂盒(过氧化物酶底物试剂盒DAB SK-4100载体)显示抗体结合,并用Crystal Violet(C5042,Sigma,St.Louis,MO,USA)进行复染。
II型胶原(Col2A1)的存在与健康组织的存在有关,当受损后肥大时,健康组织开始被X型胶原取代。另一方面,金属蛋白酶13(MMP-13)是软骨评估中最广泛使用的炎症标志物,因为它是关节软骨降解的主要蛋白酶[21,22]. 2.5. 统计分析
对于生化测试,每个实验都要进行三次。数据表示为平均值±SEM,并使用单向方差分析(ANOVA)进行分析,然后使用Prism程序10.0.2版(Graphpath)对Tukey的平均值多重比较进行事后检验,考虑到以下显著差异:第页< 0.05. 在对每个特征进行放射学和组织病理学分析的情况下,使用双向方差分析(ANOVA)对数据进行分析,然后进行Tukey均值多重比较的事后检验,考虑到以下显著差异:第页< 0.05. 除上述内容外,还对组织病理学检查的特征进行了综合分析,使用单因素方差分析(ANOVA),然后对Kruskal–Wallis均值的多重比较进行事后检验,考虑到如果第页< 0.05.
3.结果和讨论
3.1. 纳米粒子的制备与表征
使用前面描述的离子凝胶法制备了两组壳聚糖纳米粒,分别含有和不含谷胱甘肽[13]. 其表征结果如所示图1和图2和表2 3.2、。壳聚糖和谷胱甘肽浓度的估算
在制备纳米颗粒并对其进行调节以用于骨关节炎大鼠的给药后,我们根据实验大鼠的体重量化了进行关节内给药的成分浓度。纳米粒子中的壳聚糖浓度为4.436 mg/mL,通过分光光度法估算GSH 11.3 mM。然后,NP-Q和NP-GSH的关节内给药剂量为0.6壳聚糖mg/Kg(0.46 mg/Kg GSH和1.3 HA mg/Kg)。
3.3. 骨关节炎大鼠的评估
手术后一天,大鼠出现严重跛行(图3),直到术后第4天逐渐减少。目前的跛行和炎症是由手术引起的,手术涉及关节囊切开。随后,在剩下的10天里,大鼠在支撑受伤肢体时没有表现出明显的不适。 没有一只动物对所给的治疗有任何不良反应。经影像学评估证实,ACLT手术诱导OA 2周后产生中度病变(图3)这是评估疾病急性变化的理想方法。 射线照相评估
大鼠的放射照相研究(图4)分别在术后0、7和14天进行,对应于OA手术诱导前、治疗给药和牺牲前的时间。 第0天,所有动物均未出现任何损伤,凯尔格伦和劳伦斯评分均为“0”[23]. 在第7天手术诱导OA后,大鼠的ACLT膝关节出现放射学改变,包括关节表面不规则、骨赘和提示硬化的密度变化。所有与对侧膝关节相比平均得分为“2”的患者均被视为对照组,未观察到任何差异。 在第14天的影像学评估中,ACLT组表现出更严重的影像学改变,根据Kellgren和Lawrence量表得分为2到3.5分[23] (图5). 经Np-Q治疗的动物之间存在显著差异,而经HA治疗的动物最能保留ACLT膝关节之间的骨结构。尽管Np-Q和AH治疗组之间存在显著差异,但与其他ACLT治疗组相比,它们没有显示出显著差异。 与AH和Hartmann溶液治疗组相比,Np-GSH治疗组大鼠表现出轻微的非显著性变化(第页≤ 0.001). 在给予不同的治疗后,对照膝关节出现了显著的影像学变化。用哈特曼溶液、醋酸和HA治疗的动物没有表现出影像学变化(图5). 这些可能与因对侧膝关节代偿作用而产生的机械应力有关,也可能是因关节穿刺而引起的炎症过程的一部分,而不是由于所给予的治疗。
在NP治疗组的放射变化分析中,他们显示出显著变化(第页≤0.001)与其他对照组相比(图5). 这些变化包括关节表面不规则,以及与骨赘相关的图像。用Np GSH治疗的对照组表现出等级为1的变化(轻度损伤)。相反,患有Np-Q的对照组退化程度更大,达到2级病变(中度损伤),与使用AH和Hartmann溶液的ACLT组相比,没有显示出统计上的显著差异(第页≤ 0.001). 3.4. 谷胱甘肽定量
从匀浆和溶解的关节软骨和半月板中量化关节内GSH和TBARS的浓度。
图6显示了使用乙酸作为纳米粒子分散介质的对照组中GSH的最高浓度。该组GSH的显著增加归因于细胞机制的激活,以对抗暴露于该培养基的直接损伤。 在含有NP和乙酸作为载体的系统中未观察到这些影响。此外,尽管关节损伤组由于疾病期间发生的氧化应激而表现出GSH降低,但与使用哈特曼溶液的对照组相比,它们没有显示出显著差异(第页≤ 0.0001).
与预期相反,在对照组和LCC大鼠暴露于Np-GSH的关节中观察到最低的GSH浓度。其他组没有发现显著的统计差异。在体外软骨细胞的研究中也观察到类似的结果[13]. 高浓度的Np-GSH(0.6 mM GSH)显示GSH浓度低于未处理细胞中的GSH浓度,两组之间无统计学差异。这些影响可能与组织对手术引起的炎症的反应、改变实验动物的运动以及受影响区域的细胞反应有关。 3.5. TBARS量化
与其他研究报告相反[13,24,25,26],我们观察到,当用TBARS分光光度法评估时,没有OA损伤的组显示出最高的MDA浓度(图7). 仅用乙酸处理的组显示出最高的MDA浓度(3.271 nmol/mg蛋白质),可能是由于与给药载体相关的酸性微环境;然而,在接触壳聚糖纳米粒的关节中没有观察到这种作用(图7). 这表明由于抗氧化作用,NP具有保护作用(13)。一些研究表明,壳聚糖具有抗氧化能力和酸碱调节作用,因此它可能诱导MDA浓度降低(1349 nmol/mg蛋白质)。 3.6. 蜂窝网络分布
苏木精-伊红(HE)染色作为细胞和软骨基质形态学评价的基本染色方法,评价细胞分布、数量、形态细胞、软骨下骨、潮痕、关节面和MEC。为了评估胶原蛋白纤维的存在和分布,基于品红染料对胶原蛋白的选择性,我们使用van Gieson染色。在应力刺激下,关节软骨中常驻软骨细胞的分布始于形成小细胞群(等基因群)的柱状组织。随后,如果压力继续存在,细胞凋亡导致的细胞丢失会促进细胞之间出现巨大的空间,使其孤立。这种分布变化在对照组和ACLT组之间非常明显,其中柱状组织的丢失更为明显,在所分析的区域中存在差异分布(方差分析;疾病因素:F(1,30)=66.59;第页< 0.0001).
从中可以看出图8和图9(方差分析;处理因子:F(4,30)=13.52;第页<0.0001,相互作用:F(4,30)=1.191;第页=0.3348),经Np-Q治疗的健康软骨组织的丧失与ACLT组相当。Np-Q影响软骨中的细胞分布。与暴露于Hartmann溶液的对照组动物相比,使用Np-GSH治疗的动物没有观察到这种效果,与传统HA治疗诱导的效果非常相似,Np-GSH显示出在OA中保持细胞组织的能力。 3.7. 细胞群体
在患有ACLT的实验大鼠中,软骨常驻细胞群的减少不仅表现在细胞数量的减少,而且表现在细胞分布上。在完全没有细胞的区域可以发现它们是孤立的细胞。不同治疗组中观察到的变化与细胞分布的变化有关(参见图8). ECM变化最显著的区域位于软骨的脱细胞区域。 尽管在分析实验动物关节中的细胞群时,两种治疗方法之间没有观察到统计学差异(图9)(方差分析;疾病因素:F(1,27)=33.52;第页<0.0001,处理因子F(4,27)=1.6;第页=0.2029,相互作用:F(4,27)=0.6332;第页=0.6432),应注意,在给药Np-GSH后ACLT软骨的组织病理学检查中,未观察到完全脱细胞区域。细胞分布广泛。值得一提的是,用Np-GSH治疗的动物呈现出更显著数量的等基因组,这可能是软骨对细胞增殖的反应,并重新填充因手术中韧带丢失而丢失的细胞区域(见图8). 3.8. 细胞形态学
骨关节软骨细胞趋向于肥大,导致ECM的生成发生改变,从而导致其虚弱和降解(图8). 更多的肥大软骨细胞说明了关节损伤的程度以及修复的尝试。 在所给的不同治疗中,只有接受Np-Q治疗的动物软骨细胞的形态发生了变化,包括肥大软骨细胞数量的增加以及在损伤最严重的区域出现类似纤维细胞的细胞(方差分析;疾病因子:F(1,27)=1.713;第页=0.2016,处理因子:F(4,27)=9.142;第页=0.0001,相互作用:F(4,27)=2.653;第页= 0.0548). 在接受Np-Q治疗的对照组中,软骨细胞肥大的增加更为严重(参见图9). 用Np-GSH处理的实验大鼠的结果显示,软骨细胞形态与HA相同。 3.9. 潮汐标志
“潮位线”或基线是在关节软骨与软骨下骨接触之前,将关节软骨区域与钙化软骨区分开来的边界。潮痕的消失表明关节损伤已经到达软骨的最深处。这是软骨下骨变化的开始,随后会导致骨化。
在对照组和ACLT组中,服用Np-Q均会导致严重损伤(图8). 有趣的是,在Np-GSH暴露组及其对照组中未观察到这种影响。然而,基线稍有中断,这在其他对照组中没有观察到。在ACLT组中,HA组表现出最严重的基线损伤,而NP-GSH组表现出更好的软骨层保护,甚至与对照组相比(参见图9)(方差分析;疾病因素:F(1,29)=19.52;第页=0.0001,处理因子:F(4,29)=4.667;第页=0.005,相互作用:F(4,29)=5.479;第页= 0.0021). 3.10. 软骨下骨
与基线中观察到的变化一样,在软骨下骨水平观察到与深层机械应力传播有关的差异(图8和图9). 将影像学评估结果与基础状态联系起来,Np-GSH没有显示出任何保护该层的能力,我们甚至观察到对照组软骨下骨的变化,与关节软骨的发现相反(ANOVA;疾病因素:F(1,27)=14.51;第页=0.007,处理因子:F(4,27)=8.424;第页=0.0001,相互作用:F(4,27)=2.923;第页= 0.038).
3.11. 关节曲面
在急性损伤的情况下,ACLT组的关节表面观察到的变化很小,表面的轻微不规则几乎与对照组没有区别(图8)(方差分析;疾病因子:F(1,29)=9.594;第页=0.0043,处理因子:F(4,29)=84.61;第页<0.0001,相互作用:F(4,29)=5.125;第页= 0.003). 在对照组和ACLT组中,只有Np-Q显示出更严重的病变,甚至可以观察到关节软骨的严重溃疡,如图10. 3.12. 细胞外基质(MEC)
就软骨基质的构成而言,对照组和ACLT组之间的变化比表面上的变化更明显(参见图10)(方差分析;疾病因子:F(1,29)=9.594;第页=0.0043,治疗因子:F(4,29)=84.61;第页<0.0001,相互作用:F(4,29)=5.125;第页= 0.003). 再次,Np-Q突出,显示ECM向具有纤维组织特征的软骨方向发生较大变化。与这些结果相反,Np-GSH表现出更好的基质保存。 3.13。吖啶橙
此外,进行吖啶橙染色,如图11这使我们能够评估软骨细胞群中与坏死和凋亡过程相关的早期细胞损伤[27];结果表明,细胞质和细胞核的红色减少,同时细胞死亡增加;这是由于DNA降解的细胞中RNA的浓度降低。 在ACLT组中,观察到着色较少,细胞核完全为绿色的细胞,尤其是靠近脱细胞区域的区域,可能与该区域的细胞损伤有关。有趣的是,与其他组相比,接受Np-GSH治疗的组是唯一表现出差异的组,这表现在根据细胞的颜色更好地划分细胞。
3.14. 蛋白聚糖损失
据报道,甲苯胺蓝染色和藏红O染色使我们能够看到关节软骨内存在蛋白多糖(PGs)。相反,藏红O染色的强度与蛋白聚糖的浓度成正比,甲苯胺蓝染色与骨关节炎软骨的亲和力更好有关。
对照组呈现出更大的着色,如图10和图12其中,它们的条件最低(蛋白质多糖损失较少)。相比之下,ACLT组表现出着色缺失,尤其是在细胞丢失的区域,这是可以预料的,因为这些细胞合成PG。 然而,NP组表现出轻微的损失,由于强度降低,尤其是甲苯胺蓝染色,在对照组有活细胞的区域仍然可见。虽然只有患有Np-Q的ACLT组与其他治疗组的对照组相比显示出显著差异,但对照组的颜色消失程度与患有哈特曼溶液、醋酸和HA的ACLT对照组相当,而Np-GSH颜色消失程度更为温和(ANOVA;疾病因素:F(1,27)=48.46;第页<0.0001,处理因子:F(4,27)=7.583;第页=0.0003,相互作用:F(4,27)=1.316;第页= 0.2892).
3.15. 胶原蛋白2和金属蛋白酶13
Col-2与健康组织的存在有关,健康组织在损伤后肥大,并开始被X型胶原取代。另一方面,金属蛋白酶13(MMP-13)的存在是软骨评估中最常用的炎症标志物,因为它是关节软骨降解的主要蛋白酶。通过免疫染色评估Col-2的存在(图13). 结果表明,2型胶原在个体间分布不均匀,组间差异无显著性(ANOVA;疾病因素:F(1,29)=0.4921;第页=0.4886,处理因子:F(4,29)=1.132;第页=0.3608,相互作用:F(4,29)=0.3968;第页= 0.8092). 在统计评估中没有考虑一些观察到的特征,例如纤维的组织。我们发现ACLT组之间的差异最显著;与对照组相比,纤维组织发生了变化。
此外,Np-Q治疗显示免疫反应强度增加。同时,它们似乎表现出胶原纤维的聚集,而Np-GSH尽管显示出最强烈的免疫反应性和最佳的纤维组织,但仍保留了较好的纤维组织结构,即使与哈特曼溶液的对照组相比,也没有增加信号。有趣的是,HA组、对照组和ACLT组显示出最强烈的信号和最佳的纤维组织,即使与哈特曼溶液的对照组相比也是如此。
金属蛋白酶13(MMP-13)是OA的炎症标志物之一,因为它是软骨降解的主要原因之一。MMP-13在健康关节中可检测到,因为它参与ECM的正常周转[19,21]. 然而,据报道,自ACLT诱导OA后的第一周起,其急剧增加[24]. 使用哈特曼溶液、乙酸和HA的对照组没有任何迹象,或在关节中有一个或两个孤立点(图13),这看起来确实不正常[28]. 尽管如此,与整个研究中MMP-13浓度最高的HA ACLT组相比,NP组MMP-13的浓度较低,这证实了尽管HA具有机械保护功能,但它并不那么抗炎(图9)(方差分析;疾病因素:F(1,23)=11.48;第页=0.0025,处理因子:F(4,23)=3.669;第页=0.0188,相互作用:F(4,23)=4.203;第页=0.0107)。 4.结论
在骨关节炎中,氧化损伤导致慢性炎症并促进与衰老相关的分泌表型,这是骨关节炎软骨细胞在细胞因子、趋化因子和蛋白酶方面的特征。氧化应激在疾病的发展中起着重要作用,因为在缺氧环境中,一些代谢功能受到限制。
谷胱甘肽参与各种细胞功能,如细胞增殖、凋亡和维持蛋白质巯基的还原状态,从而产生各种细胞内信号级联。但最重要的功能之一是其抗氧化能力,因为它可以直接作用于自由基(ROS)或作为酶辅因子参与。已经确定了谷胱甘肽运输的两种机制。然而,没有证据表明这两个转运蛋白家族中的任何一个都可以将细胞外空间释放的谷胱甘肽重新整合到细胞中,因此如果不合成谷胱甘苷,谷胱甘氨酸最终会耗尽。
考虑到这种细胞局限性,以及导致骨关节炎的细胞事件涉及氧化还原失衡,包括炎症、细胞外基质中蛋白多糖和胶原蛋白的紊乱和功能,我们研究了谷胱甘肽纳米结构系统对手术性骨关节炎大鼠的影响。
总的来说,除了接受Np-Q治疗的组外,没有OA的组软骨形态出现了一些变化,这可能与对侧膝关节的动态代偿引起的机械应力或关节穿刺术引起的炎症有关。
醋酸被用作纳米粒子载体的对照物,是唯一刺激谷胱甘肽和丙二醛增加的治疗方法,这表明可能是由载体的pH值(pH值4.1)引起的刺激。这些影响与可能发生的细胞损伤没有显著相关性,因为与哈特曼溶液中的组织病理学变化相比,在乙酸(研究中的纳米粒子分散在其中的介质)中观察到的组织病理变化相似。
Zheng-Shun-We等人(2013)在pH值为5的醋酸中使用Np-Q,但由于溶液的pH值,没有发现负面影响。虽然我们已经证明,载体可以在pH 4.1下使用,但考虑在生理pH下使用载体是合适的,以避免在生化试验中观察到的可能的负面影响[29]. 研究表明,壳聚糖可以降低MDA浓度,同时提高抗氧化酶的活性。当壳聚糖被纳米颗粒化时,这些影响会提高到更大的程度,这有望控制体内OA的退化过程。然而,我们的研究发现,即使在控制条件下,仅使用壳聚糖纳米粒也会出现更显著的退化变化。
另一方面,已经描述了高剂量壳聚糖及其NP引起的严重炎症反应,这表明本研究中观察到的有害影响可能是由于壳聚糖的浓度高于生物体的耐受水平,导致与MMP-13增加相关的更大炎症过程,引发了组织病理学研究中观察到的关节退化[30,31,32]. 用于OA再生治疗的壳聚糖基移植物已被证明是软骨细胞增殖的理想基质,并且在结构和力学性能上与PG和HA相似。然而,新组织趋向于纤维软骨,TP浓度较低,且机械效率低于天然组织[33,34]. 在这项研究中观察到了类似的效果,其中TP含量较低的关节组织纤维化更明显。 尽管壳聚糖与前列腺素中的氨基葡萄糖聚糖(GAG)具有结构上的相似性,但已证明其可以刺激软骨生成[34],壳聚糖似乎与生长因子相互作用以刺激纤维细胞而非其他细胞[35,36]. 这可以解释为什么尽管细胞的活力增加,但它们的形态与纤维细胞相似[22]. 使用关节内Np-Q时观察到的另外两个作用是增加Col-2的生成和更显著的MMP-13。虽然Pickarski使用ACLT技术从第1周起证明Col-2和MMP-13的生成增加,但在我们的病例中,与使用哈特曼溶液和乙酸处理ACLT的关节相比,在Np-Q刺激下,这两种化合物的存在明显更高[28]. 在骨关节病大鼠中观察到并用我们的NPs治疗的Col 2的特性是刺激稳定合成的结果,再加上壳聚糖与胶原蛋白的强烈相互作用,形成一种分子复合物,可以赋予机械稳定性,反过来,更大的胶原蛋白降解保护稳定性[30,33,34]. 另一方面,Np-GSH在增加Col-2合成方面表现出与Np-Q相同的积极作用。在Np-GSH处理的关节中几乎没有观察到退行性变化,这表明GSH对疾病调节的有益作用和壳聚糖的副作用。总的来说,与Np-Q相比,Np-GSH能够保护软骨细胞免受凋亡,这表现在用这些Np治疗的组中细胞数量减少较少,细胞形态得到更好的保存,ECM得到更好的保护,表明谷胱甘肽有助于这些细胞维持ECM的正确构成。
Np-GSH引起的最明显的变化是软骨下骨内的变化,无论是在X线照片还是组织病理切片中,这些变化与Np-Q观察到的变化相似。与关节表面相比,关节的深层导致我们思考Np-GSH可能无法到达这些层,可能是由于与带负电荷的ECM相互作用的NP带正电荷,因此其治疗效果仅限于表层ECM,无法到达软骨下骨。晚期OA患者软骨下骨中Np-GSH的行为问题出现在这里,软骨的侵蚀暴露了这种结构[22,37]. 与其他研究一样,HA证明其能够调节OA过程而无任何抗炎作用。在接受哈特曼溶液治疗的动物中,观察到的变化没有显著差异。然而,HA最重要的结果是长期的,2周不足以看到OA未治疗关节的差异[38,39,40]. 值得一提的是,在纳米粒子暴露的情况下,评估的效果是亚急性的。为了彻底比较本研究中提出的治疗方法的有效性,我们认为有必要研究软骨的细胞组织以及与纳米矢量化GSH调节氧化应激相关的细胞信号,鉴于单剂量Np-GSH给药后原位观察到的有益变化,表明其能够发挥与细胞增殖、细胞外基质重塑以及与GSH依赖性抗氧化相关的调节相关的生物效应。
作者贡献
概念化,P.R.-N。;方法、P.R.-N.、I.Z.M.和M.E.V。;形式分析、P.R.-N.、I.Z.M.、B.M.G.C.、M.E.V.和R.D.-T。;调查、I.Z.M.、P.R.-N.、B.M.G.C.、M.E.V.和R.D.-T。;书面原稿,P.R.-N。;写作-审查和编辑,R.D.-T。;可视化,R.D.-T。;监管、P.R.-N.、B.M.G.C.和L.D.L.-B。;资金收购,P.R.-N.所有作者均已阅读并同意手稿的出版版本。
资金
这项工作得到了UNAMA-PAPIIT IN214321(墨西哥国立自治大学(UNAMA))的支持;Cuautitlán高级教育学院,UNAM Cátedra de Investigación:CI2225。
机构审查委员会声明
动物研究方案由CICUAE FESC实验动物护理和使用内部委员会批准,该委员会根据《联邦动物健康法》(第三篇,第一章,动物福利)和墨西哥官方标准NOM-062-ZOO-1999创建,用于动物研究。批准编号:FESC/CICUAE/06/03/2018。
数据可用性声明
支持本文报告结果的数据可以在伊利亚娜·泽蒂纳的工作日志中的多学科研究室、库奥蒂特兰高等专科学校、墨西哥国立奥托诺马大学、卡雷特拉·库奥蒂特兰-Teoloyucan Km.2.5、圣塞巴斯蒂安·沙拉、库奥蒂特兰·伊兹卡利、墨西哥埃斯塔多·德梅西科、CP 54714 1中找到。
致谢
本文作者感谢M.C.Crisóforo Mercado对捐赠、维护和最终处置所用实验动物的支持。
工具书类
- S.ánchez Naranjo,J.C。;López Zapata,D.F.Fisiopatologiaía cellular de la osteartitis:El condrocito关节昏迷主角。伊亚特里亚 2011,24, 167–178. [谷歌学者] [交叉参考]
- McIlwraith,C.Enfermedades de las articulaciones,los tendones,los ligamentos y las restructuration as relacionadas.《关节、肌腱、韧带和重建作为放松》。英语:TS Stashak。Claudicación在El Caballo 2004,5, 469–684. [谷歌学者]
- Adarmes,H。;索利斯,J。;米勒,A。;Galleguillos,M.Determinaticón de nitronico to como代谢确定马掌骨关节炎中的唾液酸脱氢酶(delóxido nitrico en elíquido sinovial de articulación)。架构(architecture)。医学兽医。 2009,41, 255–259. [谷歌学者] [交叉参考]
- 达巴,M.M。;德莱昂,C.I.P。;Goldaracena,G.L。;马丁内斯(Martínez),L.P.Situación实际的第二次再保险事故。兽医。墨西哥 2006,37, 369–378. [谷歌学者]
- Polli,M。;北卡罗来纳州卡吉亚诺。;罗兰多,J。;佩罗内,G。;马里诺,M。;De Simone,E。;Barbará,A.C.Variación del nivel de citoquinas en líquido sinovial de equinos con enfermedad con con bisfonatos.《城市新纪元》/双膦酸盐治疗马关节病滑液中细胞因子水平的变化。完成版本。中国。兽医。 2013,7, 69. [谷歌学者] [交叉参考]
- Pineda-Aranda,A.Evaluación morfológica de células pluripotenciales messiquimales de equino en un polímero生物可降解。2011年,墨西哥墨西哥城墨西哥国立自治大学硕士论文。[谷歌学者]
- 弗里斯比,D.D。;考萨克,C.E。;McIlwraith,C.W。;Werpy,N.M.关节内注射多硫酸氨基多糖或透明质酸钠治疗马实验性骨关节炎的评估。美国兽医协会。物件。 2009,70, 203–209. [谷歌学者] [交叉参考]
- Dorta,L.F.Glucosamina和sulfato de condroitina en el tratamino de la骨性关节炎。CENIC版本。中国。生物科学 2016,47, 93–99. [谷歌学者]
- Ngo,D.-H。;Vo、T.-S。;恩戈,D.-N。;Kang,K.-H。;Je,J.-Y。;Pham,H.N.-D。;Byun,H.-G。;Kim,S.-K.壳聚糖及其衍生物的生物效应。食品Hydrocoll。 2015,51,200–216。[谷歌学者] [交叉参考]
- 雷布林,I。;Sohal,R.S.,老化过程中谷胱甘肽氧化还原状态的Pro-oxidant转变。高级药物递送。版次。 2008,60, 1545–1552. [谷歌学者] [交叉参考]
- 桑多瓦尔,J。;洛佩兹,C。;Carmona,J.Terapias con potential resentivo关节再生。架构(architecture)。医学兽医。 2013,45, 229–236. [谷歌学者] [交叉参考]
- 库伊努,E.L。;Narayanan,G。;奈尔,L.S。;Laurencin,C.T.骨关节炎动物模型:分类、更新和结果测量。《矫形外科杂志》。外科研究。 2016,11, 19. [谷歌学者] [交叉参考]
- López-Barrera,L。;Díaz-Torres,R。;Macay,A.L。;López-Reyes,A。;Olmos,S.P.公司。;Ramírez-Noguera,P.软骨细胞中壳聚糖-谷氨酸硫纳米粒诱导的氧化应激调节。Die Pharm.-国际药学杂志。 2019,74, 406–411. [谷歌学者]
- Hayami,T。;Pickarski,M。;韦索洛夫斯基,G.A。;麦克莱恩,J。;骨,A。;德斯特法诺,J。;罗丹,G.A。;Duong,L.T.软骨下骨重塑在骨关节炎中的作用:阿仑膦酸钠在大鼠前交叉韧带横断模型中减少软骨变性和防止骨赘形成。大黄性关节炎。美国海军退役。风湿病。 2004,50, 1193–1206. [谷歌学者] [交叉参考] [公共医学]
- Teeple,E。;杰伊,G.D。;Elsaid,K.A。;Fleming,B.C.骨关节炎动物模型:模型选择和分析的挑战。AAPS J。 2013,15, 438–446. [谷歌学者] [交叉参考] [公共医学]
- 拉赫曼,I。;柯德,A。;Biswas,S.K.使用酶循环法定量测定谷胱甘肽和谷胱甘苷二硫化物水平的分析。《国家协议》。 2006,1, 3159–3165. [谷歌学者] [交叉参考]
- Ohkawa,H。;Ohishi,N。;Yagi,K.通过硫代巴比妥酸反应测定动物组织中的脂质过氧化物。分析。生物化学。 1979,95,351–358。[谷歌学者] [交叉参考] [公共医学]
- 普里茨克,K.P。;盖伊,S。;希梅内兹,S。;Ostergaard,K。;Pelletier,J.-P。;Revell,P。;Salter,D。;Van den Berg,W.骨关节炎软骨组织病理学:分级和分期。Osteoarther公司。卡特尔。 2006,14, 13–29. [谷歌学者] [交叉参考]
- Mainil-Varlet,P。;艾格纳,T。;Brittberg,M。;布洛,P。;Hollander,A。;Hunziker,E。;坎德尔,R。;Nehrer,S。;普里茨克,K。;Roberts,S.软骨修复的组织学评估:国际软骨修复学会组织学终点委员会的报告。JBJS公司 2003,85(补充S2),45–57。[谷歌学者] [交叉参考]
- Kamekura,S。;Hoshi,K。;Shimoaka,T。;美国钟市。;Chikuda,H。;山田,T。;内田,M。;绪方,N。;Seichi,A。;Nakamura,K.在膝关节不稳定诱导的新型实验小鼠模型中发生骨关节炎。Osteoarther公司。卡特尔。 2005,13, 632–641. [谷歌学者] [交叉参考]
- 昆特罗,M。;蒙福特,J。;Mitrovic,D.Osteoartosis:Biología,clínica和tratamiento。在骨关节病:Biologia、Fosopatologia、Clínica和Tratamiento; 《泛美医学杂志》编辑:西班牙马德里,2010年;第237-242页。国际标准图书编号978-84-9835-267-2。[谷歌学者]
- 南卡罗来纳州朱内加。;文图拉,M。;杰伊,G.D。;Veillette,C.大鼠内侧半月板切除术的一种微创方法:针对早期或轻度人类骨关节炎的模型。J.关节炎 2016,5, 193. [谷歌学者] [交叉参考]
- Kellgren,J.H。;Lawrence,J.骨关节放射评估。大黄年鉴。数字化信息系统。 1957,16, 494. [谷歌学者] [交叉参考] [公共医学]
- Vyas,S。;Sharma,H。;维亚斯,R。;Chawla,K。;Jaipal,M.骨关节炎患者血清中的氧化应激和抗氧化水平。印度科学杂志。物件。 2015,6, 37–40. [谷歌学者]
- Bai,B。;Li,Y.丹参通过抗氧化作用预防骨关节炎兔关节软骨退化。Osteoarther公司。卡特尔。 2016,24,514–520。[谷歌学者] [交叉参考] [公共医学]
- 奥斯塔洛夫斯卡,A。;伯克纳,E。;Wiecha,M。;Kasperzyk,S。;Kasperzyk,A。;Kapolka博士。;Zon-Giebel,A.膝关节原发性和继发性骨关节炎患者滑液中的脂质过氧化和抗氧化酶。Osteoarther公司。卡特尔。 2006,14, 139–145. [谷歌学者] [交叉参考] [公共医学]
- Plemel,J.R。;卡普拉里奥(Capariello),A.V。;医学学士基奥。;T.J.亨利。;Tsutsui,S。;楚,T.H。;申克,G.J。;Klaver,R。;Yong,V.W。;Stys,P.K.核酸染料吖啶橙的独特光谱特征可以通过细胞凋亡和坏死来区分细胞死亡。《细胞生物学杂志》。 2017,216, 1163–1181. [谷歌学者] [交叉参考]
- Pickarski,M。;Hayami,T。;Zhuo,Y。;Duong,L.T.大鼠前交叉韧带横断和半月板切除骨关节炎模型中关节软骨和软骨下骨的分子变化。BMC肌肉骨骼。迪索德。 2011,12, 197. [谷歌学者] [交叉参考]
- 温,Z.-S。;刘立杰。;Qu,Y.-L。;欧阳,X.-K。;Yang,L.-Y。;Xu,Z.-R.壳聚糖纳米粒减轻小鼠巨噬细胞RAW264中过氧化氢诱导的应激损伤。7个单元格。3月药物 2013,11, 3582–3600. [谷歌学者] [交叉参考]
- Kojima,K。;冈本,Y。;Kojima,K。;Miyatake,K。;富士,H。;Shigemasa,Y。;Minami,S.几丁质和壳聚糖对伤口愈合中胶原蛋白合成的影响。J.兽医。医学科学。 2004,66, 1595–1598. [谷歌学者] [交叉参考]
- 卢,H.-D。;赵,H.-Q。;王凯。;Lv,L.-L.新型透明质酸-壳聚糖纳米粒作为靶向骨关节炎的非病毒基因载体。国际药学杂志。 2011,420, 358–365. [谷歌学者] [交叉参考]
- Kang,M.L。;Ko,J.-Y。;Kim,J.E。;Im,G.-I.软骨再生用核蛋白结合壳聚糖纳米/微粒的关节内递送。生物材料 2014,35, 9984–9994. [谷歌学者] [交叉参考]
- 郝,T。;温,N。;曹建凯。;王,H.-B。;吕,S.-H。;刘,T。;林庆霞。;段,C.-M。;Wang,C.-Y.壳聚糖水凝胶支持基质积累并促进羊关节软骨缺损的体内修复。Osteoarther公司。卡特尔。 2010,18, 257–265. [谷歌学者] [交叉参考]
- Yan,L.P。;Wang,Y.J。;任,L。;Wu,G。;Caridade,S.G。;范,J.B。;Wang,L.Y。;Ji,P.H。;Oliveira,J.M。;Oliveira,J.T.Genipin交联胶原/壳聚糖仿生支架在关节软骨组织工程中的应用。J.生物识别。马特。决议A部分 2010,95, 465–475. [谷歌学者] [交叉参考]
- Enrione,J。;奥索里奥,F。;洛佩兹,D。;Weinstein-Openheimer,C。;Fuentes,文学硕士。;Ceriani,R。;D.I.布朗。;阿尔博诺兹,F。;Sánchez,E。;Villalobos,P.明胶/壳聚糖/透明质酸支架聚合物的表征。电子。生物技术杂志。 2010,13, 20–21. [谷歌学者] [交叉参考]
- 嚎叫,G.I。;Dettmar,P.W。;Goddard,P.A。;F.C.汉普森。;多尼什,M。;Wood,E.J.几丁质和壳聚糖对体外人类皮肤成纤维细胞和角质形成细胞增殖的影响。生物材料 2001,22, 2959–2966. [谷歌学者] [交叉参考] [公共医学]
- 佩雷拉,P。;卡瓦略,V。;拉莫斯,R。;用于生物医学应用的Gama,M.壳聚糖纳米粒子。壳聚糖制造道具。用法 2011,16, 321. [谷歌学者]
- 艾汉,E。;Kesmezacar,H。;Akgun,I.膝关节骨性关节炎的关节内注射(皮质类固醇、透明质酸、富含血小板的血浆)。世界J.Orthop。 2014,5, 351. [谷歌学者] [交叉参考] [公共医学]
- 柳泽,K。;Muneta,T。;Ozeki,N。;Y.中川。;乌多,M。;Saito,R。;Koga,H。;Tsuji,K。;Sekiya,I.每周注射Hylan GF 20延缓部分半月板切除大鼠膝关节的软骨退化。BMC肌肉骨骼。迪索德。 2016,17, 188. [谷歌学者] [交叉参考] [公共医学]
- 理学硕士Rezende。;A.J.埃尔南德斯。;Oliveira,C.R.G.C.M。;Bolliger Neto,R.通过大鼠内侧半月板切除术建立实验性骨关节炎模型,以及双醋酯和透明质酸注射的影响。圣保罗医学杂志。 2014,133, 4–12. [谷歌学者] [交叉参考]
图1。不同纳米粒子的尺寸分布(图中的比例为×10−10): (A类)Np-GSH灭菌前。(B)Np-GSH暴露于紫外线下14小时(C)Np-Q在紫外线杀菌前。(D类)Np-Q在紫外线照射14小时后。
图1。不同纳米粒子的尺寸分布(图中的比例为×10−10): (A类)Np-GSH灭菌前。(B)Np-GSH暴露于紫外线下14小时(C)紫外线灭菌前的Np-Q。(D类)Np-Q在紫外线照射14小时后。
图3。ACLT期间膝盖的照片。(A类)在背景中观察到颅十字韧带仍然完好(B)在横切之后。
图3。ACLT期间膝盖的照片。(A类)在背景中观察到颅十字韧带仍然完好(B)在横切之后。
图4。显示术后14天大鼠的放射图像(内侧和前后)。右骨盆肢体控制和左ACLT。(A类,B)用哈特曼溶液治疗大鼠。(C,D类)Np-GSH治疗大鼠。箭头显示了每种情况下的横断面位置。
图4。显示术后14天大鼠的放射图像(内侧和前后)。右骨盆肢体控制和左ACLT。(A类,B)用哈特曼溶液处理的大鼠。(C,D类)Np-GSH治疗大鼠。箭头显示了每种情况下的横断面位置。
图5。根据Kellgren和Lawrence量表分析不同治疗引起的损伤(ANOVA;F(9,80)79.19;第页≤0.001)。
图5。根据Kellgren和Lawrence量表分析不同治疗引起的损伤(ANOVA;F(9,80)79.19;第页≤ 0.001).
图6。术后14天大鼠软骨和半月板中的谷胱甘肽浓度和纳米粒子暴露。GSH浓度的平均值±SEM如图所示。相同字母的横线没有显著差异(方差分析;F(9,24)=15.11;第页< 0.0001).
图6。术后14天大鼠软骨和半月板中的谷胱甘肽浓度和纳米粒子暴露。显示了GSH浓度的平均值±SEM。相同字母的横线没有显著差异(方差分析;F(9,24)=15.11;第页< 0.0001).
图7。术后14天大鼠软骨和半月板中的MDA浓度和纳米粒子暴露。显示了MDA浓度的平均值±SEM。相同字母的横线没有显著差异(ANOVA;F(9,26)=5.623;第页< 0.0003).
图7。术后14天大鼠软骨和半月板中的MDA浓度和纳米粒子暴露。显示了MDA浓度的平均值±SEM。相同字母的横线没有显著差异(ANOVA;F(9,26)=5.623;第页< 0.0003).
图8。使用HE和van Gieson染色对治疗的大鼠膝盖(20×)进行组织病理学分析。所示字母表示对实验动物进行的每种治疗,如下所示:哈特曼溶液(A类——D类),乙酸(E类——H(H)),编号-Q(我——L(左)),Np-谷胱甘肽(M(M)——P(P))和透明质酸(问——T型).
图8。使用HE和van Gieson染色对治疗的大鼠膝盖(20×)进行组织病理学分析。所示字母表示对实验动物进行的每种治疗,如下所示:哈特曼溶液(A类——D类),乙酸(E类——H(H)),Np-Q(我——L(左)),Np-谷胱甘肽(M(M)——P(P))和透明质酸(问——T型).
图9。不同处理方法对形态特征的影响,采用改良的Mankin评分法以任意单位(a.u.)进行评估(细胞软骨分布(A类),细胞形态学(B),蜂窝人口(C),潮汐标志(D类)和软骨下骨(E类)). 相同字母的横线无显著差异(ANOVA;处理因子:F(4,30)=13.52;第页<0.0001,相互作用:F(4,30)=1.191;第页= 0.3348).
图9。不同处理方法对形态特征的影响,使用改良的Mankin评分(以任意单位表示)进行评估(细胞软骨分布(A类),细胞形态学(B),细胞群体(C),潮汐标志(D类)和软骨下骨(E类)). 相同字母的横线无显著差异(ANOVA;处理因子:F(4,30)=13.52;第页<0.0001,相互作用:F(4,30)=1.191;第页= 0.3348).
图10。不同处理对软骨(表面)形态特征的影响(A类)、MEC(B),PG损失(C),第2列(D类)和MMP-13(E类)). 根据观察到的信号,采用任意单位(a.u.)进行间接免疫染色分析,0:无信号,1:弱信号,2:中等信号,3:标记信号,大于3:大于标记信号。相同字母的横线无显著差异(ANOVA;疾病因素:F(1,29)=9.594;第页=0.0043,处理因子:F(4,29)=84.61;第页<0.0001,相互作用:F(4,29)=5.125;第页= 0.003).
图10。不同处理对软骨(表面)形态特征的影响(A类)、MEC(B),PG损失(C),第2列(D类)和MMP-13(E类)). 根据如下观察到的信号,使用任意单位(a.u.)通过间接免疫染色进行分析,0:无信号,1:弱信号,2:中等信号,3:标记信号,大于3:比标记信号大。相同字母的横线无显著差异(ANOVA;疾病因素:F(1,29)=9.594;第页=0.0043,处理因子:F(4,29)=84.61;第页<0.0001,相互作用:F(4,29)=5.125;第页= 0.003).
图11。膝关节组织学(10×),吖啶橙染色不同处理对照(A类——E类)和ACLT(F类——J型):哈特曼溶液(A类,F类),乙酸(B,G公司),编号-Q(C,H(H)),Np-谷胱甘肽(D类,我)和透明质酸(E类,J型).
图11。膝关节组织学(10×),吖啶橙染色不同处理对照(A类——E类)和ACLT(F类——J型):哈特曼溶液(A类,F类),乙酸(B,G公司),编号-Q(C,H(H)),Np-谷胱甘肽(D类,我)和透明质酸(E类,J型).
图12。不同处理的膝盖组织病理学(10×)、甲苯胺蓝和藏红O染色:哈特曼溶液(A类——D类),乙酸(E类——H(H)),编号-Q(我——L(左)),Np-谷胱甘肽(M(M)——P(P))和透明质酸(问——T型).
图12。不同处理的膝盖组织病理学(10×)、甲苯胺蓝和藏红O染色:哈特曼溶液(A类——D类),乙酸(E类——H(H)),编号-Q(我——L(左)),Np-谷胱甘肽(M(M)——P(P))和透明质酸(问——T型).
图13。Hartmann溶液不同处理的膝关节2A1胶原(10×)和金属蛋白酶-13(20×)免疫染色显微图(A类——D类),乙酸(E类——H(H)),编号-Q(我——L(左)),Np谷胱甘肽(M(M)——P(P))和透明质酸(问——T型).
图13。Hartmann溶液不同处理的膝关节2A1胶原(10×)和金属蛋白酶-13(20×)免疫染色显微图(A类——D类),乙酸(E类——H(H)),编号-Q(我——L(左)),Np-谷胱甘肽(M(M)——P(P))和透明质酸(问——T型).
表1。每个实验组的治疗。
| 组 | 治疗 |
|---|
| 1 | 哈特曼解决方案(比萨®) |
| 2 | 1%乙酸pH 4.1(纳米粒子介质) |
| 三 | 壳聚糖纳米粒子(Np-Q) |
| 4 | 壳聚糖/谷胱甘肽纳米粒子(Np-GSH) |
| 5 | 透明质酸(图例®) |
表2。纳米颗粒在紫外线灭菌前后的平均尺寸、PDI和ζ电位。图中显示了不同阶段的NPs/mL浓度。
表2。纳米粒子在紫外线杀菌前后的平均尺寸、PDI和zeta电位。图中显示了不同阶段的NPs/mL浓度。
| | 壳聚糖-谷胱甘肽纳米粒子 | 壳聚糖纳米粒子 |
|---|
| | 预UV | UV后 | 预UV | UV后 |
| 平均值(nm) | 354.3 | 253.3 | 330 | 292.1 |
| 交车前检查 | 0.306 | 0.444 | 0.313 | 0.346 |
| 纳米粒子/mL | 3.34 × 1010 | 5.51 × 1010 | 1.49 × 1010 | 3.15×1010 |
| Zeta电位(mV) | | 24.8 | | 32.6 |
| 免责声明/出版商注释:所有出版物中包含的声明、意见和数据仅为个人作者和贡献者的声明、观点和数据,而非MDPI和/或编辑的声明、看法和数据。MDPI和/或编辑对内容中提及的任何想法、方法、说明或产品造成的任何人员或财产伤害不承担任何责任。 |