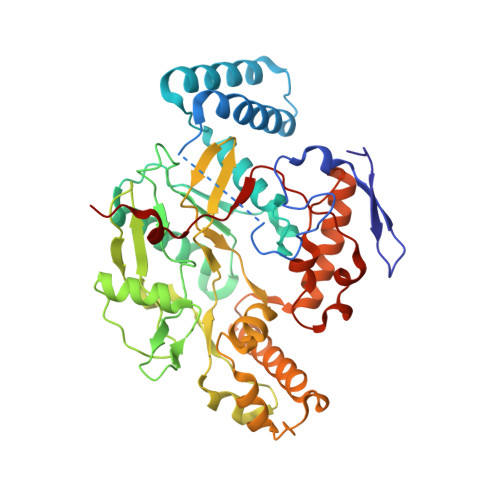
亲水性、强效和选择性7-取代2-氨基喹啉类作为改进的人类神经一氧化氮合酶抑制剂。
公共医学 : 28776992 内政部: https://doi.org/10.1021/cs.jmedchem.7b00835 相关结构的主要引文: 5伏用户界面 , 5伏UJ , 5VUK(英国) , 5伏UL , 5伏 , 5伏联合国 , 5伏单位 , 5V以上 , 5伏UQ , 5伏 , 5伏美国 , 5伏UT , 5VUU(电压单位) , 5伏紫外线 , 5伏超高压 , 5伏用户体验 , 5伏 , 5伏UZ , 5伏VV0 , 5VV1型 , 5VV2型 , 5伏VV3 , 5伏VV4 , 5VV5型 , 5VV6型 , 5个版本7 , 5VV8型 , 5VV9型 , 5瓦 , 5伏真空断路器 , 5伏交流 , 5VVD型 , 5VVG汽车 , 5VVN(五VVN) PubMed摘要: 神经一氧化氮合酶(nNOS)是抗神经退行性疾病药物开发的靶点。 大多数nNOS抑制剂模仿左旋精氨酸,生物利用度低。 2-氨基喹啉类药物有望成为生物可利用的nNOS抑制剂,但其对人类nNOS的抑制作用较低,对人类eNOS的选择性较低,并且与其他CNS靶点有显著结合。 我们旨在通过(a)截短原始支架或(b)引入亲水基团来中断亲脂性、混杂的药效团并促进与人nNOS特异性His342的相互作用,从而提高人nNOS的效力和选择性,并减少脱靶结合。 我们合成了截短的和极性的2-氨基喹啉衍生物,并对其与重组NOS酶进行了比较。 尽管苯胺和吡啶衍生物与His342相互作用,但苯腈对大鼠和人类nNOS的抑制效果最好。 氰基旁疏水取代基的引入和氨基喹啉甲基化都大大提高了亚型选择性。 最重要的是,这些修饰保持了Caco-2的渗透性,并减少了非靶向CNS结合。