概述
-
产品名称 PerCP/Cy5.5®共轭套件-Lightning-Link® -
产品概述 按照CP/Cy5.5 ® 共轭试剂盒/PerCP/Cy5.5 ® 标签试剂盒ab102911使用一种简单快速的方法对抗体进行PerCP/Cy5.5标记/结合。 它还可以用于偶联其他蛋白质或肽。 了解我们的 抗体标记试剂盒及其优点 .
将抗体与PerCP/Cy5.5结合 ® 使用此套件: -在抗体中添加修饰剂并孵育3小时 -添加淬火剂并孵育30分钟 PerCP/Cy5.5 ® 结合抗体可立即用于WB、ELISA、IHC等。无需进一步纯化,抗体可100%回收使用。
了解以下缓冲区兼容性; 对于不相容的缓冲液和低抗体浓度,请使用我们的快速 抗体纯化和浓缩试剂盒 .使用 常见问题解答 了解更多关于该技术的信息,或关于将其他蛋白质和肽与PerCP/Cy5.5结合的信息 ® .
可根据需要提供高达100 mg的定制尺寸共轭试剂盒。 请联系我们讨论您的要求。 -
笔记 该产品由Abcam公司Expedeon制造,之前称为Lightning-Link ® PerCP/Cy5.5标签套件。 763-0015与1 mg大小相同。 763-0010与3 x 100 ug尺寸相同。 763-0030与3 x 10 ug尺寸相同。 763-0005与100µg粒径相同。 与PerCP/Cy5.5结合的抗体的量和体积 ® 套件尺寸 建议的最大值 抗体量 最大抗体 体积 1 3 x 10微克 3 x 10微克 3 x 10微升 100微克 1 x 100微克 1 x 100微升 3 x 100微克 3 x 100微克 3 x 100微升 1毫克 1 x 1毫克 1 x 1毫升 1 理想的抗体浓度为1mg/ml。如果不超过最大抗体体积,可以使用0.5-1 mg/ml。 抗体>1 mg/ml或<0.5 mg/ml应稀释/浓缩。 共轭缓冲要求 缓冲液的pH值应为6.5-8.5。 兼容的缓冲成分 如果显示浓度,则成分应不超过显示的浓度。 如果几个成分接近可接受浓度的极限,那么这可能会抑制共轭。 50mM/0.6%Tris 1 0.1%牛血清白蛋白 50%甘油 0.1%叠氮化钠 美国公共广播电视公司 磷酸钾 氯化钠 HEPES公司 蔗糖 柠檬酸钠 乙二胺四乙酸 海藻糖 1 Tris缓冲盐水几乎总是≤50 mM/0.6% 不兼容的缓冲成分 硫柳汞 普鲁克林 甘氨酸 精氨酸 谷胱甘肽 DTT公司 如果含有您的抗体或蛋白质的缓冲液成分没有列在上面,请检查 常见问题解答 或 联系我们 . 只有纯化的抗体才适合使用,即在不存在其他蛋白质、肽或氨基酸的情况下:腹水、血清或杂交瘤培养物中的抗体。 储存和处理共轭试剂盒 冻干发光油墨 ® 组件具有吸湿性。 试剂盒特意在室温下与硅胶一起装运,以避免接触湿气。 收到后,将试剂盒冷冻保存并防潮。 在打开外容器之前,让冻干组件达到室温,以尽量减少冷凝。
相关产品
-
相关产品
图像
-

流式细胞术-PerCP/Cy5.5共轭试剂盒Lightning-Link(ab102911) Okagawa、Tomohiro等人的图像,Front Immunol。, 8:650,doi:10.3389/fimmu.2017.00650。 根据Creative Commons许可证复制 https://creativecommons.org/licenses/by/4.0/ Okagawa、Tomohiro等人使用了PerCP/Cy5.5 ® 共轭套件-照明链路 ® (ab102911),作为研究Boch5D2对牛白血病病毒(BLV)特异性T细胞增殖影响的一部分。 他们使用试剂盒结合PerCP/Cy5.5 ® 抗CD8抗体,克隆CC63,用于流式细胞术。 针对BLV抗原刺激的T细胞增殖。 将经羧荧光素二醋酸盐琥珀酰酯(CFSE)标记的外周血单个核细胞与胎羔肾(FLK)-BLV抗原、对照FLK抗原(A)或gp51肽(0.1和1µg/ml)(B)共培养3次,共培养6天。 用流式细胞术测定CD4+和CD8+γδTCR−T细胞中CFSElow细胞的百分比。 CFSElow细胞代表培养过程中增殖的细胞。 每个点代表三个独立实验的平均值。 通过Dunnett的多个时间点的多重比较测试确定了显著差异。*,#,† 每次刺激P<0.05 vs 0 dpi。 -

流式细胞术-PerCP/Cy5.5结合试剂盒-Lightning-Link 来自Okagawa、Tomohiro等人的图像,兽医研究,49(1):50,doi:10.1186/s13567-018-0543-9。 根据Creative Commons许可证复制 https://creativecommons.org/licenses/by/4.0/ Okagawa、Tomohiro等人使用了PerCP/Cy5.5 ® 共轭套件-照明链路 ® (ab102911)作为检测PD-1和LAG-3表达的一部分。 他们用试剂盒偶联了PerCP/Cy5.5 ® 单克隆抗CD3抗体,克隆MM1A,用于流式细胞术。 BLV感染牛CD4+T细胞PD-1和LAG-3的表达。 BLV感染牛(AL和EBL)外周血IgM−CD3+CD4+γδTCR−T细胞PD-1和LAG-3表达分析的门控策略和代表性点图。 象限中的值表示单元格的百分比。 未感染BLV(BLV)的CD3+CD4+T细胞群中PD-1+LAG-3+CD4+T细胞(B)、PD-1+LA G-3−CD4+T细胞(C)和PD-1−LAG-3+CD4+T-细胞(D)的百分比 − ; n个 = 15) ,铝(n = 22),PL(n = 11) 和EBL牛(n = 7). 横线表示组中值百分比。 使用Kruskal–Wallis检验确定各组之间的显著差异,其中P < 0.05和P < 0.001,用星号表示(分别为*和***)。 -
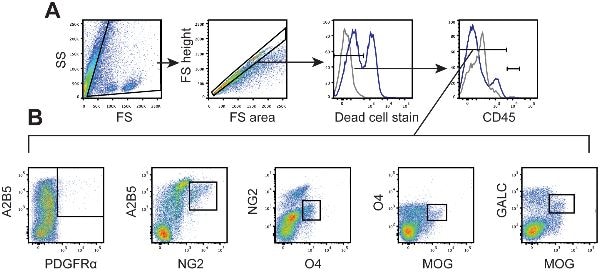
流式细胞术-PerCP/Cy5.5结合试剂盒-Lightning-Link 图片来自Robinson,Andrew P.等人,PloS one,9(9):e107649。 doi:10.1371/journal.pone.0107649。 根据Creative Commons许可证复制 https://creativecommons.org/licenses/by/4.0/ Robinson、Andrew P.等人使用了PerCP/Cy5.5 ® 共轭套件-照明链路 ® (ab102911)作为寡突胶质种群特征的一部分。 他们使用试剂盒结合PerCP/Cy5.5 ® 涉及用于流式细胞术的小鼠单克隆抗NG2抗体。 用PLP139–151免疫SJL/J小鼠,并每天对临床疾病进行评分。 处死一组SJL/J小鼠,并通过流式细胞术分析脊髓(n = 5). (A) 通过正向和侧向散射将细胞与碎片区分开来,然后将单个细胞选通。 活细胞通过死亡细胞排除进行门控,CNS驻留细胞被鉴定为CD45-或CD45low。 (B) 寡突胶质细胞通过双重阳性染色定义为:A2B5+PDGFRα+早期OPCs、A2B5+NG2+中间OPCs,NG2+O4+晚期OPCs和O4+MOG+髓鞘形成前少突胶质细胞,以及GALC+MOG+成熟少突细胞。 -
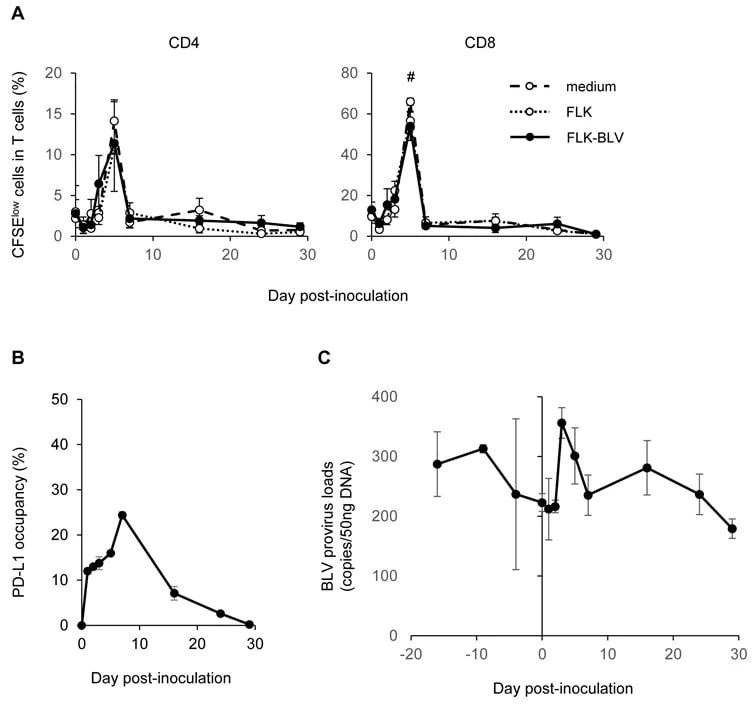
流式细胞术-PE/Cy7®结合试剂盒-Lightning-Link®(ab102911) 图片来自Nishimori,Asami等人,《公共科学图书馆·综合》第12卷,第4期,第0174916页。 2017年4月26日,doi:10.1371/journal.pone.0174916。 根据Creative Commons许可证复制 https://creativecommons.org/licenses/by/4.0/ Nishimori、Asami等人使用了PerCP/Cy5.5 ® 共轭套件-照明链路 ® (ab102911)作为检查牛白血病病毒感染的一部分。 他们使用试剂盒结合PerCP/Cy5.5 ® 抗牛CD8抗体,用于流式细胞术。 将530 mg(1 mg/kg)纯化的4G12静脉接种给一头感染BLV的奶牛(#368,荷斯坦,雌性,538 kg,31个月龄)。 (A) CD4+和CD8+T细胞对BLV抗原的增殖。 从接种4G12的奶牛中分离出的外周血单个核细胞(PBMC)用羧基荧光素二乙酸丁二酰亚胺酯(CFSE)标记,并在无刺激(培养基)或FLK或FLK-BLV细胞上清液培养6天。 培养后立即用流式细胞仪分析T细胞的增殖情况。 P值小于0.05被认为具有统计学意义。#, P<0.05(FLK-BLV,与第0天相比;单因素方差分析,然后进行Dunnett检验)。 (B) 通过4G12与牛PD-L1结合计算循环IgM+B细胞PD-L1占有率的变化。 占有率估计为体内PD-L1结合在总可用结合位点发生的百分比。 (C) 接种4G12的奶牛体内BLV前病毒载量的变化; y轴表示PBMC 50-ng DNA提取物中包含的BLV拷贝数。 数据是至少三个重复实验的平均值±SEM。 -
本图演示了一个通用程序,并将根据所用共轭物略有不同。 -

PerCP/Cy5.5®结合试剂盒-Lightning-Link®标记流式细胞术用抗犬CD4抗体 来自Maekawa N等人的图像,科学代表,7(1):8951。 图2。; doi:10.1038/s41598-017-09444-2。 根据Creative Commons许可证复制 https://creativecommons.org/licenses/by/4.0/ Maekawa N等人使用ab102911作为检测靶向PD-L1的犬嵌合单克隆抗体的一部分。 他们使用试剂盒结合PerCP/Cy5.5 ® 抗犬CD4抗体用于流式细胞术。 为了评估细胞增殖,在第2天将核苷酸类似物5-乙炔基-2′-脱氧尿苷(EdU)添加到培养基中,并在孵育2天后收集细胞 h.通过前向散射和侧向散射对淋巴细胞群进行门控,并用流式细胞仪测量EdU在(c)CD4+细胞中的掺入。 采用Wilcoxon符号秩和检验进行统计分析。
数据表和文件
-
SDS下载 -
数据表下载
工具书类 (28)
Sajiki Y公司 等人。 TLR7激动剂激活牛Th1反应并对牛白血病病毒发挥抗病毒活性。 Dev Comp Immunol公司 114:103847(2021)。 公共医学:32888966 Sajiki Y公司 等人。 蜱唾液诱导的程序性死亡-1和PD-ligand 1及其相关宿主免疫抑制。 科学代表 11:1063 (2021). 公共医学:33441793 Gamradt S公司 等人。 抑郁症患者T细胞线粒体呼吸减少。 i科学 24:103312 (2021). 公共医学:34765928 瓦苏提凡S 等人。 三阴性乳腺癌中药物诱导的耐药性和表型转换可通过个体化信号特征的分辨和靶向控制。 癌症(巴塞尔) 13:不适用(2021年)。 流动周期 . 公共医学:34638492 转到S 等人。 前列腺素E2上调PD-L1表达并增强IFN-? 用抗PD-L1抗体结合COX-2抑制剂治疗牛支原体感染。 Front Vet科学 7:12(2020年)。 公共医学:32154274





