癌细胞如何相互拖拽决定了它们能否迁移到身体的其他部位。
摘自《华尔街日报》:APL生物工程
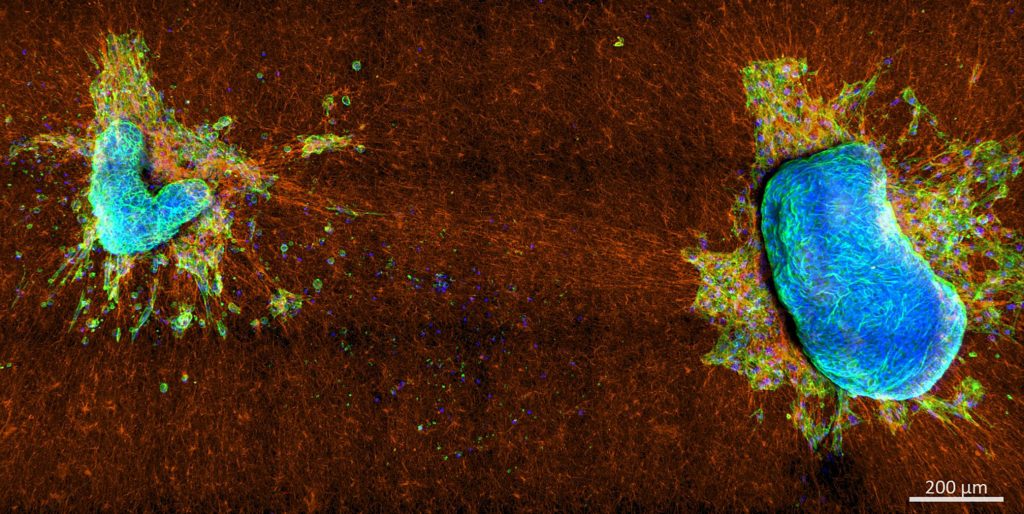 胶原网络上的两个恶性混合苗勒氏肿瘤移植体。两个肿瘤块都粘附在胶原网络上,并开始拉扯胶原纤维,导致大量胶原移位和排列,以及具有主要应力纤维收缩性的细胞逃逸。这两部分尖锐光滑的边界结构进一步表明,强大的组织表面张力阻碍了具有主要皮层收缩力的细胞逃逸。信贷:斯特芬·格罗瑟、弗兰克·索尔和埃利亚娜·布劳特
胶原网络上的两个恶性混合苗勒氏肿瘤移植体。两个肿瘤块都粘附在胶原网络上,并开始拉扯胶原纤维,导致大量胶原移位和排列,以及具有主要应力纤维收缩性的细胞逃逸。这两部分尖锐光滑的边界结构进一步表明,强大的组织表面张力阻碍了具有主要皮层收缩力的细胞逃逸。信贷:斯特芬·格罗瑟、弗兰克·索尔和埃利亚娜·布劳特
华盛顿,2024年5月7日——了解癌细胞如何从原发肿瘤扩散对于许多原因都很重要,包括确定疾病本身的侵袭性。细胞进入邻近组织的细胞外基质(ECM)是癌症进展的关键步骤,与转移的发生直接相关。
在AIP Publishing出版的APL Bioengineering中,来自德国和西班牙的一组研究人员使用乳腺癌细胞系面板和来自乳腺癌和宫颈癌患者的原代肿瘤外植体来检测两种不同的细胞收缩模式:一种产生集体组织表面张力,保持细胞团紧密;另一种,更具方向性和收缩性,使细胞能够将自己拉入ECM。
作者Eliane Blauth说:“我们关注两个参数,即细胞拉动ECM纤维并产生牵引力的能力,以及细胞相互拉动从而产生高组织表面张力的能力。”。“我们将每种特性与不同的收缩机制联系起来,并询问它们如何与癌细胞逃逸和肿瘤侵袭性联系起来。”
该团队发现,更具攻击性的细胞对ECM的拉动比对自身的拉动更强,而非侵入性的细胞对自身的拉动比对ECM的拉动更强,并且不同的拉动行为归因于细胞内肌动蛋白细胞骨架的不同结构。侵袭性细胞主要使用肌动蛋白应力纤维(跨越细胞的厚肌动蛋白束)对周围环境产生作用力,而非侵袭性细胞则通过肌动蛋白皮层产生作用力,肌动蛋白皮质是细胞膜下的一个薄网络。
研究表明,决定细胞逃逸潜能的不是这些收缩模式的总体大小,而是它们之间的相互作用。仅对中等侵袭性细胞进行的实验表明,这些细胞在ECM纤维上产生的总作用力与非侵袭性细胞相当,但它们仍然可以分离和侵袭ECM,而这对非侵入性细胞来说是不可能的。
Blauth说:“非侵袭性细胞仍具有较高的皮层收缩力,使它们保持在一起,而中等侵袭性细胞的皮层收缩能力几乎消失。”。“因此,即使它们对ECM光纤的拉力要弱得多,也不会有太大阻碍。”
该团队对患者衍生的活体肿瘤移植体的测量结果证实了他们在细胞系实验中的发现。在肿瘤进展过程中,具有高皮质收缩力的细胞数量减少。
“这进一步表明,随着肿瘤的生长,细胞相互拉动并聚集在一起的能力减弱,可能增加转移风险。”
###
有关详细信息:
温迪·贝蒂
media@aip.org
301-209-3090
文章标题
不同的收缩模式控制细胞从多细胞球体和肿瘤外植体中逃逸
作者
Eliane Blauth、Steffen Grosser、Frank Sauer、Mario Merkel、Hans Kubitschke、Enrico Warmt、Erik W.Morawetz、Philip Friedrich、Benjamin Wolf、Susanne Briest、Grit Gesine Ruth Hiller、Lars-Christian Horn、Bahriye Aktas和Josef A.Käs
第一作者单位
莱比锡大学和巴塞罗那科学技术研究所

