摘要 肿瘤细胞需要持续供应大分子前体,中断这种供应被认为是癌症的一种治疗策略。 脂质、核酸和蛋白质的前体在三羧酸(TCA)循环中生成,并从线粒体中去除,以参与生物合成反应。 因此,补充前体分子池(回补)对维持细胞生长至关重要。 许多肿瘤细胞使用谷氨酰胺来补充营养。 在这里,我们研究了“谷氨酰胺成瘾”细胞对谷氨酰胺代谢中断的反应。 谷氨酰胺酶(GLS)沉默可催化谷氨酰胺依赖性无补体的第一步,抑制但不能消除培养和体内胶质母细胞瘤细胞的生长。 通过分析GLS抑制细胞的代谢通量,揭示了丙酮酸羧化酶(PC)催化的补偿性补偿性机制的诱导,使细胞能够使用葡萄糖衍生的丙酮酸,而不是谷氨酰胺进行补偿性。 虽然当谷氨酰胺可用时,PC是可有可无的,但迫使细胞适应低谷氨酰胺条件使其完全依赖PC进行生长。 此外,在其他细胞系中,在营养充足的条件下测量PC活性可以预测对特定回复酶的依赖性。 具有高PC活性的细胞对GLS沉默具有抗性,并且不需要谷氨酰胺来维持生存或生长,但当PC沉默时,其生长受到抑制。 因此,PC-介导的葡萄糖依赖性补体使细胞实现谷氨酰胺独立性。 在谷氨酰胺代谢的慢性抑制期间诱导PC可能被证明是对谷氨酰胺水解疗法产生耐药性的机制。
关键词: 癌症代谢、Warburg效应、代谢通量分析、代谢组学
在恶性转化的许多生物学特征中,重新编程代谢活动以支持失调的细胞生长至关重要( 1 , 2 ). 细胞生长所需的能量和生物量由葡萄糖和谷氨酰胺等营养物质的增强吸收提供,这两种营养物质都被体内的肿瘤细胞大量消耗。 糖酵解是癌症代谢史上研究最广泛的标志( 三 )提供能量和一些必需的生物合成前体分子。 谷氨酰胺是呼吸的主要底物( 4 )以及用于生产蛋白质、己糖胺和大分子的氮。 癌症中以葡萄糖和谷氨酰胺代谢为靶点的概念,最初是由这两种营养素喂养的途径数量合理化的,但最近的研究表明,这两种养分的代谢均受致癌基因调控,这一观点得到了加强( 5 ). 这些发现已开始统一恶性转化的代谢和分子基础。
生产大分子前体是细胞生长的重要组成部分。 许多用于合成脂质、非必需氨基酸和核苷酸的前体是在线粒体三羧酸(TCA)循环中生成的。 如果这些中间体被提取以提供生物合成途径,除非有额外的途径参与提供草酰乙酸(OAA),否则循环将停止运作,草酰乙酸是一种与乙酰辅酶A缩合形成循环经典入口点的分子。 这些OAA生成途径被称为回补( 6 ). 活性回补通量使TCA循环中间产物的水平在生物合成前体持续流出生长期间保持恒定。
由于回补特别有助于肿瘤细胞增殖过程中生物量的产生,回补途径是癌症引人注目的治疗靶点。 然而,一般来说,尚不清楚哪些碳源为这些途径提供了营养,以及癌细胞在多大程度上可以在潜在的再生前体中进行选择。 原则上,葡萄糖和谷氨酰胺是极好的补体营养素,因为它们都很丰富,并且都可以转化为OAA,而无需首先作为乙酰辅酶A进入TCA循环。 谷氨酰胺是一些转化细胞系中首选的回补前体,占OAA总量的90%( 7 , 8 ). 剥夺这些细胞的谷氨酰胺会导致TCA循环中间产物耗尽和生长失败( 9 , 10 ). 癌基因c- myc公司 加剧谷氨酰胺依赖并刺激GLS的表达,GLS是在谷氨酰胺依赖性贫血的第一步将谷氨酰胺转化为谷氨酸的酶( 9 – 11 ). 这些研究首次提供了癌基因与无补体调节之间的机制联系。 尤其是GLS已被提议作为癌症的治疗靶点,因为GLS的反义和化学抑制可在各种模型中减少细胞生长、转化和肿瘤发生( 12 , 13 ). 相比之下,尽管绝大多数肿瘤细胞株消耗葡萄糖的速度比任何其他营养素都快,但只有少数研究表明葡萄糖是肿瘤的补体前体( 14 ).
在这里,我们使用稳定同位素示踪和代谢通量分析对GLS抑制对肿瘤细胞中间代谢和生长的影响进行了系统研究。 这项工作揭示了GLS和PC之间的补偿性关系,PC是一种允许葡萄糖衍生丙酮酸作为回补前体的酶。 研究结果表明,葡萄糖依赖性回补提供了谷氨酰胺依赖性的替代品,并揭示了一种抵抗谷氨酰胺代谢抑制的机制。
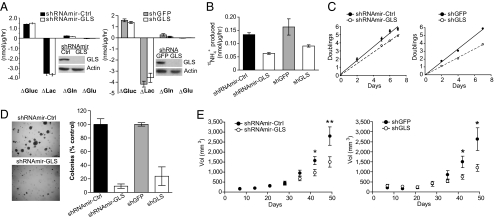
结果 靶向GLS限制了胶质母细胞瘤细胞在培养和体内的生长。 为了测试胶质母细胞瘤细胞生长是否需要GLS活性,在LN229和SF188细胞中表达了两个独立的shRNAs( 图1 和 SI附录 ,图S2 ). 我们之所以选择这些细胞系,是因为当获得营养物质的生理混合物时,两者都使用谷氨酰胺作为首选的回补前体。 此外,两种细胞系均未表达明显数量的谷氨酰胺酶亚型GLS2( SI附录 ,图S1 ),通过靶向GLS增加减少细胞生长的可能性。 抑制GLS表达可适度降低谷氨酰胺的净利用率,而不会影响葡萄糖消耗、乳酸生成或其他氨基酸的利用( 图1 A类 和 SI附录 ,图S2和表S1 ). GLS沉默减少丙氨酸分泌,可能是因为可用于转氨作用的细胞内谷氨酸减少( SI附录 ,表S1 ). 谷氨酰胺γ氮以NH形式释放 4 + GLS沉默期间,GLS通量的指标被抑制( 图1 B类 ). GLS抑制也降低细胞增殖,但不降低细胞周期分布( 图1 C类 和 SI附录 ,图S3 ). 锚定无关生长( 图1 D类 )和皮下异种移植物的生长( 图1 E类 和 SI附录 ,图S2 B类 )在GLS抑制的细胞中均减少。
图1。
谷氨酰胺酶是胶质母细胞瘤细胞在培养和体内最大生长所必需的。 ( A类 )GLS敲除对LN229细胞营养利用和代谢物分泌的影响。 控制(Ctrl)或GLS靶向shRNAmir( 左侧 )和shRNA( 赖特 )进行了测试。 正值反映利用,负值反映分泌。 数据在7小时内平均( B类 )GLS焊剂(生产 15 全日空航空公司 4 + 从L-[γ- 15 N] -谷氨酰胺)。数据为三种独立培养物的平均±SD。 ( C类 )二维培养中的细胞生长。 每个时间点是三种平行培养物的平均±SD。 ( D类 )软琼脂中菌落形成。 数据为三口独立井的平均±SD。 ( E类 )皮下移植瘤的生长。 n个 =shRNAirs的每个细胞系的9个肿瘤( 左侧 )和每个细胞系4个肿瘤的shRNAs( 赖特 ). 显示了每个细胞系的平均体积±SE* P(P) < 0.05, ** P(P) < 0.005. 葡萄糖; 乳酸; 谷氨酰胺; 谷氨酸,谷氨酸。
丙酮酸羧化酶对GLS的抑制伴随着葡萄糖依赖性贫血的增加。 GLS缺陷细胞的残留生长促使我们确定替代途径,以补偿谷氨酰胺依赖性缺乏的减少。 GLS沉默导致谷氨酰胺衍生碳对脂质的贡献适度减少,而葡萄糖依赖性脂质合成略有增加( SI附录 ,图S4 A类 ). GLS抑制还减少了TCA循环中间产物苹果酸和柠檬酸的标记 13 源于谷氨酰胺的C( 图2 A类 , 左侧 和 SI附录 ,图S4 B类 ). 为了确定提供这些池的替代营养素,我们用D-[1,6培养细胞- 13 C] -葡萄糖,并使用质谱法分析苹果酸和柠檬酸。 当GLS被沉默时,这两种中间体都含有更多的葡萄糖衍生碳( 图2 A类 , 赖特 和 SI附录 ,图S4 C类 ). 在GLS-抑制的LN229细胞中,含有两个额外质量单位(柠檬酸盐m+2)的柠檬酸盐池的分数增加了50%以上。
图2。
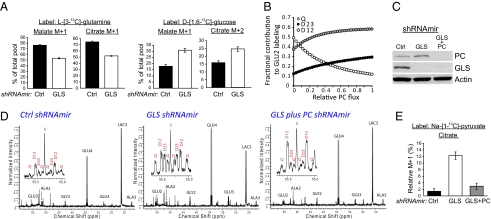
谷氨酰胺酶沉默通过丙酮酸羧化酶(PC)增加葡萄糖依赖性恢复。 ( A类 )使用气相色谱/质谱法测量L-[3培养细胞中柠檬酸和苹果酸的富集- 13 C] -谷氨酰胺( 左侧 )和D-[1,6- 13 C] -葡萄糖( 赖特 ). 结果来自用重复的7小时培养物进行的代表性实验。 ( B类 )在D-[U培养期间,增加PC通量对谷氨酸C2(GLU2)总标记中四分位(Q)、2,3双位(D23)和1,2双位(D12)的分数贡献的预测效果- 13 C] -葡萄糖。 数据是使用建模软件生成的 tcaSIM公司 假设有一个活跃的TCA循环,丙酮酸的富集度为95%,并有活跃的回补。 对TCA循环的35圈进行了模拟。 ( C类 )表达对照shRNAmir、针对GLS的shRNAmer或针对GLS和PC的shRNAmir的LN229细胞的蛋白质印迹( D类 )从细胞系中提取代谢物的核磁共振波谱 C类 用10 mM D-[U培养细胞- 13 C] -葡萄糖和4 mM未标记的谷氨酰胺维持8小时。插图突出显示了GLU2多重态。 个别峰的分裂是长程耦合的结果。 ( E类 )来自[1的柠檬酸盐标签- 13 C] -丙酮酸在相同的三种细胞系中。 柠檬酸盐m+1相对于未标记标准物的百分比(其中m+1=0%)绘制在 年 轴。 每个培养物含有5 mM Na-[1- 13 C] -丙酮酸盐,4mM谷氨酰胺,不含葡萄糖。 数据是三个7小时培养物的平均±SD。 谷氨酸; Ala,丙氨酸; 甘氨酸; 乳酸; S、 单线。
柠檬酸盐m+2增加有多种可能的解释。 最简单的是,更多的柠檬酸分子含有单一的 13 来自葡萄糖衍生的乙酰辅酶a(柠檬酸盐m+1)的C保留在循环中,产生更大比例的OAA m+1,增加了标记的OAA与标记的乙酰辅酸缩合的可能性( SI附录 ,图S5 ). 这是合理的,因为谷氨酰胺通常是OAA的主要来源( 7 )预计减少GLS通量将减少未标记OAA的总产量。 一个同样可信的替代方案是,GLS抑制伴随着PC活性的增加,PC直接从葡萄糖衍生的丙酮酸产生OAA,并在OAA m+1与葡萄糖衍生的乙酰CoA m+1浓缩后产生柠檬酸m+2( SI附录 ,图S5 ). 由于质谱无法轻易区分这两种可能性,我们使用了该程序 tcaSIM公司 模拟不同谷氨酰胺依赖性回补和PC流量对 13 碳同位素形成( 15 ). 如果细胞在D-[U培养基中培养,则增加PC通量可提高谷氨酸碳2(GLU2)处双链(或四链,Q)和2-3双链(D23)的分数贡献- 13 C] -葡萄糖( 图2 B类 ; 中的详细标签方案 SI附录 ,图S6 ). 相比之下,在PC活性没有改变的情况下,简单地减少回补可以抑制D23( SI附录 ,图S7 ). 这种区别产生了可以通过NMR监测的相对PC通量的定量标记。 生成了LN229衍生细胞系,该细胞系包含GLS单独或GLS和PC的抑制( 图2 C类 ),这些细胞在D-[U中培养- 13 C] -葡萄糖。 谷氨酸等位异构体的核磁共振分析( 16 )发现当GLS被抑制时,总回补通量下降了~45%,但仍占总TCA循环活动的很大一部分( SI附录 ,表S2 ). GLU2检测显示GLS抑制细胞中的Q和D23增强,如果PC也被抑制,这些共振恢复正常( 图2 D类 )与GLS抑制期间PC流量增加和葡萄糖依赖性恢复一致。
作为PC活性的独立测试,细胞用[1- 13 C] -丙酮酸和代谢物通过质谱分析。 丙酮酸C1以CO的形式释放 2 通过丙酮酸脱氢酶,但如果丙酮酸通过PC进入TCA循环,则被保留( SI附录 ,图S8 ). GLS抑制与6倍的 13 C从[1转账- 13 C] -丙酮酸转化为柠檬酸盐,如果PC也被抑制,则情况会逆转( 图2 E类 ). 总之,数据表明,慢性GLS抑制导致PC活性增加,部分抵消了谷氨酰胺依赖性贫血的减少。
谷氨酰胺脱除期间细胞生长需要PC。 接下来,我们测试了当谷氨酰胺代谢受损时,PC是否有必要支持生长。 SF188胶质母细胞瘤细胞对谷氨酰胺“上瘾”以维持生存和生长( 10 ). 我们之前使用过表达Bcl-xL(SF-xL)的SF188衍生细胞来检测葡萄糖剥夺和Akt抑制对中间代谢的影响( 17 ). 这些细胞保留谷氨酰胺成瘾的表型,并在几天内失去谷氨酰胺后失去生存能力( 图3 A类 和 B类 ). 与其他研究的观察结果一致( 9 , 18 ),谷氨酰胺生成细胞减少了谷氨酸和TCA循环中间产物库,并适度增加了细胞ATP含量( SI附录 ,图S9 ). 添加谷氨酸或二甲基-α-KG可完全恢复细胞活力,部分恢复谷氨酰胺生成细胞的生长( SI附录 ,图S10 A类 和 B类 ). 我们还测试了DMEM中通常缺失的其他氨基酸是否可以用于补体。 将脯氨酸、天冬氨酸和天冬酰胺添加到含有L-[U的DMEM中- 13 C] -谷氨酰胺和代谢物通过GC/MS进行分析。添加这些氨基酸不会显著改变TCA循环中间产物的标记( SI附录 ,图S10 C类 ),表明它们在TCA循环中没有明显的代谢。 此外,这些氨基酸,无论是单独还是组合,都不能在缺乏谷氨酰胺的情况下挽救细胞生长( SI附录 ,图S10 D类 ).
图3。
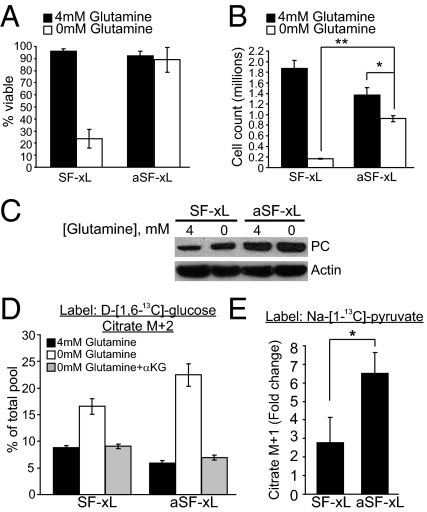
PC活性是在适应低谷氨酰胺条件期间诱导的。 ( A类 和 B类 )在谷氨酰胺丰富或缺乏的条件下,亲代SF-xL胶质母细胞瘤细胞和适应低谷氨酰胺(aSF-xL)的细胞的存活和生长。 数据是2×10的三种独立培养物的平均±SD 5 细胞在有或无谷氨酰胺的条件下生长72h( C类 )亲代SF-xL细胞和aSF-xL细胞中PC蛋白的表达。 将亲代细胞从谷氨酰胺中取出7 h,并将适应细胞给予谷氨酰胺再充满培养基7 h( D类 )在存在和不存在谷氨酰胺和4 mM二甲基α-KG的情况下,亲代和适应性细胞中柠檬酸m+2的丰度持续7小时( E类 )增加转移 13 来自[1的C- 13 C] -适应细胞中的丙酮酸到柠檬酸。 每个培养物含有5 mM Na-[1- 13 C] -丙酮酸,不含葡萄糖。 该比率显示了在7小时的实验中,谷氨酰胺生成(0 mM)和谷氨酰胺释放(4 mM)条件之间的倍数变化。 谷氨酰胺生成的亲代细胞和aSF-xL细胞中的最终柠檬酸m+1组分分别为11%和16.5%* P(P) < 0.05, ** P(P) < 0.005.
通过逐渐适应SF-xL细胞在逐渐降低的谷氨酰胺浓度下生长,我们获得了在0 mM谷氨酰胺中保持生存能力的亚系( 图3 A类 ),为在没有细胞死亡的情况下研究谷氨酰胺非依赖性代谢提供了机会。 与亲代细胞不同,适应性细胞在缺乏谷氨酰胺的情况下增殖,尽管重新引入谷氨酰胺仍能适度刺激其生长( 图3 B类 ). 这些细胞的PC蛋白表达高于亲代细胞( 图3 C类 ),但mRNA水平没有显著差异( SI附录 ,图S11 A类 ). 虽然急性谷氨酰胺缺乏不会影响亲代或适应性细胞的葡萄糖消耗( SI附录 ,图S11 B类 ),当任一细胞系与D-[1,6培养时,增加了柠檬酸m+2的丰度- 13 C] -葡萄糖,并且在适应的细胞中相对增加更高( 图3 D类 ). 添加二甲基-αKG可将柠檬酸盐m+2抑制到两种细胞系的正常水平( 图3 D类 ). 当谷氨酰胺严重缺乏时,两种细胞系中丙酮酸C1与柠檬酸的结合也增强,但在适应性细胞中相对增强更高( 图3 E类 )与PC蛋白的丰度相当。 这些数据共同表明,谷氨酰胺缺乏会导致PC蛋白丰度增加,以及葡萄糖/丙酮酸用于补充的程度增加。
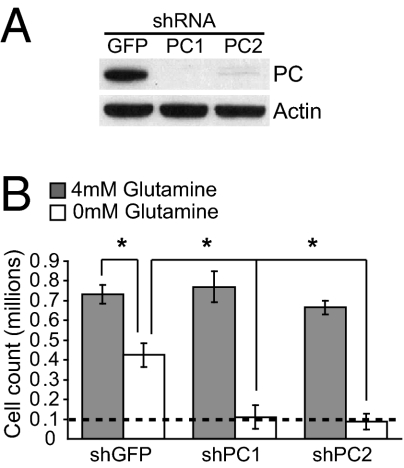
为了确定在谷氨酰胺缺乏的条件下生长是否需要PC,PC从适应细胞中稳定地耗尽( 图4 A类 )这些细胞在有无谷氨酰胺的条件下生长( 图4 B类 ). 在谷氨酰胺存在的情况下,含有一个对照shRNA或两个针对PC的shRNA中的任何一个的细胞的生长没有差异。然而,在缺乏谷氨酰胺的条件下,PC表达的沉默严重限制了细胞的生长( 图4 B类 ). 此外,当PC被沉默时,从葡萄糖到大分子的碳转移被抑制,但仅在无谷氨酰胺的条件下( SI附录 ,图S12 ),与对细胞生长的影响相似。 因此,PC对于谷氨酰胺补充型胶质母细胞瘤细胞的生长是不必要的,但当谷氨酰胺供应有限时需要PC。
图4。
细胞需要PC来逃避谷氨酰胺成瘾。 ( A类 )抑制适应低谷氨酰胺生长的SF-xL细胞中PC蛋白的表达,然后感染表达对照shRNA(GFP)或针对PC(PC1,PC2)的shRNA的慢病毒。 ( B类 )细胞在有无细胞外谷氨酰胺的情况下生长。 细胞以1×10的密度进行电镀 5 /培养72h。数据为三种独立培养物的平均±SD* P(P) < 0.05.
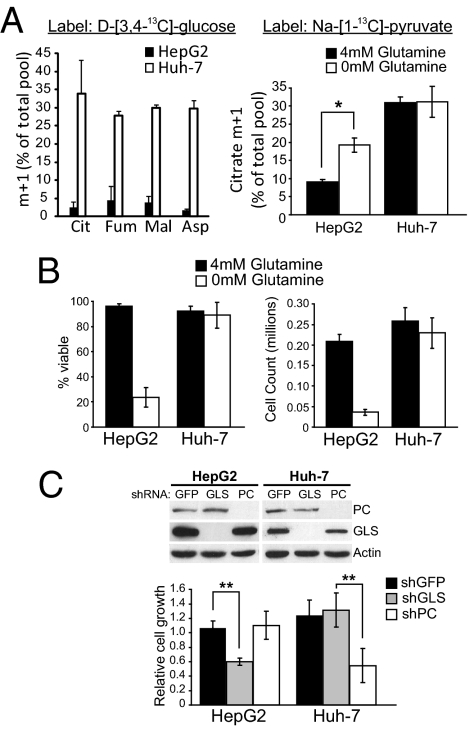
PC活性预测对谷氨酰胺戒断的抵抗力。 接下来,我们测试了在营养充足的条件下PC活性是否可以预测谷氨酰胺依赖性。 我们培养了两种肝癌细胞系HepG2和Huh-7,它们具有不同的 13 C-标记营养素,以评估其对谷氨酰胺和PC的使用情况。 首先,将每个细胞系培养在含有D-[U的培养基中- 13 C] -葡萄糖和未标记的谷氨酰胺,或在未标记的葡萄糖和L-[U中- 13 C] -谷氨酰胺。 代谢产物分析 13 C富集显示HepG2细胞(而非Huh-7细胞)使用谷氨酰胺作为主要的回补前体( SI附录 ,图S13 ). 接下来,用未标记的谷氨酰胺和D-[3,4培养每个细胞系- 13 C] -葡萄糖,代谢为[1- 13 C] -丙酮酸,可方便地读出PC活性( SI附录 ,图S8 ). 只有Huh-7细胞显示明显的 13 C进入TCA循环( 图5 A类 ). 然后用[1培养细胞- 13 C] -丙酮酸,存在和不存在谷氨酰胺。 HepG2细胞显示最小 13 当谷氨酰胺存在时,柠檬酸盐中的C标记,以及急性谷氨酰胺缺乏时标记的适度增加( 图5 A类 ). 相比之下,无论是否存在谷氨酰胺,Huh-7细胞的柠檬酸标记水平较高( 图5 A类 ). 这些数据表明Huh-7细胞具有较高的PC活性,而HepG2细胞没有。
图5。
PC活性预测细胞对谷氨酰胺和谷氨酰胺酶的独立性。 ( A类 , 左侧 )D-[3,4细胞内代谢物的标记- 13 C] -在完整培养基(包括4 mM谷氨酰胺)中生长7小时的HepG2和Huh-7细胞中的葡萄糖( 赖特 )来自[1的柠檬酸盐标签- 13 C] 在存在和不存在谷氨酰胺的情况下生长7小时的HepG2和Huh-7细胞中的-丙酮酸( B类 )HepG2和Huh-7细胞在存在和不存在谷氨酰胺的情况下72小时的存活率和生长( C类 )表达针对GFP(对照)、GLS或PC的shRNAs的HepG2和Huh-7衍生细胞系中的蛋白表达( 顶部 )以及在含有葡萄糖和谷氨酰胺的培养基中每个细胞系的生长。 数据是72小时内三种独立培养物的平均±SD* P(P) < 0.05, ** P(P) < 0.005.
与Huh-7细胞相比,HepG2细胞对谷氨酰胺的依赖性更强,Huh-7在无谷氨酰胺的条件下,其生存能力或生长没有降低( 图5 B类 ). 为了确定每个细胞系对任一回补酶的依赖性,在HepG2和Huh-7细胞中分别抑制GLS和PC。 当生长在含有葡萄糖和谷氨酰胺的培养基中时,HepG2细胞可以耐受PC表达的丧失,但如果GLS被抑制,则生长会降低( 图5 C类 ). Huh-7细胞显示出相反的结果,当GLS被抑制时,细胞没有生长损失,但当PC被靶向时,细胞生长不良( 图5 C类 ). 这些数据表明,在营养充足的条件下,某些肿瘤细胞的生长需要PC,并且可以通过基本PC活性预测谷氨酰胺的独立性。
讨论 在这里,我们确定了稳定抑制回复酶GLS对谷氨酰胺依赖性肿瘤细胞生长的影响。 结果表明,尽管GLS是这些细胞在培养物和皮下肿瘤中实现最大生长所必需的,但即使是谷氨酰胺依赖的细胞也可以通过将葡萄糖中的碳重新路由到通常由谷氨酰胺供应的代谢物池来进行补偿。 负责这种葡萄糖依赖性回补的酶,PC,对于适应低谷氨酰胺条件的细胞生长至关重要。 PC在一些谷氨酰胺依赖性肿瘤细胞系中也提供了首选的回补流量,并且靶向这些细胞中的GLS对生长没有影响。
这些发现强调了回补在肿瘤细胞生长中的重要性,因为通过一条回补途径抑制流量会诱导一条替代途径,从而实现基本上相同的OAA生成目标。 值得注意的是,这里研究的两条途径使细胞能够将两种最丰富的营养物质中的碳输送到OAA池中。 虽然许多营养物质原则上可以提供OAA池,但持续的细胞生长可能需要将最易获得的营养物质谷氨酰胺和葡萄糖转化为在强健生物合成期间维持TCA循环流量所需的OAA净量。 研究结果与以下假设一致,即回补是活肿瘤中谷氨酰胺/葡萄糖消耗的关键功能之一,并建议在体内控制回补的努力应集中在这两种营养素上。
GLS沉默对中间代谢有多种影响。 它抑制但没有消除充盈( SI附录 ,表S2 )而残留的补体越来越依赖于PC。它也增加了葡萄糖对乙酰辅酶A库的贡献( SI附录 ,表S2 ),因为谷氨酰胺酶活性时,谷氨酰胺是该池的次要碳源( 17 ). 值得注意的是,即使GLS蛋白几乎完全消除,对谷氨酰胺衍生的碳向苹果酸和柠檬酸盐池的输送也只有适度的影响( 图2 A类 和 SI附录 ,图S4 B类 ). 这反映了这样一个事实,即谷氨酰胺转化为谷氨酸,这是谷氨酰胺依赖性回补的初始步骤,不仅由谷氨酰胺酶催化,还由核苷酸和己糖生物合成途径中的酰胺转移酶催化( 19 ). 这些产生谷氨酸但不产生游离NH的酶的活性 4 + ,可能有助于解释谷氨酰胺消耗量超过NH的原因 4 + 一些胶质母细胞瘤细胞的分泌( 10 , 17 ). 这一发现提高了无补体和其他生物合成途径之间代谢协同的可能性。 例如,5-磷酸核糖基焦磷酸酰胺转移酶和氨甲酰磷酸合成酶II分别在嘌呤和嘧啶合成的早期从谷氨酰胺生成谷氨酸。 这种谷氨酸可能独立于GLS为补体提供碳源。
PC在糖异生过程中产生OAA的作用众所周知( 20 )罕见的先天性代谢错误中的全球性结构性PC缺乏会导致空腹不耐受、低血糖、乳酸中毒和其他中间代谢紊乱( 21 ). 然而,PC在肿瘤细胞中的作用尚未得到广泛研究。 大鼠肝癌相对于周围肝脏表现出PC抑制,而GLS表达与肿瘤生长率相关( 22 , 23 ). 相比之下,最近在人类肿瘤中的研究表明PC的作用更为突出。在肺癌患者中,输注D-[U- 13 C] -手术切除前的葡萄糖可以分析肿瘤的中间代谢( 14 ). 在从这些肿瘤中提取的代谢物中,核磁共振波谱揭示了 13 C标记强烈表明PC提供了显著的回补通量。 相对于周围肺组织,PC蛋白在这些肿瘤中高表达。 因此,PC可能催化一些人类肿瘤中的首选修复途径。
据我们所知,这项研究是对癌细胞中PC和谷氨酰胺代谢之间关系的独特描述。 初级星形胶质细胞利用PC介导的回补来维持谷氨酸等神经递质库( 20 , 24 , 25 ). 星形胶质细胞通常不消耗谷氨酰胺,而是从细胞外空间清除谷氨酸,并使用谷氨酰胺合成酶将其转化为谷氨酰胺。 因此,细胞外谷氨酸池保持较低水平,降低了混乱兴奋性神经传递的风险( 25 ). 在培养基中,向星形胶质细胞补充谷氨酸会抑制PC活性,这意味着这些细胞可以感受到过量的谷氨酸,并通过减少PC介导的回补反应( 26 ). 目前的研究表明,在癌细胞中也存在类似的机制,因为谷氨酰胺或α-KG抑制PC流量,即使在生长条件不具备谷氨酰胺的细胞中也是如此。 因此,在谷氨酰胺和葡萄糖依赖性补体之间进行选择,这些细胞选择谷氨酰胺。 在能量基础上,谷氨酰胺依赖性无补体是有利的,因为PC每形成一个OAA消耗一个ATP分子,而GLS不使用ATP; 相反,谷氨酰胺通过TCA循环中的酶代谢为OAA会产生氧化磷酸化的还原当量。
PC诱导的机制似乎很复杂。 在谷氨酰胺缺乏期间,PC蛋白丰度增加,但这并不需要增加mRNA丰度。 谷氨酰胺下游代谢物的可用性降低可能与诱导PC活性有关,因为其中一些代谢物在体外或培养细胞中抑制PC( 26 , 27 ). ATP(PC激活剂)的适度增加可能有助于( 28 ). 最近的工作还表明,PC在肝脏中会发生赖氨酸乙酰化( 29 ),但这种修改对PC活动的影响尚不清楚。 需要进一步研究,以了解这些因素在调节回补中的重要性。
目前的研究表明,PC可以使癌细胞抵抗谷氨酰胺酶抑制,或者在某些情况下,抵抗谷氨酰胺剥夺。 这可能为长期接触干扰谷氨酰胺摄取或代谢的药物提供了一种抵抗机制。 或者,一些细胞,如Huh-7,使用PC作为补骨术的默认机制,使它们对损害谷氨酰胺作为线粒体底物的使用的治疗不敏感。 真正的谷氨酰胺独立性可能需要额外的机制来产生少量谷氨酰胺用于蛋白质合成,并为己糖胺和核苷酸提供氮( 30 ). 确定PC和谷氨酰胺合成酶是否在癌细胞中协同调节将是一件有趣的事情。
使用稳定同位素的代谢通量分析应继续提供对培养的肿瘤细胞、动物模型和人类癌症中增殖肿瘤细胞的代谢途径的见解。 人类研究的潜力特别令人感兴趣,因为 13 C输注可与常规代谢成像相结合,以获得肿瘤代谢的广泛视图,并阐明在以下方面的发现 1 磁共振波谱、正电子发射断层扫描和其他临床方法。 通过仔细选择标记的营养素,可以将代谢活动与肿瘤分期、肿瘤遗传学和治疗反应联系起来。 该方法可用于确定体内生长的关键代谢途径,并预测代谢阻断对肿瘤生长的影响。
材料和方法 细胞培养、生长和活性测定。 SF-xL、LN229、HepG2和Huh-7细胞在添加10%FBS(HyClone)、青霉素/链霉素和6 mM L-谷氨酰胺的Dulbecco改良鹰培养基(DMEM)中培养。 DMEM与透析FBS的营养剥夺和代谢标记实验( 17 ). 通过胰蛋白酶化监测细胞生长,并使用血细胞仪或自动细胞计数器(BioRad;TC10)进行计数。 通过台盼蓝排除法测定存活率。 在所有稳定的敲除实验中,在培养物中很少观察到分离的细胞,这些细胞不包括在生长和活力计数中。 使用尼康Eclipse TE300显微镜获得相位对比图像,并使用MetaMorph(通用成像)进行处理。 为了使SF-xL细胞适应低谷氨酰胺,细胞在DMEM中生长,如上所述,但谷氨酰胺逐渐减少(3 mM 1周,然后1 mM 1周,然后0.5 mM 1星期)。 在0.5 mM谷氨酰胺中生长超过1个月后,将细胞转移到含有0 mM谷氨酸的培养基中。 存活下来并继续增殖的细胞被认为是谷氨酰胺非依赖性细胞(“aSF-xL细胞”)。
代谢分析。 使用自动电化学分析仪(BioProfile Basic-4分析仪;NOVA)从0.6-mL等分培养基中测定葡萄糖、乳酸、谷氨酰胺和谷氨酸的浓度。 全日空航空公司 4 + 分泌物用分光光度法(Megazyme)测定。 使用氨基酸分析仪(Hitachi;L8900)通过HPLC测量氨基酸的消耗和分泌。 代谢率是通过将代谢物丰度的绝对变化标准化为蛋白质含量来确定的。
RNA干扰。 所有RNA干扰(RNAi)实验都使用细胞池。 RNAi载体是从基于pGIPZ(shRNAmir)或pLKO.1(shRNA)主干(开放生物系统)的商业库中获得的。 用于RNAi的序列位于 SI附录 使用Fugene HD(Roche)将慢病毒构建物pCMVΔR8.91和pMD2.G共转染293T细胞,产生慢病毒颗粒。 转染后2天收集含病毒上清液并用于感染细胞。 感染后第2天添加嘌呤霉素(1μg/mL),在任何实验之前继续选择10天。 在1μg/mL的嘌呤霉素中维持稳定的感染池,并适当沉默。
蛋白质表达。 在RIPA缓冲液中制备全细胞裂解物,并使用BCA蛋白质分析(Thermo Scientific)进行定量。 蛋白质通过SDS/PAGE分离,转移到PVDF膜上,并用抗PC(Santa Cruz Biotechnology)、β-肌动蛋白(Sigma)、GLS或GLS2(在Matés实验室制备)的抗体进行检测。
软琼脂集落形成分析。 通过低密度的平板细胞(细胞数2×10)测定锚定非依赖性菌落形成 三 )和高密度(1×10 4 )在12孔板中,使用0.33%SeaKem GTG琼脂(Cambrex BioScience)。 2周后,在20%甲醇中用0.05%结晶紫对培养物进行染色。 低密度微孔用于计数直径>200μm的菌落,高密度微孔用于摄影。
异种移植物生长分析。 将SF-xL或LN229细胞以200×10的浓度重新悬浮在DMEM中 6 /mL,与Matrigel(Becton-Dickinson)以1:1的比例混合,并将皮下埋植到男性侧翼 北卡罗来纳州立大学 6-8周龄小鼠(20×10 6 每次注射的细胞数)。 将表达非靶向和靶向shRNAs的细胞注射到对侧侧翼。 肿瘤体积根据公式[(长)×(宽)计算 2 ]/2. 当肿瘤超过2000毫米时 三 老鼠被杀了。
使用稳定同位素的代谢实验。 除非另有说明,否则所有培养物均含有10 mM葡萄糖和2-4 mM谷氨酰胺。 将含有80–90%融合细胞的培养皿在PBS中冲洗两次,然后覆盖含有同位素富集营养素的培养基,并培养7–8 h。通过监测GLS通量的转移来测量GLS通量 15 N来自L-[γ- 15 N] -谷氨酰胺(剑桥同位素实验室) 15 全日空航空公司 4 + (详情请参见 SI附录 ). 为了通过GC/MS分析细胞内代谢物,将标记在6厘米培养皿中的细胞在冰镇生理盐水中冲洗,并在冷的50%甲醇中进行三次冻融循环。 将裂解液离心以去除沉淀蛋白,添加标准溶液(50 nmols 2-氧代丁酸钠),蒸发样品并通过三甲基硅烷化(Tri-Sil HTP试剂,Thermo Scientific)衍生。 将三微升衍生材料注入安捷伦6970气相色谱仪,该色谱仪配备有熔融石英毛细管GC柱(30米长,0.25毫米直径),并与安捷伦5973质量选择性检测器联网。 使用纯标准验证所有感兴趣代谢物的保留时间。 监测以下离子的丰度: 米/z 富马酸245–249, 米/z 苹果酸为335–339, 米/z 天冬氨酸为334–338,以及 米/z 柠檬酸盐为465–471。 这些离子的解释见 SI附录 .测量的质量同位素分布已校正为天然丰度 13 C类( 31 ).
核磁共振波谱实验使用了较大的培养物(每个样品八个15厘米的培养皿)。 按说明提取代谢物并冷冻干燥( 17 ). 核磁共振波谱是在瓦里安ANOVA 14.1 T光谱仪(瓦里安仪器)上进行的,该光谱仪配备有一个3毫米宽的探针,“观察”线圈调谐至 13 C(150兆赫)。 使用标准的WALTZ-16脉冲序列进行质子去耦。 在以下条件下获得碳谱:脉冲翻转角45°,重复时间1.5 s,谱宽35 kHz,数据点数量104986,扫描次数7000–30000,需要6–25 h。自由感应衰减被零填充到131072点,并用指数乘法切趾。 使用ACDLabs SpecManager(高级化学开发)测定相关峰面积。
致谢 我们感谢Craig Malloy、Mark Jeffrey和Aron Jaffe对数据和手稿的反馈。 Kartik Rajagopalan测量了氨基酸水平。 Carolina Cardona纯化了谷氨酰胺酶抗体。 R.J.D.得到了美国国立卫生研究院(NIH)(DK072565)、德克萨斯州癌症预防与研究所(CPRIT)(HIRP100437)、韦尔奇基金会(I-1733)和儿童临床研究咨询委员会的资助。 E.S.J.由国家卫生研究院拨款(DK078933)支持。 J.M.M.得到了西班牙财政部的资助(SAF2010-17573)。 T.C.由CPRIT培训拨款支持,a.R.M.由NIH培训拨款支持(5T32GM083831-02)。
脚注
这篇文章是PNAS直接提交的。 C.V.D.是编辑委员会邀请的客座编辑。
工具书类
1 Debrardinis RJ、Sayed N、Ditsworth D、Thompson CB。 一砖一瓦:新陈代谢和肿瘤细胞生长。 2008年通用操作技术开发; 18:54–61. doi:10.1016/j.gde.2008.02.003。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
2 Vander Heiden MG、Cantley LC、Thompson CB。 了解Warburg效应:细胞增殖的代谢需求。 科学。 2009; 324:1029–1033. doi:10.1126/science.1160809。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
三。 Warburg O.谈癌细胞的呼吸障碍。 科学。 1956; 124:269–270. [ 公共医学 ] [ 谷歌学者 ]
4 Reitzer LJ、Wice BM、Kennell D。谷氨酰胺而非糖是培养HeLa细胞的主要能量来源的证据。 生物化学杂志。 1979; 254:2669–2676. [ 公共医学 ] [ 谷歌学者 ]
5 Tennant DA,Durán RV,Gottlieb E.针对癌症治疗的代谢转化。 Nat Rev癌症。 2010; 10:267–277. doi:10.1038/nrc2817。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
6 Owen OE、Kalhan SC、Hanson RW。补充和缓解对柠檬酸循环功能的关键作用。 生物化学杂志。 2002; 277:30409–30412. doi:10.1074/jbc。 R200006200。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
7 DeBerardinis RJ等。有氧糖酵解之外:转化细胞可以参与谷氨酰胺代谢,超过蛋白质和核苷酸合成的需要。 美国国家科学院院刊2007; 104:19345–19350. doi:10.1073/pnas.0709747104。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
8 Portais JC、Voisin P、Merle M、Canioni P.通过碳13核磁共振研究C6胶质瘤细胞中的葡萄糖和谷氨酰胺代谢。 生物化学。 1996; 78:155–164. doi:10.1016/0300-9084(96)89500-9。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
9 Yuneva M、Zamboni N、Oefner P、Sachidanadam R、Lazebnik Y。谷氨酰胺而非葡萄糖缺乏诱导人类细胞MYC依赖性凋亡。 细胞生物学杂志。 2007; 178:93–105. doi:10.1083/jcb.200703099。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
10 Wise DR等。Myc调节转录程序,刺激线粒体谷氨酰胺水解并导致谷氨酰胺成瘾。 美国国家科学院院刊2008; 105:18782–18787. doi:10.1073/pnas.0810199105。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
11 Gao P等。c-Myc抑制miR-23a/b可增强线粒体谷氨酰胺酶的表达和谷氨酰胺代谢。 自然。 2009; 458:762–765. doi:10.1038/nature07823。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
12. 王建军,等。靶向线粒体谷氨酰胺酶活性抑制致癌转化。 癌细胞。 2010; 18:207–219. doi:10.1016/j.ccr.2010.08.009。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
13 Lobo C等。反义mRNA抑制谷氨酰胺酶表达会降低肿瘤细胞的生长和致瘤性。 生物化学杂志2000; 348:257–261. [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
14 Fan TW等。通过(13)C稳定同位素再溶代谢组学(SIRM)分子癌识别人类肺癌代谢途径的调节发生改变。 2009; 8:41. doi:10.1186/1476-4598-8-41。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
15 Jeffrey FM、Rajagopal A、Malloy CR、Sherry AD.13C-NMR:一种简单而全面的中间代谢分析方法。 生物化学科学趋势。 1991; 16:5–10. doi:10.1016/0968-0004(91)90004-f。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
16 Malloy CR,Sherry AD,Jeffrey FM。通过13C核磁共振波谱研究灌注心脏中柠檬酸循环途径的碳通量。 FEBS信函。 1987; 212:58–62. doi:10.1016/0014-5793(87)81556-9。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
17 Yang C等。胶质母细胞瘤细胞需要谷氨酸脱氢酶才能在葡萄糖代谢或Akt信号受损时存活。 2009年癌症研究; 69:7986–7993. doi:10.1158/0008-5472.CAN-09-2266。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
18 Choo AY等。TSC阴性细胞的葡萄糖成瘾是由代谢需求与供应的mTORC1依赖性平衡失败引起的。 分子细胞。 2010; 38:487–499. doi:10.1016/j.molcel.2010.05.007。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
19 DeBerardinis RJ,Cheng T.Q的下一篇:谷氨酰胺在代谢、细胞生物学和癌症中的多种功能。 致癌物。 2010; 29:313–324. doi:10.1038/onc.2009.358。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
20 Jitrapakdee S,华莱士JC。 丙酮酸羧化酶的结构、功能和调节。 《生物化学杂志》1999; 340:1–16. doi:10.1042/bj3400001。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
21 Marin-Valencia I,Roe CR,Pascual JM。丙酮酸羧化酶缺乏:机制、模拟物和回补。 分子遗传学。 2010; 101:9–17. doi:10.1016/j.ymgme.2010.05.004。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
22 Chang LO,Morris HP公司。 肝脏和肝肿瘤中丙酮酸羧化酶的酶学和免疫学研究。 癌症研究1973; 33:2034–2041. [ 公共医学 ] [ 谷歌学者 ]
23 Linder-Horowitz M、Knox WE、Morris HP。 大鼠肝癌的谷氨酰胺酶活性和生长速率。 1969年癌症研究; 29:1195–1199. [ 公共医学 ] [ 谷歌学者 ]
24 Shank RP,Bennett GS,Freytag SO,Campbell GL.丙酮酸羧化酶:一种与氨基酸神经递质库补充有关的星形胶质细胞特异性酶。 脑研究1985; 329:364–367. doi:10.1016/0006-8993(85)90552-9。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
25 谷氨酸-谷氨酰胺循环不是化学计量的:谷氨酸在大脑中的命运。 神经科学研究杂志,2007; 85:3347–3358. doi:10.1002/jnr.21444。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
26 Qu H,Eloqayli H,Unsgárd G,Sonnewald U。谷氨酸降低培养的小脑星形胶质细胞中丙酮酸羧化酶的活性,并将葡萄糖作为能量底物。 神经科学研究杂志,2001年; 66:1127–1132. doi:10.1002/jnr.10032。 [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
27 Scrutton MC,白色MD。丙酮酸羧化酶。 α-酮戊二酸和L-谷氨酸对哺乳动物和鸟类肝脏酶的抑制作用。 生物化学杂志。 1974; 249:5405–5415. [ 公共医学 ] [ 谷歌学者 ]
28 Keech B,Barritt GJ公司。 镁离子(Mg2+)和镁腺苷三磷酸离子(MgATP2-)对绵羊肾脏丙酮酸羧化酶的变构活化生物化学杂志。 1967; 242:1983–1987. [ 公共医学 ] [ 谷歌学者 ]
29 赵S,等。蛋白赖氨酸乙酰化对细胞代谢的调节。 科学。 2010; 327:1000–1004. doi:10.1212/science.1179689。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
30 Meng M,Chen S,Lao T,Liang D,Sang N.氮合成代谢是谷氨酰胺分解在增殖细胞中的重要性的基础。 细胞周期。 2010; 9(19):3921–3932. doi:10.4161/cc.9.13139。 [ 内政部 ] [ PMC免费文章 ] [ 公共医学 ] [ 谷歌学者 ]
31 Fernandez CA、Des Rosiers C、Previs SF、David F、Brunengraber H。天然稳定同位素丰度的13C质量同位素分布校正。 质谱学杂志。 1996; 31:255–262. doi:10.1002/(SICI)1096-9888(199603)31:3<255::AID-JMS290>3.0.CO; 2-3. [ 内政部 ] [ 公共医学 ] [ 谷歌学者 ]
关联数据 本节收集本文中包含的任何数据引用、数据可用性声明或补充材料。