人体样本
PTC组织和人脐带样本分别取自江苏大学附属医院(中国镇江)知情和同意的PTC患者和母亲。本研究得到了江苏大学附属医院伦理委员会的批准。
细胞培养
W3、TPC-1和Nthy-ori 3–1购自中国科学院细胞库,在含有10%FBS(Gibco)和1%pen/strep(Gibco)的DMEM培养基中培养,37°C,5%CO2如前所述,从新鲜脐带样本中分离出HUCMSCs[17,18]并保存在干细胞培养基中(Cyagen,广州,中国)。
慢病毒转导与寡核苷酸转染
PELI1过表达慢病毒颗粒(LV-PELI1)、抑制结构物(sh-PELIl)及其相对对照物(分别为LV-NC和sh-NC)包装并从GeneChem(中国上海)购买。根据制造商手册,PTC细胞感染重组慢病毒转导单位加上5μg/ml聚brene(Sigma,Natick,MA)。泥质1shRNA序列:5′-GCCAAATGGAAGACATCAGAT-3′;加扰shRNA:5′-TTCTCCGAACGTGTCACGT-3′。
合成miR-30c-5p模拟物、模拟对照、miR-30c-5p抑制剂和抑制剂对照购自GenePharma(中国上海)。pcDNA-Peli1质粒和空载体由中国科学院肖一川教授(中国上海)赠送。根据制造商的方案,使用Lipofectamine 2000(Invitrogen,Carlsbad,CA)将50 nM miR-30c-5p模拟物或100 nM miR-30c-5p抑制剂或miR-30c-5p模拟体加上1μg Peli1质粒转染PTC细胞。
miR-30c-5p(miR-30c-5p-EV)设计的HUCMSC-EV
用50 nM miR-30c-5p模拟物或使用Lipofectamine 2000(Invitrogen)的模拟NC转染HUCMSCs,然后用条件培养基培养[19]. 如前所述,通过超高速离心(佛罗里达州迈阿密Beckman Coulter Optima L-100 XP超离心机)从条件培养基中分离出MiR-30c-5p-EV或NC-EV[17,18].
使用透射电子显微镜观察miR-30c-5p-EV的形态(JEM-1200EX;日本东京JEOL有限公司)。根据制造商手册,使用ZetaView PMX 110(particle Metrix,Meerbusch,Germany)测定电动汽车的颗粒数量和尺寸分布。
细胞治疗
将PELI1过度表达的PTC细胞(LV-PELI1)及其对照细胞(LV-NC)接种在6孔板中。隔夜培养后,用溶于DMSO或仅用DMSO的LY294002(20μM;MedChem Express,Monmouth Junction,NJ)处理LV-PELI1细胞。培养12小时后,收集细胞进行蛋白质提取。
将PTC细胞接种在6孔板(10%无EVs的FBS完全DMEM培养基)中,并用PBS、hUCMSC-EV(104颗粒/电池),NC-EV(104颗粒/细胞)或miR-30c-5p-EVs(104颗粒/细胞),如前所述,每天三天[20].
细胞增殖试验
根据制造商的方案,使用CCK-8测定法(KeyGEN BioTECH,中国南京)测定细胞活力。简言之,将PTC细胞接种在96孔板中(2×10三/well)。在指定的培养小时(24、48、72和96)后,向每个孔中添加CCK-8溶液(10μL),然后再培养2小时。使用微孔板阅读器(Synergy HT、BioTek、BioTek Winooski、VT)在450 nm处测量吸光度。
对于集落形成分析,将转染慢病毒、寡核苷酸或EVs处理的W3和TPC-1细胞接种在6孔板(1000/孔)中,并在含有10%FBS的培养基中培养。10天后,用甲醇固定细胞,并用0.4%结晶紫溶液染色,最后拍照。对含有50个以上细胞的菌落进行计数。
细胞迁移分析
PTC细胞被镀入上Transwell室(W3:5×104; TPC-1:3×104在200μl无血清培养基中)。用600μl培养基填充下室,补充10%FBS。培养12小时后,去除上膜表面的细胞,用甲醇固定膜,用0.4%结晶紫溶液染色,用尼康显微镜成像。
对于伤口愈合测定,用200μl移液管尖端刮伤单层细胞。使用PBS清洗分离的细胞,并在显微镜下记录划痕后48小时相同区域的图像。
小鼠模型研究
从扬州大学比较医学中心(中国扬州)购买4周龄雌性BALB/c裸鼠。
为了评估PELI1对PTC生长的影响,W3细胞稳定转染sh-PELI1或对照sh-NC(2×106细胞)分别皮下注射到小鼠右侧或左侧侧翼。
为了研究miR-30c-5p-EVs对PTC生长的影响,将裸鼠右侧皮下接种W3细胞(2×106单元格)。肿瘤生长7天后,PBS(20μL)、hUCMSC-EV、NC-EV或miR-30c-5p-EVs(各种EVs:2×1010按照Bruno等人的描述,每周通过瘤内注射给药20μL PBS)[19]. 第28天,切除肿瘤进行检查。肿瘤体积(mm)三根据肿瘤的长度(L)和宽度(w)轴使用以下公式计算:V=L×w2/2。
RNA分离和实时定量PCR
根据制造商的方案,使用Trizol试剂(Invitrogen)或mirVana RNA分离试剂盒(Ambion,Austin,TX)分离总RNA。使用All-in-one™qPCR Mix(Genecopoeia)在QuantStudio 5实时系统中进行实时PCR(Thermo Fisher Scientific,Waltham,MA)。所有用于实时PCR的引物,包括PELI1(HQP0504204)、β-肌动蛋白(HQP016381)、Has-miR-30c-5p(HmiRQP0396)和U48(HmiRQP9021),均购自Genecopoeia(中国广州)。的相对表达式PELI1公司miR-30c-5p分别归一化为β-actin和U48,并通过2-ΔΔCt方法,基于前面的描述[21,22].
免疫组织化学(IHC)分析
按照之前的研究所述,对组织进行了IHC分析[17,23]. 简单地说,PTC组织切片与PELI1抗体(12053–1-AP,稀释1:200;Proteintech,Rosemont,IL)孵育;将小鼠肿瘤切片与Ki-67抗体(ab16667,稀释1:200;Abcam,Cambridge,MA)或MMP2抗体(10373–2-ap,稀释1:2200;Proteintech)在4℃孵育过夜,然后用HPR-结合二级抗体孵育。以二氨基联苯胺为底物。用苏木精对细胞核进行复染。所有照片都是用尼康显微镜拍摄的。使用Image-Pro Plus软件(X版;加利福尼亚州圣何塞Adobe)测量小鼠肿瘤切片中Ki-67和MMP2的积分光密度。
蛋白质印迹
使用RIPA缓冲液(Cell Signaling Technology Inc.,Danvers,MA)提取蛋白质,并使用BCA蛋白试剂盒(Beyotime)进行定量。如前所述进行Western blot分析[21]. 抗PELI1抗体(sc-271065)购自圣克鲁斯生物技术公司(加州圣克鲁斯);从Abcam购买磷蛋白-AKT(ab81283)、AKT(ab179463)、Ki-67(ab16667)、TSG101(ab133586)、HSP70(ab181606)和HRP-linked抗兔/鼠IgG(ab97051/ab6728);MMP2(10373–2-ap)和GAPDH(60004–1-lg)购自Proteintech。使用Image J(马里兰州贝塞斯达国立卫生研究院)对蛋白质条带的强度进行量化,并将数据与相应GAPDH条带的数据进行标准化。
萤光素酶报告基因测定
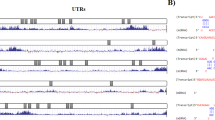
用500 ng pmiR-RB-report-h联合转染PTC细胞-PELI1公司-使用Lipofectamine 2000(Invitrogen)的3′UTR(野生型和突变型;GeneCopoeia)和50 nM miR-30c-5p miRNA(模拟和模拟NC;GenePharma)。48小时后,收集细胞,并使用Luc-Pair™Duo-luciferase HS检测试剂盒(GeneCopoeia)测量其荧光素酶活性。结果表示为相对萤火虫荧光素酶活性,这是在归一化Renilla荧光素酶活性后获得的。
统计分析
使用GraphPad Prism(5.0版;加州La Jolla)进行统计分析。数据表示为平均值±标准偏差。使用Student t检验或单向方差分析(Tukey-Kramer事后检验)对各组进行比较。P(P) < 0.05被认为具有统计学意义。