了解正常通气控制机制对于理解中枢性睡眠呼吸暂停的病理生理学很重要。严格控制正常通气以维持动脉氧(PaO)水平2)和二氧化碳(PaCO2)在狭窄范围内。这是通过包括外周和中枢化学受体、肺内迷走神经受体、脑干呼吸控制中心和呼吸肌的反馈回路实现的。
清醒时,大脑皮层区域的信号会影响呼吸,这种机制称为行为控制。众所周知,许多非化学刺激,包括肺机械感受器和行为或清醒刺激,都可以调节这种现象。睡眠期间,行为控制丧失,化学控制是调节通气的主要机制,PaCO2是通风的主要刺激因素。中枢性睡眠呼吸暂停最常见于非快速眼动睡眠(NREM),此时行为影响最小,其次是快速眼动(REM)睡眠,而完全清醒的人最不可能出现这种情况。尽管有这些变化,睡眠期间的通气控制仍与清醒时相似。
睡眠的特点是动脉二氧化碳张力(PaCO)升高2)和较高的PaCO2呼吸暂停阈值2在其下方发生呼吸暂停。减少PaCO2仅低于PaCO几毫米汞柱2设定值可能导致呼吸暂停。中枢性呼吸暂停事件通常发生在清醒和睡眠的过渡期,在这段时间内2调整设定值。
两种病理生理现象可导致中枢性睡眠呼吸暂停综合征:1)通气不稳定或2)脑干呼吸中枢或化学受体抑制。
呼吸机不稳定是CSB-CSA、高空周期性呼吸以及可能的原发性中枢性睡眠呼吸暂停的机制。
[三]与任何由反馈回路调节的系统一样,呼吸系统也容易发生不稳定。在中枢性睡眠呼吸暂停的发病机制中,通气不稳定的发生和持续可以在环路增益的背景下直观地看到,环路增益是一个工程术语,描述由反馈环路控制的系统的整体增益。
高回路增益系统对触发器的响应迅速而强烈,而低回路增益系统的响应更为缓慢而微弱。回路增益受控制器增益和工厂增益的影响。控制器增益表示对给定扰动的响应程度,而对象增益反映响应的效率。在呼吸系统中,控制器增益表现为化学反应性,而植物增益则是特定分钟通风消除二氧化碳的有效性。
环路增益的概念可以通过恒温器控制的空调将室温保持在狭窄范围内的方式来说明。微小的温度变化会触发敏感的恒温器来打开或关闭空调。恒温器对室温变化的响应程度代表控制器增益。设备增益表示响应对系统的影响,即空调制冷效应导致的房间温度变化。具有高植物增益的系统可能具有更强的空调或更小的冷却空间,从而导致更快的响应和更大的超出限制的可能性。
回路增益定义为对干扰/干扰本身的响应。在具有高环路增益的恒温器控制的空调系统中,室温的小幅升高会迅速导致冷却,这可能会超出恒温器的设置范围,很快导致空调关闭。这样的系统相对不稳定,空调经常开和关,房间温度也在波动。
在通气调节系统中,控制器增益是对高碳酸血症或缺氧的给定变化的通气反应程度,由化学受体介导。植物生长表现为通气反应对动脉氧和二氧化碳张力的影响。如果患者死亡空间低、代谢率低、功能剩余容量低或PaCO高2,通风变化的影响更为显著,导致植株获得更高的收获。
对于通气系统,可以定义环路增益,如下图所示。
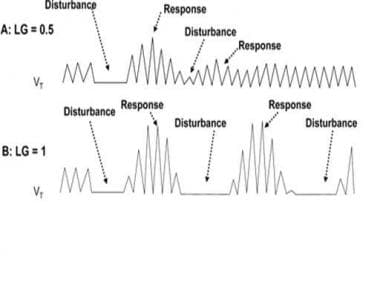 环路增益在确定呼吸不稳定中的作用。A) 当环路增益小于1时,对呼吸暂停或低通气的纠正反应过度的趋势减弱,通气恢复到稳定模式。B) 当环路增益大于或等于1时,对呼吸扰动的强烈响应会导致事件和校正之间的持续振荡,从而导致不稳定的周期性呼吸模式。改编自White DP阻塞性和中枢性睡眠呼吸暂停的发病机制。Am J Respir Crit Care Med.2005年12月1日;172(11):1363-70.
环路增益在确定呼吸不稳定中的作用。A) 当环路增益小于1时,对呼吸暂停或低通气的纠正反应过度的趋势减弱,通气恢复到稳定模式。B) 当环路增益大于或等于1时,对呼吸扰动的强烈响应会导致事件和校正之间的持续振荡,从而导致不稳定的周期性呼吸模式。改编自White DP阻塞性和中枢性睡眠呼吸暂停的发病机制。Am J Respir Crit Care Med.2005年12月1日;172(11):1363-70.
环路增益=呼吸过度(对干扰的反应)/呼吸暂停或低通气(干扰)
如果环路增益小于1,则对呼吸暂停或低通气的反应更缓慢、更小,使通气恢复到稳定模式。如果环路增益大于1,则对呼吸暂停和低通气的巨大反应会导致过度换气和呼吸暂停/低通气的摆动,导致称为周期性呼吸的不稳定状态。清醒时,行为控制可能会覆盖周期性呼吸模式,因此高回路增益对通气系统的影响在睡眠时最为明显。
除了高回路增益外,扰动检测和响应启动之间必须存在延迟,以使系统变得不稳定。由于PaCO变化之间的延迟,呼吸系统存在这种情况2并检测颈动脉体和脑干的变化。一些充血性心力衰竭患者的循环时间延长可能会加重延迟,使他们容易出现不稳定的通气状态,即CSB-CSA。
当静息PaCO时,通气系统特别有不稳定的风险2接近PaCO2呼吸暂停阈值。在高控制增益或高植物增益与低基线PaCO相关的情况下2在接近呼吸暂停阈值时,系统的轻微中断可导致中枢性呼吸暂停和超敏的周期性出现。低碳酸血症和心力衰竭患者以及那些升到高海拔地区的患者经常会出现这些情况,使他们容易出现周期性呼吸模式。这一概念的可信度得到了以下观察结果的支持:增加死空间,增加PaCO的吸入浓度2,或在某些情况下,通过乙酰唑胺增加基础通气量可以防止周期性呼吸。
心力衰竭和中枢性睡眠呼吸暂停患者对PaCO变化的通气反应增强2与心力衰竭和阻塞性睡眠呼吸暂停患者进行比较。缺氧增强了对PaCO变化的通气反应2(增加反应斜率)并容易导致通风不稳定。PaCO的变化2可能比低PaCO更重要2因为慢性肝病患者的PaCO也较低2但不要发展成中枢性睡眠呼吸暂停。据报道,在心力衰竭和中枢性睡眠呼吸暂停患者中,对运动的通气反应增加,与CSB-CSA衰竭的严重程度成正比,这表明外周和中枢化学受体反应增强。
[4]
中枢性睡眠呼吸暂停低通气综合征,如与麻醉剂使用或脑干损伤相关的综合征,是由于中枢呼吸模式中枢或外周化学受体或两者的干扰,由于觉醒或行为驱动力受到抑制,在睡眠期间可能变得更为明显。
呼吸“控制中心”涉及延髓的几个区域。在NREM睡眠期间,呼吸由一个主要受化学刺激影响的自动系统控制。在快速眼动睡眠中,抑制性和兴奋性都会对延髓呼吸神经元产生影响,表现为呼吸不规则和偶尔的“生理性”中枢性呼吸暂停。
中枢神经系统的原发性疾病,如脑膜炎或出血、肿瘤或涉及脑干的中风,可导致共济失调呼吸模式,称为Biot呼吸。Biot模式可能是不规则的,没有任何类型的周期性,也可能由类似大小的呼吸与中央呼吸暂停交替组成,如下图所示。
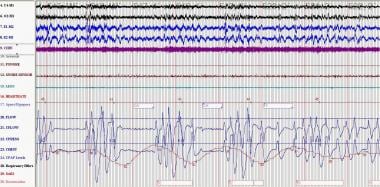 多导睡眠图显示长期服用吗啡治疗慢性疼痛的患者出现中枢性睡眠呼吸暂停和Biot呼吸。比奥模式可能是不规则的,没有任何类型的周期性,也可能是由类似大小的呼吸交替出现中枢性呼吸暂停组成。
多导睡眠图显示长期服用吗啡治疗慢性疼痛的患者出现中枢性睡眠呼吸暂停和Biot呼吸。比奥模式可能是不规则的,没有任何类型的周期性,也可能是由类似大小的呼吸交替出现中枢性呼吸暂停组成。
海洛因、吗啡和美沙酮等麻醉剂通过刺激位于髓质呼吸复合体神经元上的阿片样Mu受体而引起呼吸抑制。尽管阿片类药物的许多中枢神经系统效应产生了耐受性,但研究表明
[5]已经证明慢性麻醉剂使用者存在异常的高碳酸血症和低氧通气反应,并且有几份报告表明,长期服用阿片类药物的个体中普遍存在中枢性睡眠呼吸暂停。
[6,7]有人提出,在长期使用麻醉剂时,颈动脉体和其他外周化学受体的Mu受体抑制可能会导致更微妙的呼吸抑制。
[7]
中枢性睡眠呼吸暂停综合征和阻塞性睡眠呼吸停止综合征的发病机制是重叠的,中枢性睡眠暂停综合征患者通常会发生阻塞性事件。研究表明,在中枢性呼吸暂停事件中,下咽部可能会大大缩小。在正常吸气过程中,膈肌和上呼吸道肌肉会产生神经元放电,从而使咽部变硬和扩张,使其保持开放状态。如果膈肌和上呼吸道扩张器的活动都减少,则可能导致中枢性或阻塞性呼吸暂停。如果尽管咽肌缺乏活动,但上呼吸道仍然畅通,则会导致中枢性呼吸暂停。如果中央性呼吸暂停期间上呼吸道关闭,在咽扩张器肌张力恢复之前膈肌活动恢复,则会导致混合性呼吸暂停。
[8]
因此,上气道塌陷的易感性可能决定了由于通气不稳定导致的骑行是否会发生中枢性或阻塞性呼吸暂停。在引入持续气道正压通气(CPAP)的情况下,阻塞性呼吸暂停转为Cheyne-Stokes呼吸模式就是这种现象的一个例子。请参阅下面的图像。
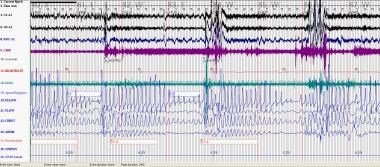 阻塞性睡眠呼吸暂停(OSA):多导睡眠图显示在持续气道正压滴定前OSA患者出现典型的低通气状态。阻塞性睡眠呼吸暂停综合征患者气流缺失或减少,但通气努力持续。
阻塞性睡眠呼吸暂停(OSA):多导睡眠图显示在持续气道正压滴定前OSA患者出现典型的低通气状态。阻塞性睡眠呼吸暂停综合征患者气流缺失或减少,但通气努力持续。
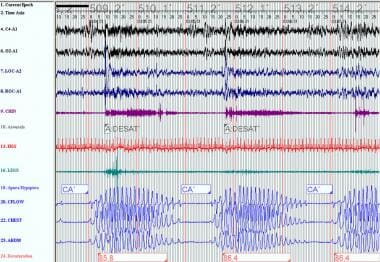 Cheyne Stokes:该多导睡眠图表示Cheyne Stokes呼吸,发生在上一媒体文件中同一患者OSA持续气道正压滴定后。Cheyne Stokes呼吸具有典型的渐强-渐弱呼吸模式。
Cheyne Stokes:该多导睡眠图表示Cheyne Stokes呼吸,发生在上一媒体文件中同一患者OSA持续气道正压滴定后。Cheyne Stokes呼吸具有典型的渐强-渐弱呼吸模式。











