介绍
心力衰竭是一个日益受到关注的公共卫生问题,其发病率和死亡率令人担忧,而心脏纤维化仍是心力衰竭的主要病理结果(1). 心脏纤维化的显著特征是过度重塑和细胞外基质(ECM)积聚(2). 研究动物模型中的替代性纤维化通常由心肌梗死建立,反应性纤维化由压力负荷模型诱导(三). 当发生损伤或压力过载时,心脏成纤维细胞分化为高度专业化的肌成纤维细胞,增加纤维胶原、基质细胞蛋白的产生/分泌,以及α-平滑肌肌动蛋白(α-SMA,ACTA2基因)的表达,以应对损伤或应激(4). 此外,心肌细胞-成纤维细胞通讯也控制着心肌纤维化的发展(5). 适当的纤维化反应有助于组织修复。然而,持续激活肌成纤维细胞导致的过度纤维化可导致组织顺应性逐渐降低,营养和氧气输送减少,心肌萎缩和细胞死亡增加,导致进行性左心室扩张和功能障碍(6–8). 最近的一项研究表明,在慢性应激下消融肌成纤维细胞具有心脏保护作用;激活肌成纤维细胞后消除应激刺激,使这些细胞恢复到静止状态,表明肌成纤维纤维细胞可能是减少纤维化和减轻疾病严重程度的潜在靶点(9). 因此,本研究探讨了心脏成纤维细胞活化和维持的分子机制,以期找到治疗心力衰竭的新方法。
ADAMTS家族蛋白(ADAMTS)在结构和功能上与金属蛋白酶(ADAM)相似(10). 主要区别在于ADAM是一种膜锚定蛋白,而ADAMTS是一种与细胞外基质(ECM)结合的分泌蛋白酶(11). 最近的报道表明,某些ADAMTS在调节细胞增殖、粘附、迁移和细胞内信号转导方面发挥重要作用(10,11). 在横向主动脉收缩(TAC)模型中,ADAMTS16的表达水平增加,其过度表达在体外活化成纤维细胞(12). 在压力过载小鼠模型中,ADAMTS2在心肌肥厚期间上调(13). 许多研究已经描述了ADAMTSs在心脏纤维化和心力衰竭中的重要作用,特别是ADAMTS8在心血管疾病中起着关键作用(14). ADAMTS8以自分泌/旁分泌的方式促进肺动脉高压(PH)和右心室衰竭的发展以及PASMCs的增殖、ECM重塑和内皮功能障碍(15). 此外,Badshah等人发现ADAMTS8在线性形态中上调,转染ADAMTS8-过表达质粒的正常成纤维细胞分化为肌成纤维细胞(16). 然而,ADAMTS8在心肌纤维化中的作用尚未被彻底研究。因此,本研究旨在探讨ADAMTS8在损伤或应激后心肌纤维化中的作用及其机制。
材料和方法
人类心脏组织
从新华医院接受手术的扩张型心肌病患者身上采集患有严重纤维化的心脏组织。正常心脏组织来自死于脑死亡的供体。获取患者左心室组织后,一部分用于蛋白质提取,另一部分用于免疫荧光染色。
动物研究
用于本研究的雄性Sprague-Dawley大鼠购自Jihui实验动物繁育有限公司(中国上海)。建立大鼠心肌梗死模型通过如前所述永久结扎冠状动脉左前降支(17). 在以50 mg/kg大鼠体重腹腔注射3%戊巴比妥钠进行麻醉后,将大鼠固定在垫子上,并对胸部进行剃毛和消毒。然后用正压人工呼吸器(潮气量7–8 mL,呼吸频率80次/min)对大鼠进行插管和通气。在大鼠胸骨左侧第三和第四肋间间隙进行开胸手术。然后,在左心耳根部下方2–3mm处用丝线缝合左冠状动脉前降支。结扎后心脏前壁立即变白,证明心肌梗死模型已成功建立。此外,如前所述,压力过载大鼠模型是由TAC诱导的(18). 简单地说,用戊巴比妥麻醉Sprague-Dawley大鼠,并将其置于呼吸机上。胸骨上切口暴露主动脉根部,并在升主动脉上放置内径为0.58mm的钽夹。假手术组的动物也经历了类似的过程,没有插入夹子。然后,闭合锁骨上切口,将大鼠送回笼子。
为了确定ADAMTS8是否促进心肌梗死后的心肌纤维化,在建立心肌梗死模型后,在大鼠心肌的明显缺血区注射腺病毒介导的ADAMTS9过表达或相应的对照,剂量为6.0×1010每只大鼠的载体基因组。两周后,再次注射。ADAMTS8过表达腺病毒由中国汉生物生物技术公司合成。
原代心脏成纤维细胞和心肌细胞的分离培养
如前所述分离和培养心脏成纤维细胞和心肌细胞(19). 从2天大的SD大鼠身上切除心室,清洗,切成小于1mm的小块三,并在4°C的D-Hanks含0.5%胰蛋白酶的平衡盐溶液中培养过夜。然后收集小块,并在37°C下用II型胶原酶(100单位/ml;美国沃辛顿)进一步消化40分钟。用补充有10%FBS的DMEM(Gibco-Life)终止消化,用移液管重新悬浮小块。通过细胞筛(200毫升)过滤得到的细胞悬浮液,在含有10%FBS的DMEM中培养70分钟。去除悬浮液中的细胞,收集附着在底部的剩余细胞,以3-5×105细胞/ml的密度重新镀膜,并在含有10%的FBS、100单位/ml青霉素、,100μg/ml链霉素和0.1 mM溴脱氧尿苷(BrdU)。
ADAMTS8在心脏成纤维细胞和心肌细胞中的过度表达
根据制造商的腺病毒操作手册,用腺病毒转染心脏成纤维细胞和心肌细胞。感染的多重性约为70 pfu个/细胞。
小干扰RNA转染
根据RiboBio的产品说明书,将小干扰靶向ADAMTS8(序列:TAGGAGCAAGAG-ATTTGTA)转染到心肌细胞和成纤维细胞。为了进行转染,心脏成纤维细胞或心肌细胞培养到60-80%的融合。根据制造商的协议,使用Lipofectamine RNAiMAX试剂(Life Technologies)将100 nM ADAMTS8-siRNA或干扰siRNA输送到细胞中(20).
心肌细胞和成纤维细胞的共培养
共培养心肌细胞的方法之一是将成纤维细胞种植在插入物中(孔径为8μm),心肌细胞在24孔培养板的底部培养并共同培养。另一种方法是在孔中放置插入物(孔径0.4μm),以放置用过表达的ADAMTS8腺病毒或siRNA转染的心肌细胞。然后在6孔培养板的底室中培养心脏成纤维细胞,并共同培养。
Transwell迁移、刮伤试验和CCK-8试验
如前一研究所述,通过transwell系统和刮伤观察到成纤维细胞迁移(21). 心脏成纤维细胞以2.0×10的浓度制备5/ml,无血清培养基。然后将转染过表达ADAMTS8腺病毒或siRNA的心肌细胞培养在24孔培养板的底室中。将一个插入物(8μm孔径)放置在微孔中,以放置心脏成纤维细胞(100μl)。心肌细胞和成纤维细胞共培养24小时后,将插入物移入含有PBS的新的24孔培养板中,以去除未附着的细胞。然后用10%福尔马林固定心脏成纤维细胞15分钟,用0.25%结晶紫染色15分钟,再用无菌水再次冲洗,然后晾干。
安在体外采用刮伤试验评价细胞运动性。因此,心脏成纤维细胞的密度为5×105/在六孔培养皿中。然后,当细胞达到90%的汇合时,用无菌的200μl微移液管尖端划伤一次,并在孔中放置一个插入物(0.4μm孔径),以放置转染过表达的ADAMTS8腺病毒或siRNA的心肌细胞。心肌细胞和成纤维细胞共培养24小时后,分别获得了亮场图像。
对于CCK-8方法,心脏成纤维细胞以5×10的密度被镀在96个钢板中三细胞/孔。将细胞暴露于条件培养基(CM)中长达48 h。然后,每个孔补充10μl CCK-8,并在37°C下培养2 h。在450 nm处测量光密度并计算增殖。
条件培养基的制备
用ADAMTS8过表达腺病毒或ADAMTS8-siRNA转染心肌细胞。培养期结束后,收集培养基作为条件培养基(CM)。
逆转录定量PCR(qPCR)
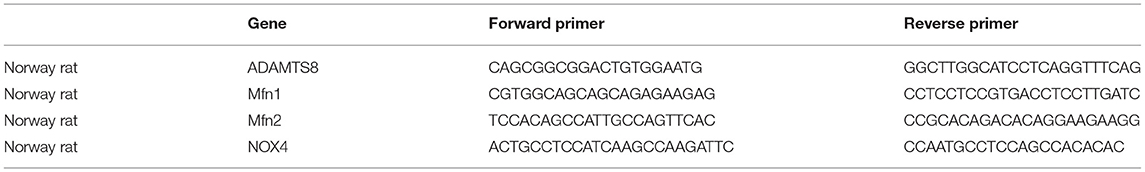
使用TRIzol(Takara)从细胞中提取总RNA。cDNA使用PrimeScript合成TM(TM)RT试剂盒(Takara)和定量PCR使用SYBR Green(Takar)进行。GAPDH被用作内部控制。引物序列如所示表1.
Western Blot分析
使用添加蛋白酶和磷酸酶抑制剂混合物(MCE)的RIPA裂解缓冲液(中国贝约汀)从分离细胞和心室组织中提取蛋白质。蛋白质在8–12%十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)上分离,并转移到聚偏二氟乙烯(PVDF)膜上。用5%的牛奶封闭1小时后,在4°C下用一级抗体孵育细胞膜过夜。我们使用了以下抗体:ADAMTS8(Santa,sc-514717)、α-SMA(Abcam,ab32575)、胶原蛋白1(Abclonal,A1352)、CTGF(Abcam,ab6992)、p-EGFR(Abca姆,ab3257)、EGFR(Abcam,ab52894)、p-ERK l,A4771),p-AKT(Proteintech,66444-1-Ig)、AKT(Protentech,10176-2-AP)、p-YAP(Cell Signaling,#4911)、YAP(Cell Signaling,#14074)、TAZ(Cell信号,#4883)、增殖细胞核抗原(Santa,sc-56)、p27kip1(Abclonal,A19095)、动力相关蛋白1(DRP-1,Cell Signoaling,#8570,1:500)、,Ser616处磷酸化的DRP-1(细胞信号,#4494),Ser637处磷酸化DRP-1,GAPDH(Abcam,ab181602)。然后彻底清洗膜,并在室温下与辣根过氧化物酶(HRP)结合的二级抗体孵育1小时。信号通过图像采集器(Tanon 5200)上的增强化学发光ECL(Thermo Scientific)显示,并通过密度测定软件(image-Pro Plus)量化。
组织学分析和免疫荧光染色
MI后4周或TAC后8周,处死大鼠,用10%福尔马林磷酸缓冲液固定左心室组织24 h,然后将固定组织石蜡包埋并切片为4μM切片。根据说明书通过PSR染色确定间质纤维化程度。根据上述方法,使用抗ADAMTS8和波形蛋白抗体进行免疫荧光染色(20). 通过Image-Pro Plus 6.0对免疫阳性区域进行量化。
二氢乙硫铵染色
ADAMTS8对活性氧生成的影响由二氢乙硫铵(DHE,BestBio,中国)检测。病毒转染24小时后,心脏成纤维细胞预加载DHE 20分钟。用PBS洗涤三次后,使用荧光显微镜(LSM780)获得DHE荧光图像。
甲苯咪唑治疗在体外
CFs接种在含有10%FBS的DMEM中的10 cm培养皿或6孔培养皿中。CFs粘附24 h,洗涤两次,在无血清培养基中饥饿24 h。然后用甲苯咪唑(5 mol/L,0.5%DMSO)或载体刺激静止细胞24 h(15).
甲苯咪唑治疗体内
MI或TAC模型1周后,成年雄性Sprague-Dawley大鼠(6周龄,150-170 g)随机接受甲苯咪唑(1%二甲基亚砜,25 mg/kg/天,腹腔注射)或溶媒治疗3周(15). 年龄匹配的对照大鼠接受等量的载药。采用简单的随机方法将大鼠分为每组。在拟定方案后,进行超声心动图检查。所有分析均以盲法进行。
左心室超声心动图测量
第28天,使用超声仪器(Vivid7,GE Healthcare)进行超声心动图检查。通过腹腔注射戊巴比妥麻醉大鼠,并将其放置在加热垫上,以保持37°C的体温(22). 从胸骨旁长轴视图获得左心室的M模式描记,以测量左心室舒张末期直径(LVEDD)尺寸和左心室收缩末期直径(LVESD)尺寸。左心室缩短分数(FS)计算为(LVEDD–LVESD)/LVEDD×100,并以百分比表示。左室射血分数计算如下:LVEF(%)=[(LVEDD3–LVESD3)/LVEDD3]×100。
数据分析
所有数值均表示为独立实验的平均值±SEM。结果由一名未配对的双尾学生进行分析t吨-测试(两组)或方差分析(三组或更多组),然后根据需要进行Bonferroni校正。所有统计测试均使用GraphPad Prism软件版本5.0进行P(P)<0.05被认为具有统计学意义。
结果
伴有严重心肌纤维化的扩张型心肌病患者ADAMTS8表达增加
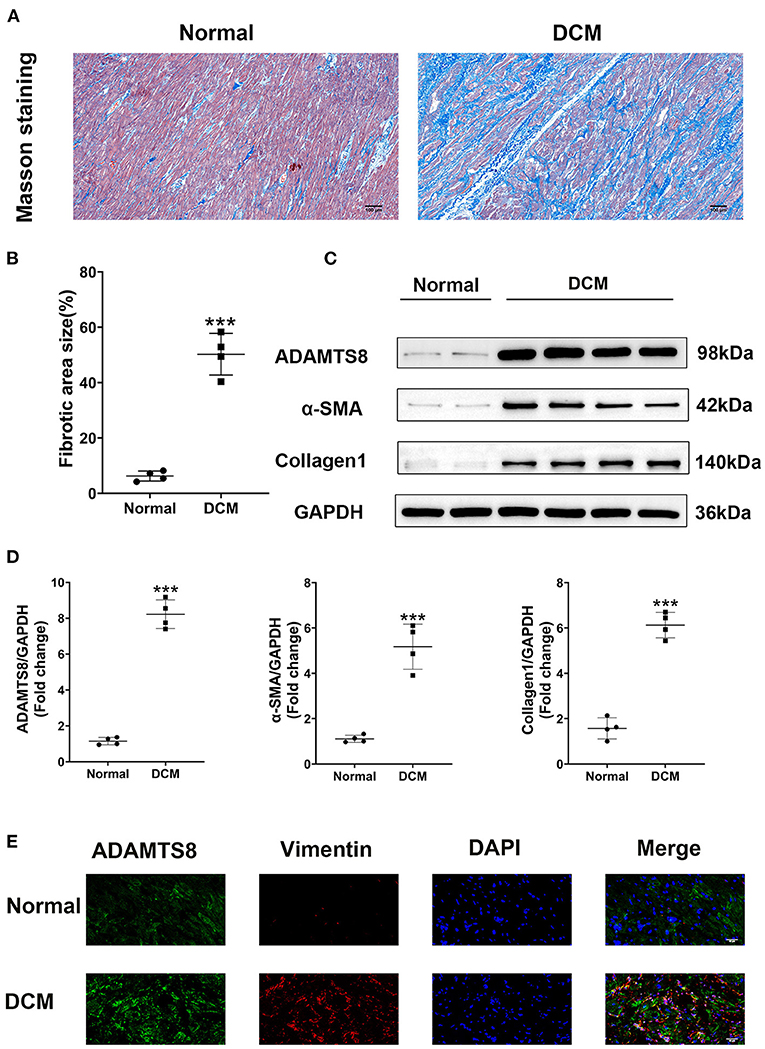
我们比较了从交通事故中的健康供体获得的正常心脏和从接受手术的扩张型心肌病(DCM)患者获得的衰竭心脏中ADAMTS8的表达。健康对照组和扩张型心肌病患者的特征列于补充表1Masson染色显示与正常心脏相比,衰竭心脏的心肌纤维化严重(图1A、B). Western blotting证实,心力衰竭患者ADAMTS8的表达增加,α-SMA和I型胶原的生成也增加(图1C、D). 免疫荧光显示,心力衰竭患者的ADAMTS8和波形蛋白显著增加(图1E).
心肌梗死大鼠模型中ADAMTS8表达增加与心肌纤维化相关
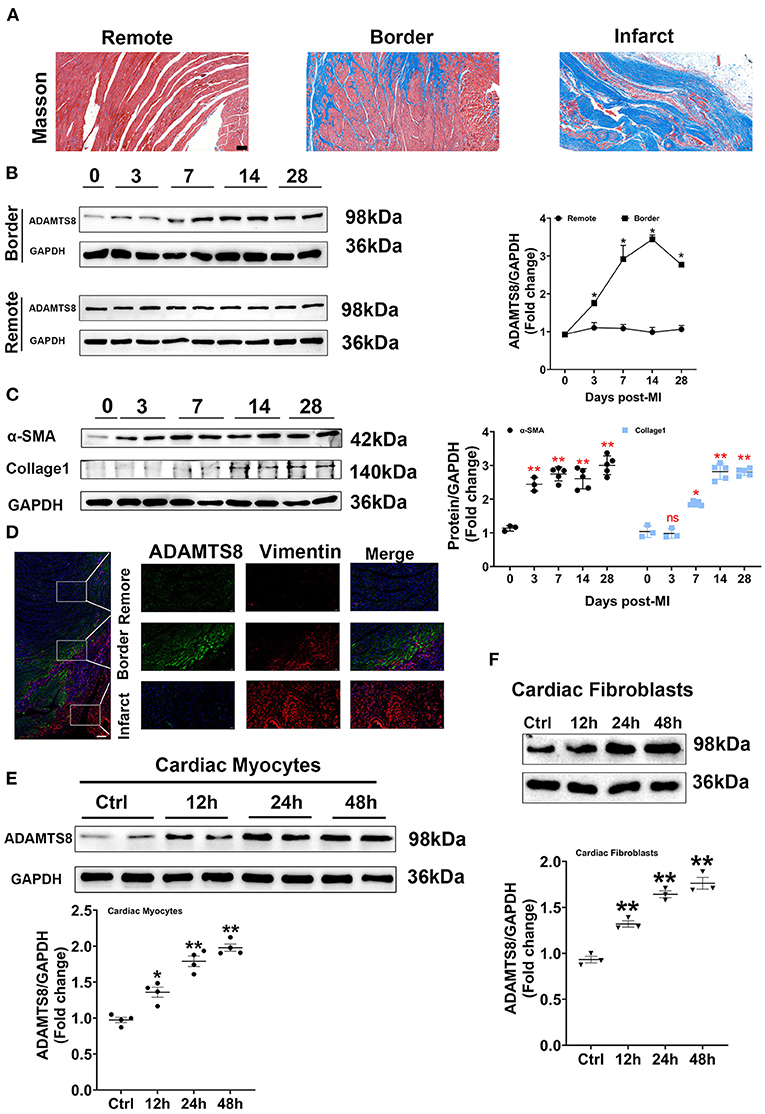
为了探讨ADAMTS8的表达是否与心肌梗死损伤和压力超负荷后的心肌纤维化相关,采用MI和TAC诱导的心力衰竭大鼠模型来表示上述两种不同的心肌纤维化反应。首先,通过Masson染色证实建模成功(图2A). 在心肌梗死大鼠模型中,我们通过western blot检测了ADAMTS8在梗死边缘区和远离梗死区域的空间表达。心肌梗死后第3天边缘区ADAMTS8水平升高,第7天显著升高,第14天达到峰值,第28天略有下降。然而,心肌梗死后28天,梗死区远端的ADAMTS8水平没有显著变化(图2B). 心肌梗死后边缘区α-SMA和胶原蛋白1的表达逐渐增加(图2C). 免疫荧光分析检测偏远地区ADAMTS8的弱染色,偏远地区未检测到波形蛋白阳性成纤维细胞(图2D). 然而,心肌梗死后28天大鼠边缘区的ADAMTS8染色呈强阳性(图2D). 此外,我们还研究了缺氧暴露后不同时间点心脏成纤维细胞和心肌细胞中ADAMTS8的表达。ADAMTS8表达在缺氧24小时后增加,48小时后保持升高,在心肌细胞中增加更为显著(图2E、F). 综上所述,上述结果提示ADAMTS8可能参与心肌梗死。
TAC诱导的大鼠心肌纤维化模型中ADAMTS8表达增加
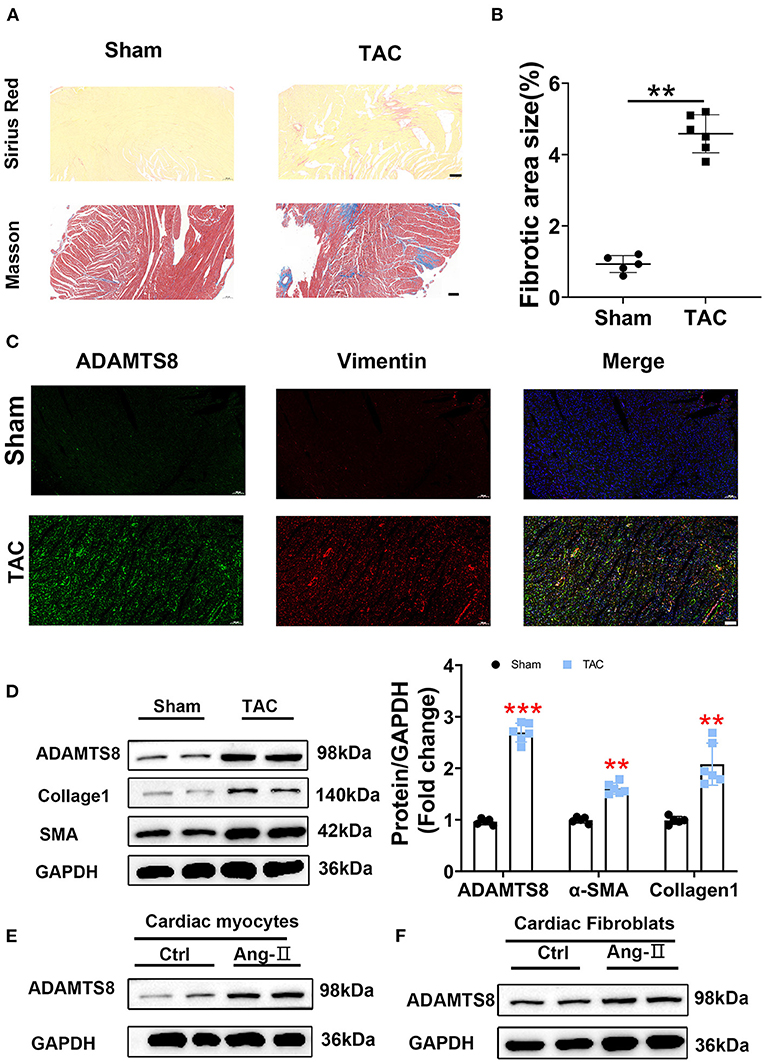
在TAC诱导的心脏纤维化中获得了与MI大鼠模型相似的结果。天狼星红和马森染色证实了建模成功(图3A、B). 免疫荧光染色检测肥厚心肌组织中ADAMTS8的表达增加(图3C). 同样,western blot结果显示纤维化心脏中ADAMTS8、α-SMA和胶原蛋白1的表达增加(图3D). 同时,我们检测了血管紧张素Ⅱ(1μM)刺激的心肌细胞和心肌成纤维细胞中ADAMTS8的表达;Ang-II刺激后,这些细胞中ADAMTS8的蛋白表达上调(图3E、F). 总之,这些结果表明,ADAMTS8表达增加与心脏损伤或压力过载大鼠的心脏纤维化有关。
ADAMTS8促进肌成纤维细胞形成在体外
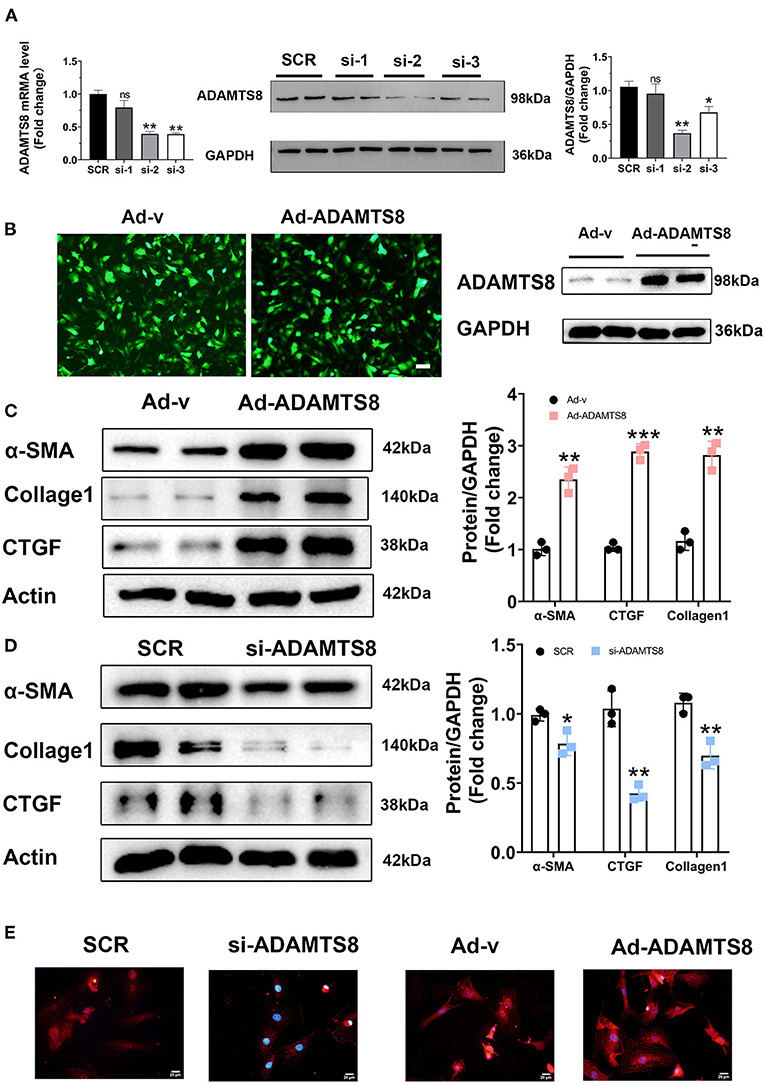
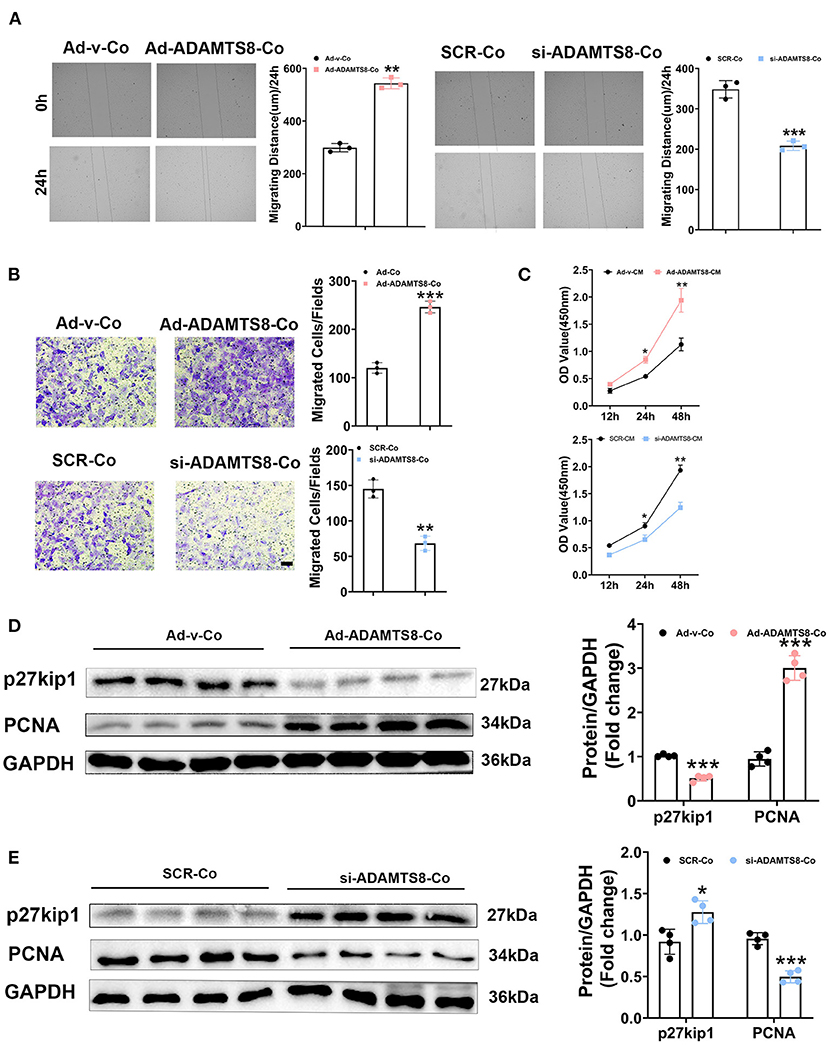
在之前的一项关于慢性低氧诱导肺动脉高压模型的研究中,心肌细胞ADAMTS8特异性敲除小鼠的右心室纤维化明显低于对照小鼠(15). 我们的研究结果表明,在缺氧和血管紧张素II刺激下,心肌细胞中ADAMTS8的表达变化比心肌成纤维细胞中更明显。考虑到心脏纤维化主要由常驻心脏成纤维细胞的激活介导,ADAMTS8的主要功能是降解细胞外基质的关键成分(23)我们推测ADAMTS8可能由心肌细胞分泌,然后通过旁分泌激活心脏成纤维细胞,从而影响心脏纤维化。为了证实这一假设,我们首先探讨了ADAMTS8是否影响成纤维细胞。使用三种ADAMTS8特异性siRNA转染心脏成纤维细胞。转染48 h后,qPCR和western blot证实si2敲除效率最高(图4A). 我们还构建了一个含有过表达ADAMTS8(Ad-ADAMTS8)和阳性对照腺病毒(Ad-v)的腺病毒。通过免疫荧光和WB验证病毒转染效率(图4B). 将培养的新生大鼠心脏成纤维细胞转染Ad-ADAMTS8或si-ADAMTS48,以进一步探讨ADAMTS8在心脏纤维化中的作用及其机制。ADAMTS8过表达促进成纤维细胞分化为肌成纤维细胞,表现为α-SMA、胶原1和CTGF的表达增加(图4C). 相反,ADAMTS8敲除抑制肌成纤维细胞活化(图4D)免疫荧光染色显示,ADAMTS8-siRNA组中α-SMA的表达与干扰siRNA组相比显著降低。同时,与Ad-v组相比,Ad-ADAMTS8治疗诱导α-SMA表达显著升高,表明ADAMTS8可以促进成纤维细胞分化为肌成纤维细胞(图4E). 这些结果为ADAMTS8加重心脏纤维化提供了证据在体外.
ADAMTS8介导心肌细胞与心肌成纤维细胞的相互作用
心肌细胞和成纤维细胞是心脏中的关键细胞类型,它们协同调节正常心脏功能和心脏对致病性刺激的反应(24). 据报道,ADAMTS8作为旁分泌介质,在肺动脉平滑肌细胞(PASMCs)和肺动脉内皮细胞(PAECs)之间的相互作用中在肺动脉高压(PH)的发生发展中起着关键作用(15). 缺氧、Ang-II或刺激后心肌细胞ADAMTS8的表达增加更明显。先前的研究表明,ADAMTS8特异性敲除小鼠心肌细胞后,与对照小鼠相比,右心室纤维化明显减少。因此,我们接下来评估了ADAMTS8心肌细胞衍生的旁分泌信号对心脏成纤维细胞的影响。我们将心脏成纤维细胞与转染过表达ADAMTS8腺病毒(Ad-ADAMTS8-co)或siRNA(si-ADAMTS_8-co。正如预期的那样,转染过表达ADAMTS8腺病毒的心肌细胞共培养增强了SD大鼠心脏成纤维细胞的迁移能力,但si-ADAMTS8-co抑制了成纤维细胞迁移(图5A、B). 为了证实我们的发现,我们从转染了Ad-ADAMTS8(Ad-ADATS8-CM)或si-ADAMTS48(si-ADAMS8-CM)的心肌细胞中制备条件培养基(CM),用于CCK8分析。结果表明,与对照组相比,用si-ADAMTS8-CM培养的心脏成纤维细胞的细胞增殖也降低(图5C). 此外,与转染过表达ADAMTS8腺病毒的心肌细胞共同培养的心脏成纤维细胞增加了增殖细胞核抗原(PCNA)的表达,但降低了kip27(细胞周期素依赖性激酶抑制剂)的表达。相反,与si-ADAMTS8-co共培养降低了CFs的PCNA表达,增加了p27Kip1的表达(图5D、E). 因此,这些数据表明,心肌细胞分泌ADAMTS8可能与心肌细胞和心脏成纤维细胞在心肌纤维化发展过程中的相互作用有关。
ADAMTS8介导的心脏成纤维细胞线粒体功能障碍和激活Ros敏感通路调节纤维反应
ADAMTS8促进肺动脉平滑肌细胞的线粒体分裂,导致ROS生成和细胞增殖增加(15). 最近的研究表明,活性氧(ROS)和线粒体功能在CF增殖和激活中发挥着新的作用。同时,线粒体分裂诱导的活性氧生成激活p38-MAPK的磷酸化,增加大鼠心脏成纤维细胞的增殖和胶原生成(25,26). 在肺成纤维细胞中,TGFβ转录诱导的线粒体ROS生成导致NOX4表达增加,这被认为是维持细胞内ROS水平升高以激活PI3K-AKT和MAPK信号通路的一种方法(27). 因此,我们探讨了ADAMTS8对心脏成纤维细胞的作用是否与细胞内线粒体分裂与融合之间的平衡有关,从而激活PI3K-AKT和MAPK信号通路。众所周知,drp1在Ser637被磷酸化,从而抑制线粒体的分裂(28). 我们发现ADAMTS8-siRNA处理激活了drp1磷酸化(Ser637)(图6A). RT-PCR显示,与SCR组相比,si-ADAMTS8组的融合前基因(Mfn1和Mfn2)显著上调(图6B). 与这些发现一致的是,ADAMTS8的过度表达显著降低了drp1在Ser637的磷酸化水平(图6C). 此外,ADAMTS8过表达增加了NOX4表达和ROS水平(图6D、E). 为了阐明ADAMTS8对成纤维细胞的潜在分子机制,我们分析了ADAMTS9是否影响上述PI3K-AKT和MAPK信号通路。与以往研究一致(29,30)si-ADAMTS8组ERK1/2、JNK和p38的磷酸化水平降低,而ADAMTS8过表达组则显著升高(图6F). 同时,在si-ADAMTS8组中AKT信号通路被抑制,而在ADAMTS8过度表达组中则显著激活(图6G). 最后,MAPK途径抑制剂SB203580和AKT抑制剂LY294002基本上消除了ADAMTS8对成纤维细胞活化的影响(图6H). 总之,这些结果表明,ADAMTS8是线粒体功能障碍的一种可能作用机制,它导致ROS依赖性激活p38-MAPK和AKT通路,以增加CFs的增殖和胶原生成。
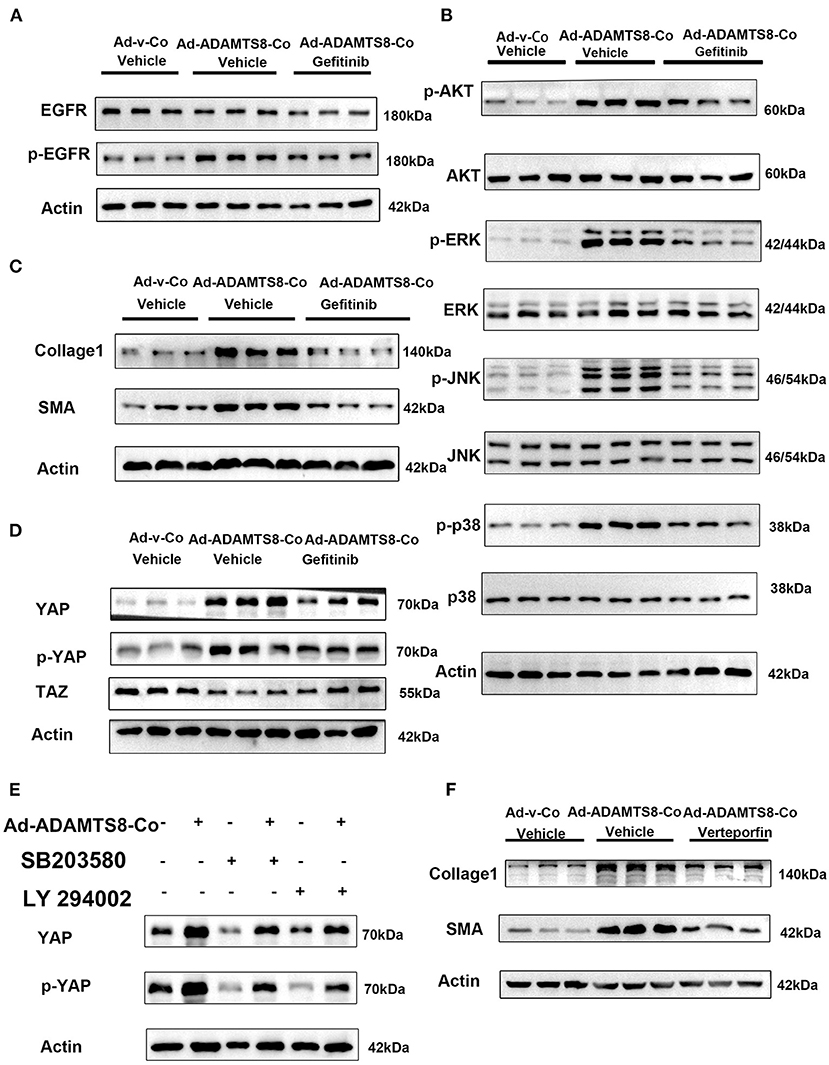
ADAMTS8激活YAP并抑制EGFR表达阻断ADAMTS8-诱导的培养心肌成纤维细胞YAP激活
众所周知,作为ECM关键成分的蛋白聚糖可以被ADAMTS8降解(23). ECM在生理和病理过程中影响细胞行为并提供结构支持。ECM还可以局部释放生长因子,如表皮生长因子(EGF),它可以作为与EGFR结合的可溶性配体。因此,通过蛋白水解降解的ECM重构可以释放这些生长因子,从而影响细胞增殖和迁移(31). 此外,ADAMTS8激活的ERK和PI3K-AKT通路是EGFR激活的不同效应通路(32). 因此,我们假设ADAMTS8释放的ECM蛋白片段可以作为可溶性配体与EGFR相互作用,然后激活ERK和PI3K信号通路。因此,我们将心脏成纤维细胞与用过表达的ADAMTS8腺病毒(Ad-ADAMTS8-co)转染的心肌细胞共同培养。结果表明,成纤维细胞EGFR磷酸化水平升高。同时,EGFR酪氨酸激酶抑制剂吉非替尼预处理可部分下调ADAMTS8诱导的p-Akt/Akt、p-ERK/ERK、p-JNK/JNK和p-p38/p38比值(图7A、B). 吉非替尼预处理也显著减弱ADAMTS8诱导的α-SMA和胶原蛋白1表达增加(图7C). 这些发现表明,ADAMTS8诱导成纤维细胞分化为肌成纤维细胞至少部分是通过激活EGFR信号通路介导的。对果蝇和糖尿病肾间质纤维化的几项研究表明,激活PI-3激酶-Akt和MAPK通路导致YAP激活(33,34)EGFR是这两条通路的上游。同时,一项研究表明,心肌梗死后阻断成纤维细胞YAP可减轻心肌纤维化(35). 因此,我们假设ERK和PI3K-Akt信号的激活依赖于EGFR,并且它们的相互作用是ADAMTS8过表达后YAP激活的上游。正如我们所料,在与转染过表达ADAMTS8腺病毒(Ad-ADAMTS8-co)的心肌细胞共同培养的CFs中,丝氨酸127(s127)处的YAP表达和YAP磷酸化上调,而TAZ(另一个河马信号效应器)下调。吉非替尼(一种EGFR酪氨酸激酶抑制剂)治疗逆转CFs中YAP表达和YAP磷酸化的增加以及TAZ表达的降低(图7D). 此外,我们发现与转染过表达的ADAMTS8腺病毒(Ad-ADAMTS8-co)的心肌细胞共同培养的CFs中I型胶原和a-SMA的上调通过YAP抑制剂verteporfin的治疗被显著抑制,这表明YAP是上述途径的下游(图7E). 同时,用SB203580抑制MAPK或用LY294002抑制PI3K也可以抑制与转染过表达ADAMTS8腺病毒(Ad-ADAMTS8-co)的心肌细胞共同培养的心脏成纤维细胞中诱导的YAP表达增加和YAP磷酸化(图7F). 这些结果表明,ADAMTS8介导了YAP的表达,EGFR位于上游。
ADAMTS8过度表达促进心肌纤维化和心功能受损体内
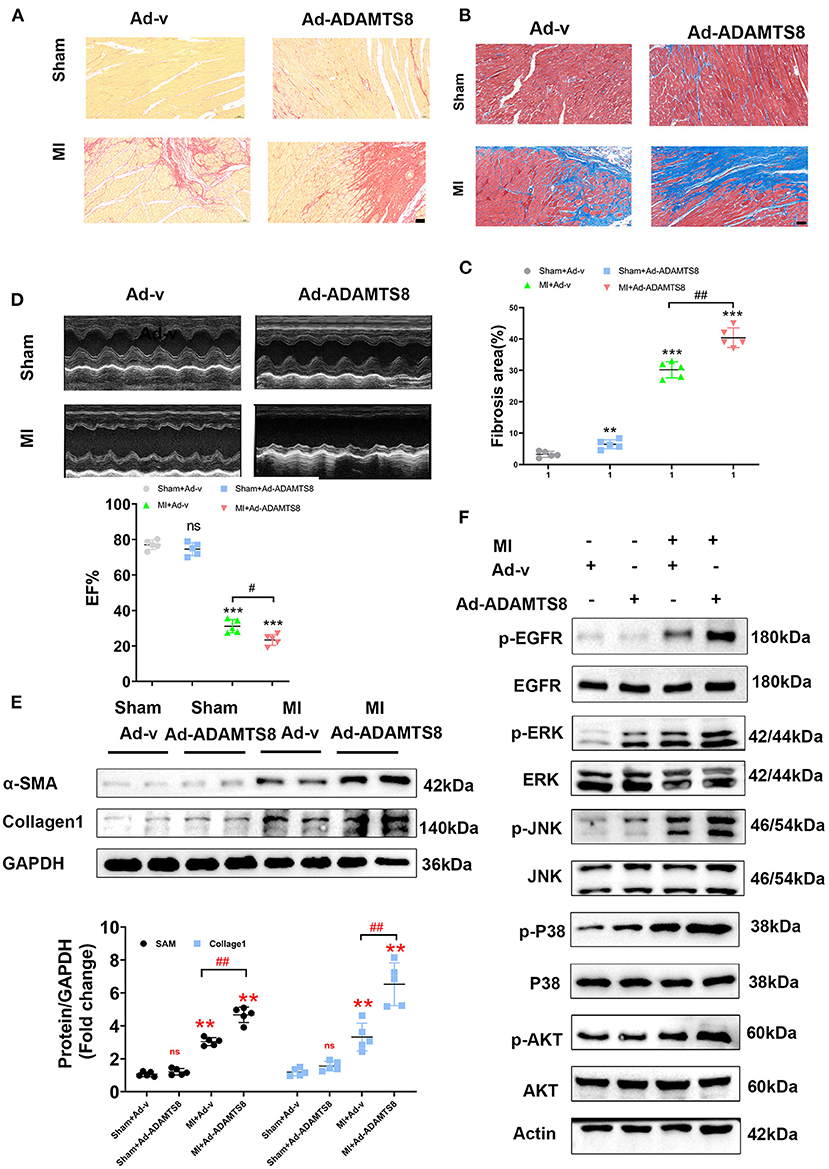
为了探讨ADAMTS8在损伤后心肌纤维化中的作用,在结扎大鼠LAD动脉后,我们在梗死边缘区的多个位置向心肌注射携带过表达ADAMTS8+阳性对照腺病毒的腺病毒(补充图1A). 心肌梗死后7天用western blot检测ADAMTS8的表达水平(补充图1B). 天狼星红染色和Masson染色结果表明,ADAMTS8的过度表达加重了心肌纤维化的程度(图8A–C). 进行超声心动图检查以评估ADAMTS8过度表达是否影响心脏功能。与注射阳性对照病毒的大鼠相比,注射过表达ADAMTS8腺病毒大鼠心肌梗死后心功能显著下降(图8D). 与上述结果一致,与注射对照病毒的大鼠相比,注射过表达ADAMTS8腺病毒大鼠的Collage1和α-SMA表达水平高于注射对照病毒大鼠,表明ADAMTS9在激活心脏成纤维细胞中起关键作用体内(图8E). 此外,我们检测了大鼠心肌梗死模型中的EGFR、MAPK和AKT通路,发现与干扰心肌梗死组相比,ADAMTS8过表达心肌梗死组中EGFR、ERK、JNK、p-38和AKT的磷酸化水平显著升高(图8F). 总之,上述结果表明ADAMTS8的过度表达促进了心脏纤维化和心功能受损体内.
甲苯咪唑下调ADAMTS8并改善心肌纤维化和心力衰竭
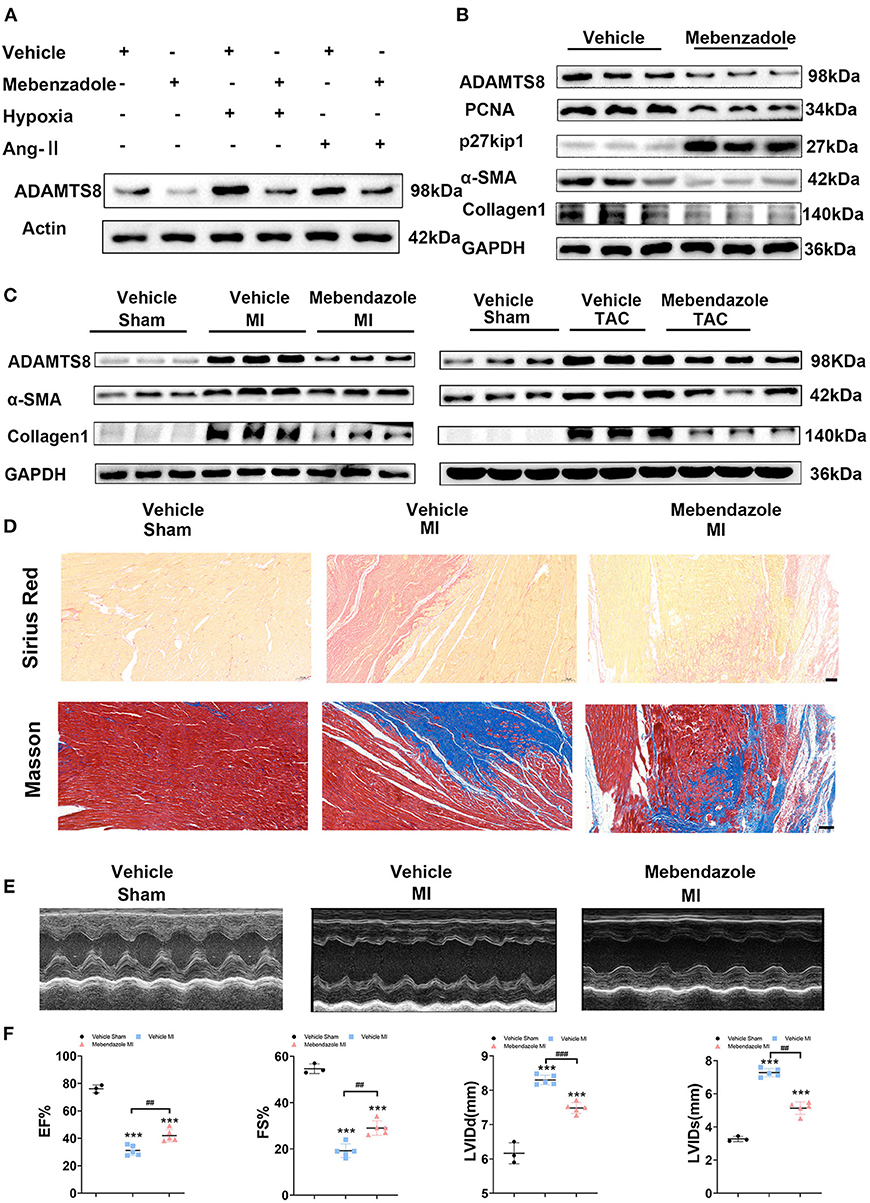
据报道,甲苯咪唑可抑制肺和右心室ADAMTS8的表达,改善肺动脉高压(15). 因此,我们探讨了甲苯咪唑是否也可以通过抑制ADAMTS8的表达来抑制心脏纤维化。我们发现甲苯咪唑治疗抑制在体外常氧和缺氧条件下心脏成纤维细胞中ADAMTS8的表达。甲苯咪唑还抑制Ang-II诱导的ADAMTS8表达(图9A). 甲苯咪唑治疗降低成纤维细胞增殖,同时抑制成纤维细胞向肌成纤维细胞的转化(图9B). 然后,我们检查了在MI和TAC大鼠模型中施用甲苯咪唑的效果。结果表明,在MI和TAC大鼠模型中,甲苯咪唑治疗可显著减弱ADAMTS8在心脏的表达。此外,在接受甲苯咪唑的TAC或MI手术组中,α-SMA和Collage1的表达水平显著降低(图9C). 心肌梗死后28天,甲苯咪唑还显著降低了梗死边缘区的间质纤维化(图9D). 尽管心肌梗死后28天LVEF和FS均下降,但与溶媒治疗组相比,甲苯咪唑治疗组的左室内径(LVEDD,LVESD)扩张较小,左室收缩功能恶化明显较小(图9E、F). 这些结果表明,甲苯咪唑抑制了心脏中ADAMTS8的表达,改善了心脏纤维化和心力衰竭。
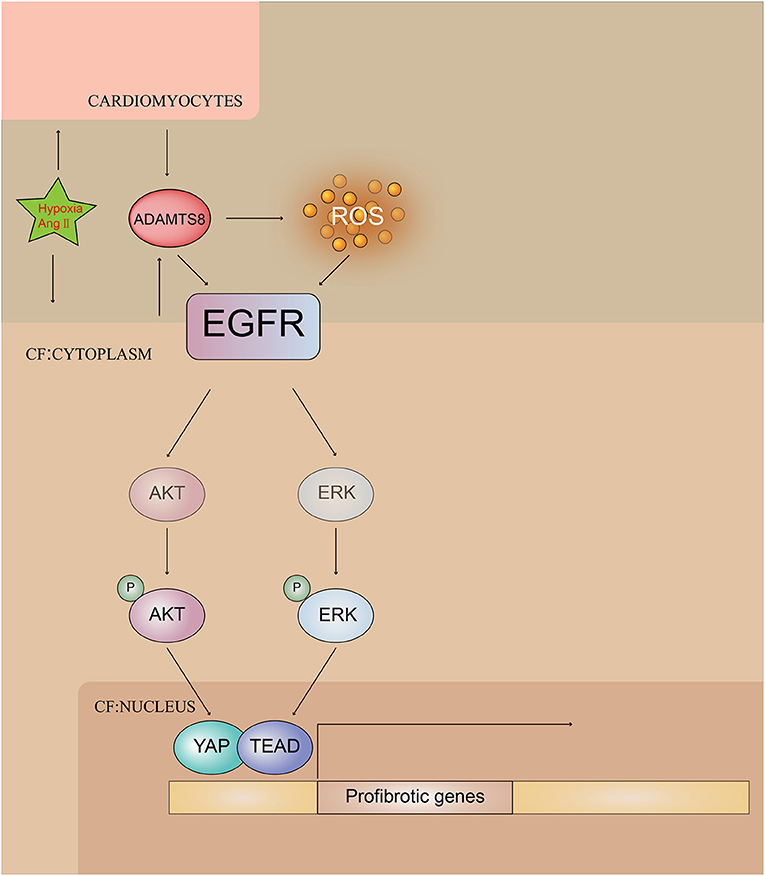
总的来说,这些结果表明ADAMTS8在心脏纤维化发病机制中起着关键作用,并揭示ADAMTS9可能是预防和治疗心脏纤维化的有用靶点(图10).
讨论
本研究的主要发现如下:(1)心肌梗死大鼠模型、主动脉横缩(TAC)诱导的心肌纤维化和心力衰竭患者中ADAMTS8表达增加,在这些疾病和模型中均伴有肌成纤维细胞活化和胶原纤维沉积。(2) EGFR和相关下游信号通路被ADAMTS8分泌增加部分激活,从而促进成纤维细胞激活在体外(3)ADAMTS8过表达体内心肌梗死大鼠模型中心功能受损并促进心肌纤维化。(4) 甲苯咪唑治疗降低了心肌细胞和成纤维细胞中ADAMTS8的表达,改善了心脏纤维化。总之,本研究首次系统地探讨了ADAMTS8的作用,并揭示了心脏纤维化的新机制。
ADAMTS是一种分泌蛋白,其特征是存在MMP结构域和数量可变的TSP-1。据报道,各种ADAMTS可以调节细胞增殖、迁移、粘附和细胞内信号转导(10,11). 例如,ADAMTS1缺乏在小鼠中诱发胸主动脉瘤和夹层,而在马凡综合征患者的主动脉中则下调(36). 此外,据报道,人类冠状动脉疾病的新基因位点ADAMTS7缺陷抑制了小鼠导线损伤后新生内膜的形成,并下调了血管平滑肌细胞的迁移(36). 众所周知,ADAMTS8在抗血管生成反应中起着关键作用。与ADAMTS1和7在各种组织中普遍表达不同,ADAMTS8在肺和心脏中特异表达(14). 目前,只有少数报告描述了ADAMTS在心肌纤维化和心肌肥厚中的重要作用。在横行主动脉缩窄(TAC)模型中,ADAMTS16的表达增强,其过度表达在体外可以激活心脏成纤维细胞(12). 另一个体内压力超负荷小鼠模型显示ADAMTS2在心肌肥厚过程中上调(13). ADAMTS8与某些疾病中的成纤维细胞激活和器官纤维化促进有关。例如,ADAMTS8在肺动脉高压和线性形态(一种结缔组织病)中的表达显著增强。许多研究表明,ADAMTS8过度表达可诱导正常成纤维细胞转化为肌成纤维细胞(15,16). 在由Sugen/缺氧模型诱导的肺动脉高压大鼠模型中,慢性缺氧后,肺和RV中ADAMTS8的水平显著升高,心肌细胞特异性ADAMTS9基因敲除小鼠的RV纤维化程度显著低于对照小鼠(15). 考虑到上述所有发现,我们假设ADAMTS8的表达也可能与心脏纤维化的发展有关。在这里,我们的结果提供了证据表明,在心肌梗死大鼠模型、横贯主动脉缩窄(TAC)诱导的心肌纤维化以及患有严重心肌纤维化的扩张型心肌病患者中,ADAMTS8的表达增加。
心肌梗死大鼠心肌梗死后28天ADAMTS8过度表达损害心功能并促进心肌纤维化体内.体外研究表明,ADAMTS8的过度表达促进了心脏成纤维细胞向肌成纤维细胞的转化,并诱导了心脏成细胞的增殖、迁移和胶原合成。因此,综合调查结果体内和在体外表明心肌梗死后梗死边缘区ADAMTS8的过度表达是CFs增强的原因之一,导致心肌梗死后心脏功能障碍和重构。因此,靶向ADAMTS8可能是一种潜在的心脏纤维化治疗方法。
线粒体活性氧(mtROS)生成和氧化磷酸化的变化对肌成纤维细胞的形成至关重要(37). 在肺成纤维细胞中,TGFβ诱导的线粒体ROS生成转录上调NOX4,可能是维持细胞内ROS水平升高以激活AKT和MAPK通路的一种手段(27). 一项研究报道,NOX4的敲除抑制SMA和FN-EDA的诱导通过肾脏中的ERK1/2信号(38). 先前的研究表明,经典的Samd信号通路和非经典的信号通路,如MAPK和PI3K/Akt,与心脏纤维化有关(39–41). 缺氧后,肺动脉平滑肌细胞(PASMCs)中ADAMTS8的敲除显示NADPH氧化酶活性和ROS水平显著降低。小鼠肺动脉平滑肌中的ADAMTS8细胞特异性敲除显著低于对照小鼠的肺动脉活性氧水平。ADAMTS8还调节PASMCs线粒体分裂和融合之间的平衡(15).体外研究表明,ADAMTS8增强了NOX4介导的ROS生成和CFs增殖。此外,CFs中ADAMTS8的敲除显著增加了线粒体分裂相关蛋白DRP-1在Ser637的磷酸化水平。成纤维细胞中ADAMTS8的过表达激活了AKT和MAPK信号通路,并且这些通路的激活被ADAMTS8敲低所抑制;同样的结果也得到了证实体内.
蛋白聚糖是ECM的关键成分,可被ADAMTS8降解(23). ECM可以隔离并局部释放生长因子,例如表皮生长因子(EGF),它可以作为与EGFR结合的可溶性配体,影响细胞增殖和迁移(31). 众所周知,G蛋白偶联受体诱导EGFR反式激活,该反式激活通过细胞内激酶如去整合素和金属蛋白酶(ADAMs)起作用,将EGFR配体裂解为激活EGFR的可溶性活性部分。该序列导致下游信号通路的随后激活,包括MAPK和Akt(32). 此外,依赖EGFR的MAPK和Akt信号通路被揭示与肺和肝纤维化以及其他器官纤维化有关(42–44). 我们的研究结果表明,ADAMTS8诱导的心肌成纤维细胞活化是通过介导的通过激活EGFR信号通路。
对果蝇和糖尿病肾间质纤维化的几项研究表明,MAPK和AKT途径的激活导致YAP的激活(33,34)EGFR是这两条通路的上游。心肌梗死后通过阻断成纤维细胞YAP减轻心肌纤维化(35). 我们发现,由ADAMTS8过度表达诱导的YAP活化和随后的磷酸化与以肌成纤维细胞活化为特征的心肌纤维化有关。抑制YAP可显著逆转ADAMTS8诱导的Collage1和α-SMA表达水平,表明ADAMTS9通过激活EGFR-MAPK/AKT-YAP信号通路调节心脏纤维化过程。此外,我们发现用于治疗寄生虫感染的甲苯咪唑抑制ADAMTS8的表达,并改善MI和TAC诱导的心脏纤维化。因此,甲苯咪唑可能是一种有前途的药物,需要进一步探索药物重新定位用于心力衰竭患者的可能性。
数据可用性声明
作者将毫无保留地提供支持本文结论的原始数据。
道德声明
上海交通大学医学院附属新华医院医学伦理委员会对涉及人类参与者的研究进行了审查和批准。患者/参与者提供了参与本研究的书面知情同意书。该动物研究由上海交通大学医学院附属新华医院医学伦理委员会审核批准。
作者贡献
列出的所有作者都对这部作品做出了实质性、直接和智力上的贡献,并批准出版。
基金
本研究得到了中国自然科学基金(批准号:81974295)的资助。
利益冲突
作者声明,该研究是在没有任何可能被解释为潜在利益冲突的商业或金融关系的情况下进行的。
出版说明
本文中表达的所有声明仅为作者的声明,不一定代表其附属组织的声明,也不一定代表出版商、编辑和审稿人的声明。任何可能在本文中进行评估的产品,或制造商可能提出的索赔,都不受出版商的保证或认可。
补充材料
本文的补充材料可以在以下网站上找到:https://www.frontiersin.org/articles/10.3389/fcvm.2022.797137/full#补充-材料
缩写
ADAMTS8,一种具有血小板反应蛋白基序8的去整合素和金属蛋白酶;CFs、心脏成纤维细胞;TAC,横行主动脉缩窄;细胞外基质;心肌梗死;扩张型心肌病;左前降支;肺动脉平滑肌细胞;EF,射血分数;α-SMA,α平滑肌肌动蛋白;表皮生长因子;CM,条件培养基。
工具书类
1.苏珊、杨丹、吴毅、谢毅、朱伟、蔡智等。EphrinB2通过调节stat3和TGF-β/Smad3信号的相互作用调节心脏纤维化。圆形Res。(2017) 121:617–27. doi:10.11161/CIRCRESAHA.117.311045
PubMed摘要|CrossRef全文|谷歌学者
2.Bonnans C,Chou J,Werb Z。发育和疾病中细胞外基质的重塑。Nat Rev摩尔细胞生物学。(2014) 15:786–801. 数字对象标识代码:10.1038/nrm3904
PubMed摘要|CrossRef全文|谷歌学者
3.Rai V、Sharma P、Agrawal S、Agraval DK。心脏研究中心肌纤维化和肥大小鼠模型的相关性。分子细胞生物化学。(2017) 424:123–45. doi:10.1007/s11010-016-2849-0
PubMed摘要|CrossRef全文|谷歌学者
4.弗朗哥吉亚尼·NG。心脏纤维化:细胞生物学机制、分子途径和治疗机会。Mol Aspects医学。(2019) 65:70–99. doi:10.1016/j.mam.2018.07.001
PubMed摘要|CrossRef全文|谷歌学者
5.Pellman J,Zhang J,Sheikh F.心肌纤维化和心律失常中的肌细胞-成纤维细胞通讯:机制和模型系统。分子细胞心血管杂志。(2016) 94:22–31. doi:10.1016/j.yjmcc.2016.03.005
PubMed摘要|CrossRef全文|谷歌学者
6.van den Borne SW、Diez J、Blankesteijn WM、Verjans J、Hofstra L、Narula J。梗死后心肌重塑:肌成纤维细胞的作用。Nat Rev Cardiol公司。(2010) 7:30–7. doi:10.1038/nrcardio.2009.199
PubMed摘要|CrossRef全文|谷歌学者
7.Weber KT、Brilla CG。病理性肥大和心肌间质。纤维化与肾素-血管紧张素-醛固酮系统。循环。(1991) 83:1849–65. doi:10.1161/01.CIR.83.6.1849
PubMed摘要|CrossRef全文|谷歌学者
8.Weber KT、Sun Y、Bhattacharya SK、Ahokas RA、Gerling IC。肌纤维母细胞介导的心脏病理重塑机制。Nat Rev Cardiol公司。(2013) 10:15–26. doi:10.1038/nrcardo.2012.158
PubMed摘要|CrossRef全文|谷歌学者
9.Kanisicak O、Khalil H、Ivey MJ、Karch J、Maliken BD、Correll RN等。遗传谱系追踪确定了受损心脏中肌成纤维细胞的来源和功能。国家公社。(2016) 7:12260. doi:10.1038/ncomms12260
PubMed摘要|CrossRef全文|谷歌学者
10.Rodríguez-Manzaneque JC、Fernández-Rodrígue R、Rodráguez-Baena FJ、Iruela-Arispe ML.血管生物学中的ADAMTS蛋白酶。基质生物. (2015) 44–6:38–45. doi:10.1016/j.matbio.2015.02.004
PubMed摘要|CrossRef全文|谷歌学者
11.Rocks N、Paulissen G、El Hour M、Quesada F、Crahay C、Gueders M等。ADAM和ADAMTS金属蛋白酶在癌症中的新作用。生物化学。(2008) 90:369–79. doi:10.1016/j.biochi.2007.08.008
PubMed摘要|CrossRef全文|谷歌学者
12.姚毅,胡聪,宋强,李毅,达欣,于毅,等。ADAMTS16激活潜在的TGF-β,加重压力超负荷心脏的纤维化和功能障碍。心血管研究。(2020) 116:956–69. doi:10.1093/cvr/cvz187
PubMed摘要|CrossRef全文|谷歌学者
13.Wang X,Chen W,Zhang J,Khan A,Li L,Huang F,et al.ADAMTS2(一种具有血小板反应蛋白基序2的崩解蛋白和金属蛋白酶)在压力超负荷诱导的心脏肥大中的关键作用。高血压。(2017) 69:1060–9. doi:10.1161/高血压AHA.116.08581
PubMed摘要|CrossRef全文|谷歌学者
14.Vázquez F、Hastings G、Ortega MA、Lane TF、Oikemus S、Lombardo M等。METH-1是ADAMTS-1的人类同源基因,METH-2是具有血管抑制活性的新蛋白质家族的成员。生物化学杂志。(1999) 274:23349–57. doi:10.1074/jbc.274.33.23349
PubMed摘要|CrossRef全文|谷歌学者
15.Omura J、Satoh K、Kikuchi N、Satow T、Kurosawa R、Nogi M等。ADAMTS8促进肺动脉高压和右心室衰竭的发展:可能的新治疗靶点。圆形Res。(2019) 125:884–906. doi:10.1161/CIRCRESAHA.119.315398
PubMed摘要|CrossRef全文|谷歌学者
16.Badshah II、Brown S、Weibel L、Rose A、Way B、Sebire N等。分泌因子SOSTDC1和ADAMTS8的差异表达导致线性形态成纤维细胞的纤维化改变。英国皮肤病杂志。(2019) 180:1135–49. doi:10.1111/bjd.17352
PubMed摘要|CrossRef全文|谷歌学者
17.张磊,甘志刚,韩磊,王浩,白洁,谭国杰,李XX,等。血红素氧化酶-1通过抑制炎症和改善肠道微循环对心衰大鼠的保护作用。老年心脏病学杂志。(2015) 12:353–65. doi:10.11909/j.issn.1671-5411.2015.04.001
PubMed摘要|CrossRef全文|谷歌学者
18.Sorokina N、O'Donnell JM、McKinney RD、Pound KM、Woldegiorgis G、LaNoue KF等。补充补偿性途径以维持氧化通量,降低肉碱棕榈酰转移酶I活性,是肥大心脏能量代谢效率低下的特征。循环。(2007) 115:2033–41. doi:10.1161/CIRCULATIONAHA.106.668665
PubMed摘要|CrossRef全文|谷歌学者
19.Hong T,Wei Y,Xue X,Li Y,Dong H,Guo X,等。新型抗凝血纳米复合物在传递miRNA-1抑制剂对抗心肌梗死微血管阻塞中的作用。Adv Healthc Mater公司。(2020)9:e1901783。doi:10.1002/adhm.201901783
PubMed摘要|CrossRef全文|谷歌学者
20.Ge Z,Chen Y,Wang B,Zhang X,Yan Y,Zhou L,等。MFGE8通过抑制TGF-β1/Smad2/3通路减轻Ang-II诱导的心房纤维化和心房颤动易感性。分子细胞心血管杂志。(2020) 139:164–75. doi:10.1016/j.yjmcc.2020.01.001
PubMed摘要|CrossRef全文|谷歌学者
21.王强,于毅,张鹏,陈毅,李C,陈杰,等。激活素A/ALK4通路在血管紧张素Ⅱ诱导的心房纤维化发病机制和心房颤动易感性中的关键作用。基础研究心脏病学。(2017) 112:47. doi:10.1007/s00395-017-0634-1
PubMed摘要|CrossRef全文|谷歌学者
22.Yang LC,Zhang PP,Chen XM,Li CY,Sun J,Hou JW,Chen RH,等。信号素3a转染到左星状神经节可降低大鼠心肌梗死后室性心律失常的易感性。欧洲。(2016) 18:1886–96. doi:10.1093/europace/euv276
PubMed摘要|CrossRef全文|谷歌学者
23.Collins-Racie LA、Flannery CR、Zeng W、Corcoran C、Annis-Freeman B、Agostino MJ等。ADAMTS-8具有聚集酶活性,在人类关节软骨中表达。基质生物。(2004) 23:219–30. doi:10.1016/j.matbio.2004.05.004
PubMed摘要|CrossRef全文|谷歌学者
24.Baudino TA,Carver W,Giles W,Borg TK。心脏成纤维细胞:朋友还是敌人?美国生理学杂志心脏循环生理学。(2006)291:H1015–26。doi:10.1152/ajpheart.00023.2006
PubMed摘要|CrossRef全文|谷歌学者
25.Huang G,Cong Z,Wang X,Yuan Y,Xu R,Lu Z,等。靶向HSP90通过抑制线粒体分裂减弱血管紧张素Ⅱ诱导的外膜重塑。心血管研究。(2020) 116:1071–84. doi:10.1093/cvr/cvz194
PubMed摘要|CrossRef全文|谷歌学者
26.陆H,田A,吴杰,杨C,邢R,贾平,等。丹参素通过ROS/p38 MAPK轴抑制β肾上腺素能受体介导的心肌纤维化。生物制药牛。(2014) 37:961–7. doi:10.1248/bpb.b13-00921
PubMed摘要|CrossRef全文|谷歌学者
27.Jain M、Rivera S、Monclus EA、Synenki L、Zirk A、Eisenbart J等。线粒体活性氧物种调节转化生长因子-β信号传导。生物化学杂志。(2013) 288:770–7. doi:10.1074/jbc。M112.431973号
PubMed摘要|CrossRef全文|谷歌学者
28.Chang CR,Blackstone C.Drp1的环AMP依赖性蛋白激酶磷酸化调节其GTPase活性和线粒体形态。生物化学杂志。(2007) 282:21583–7. doi:10.1074/jbc。C700083200号
PubMed摘要|CrossRef全文|谷歌学者
29.Liu RM,Choi J,Wu JH,Gaston Pravia KA,Lewis KM,Brand JD,等。核分裂原活化蛋白激酶磷酸酶1的氧化修饰参与转化生长因子β诱导的纤溶酶原激活物抑制剂1在成纤维细胞中的表达。生物化学杂志。(2010) 285:16239–47. doi:10.1074/jbc。M110.111732号
PubMed摘要|CrossRef全文|谷歌学者
30.Anilkumar N、San Jose G、Sawyer I、Santos CX、Sand C、Brewer AC等。NADPH氧化酶-4的28-kDa剪接变体是细胞核定位的,参与血管细胞中的氧化还原信号传导。动脉硬化血栓血管生物学。(2013)33:e104–12。doi:10.1161/ATVBAHA.112300956
PubMed摘要|CrossRef全文|谷歌学者
33.Reddy BV,Irvine KD公司。通过Ajuba家族蛋白通过EGFR-MAPK信号调节河马信号。开发单元。(2013) 24:459–71. doi:10.1016/j.devcel.2013.01.020
PubMed摘要|CrossRef全文|谷歌学者
34.Chen J,Harris RC。糖尿病肾脏中EGF受体与河马途径的相互作用。《美国肾脏病杂志》。(2016) 27:1689–700. doi:10.1681/ASN.2015040415
PubMed摘要|CrossRef全文|谷歌学者
35.Francisco J、Zhang Y、Jeong JI、Mizushima W、Ikeda S、Ivessa A等。阻断成纤维细胞YAP通过抑制MRTF-A减轻心脏纤维化和功能障碍。JACC基础翻译科学。(2020) 5:931–45. doi:10.1016/j.jacbts.2020.07.009
PubMed摘要|CrossRef全文|谷歌学者
36.Oller J、Méndez-Barbero N、Ruiz EJ、Villahoz S、Renard M、Canelas LI等。一氧化氮在金属蛋白酶Adamts1缺陷小鼠和马凡综合征小鼠模型中介导主动脉疾病。自然医学。(2017) 23:200–12. doi:10.1038/nm.4266
PubMed摘要|CrossRef全文|谷歌学者
37.吉布AA,拉扎罗普洛斯议员,埃尔罗德JW。肌成纤维细胞和纤维化:细胞分化的线粒体和代谢控制。圆形Res。(2020) 127:427–47. doi:10.1161/CIRCRESAHA.120.316958
PubMed摘要|CrossRef全文|谷歌学者
38.Bondi CD、Manickam N、Lee DY、Block K、Gorin Y、Abboud HE等。NAD(P)H氧化酶介导TGF-β1诱导的肾肌成纤维细胞活化。《美国肾脏病杂志》。(2010) 21:93–102. doi:10.1681/ASN.2009020146
PubMed摘要|CrossRef全文|谷歌学者
39.Derynck R,Zhang YE。TGF-β家族信号传导中的Smad依赖性和Smad依赖途径。自然。(2003) 425:577–84. doi:10.1038/nature02006
PubMed摘要|CrossRef全文|谷歌学者
40.Gruhle S、Sauter M、Szalay G、Ettischer N、Kandolf R、Klingel K。前列环素激动剂伊洛前列素通过调节ERK信号和iNOS表达增加,加重肠病毒性心肌炎的纤维化并增强病毒复制。基础研究心脏病学。(2012) 107:287. doi:10.1007/s00395-012-0287-z
PubMed摘要|CrossRef全文|谷歌学者
41.Kang HR、Cho SJ、Lee CG、Homer RJ、Elias JA。转化生长因子(TGF)-β1刺激肺纤维化和炎症通过涉及基质金属蛋白酶-12的Bax依赖的双激活途径。生物化学杂志。(2007) 282:7723–32. doi:10.1074/jbc。M610764200个
PubMed摘要|CrossRef全文|谷歌学者
42.艾伟,张毅,唐庆泽,颜磊,卞志勇,刘C,等。水飞蓟宾通过阻断EGFR-依赖性信号通路减轻心肌肥厚和纤维化。J细胞生物化学. (2010) 110:1111–22. doi:10.1002/jcb.22623
PubMed摘要|CrossRef全文|谷歌学者
43.Fuchs BC、Hoshida Y、Fujii T、Wei L、Yamada S、Lauwers GY等。表皮生长因子受体抑制可减轻肝纤维化和肝细胞癌的发展。肝病学。(2014) 59:1577–90. doi:10.1002/hep.26898
PubMed摘要|CrossRef全文|谷歌学者
44.周瑜、李俊英、李CM、赵WK、康美杰、科夫JL等。表皮生长因子受体配体Amphiregulin在转化生长因子-β诱导的肺纤维化的发病机制中起着重要作用。生物化学杂志。(2012) 287:41991–2000. doi:10.1074/jbc。M112.356824号
PubMed摘要|CrossRef全文|谷歌学者